Introducción
El cáncer es un grupo de enfermedades caracterizadas por la presencia de mutaciones genéticas que implican la sustitución, adición o deleción de nucleótidos, y que afectan el ciclo y muerte celular (Matlashewski et al., 1984; Shtivelman, Lifshitz, Gale, & Canaani, 1985). Según datos de la Organización Panamericana de la Salud (OPS) y la Organización Mundial de la Salud (OMS), el cáncer es la segunda causa de muerte en la población americana. En 2018, se diagnosticaron 3,8 millones de nuevos casos y se registraron 1,4 millones de muertes por estas enfermedades. Los cánceres más comunes en los hombres son el de próstata (21,7%), pulmón (11,5%) y colorrectal (8,0%), mientras que en las mujeres el más prevalente es el de mama (25,2%), seguido del de pulmón (8,5%) y colorrectal (8,2%) (Bray et al., 2024). En México, el cáncer de mama tiene la mayor incidencia y se encuentra entre los más mortales, superado solo por el cáncer de piel no melanoma y el de próstata (Beltran-Ontiveros et al., 2024).
Los tratamientos para el cáncer de mama incluyen cirugías parciales, radicales y totales, así como el uso de quimioterapia y radioterapia. Uno de los principales inconvenientes de los tratamientos actuales es su baja selectividad, lo que provoca efectos adversos en los pacientes que afectan su calidad de vida (Kerr et al., 2022; Waks & Winer, 2019). Por ello, diversas investigaciones se han enfocado en encontrar moléculas con mayor especificidad, siendo las plantas las fuentes más exploradas debido a la diversidad de compuestos que integran su metaboloma y a la facilidad de extracción (Calderón-Montaño et al., 2021; Jiménez-González et al., 2023). México cuenta con alrededor de 5,000 plantas medicinales, de las cuales se cree que 300 especies tienen propiedades anticancerígenas (Alonso-Castro et al., 2011; Cruz-Pérez et al., 2021).
Las solanáceas del género Solanum han cobrado gran importancia farmacológica debido a las propiedades antineoplásicas de sus terpenos, alcaloides, aceites esenciales e incluso proteínas (Aguilar-Santamaría et al., 2013; Li et al., 2008; Yao et al., 2013). S. elaeagnifolium es un miembro de la familia Solanaceae en el cual se han encontrado altas concentraciones de glicoalcaloides pertenecientes a la clasificación de alcaloides esteroideos, siendo la α-solanina y la solanidina los más reportados (Delbrouck et al., 2023; Hawas et al., 2013; Sammani, Shammaa, & Chehna, 2013). La α-solanina estimula receptores específicos en las mitocondrias celulares, activando la producción del gen supresor BAX e inhibiendo la expresión de Bcl-2, una proteína antiapoptótica. A través de estos procesos de regulación de la expresión de diferentes marcadores apoptóticos, la α-solanina induce apoptosis en líneas celulares de cáncer de mama (Mohsenikia et al., 2013).
Otros compuestos identificados en el extracto metanólico del fruto de S. elaeagnifolium son el ácido quínico, el ácido clorogénico y el ácido dicafeoilquínico, los dos últimos considerados compuestos fenólicos. Este extracto mostró un efecto citotóxico sobre células HeLa (cáncer de cuello uterino) y MCF-7 (cáncer de mama), sin presentar efectos tóxicos sobre las células Vero (derivadas del riñón de un mono verde africano) usadas como control de células sanas. Por ello, se consideró que el extracto presentaba un efecto selectivo sobre líneas celulares tumorales (Hernández O. et al., 2017).
Todo esto presenta a S. elaeagnifolium como una fuente potencial de moléculas con actividad anticancerígena. Por esta razón, en el presente trabajo se evaluó el efecto citotóxico del extracto etanólico y de la fracción de saponinas terpénicas aisladas del fruto de S. elaeagnifolium en un modelo de células de cáncer de mama triple negativo, MDA-MB-231.
Materiales y métodos
Material vegetal y extracción
La recolección de ejemplares de S. elaeagnifolium Cav. (Solanaceae) se llevó a cabo entre agosto y octubre de 2016, enfocándose en aquellas plantas cuyos frutos presentaban un color amarillo verdoso. Las muestras fueron recolectadas en una zona de Ciudad Juárez, Chihuahua, México, ubicada en las coordenadas 31°36'21.8"N 106°22'59.9"W. El ejemplar fue identificado por la Dra. Coyolxauhqui Figueroa-Batalla, registrado con el numero #2602 y depositado en el herbario del Instituto de Ciencias Biomédicas de la Universidad Autónoma de Ciudad Juárez, Chihuahua, México. Las muestras fueron tratadas con hipoclorito de sodio al 1% y agua destilada; posteriormente, se llevó a cabo un proceso de secado a 45°C seguido de pulverización mecánica. La extracción se realizó a partir de 10 g de muestra de fruto que se procesaron por extracción fraccionada en un equipo Soxhlet, con ciclos de reflujo de 4 horas y utilizando como solventes hexano, acetato de etilo y etanol. Para concentrar los productos de extracción, se utilizó un equipo Büchi Rotavapor R-114 a 45°C y 49 cm Hg de presión.
Pruebas Fitoquímicas preliminares
El extracto etanólico seco obtenido se resuspendió en una solución de etanol al 30% en agua. Posteriormente, esta solución se sometió a pruebas fitoquímicas para la detección de metabolitos secundarios como alcaloides, fenoles, terpenos, glucósidos cardenólidos y saponinas.
Identificación de alcaloides
El proceso de identificación se inició colocando 0.5 mL del extracto en un tubo de ensayo, para posteriormente agregar 2 mL de HCl al 5%. Luego de su homogeneización, se agregaron 2 gotas de reactivo de Dragendorff (solución a: 40% de nitrato de bismuto en 20 mL de ácido nítrico al 30% en agua + solución b: 50 mL de yoduro de potasio al 54.4% en agua). La formación de un precipitado de color naranja a rojo indica la presencia de alcaloides.
Identificación de compuestos fenólicos
Prueba de acetato de plomo para taninos. En un tubo de ensayo se agregaron 5 mL del extracto y cuatro gotas de acetato de plomo al 1%; un precipitado amarillo indica la presencia de taninos.
Prueba de alcalinización de flavonoides. La prueba consistió en colocar en un tubo de ensayo 1 mL del extracto y 5 gotas de hidróxido de sodio al 50%; la reacción es positiva si aparece un color amarillo intenso que desaparece cuando se añaden 5 gotas de HCl.
Identificación de glicósidos cardenólidos
La prueba legal para los glucósidos cardenólidos. Se colocaron 2 mL del extracto y 0.5 mL de HCl concentrado en un tubo de ensayo, la mezcla se incubó durante 4 h; posteriormente se añadió 1 mL de piridina y cuatro gotas de nitroprusiato de sodio. Luego, se alcalinizó la solución con hidróxido de sodio, la aparición de un color rosado a rojo indica una prueba positiva.
Identificación de saponinas
Prueba de espuma. Se colocaron 3 mL del extracto en un tubo de ensayo y se agitó vigorosamente durante 2 min; una espuma 1 cm de altura y estable durante al menos 1 hora es indicativa de una prueba positiva.
Prueba de Rosenthaler. Para la identificación de las saponinas se colocaron 5 mL del extracto en un tubo de ensayo de vidrio al que se le agrego 1 mL de vainillina al 1% en etanol. Luego, se agregó 1 mL de ácido sulfúrico concentrado. La formación de un anillo violeta se consideró como positivo.
Efecto hemolítico. La prueba de realizó utilizando una suspensión de sangre humana entera al 1% en tampón salino de fosfato (PBS 1 X; NaCl al 0.8%, KCl al 0.02%, Na2HPO4 al 0.114%, KH2PO4 al 0.02%). Las muestras se analizaron combinando 490 μL de la suspensión de sangre con diluciones de los extractos. Se utilizó dodecilsulfato de sodio (SDS) como control positivo para la hemólisis a una concentración final de 10 μg/mL y PBS como control negativo. Las muestras se incubaron a 37°C durante 24 h. El efecto hemolítico se observó con la aparición de color rojo en la suspensión.
Identificación de esteroides y terpenos
Los terpenos se identificaron mediante la prueba de Liebermann-Burchard. Para ello, se colocaron 5 mL del extracto en un tubo de ensayo de vidrio, al que se le añadió lentamente y a lo largo de las paredes, 1 mL de cloroformo, seguido de 1 mL de anhídrido acético y 2 mL de ácido sulfúrico concentrado. La aparición de un anillo rojo-violeta se consideró un resultado positivo. Para identificar los esteroides, se modificaron las proporciones y se colocaron 1 mL del extracto en un tubo de ensayo junto con 10 mL de cloroformo, seguido de 1 mL de anhídrido acético y un volumen igual de ácido sulfúrico. En este caso, la capa superior se tornará roja y la capa de ácido sulfúrico mostrará un color amarillo-verde fluorescente si hay esteroides presentes.
Obtención de fracción de saponinas terpénicas
Las saponinas fueron concentradas utilizando 1 g de extracto etanólico (EetOH) diluido en 10 mL de una mezcla de etanol-agua, en una proporción de 1:3. La solución fue lavada con n-butanol, recuperado para concentrarlo. El producto obtenido se diluyó en 10 mL de etanol-agua (1:3) y se lavó al menos dos veces con 10 mL de éter etílico. La fase acuosa fue recuperada y se concentró con ayuda de un concentrador Eppendorf® modelo 5301. La masa de la fracción de saponinas terpénicas obtenidas (Esapo) se calculó por diferencia de peso.
Líneas y cultivo celulares
La línea celular de cáncer de mama humano (MDA-MB-231) y los fibroblastos de ratón (3T3) se obtuvieron de la Colección Americana de Cultivos Tipo (ATCC, Manassas, VA, EE. UU.). Las líneas celulares se nutrieron con medio Eagle modificado por Dulbecco (DMEM), suplementado con suero fetal bovino al 10% y al 1% de una solución de 10,000 unidades de penicilina, 10 mg de estreptomicina y 25 µg de anfotericina por mL (Sigma-Aldrich®, A5955). La incubación de las células se realizó bajo condiciones de cultivo, a 37 °C, con 5% de CO2 y una humedad relativa del 50%.
Ensayo citotóxico
Las líneas celulares se sembraron en una placa de 96 pocillos a una densidad de 5,000 células por pocillo. El extracto etanólico y la fracción de saponinas se disolvieron en medio de cultivo a concentraciones que variaron entre 1 y 80 µg/mL, y se incubaron durante 24, 48 y 72 horas en condiciones de cultivo. Después de la incubación, se añadieron 20 μL de solución de MTT (5 mg/mL; Sigma-Aldrich®, M2128) por pozo y se incubaron durante 1 hora más. Luego, el líquido de cada pocillo fue decantado, y se añadieron 100 μL de DMSO a cada uno. A continuación, se agitaron los pocillos durante 1 minuto a 100 rpm. La absorbancia de las muestras se leyó a 570 nm utilizando el lector de microplacas Benchmark Plus™ de BioRAD. Cada concentración fue evaluada en 9 réplicas.
Cambios morfológicos inducidos por muerte celular
En una caja de cultivo de 6 pocillos, se sembraron 50 mil células MDA-MB-231 por pozo y se incubaron durante 96 h en condiciones de cultivo. Pasado este tiempo, las células se trataron con el CI50 de extracto etanólico de S. elaeagnifolium (14.33 μg/mL) y CI50 de saponinas (14.5 μg/mL). El control negativo fueron células no expuestas a ningún extracto. El ensayó se llevó a cabo con una incubación durante 24, 48 y 72 h, en condiciones de cultivo. Transcurrido el tiempo, se eliminó cuidadosamente el medio y se realizaron dos lavados con PBS 1X para eliminar las células no adherentes. A continuación, las células se fijaron con Spray Fix disquim® (laca de polietilenglicol y polivinilpirrolidona, PVP, en medio alcohólico). Posteriormente, se añadió a los pozos 1 mL de azul de anilina al 1% y se dejó actuar durante 30 min, transcurrido el tiempo se eliminaron los residuos de colorante. Luego, se realizó el desteñido utilizando ácido acético al 0.05%, lavando en 3 ocasiones. Finalmente, las muestras se secaron y se realizó su observación en un microscopio óptico invertido.
Fragmentación del ADN
El ensayo comenzó con 1,000,000 de células tumorales sembradas en placas de 25 cm2, incubadas en condiciones de cultivo durante 24 h. Posteriormente, se trataron con 14.5 μg/mL de la fracción de saponinas y se incubaron durante 24 h más. El control positivo para la necrosis fueron células llevadas a ebullición en agua y el control positivo para la apoptosis fueron células tratadas con Taxol® a 0.25 μg/mL. Cuando finalizó la incubación, se recuperaron las células flotantes y adheridas por centrifugación a 2,500 rpm por 5 min. Luego, los sedimentos se trataron con 100 µL de tampón de lisis (Tris-HCL 1 mM, EDTA 10 mM y SDS al 0.5%; pH 8) durante 10 minutos a 4°C, las muestras se centrifugaron a 10,000 rpm durante 30 minutos y la solución acuosa fue recuperada. Enseguida, se agregaron 5 μL de proteinasa K (20 mg/mL) y se incubaron durante 1 h. Cuando terminó este tiempo se agregaron 20 μL de cloruro de sodio 5 M y 120 μL de isopropanol frío y se incubaron toda la noche a 4°C. Posteriormente, las muestras fueron centrifugadas a 10,000 rpm durante 30 min y el precipitado fue resuspendido en 30 μL de tampón TE (Tris-HCL 10 mM y EDTA 1 mM a pH 8,0). Finalmente, el ADN fue cuantificado y evaluado mediante análisis de electroforesis, se utilizaron 2,500 ng de ADN por muestra y el corrimiento electroforético se realizó en un gel de agarosa al 1.8%.
Análisis estadístico de los datos
El análisis estadístico para evaluar el efecto de las diferentes concentraciones de extractos y los tiempos de incubación se llevó a cabo mediante un análisis de varianza de dos vías (ANOVA) con un nivel de significancia de p<0.01. Se realizaron comparaciones múltiples utilizando las pruebas de Tukey y Dunnett, con un nivel de significancia de p<0.05. Las CI50 se calcularon mediante un análisis de regresión no lineal, considerando los valores de las 9 réplicas de cada tratamiento. La comparación del efecto de la CI50 de Esapo en los tiempos de incubación de 24, 48 y 72 horas se realizó mediante la prueba t-student, con un nivel de significancia de p<0.05. Los datos se presentan en el gráfico acompañados de su desviación estándar. El análisis de los datos y la elaboración de los gráficos se realizaron con el programa GraphPad Prism versión 6.0.
Resultados
Identificación de metabolitos
El extracto etanólico del fruto de S. elaeagnifolium, previamente obtenido mediante extracción fraccionada, mostró actividad positiva para fenoles, taninos, terpenos, glicósidos cardenólidos y saponinas (Tabla 1).
Tabla 1 Resultados de la identificación de metabolitos secundarios del extracto de fruto de S. elaeagnifolium.Table 1. Results of the identification of secondary metabolites of the S. elaeagnifolium fruit extract.
| Ensayo | Metabolito identificado | Observación |
|---|---|---|
| Dragendorff | Alcaloides | Negativo |
| Alcalinización | Compuestos fenólicos | Positivo |
| Acetato de plomo | Taninos | Positivo |
| Liberman-Burchard | Esteroides/Terpenos | Positivo a terpenos |
| Prueba Legal | Glicósidos cardenólidos | Positivo |
| Prueba de espuma/Rosenthaler | Saponinas | Positivo |
Potencial citotóxico de los metabolitos de S. elaeagnifolium
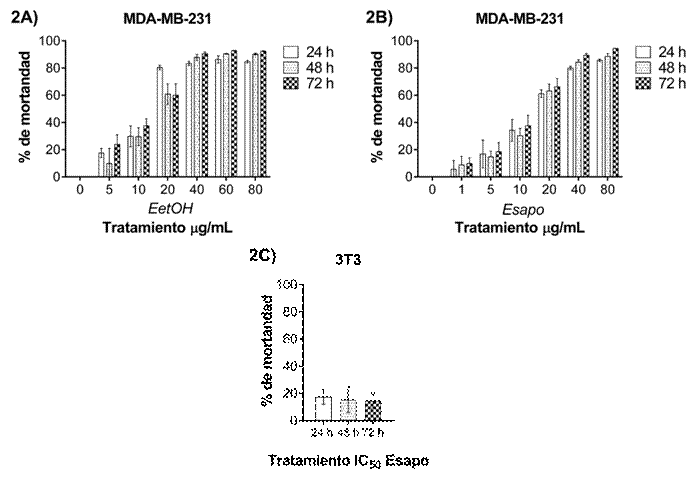
En primer lugar, se probaron concentraciones en un intervalo entre 5 y 250 μg/mL de EetOH sobre células cancerosas de mama triple negativas MDA-MB-231. Esto se hizo para seleccionar las concentraciones citotóxicas óptimas, además de conocer su comportamiento a diferentes tiempos de incubación. Después de exponer a las células con diferentes concentraciones de extracto y en diferentes tiempos de incubación, se tomaron fotografías para observar la estabilidad del monocapa celular. En la Figura 1 se observa que las células no expuestas (control) incrementan su confluencia a medida que aumenta el tiempo de incubación, llegando a formar una monocapa al cabo de 72 h de incubación. Por otro lado, se observa que las concentraciones de EetOH utilizadas inducen una menor cantidad de células en comparación con el control. A partir de 100 µg/mL, se nota un marcado impedimento en la formación de la monocapa, y las células muestran una pérdida de la morfología epitelial, adoptando una forma redondeada.

Figura 1 Evaluación del efecto de EetOH sobre la inhibición de la formación de monocapa de células MDA-MB-21 tratadas con concentraciones de 5 a 250 µg/mL con incubación de 24, 48 y 72 h.
Con base en los resultados mostrados anteriormente, se decidió evaluar el efecto de concentraciones inferiores a 100 µg/mL sobre células MDA-MB-231, ajustándose a un intervalo entre 5 y 80 μg/mL con incubaciones de 24, 48 y 72 h. Los análisis de comparaciones múltiples indican que para el EetOH todas las concentraciones presentan un incremento significativo en el valor de la mortalidad con respecto al control. Los resultados indican que, en los diferentes tiempos de incubación, a las concentraciones de 5 y 10 μg/mL las células presentan una mortalidad inferior al 38%, mientras que con 20 μg/mL aumenta a más del 60% durante los 3 días. En concentraciones que oscilan entre 40 y 80 μg/mL, la muerte es superior al 80% para todos (Figura 2A). La CI50 se calculó en un valor de 14.3 µg/mL para las 24 h de exposición. El Esapo se evaluó a concentraciones de 1, 5, 10, 20, 40 y 80 μg/mL. En esta fracción de saponinas se identificó que todas las concentraciones indujeron valores significativos de mortandad a los 3 tiempos de incubación, con respecto al control. La concentración de 20 μg/mL indujo la muerte de más del 60% de las células MDA-MB 231 en los tres tiempos de incubación. En el caso de 40 y 80 μg/mL se logró una tasa de mortalidad superior al 80% (Figura 2B). La CI50 calculada para este caso fue de 14.5 μg/mL. Esta concentración se utilizó para evaluar el efecto de las saponinas en células sanas; el modelo utilizado fue la línea celular de fibroblastos embrionarios de ratón 3T3. En estas células se observó que a las 24 h la muerte celular fue del 19% (Figura 2C) y se mantuvo sin cambios significativos hasta las 72 h. Esto significa que la fracción de saponinas terpénicas muestran selectividad por las células tumorales.
Análisis morfológico
La evaluación morfológica reveló que las células MDA-MB-231 no expuestas a los extractos se observan alargadas, con un núcleo único e integral y un citoplasma abundante. También se pueden apreciar las interacciones célula-célula y célula-matriz extracelular (Figura 3). La exposición a EetOH indujo cambios a partir de tiempos cortos, por lo que las incubaciones se dieron a las 4 y 8 h, con un seguimiento hasta las 48 h. En todos los tiempos de incubación se identifican células con condensación de cromatina de diferentes tipos, como las de tipo arriñonado o algunas que se asemejan a un núcleo gigantesco. Por otro lado, se observaron cambios en la forma de la membrana plasmática con células parecidas a palomitas de maíz, debido a invaginaciones membranales presentadas. También se observan células con núcleos en ebullición, que se asemejan al burbujeo provocado en un líquido por la acción de la temperatura. Además, se aprecian burbujas citoplasmáticas en el centro de las células y entre los fragmentos de membrana (Figura 3) (Cairrao & Domingos, 2010; Chaabane et al., 2013).

Figura 3 Análisis morfológico de células de cáncer de mama MDA-MB-231 tratadas con CI50 de EetOH a 24, 48 y 72 h. (PM) Células con forma de palomita de maíz, (CC) Células con condensación de la cromatina y (CE) Células en ebullición.
En el caso de Esapo los principales cambios morfológicos aparecieron después de las 24 h. La morfología presentada fue similar a la inducida por EetOH. Los cambios morfológicos más comunes fueron la condensación de la cromatina en forma de media luna, la presencia de cuerpos apoptóticos y algunas células presentaron estallamiento, algo común de la necrosis (Figura 4) (Yeung et al., 1999).
Evaluación del patrón de fragmentación del ADN
El carril 2 del gel de agarosa al 1.8% (Figura 5) se presenta ADN extraído de las células control donde, aunque se aprecia la ligera aparición de bandas referentes a la fragmentación del ADN, la más abundante es la del ADN integral localizado en la parte superior. En el carril 3 se colocó ADN de células tratadas con ebullición, donde se puede observar una fragmentación no específica que es típica de una célula que murió por necrosis. En los carriles 4 y 5 se cargó ADN de células expuestas a Taxol durante 24 y 48 h; este fármaco provoca la inhibición de la proliferación y muerte celular por apoptosis (Yeung et al., 1999); por lo tanto, las bandas observadas a 200, 400 y 600 pb son características de la escisión del ADN generada por la activación de las endonucleasas (Huang et al., 2010). En los carriles 6 y 7 se observa el patrón de fragmentación del ADN obtenido de células expuestas a la CI50 de Esapo con tiempos de incubación de 24 y 48 h. En los carriles 8 y 9, el ADN de las células expuesto a una concentración de 30 μg/mL Esapo con incubaciones de 24 y 48 h. En ambos casos el patrón de fragmentación es idéntico al presentado por el taxol. Las bandas observadas a 700 y a 1500 pb corresponden a ARN ribosómico.
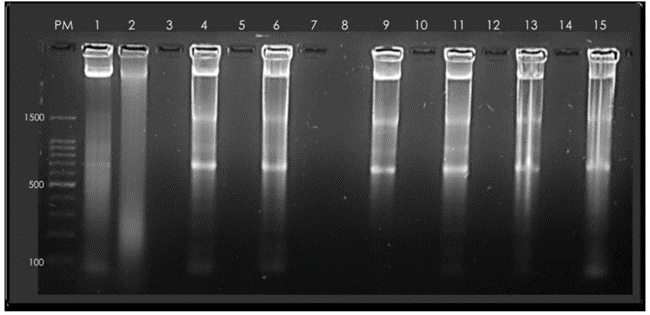
Figura 5 Perfil de fragmentación del ADN extraído de células MDA-MB-231. PM) marcador de peso molecular de 100 a 1000 pb, 1) células control, 2) células necróticas, 4) y 6) células expuestas a 0,25 μg/mL de taxol durante 24 y 48 h respectivamente, 9) y 11) células expuestas a 15 μg/mL de Esapo durante 24 y 48 h respectivamente, 13) y 15) células expuestas a 30 μg/mL de Esapo durante 24 y 48 h.
Discusión
En EetOH se pudo identificar la presencia de compuestos fenólicos y glucósidos, como las saponinas que son heterósidos cuyas geninas pueden ser esteroides (neutrales) o triterpenoides (ácidas). Una forma de identificar el tipo de saponina es la prueba de Liebermann-Burchard, que en esta investigación mostro un resultado positivo. Esto permite inferir la presencia de saponinas triterpénicas; lo cual concuerda con el hecho de que las plantas superiores pertenecientes a la clase de las dicotiledóneas son una rica fuente de saponinas triterpénicas (saponósidos); grupo al que pertenece la familia Solanaceae (Delporte, 2010; Huang, Syu, & Lin, 2010). Sin embargo, anteriormente no se ha identificado este tipo de moléculas en S. elaeagnifolium. Al comparar lo identificado en EetOH con lo reportado en diferentes frutos de otras especies del género Solanum, se identifica que contienen principalmente compuestos fenólicos cumarínicos, lactonas sesquiterpénicas, glucósidos y terpenos. En algunos casos solo difieren en la presencia de los alcaloides, un ejemplo de esto es el extracto acuoso de S. aethiopicum L. y los extractos metanólicos de S. incanum (Chinedu et al., 2011; Sambo et al., 2016). Específicamente, en S. elaeganifolium, un informe donde se realizó el fraccionamiento dirigido de un extracto de su fruta, se logró la identificación de moléculas como lactonas sesquiterpénicas, alcaloides y cumarinas (Hernández O. et al., 2017). Contrariamente, en el presente trabajo la identificación de los alcaloides no se logró mediante pruebas fitoquímicas, esto puede deberse a que sus concentraciones son muy bajas y por lo tanto no fueron perceptibles en la reacción. Sin embargo, el dato concordante es la presencia de compuestos fenólicos, ya que previamente se ha podido identificar al ácido quínico, ácido clorogénico y ácido dicafeoilquínico en extractos metanólicos de S. elaeagnifolium. En otro estudio realizado con extractos de diferentes solventes realizados con semillas de S. elaeagnifolium, el extracto metanólico presentó mayor rendimiento, demostrando que las semillas son ricas en compuestos polares; esto fue confirmado por la presencia predominante de saponinas y taninos (Feki et al., 2014). En la presente investigación, los análisis fitoquímicos demostraron que las saponinas identificadas en los frutos corresponden saponinas triterpénicas. Este informe es el primero en mostrar la presencia de este tipo de saponinas en la planta S. elaeagnifolium, según nuestra revisión de la literatura, ya que estudios previos solo habían evidenciado aquellas de tipo esteroide y de tipo alcaloide esteroidal.
Estudios realizados en S. nigrum, demostraron que el extracto etanólico de su fruto maduro presenta una tasa de mortalidad del 70% a una concentración de 50 µg/mL sobre células de cáncer de mama (MCF-7), después de 12 h de incubación (Son et al., 2003). Mientras que los extractos etanólicos del fruto verde de esta planta presentaron valores de CI50 de 12.66, 16.6 y 47 μg/mL en las células MCF-7 de cáncer de mama, HepG2 de cáncer de hígado y T47D de cáncer mamario, respectivamente (Anindyajati et al., 2010; El-Hawary et al., 2015). Por otro lado, un extracto metanólico de dicho fruto presentó efecto citotóxico sobre una línea celular de cáncer de cuello uterino (HeLa) y de riñón de mono verde (Vero), con valores de CI50 de 10 y 0.0196 mg/mL respectivamente (Patel et al., 2009). Esto permite apreciar que la CI50 de Esapo (14.3 μg/mL) en la línea de cáncer de mama MDA-MB-231, es muy similar a la reportada para S. nigrum contra la línea MCF-7.
En un trabajo de fraccionamiento del extracto metánolico del fruto de S. elaeagnifolium mediante cromatografía líquida al vacío, una de las fracciones obtenidas (FVLC7) mostró actividad citotóxica contra las líneas tumorales MCF-7, HeLa y células Vero. El tratamiento con 100 µg/mL, redujo la viabilidad en un 39, 15 y 66% para las células Vero, HeLa y MCF-7, respectivamente. En este caso, FVLC7 evidenció la presencia de ácido quínico, ácido clorogénico, ácido dicafeoilquínico y un alcaloide, a los cuales se les atribuyó la actividad biológica evaluada (Hernández et al., 2017). Las diferencias entre el efecto y las concentraciones utilizadas en los ejemplos mencionados anteriormente pueden sugerir que, al aislar parcial o totalmente los metabolitos secundarios presentes en un extracto se pueden perder algunas interacciones farmacológicas. Es decir, puede ser que las moléculas presentes en los extractos totales presenten un efecto sinérgico que se pierde al fraccionarlos (Caesar & Cech, 2019).
Los reportes de saponinas en plantas del género Solanum como S. elaeagnifolium, S. nigrum y S. vellosum indican solo la presencia de saponinas de tipo esteroidal y alcaloide esteroideo(Sammani et al., 2013). Sin embargo, también se ha reportado que plantas como S. melongena y S. lycompersicum poseen la estructura enzimática para la biosíntesis de lupeol, α-amirina y β-amirina que corresponde a las bases agliconas de saponinas triterpenicas (Kwon et al., 2015; Yasumoto et al., 2017). Esta información podría dar sustento a hecho de haber identificado saponinas terpénicas en esta investigación. En cuanto a saponinas esteroidales de solanáceas, se ha identificado que las saponinas contenidas en las hojas de S. trilobatum inhiben el crecimiento de células Hep-2 del carcinoma epitelial a una CI50 de 1,000 µg/mL mediante la activación de la apoptosis (Kanchana & Balakrishnan, 2011). Mientras que la solasodina aislada de frutos inmaduros de S. xanthocarpum mostró actividad citotóxica contra células HeLa con una CI50 de 12.7 μg/mL e inhibió el 94.96% del crecimiento de la línea celular de leucemia mieloide humana U937 a 40 μg/mL (Bhattacharya et al., 2013). En este trabajo la concentración utilizada de Esapo (14.5 µg/mL) fue menor de las que se han utilizado para otros concentrados de moléculas, por lo cual consideramos que presenta potencial como tratamiento contra el cáncer.
Conclusiones
La presencia de metabolitos secundarios en el extracto etanólico (EetOH) es diversa. En esta ocasión, se identificaron compuestos fenólicos, taninos, esteroides, terpenos, glicósidos cardenólidos y saponinas terpénicas. El extracto etanólico mostró un efecto citotóxico sobre las células de cáncer de mama, presentando una CI50 de 14.33 µg/mL. Por otro lado, Esapo provocó la muerte de las células MDA-MB-231 hasta en un 80% con una concentración inhibidora media de 14.5 µg/mL. Al aplicar esta concentración sobre fibroblastos embrionarios de ratón, solo se indujo un 20% de mortalidad, lo cual evidencia su selectividad. Las CI50 calculadas para el EetOH y el Esapo prácticamente no presentan variación, pero hay que considerar que los procesos de purificación pueden impedir las interacciones farmacológicas sinérgicas que pueden presentar diferentes moléculas en un extracto total.
Además, en las células MDA-MB-231, ambos extractos produjeron la formación de cuerpos burbujeantes a nivel citoplasmático, invaginaciones de membrana, condensación de cromatina y fragmentación del núcleo. Aún es necesario realizar más estudios para determinar el tipo de saponinas presentes en dicho extracto y el mecanismo bajo el cual actúan. Sin embargo, el presente trabajo abre un campo de investigación para buscar nuevos posibles tratamientos contra el cáncer de mama a partir del fruto de S. elaeagnifolium.











 nueva página del texto (beta)
nueva página del texto (beta)