Introducción
En el Continente Americano se reportan 211 especies de Agave, el 75% (159) prosperan en México (García-Mendoza et al, 2019). Según Olvera-Vargas et al. (2022), el agave, también conocido como maguey, posee un valor ambiental, agroecológico, económico y sociocultural evidenciado por la utilización de hasta 48 especies para la producción de bebidas fermentadas y destiladas (tequila, mezcal y pulque). Para la producción del mezcal sobresalen 14 especies de las cuales destacan Agave angustifolia, A. cupreata, A, potatorum, A. karwinskii y A. marmorata (Jesús, 2018). El A. cupreata es una planta que alcanza la madurez sexual entre 7 y 15 años y no se reproduce vegetativamente. Además, sus poblaciones están siendo diezmadas debido a que los individuos maduros se cosechan justo antes de su floración, para producir el mezcal en destilerías artesanales, lo cual evita la reproducción de la especie y la pone en peligro de extinción (Avendaño-Arzate et al., 2015). Aunado a esto, también se han incrementado sus problemas fitosanitarios causados por hongos, bacterias, nematodos e insectos. Una de las bacterias que más impacto tiene es Pectobacterium carotovorum que causa la pudrición blanda del cogollo en agave y su capacidad de permanecer latente en tejido infectado dificulta su manejo . Aquino-Bolaños et al. (2020) estimaron que de 203 millones de plantas de Agave tequilana cultivadas, el 22.3% se encontraban dañadas en diferentes grados de afectación por esta bacteria.
El principal control de P. carotovorum es la aplicación de productos químicos entre ellos fungicidas y bactericidas como son Cupravit (oxicloruro de cobre), Hidrocob77 (hidróxido de cobre), Mancoseb (Dietilditiocarbamato), Carbendazin (Bencimidazol), Agrigeen 800 (Sulfato de gentamicina + Clorhidrato de oxitetraciclina) que controlan e inhiben el crecimiento de esta bacteria con gran eficiencia. Sin embargo, el uso indiscriminado de productos químicos para el manejo y control de patógenos ha provocado problemas, tales como resistencia genética, alteraciones de los ecosistemas, aparición de nuevas plagas, movilidad en el ambiente y finalmente riesgo para la salud humana (Rashid et al., 2013).
Por ello, es importante emplear estrategias que no dañen la salud humana y que sean más amigables con el ambiente y eficientes para el control de patógenos de importancia agrícola mundial. Entre este tipo de estrategias se encuentran los métodos biorracionales, tales como la utilización de nanopartículas de plata (AgNPs), las cuales tienen aplicaciones antimicrobianas y pueden ser sintetizadas empleando métodos de síntesis verde que utilizan agentes reductores biológicos como extractos de plantas. Martínez et al. (2024), mostraron la eficiencia de la inhibición de Bacillus licheniformis, mediante el uso nanopartículas de plata (AgNPs) de síntesis verde utilizando extractos de Agave salmiana.
Otro método biorracional para el control de P. carotovorum es la aplicación de microorganismos benéficos con capacidad antagónica, tales como la bacteria Bacillus subtilis y el hongo Trichoderma lignorum que se les conoce como agentes de biocontrol debido a que poseen un crecimiento y desarrollo acelerado, pueden tolerar condiciones ambientales extremas y son capaces de parasitar, controlar y destruir hongos, bacterias, nematodos y otros fitopatógenos utilizando diferentes estrategias como resultado de su metabolismo.
El objetivo de este trabajo fue evaluar el efecto bactericida in vitro de dos tipos de nanopartículas de plata (AsA-AgNPs y AsB-AgNPs) sintetizadas con extractos de A. salmiana, así como el uso de Bacillus subtilis, Trichoderma lignorum, comparándolos con un producto comercial (Agry-gent® Plus 800) para el control de P. carotovorum.
Materiales y métodos
El material biológico, utilizado como tratamientos biorracionales en este estudio fue:
Inóculo in vitro de Pectobacterium carotovorum aislado en medio Papa Dextrosa Agar (PDA). A partir de esta muestra se preparó una solución bacteriana a una concentración a 3x108 UFC.
Las nanopartículas de plata (AsA-AgNPs y AsB-AgNPs) sintetizadas con de extractos de Agave salmiana. Para la biosíntesis de los dos tipos de nanopartículas se utilizó 1x10-3 mol/L de nitrato de plata y extractos acuosos de Agave salmiana a una concentración de 10µg/mL como agente reductor, de acuerdo a la metodología propuesta por ( González-Pedroza et al., 2021). El extracto acuoso se obtuvo a diferentes temperaturas tal como se muestra en la Tabla 1, se filtró con tubos de 30 k Amicon Ultra-15 Centrifugal filter devices, a 300 rpm durante 10 min. Luego, se obtuvo el extracto crudo a partir del mismo con el uso de presión reducida. Las diferencias registradas en la síntesis de AsA-AgNPs y AsB-AgNPs fueron la temperatura de obtención y la exposición a la radiación UV (Tabla 1). Una vez obtenidos ambos tipos de AgNPs, la muestra fue preparada a partir de una alícuota colocada en una rejilla de cobre, dejando secar a temperatura ambiente para posteriormente ser analizada y finalmente se determinaron sus características morfológicas y el diámetro de partícula (nm). Para esto se realizó un análisis espectroscópico UV-Vis a fin de monitorear la formación de AgNPs utilizando un espectrofotómetro UV-Vis (espectrofotómetro VE-5100UV, VELAB EE. UU.), en un rango de 200 a 800 nm, en modo de absorción, según lo reportado por (Martínez et al., 2024). Posteriormente con ayuda de un microscopio electrónico de transmisión (TEM) (número de serie JEOL-JEM-2010 TEM) y el software imageJ, se caracterizaron las propiedades estructurales de los sistemas nanopartículados tomando en cuenta la distribución, morfología y tamaño de partículas.
Tabla 1 Condiciones físicas de síntesis de AgNPsTable 1. Physical conditions for synthesis of AgNPs
| Muestras | Temperatura | Tiempo de exposición a radiación UV |
Porcentaje de plata y extracto de A. salmiana (V: V) |
|---|---|---|---|
| AsA-AgNPs | 93°C | 5 min | 3:5 |
| AsB-AgNPs | 25°C | 1 min | 3:5 |
Inóculo in vitro de Trichoderma lignorum en PDA, donado por el Instituto de Investigación y Capacitación Agropecuaria, Acuícola y Forestal del Estado de México (ICAMEX).
Bacillus subtilis, aislada del biofungicida comercial Baktillis ® (Biokrone), con 1x1012 UFC/mL. Posteriormente se aisló en medio de cultivo PDA, se incubaron a 28°C durante un período de 48 horas.
Agry-gent® Plus 800, como producto bactericida comercial, con sulfato de gentamicina + clorhidrato de oxitetraciclina como ingredientes activos.
Para cada uno de los métodos biorracionales y el bactericida comercial se determinaron tres concentraciones experimentales para las pruebas in vitro para el control de P. carotovorum utilizando agua destilada estéril como diluyente, tal como se observa en la Tabla 2.
Tabla 2 Concentraciones de los tratamientos biorracionales y químico para las pruebas in vitro.Table 2. Concentrations of the biorational and chemical treatments for in vitro tests.
| Tratamiento | Concentración |
|---|---|
| T1 = AsA-AgNPs | [C1: 0.04, C2: 0.06, C3: 0.08 mg/mL] |
| T2 = AsB-AgNPs | [C1: 0.04, C2: 0.06, C3: 0.08 mg/mL] |
| T3 = Trichoderma lignorum | [C1: 3x106, C2: 6x106, C3: 9x106 Conidios] |
| T4 = Bacillus subtilis | [C1: 2x107, C2: 4x107, C3:6x107UFC] |
| T5 = Sulfato de gentamicina + Clorhidrato de oxitetraciclina (Agry-gent® Plus 800) | [C1: 6, C2: 7, C3: 8 mg/L] |
| T6 = Control negativo | Agua destilada estéril |
Evaluación de la patogenicidad de P. carotovorum
Para determinar la patogenicidad de P. carotovorum se usaron plantas de A. cupreata; y como control positivo plantas de Aloe vera y de Haworthia arachnoidea como control negativo. Se disectaron tres hojas de cada planta y se lavaron con jabón y agua abundante, después se sumergieron en hipoclorito de sodio al 2% durante 2 min y luego en alcohol al 70% durante 2 min y en seguida se lavaron tres veces con agua destilada estéril. Posteriormente, se hizo una incisión de 1.0 cm en cada hoja y con un asa bacteriológica se inoculó 0.05ml de P. carotovorum a una concentración de 1x10 6 UFC, en dos de las tres hojas de cada especie, dejando la restante como control a la cual se le colocó 0.5mL de agua destilada estéril; las muestras inoculadas se incubaron en cámaras húmedas a temperatura ambiente durante un periodo de 96 h, durante este periodo se registró la sintomatología observada. Cabe mencionar que de esta prueba se hicieron tres repeticiones. Posteriormente se hicieron preparaciones microscópicas y tinción Gram de P. carotovorum, las cuales se observaron en un microscopio óptico BOECO a 100X.
Evaluación in vitro del control de los tratamientos hacia P. carotovorum
Se evaluó el efecto bactericida in vitro de los tratamientos (Tabla 2) sobre P. carotovorum. Se sembró P. carotovorum en extensión en cajas Petri con medio PDA y enseguida, en forma de cuadrante sobre la superficie del medio de cultivo, se colocaron cuatro discos de 6 mm de papel filtro estéril (Whatman No. 2), tres discos previamente impregnados con cada una de las concentraciones a evaluar (durante 5 minutos) y un disco impregnado con agua destilada estéril como control. Se hicieron tres repeticiones por tratamiento, las muestras se incubaron a 28°C por 96 h, con un vernier digital, marca Steren se midió el diámetro del halo de inhibición (mm) resultante del efecto bactericida de cada tratamiento.
Diseño experimental y análisis estadístico
Se utilizó un diseño completamente al azar con arreglo trifactorial donde: el factor A fueron los tratamientos, el factor B las concentraciones y el factor C los días de medición del halo, esto con la finalidad de evaluar el efecto bactericida sobre P. carotovorum de los cinco tratamientos (con sus respectivas concentraciones), sus tres repeticiones y un control (p≤ 0.05). Los datos obtenidos fueron sometidos a un Análisis de Varianza usando Statgraphics versión 5.0; y la prueba de Tukey (p≤ 0.05) para la comparación múltiple de medias.
Resultados
Biosíntesis de las nanopartículas de plata con extracto de Agave salmiana
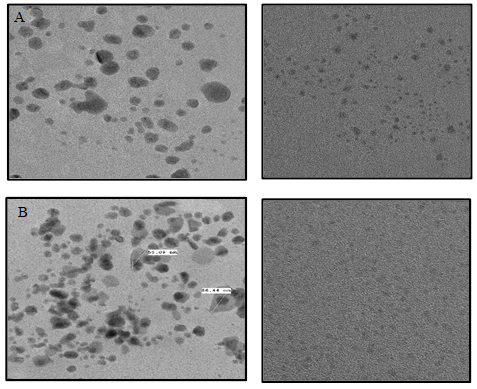
Las micrografías TEM de las AgNPs (Figura1) se obtuvieron a una concentración 3:5 de Agave salmiana. Para los dos tipos de nanopartículas AsA-AgNPs y AsB-AgNPs, se observaron formas cuasi esféricas con un tamaño que osciló entre ~1.3 y 65.2 nm (X = 14.51 nm, σ = 15 nm), y una media de 14.51, mientras que el tamaño de AsB-AgNPs osciló entre ~1.04 y 95.45 nm (X = 20.80 nm, σ = 21nm).
Pruebas de patogenicidad de P. carotovorum
Las pruebas de patogenicidad resultaron positivas para A. cupreata y Aloe vera, observándose la sintomatología característica de pudrición blanda a las 96 h después de la inoculación de las hojas con P. carotovorum, respectivamente (Figura 2, 1b y 2b). Las observaciones microscópicas 1c y 2c (100X) confirmaron la presencia de bacilos de forma abastonada con flagelos peritrícos, sus colonias mostraron elevación convexa de color blanco cremoso, además esta bacteria resultó ser Gram negativa, estas características corresponden a P. carotovorum. Mientras que para Haworthia arachnoidea esta prueba fue negativa a la infección con por P. carotovorum ya que no se observó esa apariencia acuosa.
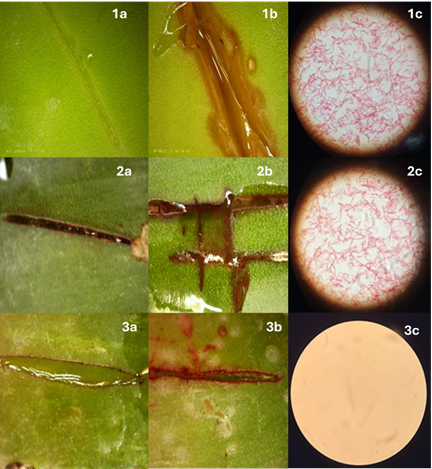
Figura 2 Sintomatología inducida por P. carotovorum: 1a, 2a, 3a, hojas de A cupreata, Aloe vera y Haworthia arachnoidea (controles); 1b, hoja de A. cupreata con necrosis bacteriana acuosa color marrón, 2b hoja de A. vera con necrosis bacteriana acuosa color marrón y 3b hoja de H. arachnoidea sin necrosis acuosa; 1c y 2c bacilos Gram negativos de P. carotovorum y 3c sin presencia de bacteria.
Evaluación del efecto antagónico in vitro de los tratamientos biorracionales
El análisis estadístico del efecto bactericida por tratamiento biorracional reveló que las nanopartículas tipo AsA-AgNPs presentaron un halo de inhibición de 1.97 mm, resultando más eficientes para el control del crecimiento in vitro de P. carotovorum, seguido del bactericida comercial Agry-gent® Plus 800 con el que se observó un halo de inhibición de 1.95 mm; mientras que con las nanopartículas tipo AsB-AgNPs mostraron un halo de 1.55 mm lo cual indica una eficiencia menor de control, así mismo T. lignorum y B. subtilis mostraron un halo de 1.29 mm, lo que indica una baja eficiencia en el control de P. carotovorum (Tabla 3).
Tabla 3 Comparación de medias del efecto bactericida de los tratamientos biorracionales.Table 3. Comparison of means of the bactericidal effect of biorational treatments.
| Tratamiento biorracional | Halo de inhibición promedio (mm)* |
|---|---|
| AsA-AgNPs | 1.97a |
| Agry-gent® Plus 800 | 1.95a |
| AsB-AgNPs | 1.55ab |
| T. lignorum | 1.29b |
| B. subtilis | 1.29b |
*De tres repeticiones. Valores con la misma letra no son estadísticamente significativos. Tukey p≤ 0.05
*Three repetitions. Values with the same letter are not statistically significant. Tukey p≤ 0.05
Los resultados de análisis estadístico del efecto bactericida de las concentraciones por tratamiento biorracional mostraron que las AsA-AgNPs, a una concentración de 0.06 mg/mL presentó un halo de inhibición 3.14 mm, siendo la mejor concentración de respuesta bactericida contra P. carotovorum. El Agry-gent® Plus 800, a una concentración de 0.008 mg/mL fue la segunda concentración de control hacia la bacteria en estudio. A esta misma concentración las AsB-AgNPs tuvieron el más alto halo de inhibición. Mientras que T. lignorum y B. subtilis presentaron su mejor halo de inhibición a una concentración de 3x106 conidios/mL y 4x107UFC/mL, respectivamente. No hay un patron de respuesta de los tratamientos biorracionales sobre la concentración utilizada para el control de P. carotovorum.
En relación a los resultados de los halos de inhibición sobre el efecto bactericida de los tratamientos biorracionales, se observó un campo claro alrededor de los discos impregnados por las diferentes concentraciones indicado por una flecha de color naranja (Figura 3B, 3C y 3D).

Figura 3 Halos de inhibición in vitro (mm) resultantes del efecto bactericida de las concentraciones más eficientes sobre P. carotovorum, comparadas con el tratamiento control: A) Control sin halo; B) AsA-AgNPs (0.06 mg/mL) con halo de 3.14 mm; C) Agry-gent® Plus 800 (0.008 mg/mL) con halo de 2.67 mm y D) AsB-AgNPs (0.08 mg/mL) con halo de 2.64.
Discusión
En relación a las pruebas de patogenicidad permitieron confirmar que la bacteria P. carotovorum afecta a Agave cupreata y las características coinciden con lo reportado por Amaya et al. (2021). Aunque, no se han reportado estudios in vitro para evidenciar la patogenicidad de P. carotovorum en esta especie de agave, nuestro estudio también concuerda con lo observado por Jiménez-Hidalgo et al. (2004) quienes confirmaron la presencia de lesiones cloróticas en el sitio de inoculación de P. carotovorum a los 15 y 20 días después, en plantas de A. tequilana.
En el presente estudio, los resultados de microscopía electrónica de transmisión (TEM) (Figura 1) de la biosíntesis de las nanopartículas, revelaron que las AsA-AgNPs presentaron una forma cuasi esférica y un menor tamaño, en comparación con las AsB-AgNPs, esto se debe a que las primeras estuvieron a una mayor exposicón de UV y a una temperatura mas alta, lo cual deriva en un alto potencial bactericida. Esto coincide con Martínez et al. (2024) quienes reportaron nanopartículas sintetizadas con extracto de Agave salminana con tamaños entre ~1 y 50 nm (X = 5,6 nm, σ = 6 nm). Así mismo, (Iravani et al., 2014) mencionan que la forma, el tamaño y la cantidad de nanopartículas tienen un efecto sobre el potencial antimicrobiano de las nanopartículas de plata. También coincide con lo que mencionan Martínez et al. (2024) respecto a que el tamaño de las nanopartículas metálicas garantiza una superficie de contacto significativamente más grande con el efluente bacteriano. Cabe destacar que, las AgNPs con tamaños inferiores a 10 nm son más tóxicas para las bacterias. Al penetrar en el citoplasma las AgNPs pueden interactuar con biomoléculas como proteínas, lípidos y ADN. En ciertos casos, pueden interactuar con el sistema enzimático respiratorio, generando especies reactivas de oxígeno (ROS) como peróxido de hidrógeno (H2O2), radicales hidroxilos (OH) y superóxido (O2 −), que inducen estrés oxidativo y daños a proteínas y ácidos nucleicos, que conducen a la muerte del patógeno (Liao et al., 2019; Santos y Barrios, 2022).
Además, Solis et al, (2019) afirman que las nanopartículas biogénicas de plata muestran una amplia distribución de tamaños y formas que varían de 2-75 nm diámetro empleando extractos vegetales en la obtención de AgNPs como agentes reductores, con mayor eficiencia en el control de patógenos. Así mismo, Solís et al., (2019) realizaron estudios sobre el efecto de las propiedades antimicrobianas de las AgNPs sintetizadas biológicamente con extracto acuoso de Anona muricata las cuales mostraron mayor efectividad en el control de P. aeruginosa ˃ E. coli ˃ S. aureus ˃ C. albicans en comparación con las AgNPs de síntesis química. Esto apoya nuestros resultados donde se demuestra que las nanopartículas de síntesis verde con extractos de Agave salmiana tipo A (AsA-AgNPs) tienen un efecto bactericida para el control de P. carotovorum. Probablemente se deba a la utilización del extracto de A. salmiana para recubrir a las nanopartículas ya que esto influye de manera positiva en la estabilidad de las mismas.
Por otra parte, en nuestros estudios quedó demostrado el efecto bactericida de los tratamientos biorracionales usando las nanopartículas tipo AsA-AgNP sobre esta bacteria Gram negativa que afecta al agave, lo cual coinciden con Ahmed et al. (2016) ya que ellos mostraron que las AgNPs sintetizadas a base de extractos acuosos de Agave americana poseen un potencial antimicrobiano significativo con un 96% de efectividad contra bacterias patógenas Gram negativas. Sin embargo, no coincide con lo reportado por Martínez et al. (2024) quienes realizaron estudios utilizando AgNPs sintetizadas con extractos de A. salmiana para el control de Bacillus licheniformis sin lograr el control de esta bacteria Gram positiva.
Al respecto, se ha estudiado que este tipo de síntesis verde es eficiente para el control de bacterias Gram negativas y Gram positivas, teniendo mejor acción en las Gram negativas. Esto debido a que la pared celular de las Gram negativas tiene un grosor de 2-7 nm y además contiene dos capas situadas en el exterior de la membrana citoplasmática, inmediatamente después se encuentra una delgada capa de peptidoglicanos, seguidamente se encuentra la membrana externa, la cual es exclusiva de las células Gram negativas, la cual está conformada por una bicapa lipídica donde la parte interna está constituida por fosfolípidos y la externa por lipopolisacáridos (LPS). Mientras que en las Gram positivas tienen un grosor de 20-80 nm por lo tanto la pared celular es más gruesa, compuesta de varias capas de peptidoglucanos, conteniendo también una gran cantidad de ácidos teicoicos, polímeros de glicerol y ribitol (Rojas-Avelizapa et al., 2020). Según Anandalakshmi et al, (2016), la acción bactericida de las nanopartículas de plata contra las bacterias Gram negativas ocurre cuando éstas poseen un tamaño entre 1 y 10 nm. De acuerdo a lo anterior cabe destacar que el mecanismo antimicrobiano de las AgNPs consiste en la unión de estas nanopartículas en la superficie de la membrana celular bacteriana, afectando las funciones respiratorias de la célula y provocando la desnaturalización de la membrana, lo que causa la fuga del contenido celular y la eventual muerte de la célula. En relación a esto, expresa que los estudios realizados para analizar la actividad antimicrobiana de las nanopartículas de plata sintetizadas biológicamente frente a microorganismos, han revelado mayor eficiencia en el control de bacterias Gram negativas como Escherichia coli, que a diferencia de las bacterias grampositivas como el Streptomyces aureus, que posee una gruesa capa de peptidoglicanos y membrana plasmática, lo cual impide que las nanopartículas sintetizadas ingresen con facilidad al interior de la membrana (Villamizar y Monroy, 2015).
Por otra parte, la comparación estadística entre las concentraciones de cada tratamiento biorracional mostró diferencias significativas al encontrar que la dosis de 0.06 mg/ml de AsA-AgNPs, seguida del bactericida comercial Agry-gent® Plus 800 (0.008 mg/ml) y de AsB-AgNPs (0.08 mg/mL) (Tabla 4), fueron los tratamientos más eficientes en el control del crecimiento in vitro de P. carotovorum, al comparar el diámetro promedio de los halos de inhibición resultantes (3.15, 2.68 y 2.64 mm, respectivamente), en cambio para acción bactericida, las concentraciones de T. lignorum (3x106 conidios/mL) y B. subtilis (4x107 UFC/mL), originaron halos de inhibición con menor diámetro promedio (1.41 y 1.34 mm, respectivamente). Esto evidencia que, en relación a la concentración de los tratamientos biorracionales no hay un patrón que indique que entre mayor sea la concentración mayor es el control hacia la bacteria P. carotovorum.
Tabla 4 Comparación de medias del efecto bactericida in vitro entre concentraciones de los tratamientos biorracionales aplicados para el control de Pectobacterium carotovorum.Table 4. Comparison of means of the in vitro bactericidal effect between concentrations of the biorational treatments applied to control Pectobacterium carotovorum.
| Tratamientos | Concentración | Halo de inhibición (mm) |
|---|---|---|
| AsA-AgNPs | 0.04 mg/mL | 0.88c |
| AsA-AgNPs | 0.06 mg/mL | 3.14a* |
| AsA-AgNPs | 0.08 mg/mL | 0.74c |
| AsB-AgNPs | 0.04 mg/mL | 2.06b |
| AsB-AgNPs | 0.06 mg/mL | 1.20b |
| AsB-AgNPs | 0.08 mg/mL | 2.64a |
| Agry-gent® Plus 800 | 0.006 mg/mL | 1.47b |
| Agry-gent® Plus 800 | 0.007 mg/mL | 1.74b |
| Agry-gent® Plus 800 | 0.008 mg/mL | 2.67a |
| T. lignorum | 3x106 Conidios/mL | 1.41b |
| T. lignorum | 6 x106 Conidios/mL | 1.22c |
| T. lignorum | 9x106 Conidios/mL | 1.24c |
| B. subtilis | 2x107 UFC/mL | 0.98c |
| B. subtilis | 4x107UFC/mL | 1.34b |
| B. subtilis | 6x107 UFC/mL | 1.32b |
*De tres repeticiones. Letras diferentes indican diferencias estadísticas significativas (Tukey, p ≤0.05).
*Three repetitions. Different letters indicate significant statistical differences (Tukey, p ≤0.05).
En relación al efecto en el control de P. carotovorum por a la acción del bactericida comercial Agry-gent® Plus 800 este, resultó más efectivo que los agentes biológicos (T. lignorum y B. subtillis). Cabe mencionar que es un bactericida sistémico de amplio espectro de acción rápida para el control de la pudrición de cogollo del agave, causada por Erwinia sp. ahora clasificada como Pectobacterium. carotovorum.
Aunque se ha reportado la eficiencia de las especies de los géneros Trichoderma y Bacillus como agentes bactericidas, donde mencionan que la cepa de B. subtilis 9B14 tuvo una gran eficiencia contra P. carotovorum, con un halo de inhibición de 9.16 mm (García-Martínez et al. 2022), en nuestro estudio no resultaron con un alto potencial de control. .
Por otra parte, en relación a Trichoderma,Guerrero et al. (2017) mencionan que las cepas de la misma especie de Trichoderma spp. muestran diferentes grados de acción sobre el crecimiento de patógenos y también su mecanismo puede variar de un cultivo a otro.
Conclusiones
El efecto bactericida de las nanopartículas de plata AsA-AgNPs, sintetizadas biológicamente con extractos de Agave salmiana, empleadas como tratamiento biorracional fue eficiente para el control del crecimiento in vitro de Pectobacterium carotovorum, lo que podría ser un método prometedor como un tratamiento ecológico y eficiente como posible sustituto del control químico.
En este estudio Trichoderma lignorum y Bacillus subtilis no fueron tan eficientes para el control in vitro de Pectobacterium carotovorum agente causal de la marchitez en agave.











 nueva página del texto (beta)
nueva página del texto (beta)