ANTECEDENTES
De acuerdo con la Organización Mundial de la Salud (OMS), la endometriosis es una enfermedad en la que tejido similar al que reviste la cavidad uterina, crece fuera del útero.1 El proceso fisiopatológico mediante el cual se desarrollan estas lesiones sigue siendo motivo de controversia y por ende el desarrollo de una serie de teorías. Estas teorías son diversas en su conceptualización del problema, pero todas confluyen en la generación de un proceso inflamatorio que causa el dolor, la inflamación e infertilidad característica de la endometriosis. Por ello, se reconoce a la endometriosis como un síndrome caracterizado por un proceso crónico inflamatorio (punto pivote o fulcro), estrógeno dependiente que afecta, principalmente, a estructuras pélvicas.2.Figura 1
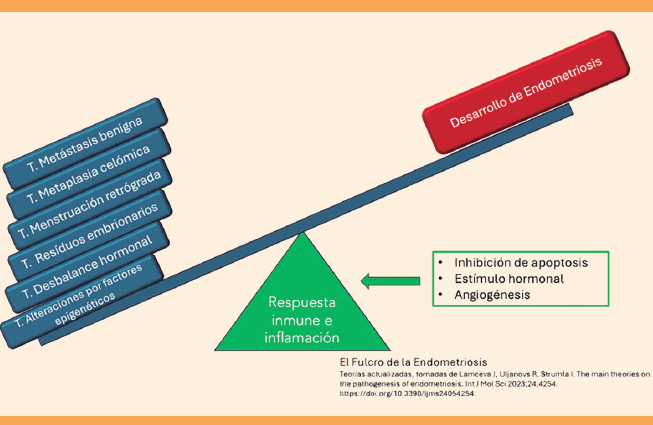
Figura 1 El fulcro de la endometriosis. Todas las teorías referentes a la fisiopatología de la endometriosis confluyen en un punto decisivo: un proceso inflamatorio en donde participa una respuesta autoinmunitaria que se expresa con dolor e infertilidad secundaria a un proceso pélvico inflamatorio. Por ello, el sistema inmunológico se ve como un “fulcro”; es decir, el punto pivote que conduce a la inflamación y sus complicaciones.
A nivel global se estima que el 10% de las mujeres en edad reproductiva tienen algún grado de endometriosis. Su diagnóstico siempre ha sido complicado ya que un porcentaje significativo de pacientes pueden ser asintomáticas o tener manifestaciones atípicas.3,4 En México, debido a los pocos estudios epidemiológicos al respecto y la complejidad del diagnóstico se estima que, de la población con infertilidad, el 34.5% tiene endometriosis y de los que recurren a tratamientos de reproducción asistida, la prevalencia de endometriosis es de 0.7%.5,6 Esto deja fuera a las pacientes con sintomatología de dolor severo por lo que se especula que la población pueda ser mucho mayor.
METODOLOGÍA
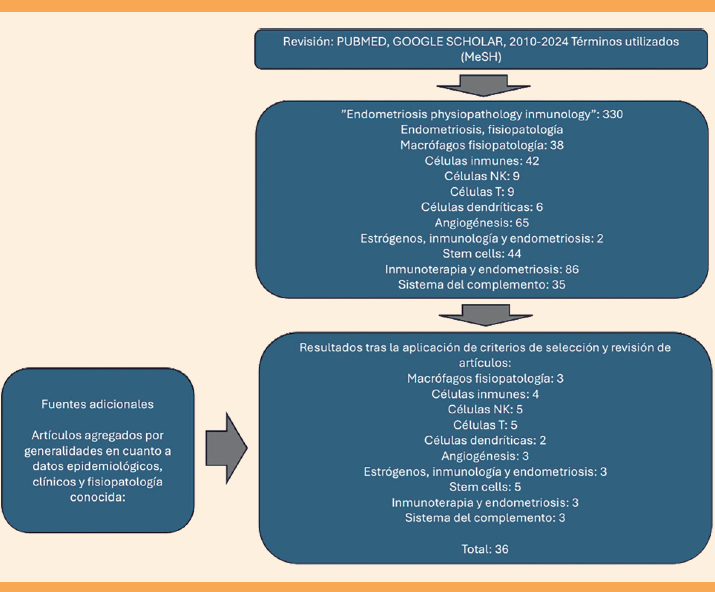
Estudio retrospectivo en el que se buscaron artículos publicados de 2010 a 2024 en las bases de datos de PUBMED (National Library of Medicine) y Google Académico, buscando los términos específicos con las palabras clave (MeSH): “endometriosis and physiopathology inmunology”, generando 75 resultados por lo que se buscaron las células inmunitarias implicadas, estrógenos, angiogénesis e inmunoterapia con los siguientes resultados: “endometriosis and macrophages physiopathology”, generó 38 resultados escogiendo 3, “endometriosis and inmune cells physiopathology” generó 42 y se seleccionaron 4 , “endometriosis and NK cells physiopathology” generó 9 artículos y se seleccionaron 5, “endometriosis and T cell physiopathology generó 9 artículos y se seleccionaron 5; “endometriosis and angiogénesis physiopathology” generó 65 y se escogieron 3, “estrogens and endometriosis inummunology” generó 3, seleccionándose estas, “endometriosis and stem cells physiopathology” generó 44, seleccionamos 5, “inmunotherapy endometriosis” generó 86 artículos y se escogieron 3, “endometriosis and complement system, generó 35 resultados y se seleccionaron 3. Descartamos artículos que no tuvieran en enfoque central en endometriosis, así como aquellos que presentaran teorías inmunológicas enfocadas más en moléculas específicas y no en el desarrollo de endometriosis. También eliminamos artículos repetidos en cada búsqueda. Se seleccionaron artículos que mencionan mecanismos inmunológicos específicos que desarrollan endometriosis y su potencial uso terapéutico, agregando 6 artículos. La búsqueda generó un total de 84 y se seleccionaron 36. Algunos artículos incluidos son previos a 2010, debido a su importancia para el presente manuscrito fueron incluidos, también se incluimos artículos que hacen referencia a generalidades, manifestaciones clínicas, epidemiología y otras generalidades de la patología en cuestión. Con ello tenemos un total de 43 artículos utilizados como referencia. Figura 2
Complicaciones para el estudio de la endometriosis
La endometriosis está claramente asociada al sistema autoinmunitario observando fisiopatología asociada con enfermedades como lupus eritematoso sistémico, síndrome de Sjögren, artritis reumatoide, alteraciones autoinmunitarias de la tiroides, enfermedad celiaca, esclerosis múltiple, enfermedad intestinal inflamatoria y enfermedad de Addison.7 Con base en lo anterior puede considerarse una proclividad con fundamento fisiopatológico para el desarrollo de las alteraciones que llevan a desarrollar endometriosis.
Debido a que la fisiopatología de la endometriosis permanece elusiva y basada en teorías, el conocimiento que se tiene al respecto se circunscribe a modelos animales como primates y humanos donde se induce el desarrollo de implantes. El ratón ha ofrecido una plataforma versátil y económica para estudiar a los implantes endometriósicos aunque aún se tienen que mejorar las variables celulares y, con ello, poder generar estudios transgeneracionales a largo plazo a fin de establecer la conducta de esta afección.8
Alteraciones inmunológicas
Una de las propuestas más estudiadas en la fisiopatología de la endometriosis es la desregulación inmunológica caracterizada por un reclutamiento de células inmunitarias, adhesión celular e incremento en el proceso inflamatorio que puede facilitar la supervivencia de la célula endometriósica. Está demostrado cómo ciertos patrones de metilación en genes se asocian desde la modulación de la respuesta inmunológica, hasta la regulación de la apoptosis.9 Con independencia de las teorías propuestas para la generación de la apoptosis, la célula de endometriosis sobrevive en un medio altamente protegido por el sistema autoinmunológico, por lo que una alteración en la inmunomodulación puede facilitar su existencia.10
Células inmunitarias
El microambiente endometriósico y las lesiones endometriósicas muestran una cantidad aumentada de macrófagos M2 (con actividad angiogénica). En las células endometriales eutópicas la población dominante es de macrófagos M1. Los macrófagos peritoneales de pacientes con endometriosis muestran mayor activación de factores proinflamatorios: factor kappa B, factor de necrosis tumoral alfa (TNF-a), interleucina 6 (IL-6) e interleucina 1 beta (IL-1 beta). En pacientes sanas los monocitos estimulados inhiben la proliferación endometrial, lo que contrasta con el estímulo proliferativo en pacientes con endometriosis.11
Otras células ampliamente estudiadas con las uterine Natural Killer (uNK), caracterizadas por una menor citotoxicidad, facilitan la implantación embrionaria. Las células uNK presentes en peritoneo también expresan esta citotoxicidad disminuida, con menor capacidad para inducir apoptosis, disminuyendo su eficacia ante la presencia de agentes externos.12 Factores identificados como potenciales inhibidores de las células NK son IL-6, TGF-beta1 e interleucina 15 (IL-15). Los mastocitos aumentan su actividad y número durante la menstruación, participando en la angiogénesis y regeneración del endometrio, sus números también se ven aumentados en las lesiones endometriósicas, así como su producción de citocinas proinflamatorias como el factor de necrosis tumoral alfa (TNF-alfa).9 Estos también se acumulan en lesiones de endometriosis profunda, sugiriendo un papel en el dolor e hiperalgesia de estas lesiones, y con el proceso de adhesión y fibrosis.13
Los neutrófilos, elementos decisivos para la respuesta inflamatoria, también se elevan significativamente en el endometrio eutópico de pacientes con endometriosis. Hay un aumento de radicales de oxígeno (ROS) y expresión de CD11b. Estos neutrófilos, al ser liberados al líquido peritoneal producen VEGF, IL-8 y CXCL10, lo que conduce al avance de la enfermedad.11 Figura 3
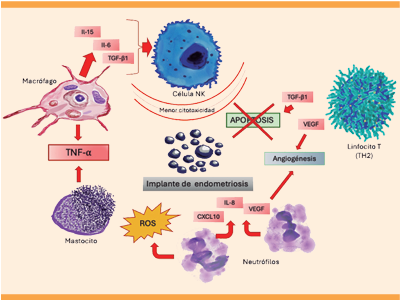
Figura 3 Elementos inmunitarios de la fisiopatología de la endometriosis. Se resume la participación de varios factores inmunitarios para la supervivencia del implante endometriósico. La célula NK tiene afectada la citotoxicidad por lo que no comunica o activa otros factores citotóxicos, tampoco puede participar en la activación de la endometriosis. El linfocito T (TH2), al incrementar la expresión de VEGF y TGF-β1, inhibe la apoptosis y estimula la angiogénesis; ambos favorecen el crecimiento del implante endometriósico. Los neutrófilos secretan también VEGF, IL-8, CXCL-10 y ROS lo que hace que disminuya la efectividad de los factores inmunitarios para eliminar al implante. El mastocito libera TNF-a, que activa otros factores proinflamatorios y el macrófago activado libera, también, TNF-a y otros factores como IL-15, IL-6 y TGF-β 1 que promueven la inflamación e inhiben la actividad citotóxica de la célula NK.
Células Natural Killer (NK)
Varias observaciones relacionadas con la citotoxicidad abrogada de las células NK se han citado como uno de los factores más relevantes para la capacidad de supervivencia de las células endometriósicas, particularmente la propuesta de la teoría del reflujo menstrual.14 Es importante identificar los puntos de censo de la actividad autoinmunitaria porque las células NK deben exponerse a los factores en estos puntos para lograr su activación. La eliminación o evasión de alguno de estos puntos de censo que contienen sistemas moleculares y enzimáticos, pueden llevar a una inactividad de las células NK y de algunos macrófagos.15 Todos estos puntos de censo pueden actuar como blancos terapéuticos para endometriosis. Las células NK son grandes linfocitos granulares con fenotipos de diferenciación CD3-CD56+CD16 ± CD57±, capaces de reconocer y destruir una gran variedad de células infectadas por virus, células neoplásicas o bajo estrés.
Otras acciones identificadas son: la presentación de antígenos, autoinmunidad, inflamación, embarazo y rechazo de transplantes.16 El 90% de la población de células NK se divide en dos poblaciones: CD56dimCD16+ (altamente citotóxicas) y las CD56brightCD16- con funciones reguladoras al producir citocinas como interferón gamma (INF-g) y TNF. En el útero, las CD56bright se encuentran en el endometrio y participan en la remodelación de las arterias espirales, desarrollo placentario y mantenimiento del embarazo.16 La citotoxicidad de estas células es a través de la inducción de apoptosis en células blanco que liberan los gránulos citolíticos o por activación del receptor Fas o TRAIL, con la activación de granzimas y perforinas, esenciales para eliminar a la célula blanco17 Las células NK identifican a las células blanco a través de moléculas de adhesión, factores estimulantes e inhibitorios de receptores de inmunoglobulinas tipo asesinas (KIRs), (glicoproteínas expresadas en la superficie de las células NK), así como los receptores con inmunoglobulinas tipo leucocitos (LILRs), receptores de citotoxicidad natural (NCRs) y receptores de asesinos celulares tipo lectina (KLRs) así como receptores para NK y subfamilias (NKRP1). Todos constituyen los puntos de censo para la progresión, funcionamiento y activación de las células NK.16
El riesgo de citotoxicidad en pacientes con endometriosis se describió en células NK comparadas con células K562; sin embargo, sus mecanismos aún no están totalmente descritos. Al parecer se deben, parcialmente, a una variación en la cantidad de células efectoras circulantes CD57+CD16- o CD56+CD16+NK.18 Los reportes son controvertidos, por lo que la disminución de poblaciones celulares no explica la afectación de las células NK y su citotoxicidad. Esto sugiere un mecanismo alterado o alguna deficiencia cualitativa de las proteínas implicadas.
La inhibición de la citotoxicidad de las células NK en endometriosis puede ser secundaria a una expresión alterada en la estimulación e inhibición de los receptores de las células NK. Existen varios receptores inhibitorios de estas células con expresión aumentada ante endometriosis, como el antígeno de leucocitos humanos (HLA)-C2 que reconoce al receptor inhibitorio KIR2DL1 en sangre y líquido peritoneal, lo mismo sucede con KIR3DL1. La familia de los receptores KIR reconoce las moléculas del complejo mayor de histocompatibilidad I (MHC I), que se han visto con una expresión aumentada en el endometrio de pacientes con endometriosis. Entre los complejos inhibitorios, destaca la sobreexpresión de NKG2A (un complejo inhibitorio de citotoxicidad para células NK) en el líquido peritoneal de pacientes con endometriosis, MICA (complejo mayor de histocompatibilidad clase I, cadena A) y MICB (cadena b), su incremento parece correlacionarse con la gravedad de la enfermedad, lo que afecta la respuesta de las células NK.
Otras moléculas ampliamente estudiadas en endometriosis son las moléculas de adhesión intercelular (ICAM), con una participación en el proceso de adhesión del implante endometriósico, que requiere interacción con el antígeno de función leucocitaria (LFA-1). Al parecer, las moléculas de adhesión intercelular pueden actuar como inhibidoras de la citotoxicidad de NK. Existen varios estudios en controversia referentes al nivel de expresión de ICAM, cuya cantidad puede afectar la eficacia de las células NK.16,18
Existen varias citocinas cuya acción inhibitoria interfiere con la respuesta autoinmunitaria, entre estas destacan: el factor de transformación y crecimiento beta (TGF-β), el propio líquido peritoneal y, la IL-6 que afecta a granzima B y perforina (ambas proteasas propias de las células NK con efectos citolíticos), las interleucinas 10 y 12.18
Los receptores “killer cell immunoglobulin like receptors” (KIR) contienen 14 genes relacionados con tipos específicos de KIR y polimorfismos, hay 30 haplotipos, el grupo A tiene 9 genes inhibitorios y el grupo B es muy variable en sus funciones. Esto sugiere una gran variedad de combinaciones de haplotipos y genes que pueden establecer una función inhibitoria. A la fecha, solo se han visto polimorfismos de genes inhibitorios identificados como LILRB1 y LILRB2. En los estudios actuales se ha reportado mayor incidencia de endometriosis en pacientes con menor expresión de KIR3DS1 y KIR2DS5.19 Las células NK tienen varios niveles de expresión y factores con potencial terapéutico.
Los exosomas (vesículas extracelulares con propiedades inmunomoduladoras) pueden alterar la respuesta inmunitaria a través de una disminución de la citotoxicidad de NKG2D y de la apoptosis inducida por FasL/TRIAL de células autoinmunitarias activadas. Funcionan como un escudo alrededor de la lesión endometriósica al generar un gradiente inmunosupresor que protege al implante.20 Figura 4
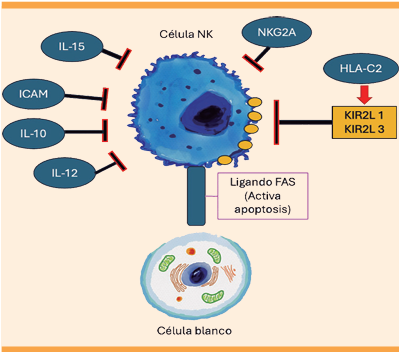
Figura 4 Inhibición de las células NK. Existen varios factores, como las interleucinas, indispensables en un proceso inflamatorio en donde participan en la señalización (IL-15, IL-10, IL-12) e inhibición de la respuesta citotóxica de la célula NK. ICAM logra adherir al implante endometriósico a la superficie peritoneal, junto con una sobreexpresión de NKG2A que generan una fuerte inhibición de la citotoxicidad de la célula NK. El factor HLA-C2 promueve la expresión de KIR2L1 y 3 e interfiere con los receptores y la capacidad de interacción de la célula NK. Con la expresión de estos factores y los exosomas se afecta la función del ligando FAS, que bloquea la activación de la apoptosis en la célula de endometriosis.
Linfocitos T
Los linfocitos T de mujeres con endometriosis también exhiben una menor citotoxicidad aparente, reversible por estimulación con IL-2.11,21 Un mecanismo que debilita la respuesta de los linfocitos T es el ligando Fas (FasL) que, junto con IL-8 y CCL-2, son componentes que activan la apoptosis de los linfocitos. También hay un decremento en la relación de CD4:CD8 que disminuye su activación.9,12 Las interleucinas 4 y 10 se encuentran aumentadas en linfocitos de mujeres con endometriosis y en combinación con una baja en el IFN-g conduce a un predominio de las células T cooperadoras tipo 2 (Th2), decisivas para la existencia de anticuerpos antinucleares, anti-ADN y anti-fosfolipídicos que afectan al endometrio y a los espermatozoides.22
Células dendríticas
Las células dendríticas son las principales responsables de la presentación de antígenos porque permiten la reacción coordinada del sistema inmunitario innato y adaptativo. Pueden activar células B, NK y NKT, inducir moléculas MHC, procesar antígenos para la diferenciación de células T específicas al patógeno presentado,23 y secretar citocinas que promueven la tolerancia inmunológica.24
Esas células derivan de células progenitoras hematopoyéticas (CD34+) de la médula ósea; generan líneas mieloides y plasmocitoides. En estudios efectuados en animales y en humanos ha quedado demostrado que las células dendríticas forman parte de lesiones endometriósicas; son más abundantes que en el endometrio eutópico. Se observan, también, en el líquido peritoneal, con citocinas IL-2 y 10. Su existencia cerca de la neovascularidad de lesiones endometriósicas y su respuesta a VEGF sugiere una participación en la angiogénesis, característica de las células inmaduras.24
Alarminas y patrones moleculares
Las alarminas, o patrones moleculares asociados a daño (DAMPs), son moléculas inmunoestimulantes liberadas ante una lesión tisular. Una de estas es el grupo de alta movilidad caja 1 (HMGB1) que se encuentra en el flujo menstrual, que actúa como mediador y factor angiogénico a través del receptor de productos de glicación avanzada (RAGE) y por los receptores cuota o “toll like receptor-4” (TLR-4). TLR-4 se expresa en macrófagos, células dendríticas, neutrófilos y células NK. Su estímulo angiogénico causa un incremento de VEGF, lo que sugiere una participación en la patogenia de la endometriosis.25,26Estos patrones de receptores de reconocimiento (PRR), reconocen patrones moleculares asociados con patógenos, como lipopolisacáridos bacterianos, lipoproteínas, ARN viral y paredes celulares micóticas. Cuando estos patrones se reconocen se inicia una reacción con su receptor-ligando, que genera una respuesta inmunitaria y la remoción del patógeno.
Existen cinco familias de PRR: 1) receptores tipo cuota (Toll-like receptors, TLR), 2) receptores tipo c-lectina (CLR), 3) receptores tipo nodo (NLR), 4) receptores de genes de ácido retinoico inducibles (RLR) y 5) receptores ausentes en melanoma 2 (AIM-2). Cada una de estas familias se ha relacionada con la activación de diferentes citocinas proinflamatorias: TNF-a, INF-γ, IL-1β, IL-6, IL-18, entre otras. La endometriosis puede iniciar con un proceso infeccioso que detona la respuesta de algún complejo PRR, posteriormente una inflamación aséptica que puede inhibir la apoptosis y generar una desregulación inmunitaria. En la actualidad se estudia su posible utilidad como marcadores séricos para endometriosis. Al mismo tiempo se ha descubierto cómo la aspirina puede regular a TLR4 y a los receptores NLR. De la misma manera, la progesterona puede suprimir la expresión de TLR7, NLRP3-caspasa-1 y, con ello, modificar la respuesta del inflamosoma.26
Los receptores tipo c-lectina (CLR) están directamente implicados en la identificación de las formas de los carbohidratos,27 y son imprescindibles para iniciar la respuesta anti-inflamatoria inmunitaria por su acción combinada con moléculas de adaptación de ARN mensajero, inmunoglobulina G, A y M. Estas interacciones también las hacen un potencial blanco terapéutico.26
Mecanismos adaptativos inmunitarios en endometriosis
Los mecanismos de la inmunidad adaptativa, establecidos por linfocitos T y los anticuerpos producidos por linfocitos B, se han visto implicados en la aparición de endometriosis.27
Las células T son CD-4+ y, en el caso de la endometriosis, prevalecen las citocinas tipo 2 y, por ende, una respuesta TH2. En el caso de TH17 existe una mayor expresión de las interleucinas 10 y 17 que induce la aparición de citocinas angiogénicas, como la IL-17 que promueve la inflamación en endometriosis. Las células T reguladoras (Treg) parecen tener participación en el dolor pélvico y en la infertilidad. Se asocian con varias citocinas y quimiocinas que participan con Treg. En el líquido peritoneal de pacientes con endometriosis se ha observado una gran cantidad de CD4+, CD25+, Foxp3+ asociadas con Tregs,28 sin establecer un mecanismo directo para desencadenar la enfermedad. Tregs solo están asociados con una participación en la inflamación, proliferación, angiogénesis e invasión. CCL25 tiene mayor expresión en endometriosis: expresa Tregs y produce IL-10 y TGF-β, así como supresión de la apoptosis.
Los linfocitos B, además de su producción de anticuerpos, también participan en la generación de las IL-6, IL-17, factor estimulante de colonias de granulocitos-macrófagos entre otros factores que modulan la respuesta inmunitaria. En casos de endometriosis el estimulador de linfocitos B se ha visto aumentado lo que sugiere un mecanismo independiente al de las células T. La participación de linfocitos B en endometriosis requiere más estudios.15,29
Angiogénesis
Para que aparezca la lesión endometriósica se requiere de la angiogénesis, misma que es regulada por células inmunitarias y sus mecanismos de desarrollo. Se ha especulado que la interferencia de este proceso puede ofrecer una alternativa de tratamiento. El factor de crecimiento vascular (VEGF) parece incrementarse cuando ya hay una lesión endometriósica, lo que establece un mecanismo de supervivencia para el implante de endometriosis. La expresión del factor de crecimiento vascular se ha observado en el estroma, epitelio glandular y macrófagos infiltrantes. La interacción de citocinas, factores de crecimiento y factores angiogénicos establece la progresión de los implantes endometriósicos. Citocinas como la interleucina 1β (IL-1β), interleucina 6 (IL-6), e interleucina 8 (IL-8) actúan como factores proangiogénicos. La interleucina 17 incrementa estos factores y el factor de crecimiento vascular. Las concentraciones fluctuantes de estrógenos y progesterona pueden alterar la expresión del factor de crecimiento vascular en el endometrio eutópico y en endometriosis. Se han determinado factores de transcripción que también intervienen en este proceso, como el factor inducible por hipoxia (HIF-1 alfa), receptores de estrógenos, aromatasa y el factor esteroidogénico 1 (SF1).15,30
Al parecer, el 17-b estradiol incrementa la expresión del factor de crecimiento vascular a través de un eje Wnt/b-catenina. Los receptores estrogénicos alfa regulan la neuroangiogénesis en la pared peritoneal y el receptor estrogénico b regula a HIF-1 alfa, factor de crecimiento vascular y a la angiotensina 1. En lesiones por endometriosis, macrófagos, hormonas asociadas con estrés e inflamación por endometriosis los receptores estrogénicos asociados con la proteína G tienen concentraciones elevadas. Algunos compuestos hormonales, como la melatonina, pueden generar una regulación proapoptósica vía la regulación de la actividad de metalopeptidasas así como el sorafenib tiene efecto antiproliferativo en MAPK/ERK y actividad antiangiogénica en VEGF.31 Algunos bloqueadores angiogénicos podrían ser una alternativa para tratar endometriosis, como la quinagolida, las estatinas, bevacizumab, leuprolide, progesterona y danazol que causan una reducción en la densidad microvascular y expresión de VEGF/VEGFR2 entre otros genes. También se ha visto la reducción de áreas vascularizadas con celecoxib, rofecoxib y parecoxib.30
Estrógenos y la inmunidad
Los estrógenos claramente inducen la aparición de lesiones endometriósicas que logran la biosíntesis de esta hormona de forma local junto con el proceso inflamatorio, asegurando su crecimiento y supervivencia en el medio peritoneal. El estradiol activa sus receptores ERalfa y β (ERa, ERβ) cuya expresión se ve alterada en el tejido endometriósico. En específico, ERa promueve la proliferación, adhesión y angiogénesis de las lesiones. E2/ERa/IL6 parece estar implicada en el inicio de lesiones y algunas isoformas proteicas como el coactivador 1 del receptor esteroideo (SRC-1) que interactúan con receptores estrogénicos (ERβ).31,32 Estos receptores también promueven al TNFa en sus funciones proinflamatorias con la activación de citocinas y metaloproteinasa 9, además de inhibir la apoptosis celular. El receptor ER promueve la activación de receptores de compuestos pertenecientes al inflamosoma que perpetúa la producción de IL-1β y, con ello, la inflamación. Se ha experimentado la indicación de clorindazole y oxabiciclohepteno sulfonato que logran mediar la expresión de los receptores ERa y ERβ, respectivamente, al reducir la proliferación, vascularización, inflamación, producción de citocinas e infiltración de macrófagos. Al parecer estas sustancias no parecen alterar la fertilidad o los ciclos estros en los modelos experimentales de roedores.30,32.Figura 5
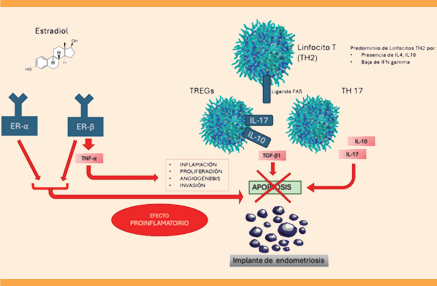
Figura 5 Células autoinmunitarias: macrófagos, linfocitos T, neutrófilos y células NK que expresan interleucinas, citocinas y estimulan VEGF. La hipoxia es el estímulo esencial para la angiogénesis al activar HIF-1α. La aromatasa y el factor esteroidogénico 1, junto con factores del estroma y epitelio glandular, incrementan VEGF y promueven la angiogénesis.
Sistema del complemento
La vía del complemento posee varias proteínas que inducen la activación de varios precursores, reguladores y receptores celulares de superficie que reconocen patógenos, células necróticas o la apoptosis, agregados proteicos y células tumorales. También puede actuar como un modulador de la respuesta inmunitaria adaptativa. Existen tres vías principales: clásica, lectina y la alterna, con diferentes complejos que inician su cascada y convergen en la C3 convertasa, desde donde continúan con una cascada común. Componentes como C5 llevan a la formación de complejos que generan un desequilibrio osmótico celular al inducir la lisis de la célula.33
Varios factores del complemento se expresan en las lesiones por endometriosis. En 1980 se confirmó la existencia de C3 y C4, además de la de polimorfismos de nucleótido único (SNP’s) que aumentan la expresión de C3.29 En la vía alterna se ve una activación por properidina, pero destaca como el perfil genético de células endometriósicas y del endometrio presentan a C3, C7, SERPIN5 y PTX3.34 Al parecer, el estradiol es un factor estimulador para la expresión de C3, con la existencia de TNF-a y IL1-β, aumentados en casos de endometriosis.35 Otras moléculas coexistentes son: el factor B, factor D, factor H y manosa asociada con serina proteasa 1(MASP1) que contribuyen a la activación de la vía del complemento y al proceso inflamatorio.29 El peritoneo también puede generar la activación de C3a y C5a, anafilotoxinas que estimulan a los macrófagos e inician una cascada que deriva en inflamación y dolor.
Inmunoterapia para endometriosis
Hoy en día ninguno de los tratamientos para la endometriosis cura o elimina la enfermedad, simplemente disminuyen la cantidad y concentración de las lesiones y evitan el surgimiento de nuevos focos endometriósicos. La cirugía no puede garantizar la eliminación total de estos focos que, además de las tasas de reincidencia, se asocian con disecciones extensas, dolorosas y con alta posibilidad de generar más adherencias y distorsión anatómica. Debido a esto, la inmunoterapia es una alternativa que amerita ser estudiada.
Entre los factores inmunitarios para la endometriosis destaca la fagocitosis por macrófagos. La expresión de CD-47 bloquea la fagocitosis de la célula blanco, que se expresa en la endometriosis; la indicación de siRNA o anticuerpos neutralizantes disminuye la expresión de CD47 y con ello induce la fagocitosis de la célula.36
Las células NK requieren de moléculas que constituyen puntos de revisión, importantes para su adecuada activación. Esto sugiere que C3 puede generar un desequilibrio en la función de las células NK y, con ello, un inhibidor de C3 (iC3b/CR3) puede mejorar la respuesta citotóxica de las células NK.29 Los probióticos orales también pueden activar a las células NK al disminuir la formación de endometriosis y un extracto del árbol Hexilor A puede efectuar esa activación.36
Bloquear el sistema del complemento, particularmente al factor C5 y detener la respuesta inflamatoria excesiva, es una propuesta prometedora. Se contempla la indicación de medicamentos como eculizumab (actualmente indicado para angioedema hereditario y hemoglobinuria paroxística nocturna), ravulizumab (con las mismas indicaciones), y crovalimab. A estos últimos se les han incorporado residuos de histidina en las regiones utilizadas para fijar el antígeno lo que hace que el anticuerpo pierda su afinidad en el medio ácido (pH 6.0) del endosoma. Estos anticuerpos se dirigen a C5, lo que no bloquea a C3, lo que complica la situación porque este último es un factor clave para el inicio de la lesión endometriósica. Un inhibidor dirigido a C3 es AMY-101, indicado en pacientes con COVID-19 lo mismo que narsoplimab.29
La inhibición del TNF, producido por macrófagos, podría tener una repercusión en la enfermedad, para la pentoxifilina, leflunomida, etanercept, infliximab y la proteína recombinante fijadora de TNF, por lo que prometen resultados positivos al respecto. La pentoxifilina inhibe la producción de mediadores proinflamatorios, la fagocitosis y la producción de radicales de oxígeno (ROS) lo que disminuye la inflamación del TNF e IL-1.37
Otras propuesta es la loratadina, que tiene un efecto inmunomodulador en mastocitos. Se ha visto, también, su estimulación en macrófagos, células T, aumento de la citotoxicidad de células NK y proliferación de células B, así mismo IL-1alfa, TNF, TNF-beta, IL-6 e INF-a y γ, son blancos potenciales para la loratadina.38
Otros inmunomoduladores en estudio son: interferón, danazol, inhibidores de la ciclooxigenasa y las estatinas, estas últimas parecen inhibir la expresión de genes inflamatorios; destaca la proteína de quimio-atracción para monocitos 1 (MCP-1), que activa monocitos y macrófagos.27,38 Cuadro 1
Cuadro 1 Inmunomoduladores en estudio
| Estrategia terapéutica inmunológica | Mecanismos principales |
|---|---|
| Actividad de células NK | Bloquear los puntos de control con respuesta negativa de células NK |
| Vacunas inmunorreguladoras y BCG | Aumento de citotoxicidad de células NK y de población de células NK, reprogamación de monocitos, inducción de inmunidad Th1, modificación en la secreción de citocinas proinflamatorias: interferón gamma, TNF alfa, IL-2, IL-17 e IL-6; citocinas de Th2 (IL-4, IL-5, IL-10), factores de crecimiento y quimiocinas |
| Antagonistas de receptores opiáceos | Naltrexona a baja dosis, modula a las células dendríticas y macrófagos, evita la proliferación de CD4+, CD8+T y linfocitos B. Disminuye los síntomas |
| Antagonistas de TNF | Disminuyen el tamaño de la lesión, mejoran la fertilidad. El etanercept aumenta la tasa de embarazos en reproducción asistida |
| Liodol | En pacientes con endometriosis mejora la respuesta de las células NK, células dendríticas, células TREG y la respuesta peritoneal inhibe a los macrófagos y detiene la proliferación de linfocitos peritoneales |
| Factor estimulante de colonias de granulocitos | Reclutamiento de neutrófilos en el ovario y disminución de la incidencia del folículo luteinizado no roto |
| Aminorar situaciones de hipoxia tisular | Abolición de mecanismos dependientes de hipoxia que afectan la implantación, vigilancia inmunológica y la aparición de lesiones endometriósicas |
| Agentes aprobados para tratamiento de endometriosis dirigidos a la vía del complemento | Ravalizumab, Eculizumab(actúan sobre C5; en fase 3 de desarrollo: Avacopan, Nomacopan (actúan sobre C5 y C5a/C5aR), Narsoplimab (actúa sobre la vía de las lectinas), APL-2 (actúa sobre la vía alterna C3), Berinert y Sutimlimab (actúa sobre la vía clásica) |
| Resveratrol | Actividad antiangiogénica, antioxidante, proapoptósica, regulación hormonal y antiadherente |
Células madre
Las características fisiológicas del endometrio uterino sugieren la existencia de células madre, progenitoras de las células endometriales de cada ciclo menstrual que derivan del endometrio basal.39 Estas células se denominan: CD140b+CD146+ o SUSD2+, células madre mesequimales derivadas del endometrio (endometrial epitelial stem/progenitor cells, eMSCs). Las células derivadas del flujo menstrual son células madre menstruales (menstrual stem cells, MenSCs). Las poblaciones de CD146+CD140b+ tienen porcentajes y capacidad de clonación en relación con las fases del ciclo menstrual, con incrementos de la expresión 1518, genes en estas poblaciones celulares, varios de ellos implicados en procesos de angiogénesis, inmunomodulación, respuestas a hormonas esteroideas, hipoxia, inflamación, comunicación celular, proteólisis y en la expresión del factor de crecimiento tipo insulinoide (IGF), Notch, TGF-beta y varias proteínas.40 Un marcador útil para estas poblaciones celulares es SUSD2+, que distingue a un grupo de células de la familia de eMSCs perivasculares tanto en el estrato endometrial basal como el funcional.
Las células troncales menstruales (MenSCs) se identificaron a partir de la sangre menstrual, al igual que las eMSCs tienen el potencial de diferenciarse en varios tejidos. Las células MenSCs pueden interactuar con varios tipos de células inmunitarias: monocitos en sangre menstrual que pueden ser inducidos a células dendríticas y estas detectar patógenos al activar la inmunidad adaptativa y la inmunomoduladora, observada en células T CD4+ y CD8+, al disminuir la expresión de IL-1β, IL-6, y TNF-a de ratones, recibiendo un transplante de MenSCs.39,40,41
Varios estudios han identificado patrones cíclicos en la expresión de receptores estrogénicos y de progesterona en las células del estrato basal en el endometrio de lesiones endometriósicas, donde destaca la expresión de factores como Musashi-1, OCT 4, SOX 15, SOX 2, C kt, Notch y Numb y la importina 13. Aquí se observan telómeros más largos en linfocitos de endometriosis, que en controles sanos, lo que apoya el origen de la endometriosis a partir de células troncales (stem cells).40,41
Si se parte del concepto de que el microambiente del líquido peritoneal altera la respuesta inmunitaria, la angiogénesis, la proliferación celular, la adhesión celular y la apoptosis se requiere de un patrón de expresión específico de proteínas, particularmente en endometriosis profunda. Los fragmentos de endometrio en peritoneo interactúan con citocinas, secretan quimiocinas y llevan a la inducción de células madre derivadas de la médula ósea (BMDSCs). Se han identificado 74 citocinas aumentadas en el líquido peritoneal con endometriosis. Las células madre mesenquimales (eMSCs) ectópicas de endometriosis tienen mayor capacidad proliferativa, migración y angiogénesis que los eutópicos y, mayor expresión de COX-2. Estos cambios en la expresión de genes asociados con células troncales se han propuesto como una causa de endometriosis.40,41,42
Las células madre derivadas de la médula ósea incrementan la proliferación de células endometriales ectópicas a través de la secreción de citocinas. En este proceso, las células endometriósicas estimulan a las células madre derivadas de la médula ósea y aumentan la expresión de PD-1 en células T. Además, las células troncales migran al endometrio uterino, donde inducen una disfunción del endometrio eutópico. El 17-β estradiol promueve la quimiotaxis y migración de células madre derivadas de la médula ósea al aumentar la secreción de la quimiocina SDF-1alfa. Otros factores expresados por células madre derivadas de la médula ósea son: CXCR4, receptor de CXCL12, este agonista parece guiar la migración de las células troncales, lo que promueve la implantación de nuevas lesiones endometriósicas.42,43
Independiente de su localización, estas células logran sobrevivir en medios potencialmente hostiles a todo tejido ajeno a dichas zonas histoanatómicas. Los mecanismos propios celulares, como la apoptosis, son inhibidos. Varios factores proinflamatorios son estimulados por diversas vías y de forma simultánea, las hormonas propias para el desarrollo del ciclo menstrual como los estrógenos, estimulan a sus receptores que, a su vez, estimulan sistemas proinflamatorios y, finalmente, la angiogénesis que es decisiva para la supervivencia del implante o lesión de endometriosis. Un tratamiento dirigido contra alguna de estas proteínas o moléculas autoinmunitarias puede detener o disminuir el proceso inflamatorio, mejorar la respuesta inmunológica o suprimir la angiogénesis. Esto podría tener un verdadero efecto en el control o curación a nivel celular y clínico de la endometriosis.
CONCLUSIONES
El tratamiento actual de la endometriosis es insuficiente para atender los principales problemas clínicos asociados con esta enfermedad: infertilidad, dolor pélvico o la dismenorrea. Todas las teorías de inicio de la endometriosis convergen en el punto del surgimiento de una lesión endometriósica que genera un proceso inflamatorio y la subsecuente fibrosis y adherencias. La respuesta autoinmunitaria afectada, la estimulación de vías inflamatorias y del complemento, los receptores estrogénicos, las células NK, la angiogénesis y la supresión de la apoptosis presentan varias proteínas en su fisiología que pueden ser blancos potenciales para su inhibición, neutralización o, bien, estimulación para inhibir la formación de la lesión de endometriosis, lo que aportaría un tratamiento de mayor precisión y efectividad.











 nueva página del texto (beta)
nueva página del texto (beta)