METODOLOGÍA
Se llevó a cabo una revisión semisistemática que incluyó artículos en inglés y español, de tipo ensayos clínicos controlados, estudios de cohorte y observacionales, con fecha de publicación de los últimos 11 años (2014 a 2024). La búsqueda de referencias estuvo limitada a la base de datos PubMed-Medline (https://pubmed.ncbi.nlm.nih.gov) con la estrategia de búsqueda definida por las palabras clave (MeSH): “Hemorrhage/prevention & control”, “Hemorrhage/therapy”, y operadores boleanos para combinarlos: (“Postpartum Hemorrhage”[MeSH] OR “postpartum hemorrhage” OR “PPH”) AND (“prevention”[MeSH] OR “management”[MeSH] OR “treatment”[MeSH]) AND (“vacuum-induced”[All Fields] AND (“uterin”[All Fields] OR “uterines"”[All Fields] OR “uterus”[MeSH Terms] OR “uterus”[All Fields] OR “uterine”[All Fields]) AND (“tamponade”[All Fields] OR “tamponaded”[All Fields] OR “tamponades”. La misma estrategia de búsqueda se siguió en buscadores de sitios web oficiales relevantes: International Federation of Gynecology and Obstetrics (FIGO, https://www.figo.org/), World Health Organization (WHO, https://www.who.int/), American College of Obstetricians and Gynecologists (ACOG, https://www.acog.org/), y California Maternal Quality Care Collaborative (CMQCC, https://www.cmqcc.org/).
Se encontraron 1083 artículos. En la primera fase del proceso de selección (título y resumen) se conservaron 300 artículos. En la segunda fase (texto completo) se seleccionaron 35 y el resto se rechazaron por no estar directamente relacionados con la hemorragia posparto, artículos duplicados, estudios con metodología débil o no relevantes. Este diseño se denomina revisión híbrida, semisistemática o revisión narrativa aumentada. La estrategia definida de búsqueda puede facilitar una selección sistemática de los artículos más relevantes, en este caso enfocada en identificar intervenciones efectivas y basadas en evidencia para controlar la hemorragia posparto. Como limitación, no se realiza un metanálisis ni se evalúa el riesgo de sesgo de los estudios clínicos disponibles, por lo que es menos rigurosa que una revisión sistemática formal.
ANTECEDENTES
Epidemiologia y definición
En todo el mundo la hemorragia obstétrica es la principal causa evitable de muerte materna directa, representa alrededor del 27.1% de éstas.1,2,3 La prevalencia de hemorragia posparto varía de una región a otra, desde 7.2% en Oceanía, 8% en Latinoamérica y 25.7% en África.4 La mortalidad materna por hemorragia posparto representa 21% de los casos en Latinoamérica,5 mientras que una de cada cinco muertes maternas en América se debe a hemorragia obstétrica durante o inmediatamente después del parto.6 En México, el informe de vigilancia epidemiológica indica que, en 2023, la incidencia de muerte materna fue de 26.5 defunciones por cada 100,000 nacimientos, y la hemorragia obstétrica fue la causa más común con 19.4% del total de casos reportados en el país.7
Según la guía que se utilice, la hemorragia posparto tiene diversas definiciones. La Organización Mundial de la Salud emitió la primera en 1989 como la pérdida de 500 mL después de un parto.8 Esta definición ha permanecido como una de las más aceptadas, aunque hay algunas variaciones en las emitidas por otros organismos con igual reconocimiento, como la International Federation of Gynecology and Obstetrics (FIGO), que mantiene los 500 mL después del parto pero especifica una cantidad mayor de 1000 mL luego de una cesárea.9 En contraste, el American College of Obstetricians and Gynecologists (ACOG) considera como referencia la pérdida sanguínea superior a 1000 mL, independientemente de la vía de nacimiento, pero ya incorpora la asociación de signos y síntomas de hipovolemia en las primeras 24 h.10
Por desgracia, ha sido difícil llegar a un consenso global y establecer una definición comúnmente aceptable de hemorragia posparto porque las definiciones varían según los países, las especialidades médicas, las pautas de la sociedad científica e, incluso, de un médico a otro.11 Una definición más sólida debe incluir la pérdida de sangre, los signos clínicos y los parámetros cardiovasculares, siempre considerando la variabilidad en la aparición de estos parámetros en una paciente embarazada para la identificación rápida y precisa de la hemorragia posparto.12
Etiología y factores de riesgo
Para estudiar correctamente a una paciente debe crearse un sistema de evaluación continua de factores de riesgo (Cuadro 1) de hemorragia que se base en las características de la madre y obstétricas al momento del ingreso, durante el trabajo de parto y después de éste.13 El uso de la nemotecnia de las “4 T”, que representa las causas más comunes de la hemorragia posparto: tono, traumatismo, tejido y trombina,14 es útil para evaluar los factores de riesgo en cada una de estas categorías (Cuadro 2) y determinar una causa potencial de la hemorragia posparto.15 El conocimiento e identificación de estos factores, y la anticipación ante una paciente que sangra, tienen el potencial de reducir, significativamente, la morbimortalidad materna por hemorragia posparto.16
Cuadro 1 Método de evaluación de riesgo de hemorragia posparto14
| Riesgo bajo | Riesgo medio | Riesgo alto |
|---|---|---|
| Embarazo único | Cesárea o cirugía uterina previa | Placenta previa, acreta, increta o percreta |
| Menos de cuatro partos previos | Más de cuatro partos anteriores | Hematocrito <30 |
| Útero sin cicatrices | Gestación múltiple | Sangrado al ingreso |
| Ausencia de antecedentes de hemorragia posparto | Fibromas uterinos grandes | Defectos de coagulación conocidos |
| Corioamnionitis | Antecedentes de hemorragia posparto | |
| Uso de sulfato de magnesio | Signos vitales anormales (taquicardia e hipotensión) | |
| Uso prolongado de oxitocina |
Cuadro 2 Causas y factores de riesgo de hemorragia posparto6,9,15
| Alteraciones | Etiología | Factor de riesgo |
|---|---|---|
| Tono: anormalidades en la contracción uterina | Sobredistensión uterina | Polihidramnios, gestación múltiple, macrosomía fetal |
| Infección intraamniótica | Fiebre, ruptura prolongada de membranas | |
| Funcional-anatómica | Parto precipitado o prolongado, miomatosis, placenta previa, anormalidades uterinas | |
| Relajantes uterinos | Terbutalina, agentes anestésicos halogenados, sulfato de magnesio, nifedipina. | |
| Distención vesical | Cateterismo vesical debe ser un paso inicial ya que la vejiga llena puede evitar la contracción uterina15 | |
| Tejido: retencion de fetos | Retención de cotiledones de la placenta | Expulsión incompleta de placenta |
| Espectro de placenta acreta | Instrumentaciones previas | |
| Retención de coágulos | El segmento uterino inferior debe ser limpiado de coágulos para permitir que el útero se contraiga15. | |
| Traumatismo: lesiones genitales | Laceraciones en la cesárea | Mal posición, profundidad |
| Ruptura uterina | Cirugía previa uterina | |
| Inversión uterina | Multiparidad con excesiva tracción del cordón | |
| Trombina: anormalidades en la coagulación | Estados preexistentes | Coagulopatías hereditarias (enfermedad de Von Willebrand, hemofilia) Púrpura trombótica idiopática |
| Adquirido durante el embarazo | Preeclampsia Coagulopatía intravascular diseminada Muerte fetal Infección grave Desprendimiento de placenta Embolia de líquido amniótico | |
| Iatrogénica | Anticoagulación terapéutica |
Importancia de la atención temprana y oportuna: morbilidad materna extrema
En el ámbito mundial se registran alrededor de 118 casos de morbilidad materna extrema por cada muerte materna,17 y la hemorragia posparto es una de sus principales causas. Esto se evidencia cuando la hemorragia posparto genera choque hipovolémico, problemas de coagulación, el ingreso a unidades de cuidados intensivos, las politransfusiones, y la cirugía adicional que empeoran la salud de las mujeres debido a la falta de reconocimiento y atención temprana de la hemorragia.18
Por lo tanto, la vigilancia de la morbilidad materna extrema debe considerarse un complemento indispensable de la epidemiología de la mortalidad materna,18 como una vigilancia constante de la calidad de la atención obstétrica de urgencia. En consecuencia, la generación de capacidades para la atención de la paciente obstétrica desde los diferentes niveles de complejidad (baja, mediana y alta), y la actualización en las opciones terapéuticas disponibles, garantiza la estabilización inicial, la remisión del evento agudo, y la capacidad resolutiva del sistema de salud.18
Así, se recomienda que las unidades donde se atienden pacientes obstétricas comiencen a monitorear y cuantificar con precisión y de forma acumulativa el sangrado de las pacientes durante las primeras 24 horas. Las estimaciones visuales subestiman, significativamente, el verdadero volumen de pérdida sanguínea.15
Prevención de la hemorragia posparto
La principal causa de hemorragia posparto es la atonía uterina,16 con 70% de los casos,16,19 de los que gran parte pueden anticiparse. La evaluación rutinaria del tono uterino sigue siendo una parte decisiva de la toma de decisiones clínicas y debe practicarse durante la tercera etapa del trabajo de parto.20 La vigilancia activa del tercer periodo del trabajo de parto es una estrategia efectiva para prevenir la hemorragia posparto. Esta estrategia incluye tres componentes: agente uterotónico después de la extracción de la cabeza del recién nacido,21 pinzamiento temprano del cordón, y tracción controlada del mismo para expulsar la placenta.15 La OMS agrega a estos componentes el masaje uterino como parte del procedimiento preventivo.20
Las recomendaciones para la indicación de uterotónicos profilácticos sugieren a la oxitocina (10 UI) intramuscular o intravenosa como primera línea de elección en el parto y en la cesárea.20,22 En los entornos donde no se dispone de oxitocina o no se puede garantizar su calidad, puede recurrirse a otros uterotónicos, como la ergometrina (200 μg IM/IV), la carbetocina termoestable 100 µg IM/IV o incluso el misoprostol oral (400 a 600 µg) como opciones viables para la profilaxis en casos de hemorragia posparto.23 Un matanálisis de la efectividad de la vía de administración de los uterotónicos indicados para la prevención de la hemorragia posparto sugiere que la carbetocina y la oxitocina intravenosa, o bien, la combinación de ergometrina más oxitocina intramuscular son, quizá, más efectivas que la oxitocina intramuscular, en términos de reducir el riesgo de sangrado excesivo y la morbilidad materna grave.24
Tratamiento actual e innovaciones terapéuticas
Estadios de tratamiento en la hemorragia posparto
Las guías de hemorragia posparto establecen un plan de urgencia por etapas que engloba las acciones más relevantes a practicar. Una de ellas, el Proyecto de Colaboración para la Atención Materna de Calidad de California (CMQCC)25 marca el protocolo general de atención para la hemorragia obstétrica. Figura 1

Figura 1 Protocolo general de la atención de la hemorragia obstétrica. Modificado de Improving Health Care Response to Obstetric Hemorrhage, V2.0Toolkit, funded by the California Department of Public Health in 2015; supported by Title V funds25
En tiempos recientes, la indicación del ácido tranexámico en el transcurso de las primeras tres horas posteriores al nacimiento, se recomienda para todos los casos de hemorragia posparto, independientemente de si el sangrado se debe a un traumatismo en el aparato genital o a otras causas. Debe considerarse al ácido tranexámico como parte de las opciones de primera respuesta en caso de sangrado por traumatismo de la vía del parto.23 De acuerdo con la evidencia, el retraso del tratamiento en la indicación del ácido tranexámico disminuye su beneficio en 10% cada 15 minutos, sin que se registre alguna ventaja después de tres horas.9 La indicación de fármacos uterotónicos adicionales se sugiere cuando el inicial no haya producido suficiente tono uterino en cuatro minutos, o bien, administrarlos de manera simultánea con el agente profiláctico en pacientes con mayor riesgo de hemorragia posparto.15
Si las medidas farmacológicas no logran controlar la hemorragia, las intervenciones quirúrgicas deben iniciarse lo antes posible. Se pueden intentar intervenciones quirúrgicas conservadoras como segunda línea, dependiendo de las circunstancias clínicas y la experiencia disponible.9 Cuando los agentes uterotónicos no logran controlar de manera adecuada la hemorragia posparto, se debe intensificar rápidamente el tratamiento con otras intervenciones (mecánicas o quirúrgicas), así como aumentar la intensidad del cuidado con el equipo multidisciplinario de atención.14 Se recomiendan la compresión uterina bimanual, la compresión aórtica externa y el uso de prendas antichoque no neumáticas como medidas provisionales hasta que se disponga de atención específica.20
El sistema JADA: una nueva opción terapéutica de baja complejidad
La compresión intrauterina puede ser efectiva para controlar la pérdida de sangre en pacientes con hemorragias leves a moderadas. Es decisivo priorizar la contracción uterina como mecanismo fisiológico para el control del sangrado posparto. Este enfoque promueve las contracciones del útero fisiológicas o inducidas por medicamentos,26 como tratamiento específico de la hemorragia posparto por atonía uterina.
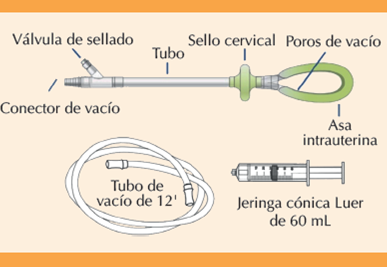
El dispositivo intrauterino de control de hemorragia por vacío, conocido como sistema Jada o JADA, está diseñado para proporcionar un tratamiento rápido. Utiliza un vacío intrauterino de baja intensidad para apoyar las contracciones uterinas fisiológicas, lo que ayuda a contraer los vasos sanguíneos del miometrio y alcanzar la hemostasia.26 El objetivo principal del procedimiento de este dispositivo es controlar eficaz y rápidamente el sangrado excesivo cuando las terapias conservadoras de primera línea han fallado y, al hacerlo, reducir la pérdida de sangre y la morbilidad y mortalidad materna asociadas con hemorragia posparto resultantes de atonía uterina.27
El dispositivo intrauterino de control de hemorragia por vacío está elaborado con silicona de tipo médico. En su extremo distal el dispositivo de 41cm de largo tiene un asa intrauterina elíptica, mientras que en el extremo proximal cuenta con un conector de vacío que se conecta a un tubo estándar para permitir la conexión a un recipiente graduado en línea, y a un sistema de vacío regulado de bajo nivel (80 ± 10 mmHg). La superficie interna del asa intrauterina posee 20 poros que facilitan la creación de vacío dentro de la cavidad uterina. La superficie externa está cubierta por un escudo que sobresale de los poros de vacío, protegiendo el tejido materno del vacío y evitando que los poros se obstruyan con tejido o coágulos26 (Figura 2). Además, está diseñado para minimizar el riesgo de lesiones, distribuir de manera simétrica la fuerza de vacío baja, asegurar un sellado completo para un efecto inmediato y permitir la observación y medición directa de cualquier sangrado persistente.27
Una de las ventajas del dispositivo de vacío es su facilidad de uso y el seguimiento del tratamiento de la paciente. Una vez colocado el sistema Jada, se aplica un vacío continuo que se mantiene durante al menos una hora después de controlar la hemorragia, mientras se palpa un útero firme y se observa directamente el control del sangrado. Al completar la terapia activa, se desconecta el vacío y se vacía el sello cervical. El dispositivo se deja en su lugar durante un mínimo de 30 minutos para permitir una observación minuciosa de cualquier retorno de atonía o sangrado anormal que requiera tratamiento adicional antes de retirarlo (Figura 3). Para retirar el dispositivo, se coloca una mano sobre el abdomen para sostener el fondo uterino mientras con la otra mano se retira, lentamente, el dispositivo a través de la vagina.26
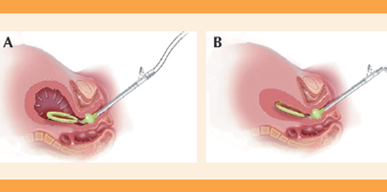
Figura 3 (A) Colocación del sistema JADA con el sistema generador de vacío de baja intensidad conectado y (B) Contracción uterina con el sistema JADA.
Este dispositivo de inducción de vacío ha demostrado ser eficaz y seguro en el control de la hemorragia posparto. En el estudio PEARLE (estudio clínico de registro con el que se aprobó en la FDA), en 106 pacientes diagnosticadas con hemorragia posparto por atonía uterina, el dispositivo de control de hemorragia por vacío intrauterino mostró una tasa de éxito de 94% (100/106, IC95%: 88 a 98%) con un tiempo medio de control de la hemorragia de tres minutos. Se reportaron ocho eventos adversos relacionados con el dispositivo o el procedimiento, incluidos: endometritis (n = 5), rotura de una reparación de laceración vaginal (n = 1), vaginosis bacteriana (n = 1), y candidiasis vaginal (n = 1). Todas las complicaciones se resolvieron con tratamiento y no hubo secuelas adversas graves. Para los seis casos que no respondieron al tratamiento con el dispositivo de vacío, uno se debió a la falta de reconocimiento temprano de una laceración cervical que, posteriormente, fue tratada con sutura. Los cinco restantes requirieron tratamiento adicional complementario, y no se observó asociación directa con el uso del dispositivo.26
Como parte de un tratamiento rápido para controlar la hemorragia, el uso del dispositivo de vacío permitió el colapso inicial del útero en una mediana de un minuto (rango intercuartil 1 a 2). En 82% de los casos en los que el dispositivo controló el sangrado anormal, que se logró en los primeros cinco minutos, con una mediana de 3 (rango intercuartil 2 a 5). En este estudio, la mediana del tiempo de tratamiento con vacío fue de 144 minutos (rango intercuartil 85.8 a 295.8) y la mediana del tiempo total desde la colocación hasta el retiro del dispositivo fue de 191 minutos (rango intercuartil 132.8 a 365.8).26
En otro estudio con 114 pacientes se comparó el taponamiento uterino con balón de Bakri (n = 78, 68.4%) con el dispositivo de control por vacío Jada (n = 36, 31.6%) como procedimientos para cohibir la hemorragia posparto primaria. Se concluyó que el sistema Jada se asoció con menos trasfusiones masivas (2.8 en comparación con 20.5%; OR 0.11; IC95%: 0.01 a 0.87, p < 0.01) y una menor pérdida sanguínea (1000 comparados con 2500 mL, p < 0.003), en comparación con el dispositivo de taponamiento con balón comúnmente utilizado.28
En el estudio (Treating Abnormal Postpartum Uterine Bleeding or Postpartum Hemorrhage with the Jada System) llevado a cabo en 16 centros médicos en Estados Unidos, con 800 casos (n = 530, 66.25% de parto y n = 230, 33.75% de cesárea) tratados con el dispositivo intrauterino de inducción de vacío, se demostró la tasa de éxito del tratamiento de 92.5% para los partos y de 83.7% para las cesáreas (95.8% [n = 307] y 88.2% [n = 220]) con un tiempo medio de permanencia del dispositivo (de inserción al retiro) de 3.1 y 4.6 horas, respectivamente. En consistencia con lo reportado en el estudio de registro, el control definitivo del sangrado se consiguió en cinco minutos en 73.8% de los partos (n = 178) y en 62.2% de las cesáreas (n = 94) y en el transcurso del primer minuto para 45.6 (n = 110) y 34.4%, (n = 52), respectivamente.29
La evidencia de la facilidad de uso, la efectividad demostrada y la breve duración del tratamiento, sugieren al sistema Jada como una nueva opción de tratamiento de baja complejidad, que podría ser útil como una intervención más temprana en el control de la hemorragia posparto. Esto apoya su inclusión en etapas más tempranas de los algoritmos de tratamiento de hemorragia posparto,30 con el propósito de reducir el riesgo de morbilidad materna.
Objetivo del tratamiento quirúrgico de la hemorragia posparto persistente
Si con las medidas iniciales no se consigue controlar el sangrado, es necesario un procedimiento quirúrgico urgente. Entre las opciones disponibles están: la ligadura de la arteria uterina, de la arteria ilíaca interna, la embolización, las suturas de compresión uterina y la histerectomía, todas ellas intervenciones potencialmente efectivas para controlar la hemorragia.15
Esas técnicas quirúrgicas se dividen, en términos generales, en tres categorías: 1) restaurar la contractilidad uterina (eliminación del tejido retenido, reparación de traumatismos o laceraciones y la reposición de la anatomía uterina normal después de la inversión) con la finalidad de reintegrar el proceso de involución uterina; 2) disminuir la pérdida de sangre (trombina) mediante la ligadura vascular quirúrgica y la embolización de la arteria uterina, al mismo tiempo que se da tiempo para que el efecto uterotónico restablezca el tono y 3) proporcionar “tono” al replicar la compresión vascular de la involución uterina mediante taponamiento a través de suturas compresivas de taponamiento interno o externo.31
La optimización del momento para iniciar las intervenciones quirúrgicas,20 técnicas de radiología intervencionista y hemostáticas en estas pacientes, así como el momento adecuado para cambiar de la reanimación con líquidos claros a la transfusión de productos sanguíneos, es decisiva para mejorar el desenlace de la madre.32
DISCUSIÓN
En esta revisión de la bibliografía con estrategia definida de búsqueda, se repasaron los aspectos generales (conceptos, epidemiología, etiología, prevención y tratamiento) de la hemorragia posparto, con un enfoque en innovaciones recientes en el tratamiento no quirúrgico. Se procuró la objetividad, la experiencia clínica del autor, así como su interés por estrategias de atención que pudieran haber influido en la selección e interpretación de la bibliografía disponible.
Para reducir la mortalidad materna es fundamental implementar actividades de capacitación para los profesionales del sector salud, aplicar protocolos y guías integrales de urgencias obstétricas adaptadas a cada unidad médica, y garantizar la disponibilidad de insumos necesarios en todas las instituciones de salud. Las iniciativas de atención de calidad en el proceder médico de las urgencias obstétricas han demostrado que el trabajo en equipo y la comunicación efectiva, junto con la capacitación con equipos de simulación y la retroalimentación posterior a los episodios de hemorragia posparto, mejoran los desenlaces clínicos15 y aseguran que los protocolos reduzcan, eficazmente, la incidencia de hemorragias.33
El acceso a nuevas tecnologías disponibles para la atención de esta complicación obstétrica es decisivo para prevenir reacciones no esperadas, mejorar la toma de decisiones y elevar la calidad de la atención.34 Un diagnóstico rápido y una atención correcta y oportuna contribuyen a la disminución de la mortalidad materna.18 Por lo tanto, las sugerencias a resaltar para la implementación de un protocolo exitoso para la atención de la hemorragia posparto por atonía incluyen los siguientes puntos:
La piedra angular de una reducción efectiva de la mortalidad incluirá la identificación de los factores de riesgo, el diagnóstico rápido y la gestión oportuna de la urgencia obstétrica.5
La mayor parte de las muertes por hemorragia posparto podría evitarse mediante el tratamiento activo de la tercera etapa del trabajo de parto y la aplicación rápida y efectiva del paquete de primera respuesta (uterotónicos, masaje uterino, reposición de líquidos y ácido tranexámico).23
En pacientes con hemorragia y atonía uterina sin respuesta al primer uterotónico aplicado, se sugiere administrar, sin demora, un segundo uterotónico como metilergometrina o carbetocina, siempre y cuando no haya contraindicaciones.33
La técnica de compresión manual del útero, a través del abdomen y la vagina, debe usarse activamente hasta que los medicamentos comiencen a funcionar o hasta que se inicie una intervención adicional.15
En pacientes con hemorragia posparto y atonía y resistencia a un segundo uterotónico, la colocación temprana de un balón de taponamiento intrauterino (balón de Bakri) o un dispositivo de vacío intrauterino (sistema Jada) debe considerarse antes de que la pérdida de sangre supere los 1.5 L.33
Los datos clínicos indican que el sistema JADA es seguro, eficaz y fácil de aplicar, lo que apoya su inclusión como una opción prometedora en la contención del sangrado uterino anormal y la hemorragia posparto en etapas tempranas.30
El sistema JADA parece prometedor al ofrecer un acceso no quirúrgico y alcanzar hemostasia rápidamente a través de crear un vacío dentro del útero (en lugar de inflar un balón en su interior). Esto puede ayudar a evitar complicaciones, transfusiones, cirugía y muerte materna. Hacen falta más estudios para comparar este sistema con otros tratamientos habituales, en especial con alternativas no quirúrgicas que permiten a las pacientes preservar su fertilidad. Comparado con otras técnicas de control de la hemorragia posparto, el dispositivo de vacío es relativamente fácil de usar, lo que puede ser decisivo en situaciones de urgencia. Algunas preocupaciones que surgen de revisar la evidencia disponible: la misma parece limitada en el tratamiento de los casos más graves; conforme existan más estudios en el mundo real estará disponible mayor información acerca del riesgo de la colocación inadecuada, infecciones y funcionamiento defectuoso; la selección apropiada de pacientes y las consideraciones de costo y cobertura pueden ser importantes. Como con cualquier dispositivo médico, es importante siempre considerar los riesgos potenciales y beneficios caso por caso.
CONCLUSIÓN
La elección del tratamiento dependerá de la gravedad y la causa de la hemorragia, la respuesta de la paciente al tratamiento general inicial y la disponibilidad de recursos y equipo médico especializado. Puede incluir una combinación de medidas no invasivas o invasivas que pueden ir desde un tratamiento homeostásico hasta intervenciones quirúrgicas. La evidencia ha demostrado que el dispositivo intrauterino de control de hemorragia por vacío es efectivo de manera temprana para controlar rápida y eficazmente la hemorragia posparto.











 nueva página del texto (beta)
nueva página del texto (beta)