ANTECEDENTES
El sangrado uterino anormal es de alta prevalencia; se estima hasta en un 30% en mujeres en edad reproductiva, no embarazadas.1 En Colombia corresponde a 1 de cada 5 consultas a los servicios de Ginecología. 2 Es el principal motivo de consulta de las adolescentes3 y resulta en una afección que puede derivar en anemia ferropénica y posible disminución de la calidad de vida. 4
Durante años se usó una terminología que incluía los vocablos: menorragia, hipermenorrea, metrorragia, menometrorragia, entre otros; sin embargo, el tiempo demostró que esas palabras generaban confusión; por ejemplo, el término “menorragia” para el 22% de los autores era un diagnóstico, mientras que el 78% lo consideraban un síntoma: no había una definición clara. Para todos era sangrado uterino abundante, sin que existiera un consenso si era un sangrado estrictamente regular o podía ser de igual forma irregular, o si era necesario o no que hubiera una afección detectable. 5 Debido a la poca precisión de esa terminología y carencia de orientación a su causa, se decidió dejar de usarla.1,6,7
Por lo anterior, el objetivo de esta revisión fue: actualizar la publicación previa de dos de los autores8 y describir los cambios de los últimos cinco años en el sistema de clasificación PALM-COEIN, propuesto por la Federación Internacional de Ginecología y Obstetricia (FIGO) para sangrado uterino anormal y reunir la nueva evidencia reportada a partir del 2018 acerca de PALM-COEIN.
METODOLOGÍA
Estudio retrospectivo fundamentado en la búsqueda en las bases de datos PubMed, LILACS, Scopus y Web of Science con el MeSH “PALM-COEIN”. La búsqueda se limitó aartículos publicados del 2018 a agosto del 2023 y que estuvieran escritos en inglés, español, portugués o francés. Se obtuvieron 103 resultados: PubMed 28, LILACS 1, Scopus 47 y Web of Science 27. Con auxilio de la herramienta Rayyan se eliminaron los duplicados y se seleccionaron, por título y resumen, los artículos relacionados con el tema. Finalmente, mediante la lectura completa de los artículos se seleccionaron los que hacían referencia a la clasificación actual del sangrado uterino anormal. Se excluyeron los estudios con la terminología clásica. Al final de todo el proceso se eligieron 20 artículos que fueron la base de la revisión, se agregaron otros 38 artículos para complementar el tema. Este proceso se recopiló mediante la herramienta PRISMA. Figura 1
Sangrado uterino anormal, clasificación PALM-COEIN
El sangrado uterino anormal en mujeres no embarazadas, en edad fértil, se divide en: crónico y agudo. El primero es el que durante la mayor parte de los últimos seis meses ha sido anormal en frecuencia, duración, regularidad o volumen. El agudo es un episodio de sangrado abundante que, médicamente, es de cantidad suficiente para requerir una intervención que ayude a minimizar o prevenir una mayor pérdida de sangre. 1
Se considera que una frecuencia es normal cuando el ciclo menstrual dura entre 24 a 38 días o, visto de una forma más práctica, entre 31 ± 7 días. Una duración normal es la menor a ocho días. 9 Con respecto al parámetro de regularidad se establecieron dos grupos: el primero de mujeres entre los 26 y 41 años; el segundo entre 18 a 25 años o 42 a 45 años. 1 Para el primer grupo la normalidad se estableció cuando la diferencia entre el ciclo más largo y el más corto, reportado en los últimos seis meses, era menor o igual a 7 días. Para el segundo grupo se considera normal en quienes esta diferencia es menor o igual a 9 días. 1
El volumen es otro parámetro que ha cambiado; antes se definía como normal a un sangrado entre 5 a 80 mL y anormal cuando se salía de esos parámetros. En tiempos recientes se adoptó la definición del National Institute for Health and Care Excellence, que describe como anormal o abundante a “una excesiva pérdida de sangre menstrual que interfiere en la calidad de vida física, social, emocional o laboral de la mujer”. 10 Por último, se agrega el sangrado intermenstrual, que es el espontáneo, que ocurre entre periodos menstruales y que puede ser cíclico o aleatorio. 10 Figura 2
Figura 2 Parámetros de normalidad y anormalidad en el sangrado uterino.
| Frecuencia | Ausente: amenorrea |
| Infrecuente: mayor a 38 días | |
| Normal: entre 24 y 38 días | |
| Frecuente: menor a 24 días | |
| Duración | Normal: menor o igual a 8 días |
| Prolongado: mayor de 8 días | |
| Regularidad | Normal o regular |
| Mujeres entre 26 y 41 años: variación menor o igual a 7 días | |
| Mujeres entre 18 a 25 ó 42-45 años: variación menor o igual a 9 días | |
| Irregular: variación mayor a la mencionada | |
| Volumen | Normal: no interfiere con la calidad de vida |
| Abundante: interfiere con la calidad de vida |
La Federación Internacional de Ginecología y Obstetricia (FIGO) introdujo el acrónimo PALM-COEIN que describe la clasificación para sangrado uterino anormal en mujeres no embarazadas en edad fértil. Lo divide en dos grandes grupos: PALM (palma en inglés) que incluye las causas estructurales: pólipos (P), adenomiosis (A), leiomioma (L) y malignidad e hiperplasia (M) y COEIN (moneda en inglés, agregando la letra “e”) que abarca las causas no estructurales: coagulopatía (C), disfunción ovárica (O), endometrio (E), iatrogenia (I) y no clasificados en otra parte (N).11,12 Cada causa está descrita en la Figura 3.
Pólipos (P)
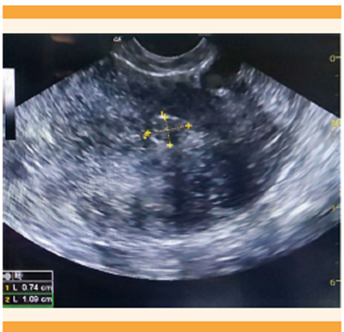
Los pólipos endometriales son protrusiones benignas del endometrio conformadas por un componente vascular, glándulas y estroma, que pueden variar en cantidad, textura y tamaño que puede ir desde milímetros hasta varios centímetros (Figura 4). 13 Los factores de riesgo descritos para los pólipos endometriales son: la edad, hipertensión, obesidad y tratamientos con tamoxifeno. 14 Por lo general, son asintomáticos, pero en algunas pacientes pueden ser la causa de sangrado uterino anormal. 15
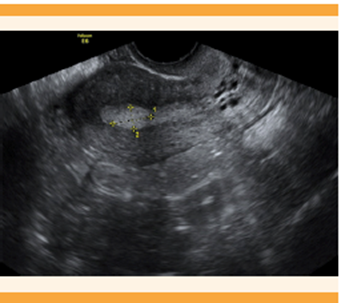
Figura 4 Imagen ecográfica de una paciente de 30 años con sangrado uterino anormal consistente en manchado intermenstrual, se evidencia un pólipo endometrial de 12 x 7 mm.
En diferentes cohortes se ha encontrado la causa de alrededor del 16% de los síntomas de sangrado uterino anormal.16,17 El riesgo de una lesión maligna aumenta en las pacientes posmenopáusicas con síntomas de sangrado uterino anormal.18,19 La prevalencia de neoplasia endometrial en pólipos en mujeres con sangrado sintomático es del 4.15%, casi el doble en comparación con las que no tienen sangrado que es del 2.16%. El riesgo es casi tres veces más en mujeres posmenopáusicas sintomáticas con pólipos endometriales que en mujeres posmenopáusicas asintomáticas. 18
La ecografía transvaginal es la modalidad de imagen diagnóstica de elección para la detección de pólipos endometriales (Figura 5). Su precisión aumenta cuando se utiliza Doppler color o se practica una ecografía con infusión de solución salina (histerosonografía).20,21 Es importante tener en cuenta el endometrio de aspecto polipoide, que se considera una variante normal. 12
Adenomiosis (A)
La adenomiosis es una alteración benigna, en la que las glándulas endometriales penetran al tejido miometrial de una forma focal o global. 22 Su prevalencia se estima del 5 al 70%.11 Pese a que las mujeres con adenomiosis pueden manifestar un cuadro clínico de sangrado uterino anormal, dismenorrea, dispareunia o infertilidad, 1 de cada 3 puede permanecer asintomática. 23
Existen diferentes hipótesis acerca de la aparición de la adenomiosis, la más extendida es que se origina por la invaginación de la base del endometrio en el miometrio. Otra teoría plantea que la invaginación basal afecta a lo largo del sistema linfático intramiometrial. 24 Una tercera teoría sugiere que se produce, de novo, un proceso metaplásico que se inicia a partir de tejido endometrial intramiometrial ectópico. 24 La patogenia compleja y la manifestación variable de la adenomiosis, además de que suele estar acompañada de otras afecciones que también pueden ser causa de sangrado, la convierten en una de las causas más difíciles de diagnosticar y tratar de la clasificación PALM-COEIN. 25 Entre los factores de riesgo están: la multiparidad, exposición a tratamientos con tamoxifeno, edad avanzada, mayor exposición a estrógenos, factores genéticos y epigenéticos. 8
Está demostrado que la ecografía transvaginal tiene una sensibilidad y especificidad similares para diagnosticar adenomiosis cuando se compara con la resonancia magnética nuclear. 1,26 En la actualidad, para el diagnóstico de adenomiosis se utilizan los criterios del grupo MUSA, 27 en donde dos o más criterios son por demás sugerentes de adenomiosis. Los criterios son: engrosamiento miometrial asimétrico, quistes miometriales, islas hiperecogénicas, sombreado en forma de abanico, líneas y brotes subendometriales ecogénicos, vascularización translesional, cuando haya una zona de unión irregular y una zona de unión endometrial interrumpida. A pesar de lo anterior, aún se está trabajando en un consenso internacional que pueda definir un sistema de clasificación de adenomiosis que permita fenotipar el trastorno de una manera estandarizada. 1 Figura 6
Leiomioma (L)
Los leiomiomas, miomas, o fibromas uterinos son tumores benignos que surgen del músculo liso miometrial. 28 Se estima que alrededor del 70% de las mujeres de raza blanca y el 80% de ascendencia africana lo padecerán a lo largo de su vida y la mayoría permanecerán asintomáticas. 29 Las pacientes con síntomas, además de sangrado uterino anormal, pueden padecer anemia, dolor, sensación de masa, polaquiuria, estreñimiento o infertilidad. 29 Su importancia radica en que en algunas poblaciones puede llegar a ser la causa de casi un 50% de las consultas por sangrado uterino anormal en los servicios de Ginecología. 16,30 Un factor tranquilizante de este tumor es que solo el 0.25% de las pacientes que se operan por miomas uterinos tiene riesgo de leiomiosarcoma. 31
Las hormonas sexuales esteroideas tienen un papel importante en la patogenia del leiomioma. De igual manera, se ha encontrado una asociación etiológica con la desregulación de las vías de señalización celular, expresión de micro-ARN y anomalías citogenéticas. 28 Los factores de riesgo de leiomiomatosis son: edad, raza, hormonas endógenas y exógenas, obesidad, infección uterina y el estilo de vida, como la dieta, el consumo de cafeína y alcohol, actividad física, estrés y tabaquismo; no obstante, algunos de este último grupo no están definidos claramente. 32 El diagnóstico se establece mediante ecografía, mientras que la resonancia magnética se reserva, principalmente, para las pacientes con cuatro o más masas. 33 Figuras 7y8
El sistema de subclasificación de leiomiomas FIGO, desde la versión de 2018, los clasifica con números, que van del 0 al 8, en cuatro grupos: submucosos, intramurales, subserosos y transmurales (Figura 9). 1 Las lesiones tipo 0 son las intracavitarias adheridas al endometrio por un tallo menor o igual al 10%. Las tipo 1 tienen el 50% del diámetro medio intramural y las tipo 2 el 50% o más. Las lesiones de tipos 3 y 4 son totalmente intramurales, pero las tipo 3 tienen contacto con el endometrio y son parte de las lesiones submucosas. Las lesiones tipos 5, 6 y 7 son subserosas. Las tipo 5 son, al menos, 50% intramurales. Las tipo 6 menos del 50 % y las tipo 7 están unidas a la serosa por un tallo que, igualmente que las tipo 1, es menor o igual al 10%. Las lesiones tipo 8 son las que se encuentran en un lugar que no se relaciona con el miometrio, como el cuello del útero, ligamentos redondos o anchos, entre otros. 1 Por último, las lesiones transmurales son las que tienen relación con el endometrio y la serosa y se clasifican como una combinación de los mencionados; es decir, una lesión tipo 2-5. 1
Malignidad e hiperplasia (M)
Este grupo es relativamente poco común; sin embargo, la hiperplasia atípica y la malignidad son causas importantes que deberían descartarse en toda mujer en edad reproductiva, sobre todo en las que se encuentran en la posmenopausia. 8,11 En pacientes con sangrado uterino anormal tiene una prevalencia que varía, dependiendo de la población, desde menos del 1% hasta el 10%.34,35,36 Los factores de riesgo reportados son: edad mayor de 45 años, obesidad, menarquia temprana, menopausia tardía, diabetes, nuliparidad, síndrome de ovario poliquístico, terapia con tamoxifeno, antecedente familiar de cáncer y síndrome de Lynch o síndrome de Cowden. 37 Los dos últimos son trastornos hereditarios que predisponen a la aparición de neoplasias. El primero se asocia con mutaciones en los genes MLH1, MSH2, MSH6, PMS1 y PMS2 mientras que el segundo se relaciona con mutaciones en el gen PTEN. 38
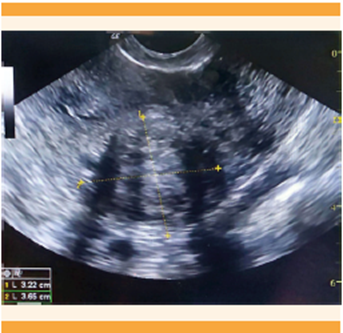
En mujeres posmenopáusicas el grosor endometrial ha demostrado ser un indicador de riesgo de hiperplasia atípica y carcinoma endometrial (Figura 10). Se debe sospechar malignidad, principalmente, en mujeres posmenopáusicas con síntomas y grosor endometrial mayor o igual a 5 mm. 39 Para las pacientes asintomáticas, el punto de corte previamente definido, según el trabajo de Smith R y colaboradores, era de 11 mm; 40 sin embargo, recientemente se propuso un grosor diferente. Se encuentran umbrales muy bajos, como ≥ 5 mm, que han demostrado muy buena sensibilidad, aunque implican costos financieros significativos y una carga emocional debida al seguimiento de una posible malignidad. Con umbrales muy altos (≥ 14 mm) pueden llegarse a perder hasta el 72% de los casos. 41 La evidencia actual demuestra como óptimo un umbral de grosor endometrial ≥ 8 mm, debido a su buen rendimiento para detectar carcinoma endometrial e hiperplasia atípica en pacientes posmenopáusicas asintomáticas. 42 Este umbral ha resultado en un equilibrio entre buena sensibilidad y costos no tan elevados al sistema de salud.
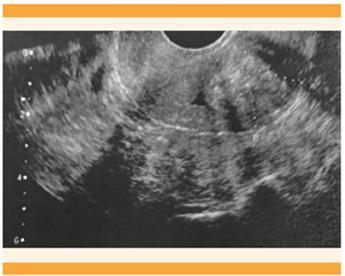
Figura 10 Paciente de 64 años con reporte ecográfico de pólipo endometrial, posterior a histeroscopia. Se evidencian los hallazgos que sugieren malignidad; reporte de patología: adenocarcinoma endometrial de tipo endometrioide.
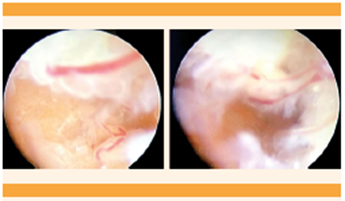
La alta precisión, sensibilidad y especificidad de la histeroscopia para evaluar la patología intrauterina están bien estudiadas; por lo tanto, se recomienda que en las mujeres con sangrado uterino anormal y que se considere necesaria una biopsia endometrial, se realice por medio de una histeroscopia de consultorio, en lugar de un muestreo ciego (Figura 11). 43 La hiperplasia sin atipias tiene un riesgo de progresión que va desde 1 a 3%, mientras que la neoplasia endometrial intraepitelial tiene un riesgo que puede llegar hasta un 45%.44 Finalmente, también hay que tener en cuenta otras neoplasias: cáncer de cuello uterino, rabdomiosarcoma, tumores malignos de ovario, tumores de vulva y de vagina. 45
Coagulopatía (C)
Comprende una amplia gama de trastornos de la hemostasia. Es de las causas menos frecuentes de sangrado uterino anormal, con una prevalencia de alrededor del 1% entre las mujeres que consultan; 17,34,46,47 sin embargo, se encuentra hasta en un 13% de las pacientes con sangrado menstrual abundante11 y debe sospecharse, principalmente, en quienes expresen el cuadro clínico. 1,43 Figura 12
Figura 12 Factores asociados con coagulopatía.
| El siguiente | Sangrado menstrual abundante desde la menarquia |
| Uno de los siguientes | Hemorragia posparto |
| Sangrado relacionado con una cirugía | |
| Sangrado asociado con un procedimiento dental | |
| Dos o más de los siguientes | Equimosis 1-2 veces por mes |
| Epistaxis 1-2 veces por mes | |
| Sangrado frecuente de las encías | |
| Antecedentes familiares de síntomas hemorrágicos |
La principal causa es la enfermedad de von Willebrand, aunque existen otras, como la hemofilia A y B hereditaria o adquirida, enfermedad hepática crónica, deficiencia de vitamina K, y los trastornos de la fibrinólisis. Las afecciones trombocitopénicas pueden causar sangrado uterino anormal, pero son extremadamente raras. 48 En este grupo no están incluidas las pacientes que tomen algún medicamento que interfiera con la coagulación. 2,8
Disfunción ovulatoria (O)
El sangrado uterino anormal relacionado con la disfunción ovulatoria se asocia con sangrado irregular, que varía en volumen. 49 Las mujeres con trastornos de la ovulación pueden tener amenorrea o manifestarse con ciclos poco frecuentes, igualmente pueden experimentar ciclos prolongados y sangrado de una variedad de duración y volumen. 43 Es la principal causa no estructural de sangrado uterino anormal. Los estudios demuestran que es la causa subyacente de aproximadamente el 37% de las pacientes que consultan por esta causa. 16,50
Además de las causas fisiológicas, como la adolescencia, perimenopausia, lactancia y embarazo, en este grupo están incluidas todas las causas de disfunción ovulatoria establecidas en la nueva clasificación FIGO. 1 El sistema de clasificación FIGO para trastornos ovulatorios propone cuatro grupos: tipo I: causas hipotalámicas; tipo II: causas hipofisarias; tipo III: causas ováricas; y tipo IV: síndrome de ovario poliquístico. 51 En esta nueva agrupación se proponen dos mnemotecnias, la primera es “HyPO-P” para los grupos de la nueva clasificación, y la segunda es “GAIN-FIT-PIE” para las causas fisiopatológicas de cada grupo. 51 Figura 13
Endometrio (E)
El sangrado uterino anormal relacionado con disfunción endometrial se considera después de la exclusión de causas estructurales, disfunción ovulatoria o de la coagulación; por lo general, el sangrado es predecible, lo que indica una ovulación cíclica normal, pero intensa o prolongada. 52 La causa aún no se encuentra establecida, el trastorno primario puede estar relacionado con deficiencias en la producción local de vasoconstrictores, como la endotelina-1 y la prostaglandina F2α, producción excesiva del activador del plasminógeno o aumento de la producción local de prostaglandina E2 y prostaciclina. 53,54
Existen datos que indican una relación entre la infección subclínica por Chlamydia trachomatis. 55 De igual forma, en la bibliografía también se encuentra evidencia que respalda el aumento de los factores proangiogénicos y la disminución de los antiangiogénicos que causan una maduración deficiente de los vasos, lo que da como resultado vasos más frágiles y permeables que parecen desempeñar un papel importante en la fisiopatología de esta afección. 56
Iatrogenia (I)
Diversos medicamentos pueden llegar a producir sangrado uterino anormal, como los estrógenos, progestinas, andrógenos y los agentes que afectan, directamente, su producción o función local. 2 Figura 14

Figura 14 Paciente de 21 años, usuaria de anticonceptivos orales, con sangrado uterino anormal consistente en manchado continuo y escaso, de 4 meses de duración. En la ecografía se evidencia la atrofia endometrial.
Esta categoría incluye, también, fármacos no esteroideos que contribuyen a los trastornos ovulatorios, como los que afectan el metabolismo de la dopamina, incluidas las fenotiazinas y los antidepresivos tricíclicos. Igualmente, en este grupo están los anticoagulantes, que antes se ubicaban en el de la coagulopatía. Esto incluye a los antagonistas modernos que no son de la vitamina K, como el rivaroxabán o apixaban, 2 que parecen tener un mayor efecto en el volumen del sangrado menstrual que los antagonistas tradicionales de la vitamina K. 57
No clasificado en otra parte (N)
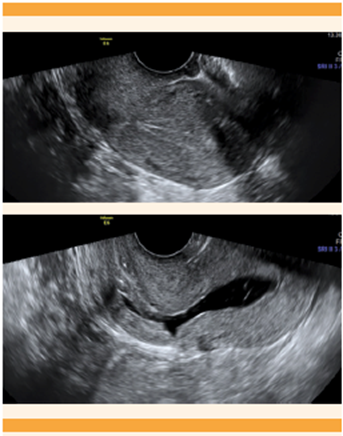
Se contemplan afecciones que rara vez se encuentran o que están mal definidas. Algunos ejemplos son las malformaciones arteriovenosas y el defecto de la cicatriz uterina o istmocele (Figura 15). A propósito de este último hay una breve discusión, existe una fuerte asociación entre pacientes con defecto en la cicatriz uterina y sangrado uterino anormal. Estas pacientes experimentan un patrón de sangrado que se caracteriza por una menstruación prolongada, con sangrado intermenstrual temprano en el ciclo. 2 Estos datos impulsan la inclusión del defecto de cicatriz uterina como un padecimiento distinto en el sistema de clasificación PALM-COEIN. 58 Debido a esto, en un futuro, después de una nueva actualización en la que se incluya esta afección como parte de las causas estructurales, seguramente se hablará de una nueva clasificación denominada “PALMS-COEIN”.
CONCLUSIONES
El sistema de clasificación del sangrado uterino anormal ha recibido diversas modificaciones que es necesario conocer y utilizar en la terminología actual propuesta por la FIGO. Ello ayudará al entendimiento y a una mejor comunicación de este diagnóstico. También ha demostrado su efectividad al momento de orientar la causa conforme a las características del sangrado, lo que contribuye a mejorar la investigación epidemiológica de las pacientes que padecen alguna enfermedad contemplada en el sistema PALM-COEIN.











 nueva página del texto (beta)
nueva página del texto (beta)