INTRODUCCIÓN
La brucelosis o fiebre de Malta es una enfermedad zoonótica producida por bacterias del género Brucella. Es una de las zoonosis más importantes del orbe y su incidencia en humanos está relacionada íntimamente con la enfermedad en animales domésticos, conocida desde el siglo XIX; sin embargo, hasta hace 40 años se creía que sólo afectaba al ganado. Actualmente se reconocen 14 especies con una amplia variedad de hospederos, incluyendo animales silvestres como peces, anfibios, reptiles y aves (Ramos-Ramírez et al. 2020, Cruz-Aviña et al. 2021a, b, Aguilar et al. 2022, Occhialini et al. 2022). Su distribución es mundial y, a pesar de que algunas especies de Brucella han sido erradicadas en países desarrollados, son un grave problema para la salud pública (medio millón de nuevos pacientes se infectan al año) y salud animal (causando abortos, mortinatos y fiebre de Malta) en países emergentes como México (Almuneef et al. 2004, Corbel 2006, Cruz-Aviña et al. 2021b).
Brucella spp. tiene afinidad por el eritrol en los tejidos de los órganos reproductivos; en consecuencia, los organismos sexualmente maduros o en estado de preñez son más susceptibles a la infección. Los animales infectados eliminan las bacterias después de un aborto (o un parto), así como a través de la leche, secreciones vaginales, semen, sangre, orina y heces, llegando a contaminar suelo, pastos y agua. De esta forma se completa el ciclo infeccioso, motivando la contaminación de otros animales y la persistencia del germen en la naturaleza. Brucella spp. puede sobrevivir en el ambiente y mantener su infectividad durante periodos variables, de acuerdo con las condiciones del medio (Ortega et al. 2013, Whatmore y Foster 2021). Tiene la capacidad de sobrevivir en una gran variedad de nichos: B. abortus y B. suis sobreviven en el aire como bioaerosoles (Ollé-Goig y Canela-Soler 1987); B. abortus sobrevive en agua marina y B. melitensis sobrevive como contaminante emergente en lagos de cráter o Maars (vocablo de origen alemán, que se utiliza ampliamente en limnología y se refiere a los lagos que ocupan cráteres volcánicos) de acuerdo con White y Ross (2011). Recientemente se ha registrado a B. abortus y B. suis en aguas de bordos de uso agropecuario (Ramos-Ramírez et al. 2020, Cruz-Aviña et al. 2022). La presencia de B. microti también se ha verificado en el suelo como vector en la interfaz suelo-animal-humano (Scholz et al. 2008, Godfroid 2018, Dadar et al. 2021).
Cabe señalar que los métodos microbiológicos se basan en diferentes tipos de pruebas para establecer la sospecha, detección y cuantificación de los microorganismos, según su capacidad de crecer en un medio de cultivo específico (lo cual recibe el nombre de primoaislamiento). Posteriormente se realiza la resiembra del cultivo para disponer del microorganismo investigado, conforme a los postulados de Koch (se preservan en ultracongelación a corto o mediano plazo en bancos y colecciones científicas bacterianas, para futuros estudios, como referencia o para aplicaciones biotecnológicas), y confirmar su presencia mediante ensayos bioquímicos (i.e., metabólicos). Estas pruebas siguen siendo el estándar de oro en microbiología (Krieg 2005). La identificación bacteriana implica la confirmación del aislado mediante otras pruebas y ensayos, como la prueba de sobrevivencia y la de reacción en cadena de la polimerasa (PCR, por sus siglas en inglés) (MacFaddin 2000).
Por su parte, el suelo, como recurso natural, es considerado no renovable, dinámico y primordial para la vida (Dominati et al. 2010, Schoonover y Crim 2015), por lo que constituye un reservorio importante de microorganismos que impactan tanto a las plantas como a sus propiedades físicas y químicas. Por ello puede definirse como un sistema complejo de interacción entre las fases sólida, líquida y gaseosa (Schoonover y Crim 2015).
Durante la fase sólida, el tipo y composición de la materia mineral están determinados por las características de las rocas madre y por los procesos edáficos que intervienen. En este sentido, la porción inorgánica es importante por su influencia en la disponibilidad de nutrientes, aireación y retención de agua. La materia orgánica procede de la actividad de los distintos microorganismos del suelo, de su composición y cantidad, la cual varía principalmente en función del tipo de cubierta vegetal. Una de las capas del suelo está constituida por espacios porosos que, a su vez, están ocupados por agua y gases que constituyen la atmósfera edáfica (Schoonover y Crim 2015). En este sentido, el género Brucella guarda estrechas relaciones filogenéticas con las α-proteobacterias Gram negativas parasitarias del suelo, entre las que destacan: Agrobacterium, Rickettsia, Rhizobium y Rhodobacter (Moreno et al. 1990, Velasco et al. 2000).
Se hipotetizaba que el suelo constituía un reservorio potencial para Brucella, pero su relación filogenética con Ochrobactrum permitió corroborar que ambos géneros comparten la inusual característica de que sus membranas externas son permeables y resistentes ante sondas hidrofóbicas, al tiempo que pueden desestabilizarse al interactuar con péptidos policatiónicos (Velasco et al. 2000, Wattam et al. 2009, Dadar et al. 2021). La mayor parte de las α-proteobacterias son simbiontes intracelulares o patógenos de plantas y animales (Ugalde 1999), y destacan por su capacidad para degradar compuestos y fijar nitrógeno en el rizobioma (Krieg 2005). Con independencia de lo anterior, las primeras sospechas de sobrevivencia de Brucella spp. en suelo fueron evidenciadas por Zakharova (1956) y corroboradas por van Donsel et al. (1967) utilizando los postulados de Koch. En 2007 se aisló a Brucella en muestras de suelo de una comunidad en la República Checa (al principio la tipificaron como una variante de Brucella melitensis, pero en análisis posteriores resultó ser una nueva especie que con el tiempo se llamó B. microti) (Hubalek et al. 2007). Posteriormente se vinculó a B. microti con los ratones de campo (topillos) infectados que utilizan al suelo como madrigueras y que contaminan con bacterias de Brucella el suelo agrícola de esa comunidad a través de sus excretas y orina (Scholz et al. 2008).
Desde la década de 1980, considerando los resultados de van Donsel et al. (1967), se atribuyeron al sistema suelo todos los requisitos potenciales para ser colonizado en diferentes áreas geográficas por el género Brucella spp. (García-Carrillo 1987). Actualmente, esta sospecha ha sido confirmada en diferentes regiones y los procesos de colonización se han verificado ampliamente (Scholz et al. 2008, Ahmed et al. 2017, Janowicz et al. 2018).
Por lo tanto, el objetivo de este trabajo fue aislar a Brucella melitensis en suelo agrícola de una zona con alta incidencia y prevalencia de brucelosis humana (10 y 33 %, respectivamente) y de ganado (30 y 50 %, respectivamente) en Puebla, México.
MATERIALES Y MÉTODOS
Sitio de estudio
La comunidad Emilio Portes Gil pertenece al municipio de San Nicolás Buenos Aires, Puebla, México (19º18’ 30” N, 97º51’ 00” W) y está situada a 2350 msnm. El clima de la región es semiárido, templado y con lluvias en verano. Su principal actividad económica es la agricultura de riego. El número de habitantes es de 2174. La zona presenta una alta incidencia de casos de brucelosis animal (30 %) y humana (10 %), con referencias históricas desde 1923, fecha que coincide con los primeros registros de importación de cabras murcianas-granadinas (españolas) en la zona (Cruz-Aviña et al. 2022). En estos suelos, cuyos sitios se muestran en la figura 1, el ganado caprino pastorea y transita itinerante en la zona, de manera extensiva y sin control de buenas prácticas.
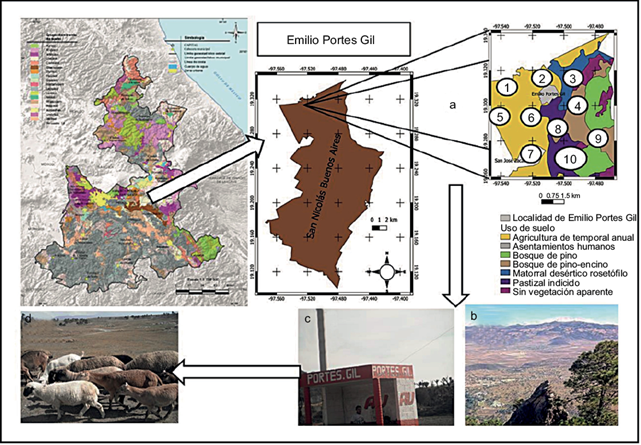
Fig. 1 Problemática del área de estudio (comunidad Emilio Portes Gil, municipio de San Nicolás Buenos Aires, Puebla). (a) Vista panorámica de la zona de muestreo, (b) sitios de muestreo de suelo agrícola, (c) entrada o acceso principal a la comunidad, (d) ganado caprino que transita libre e itinerante en la región. Elaboración propia basada en INEGI (2022).
Trabajo de campo
Toma de muestras
Entre 2017 y 2019 se recolectaron por triplicado muestras de suelo agrícola en 10 sitios diferentes (n = 90). Se depositaron para su homogenización en tinas de plástico (30 L) y se tamizaron hasta obtener una muestra final (1.5 kg). El criterio seleccionado fue al azar, con una distancia de 2 ha entre cada muestreo, y la forma de recolección fue en zigzag, a una profundidad aproximada de 0-30, 30-60 y 60-100 cm, conforme a la NOM-021-RECNAT-2000 (SEMARNAT 2002).
Análisis estadístico
Se realizó un análisis de varianza (ANDEVA) paramétrico. Para determinar las diferencias entre las medias se utilizó la prueba de mínima diferencia significativa (LSD, por sus siglas en inglés; p ≤ 0.05) con el programa estadístico Statgraphics Plus 5.1. Los valores de p significativos se expresan con un valor de significancia de 0.05 y 001.
Análisis de laboratorio
Trabajo de laboratorio
Las muestras recolectadas en campo fueron puestas en hielo y preparadas para su traslado (t < 3 h). Su caracterización tuvo lugar en el Laboratorio de Patogenicidad Bacteriana del Centro de Investigaciones en Ciencias Microbiológicas de la Benemérita Universidad Autónoma de Puebla, donde se analizaron sus características químicas y físicas de acuerdo con el método señalado por Díaz-Romeau y Hunter (1978).
Los análisis de rutina en el laboratorio de suelos incluyeron los propuestos por Quintana et al. (1983). Esta práctica siguió diferentes protocolos según el parámetro evaluado. Para la determinación de la textura se siguió a Bouyoucos (1962); para los indicadores de reacción del suelo (pH) y materia orgánica (MO, %), a Walkley y Black (1934); para la densidad aparente (g/ cm3), a Rhoades (1982), y para el macronutriente fósforo disponible (P, ppm), a Olsen et al. (1954), con adecuaciones con el ácido sulfúrico 6 N, según Nelson y Bremner (1972).
En cuanto a los reactivos, los patrones utilizados para realizar la curva de calibración fueron preparados con soluciones estándares de 500 mg/L para Ca y Mg y 1000 mg/L para K, a partir de sal de carbonato de calcio al 100 %, cinta de magnesio al 100 % y sal de cloruro de potasio 99 % de pureza, respectivamente. Todos los productos utilizados fueron de la marca Sigma-Aldrich. En la disolución estándar de ácido tricloroacético (24% V/V) al 98%, disolución de cloruro de lantano al 5% m/V al 99% y ácido clorhídrico al 1% V/V al 37% de pureza, respectivamente, la totalidad de los productos utilizados fueron de la marca Sigma-Aldrich. La determinación de calcio (Ca), magnesio (Mg), potasio (K) y sodio (Na) se realizó por el método del acetato de amonio 1N pH 7 (Rhoades 1982); su lectura se realizó con un espectrofotómetro de absorción atómica (Jackson 1964) y se hizo efectiva por el desplazamiento con KCl, 1N (Díaz-Romeau y Hunter 1978). En suelos calcáreos se recomienda extraer con acetato de amonio 1 N a pH de 8.5, para evitar sobreestimaciones de calcio y magnesio. La acidez intercambiable (Al + H) se obtuvo por el método de Yuan (1958) y para la determinación del cadmio (Cd) y el plomo (Pb) disponibles se empleó ácido etilendiaminotetraacético (EDTA) como agente quelante (EDTA 0.05 M pH 7) (Westerman 1990).
Las muestras recolectadas y preparadas se pusieron en hielo, se trasladaron al Laboratorio de Patogenicidad Bacteriana de la Benemérita Universidad Autónoma de Puebla (LPB-ICUAP-BUAP) y se procesaron para su caracterización correspondiente en el apartado “material no consolidado” (compuesto por partículas inorgánicas, materia orgánica, agua, aire y organismos), el cual comprende desde la capa superior de la superficie terrestre hasta diferentes niveles de profundidad del suelo de acuerdo con la NOM-138-SEMARNAT/SSA1-2012 (SEMARNAT 2013).
Caracterización física y química
Se realizó la caracterización de las muestras de suelo conforme a la NOM-021-RECNAT-2000 (SEMARNAT 2002), determinándose las especificaciones a reportar como textura, humedad, color, pH, materia orgánica, nitrógeno, composición de minerales petrogénicos, salinidad y sodicidad.
Caracterización microbiológica
Se siguió el protocolo ISO 6887 1993 (ISO 1993) para estimar el número de bacterias aerobias mesófilas entre 30 y 37 ºC, conocido también como recuento de placas aeróbicas (APC), por sus siglas en inglés, que es el método oficial para determinar el número de microorganismos viables. Se utilizó el medio de cultivo agar-chocolate cuenta estándar (ACE, por sus siglas en inglés) atemperado a 45 ºC. Las muestras de suelo se homogenizaron y diluyeron hasta 10-4. Las diluciones 10-1,10-2, 10-3 y 10-4 se inocularon en placas de Petri y se añadió el ACE según el método de vaciado en placa. Se homogenizó el medio con movimientos lentos y circulares por 10 s dejando solidificar el agar y secar las placas abiertas en posición invertida en una estufa a 37 ºC durante 30 min. Posteriormente se incubó la muestra entre 35 y 37 ºC durante 24-48 h. Finalmente se contaron las unidades formadoras de colonias (UFC) y se reportó el resultado en log de UFC/mL (Maturin y Peeler 2001, Pepper y Gerba 2005).
Caracterización de hongos
Se recolectaron 30 g de muestra de la rizosfera a una profundidad de 10 a 20 cm. También se recolectaron muestras de suelo de hormigueros, así como de adultos y larvas de hormigas, estas últimas como fuente de actinomicetos antagónicos (Schuppler et al. 1995). Las muestras de suelo se trataron con agua fenolizada por 30 min y posteriormente se difundió 1 mL en placas de Petri con diferentes medios de aislamiento como agar dextrosa papa (PDA), agar caseína almidón (ACA), agar de actinomicetos (AA) y agar Czapek-Dox (ACD), conforme a lo expuesto por Lunge y Patil (2012). Las hormigas adultas y larvas se colocaron directamente sobre los medios de cultivo. Las cajas se incubaron a 28 ± 2 ºC durante 5 a 7 d. Se aislaron y purificaron actinomicetos en PDA de acuerdo con sus características morfológicas macroscópicas (colonias polvosas secas que presentaron halos de inhibición y filamentos característicos en la observación microscópica conforme al método propuesto por Hayakawa et al. [2004]). Estas poblaciones se cuantificaron mediante la técnica de dilución en placa (Chen et al. 2003).
Primoaislamiento
Las muestras de suelo se sembraron en placas de Petri con medio Agar Brucella-BUAP (medio específico para Brucella spp.) más 5 % (v/v) de Agar chocolate, antibiótico y cristal violeta (Alton et al. 1976, Eisenberg et al. 2012). Se realizaron pruebas microbiológicas estándar a las colonias cultivadas conforme al método de Alton et al. (1976). Los cultivos se incubaron a 37 ºC durante 48 h con una atmósfera de CO2 al 5 % para el primoaislamiento (Alton et al. 1972, 1988).
Resiembra
Los primoaislamientos se resembraron y separaron en las siguientes 8 a 24 h en las condiciones anteriormente descritas. Posteriormente se realizaron diluciones para pruebas de tinción de Gram y de actividad metabólica (TSI, LIA, URE, CIT, MIO, OXI, CAT, RM-VP y H2S), así como curva de crecimiento (Alton et al. 1976, 1988). Se llevaron a cabo pruebas estándar de rutina para diagnóstico por sensibilidad a diferentes tintes colorantes derivados de la anilina: tionina (115929 Merck Millipore) a las diluciones 1:100 000, 1:50 000 y 1:25 000; fucsina (115937 Merck Millipore) a una dilución de 1:10 000, y safranina (115948 Merck Millipore) a una dilución de 1:10 000 (Alton et al. 1976, 1988). Se calculó el total de resultados positivos obtenidos para Brucella spp. derivados de estos cultivos (Alton et al. 1988).
Sobrevivencia de Brucella en suelo
A partir de las muestras recolectadas se realizó una combinación de todas las muestras ordenadas por mismo peso (w/w) y volumen (v/v). Posteriormente se pesaron 25 g de esta muestra compuesta de suelo, se esterilizaron en autoclave vertical (Sigma-Aldrich) a 200 ºC en tres series con tres repeticiones cada una y se diluyeron en 75 mL de agua destilada. Luego se inocularon con 1 mL de la suspensión bacteriana de B. melitensis M16 (NCTC 301), B. abortus S19 (NCTC 305) y B. abortus RB51 (B-0653-048) ajustada a densidad óptica (DO600) = 1 en caldo Brucella-BUAP. Posteriormente se monitoreó la sobrevivencia de las poblaciones resembradas cada 4 h en 100 µL de la suspensión en estudio, en medio Agar Brucella-BUAP hasta que la población bacteriana presentó muerte experimental.
Extracción de ADN total del suelo
Las muestras de suelo (250 mg) se procesaron para la extracción de ADN utilizando un kit de aislamiento (Soil Microbe DNA, Zymo Research®) según las recomendaciones del fabricante. Después de la extracción las muestras fueron sometidas a lisis celular por medio de centrifugación y filtrado por columna de purificación (Vfinal = 100 µL). Se determinó su calidad utilizando un NanoDrop 1000 a DO600 = 1 con un espectrofotómetro (Thermo Scientific, EUA).
Para la observación de ADN total del suelo se realizó un corrimiento en gel de agarosa al 0.8% con 5 µL de muestra de ADN y 6 µL del marcador de peso molecular (Sambrook y Russell 2001).
Análisis molecular
Se realizó PCR de punto final (PCR-PF) con la mezcla sugerida por Cloeckaert et al. (2000): 25 µL de Oligo 1 (59 GCCCCTGACATAACCCGCTT 39) y Oligo 2 (59 GAGCGTGACATTTGCCGATA 39), 5 µL de la muestra de ADN total de suelo y 5 µL de H2O estéril (Cloeckaert et al. 1996). Se utilizaron los carriles o columnas 1 a 7 para las muestras de suelo agrícola, el Carril 8 con el ADN de la cepa vacunal de Brucella melitensis (BM16 NCTC 301) como testigo positivo y el Carril 9 con ADN de E. coli como testigo negativo. La reacción se practicó en un termociclador MasterCycler con el siguiente ciclo: naturalización inicial a 94 ºC (5 s), seguida de 30 ciclos: hibridación a 58 ºC (1 min), elongación a 70 ºC (1.5 min), desnaturalización a 94 ºC (1 min), hibridación a 58 ºC (1 min) y elongación final a 70 ºC (10 min). Por último, se mantuvo la reacción a 4 ºC por 30 min.
Se realizaron amplificaciones del ADN bacteriano por PCR, las cuales se visualizaron en gel de agarosa al 1.3 % (p/v) y se tiñeron con bromuro de etidio (0.5 μg/mL) para visualizar los productos de la amplificación del gen bp26/IS711, que es específico del género Brucella (Cloeckaert et al. 2000). Se observaron las bandas de amplificación del gen bp26 en un transiluminador de rayos UV (marca Spectroline) y las fotografías de los geles se tomaron con un equipo Kodak-Edas.
RESULTADOS
Análisis físico y químico de las muestras de suelo agrícola
En el agrosistema del municipio Emilio Portes Gil, los suelos son profundos, de color claro (gris), con textura salina franco-arenosa. En cuanto a su clasificación se identificaron como de tipo Solonchak (suelos de color pálido o gris que se encuentran en condiciones áridas y con mal drenaje). Por otra parte, en cuanto su edafología, los suelos dominantes son arenosoles (40.28 %), phaeozem (22.44 %), leptosoles (15.34 %), andosoles (13.84 %) y fluvisoles (5.73 %) (FAO 2020, INEGI 2020). En el Cuadro I se resumen los resultados de los análisis físicos y químicos de las muestras agrícolas: porcentaje de materia orgánica (MO %), pH, humedad (%), nitrógeno total (NT) y coeficiente de variación (VAR) (NOM-021-RECNAT-2000; SEMARNAT 2002). El ANDEVA arrojó interacciones significativas para las combinaciones pH-sitio: F(5,9) = 11.512, p = 0.00107; y MO %-sitio: F(5,9) = 5.8043, p = 0.0115.
CUADRO I RESULTADOS DE LA CARACTERIZACIÓN FÍSICA Y QUÍMICA DE LAS MUESTRAS DE SUELO AGRÍCOLA DE LA COMUNIDAD EMILIO PORTES GIL, PUEBLA, MÉXICO.
| Sitios | Materia orgánica (%) | pH | Humedad (%) | Nitrógeno total (%) | Coeficiente de variación |
| 1 | 7.17 | 8.2 | 15.51 | 0.17 | 0.006 |
| 2 | 7.69 | 8.4 | 18.57 | 0.25 | 0.005 |
| 3 | 8.14 | 8.1 | 18.92 | 0.25 | 0.005 |
| 4 | 9.01 | 7.9* | 22.94 | 0.07 | 0.004 |
| 5 | 9.09 | 7.8* | 19.88 | 0.14 | 0.007 |
| 6 | 4.44** | 8.8 | 17.22 | 0.25 | 0.005 |
| 7 | 7.51 | 8.2 | 21.70 | 0.80 | 0.005 |
| 8 | 8.20 | 8.5 | 21.05 | 0.25 | 0.005 |
| 9 | 6.88** | 8.7 | 17.66 | 0.25 | 0.005 |
| 10 | 9.95 | 7.8* | 18.89 | 0.45 | 0.003 |
*pH medianamente alcalino; **bajo porcentaje de materia orgánica.
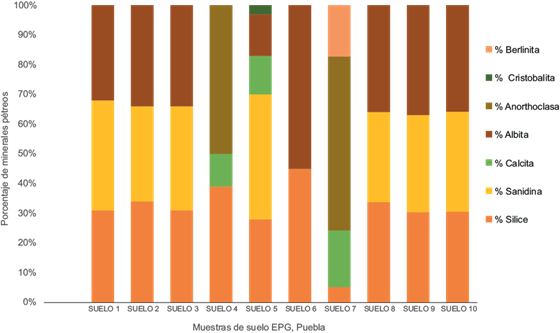
Determinación de minerales petrogénicos
En la figura 2 se aprecian los principales minerales petrogénicos detectados en las muestras de suelo analizadas. De acuerdo con los resultados del análisis en la comunidad Emilio Portes Gil predominan los minerales pétreos: albita, sanidina y sílice, siendo los de menor proporción la calcita y la cristobalita.
Análisis microbiológico
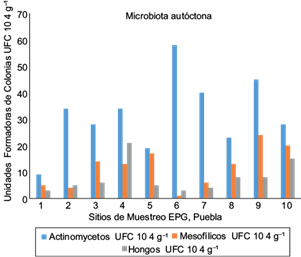
Microbiota autóctona
Se muestran los resultados (en porcentajes) del análisis de microbiota autóctona para hongos, organismos mesolíticos y actinomicetos en cada una de las muestras (Fig. 2). Nuestros resultados indican que los actinomicetos constituyen un componente significativo de la población microbiana del suelo (casi un millón por gramo de suelo); en segundo término, están los organismos mesofílicos. Entre los organismos termófilos se encuentran los géneros Clostridium, Streptomyces, Chaetomium y Humicola, presentes en el estiércol y los vegetales en descomposición. El ANDEVA arrojó una interacción significativa para la combinación Shannon-sitio: F(5,9) = 4.0068, p = 0.0344). Los microbios celulolíticos del suelo son principalmente mesófilos (Fig. 3 ).
Primoaislamiento
El aislamiento de Brucella spp. constituye el método diagnóstico definitivo. De los 10 sitios de muestreo de suelo analizados en este estudio, se realizó primoaislamiento para Brucella spp. en el total (100 %) de las muestras estudiadas.
Actividad metabólica
Debido a que Brucella es un género monoespecífico, contiene enzimas que están codificadas en todas sus especies, lo que permite su diferenciación. Este género se caracteriza por su baja producción de CO2, crecimiento lento y actividad metabólica reducida. Además, presenta bacterias oxidativas. Por lo tanto, en pruebas que normalmente evidenciarían la utilización de carbohidratos a través de la fermentación en su metabolismo, como en los casos de TSI, CIT y RMVP, o pruebas que implican descarboxilación o desaminación de aminoácidos, como LIA y MIO, los resultados en este género difieren de otras bacterias y suelen ser negativos. La evaluación de la actividad metabólica de Brucella spp. a partir de su primoaislamiento en suelo de la comunidad Emilio Portes Gil dio como resultado lo siguiente: CO2 independiente (-), no produjo H2S (-), mostró crecimiento positivo en presencia de fucsina básica (+) y de tionina (+), positivo para safranina (+) e hidrolizó de manera normal la urea (+). Estos resultados concuerdan con la actividad metabólica de Brucella melitensis medida con los métodos microbiológicos clásicos.
Sobrevivencia de Brucella spp.
En este experimento Brucella sobrevivió hasta 120 días en promedio (muerte experimental) en muestras de suelo inoculadas con las siguientes cepas vacunales de referencia: B. melitensis M16 (NCTC 301), B. abortus S19 (NCTC 305) y B. abortus RB51 (B-0653-048).
Purificación de las muestras
A partir de las resiembras efectuadas en los 10 sitios de muestreo, sólo en siete de ellos se obtuvo ADN bacteriano de calidad (69.8 %), el cual se resguardó en la colección bacteriana del LPB-ICUAP-BUAP a -4 ºC para su posterior análisis.
Detección por PCR-PF
Se amplificó el gen bp26/IS711, que es específico del género Brucella, con 1029 pb [pares de bases]. El gen bp26 codifica la proteína BP26 (Omp28) que es un antígeno inmunodominante en la infección de Brucella sp. en fauna y humanos. Carril M, (marcador molecular), carriles 1-7 muestras problema (ADN bacteriano purificado a partir de suelo agrícola) (57 %), y se compararon con el testigo positivo (ADN de Brucella melitensis vacunal BM16) (+) Carril 8 (ADN de E. coli) y en el Carril 9 como testigo negativo (-) (Fig. 4, Cuadro II).
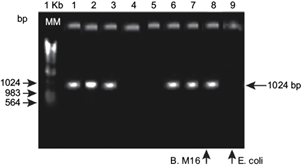
Fig. 4 Imagen en gel agarosa de la amplificación por prueba de reacción en cadenas de polimerasas (PCR) los genes bp26 (1024 pb) (cebador directo; 59GCCCCTGACATAACCCGCTT39) y bp26B (cebador inverso; 59GAGCGTGACATTTGCCGATA39) (GenBank U45996). Carriles 1-7: muestras problema de suelo agrícola; carril 8: cepa vacunal de Brucella M16 NTC 301 como testigo positivo; carril 9: Escherichia coli como testigo negativo.
CUADRO II PARÁMETROS EVALUADOS EN MUESTRAS DE SUELO QUE RESULTARON POSITIVAS PARA Brucella SEGÚN LA PRUEBA DE REACCIÓN EN CADENAS DE POLIMERASAS (PCR).
| Variable | Muestras | ||||||
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | |
| Materia orgánica del suelo (suelos volcánicos) (%) | 7.17 | 7.69 | 8.14 | 9.01 | 9.09 | 4.44 | 17.51 |
| pH | 8.2 | 8.4 | 8.1 | 8.2 | 8.3 | 7.8 | 8.2 |
| Humedad del suelo (%) | 15.15 | 18.57 | 18.92 | 22.94 | 19.88 | 17.22 | 21.7 |
| Cuarzo (%) | 31 | 33 | 31 | 39 | 28 | 45 | 5.1 |
| Sanidina (%) | 37 | 32 | 35 | 0 | 42 | 0 | 0 |
| Calcita (%) | 0 | 0 | 0 | 11 | 13 | 0 | 19.2 |
| Albita (%) | 32 | 33 | 34 | 0 | 14 | 55 | 0 |
| Anortoclasa (%) | 0 | 0 | 0 | 50 | 0 | 0 | 58.6 |
| Cristobalita (%) | 0 | 0 | 0 | 0 | 3 | 0 | 0 |
| Berlinita (%) | 0 | 0 | 0 | 0 | 0 | 0 | 17.2 |
| Actinomicetos (UFC × 104)/g | 9 | 34 | 28 | 34 | 19 | 58 | 40 |
| Bacterias mesófilas (UFC × 104)/g | 5 | 4 | 14 | 13 | 17 | 1 | 6 |
| Hongos (UFC × 104)/g | 3 | 5 | 6 | 21 | 5 | 3 | 4 |
| Supervivencia en suelo estéril (días) | 35 | 30 | 34 | 31 | 30 | 31 | 32 |
| ADN total del suelo y Brucella por prueba PCR | Positiva | Positiva | Positiva | Positiva | Positiva | Positiva | Positiva |
| Nitrógeno total (%) | 0.17 | 0.25 | 0.25 | 0.07 | 0.14 | 0.25 | 0.8 |
| Proteínas y nitrógeno (%) | 1.0625 | 1.5625 | 1.5625 | 0.4375 | 0.875 | 1.5625 | 5 |
UFC: unidades formadoras de colonias.
DISCUSIÓN
Diversos estudios microbiológicos han alertado sobre el riesgo de las excretas contaminadas como vectores de diseminación de microorganismos patógenos en suelos (Hutchison et al. 2005). Los resultados obtenidos en el presente estudio concuerdan con lo registrado por Morales-Estrada et al. (2016), quienes demostraron la presencia de Brucella spp. en heces de vacas y cabras en México. Como resultado de procesos de deflación e infiltración, este material puede contaminar la tierra de pastura al utilizar el suelo como reservorio. Por su parte, Li et al. (2015) registraron un porcentaje significativo de suelo contaminado por ADN de B. melitensis en excretas de cabras en una zona endémica de brucelosis en Pakistán. Sin embargo, tanto Hutchinson et al. (2005) como Li et al. (2017) realizaron sus aislamientos en suelo urbano y suburbano, y manejaron como factor de riesgo la cercanía a un mercado de venta de animales y un área de sacrificio.
En contraste, el tipo de suelo analizado en este estudio fue agrícola en su totalidad, donde es común observar el paseo itinerante de hatos de cabras. Estas malas prácticas agropecuarias son el factor de riesgo principal, conforme a lo sugerido por Cruz Aviña et al. (2021a, 2022). Se ha registrado una sobrevivencia para B. abortus de hasta 100 días como bioaerosol, así como su empleo como arma biológica por su amplio potencial de infección (Kuzdas y Morse 1954, Whatmore y Foster 2021). En este sentido, las características climáticas comunes de esta zona (tolvaneras y remolinos durante casi todo el año) hacen que la formación de bioaerosoles sea altamente factible (Cruz-Aviña et al. 2021b).
Por su parte Franz et al. (1997) evidenciaron que Brucella spp. sobrevive en el suelo y el polvo durante semanas. Por ejemplo, Brucella abortus sobrevive en fetos abortados hasta 135 días en invierno y más de dos meses en verano (WOAH 2016). Si los fetos están a la sombra, su sobrevivencia llega hasta seis meses (Corbel y Wray 1975). Asimismo, B. abortus puede sobrevivir hasta 66 días en suelo húmedo cuando la humedad aumenta a 90 % (Nicoletti 2001). Por el contrario, la luz del sol y altas temperaturas provocan un efecto negativo sobre la supervivencia de B. abortus en el ambiente suelo (Jones et al. 2010).
En nuestro experimento, Brucella melitensis M16 y B. abortus S19 sobrevivieron hasta 120 días en promedio a 20 ºC, lo que supera lo expuesto por Nicoletti (2001). Esto indica que las condiciones ambientales de la región en estudio desempeñaron un papel importante, ya que se trata de un desierto semifrío con bajas temperaturas y clima seco, por lo que reúne las condiciones ambientales ideales para la persistencia de Brucella (Cruz-Aviña et al. 2022) De igual manera, la prevalencia de Brucella en el suelo es uno de los factores de riesgo para su propagación a animales silvestres (i.e., anfibios, reptiles, roedores, cánidos, etc.) y para la interfaz ganado-fauna silvestre-humano y medio ambiente (agua natural) según refieren Cruz-Aviña et al. (2021a, b, 2022).
El ADN bacteriano es liberado activamente en el medio de las células vivas o pasivamente en el medio de las células muertas (Whatmore y Foster 2021). Se registra autólisis de las células bacterianas y liberación de contenidos intracelulares, incluido el ADN (Palmen y Hellingwerf 1995, 1997). El ADN bacteriano persiste en el suelo durante un largo periodo cuya duración depende de la disponibilidad de enzimas de degradación y el tipo de suelo (DeSalle et al. 1992, Smith et al. 2018).
En el suelo, las moléculas de ADN se adsorben y los coloides minerales permiten o impiden su degradación enzimática, particularmente por ADNasas (Romanowski et al. 1991). Los suelos analizados en esta investigación son de origen volcánico, cineríticos y muy arenosos (Solonchak), lo que facilita la deflación e infiltración. Adicionalmente (como se mencionó antes), la zona es un desierto semifrío con temperaturas invernales de hasta -8 ºC, lo que favorece la supervivencia de B. melitensis en el lugar. De forma similar, los cationes divalentes promueven la adsorción de ADN.
En el presente estudio, la arena, el pH y la materia orgánica que se encontraron en el suelo estuvieron asociados positivamente con la prevalencia de Brucella spp., y las muestras obtenidas en el sitio de estudio correspondieron a suelos formados por arena. Según lo establecido por Lorenz y Wackernagel (1994), los suelos arenosos están compuestos principalmente por arena, es decir, fragmentos de rocas y minerales. Estos suelos presentan una textura granular, son secos, tienen un drenaje rápido y suelen ser poco fértiles. En contraste, los limos tienen partículas con tamaños que fluctúan entre 0.002 y 0.05 mm, mientras que las arcillas cuentan con partículas de tamaño ≤ 0.002 mm. Por lo tanto, la arena puede ser hasta 100 veces mayor en tamaño que los limos y las arcillas, lo que facilita su capacidad de infiltración, tal como señalan también Levy-Booth et al. (2007).
Los suelos ácidos adsorben una mayor proporción de ADN que los alcalinos (Stotzky 2000); sin embargo, Brucella spp. prefiere los ambientes alcalinos para su sobrevivencia, ya que en el medio ácido no persiste (Cruz-Aviña et al. 2021a). En este estudio, la sobrevivencia de Brucella spp. in vitro fue de hasta 120 días en muestras compuestas de suelo arenoso salino (Cruz-Aviña et al. 2021b, 2022).
Asimismo, se ha establecido que un suelo alcalino es aquel que contiene azufre, calcio, magnesio, manganeso y sodio en mayor proporción o en concentraciones mayores que otros compuestos (FAO 2020). En este estudio, los elementos óxido de sodio (Na2O), óxido de magnesio (MgO), trióxido de azufre (SO3) y óxido de hierro III (Fe2O3) en suelo no mostraron asociación con la prevalencia de B. melitensis, en tanto que la concentración de óxido de silicio IV (SiO2) en el ambiente favoreció su persistencia, al igual que cantidades moderadas de óxido de calcio (CaO) y óxido de aluminio (Al2O3; Fig. 5). Esto contrasta con lo expuesto por Tsuzuki et al. (1994), quienes enfatizaron el papel de la inducción de citotoxicidad y roturas de ADN por cromato (VI), cadmio (II) y mercurio (II) en células resistentes, así como por peróxido de hidrógeno (H2O2).
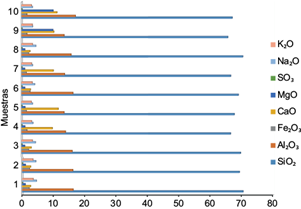
Fig. 5 Composición de óxidos básicos (%) detectados en las muestras de suelo agrícola de la comunidad Emilio Portes Gil, Puebla, México.
En la caracterización física y química del suelo en este estudio no se detectaron metales pesados; sin embargo, la presencia de SO3 puede vincularse con lluvia ácida o actividad volcánica reciente (hay varios volcanes cercanos al área de estudio y una zona de humeros a 15 km), al igual que la de CaO, también asociado con actividad volcánica reciente. De igual importancia son los resultados de Trevors (1996), quien sugiere que la presencia de magnesio (Mg) y calcio (Ca) en suelo disminuye la eficiencia de adsorción del ADN bacteriano, ya que los cationes de sodio y magnesio entran en competencia y reducen dicha eficiencia (Nguyen y Chen 2007).
En el presente estudio, los elementos del suelo como nitrógeno (N), fósforo (P), hierro (Fe), cobre (Cu) y níquel (Ni) no mostraron resultados positivos o detectables en las pruebas para su asociación potencial con la prevalencia de B. melitensis; sin embargo, en algunas comunidades los productores suelen aplicar estiércol de ganado y excretas de aves (que consiguen con facilidad, ya que en la zona existen granjas intensivas de estos animales) como fertilizantes. En la nutrición de estos animales con alimentos balanceados se agregan dosis de cobre, selenio y zinc que se bioacumulan; por lo tanto, las heces pueden provocar contaminación del suelo por metales pesados (Martín et al. 2021).
El suelo contaminado con metales como níquel, cadmio y cromo degrada el ADN y aumenta el porcentaje de ADNasas (Schmidt 1996). Por otro lado, de acuerdo con la prueba de sobrevivencia realizada en el Laboratorio de Patogenicidad Bacteriana del Centro de Investigación en Ciencias Microbiológicas de la Benemérita Universidad Autónoma de Puebla (CICM-BUAP), el suelo agrícola de la comunidad Emilio Portes Gil resultó fuertemente positivo para B. melitensis (cepa vacunal) y potencialmente viable para B. abortus (cepa vacunal) hasta por 120 días. Esta información concuerda con lo registrado anteriormente por Cruz Aviña et al. (2021a, b, 2022) para una zona cercana (el municipio de Guadalupe Victoria) en la que se ha señalado un problema zoonótico importante por B. melitensis; éste ha traspasado los compartimientos ecológicos de la interfaz (ganado-humano-fauna silvestre) y medio ambiente (agua natural de los lagos cráter), volviéndose un problema complejo (es decir B. melitensis está presente tanto en las personas de manera crónica y aguda, como en el ganado caprino, la fauna silvestre (peces, anfibios, reptiles y mamíferos pequeños) y el agua de lagos, suelo y aire (bioaerosol) de la región de Guadalupe Victoria, bajo el concepto integrador “una sola salud”, que enfatiza la interdependencia entre la salud humana, la sanidad animal y la salud ambiental, promoviendo un enfoque global basado en la colaboración multidisciplinaria (Beveridge y Koval 1981, FAO 2020, Cruz-Aviña et al. 2022). Por ello, en el futuro se esperan propuestas de estudios y experimentos con un enfoque integral y multidisciplinario. Respecto del suelo de la región de estudio, éste se caracterizó como Solonchak, es decir, salino (hiperhalino) y franco-arenoso. Este suelo soporta gran estabilidad de ADN bacteriano (hasta dos meses), como describieron Romanowski et al. (1993).
Por lo anterior, las posibilidades de sobrevivencia y estabilidad del ADN en la comunidad de Emilio Portes Gil son muy altas debido a este tipo de suelo y las bajas temperaturas, en concordancia con lo reportado por Selenska y Klingmüller (1992). Estos autores destacan también características positivas y asociaciones complejas con la microbiota autóctona, lo cual resulta interesante, ya que en este estudio se encontró un mayor porcentaje de actinomicetos, seguidos por organismos mesofílicos y, en menor porcentaje, hongos, lo cual nos da una idea de la complejidad de esta rizosfera. En contraparte y de manera alternativa, Ahmed et al. (2017) proponen en su estudio, como factor de riesgo principal, la escasa distancia (< 1 km) del mercado de animales vivos y de los mataderos (rastros de venta de carne), donde los animales infectados por Brucella spp. contaminan al ganado sano, utilizando como reservorio al sustrato suelo (y la formación de bioaerosoles), como han destacado también Musallam et al. (2015).
Es válido mencionar que la ausencia de polimorfismo genético de las especies de Brucella dificulta su identificación, ya sea por electroforesis, amplificación aleatoria de ADN o PCR-PF (Cloeckaert et al. 2000). A diferencia de lo que sucede con otras bacterias patógenas, la identificación de las especies de Brucella no se logra mediante la secuenciación directa del ARNr 16S (Moreno et al. 1990) ni con la amplificación de la región del ADN ribosómico situada entre 16S y 23S (Cloeckaert et al. 2000). Una de las técnicas más eficientes para la diferenciación entre especies consiste en aprovechar la secuencia de inserción en el cromosoma IS711, generando diferentes tamaños de amplificación según la especie. De esta forma se puede diferenciar B. melitensis del resto de las especies de Brucella con un rango de 1024-1030 pb (Moreno et al. 1990).
En este estudio se optó por la amplificación de la región bp26 (Omp28) con resultados satisfactorios. En correspondencia, se utilizó PCR-PF para amplificar el gen bp26/IS711 (Cloeckaert et al. 2000), que codifica para la proteína BP26 (Omp28), un antígeno inmunodominante en la infección de Brucella en fauna silvestre y humanos. Esto reafirma que existe un problema zoonótico en la región. De acuerdo con la secuencia de genes en el ARNr 16S, el género Brucella está categorizado como una proteobacteria (α-2) cercana filogenéticamente a los grupos Agrobacterium, Rickettsia, Rhizobium y Rhodobacteraceae (Moreno et al. 1990).
Es importante destacar que se utilizó un enfoque polifásico para incorporar las detecciones microbiológicas estándar; no obstante, el aislamiento y resiembra del patógeno sigue siendo la prueba de oro confirmatoria en el estudio de la brucelosis (Godfroid 2002, Godfroid et al. 2010, 2011), al igual que técnicas moleculares confirmatorias (basadas en PCR-PF) para examinar los efectos de las diferentes muestras del suelo.
Asimismo, es necesario aclarar que el impacto de la gestión del uso de la tierra, así como las buenas prácticas y regímenes de cultivo sobre las estructuras y comunidades microbianas de los suelos activos, no fueron consideradas en este estudio.
Autores como Suzuki et al. (1998) reconocen el sesgo en métodos basados en PCR-PF en algunos estudios; sin embargo, las comparaciones relativas entre comunidades microbianas basadas en estos métodos se han aplicado rutinariamente como pruebas confirmatorias para el estudio de la diversidad microbiana dentro de entornos complejos, superando de esta forma los sesgos resultantes de la baja tasa de cultivo de la mayoría de los microorganismos encontrados en suelos (Escalante-Lozada et al. 2004). Sin embargo, en este estudio el aislamiento de las muestras de suelo con el medio selectivo Brucella-BUAP fue del 100 % respecto de su primoaislamiento, del 68. 9 % en cuanto a su purificación y del 57 % con relación a su detección por PCR-PF.
La presencia de B. melitensis en suelos agrícolas de México activa las alarmas en el territorio nacional, ya que se le considera como una de las especies más nocivas para la salud humana (Theron y Thantsha 2014) y su capacidad de colonización en otros organismos es notable, por ejemplo, en peces, anfibios, lacertilios y ratones de campo (Cruz-Aviña et al. 2020, 2021a, 2022, Mazlina et al. 2021). Según la Organización Mundial de la Salud la brucelosis es responsable de más enfermedades, miseria y pérdidas económicas que cualquier otra enfermedad animal conocida que afecte a los humanos (NOM-138-SEMARNAT/SSA1-2012; SEMARNAT 2013). Esta enfermedad ejemplifica la falta de interacción entre los sectores de salud pública y veterinaria, que la ha convertido en una de las zoonosis más frecuentes en el mundo (Cruz-Aviña et al. 2017, 2022). Su presencia en suelo agrícola, donde la interacción con los agricultores es constante, es de vital importancia para considerar la brucelosis como enfermedad prioritaria en los planes de manejo de zonas afectadas con este patógeno. Por esta razón debe destacarse que las cepas de referencia B. abortus S19 y B. melitensis M16 son parte importante de los programas gubernamentales de control y erradicación de brucelosis de la Secretaría de Agricultura, Ganadería, Desarrollo Rural, Pesca y Alimentación (SAGARPA) en el área de estudio. De ahí la importancia de este estudio y la utilización de estas especies de manera vacunal como controles.
CONCLUSIONES
Este es el primer registro de aislamiento de B. melitensis en suelos agrícolas en México. Se pudo aislar y confirmar la presencia de este microorganismo en suelo de una región endémica para brucelosis en Puebla.
Se determinó la presencia de B. melitensis con una eficacia del 100 % en el primoaislamiento, 69.8 % en el proceso de resiembra y purificación del ADN bacteriano, y 57 % en pruebas confirmatorias por PCR-PF.











 nueva página del texto (beta)
nueva página del texto (beta)