Introducción
El aprendizaje de la química orgánica puede ser un reto en los distintos niveles de enseñanza debido a múltiples factores (Gutiérrez-Mosquera y Barajas-Perea, 2019). Uno de los desafíos que tiene el estudiantado es entender las distintas representaciones que puede tener una misma molécula o macromolécula (Salgado-Chavarría y Palacios-Alquisira, 2021) a través de representaciones en 2-D a una visualización mental en 3-D. Tradicionalmente, las estructuras químicas tridimensionales se representan bidimensionales, y el estudiantado está expuesto a todas ellas en los cursos de química (Marzábal et al., 2024), en especial en los cursos de química orgánica cuando se estudia estereoquímica (Stieff, 2011; Durmaz, 2018; Pineda et al., 2019) la cual estudia la distribución espacial de las moléculas tridimensionalmente (López et al., 2023). Sin embargo, la comprensión de la estereoquímica no es una tarea fácil, especialmente cuando se abordan conceptos complejos como la quiralidad (Da Silva et al., 2021; Elford et al., 2021), la cual se refiere a la propiedad que tiene una molécula de no ser superponible con su imagen especular, esto quiere decir, que un carbono al tener un centro asimétrico posee cuatro átomos o grupos de átomos diferentes entre sí (McMurry, 2017; Zuñiga-Estrada y García, 2023).
Existen diversas estrategias que ayudan al desarrollo de habilidades visoespaciales (Pineda et al., 2019) para la comprensión de las diferentes representaciones y su relación con las moléculas en tres dimensiones. Las principales representaciones utilizadas en química orgánica son las fórmulas de Haworth, y de cuñas y líneas, proyecciones de Fischer, conformación de silla y representaciones de Newman (Kumi et al., 2013; Dickenson et al., 2020; Butler, 2021), y cada representación nos brinda una información diferente (Stieff et al., 2016), por lo que es importante trabajar simultáneamente con esas representaciones para profundizar los conceptos (Treagust et al., 2003; Habig, 2020). A su vez, el proceso de cambio entre representaciones, es decir, interconvertir, se conoce como traducción representacional (Mistry et al., 2020), y para ello, se debe crear una imagen mental, utilizando habilidades espaciales o visoespaciales (Carlisle et al., 2015; Suárez y Betancourt, 2023). Las habilidades visoespaciales están relacionadas con el rendimiento académico (Elford et al., 2022). Para la asignación de configuración absoluta de estereocentros los estudiantes pueden utilizar rotaciones mentales o estrategias específicas diseñadas por el docente, y la evidencia muestra que aquellos estudiantes que aplican esas estrategias específicas son más precisos en la asignación (Wu y Shah, 2004).
En química orgánica, el uso de modelos representacionales de estructuras químicas es fundamental para comprender sus propiedades fisicoquímicas, la reactividad o un mecanismo de reacción (Marzábal et al., 2024), por ello, es muy importante que el estudiantado logre desarrollar competencias representacionales para construir modelos de las moléculas. Las habilidades para comprender con precisión representaciones visuales se denominan competencias representacionales perceptivas (Oliver-Hoyo y Babilonia-Rosa, 2017; Rau, 2017). El profesorado suele utilizar modelos físicos, teóricos o visuales para representar compuestos químicos (Casselman et al., 2021), y con el desarrollo tecnológico estos últimos se convierten en una opción interesante. Las competencias perceptivas y representacionales podrían abordarse a través de múltiples ejemplos en un juego, donde los estudiantes deben interconvertir entre diferentes representaciones (Eastwood, 2013; Rizzatti y Prestes-Jacaúna, 2022). El uso de la tecnología en el desarrollo de la traducción representacional ayuda a visualizar estructuras químicas en 3-D y, junto con juegos interactivos, podemos mejorar la participación en el proceso de aprendizaje en química (Da Silva Junior et al., 2019; Monnot et al., 2020; Elford et al., 2021).
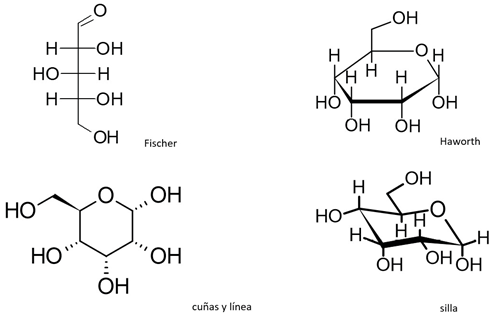
En este estudio se aborda un método instruccional para representar un monosacárido de proyección de Fischer a fórmula de Haworth y finalmente a la representación de cuñas y líneas para reducir los conceptos erróneos o las propias suposiciones (Carlisle et al., 2015). La elección de utilizar monosacáridos es debido a que tienen una fórmula molecular que puede representar a más de cien estructuras diferentes, ya sean de formas lineales o cíclicas, y comúnmente se abordan en diferentes representaciones, como Fischer, Haworth, cuñas y líneas, y silla (Rahi, 1991; Arya y Kumar, 2020), por lo que existen múltiples posibilidades que generan isómeros (Figura 1). El objetivo de este estudio es identificar las representaciones que son más sencillas para el estudiantado, utilizando una estrategia didáctica para la comprensión y asignación de configuración absoluta de estereocentros en la estereoquímica de compuestos orgánicos.
Metodología
La química orgánica tiene como objetivo desarrollar en los estudiantes las habilidades necesarias para explicar la formación, composición, estructura y reacciones químicas de los compuestos químicos orgánicos y sus derivados, utilizando los conceptos básicos de la química orgánica. Esta asignatura proporciona el conocimiento de la nomenclatura y propiedades fisicoquímicas de las diferentes estructuras presentes en fármacos, correspondientes a las bases del conocimiento de los mecanismos de acción y funcionamiento de los fármacos que se profundizan en cursos específicos posteriores y que son de gran interés para los estudiantes de la carrera de Química y Farmacia.
Contexto y muestra
La muestra de 17 estudiantes correspondiente al estudiantado de cuarto semestre de la carrera de Química y Farmacia que se encuentran cursando la actividad curricular Química Orgánica.
Esta actividad curricular pertenece al ciclo inicial del plan de estudios de la carrera de Química y Farmacia. Además, el curso de Química Orgánica corresponde al área de formación teórico-práctica, permitiendo la síntesis de fármacos en laboratorio y es un requisito previo para la asignatura de Fármaco-Química que se imparte en el semestre siguiente (Barrientos y Moris, 2022).
Para llevar a cabo la intervención, el estudiantado fue dividido en dos grupos, grupo control (Grupo A) de 9 estudiantes y un grupo experimental (Grupo B) 8 estudiantes, en el que posterior a la intervención, se les aplicó una prueba con el mismo número y tipo de ejercicios. La subdivisión del curso es debido a que trabaja en talleres de no más de 10 estudiantes por grupo siguiendo los lineamientos de la universidad.
Grupo A: se le explicaron las reglas de Cahn Ingold Prelog (CIP) para estereoquímica sólo con diapositivas que mostraban diferentes estructuras con diferentes representaciones, así como muchos libros de química orgánica, donde deben asignar la configuración absoluta con estereodescriptores (R y S).
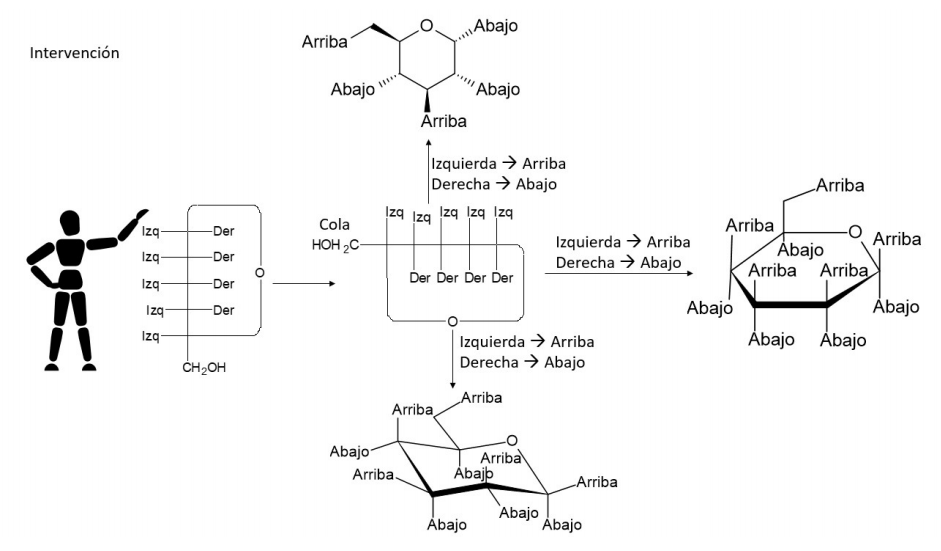
Grupo B: al grupo se les explica la interconversión entre la proyección de Fischer, la conformación de silla, las fórmulas de Haworth y de cuñas y líneas utilizando la Figura 2, siguiendo los pasos de la estrategia didáctica.
Estrategia didáctica para la interconversión de representaciones
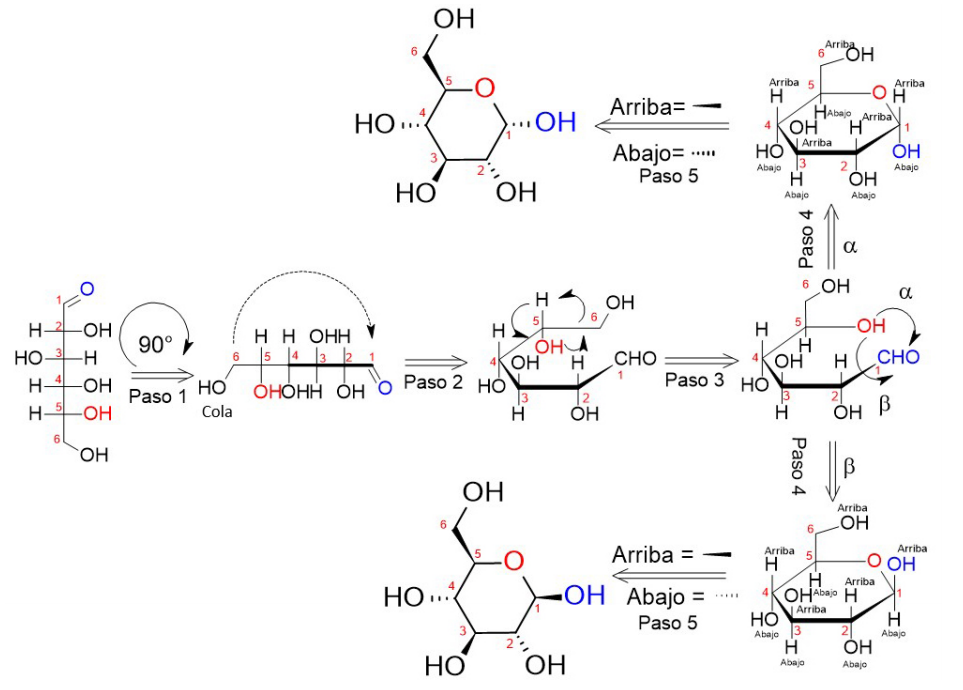
A continuación, se describe el paso a paso de la estrategia planteada para dibujar la formación de anómeros a partir de la proyección de Fischer asignando los estereocentros (Figura 3).
Paso 1. Girar 90º hacia la derecha la proyección de Fischer.
Paso 2. Etiqueta el grupo de la izquierda como “cola”.
Paso 3. Etiquetar la cola como “arriba” si el sustituyente en el carbono más cercano está en la posición inferior, o etiquetar “abajo” si está el sustituyente se encuentra en la posición superior.
Paso 4. Etiqueta como “abajo” el resto de los sustituyentes que se encuentran en la posición inferior.
Paso 5. Etiqueta como “arriba” el resto de los sustituyentes que se encuentran en la posición superior.
Paso 6. Para la fórmula de Haworth y la conformación de silla, mantenga la etiqueta “arriba” y “abajo” y, si el sustituyente más cercano a la “cola” está etiquetado como “abajo” o “arriba”, entonces la cola estará “arriba” o “abajo” respectivamente.
Paso 7. Utilice cuña sólida o punteada para los sustituyentes etiquetados como “arriba” y “abajo” respectivamente, para la fórmula de cuñas y líneas.
Resultados y discusión
Previo a la intervención con el grupo B, se desarrolló una clase de introducción a la estereoquímica con un barrido histórico desde los primeros planteamientos hasta los más actuales, además se trabajaron con ejemplos de cómo se presenta una molécula en proyección de Fischer. Posteriormente, se aplicó un pretest con ambos grupos, en el que se plantean cuatro ejercicios para asignar la configuración absoluta de estereocentros a las representaciones de Fischer, Haworth, cuñas y líneas, y silla, como se presenta en la Figura 1, dando como resultados que sólo asignaron la configuración absoluta de los estereocentros a las representaciones de Fischer, y cuñas y líneas.
Durante la intervención, al estudiantado del grupo B se les explicó cómo realizar la interconversión a partir de las proyecciones de Fischer a conformaciones de silla, fórmulas de Haworth y de cuñas y líneas descrita con la estrategia didáctica y la Figura 3. En paralelo, con ambos grupos se trabajó con modelos moleculares concretos, en los que pudieron generar moléculas en 3-D a partir de las representaciones planas 2-D que se visualizan en las guías de trabajo. Tras las 10 sesiones de clases de la unidad completa y solo 2 correspondientes a estereoquímica y quiralidad, se aplicó un test posterior a ambos grupos similar en número y tipo de ejercicios al test previo. De esta manera, en el postest, el estudiantado pudo asignar la configuración absoluta de los estereocentros en las proyecciones de Fischer y en las fórmulas de cuñas y líneas, así mismo, pudieron realizar la interconversión entre las fórmulas de Haworth y las fórmulas de silla a partir de la proyección de Fischer (Figura 4).
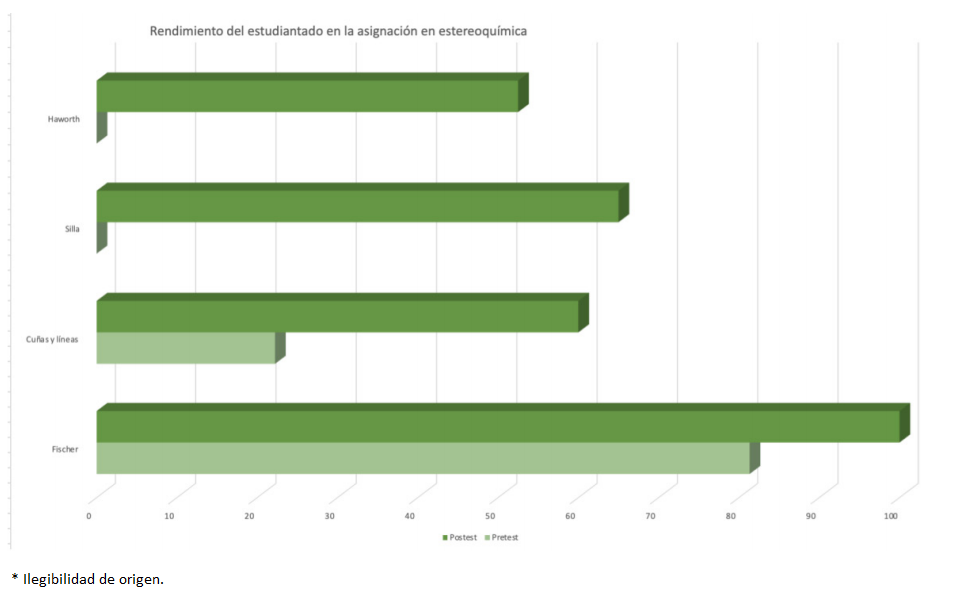
Figura 4 Rendimiento del estudiantado en la asignación de configuración absoluta de estereocentros en moléculas orgánicas.
Como se muestra en la Figura 4, hubo un gran aumento en el rendimiento académico para asignar la configuración absoluta de estereocentros para las fórmulas de Haworth y silla, de 0% a 65% y de 0% a 52,5% respectivamente; para las fórmulas de cuñas y líneas el aumento fue de 22,2% a 60% y para las proyecciones de Fischer de 81,3% a 100% mostrando que la proyección de Fischer fue la representación más sencilla para la asignación de configuración absoluta de estereocentros. Los datos anteriores permiten visualizar que la estrategia didáctica que se presentó al estudiantado los ayudó para la asignación de la configuración absoluta de estereocentros de diversas moléculas orgánicas, pudiendo desarrollar habilidades visoespaciales para la interconversión de las diferentes representaciones.
Los mejores resultados para la asignación de estereocentros son para las proyecciones de Fischer y las fórmulas de cuñas y líneas, lo que indica una mayor facilidad para comprender la estereoquímica de un compuesto con tales representaciones. Sin embargo, ¿a qué se debe que sea más sencillo para el estudiantado entender las representaciones de Fischer y cuñas y líneas? Según lo reportado por la literatura y lo analizado en este estudio, el estudiantado logra dimensionar y visualizar de mejor manera la asignación de estereocentros por la disposición de la estructura molecular de las moléculas (García-Ruíz et al., 2012), ya que se encuentra abierta para observar y analizar la quiralidad de la molécula (Valdivia-Giménez, 2022), muy similar a lo que ocurre en las fórmulas de cuñas y líneas, identificando los enlaces que van hacia adelante y hacia atrás del plano.
Consideraciones finales
Con este estudio se evidencia una forma sencilla para la comprensión de la interconversión a partir de las proyecciones de Fischer a fórmulas de Haworth, de cuñas y líneas, y conformaciones de silla. Esta intervención permitió a los estudiantes realizar con mayor facilidad interconversiones entre las diferentes representaciones, aumentando radicalmente el porcentaje de logros en la prueba realizada. Este tipo de estrategia posiblemente ayudó al estudiantado a crear una imagen mental 3-D a partir de una representación 2-D y facilitó la asignación de estereocentros con los estereodescriptores R y S y cómo se ve este estereocentro con diferentes representaciones (Valdivia-Giménez, 2022).
El estudiantado puede utilizar las diferentes representaciones para asignar correctamente una configuración en una representación desconocida, y esto beneficiará la comprensión de la disposición espacial y los sitios reactivos, lo que permitirá un mejor entendimiento de cómo se desarrollan los mecanismos de reacción en la química orgánica.











 nueva página del texto (beta)
nueva página del texto (beta)