Introducción
En México, los ingresos por la producción de tomate ascendieron a $ 36,508 millones de pesos mexicanos en el cierre del año 2023 (SIAP, 2024), siendo uno de los principales productos agrícolas de exportación. Diversos agentes patógenos, como hongos, bacterias, insectos y virus afectan los cultivos de tomate, lo cual genera pérdidas económicas importantes. El complejo de especies conocidas como Ralstonia solanacearum, RSSC por sus siglas en inglés, es el agente causante de marchitez bacteriana en distintas especies de plantas de importancia económica, tales como berenjena, plátano y tomate. Existen reportes en la literatura relacionados con el aislamiento de R. solanacearum en plantas de tomate en varios estados mexicanos como Morelos, Sinaloa, Baja California y Jalisco (Hernández-Romano et al., 2012; Perea et al., 2011); sin embargo, no se conocen las estadísticas del daño ocasionado por esta enfermedad en México. Se estima que esta bacteria es la responsable de la pérdida del 30 al 90% de las cosechas de papa (Solanum tuberosum) alrededor del mundo, por lo que está considerada entre los primeros 10 fitopatógenos más peligrosos a nivel mundial (Karim et al., 2018; Yuliar et al., 2015).
Recientemente, las bacterias incluidas dentro del RSSC fueron divididas en tres especies: R. pseudosolanacearum, que incluye cepas pertenecientes a los filotipos I y III, cuyo origen geográfico se sitúa en Asia y África; R. solanacearum, que incluye especies americanas pertenecientes al filotipo II; finalmente, R. syzygii, que abarca las cepas del filotipo IV, cuyo origen se sitúa en Indonesia y Japón (Paudel et al., 2020; Prior et al., 2016).
En nuestro grupo de investigación se han aislado distintos bacteriófagos líticos para ser empleados como agentes antimicrobianos en el combate de R. solanacearum (Hernández-Romano et al., 2019), y se prevé que su aplicación en plantaciones de tomate ayudará a prevenir la marchitez bacteriana. En este contexto, la evaluación del efecto protector de los bacteriófagos, así como su aplicación en invernaderos experimentales y comerciales hace necesario el desarrollo de un bioproceso para lograr la producción de grandes volúmenes de soluciones virales.
Considerando que R. solanacearum es el sustrato para llevar a cabo la amplificación viral, en este estudio se aborda la determinación de los parámetros cinéticos y estequiométricos de este microorganismo. Los datos generados en este estudio permitirán un mejor entendimiento de la fisiología del fitopatógeno; además, son necesarios en el desarrollo de un bioproceso para la producción de bacteriófagos. En un estudio reciente, se caracterizó el crecimiento de la cepa R. pseudosolanacearum GMI1000 en diferentes fuentes de carbono (Baroukh et al., 2022), obteniéndose sus parámetros cinéticos, características importantes para entender el crecimiento de la bacteria en el xilema. Existen reportes en los que se empleó una cepa de R. solanacearum aislada en Brasil como plataforma para la producción de poli(3-hydroxybutirato); sin embargo, los autores no reportaron los parámetros relativos al crecimiento de esta cepa (Alves et al., 2019). Por lo que se sabe, éste es el primer reporte de parámetros cinéticos y estequiométricos para una cepa de R. solanacearum perteneciente al filotipo II aislada en México.
Materiales y métodos
La cepa RsJ0314 se aisló de plantas de tomate con marchitez bacteriana en el municipio de Jiutepec, Morelos en marzo de 2014. Para mantenimiento de R. solanacearum RsJ0314 y la preparación de inóculos se empleó el medio NBYS (peptona de caseína, 5.0 g L-1, extracto de carne 3.0 g L-1, extracto de levadura 2.0 g L-1, K2HPO4 2.0 g L-1, KH2PO4 0.5 g L-1, MgSO4 0.25 g L-1, sacarosa 25 g L-1). Para evaluar distintas fuentes de carbono se utilizó un medio mineral (MM) cuya composición fue la siguiente: (NH4)2SO4 0.5 g L-1, KNO3 0.38 g L-1, K2HPO4 1.0 g L-1, KH2PO4 0.5 g L-1, MgSO4 0.1 g L-1 y CaCl2 0.02 g L-1. Como únicas fuentes de carbono se emplearon glucosa (MMG), sacarosa (MMS) y maltosa (MMM), y fructosa a una concentración final de 1.0 g L-1. Las cinéticas de crecimiento se realizaron en los minibiorreactores RTS-1C (Biosan Ltd., RTS1C, Riga, Letonia), con un volumen de operación de 25 mL. Las condiciones de cultivo fueron 30 °C, 2000 rpm de agitación y spin de 1 s-1. La Figura 1 muestra los promedios y desviaciones estándar de tres experimentos independientes para cada fuente de carbono. Para la determinación de la constante de afinidad (Ks), biomasa en peso seco y el rendimiento biomasa-sustrato (Yxs) se realizaron cinéticas en el biorreactor Biostat A (Sartorius, Götingen, Alemania) con un volumen de operación de 3.0 L. Las condiciones de cultivo fueron 300 rpm, 700 mL min-1 de aire, 30 °C. La concentración de biomasa de las muestras fue cuantificada determinando la densidad óptica a 600 nm (DO600nm) y mediante la determinación del peso seco celular. La concentración de glucosa residual se cuantificó por medio de un glucómetro (Countour TS, Bayer, Mishawaka, Indiana, Estados Unidos). En la Figura 2 se muestra el promedio y la desviación estándar de dos experimentos independientes.
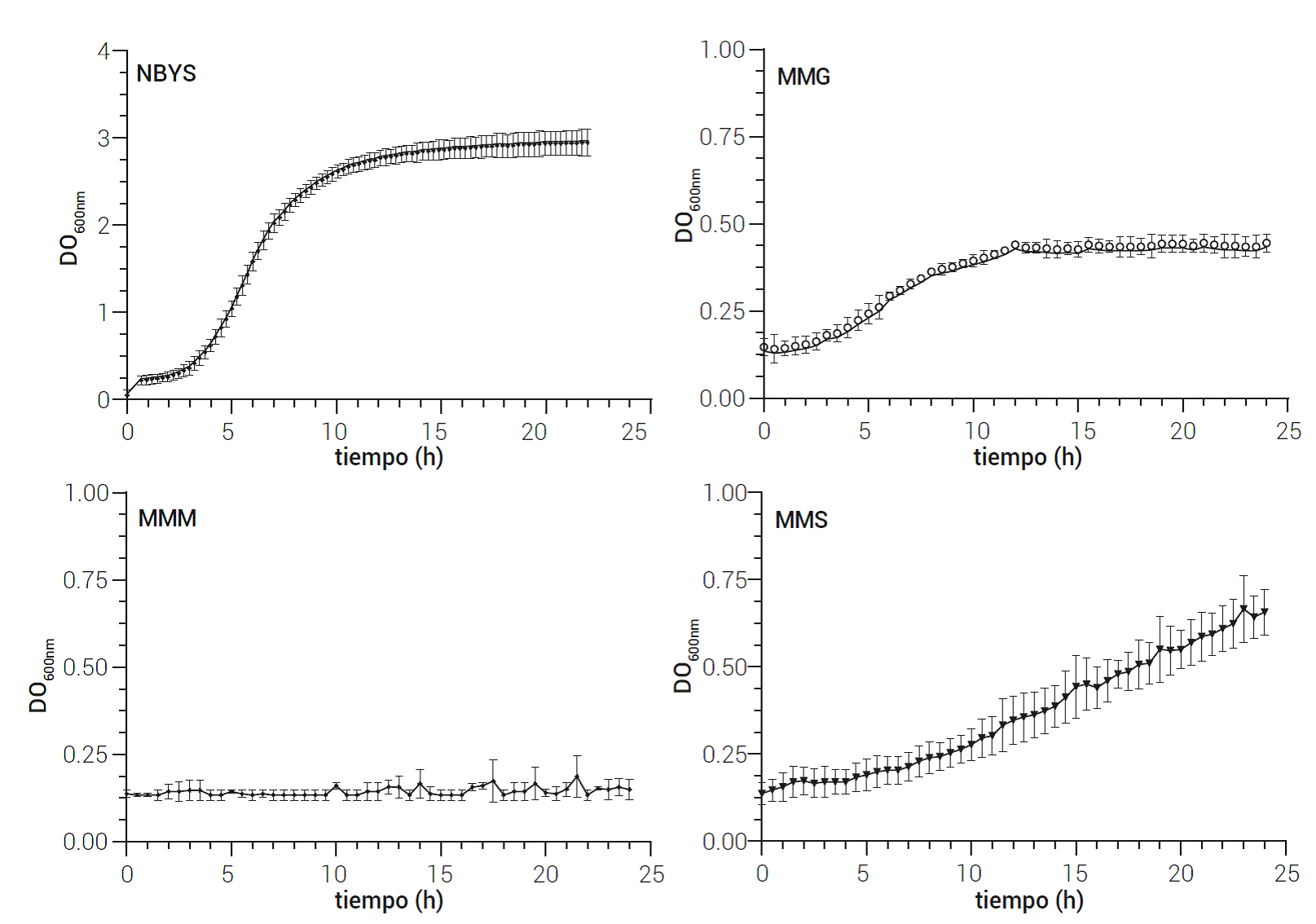
Figura 1 Crecimiento de R. solanacearum en distintas fuentes de carbono. NBYS: medio NBY con sacarosa, MMG: medio mineral con glucosa, MMM: medio mineral con maltosa, MMS: medio mineral con sacarosa. Los resultados mostrados son el promedio con la desviación estándar de tres experimentos independientes.
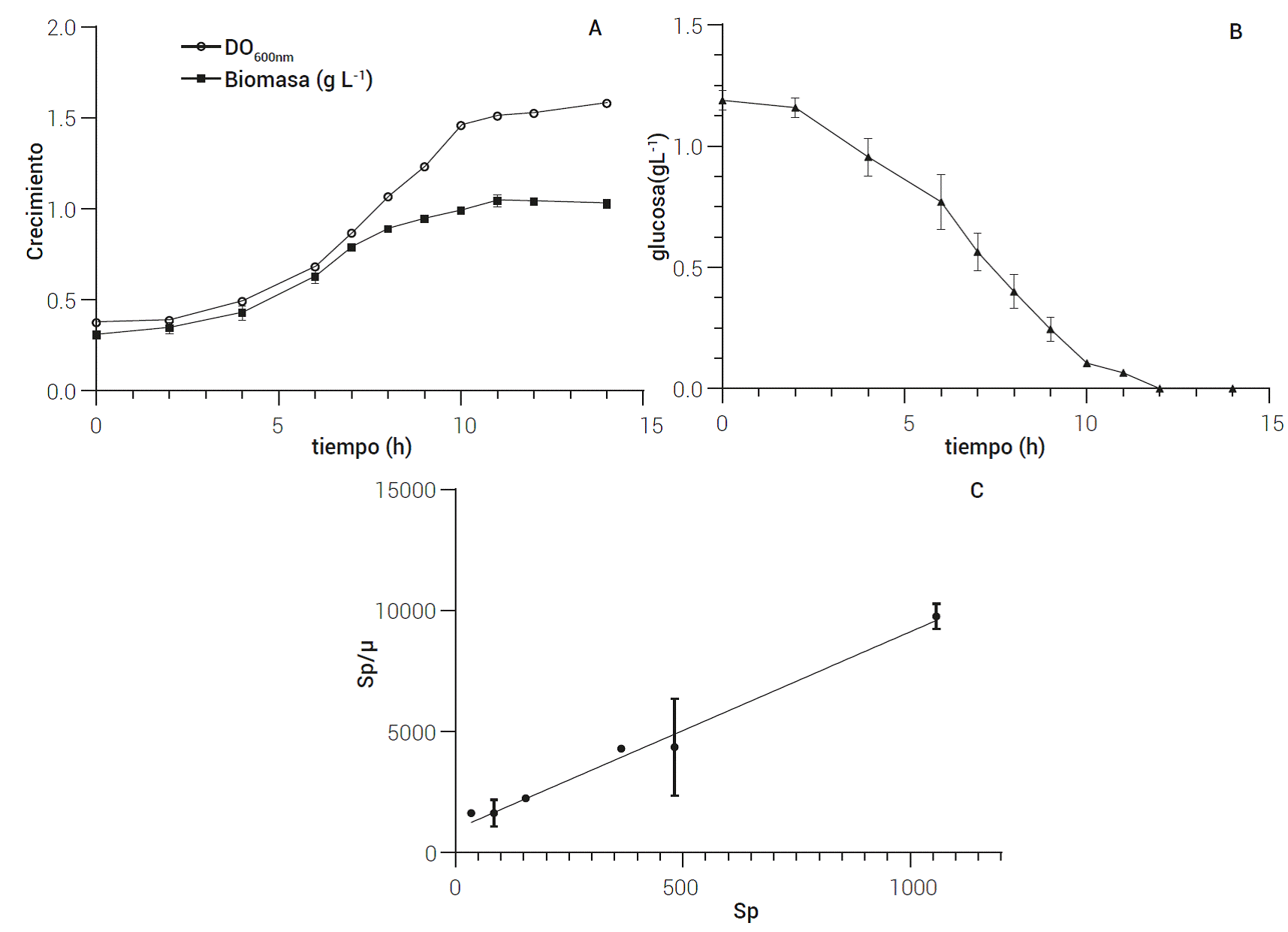
Figura 2 Crecimiento de la cepa RsJ0314 en cultivo por lote a un volumen de operación de 3.0 L. [A] Perfil de crecimiento en mg L-1 y DO600nm, [B] consumo de sustrato (mg L-1). [C] Diagrama de Langmuir para el cálculo de Ks. La ecuación de la recta es y = 9.155x + 960.2 con una R2 = 0.9389. En los gráficos se muestran el promedio y la desviación estándar de los datos obtenidos de dos experimentos independientes.
Para comparar cuantitativamente el crecimiento en las distintas fuentes de carbono se calculó la velocidad específica de crecimiento (µ) y el tiempo de duplicación (t d ) con la siguiente ecuación:
Donde t es el tiempo y x la concentración celular. El tiempo de duración de la fase lag (tL) y la biomasa máxima (Xm) fueron estimados con el apoyo del programa GraphPad Prism 9.0 y la ecuación de Gompertz, la cual se muestra a continuación:
Donde x 0 representa la biomasa inicial.
Para la determinación de la constante de afinidad (k s ) se usó una linealización de la ecuación de crecimiento de Monod:
Donde s p es la concentración promedio de la fuente de carbono.
Con los parámetros obtenidos de las cinéticas de crecimiento (Cuadro 1) se realizó análisis de varianza (ANOVA) de un factor con un nivel de significancia α = 0.05, además de la prueba de Fisher con un intervalo de confianza del 95 %. Ambos análisis se realizaron con el apoyo del programa Minitab 21.3.
Cuadro 1 Parámetros de crecimiento de R. solanacearum en diferentes medios de cultivo.
| Medio de cultivo | µ (h-1) | td (h) | tL (h) | Xmáx (DO600) |
| NBYS | 0.42± 0.05a | 1.42±0.16a | 0.41±0.04a | 2.91±0.13a |
| MMG | 0.15±0.03b | 4.65±0.79b | 0.22±0.01b | 0.45±0.02b |
| MMS | 0.08±0.01b | 8.29±0.70c | 0.03±0.00c | 3.02±0.75a |
µ: velocidad específica de crecimiento, td: tiempo de duplicación, tL: tiempo de duración de la fase lag, Xmáx: biomasa máxima en DO600nm. Existen diferencias estadísticamente significativas entre las medias que tienen distintas letras (a, b, c) en cada columna.
Resultados y discusión
En este estudio se caracterizó la cepa de R. solanacearum RsJ0314, perteneciente al filotipo II. Los parámetros de crecimiento calculados para esta cepa (Cuadro 1) se compararon con R. pseudosolanacearum GMI1000 que pertenece al complejo de especies RSSC (Baroukh et al., 2022). El primer grupo de experimentos se inició con la caracterización de R. solanacearum RsJ0314 en medio NBYS, ya que fue el medio de cultivo empleado para la preparación de inóculos y mantenimiento de la cepa (Figura 1, Cuadro 1). La µ en el medio NBYS fue de 0.42 ± 0.05 h-1, 2.3 veces superior en comparación con el medio MMG. La concentración celular máxima alcanzada en NBYS fue similar al MMS; sin embargo, el valor del tL en el medio NBYS fue mayor en comparación con los medios minerales. El medio mineral con sacarosa, glucosa, maltosa y fructosa mostró claras diferencias en el crecimiento de R. solanacearum RsJ0314. La µ en glucosa como única fuente de carbono fue de 0.15 ± 0.03 h-1, 1.9 veces superior a la µ en sacarosa, mientras que el td fue 1.8 veces superior en glucosa que en sacarosa. Este patrón coincide con los reportes de que la cepa R. pseudosolanacearum GMI1000, que tiene una µ en glucosa, es seis veces superior que en sacarosa (Baroukh et al., 2022). Una posible razón para explicar que la velocidad de crecimiento en glucosa sea mayor que en sacarosa se apoya en un reporte reciente en el que se demostró que las cepas pertenecientes a RSCC emplean principalmente la vía de Entner-Doudoroff (ED) para oxidar la glucosa, ya que carecen del gen pfk-1, que codifica para la fosfofructoquinasa; además, en este estudio se demostró que estas cepas no tienen el gen gnd (que codifica para la fosfogluconato deshidrogenasa), por lo que solamente emplean el brazo no oxidativo de la vía de las pentosas para metabolizar algunos azúcares y reciclarlos a glucosa-6-fosfato y gliceraldehído-3fosfato, lo cual también tendría implicaciones en la velocidad de crecimiento en sacarosa (Jyoti et al., 2020). Finalmente, en otro estudio se sugiere que la vía de ED es termodinámicamente más favorable que la glucólisis (Flamholz et al., 2013). Por otra parte, se generó una concentración de células 6.7 veces superior en sacarosa en comparación con la glucosa (Cuadro 1), lo cual pudiera deberse a que la sacarosa es un disacárido que, para metabolizarse, se descompone en glucosa y fructosa, lo que representa una mayor cantidad de carbono disponible para el crecimiento.
Por otro lado, no se observó crecimiento con maltosa como única fuente de carbono, lo cual fue un resultado esperado en las cepas que pertenecen al filotipo II, como R. solanacearum RsJ0314; así mismo, no se observó crecimiento en MM con fructosa (datos no mostrados), en comparación con la cepa GMI1000 que sí crece en esta fuente de carbono (Baroukh et al., 2022). Las razones por las cuales R. solanacearum RsJ0314 no creció con fructosa como única fuente de carbono aún deben determinarse, sin embargo, se tiene la hipótesis que ante la posible ausencia de los genes pfk-1 y gnd, se requiera de la presencia de otra fuente de carbono, como la glucosa, para que la bacteria crezca.
Para determinar el rendimiento biomasa-sustrato, la velocidad de consumo de sustrato y la k s de R. solanacearum RsJ0314 fue necesario realizar los experimentos en un biorreactor con un mayor volumen. Se eligió la glucosa porque es fuente de carbono con una µ y td mayores que en sacarosa, lo que podría acortar los tiempos del proceso. Los perfiles de crecimiento y consumo de sustrato se muestran en la Figura 2. La µ fue de 0.15 ± 0.02 h-1, el rendimiento fue de 0.61 ± 0.02 g biomasa g-1 glucosa (Yxs), la velocidad específica de consumo de glucosa (qs) fue de 0.28 ± 0.02 g glucosa g-1 biomasa h-1.
En el caso de la cepa R. pseudosolanacearum GMI1000, en condiciones similares de crecimiento, se reportó que tenía una µ de 0.23 h-1, Yxs de 0.45 g glucosa g-1 biomasa, y una qs igual a 0.5 g glucosa g-1 biomasa h-1(Baroukh et al., 2022) que son datos similares a los de RsJ03014. Con el apoyo del diagrama de Langmuir se determinó que la Ks de R. solanacearum RsJ0314 tiene valor de 117 ± 88 mg L-1(Figura 2), que es un valor que no había sido reportado previamente para esta bacteria.
Los datos obtenidos en este estudio coindicen con otros reportes en que la glucosa es una de las fuentes de carbono preferidas para R. solanaceraum, y que la sacarosa es muy importante en la colonización de la planta y la virulencia (Hamilton et al., 2021; Lowe-Power et al., 2018). Por lo anterior, ambas fuentes de carbono podrían ser usadas para el crecimiento de esta bacteria en un proceso biotecnológico.
Finalmente, es importante resaltar que ésta es la primera vez que se reportan los parámetros cinéticos y estequiométricos para una cepa de R. solanacearum perteneciente al filotipo II, de tal manera que este estudio contribuye al conocimiento que se tiene del fitopatógeno, además de ser una base para comparar las variaciones fenotípicas que puedan existir entre las cepas americanas.











 nueva página del texto (beta)
nueva página del texto (beta)


