Introducción
Los macromicetos degradadores de madera caída se consideran organismos clave en uno de los procesos más importantes para la vida en la Tierra, que es la descomposición de la lignocelulosa (Rolstad et al., 2004; Osono, 2007). Dichos hongos producen las enzimas más diversas y efectivas para la desintegración de celulosa, hemicelulosa y lignina, haciendo que los componentes de estos polímeros se reintegren al sistema suelo y a los ciclos de nutrientes (Floudas et al., 2012; Riley et al., 2014; Alshammari et al., 2021). Además, estos hongos son la base de una red compleja de organismos, que se ha calculado incluye de 400,000 a 1 millón de especies alrededor del mundo, asociados directa o indirectamente a la madera caída (Stokland et al., 2012).
La madera caída es desintegrada por los macromicetos por medio de tres tipos de pudrición, cuya clasificación se basa en una descripción visual, así como en los mecanismos que emplean los hongos para desintegrar la hemicelulosa, celulosa y lignina (Fukasawa, 2021). Así, hay especies de hongos que causan pudrición café, como los del Phylum Basidiomycota, en la cual los hongos involucrados metabolizan la celulosa y hemicelulosa, y modifican la lignina, de modo que la madera afectada adquiere un color oscuro y se fragmenta en forma de cubos (Pawlik et al., 2019). En la pudrición blanca, que la llevan a cabo hongos del Phylum Basidiomycota y la familia Xylariaceae del Phylum Ascomycota, los hongos involucrados metabolizan celulosa, hemicelulosa y lignina, y la madera toma un color blanco y una textura fibrosa (Schmidt, 2006). En la pudrición blanda, realizada por especies del Phylum Ascomycota y sus anamorfos, los hongos metabolizan hemicelulosa y celulosa de la capa central de la pared secundaria, y la apariencia de la madera es similar a la pudrición blanca; la consistencia es suave de peso, ligera o bofa (Kuhad et al., 2013).
Existen diferentes factores abióticos y bióticos que influyen en la diversidad de hongos que habitan la madera caída y determinan la estructura de la comunidad fúngica (Lee et al., 2020; Yang et al., 2021). Entre esos factores destacan la precipitación, temperatura y tipo de vegetación, las características de los macromicetos como son la capacidad enzimática, especificidad de sustrato e interacciones ecológicas entre ellos y con otros organismos, así como las características fisicoquímicas del sustrato (Siitonen et al., 2000; Purahong et al., 2016; Dighton y White, 2017).
Sobre las características fisicoquímicas del sustrato es importante mencionar que hay un efecto bidireccional entre estas y los macromicetos. Es decir, al inicio de la descomposición estas características influencian el establecimiento, crecimiento, reproducción, metabolismo y diversidad de los hongos; a su vez, las actividades biológicas de los hongos provocan cambios en la estructura química y física de la madera caída (Schwarze et al., 2000; Song et al., 2012; Brabcová et al., 2022).
La cuantificación de las características físicas de la madera caída es de gran importancia ya que puede reflejar diferentes aspectos de la descomposición y explicar, en cierta medida, la presencia y abundancia de los macromicetos degradadores (Mäkinen et al., 2006). Una de esas características, la densidad, es una de las variables más relacionadas con la composición y estructura de la comunidad fúngica, así como con la riqueza, abundancia de esporomas y sucesión de macromicetos (Kubartová et al., 2015; Rajala et al., 2015; Arnstadt et al., 2016; Hoppe et al., 2016; Purahong et al., 2016; Yang et al., 2021).
También se ha reportado la relación de la densidad con la humedad de la madera y su incorporación a los esquemas de etapas de descomposición (Rajala et al., 2012; Shorohova et al., 2022), que anteriormente estaban más determinados por aspectos visuales como la dureza de la madera (p. ej., cantidad de centímetros que se entierra un cuchillo dentro de los troncos caídos). En cuanto a dichos esquemas, algunos autores (Renvall, 1995; Heilmann-Clausen y Christensen, 2003; Penttilä et al., 2004) reportan una mayor diversidad de macromicetos en etapas intermedias y otros en etapas finales de la descomposición de la madera.
Otra de las características físicas bien documentadas es el tamaño de los troncos caídos, pues se ha reportado que los de gran tamaño o CWD (Coarse Woody Debris) con diámetro mayor a 10 cm presentan una mayor riqueza fúngica (Sippola y Renvall, 1999; Krah et al., 2018), que las pequeñas ramas o FDW (Fine Woody Debris) con diámetros entre 5 y 9 cm. Sin embargo, se sabe que estas últimas son de gran importancia para la diversidad de ciertos grupos taxonómicos de hongos (Kruys et al., 1999; Nordén et al., 2004).
Por otro lado, el volumen de los troncos ha sido correlacionado con la riqueza y diversidad de los macromicetos, y se ha confirmado su influencia en la estructura de la comunidad (Pouska et al., 2011; Hoppe et al., 2016). Otras variables reportadas en participar tanto en la estructura como en la composición de la comunidad son el contenido de humedad, los microclimas alrededor y dentro de la madera, y el pH, que adicionalmente ha sido relacionado con la diversidad de los macromicetos y con la acidificación del microambiente que permite la acción de enzimas como las lacasas y peroxidasas (Kubartová et al., 2015; Müller et al., 2020; Yang et al., 2021; Li et al., 2022).
Considerando lo anterior, la presente contribución tiene como objetivo determinar qué características físicas y microambientales en torno a la madera de troncos caídos de Abies religiosa (Kunth) Schltdl. & Cham. en la localidad de Huixquilucan, Estado de México, México, podrían estar relacionándose entre sí y con la riqueza y abundancia de esporomas de los macromicetos degradadores. Estas relaciones no solo influyen en la comunidad fúngica, sino que ayudan a entender la importancia que tienen los hongos degradadores en estos ecosistemas y parte del funcionamiento de la degradación de la madera en los bosques de Abies religiosa (oyamel) que debido al cambio climático están en peligro de desaparecer (Argüelles-Moyao y Garibay-Orijel, 2018; Agüelles-Moyao et al., 2022).
Materiales y Métodos
Área de estudio
La zona de muestreo se localiza en el centro del Estado de México, en la localidad Las Peñas Barrón dentro del Parque Nacional Insurgente Miguel Hidalgo y Costilla, mejor conocido como La Marquesa (Fig. 1). Específicamente esta zona pertenece al municipio Huixquilucan (coordenadas 19°18'14''N y 99°21'55''O) con una altitud que va de 2900 a 3800 m (CONANP, 2019; Google Earth, 2022). En el Parque Nacional se presenta un clima de tipo C (b) (w2) (w) Semifrío, subhúmedo con verano fresco largo (García, 1988). La temperatura media anual se reporta entre 5 y 12 ºC, y la del mes más frío entre -3 y 18 ºC, mientras que la del mes más caliente por debajo de 22 °C; además, se registra una precipitación promedio de 1306.5 mm con máxima mensual de 914.1 mm (CONANP, 2019).
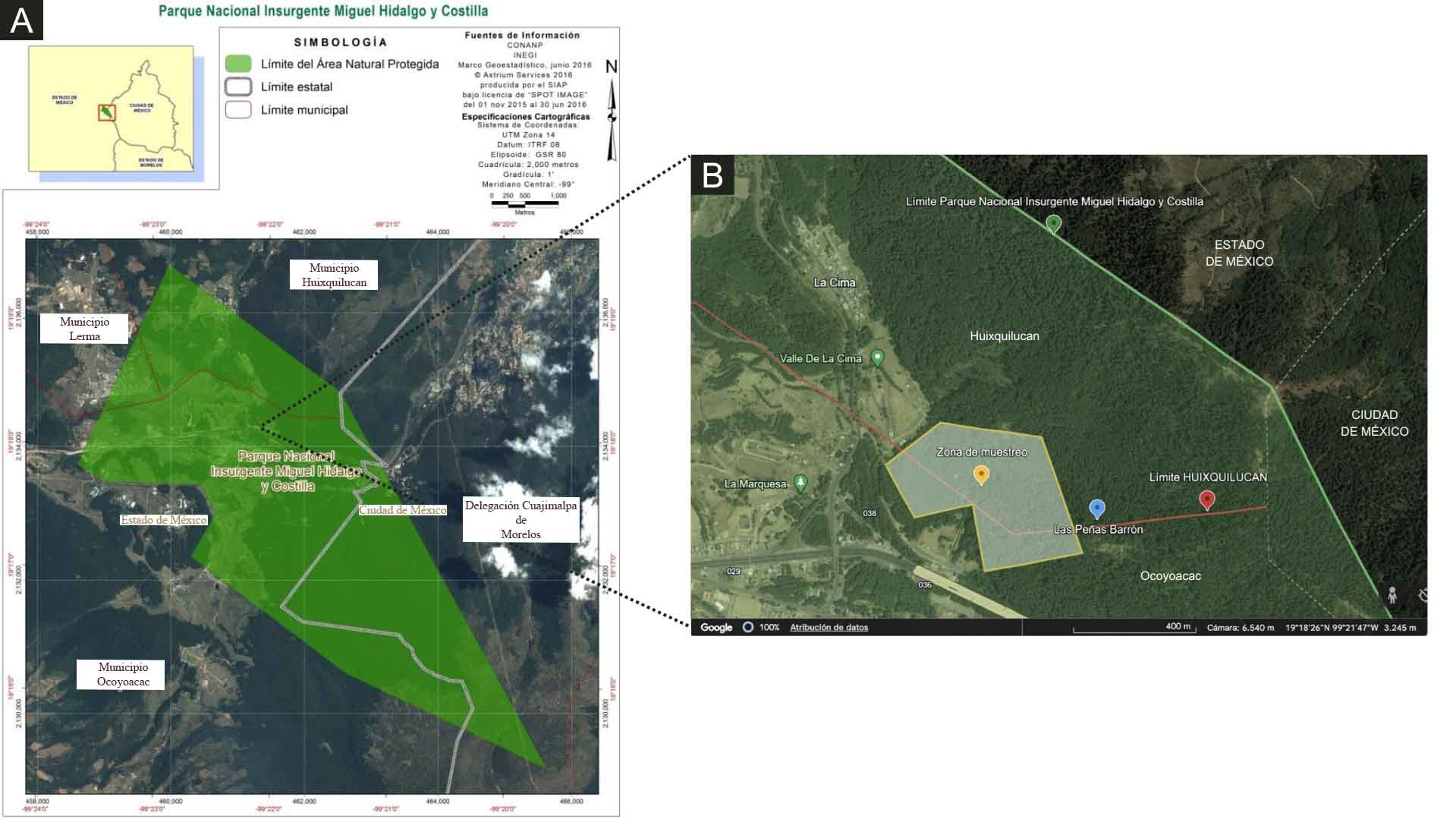
Figura 1: Área de estudio. A. mapa oficial del Parque Nacional Insurgente Miguel Hidalgo y Costilla (Modificado de CONANP, 2019); B. acercamiento a la zona de muestreo ubicada dentro del Parque Nacional Insurgente Miguel Hidalgo y Costilla, en la localidad Las Peñas Barrón, municipios Huixquilucan y Ocoyoacac, Estado de México, México. Elaborado en Google Earth v. 10.41.2.1 (Google Earth, 2023).
La vegetación del sitio estudiado está dominada por Abies religiosa, que se distribuye principalmente en cumbres y laderas de montañas, cañadas o barrancas hasta 3800 m s.n.m. y corresponde a un bosque monoespecífico. Más de 30 m es la altura promedio de los árboles que forman masas homogéneas y se distribuyen sobre suelos rocosos, profundos, bien drenados y ricos en materia orgánica (CONANP, 2019). El estrato arbustivo y herbáceo está bien desarrollado y su composición varía en función de la exposición a la luz solar, las condiciones de desarrollo del suelo y de humedad, y el grado de perturbación (CONANP, 2019).
Se realizaron cinco muestreos en septiembre y octubre de 2021 durante la temporada de lluvias. En cada salida al campo se hicieron recorridos donde se seleccionaron troncos caídos y tocones de Abies religiosa cuyo diámetro midiera 10 cm o más y su superficie presentara uno o más esporomas. Se estudió un total de 100 troncos.
Variables analizadas en la madera
Para la madera se evaluaron las siguientes variables físicas: pH, temperatura, dureza, humedad, densidad y volumen. De cada tronco, con cinta métrica de 50 m, se midieron largo y diámetro, y con estas medidas se estimó el volumen. El pH y la temperatura se obtuvieron insertando, dentro de cada tronco, la sonda de metal de un medidor digital (HSCo WEIGHING SOLUTIONS, Show Range SR3008, Mumbai, India). Como medida de dureza de la madera y siguiendo el método propuesto por Renvall (1995), se registraron los centímetros que se enterró un cuchillo de una hoja de aproximadamente 10 cm de largo, 2 cm de ancho y 2.5 mm de grosor, el cual se enterró, siempre por la misma persona tratando de aplicar la misma fuerza, una sola vez en el punto donde se encontraban la mayoría de los esporomas.
Con la finalidad de medir la humedad y la densidad, se tomó una muestra in situ de aproximadamente 200 g de peso fresco de madera, de cada uno de los 100 troncos estudiados. La muestra fue extraída de los sitios donde se encontró la mayor cantidad de esporomas, sin corteza y hasta una profundidad de 5 cm. Las muestras se trasladaron, en bolsas de plástico cerradas con ligas para evitar la pérdida de humedad, al Laboratorio de Hongos Tremeloides (Heterobasidiomycetes) de la Facultad de Ciencias, de la Universidad Nacional Autónoma de México (UNAM). Posteriormente fueron pesadas para la obtención del peso húmedo y secadas en un horno de secado (NOVATECH, HS35-ED, San Pedro Tlaquepaque, México) durante cinco días a 100 °C; enseguida se volvieron a pesar para obtener el peso seco. A continuación, las muestras se guardaron en bolsas de papel a temperatura ambiente en el Laboratorio de Hongos Tremeloides (Heterobasidiomycetes), para la posterior determinación de la humedad y densidad.
La humedad se determinó por el método propuesto por Núñez (2007), que consiste en la diferencia entre el peso húmedo y el seco, mediante la siguiente fórmula:
Donde:
∆P=Diferencia entre los pesos
PM=Peso de la madera saturada o peso máximo. En el caso de la determinación de la humedad es el peso húmedo de la madera en campo.
Pm=Peso seco o peso mínimo
La densidad básica o aparente de la madera fue determinada usando el método de Arquímedes descrito en Valencia Manzo y Hernández (1997), mediante la siguiente fórmula:
Db=Po/Vv (g/cm3)
Donde:
Db=Densidad básica
Po=Peso anhidro de la muestra o peso seco de la muestra
Vv=Volumen verde de la muestra o peso del agua desplazada por la muestra
Para determinar la densidad, las muestras se pesaron y después se colocaron en un recipiente con agua donde permanecieron de 12 a 20 días hasta su saturación. Posteriormente, utilizando una probeta de 1000 ml con agua a la mitad de su capacidad se introdujeron las muestras de madera sin que tocaran las paredes ni el fondo de dicho instrumento. Esto se logró atando a cada muestra un hilo delgado a su alrededor; así fue posible medir la cantidad de agua que desplazaba cada muestra (que corresponde al volumen de la muestra). La densidad se calculó dividiendo el peso de la muestra antes de saturarla de agua entre la cantidad de agua desplazada (volumen) (Valencia Manzo y Hernández, 1997).
Macromicetos y esporomas
Para determinar la abundancia y riqueza de esporomas de macromicetos presentes en los troncos, se contaron los esporomas por especie presente. Se tuvo en consideración el rango de hongos inhabituales (1 a 10 esporomas), escasos (11-100), abundantes (101-1000) y muy abundantes (más de 1000 esporomas). Se recolectaron los esporomas y se hizo un registro fotográfico de los taxones. Con esos datos se calculó riqueza, la abundancia absoluta (AA) por especie, la abundancia relativa de esporomas por especie (AR) y la frecuencia temporal (FT) y temporal relativo (FTR) de los macromicetos (Garibay-Orijel et al., 2009; Rodríguez-Gutiérrez et al., 2020).
Cabe señalar que el grupo funcional (tipo de pudrición u hongos ectomicorrízicos) se basó en lo publicado previamente por Valenzuela et al. (2004) y no se llevaron a cabo pruebas para su corroboración experimental. Esto aunado a que muchos hongos se determinaron únicamente hasta el nivel de género y por ende no se pudo establecer la asociación con su tipo de pudrición. De los ejemplares recolectados se hizo una descripción de características macroscópicas de los esporomas en fresco; posteriormente se colocaron en una secadora de aire caliente (ATVIO, modelo FH-05W, without city, China) para su deshidratación. A continuación, se guardaron en bolsas de papel para su posterior revisión.
Para determinar taxonómicamente los ejemplares recolectados, se revisaron macromorfológica y micromorfológicamente, y se consultaron claves taxonómicas especializadas (McNabb, 1973; Gilbertson, 1980; Sierra y Cifuentes, 2005; Shirouzu et al., 2009; Contreras-Pacheco et al., 2018). Los nombres y autores de las especies se actualizaron de acuerdo con Index Fungorum (2023). Todo el material se encuentra depositado en la colección de hongos del Tecnológico de Estudios Superiores de Huixquilucan, Estado de México, México.
Análisis estadístico
Para la madera se evaluaron las siguientes variables físicas: humedad, densidad, volumen, dureza, temperatura y pH. Para los macromicetos se evaluó la riqueza taxonómica (géneros) y la abundancia de esporomas. Para cada una de las muestras de madera (N=100) se obtuvo la abundancia relativa de sus esporomas, riqueza taxonómica (géneros) y diversidad a través del índice de Shannon. Posteriormente, se evaluó el posible efecto de las variables físicas (densidad, volumen y dureza) y microambientales (temperatura, humedad y pH) con las medidas de riqueza y diversidad utilizando un Análisis de Correspondencia Canónica (ACC). Todos los análisis estadísticos fueron realizados en el programa PAST v. 4 (Hammer et al., 2001) con un nivel de confianza al 95% (p<0.05).
Resultados
Macromicetos y esporomas
Se registró una riqueza de 150 taxones, agrupados en 46 géneros y 75 morfoespecies, determinando 27 a nivel de especie. Dentro de la comunidad hay cuatro grupos funcionales: macromicetos causantes de pudrición café (37%), pudrición blanca (43%), pudrición blanda y macromicetos micorrízicos (10% cada una) (Cuadro 1, Fig. 2). Se registró un total de 19,985 esporomas con un promedio de 200 por tronco. En septiembre se alcanzó un promedio de 124, mientras que para octubre fueron 222 por tronco.
Cuadro 1: Listado taxonómico de hongos degradadores de madera de Abies religiosa (Kunth) Schltdl. & Cham. en el Parque Nacional Insurgente Miguel Hidalgo y Costilla, Huixquilucan, Estado de México, México. *Registrados también por Valenzuela et al., 2004. Todo el material se encuentra depositado en la colección de hongos del Tecnológico de Estudios Superiores de Huixquilucan, Estado de México, México.
| Phylum | Orden | Familia | Taxones | Tipo de pudrición | Colector y núm. de identificador |
|---|---|---|---|---|---|
| Ascomycota | Helotiales | Lachnaceae | Lachnum bicolor (Bull.) P. Karst. | Blanda | Guzmán-Ramírez 2021-14 |
| Pezizales | Pezizaceae | Peziza sp. | Blanda | Guzmán-Ramírez 2021-27 | |
| Discomycete sp.1 | Blanda | Guzmán-Ramírez 2021-47 | |||
| Discomycete sp. 2 | Blanda | Guzmán-Ramírez 2021-56 | |||
| Pyronemataceae | Humaria sp. | Blanda | Guzmán-Ramírez 2021-15 | ||
| Scutellinia scutellata (L.) Lambotte | Blanda | Guzmán-Ramírez 2021-28 | |||
| Ascomyceto sp. 1 | Sin información | Guzmán-Ramírez 2021-48 | |||
| Basidiomycota | Agaricales | Agaricaceae | Agaricus sp. | Blanca | Guzmán-Ramírez 2021-13 |
| Agarical sp. 1 | Sin información | Guzmán-Ramírez 2021-50 | |||
| Agarical sp. 2 | Sin información | Guzmán-Ramírez 2021-66 | |||
| Coprinus sp. | Blanca | Guzmán-Ramírez 2021-29 | |||
| Crepidotaceae | Crepidotus sp. 1 | Blanca | Guzmán-Ramírez 2021-12 | ||
| Crepidotus sp. 2 | Blanca | Guzmán-Ramírez 2021-57 | |||
| Entolomataceae | Entoloma sp. | Ectomicorrízico | Guzmán-Ramírez 2021-65 | ||
| Inocybaceae | Inocybe sp. | Ectomicorrízico | Guzmán-Ramírez 2021-70 | ||
| Lycoperdaceae | Apioperdon pyriforme Schaeff. | Blanca | Guzmán-Ramírez 2021-01 | ||
| Mycenaceae | Mycena pura (Pers.) P. Kumm. | Blanca | Guzmán-Ramírez 2021-31 | ||
| Mycena sp. 1 | Blanca y café | Guzmán-Ramírez 2021-30 | |||
| Mycena sp. 2 | Blanca y café | Guzmán-Ramírez 2021-16 | |||
| Mycena sp. 3 | Blanca y café | Guzmán-Ramírez 2021-49 | |||
| Mycena sp. 4 | Blanca y café | Guzmán-Ramírez 2021-58 | |||
| Xeromphalina aff. campanella | Blanca | Guzmán-Ramírez 2021-02 | |||
| Psathyrellaceae | Homophron spadiceum (P. Kumm.) Örstadius & E. Larss. | Sin información | Guzmán-Ramírez 2021-10 | ||
| Strophariaceae | *Hypholoma sp. | Blanca | Guzmán-Ramírez 2021-11 | ||
| Pholiota sp. | Blanca | Guzmán-Ramírez 2021-17 | |||
| Incertae sedis | Calyptella sp. | Sin información | Guzmán-Ramírez 2021-51 | ||
| *Tricholomopsis rutilans (Schaeff.) Singer | Blanca | Guzmán-Ramírez 2021-32 | |||
| Auriculariales | Auriculariaceae | Exidia glandulosa (Bull.) Fr. | Blanca | Guzmán-Ramírez 2021-18 | |
| Incertae sedis | *Pseudohydnum sp. | Blanca | Guzmán-Ramírez 2021-19 | ||
| Boletales | Hygrophoropsidaceae | Hygrophoropsis aurantiaca (Wulfren) Maire | Café | Guzmán-Ramírez 2021-20 | |
| Cantharellales | Hydnaceae | Clavulina sp. 1 | Ectomicorrízico | Guzmán-Ramírez 2021-43 | |
| Clavulina sp. 2 | Ectomicorrízico | Guzmán-Ramírez 2021-64 | |||
| Dacrymycetales | Dacrymycetaceae | Calocera cornea (Batsch) Fr. | Café | Guzmán-Ramírez 2021-54 | |
| *Calocera macrospora Brasf. | Café | Guzmán-Ramírez 2021-55 | |||
| Calocera sp. | Café | Guzmán-Ramírez 2021-44 | |||
| Dacrymyces chrysospermum Berk. & M.A. Curtis | Café | Guzmán-Ramírez 2021-33 | |||
| Dacrymyces punctiformis Neuhoff | Café | Guzmán-Ramírez 2021-34 | |||
| Dacrymyces sp. 1 | Café | Guzmán-Ramírez 2021-35 | |||
| Dacrymyces sp. 2 | Café | Guzmán-Ramírez 2021-36 | |||
| Dacrymycetoide sp. | Café | Guzmán-Ramírez 2021-52 | |||
| Dacryopinax sp. 1 | Café | Guzmán-Ramírez 2021-67 | |||
| Dacryopinax sp. 2 | Café | Guzmán-Ramírez 2021-22 | |||
| Ditiola radicata (Alb. & Schwein.) Fr. | Café | Guzmán-Ramírez 2021-03 | |||
| Guepinopsis alpina (Tracy & Earle) Braasf. | Café | Guzmán-Ramírez 2021-04 | |||
| Heterotextus sp. | Café | Guzmán-Ramírez 2021-45 | |||
| Geastrales | Geastraceae | Sphaerobolus stellatus Tode | Blanca | Guzmán-Ramírez 2021-46 | |
| Gloeophyllales | Gloeophyllaceae | *Gloeophyllum abietinum (Bull.) P. Karst. | Café | Guzmán-Ramírez 2021-09 | |
| Veluticeps abietina (Pers.) Hjortstam &Tellería | Café | Guzmán-Ramírez 2021-22 | |||
| Gomphales | Gomphaceae | Phaeoclavulina sp. | Ectomicorrízico | Guzmán-Ramírez 2021-60 | |
| Hymenochaetales | Incertae sedis | Trichaptum abietinum (Pers. ex J.F. Gmel.) Ryvarden | Blanca | Guzmán-Ramírez 2021-21 | |
| Polyporales | Dacryobolaceae | Postia sp. | Café | Guzmán-Ramírez 2021-53 | |
| Fomitopsidaceae | Fomitopsis pinicola (Sw.) P. Karst. | Café | Guzmán-Ramírez 2021-71 | ||
| Irpicaceae | Vitreoporus dichrous (Fr.) Zmitr. | Blanca | Guzmán-Ramírez 2021-61 | ||
| Phanerochaetaceae | Phlebiopsis gigantae (Fr.) Júlich | Blanca | Guzmán-Ramírez 2021-05 | ||
| Polyporaceae | Cyanosporus caesius (Schrad.) McGinty | Café | Guzmán-Ramírez 2021-37 | ||
| Perenniporia sp. | Blanca | Guzmán-Ramírez 2021-68 | |||
| Trametes sp. | Blanca | Guzmán-Ramírez 2021-62 | |||
| Steccherinaceae | Steccherinum sp. | Blanca | Guzmán-Ramírez 2021-06 | ||
| Incertae sedis | *Climacocystis borealis (Fr.) Kotl. & Pozar | Blanca | Guzmán-Ramírez 2021-23 | ||
| Poliporoide sp. 1 | Sin información | Guzmán-Ramírez 2021-24 | |||
| Poliporoide sp. 2 | Sin información | Guzmán-Ramírez 2021-40 | |||
| Russulales | Bondarzewiaceae | *Heterobasidion abietinum Niemelä & Korhonen | Blanca | Guzmán-Ramírez 2021-72 | |
| Peniophoraceae | Asterostroma cervicolor (Berk. & M.A. Curtis) Massee | Blanca | Guzmán-Ramírez 2021-25 | ||
| Russulaceaae | Lactarius sp. | Ectomicorrízico | Guzmán-Ramírez 2021-75 | ||
| Stereaceae | Stereum sanguinolentum (Alb. & Schwein) Fr. | Blanca y café | Guzmán-Ramírez 2021-63 | ||
| Corticioide sp. | Sin información | Guzmán-Ramírez 2021-38 | |||
| Corticioide sp. 1 | Sin información | Guzmán-Ramírez 2021-42 | |||
| Corticioide sp. 2 | Sin información | Guzmán-Ramírez 2021-69 | |||
| Corticioide sp. 3 | Sin información | Guzmán-Ramírez 2021-39 | |||
| Corticioide sp. 4 | Sin información | Guzmán-Ramírez 2021-41 | |||
| Corticioide sp. 5 | Sin información | Guzmán-Ramírez 2021-74 | |||
| Corticioide sp. 6 | Sin información | Guzmán-Ramírez 2021-73 | |||
| Corticioide sp. 7 | Sin información | Guzmán-Ramírez 2021-07 | |||
| Corticioide sp. 8 | Sin información | Guzmán-Ramírez 2021-08 | |||
| Tremellales | Phragmoxenidiaceae | Phyllogloea herrerae S. Sierra & Cifuentes | Sin información | Guzmán-Ramírez 2021-26 |

Figura 2: Diversidad de macromicetos degradadores de madera de Abies religiosa (Kunth) Schltdl. & Cham. A. Calyptella sp.; B. Dacrymyces chrysospermus Berk. & M.A. Curtis; C. Heterotextus sp.; D. Trichaptum abietinum (Pers. ex J.F. Gmel.) Ryvarden; E. Fomitopsis pinicola (Sw.) P. Karst.; F. Apioperdon pyriforme Schaeff. Crédito de las fotos: Daniela Guzmán.
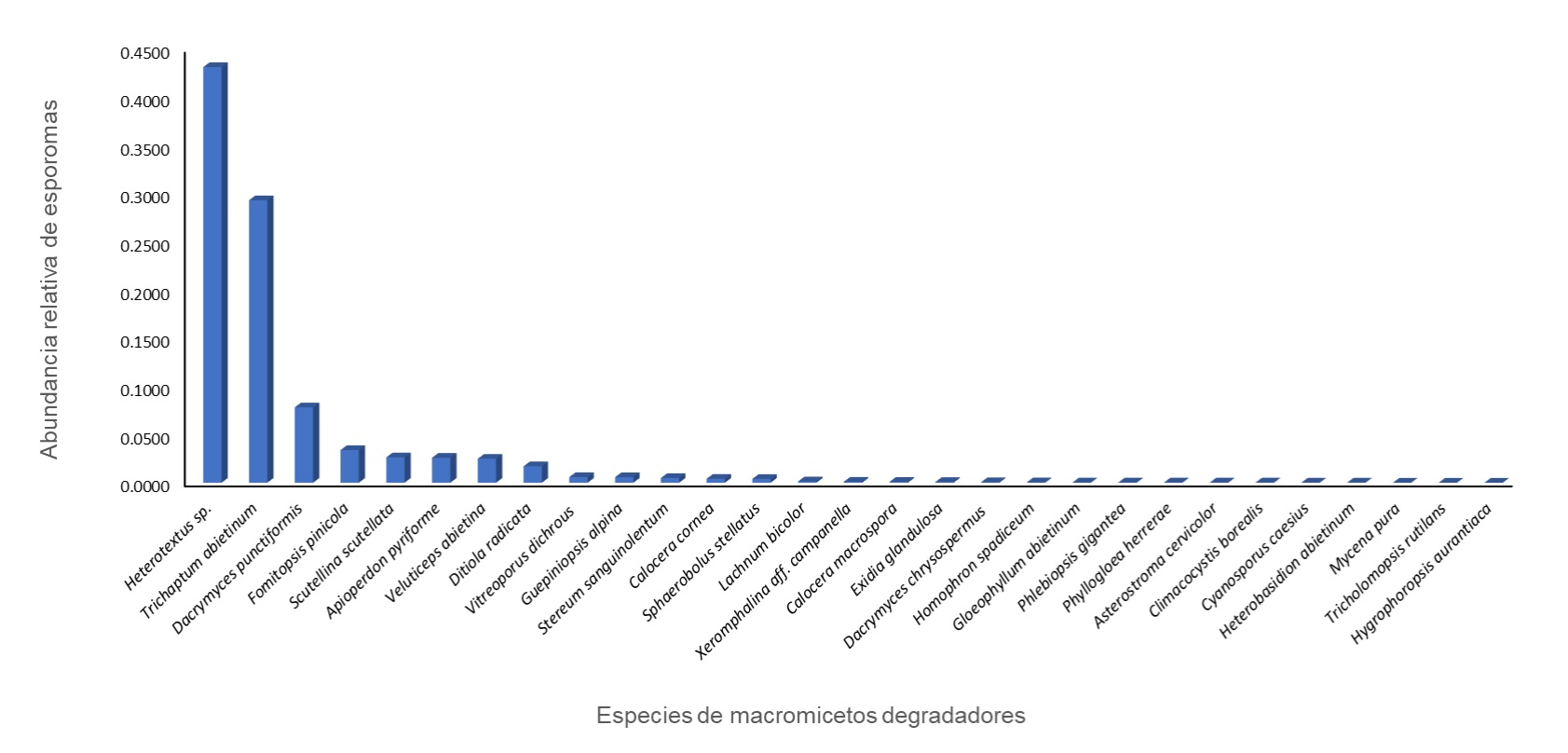
Los taxones más abundantes fueron Heterotextus sp., Trichaptum abietinum (Pers. ex J.F. Gmel.) Ryvarden y Dacrymyces punctiformis Neuhoff. En cuanto a la presencia de hongos por tronco, Fomitopsis pinicola (Sw.) P. Karst. se encuentra en 44 de 100 troncos, seguida de Trichaptum abietinum en 43, Dacrymyces punctiformis en 29 y Heterotextus sp. en 17 (Cuadro 2, Fig. 3).
Cuadro 2: Variables ecológicas en la producción de esporomas de hongos degradadores de madera de Abies religiosa (Kunth) Schltdl. & Cham. en el Parque Nacional Insurgente Miguel Hidalgo y Costilla, Huixquilucan, Estado de México, México. AA: Abundancia absoluta; AR: Abundancia relativa; FT: Frecuencia temporal; FTR: Frecuencia temporal relativa. *especies muy abundantes; **especies abundantes; ***especies escasas; **** especies raras.
| Especie | AA | AR | FT | FTR |
|---|---|---|---|---|
| *Heterotextus sp. | 8620 | 0.4313 | 0.6 | 0.17 |
| *Trichaptum abietinum (Pers. ex J.F. Gmel.) Ryvarden | 5858 | 0.2931 | 1 | 0.43 |
| *Dacrymyces punctiformis Neuhoff | 1563 | 0.0782 | 1 | 0.29 |
| **Fomitopsis pinicola (Sw.) P. Karst. | 677 | 0.0339 | 1 | 0.44 |
| **Scutellina scutellata (L.) Lambotte | 526 | 0.0263 | 1 | 0.31 |
| **Apioperdon pyriforme Schaeff. | 518 | 0.0259 | 0.2 | 0.03 |
| **Veluticeps abietina (Pers.) Hjortstam &Tellería | 497 | 0.0249 | 1 | 0.19 |
| **Ditiola radicata (Alb. & Schwein.) Fr. | 341 | 0.0171 | 1 | 0.16 |
| **Vitreoporus dichrous (Fr.) Zmitr. | 117 | 0.0059 | 0.2 | 0.02 |
| **Guepiniopsis alpina (Tracy & Earle) Braasf. | 114 | 0.0057 | 0.2 | 0.01 |
| ***Stereum sanguinolentum (Alb. & Schwein) Fr. | 97 | 0.0049 | 0.4 | 0.05 |
| ***Calocera cornea (Batsch) Fr. | 81 | 0.0041 | 0.2 | 0.03 |
| ***Sphaerobolus stellatus Tode | 79 | 0.0040 | 0.4 | 0.04 |
| ***Lachnum bicolor (Bull.) P. Karst. | 27 | 0.0014 | 0.4 | 0.02 |
| ***Xeromphalina aff. campanella | 20 | 0.0010 | 0.6 | 0.08 |
| ***Calocera macrospora Brasf. | 19 | 0.0010 | 0.2 | 0.01 |
| ***Exidia glandulosa (Bull.) Fr. | 15 | 0.0008 | 0.2 | 0.01 |
| ***Dacrymyces chrysospermus Berk. & M.A. Curtis | 11 | 0.0006 | 0.4 | 0.02 |
| ****Homophron spadiceum (P. Kumm.) Örstadius & E. Larss. | 8 | 0.0004 | 0.2 | 0.01 |
| ****Gloeophyllum abietinum (Bull.) P. Karst. | 6 | 0.0003 | 0.2 | 0.02 |
| ****Phlebiopsis gigantea (Fr.) Júlich | 6 | 0.0003 | 0.4 | 0.02 |
| ****Phyllogloea herrerae S. Sierra & Cifuentes | 6 | 0.0003 | 0.4 | 0.02 |
| ****Asterostroma cervicolor (Berk. & M.A. Curtis) Massee | 5 | 0.0003 | 0.4 | 0.04 |
| ****Climacocystis borealis (Fr.) Kotl. & Pozar | 5 | 0.0003 | 0.4 | 0.02 |
| ****Cyanosporus caesius (Schrad.) McGinty | 3 | 0.0002 | 0.4 | 0.02 |
| ****Heterobasidion abietinum Niemelä & Korhonen | 3 | 0.0002 | 0.4 | 0.02 |
| ****Mycena pura (Pers.) P. Kumm. | 1 | 0.0001 | 0.2 | 0.01 |
| ****Tricholomopsis rutilans (Schaeff.) Singer | 1 | 0.0001 | 0.2 | 0.01 |
| ****Hygrophoropsis aurantiaca (Wulfren) Maire | 1 | 0.0001 | 0.2 | 0.01 |
Variables analizadas en la madera
En cuanto a las variables físicas y microambientales de la madera caída se encontró que el valor promedio para el pH es de 6.8 (min=6, máx=7, DE=0.27), la temperatura de 11.67 °C (min=8 °C, máx=17 °C, DE=1.66 °C), humedad de 2.22 H2O g (min=0.09, máx=5.3, DE=1.31), densidad 0.3 g/cm3 (min=0.09, máx=0.94 , DE=0.14), dureza 2.98 cm (min=0.5, máx=22, DE=2.99) y volumen de 0.56 m3 (min=0.002, máx=7.39, DE=0.91).
Referente a la diversidad, se registraron troncos con valores de diversidad de Shannon mínimos de 0.13 y máximos de 1.72 (media=0.78, DE=0.47). Al evaluar la posible asociación entre las variables con la riqueza y diversidad se reporta que el modelo del ACC refleja que el eje 1 explica 99% de la varianza de los datos, donde la riqueza y diversidad de los esporomas está mayormente influenciada por la dureza, densidad y humedad de los restos de madera (Fig. 4).
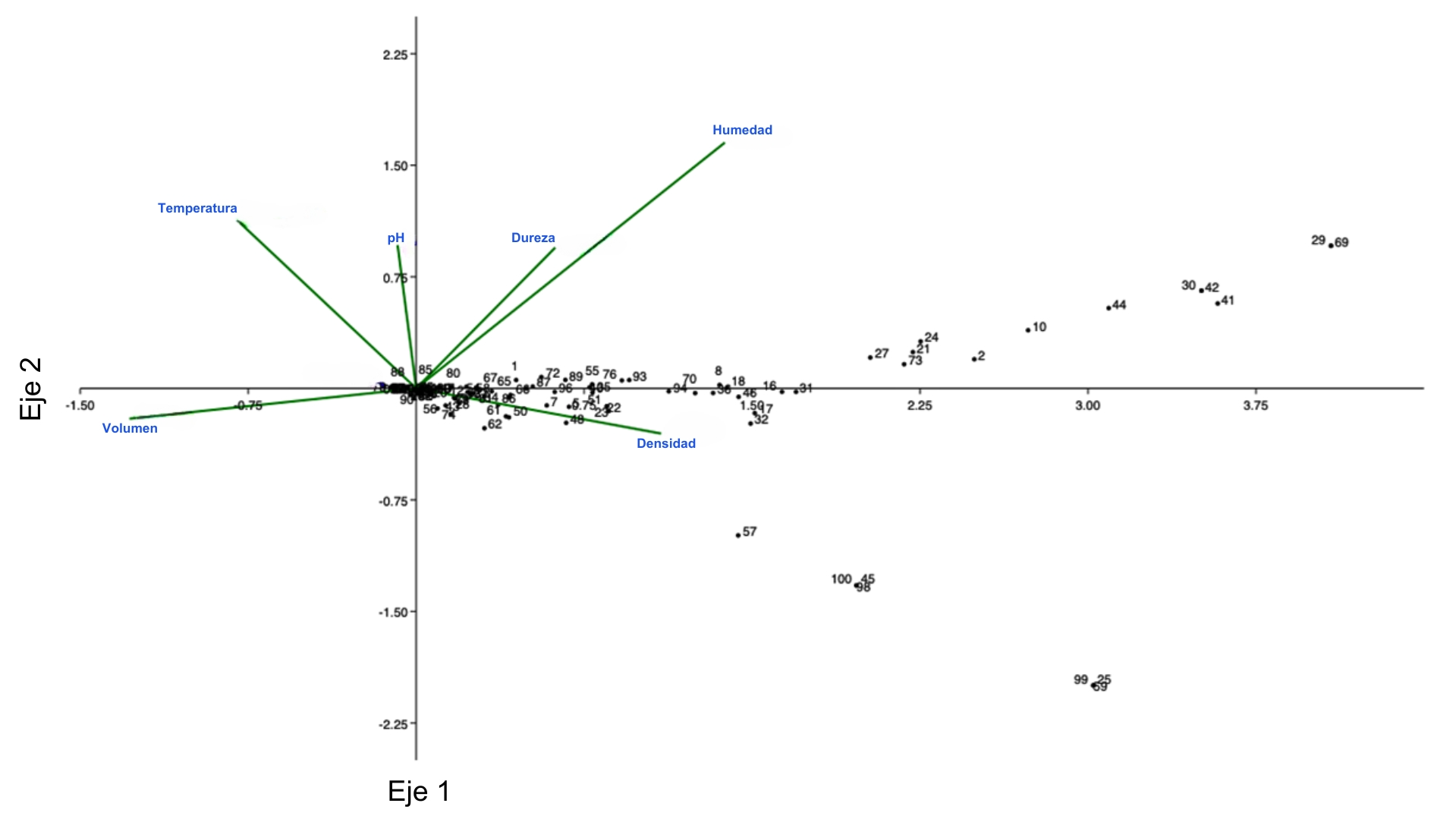
Figura 4: Análisis de Correspondencia Canónica (ACC) entre las variables físicas y microambientales con la riqueza y diversidad de especies de macromicetos en madera de Abies religiosa (Kunth) Schltdl. & Cham. en el Parque Nacional Insurgente Miguel Hidalgo y Costilla, Huixquilucan, Estado de México, México.
La mayoría de los datos de riqueza y diversidad se ubican en los cuadrantes inferior y superior derecho de la Figura 4 del ACC. En ella, la densidad, la humedad y la dureza son las variables que mejor explican el eje 1 y 2. En los cuadrantes mencionados se encontró una mayor densidad, mayor humedad y suavidad.
Discusión
El listado taxonómico que se obtuvo (Cuadro 1) representa una importante adición al conocimiento de los hongos para el municipio de Huixquilucan y para el Parque Nacional Insurgente Miguel Hidalgo y Costilla, ya que los trabajos sobre estos organismos en dichos lugares son muy escasos. El programa de manejo del parque, que fue presentado por la Comisión Nacional de Áreas Naturales Protegidas (CONANP) en 2019 (CONANP, 2019) contempla únicamente la flora y la fauna, y deja de lado a la micobiota. Sobre los hongos solamente se hace alusión a su recolecta como alimento y como parte de las áreas de bosque de pino, aun cuando estos organismos también están presentes en bosque de oyamel.
En el Parque Nacional Insurgente Miguel Hidalgo y Costilla, Valenzuela et al. (2004) reportaron 14 especies de macromicetos sobre Abies religiosa, de las cuales tres especies se registraron en el presente estudio (Tricholomopsis rutilans (Schaeff.) Singer, Climacocystis borealis (Fr.) Kotl. & Pozar y Calocera macrospora Brasf.) y cuatro géneros (Hypholoma (Fr.) P. Kumm., Gloeophyllum P. Karst., Heterobasidion Massee y Pseudohydnum P. Karst.). Por ello, se están añadiendo al menos 42 géneros y 24 especies de macromicetos al listado de hongos de este Parque Nacional. Lo anterior deja en claro que la diversidad fúngica en el lugar es muy alta (Fig. 2) y faltan zonas por explorar.
Los hongos causantes de la pudrición blanca fueron los mejor representados. Lo anterior se debe, quizá, a su alta capacidad enzimática para degradar la madera, a que muchos de ellos están reportados como colonizadores primarios y a que en casi todas las etapas de descomposición aparecen como un grupo dominante en comparación con otros hongos degradadores de la madera (Renvall, 1995; Kuhad et al., 2013; Fukasawa, 2021).
El microambiente que se genera dentro de la madera caída presenta grandes variaciones de temperatura y pH. Si bien no obtuvimos asociaciones significativas en cuanto a esas variables y los macromicetos, sí identificamos algunas tendencias. Por ejemplo, un ligero incremento de riqueza (hasta nueve géneros) y abundancia (hasta 4200 esporomas) cuando el pH es igual a 7, y mayor abundancia de esporomas cuando la temperatura es igual a 12 °C (hasta 4200 esporomas). Otros estudios (Müller et al., 2020; Li et al., 2022) sí reportan la influencia del microambiente en la comunidad fúngica, como la influencia del pH en la estructura de la comunidad y mayor actividad de enzimas fúngicas en pH bajos (3-5). También una adaptación de diferentes hongos a las distintas temperaturas que se presentan en lugares donde el dosel está abierto o en dosel cerrado y sombreado (Krah et al., 2018).
La riqueza y diversidad están influenciadas por la densidad, lo que refleja indirectamente el proceso de descomposición. En el presente trabajo en el ACC la variable densidad explica 99% de la varianza de los datos. Por lo general los troncos recién caídos son más densos y están poco descompuestos, por lo que contienen una baja humedad; por el contrario, los troncos menos densos y que están más descompuestos tienen mayores contenidos de humedad (Mäkinen et al., 2006). La relación entre densidad y humedad ya ha sido reportada en diferentes estudios (Christensen y Vesterdal, 2003; Fukasawa et al., 2009; Rajala et al., 2012; Shorohova et al., 2022) y se explica porque al avanzar el proceso de descomposición se crean espacios vacíos dentro de la madera y al ser ésta un material higroscópico, se almacena cada vez más agua en dichos espacios (Flournoy et al., 1991; Rawat et al., 1998; Karppanen et al., 2008). También se sabe que los cambios en el contenido de humedad pueden deberse a los cambios en la composición química y al agua que producen los hongos como resultado de la respiración fúngica (Thybring, 2017).
La dureza de la madera utilizando el método del cuchillo como un criterio para establecer etapas de la desintegración de la madera es una metodología que ha sido empleada por muchos años para los sistemas de clasificación de etapas de descomposición de la madera en estudios de plantas, animales y hongos que la habitan (Söderström, 1988; Renvall, 1995; Stokland, 2001; Heilmann-Clausen y Christensen, 2003; Pouska et al., 2011; Purahong et al., 2016). Sin embargo, se ha considerado como una variable cualitativa y susceptible a subjetividad humana, pues la suavidad de la madera no refleja por sí sola el proceso de descomposición (Grove et al., 2011). En nuestro estudio la mayor riqueza y diversidad de hongos se encuentra en aquellos troncos con menor dureza, lo cual corresponde a los troncos que presentan una menor densidad y alta humedad; por lo cual el método del cuchillo da un buen acercamiento de que en las etapas de mayor desintegración existen más cantidad de especies fúngicas.
Conclusiones
La madera caída de Abies religiosa alberga una alta diversidad de macromicetos degradadores. El proceso de descomposición de sus troncos y la riqueza y diversidad de esporomas está influenciado, principalmente, por la humedad, la dureza y la densidad de su madera. Con la presente contribución se registran por primera vez para el municipio de Huixquilucan 27 especies de las cuales 24 son nuevos registros de hongos descomponenores en A. religiosa para el Parque Nacional Insurgente Miguel Hidalgo y Costilla.











 nueva página del texto (beta)
nueva página del texto (beta)