Introducción
Es común que en la zona montañosa de México, las áreas protegidas de barlovento o con cañadas en altitudes elevadas, donde el vapor de agua atmosférico se condensa por efectos adiabáticos, se desarrolle el bosque de niebla, o bosque mesófilo de montaña (BMM sensuRzedowski, 1978). Por el simple hecho de que se estima que este tipo de vegetación en México ocupa 0.4% del territorio nacional como vegetación primaria (INEGI, 2009a), el BMM es reconocido como un sistema prioritario para la conservación y restauración, debido al papel vital que desempeña en servicios ambientales ligados al agua, la biodiversidad y otros bienes (Hamilton et al., 1995; Bruijnzeel, 2004; CONABIO, 2010).
Una de las zonas de ocupación más relevantes del BMM en México es la Sierra Norte del estado de Puebla, perteneciente a la región III sensuCONABIO (2010). Esta área forma parte de las Regiones Terrestres Prioritarias (RTPs) Sierra Gorda-Río Moctezuma y Bosques Mesófilos de la Sierra Madre Oriental (SMOr), así como del Área de Importancia para la Conservación de las Aves (AICA) Reserva de la Biosfera Sierra Gorda y Tlanchinol (CONABIO, 2010). Lo anterior se debe a que la Sierra Norte de Puebla está sujeta a un fuerte impacto antrópico donde el cambio de uso de suelo es extensivo y provoca que los mosaicos de vegetación remanentes estén especialmente predispuestos al cambio climático. Por ello, las oportunidades para la conservación de estos mosaicos forestales son en general bajas; el nivel de conocimiento biológico que se tiene de ella puede jugar un papel importante en el futuro de su conservación (CONABIO, 2010; Cruz-Elizalde et al., 2022).
Las masas forestales de la zona sur de la SMOr han recibido especial atención botánica en los estados de Hidalgo (Luna-Vega et al., 1994; Alcántara-Ayala y Luna-Vega, 1997, 2001; Escutia-Sánchez, 2004; Ponce-Vargas et al., 2006) y Veracruz (Luna-Vega et al., 1988; García-Franco et al., 2008; García-De la Cruz et al., 2013; Castillo-Hernández y Flores-Olvera, 2017; Vázquez-Torres, 2000), pero no así los de la región norte de Puebla (Ruiz Jiménez et al., 2012). Sin embargo, la magnificencia del BMM en Puebla ha atraído la atención de los pteridólogos, quienes han generado diversos trabajos en esta taxocenosis (Cerón-Carpio et al., 2006, 2012; Jano-Tolama y Andrés-Hernández, 2011; Mendoza-Ruiz y Ceja-Romero, 2020; Tzompa-Coatl et al., 2022). También han sido prolíficos los estudios relacionados con la flora útil como el de Martínez et al. (2007), en la zona de cafetales en la Sierra Norte de Puebla, México, quienes indican que un total de 319 especies son relevantes y, como el de Freire-Álvarez (2019), quienes, al evaluar los patrones de uso de un BMM y vegetación asociada en San Juan Tahitic (Zacapoaxtla), enlistan una riqueza de 293 especies.
Por lo anterior, el objetivo de este estudio es contribuir al conocimiento florístico del BMM por medio de la documentación de las plantas vasculares de un fragmento de bosque ubicado al oeste de la cabecera municipal Xicotepec de Juárez, Puebla. Se pretende, además, analizar aspectos del valor de conservación a partir de indicadores florísticos.
Materiales y Métodos
Área de estudio
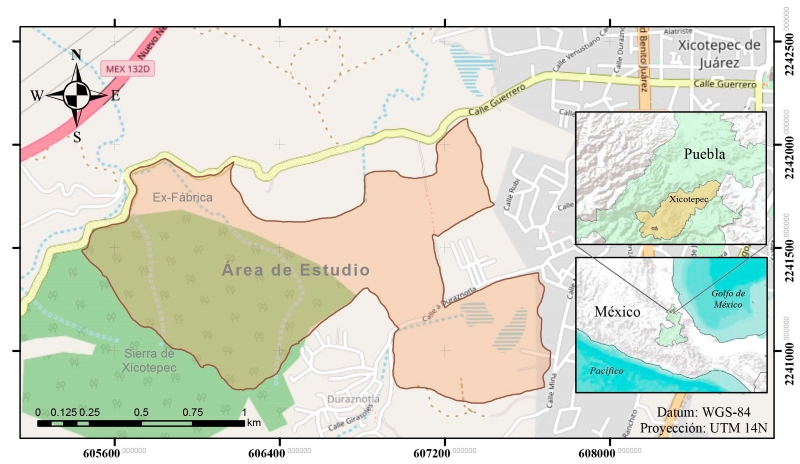
El área elegida para este estudio es un polígono irregular de 73 ha, ubicado al oeste del poblado Xicotepec de Juárez. Las coordenadas extremas son 20°16'12''N, 97°59'24''W (al noroeste) y 20°15'34''N, 97°57'36''W (al sureste). Se trata de la estribación oeste de la Sierra de Xicotepec, constituida por cerros y cárcavas derivadas de los escurrimientos de agua que forma el río Duraznotla, delimitada en el extremo este por la zona urbana y rural de poblado Xicotepec de Juárez, y sitios aledaños como la localidad de Ex-Fábrica al norte y la colonia Duraznotla al sur (Fig. 1). En este polígono se presenta un intervalo de altitud de 326 m, donde la más baja es de 1116 m s.n.m. en la zona periurbana de Xicotepec y la más alta 1442 m en la sierra de Xicotepec. Su acceso es por la carretera federal 130 Huauchinango-Poza Rica (SEDESOL, 2010).
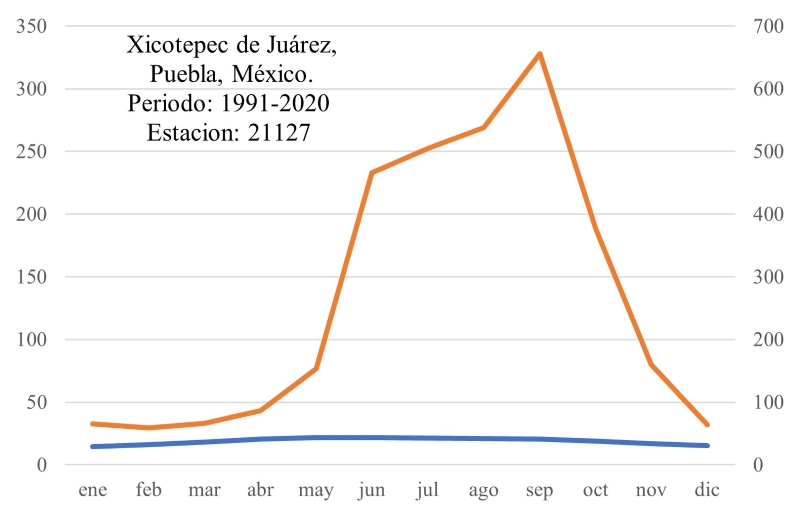
La zona de estudio forma parte de la subprovincia Carso-Huasteco, en el sur de la SMOr (CONABIO, 2010). El clima es semicálido, húmedo, con lluvias todo el año (CONANP, 2013). De acuerdo con la normal climatológica de Xicotepec de Juárez (CONAGUA, 2023), el agua de precipitación acumulada anual es de 3158 mm, sin tener déficit de humedad. Sin embargo, se observa una diferencia notable en la precipitación entre los meses verano (junio a octubre) y los de invierno-primavera (noviembre a mayo) (Fig. 2). La temperatura promedio anual es 18.4 °C, con los meses más calientes (arriba de 20 °C) entre abril y septiembre y los templados entre octubre y mayo, donde el más frío es enero con 13.1 °C. La fórmula climática de acuerdo con García (2004) es ((A)Ca(fm)(e)gw”). Los suelos presentes en las zonas bajas, al noroeste y sureste del área de estudio, son principalmente acrisoles (INEGI, 2010). Se localizan regosoles en pequeños enclaves de la zona de laderas, al suroeste, centro y noreste (INEGI, 2010). El área de trabajo cuenta con numerosos escurrimientos como arroyos y manantiales, p.ej. Duraznotla. Este sistema de aguas superficiales desemboca en el río Xochipila, el cual drena hacia el este y pasa a formar parte de los ríos San Marcos y Cazones consecutivamente (INEGI, 2009b). El polígono seleccionado como área de trabajo cuenta con una masa forestal mixta, compuesta por encinares y por BMM que se desarrollan en topoformas irregulares de tipo cerril y con laderas empinadas que corresponden a la cadena de montañas que enmarcan al poblado de Xicotepec de Juárez (INEGI, 2024). Esta masa forestal colinda a su vez con potreros, áreas urbanas y huertas de cultivo de plantas ornamentales perennes.
Trabajo de campo
La recolecta de ejemplares botánicos se hizo en el periodo de agosto de 2014 a abril de 2016. Mediante recorridos libres por diferentes veredas dentro de la zona de estudio y con especial atención para las zonas que mostraban diferencias en su fisonomía, se recogieron y prensaron plantas en floración de acuerdo con los métodos propuestos por Lot y Chiang (1986). Además, a partir de una gradilla de cuadrantes de 500 × 500 m, se hicieron listas (y recolectas) intensivas en el centro de cada cuadro. La eficiencia de recolecta se decidió subjetivamente, cuando la probabilidad de encontrar más especies distintas disminuyó, dado que los ejemplares observados y enlistados pertenecían reiterativamente a las especies previamente recolectadas. Este protocolo ad hoc suele ser más eficiente en el registro de flora que los muestreos estructurados, sistemáticos o al azar, dado que se visitan microambientes y sitios de difícil acceso que dejan mayores avistamientos de especies raras (Gordon y Newton, 2006; Jayakumar et al., 2009). Para cada espécimen, al ser recolectado, se anotaron los datos estándar recomendados en Palmer et al. (1995); el tipo de nutrición de acuerdo con Frías-Castro et al. (2013) (autótrofa, saprófita, hemiparásita y holoparásita); el hábitat donde crece y la forma de vida (FV). Esta última de acuerdo con la propuesta de Raunkiaer (1934), que considera la ausencia o posición de la yema meristemática de reacción al estrés ambiental con relación al substrato (terófito, hemicriptófito, criptófito, caméfito y fanerófito); se consideró las siguientes subcategorías de crecimiento en especímenes fanerófitos: cespitoso, escaposo y lianas.
Trabajo de gabinete
La determinación de los especímenes se realizó por medio del uso de claves dicotómicas de literatura especializada, principalmente Flora del Bajío y de regiones adyacentes y Flora de Veracruz, publicadas por el Instituto de Ecología A.C., así como la consulta de Mickel y Smith (2004) para los pteridobiontes. Los ejemplares nominados se cotejaron por comparación con los tipos en JSTOR Global Plants (JSTOR, 2024). El nombre aceptado y la forma de citar a los autores se copió directamente de POWO (2024) (entrada por el IPNI, 2024) y World Ferns (Hassler, 2024) para evitar errores de transcripción. Algunas familias fueron presentadas a especialistas para su verificación final (ver agradecimientos). Los ejemplares se depositaron en el Herbario Nacional de México (MEXU), de los cuales se otorgaron copias para donación a los herbarios de la Benemérita Universidad de Puebla (HUAP) y del Missouri Botanical Garden (MO) (acrónimos de los herbarios de acuerdo con Thiers, 2021).
Se construyó una base de datos en Microsoft Excel con la información recabada en campo y gabinete de las especies. Con este mismo programa se realizaron los análisis estadísticos mencionados en el siguiente párrafo. La lista de especies obtenida y sus cualidades ambientales y de protección se muestran en el apéndice, bajo un arreglo alfabético y circunscripciones taxonómicas de APG IV para angiospermas (APG, 2016); PPG (PPG I, 2016) para pteridobiontes y Christenhusz et al. (2011) para gimnospermas; todo este conjunto de grupos se subordina a la clase Embryopsida (sensuPirani y Prado, 2012).
Análisis de biodiversidad
Se comparó la riqueza florística con otros estudios similares usando el Índice de Biodiversidad Taxonómica (IB), definido como el número de especies dividido entre logaritmo natural del área:
donde S es el número de especies registradas y A el área en hectáreas del sitio de estudio (Squeo et al., 1998).
Por su significado como indicador ecológico, se calculó la proporción de plantas epífitas entre el cociente de plantas en este substrato (E) y el total de especies del polígono (S): Pe= E/S (Chávez-Esquivel, 2023). Esta proporción toma valores de 0 a 1, en donde entre más alto el valor, mayor proporción de epífitas existe en un sitio.
Conservación y endemismo
Para conocer las especies bajo algún instrumento de conservación y/o regulación de su comercio, el listado taxonómico obtenido se cotejó con la NOM-059-SEMARNAT-2010 y su actualización más reciente (SEMARNAT, 2010; 2019), la Lista Roja de la IUCN (IUCN, 2023) y los apéndices del CITES (CITES, 2023). La identificación de endemismos se realizó por medio de la consulta de las bases de datos del Catalogue of Life (Catalogue of Life, 2024)), Plants of the World Online (POWO, 2024) y Villaseñor (2016). Las especies exóticas se verificaron por medio del listado de Villaseñor y Espinosa-García (2004).
Resultados
Riqueza florística
En total se recolectaron 1476 ejemplares de plantas vasculares. Una vez determinados, se enlistaron 536 especies en 342 géneros y 127 familias (Fig. 3; Apéndice). Cabe destacar que a nivel de subclase (Embryopsida sensuPirani y Prado, 2012) (Cuadro 1), la riqueza se raciona de la siguiente forma: Lycopodiidae (15 spp.), Polypodiidae (117), Cycadidae (1), Pinidae (1), y Magnoliidae (402). Las 13 familias mejor representadas (con 10 o más especies) representan 49.81% del total y son: Asteraceae (41 spp., 7.64%), Orchidaceae (33, 6.15%), Fabaceae (29, 5.41%), Polypodiaceae (25, 4.66%), Rubiaceae (17, 3.17%), Solanaceae y Poaceae (16, 2.98% c/u), Thelypteridaceae (14, 2.6%), Bromeliaceae, Dryopteridaceae y Melastomataceae (13, 2.42% c/u), Malvaceae (12, 2.23%) y Lamiaceae (9, 1.67%). Por su parte, los 10 géneros más diversos (con cinco o más especies) son Tillandsia L. (10, 1.85%), Solanum L. (9, 1.67%), Pleopeltis Humb. & Bonpl. ex Willd. (8, 1.48%), Elaphoglossum Schott ex J. Sm. (7, 1.3% c/u), Amauropelta Kunze, Asplenium L., Begonia L., Diplazium Sw., Miconia Ruiz & Pav. y Piper L. (6, 1.15% c/u). Estos en conjunto albergan 11.89% del global de 342 géneros. El IB de la zona de estudio ostenta 124.92 (spp./ha).

Figura 3: Especies del bosque mesófilo de montaña de Xicotepec de Juárez, Puebla, México. A. Helosis cayennensis (Sw.) Spreng.; B. Columnea schiedeana Schltdl.; C. Disocactus phyllanthoides (DC.) Barthlott; D. Podocarpus matudae Lundell. Fotografías: J. D. Tejero-Díez.
Cuadro 1: Diversidad de familias, géneros y especies por clase, de plantas vasculares identificadas en un polígono aledaño a Xicotepec de Juárez, Puebla, México. Subclases subordinadas al concepto de Clase de Embryopsida (sensu Pirani y Prado, 2012).
| Clase | Familias | Géneros | Taxones |
| Lycopodiidae | 2 | 8 | 15 |
| Polypodiidae | 22 | 57 | 117 |
| Cycadidae | 1 | 1 | 1 |
| Pinidae | 1 | 1 | 1 |
| Magnoliidae | 101 | 275 | 402 |
Nutrición
Solo 1.49% (8 spp.) del total de especies identificadas en la zona de estudio pertenecen a plantas heterótrofas. De estas, las hemiparásitas son las más diversas, puesto que representan tres familias y cinco especies: Loranthaceae (Psittacanthus schiedeanus (Schltdl. & Cham.) G.Don y Struthanthus crassipes (Oliv.) Eichler), Orobanchaceae (Castilleja arvensis Schltdl. & Cham.) y Santalaceae (Phoradendron carneum Urb. y Phoradendron quadrangulare (Kunth) Griseb). Dos especies son saprófitas: Apteria aphylla (Nutt.) Barnhart ex Small (Burmanniaceae) y Voyria flavescens Griseb. (Gentianaceae). El holoparasitismo solo está representado por Helosis cayennensis var. mexicana (Liebm.) B.Hansen (Balanophoraceae). El resto de las especies (528, 98.51%) son autótrofas.
Hábitat
El substrato terrícola-humícola es el más importante al estar ocupado por 428 spp. (81.66%). El segundo en importancia es el corticícola (epífitas) con 99 spp. (18.4%). El resto de las plantas se encuentran en los siguientes substratos: paludícolas y acuícolas (13 spp., 2.41%), rupícolas (3 spp., 0.55%). La proporción de plantas epífitas (Pe) se estimó en 0.18.
Formas de vida
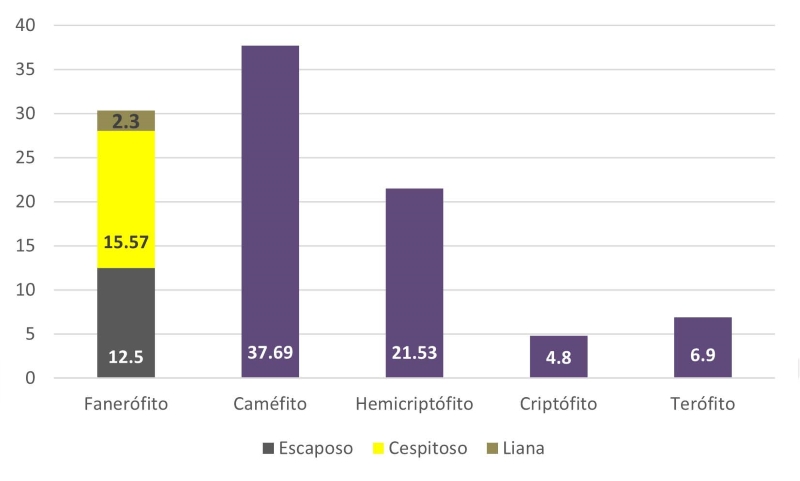
Todas las formas de vida se encuentran en la zona de estudio (Fig. 4). Las más importantes son los caméfitos (189 spp.) y hemicriptófitos (104 spp.), que en conjunto representan 54.46% de la riqueza florística encontrada. Por su parte el grupo de los fanerófitos representa 30.66%, de las cuales las escaposas albergan 81 especies, las lianas o bejucos 12 spp. y las cespitosas a 84 spp. Los terófitos (49 spp.) y criptófitos (38 spp.) están poco representados.
Instrumentos de conservación
Las especies que están incluidas bajo algún instrumento de protección son 177 (32.4%) (Apéndice). Con la actualización de la NOM-059-SEMARNAT-2010 (SEMARNAT, 2019) coinciden 16 taxones (2.97%), mientras que con la Lista Roja de la IUCN son 132 (24.53%) y con los apéndices del CITES 41 (7.62%). De las 67 familias con especies incluidas en estas regulaciones, seis son las que contienen cinco o más: Orchidaceae (33 spp.), Fabaceae (17), Asteraceae, Rubiaceae y Solanaceae (8 cada una), Malvaceae (6), las cuales representan 45.19% de este contingente de especies.
Distribución
Al menos 77 especies son endémicas al país, de las cuales seis son endémicas a la SMOr. Vale la pena señalar que 59 spp. son nuevos registros para el estado de Puebla. Por otra parte, 33 spp. son introducidas dentro del área de estudio (Apéndice).
Discusión
Riqueza florística
Las 536 especies de plantas registradas en el fragmento de BMM de Xicotepec representan 10.24% de las reportadas para el estado de Puebla (5232 spp.; Villaseñor (2016)). A su vez, representan 18.57% de la flora del bioma bosque húmedo de montaña de México (sensuVillaseñor y Ortiz, 2014) donde Rodríguez-Acosta et al. (2014) reportaron la presencia de 2886 especies en Puebla.
Las comparaciones florísticas mediante el índice de biodiversidad taxonómica (Squeo et al., 1998) otorgan una perspectiva de interés conservacionista, aunque para ello es un problema común la falta de exactitud en la dimensión del área de estudio, o bien, la delimitación de una formación vegetal debido a su complejidad y traslape con otros tipos de vegetación, como sucede con el BMM (Vargas-Rueda et al., 2021; López-Pérez et al., 2011). Si bien el número de especies obtenidas en este estudio solo es superado por los encontrados en Landa de Matamoros, Querétaro (Cartujano et al., 2002), el Cañón del Río Blanco, Veracruz (Vargas-Rueda et al., 2021) y Jilotepec, Veracruz (Vázquez-Torres et al., 2000), al aplicar la relación logarítmica con el tamaño del área de estudio, Xicotepec en realidad contiene la mayor riqueza de especies de muchas de las zonas estudiadas en la región de influencia (Cuadro 2). Por lo anterior, se puede confirmar que el BMM de Xicotepec es un relicto de enorme importancia en la conservación, ya que alberga 124.92 spp./ha en un espacio reducido de terreno que forma parte de la Región Terrestre Prioritaria de México 102 (CONABIO, 2004).
Cuadro 2: Comparativo de la riqueza de especies y el Índice de Biodiversidad Taxonómica (IB) (cuando el estudio lo permite) con otras localidades que presentan bosque mesófilo de montaña (BMM) en México. NR=No Reportada.
| Estudio | Área (ha) | Riqueza | IB (spp./ha) |
| Xicotepec, Puebla (este estudio) | 73 | 536 | 124.92 |
| Reserva del Bicentenario, Zongolica, Veracruz (Castillo-Hernández y Flores-Olvera, 2017) | 63 | 401 | 96.78 |
| Landa de Matamoros, Querétaro (Cartujano et al., 2002) | 5400 | 774 | 90.06 |
| Molote, Guerrero (Lozada et al., 2003) | 700 | 458 | 69.91 |
| Valle de Bravo, Estado de México (López-Pérez et al., 2011) | 1870 | 391 | 51.9 |
| Lolotla, Hidalgo (Ponce-Vargas et al., 2006) | 1022 | 359 | 51.8 |
| Sierra de Sultepec, Estado de México (Torres-Zúñiga y Tejero-Díez, 1998) | 20,000 | 507 | 51.19 |
| Miahuatlán, Oaxaca (Campos-Villanueva y Villaseñor, 1995) | 4300 | 353 | 42.19 |
| Teocelo, Veracruz (Luna-Vega et al., 1988) | 2100 | 277 | 36.21 |
| Omiltemi, Guerrero (Jiménez-Ramírez et al., 1993) | 3000 | 244 | 30.47 |
| Ocuilan, Morelos y Estado de México (Luna et al., 1989) | 1220 | 160 | 22.51 |
| PN Cañón del Río Blanco, Veracruz (Vargas-Rueda et al., 2021) | NR | 663 | NA |
| Jilotepec, Veracruz (Vázquez-Torres, 2000) | NR | 603 | NA |
| Tenango de Doria, Hidalgo (Alcántara-Ayala y Luna-Vega, 1997) | NR | 452 | NA |
| San Juan Tahitic, Puebla (Freire-Álvarez, 2019) | 0.6 | 219 | NA |
Evidentemente esta alta diversidad registrada en la zona de estudio se debe a que convergen factores físicos que provocan una variación horizontal y vertical de la cubierta vegetal, tal como la presencia de microambientes topográficos encontrados, a una altitud donde los vientos alisios se condensan dejando una elevada humedad atmosférica y la temperatura se muestra intermedio entre lo cálido y templado. Además, en esta riqueza de flora influye la entrada de especies sinantrópicas, debido a que el área muestreada limita con potreros y el poblado de Xicotepec. En las zonas conservadas, las familias características con mayor representatividad son Orchidaceae, Bromeliaceae, Fagaceae y Rubiaceae, junto con los pteridobiontes (como Polypodiaceae), típicas de sistemas templado húmedo de México, donde el componente de las epífitas es preponderante (CONABIO, 2010). Mientras que, en sitios de pastizal, acahual y bosque secundario, la flora sinantrópica presenta familias dominantes como Asteraceae, Poaceae, Fabaceae y Melastomataceae (Rzedowski, 1993; Colmenero-Robles et al., 2001; Bécquer-Granados, 2004).
Nutrición
En la localidad de estudio solo 1.48% de las plantas son heterótrofas. En general, estas plantas no superan el 3% en los ecosistemas (Nickrent, 2020), pero se vuelven un indicador de impacto cuando la dominancia de las especies parásitas y hemiparásitas afecta al rendimiento del hospedante y termina por provocar cambios en la comunidad vegetal (Press y Phoenix, 2005). Por lo pronto, la proporción de plantas heterotróficas aquí reportada es más o menos similar a otros bosques semejantes circunvecinos (López-Pérez et al., 2011; Castillo-Hernández y Flores-Olvera, 2017; Vargas-Rueda et al., 2021) y, de acuerdo con nuestras observaciones, ninguna de las especies destaca por presentar alta frecuencia-abundancia. Con ello, se puede asegurar que el impacto ambiental aun no afecta la parte profunda de la estructura del bosque. Sin embargo, es de interés conservacionista mantener vigiladas poblaciones de Psittacanthus schiedeanus y Phoradendron quadrangulare, dada su potencialidad como plaga, al ser las más abundantes de entre las parasitas en la zona de estudio.
Hábitat
Evidentemente y en ausencia de afloramientos rocosos o taludes en cuencas húmedas en la localidad, la preferencia del substrato de ocupación por parte de las plantas en la zona estudiada es la terrícola-humícola, substrato que al parecer es donde el BMM tiene su máxima expresión en México, debido a que el rocoso es de índole xerófilo (Cartujano et al., 2002; Ponce-Vargas et al., 2006; Castillo-Hernández y Flores-Olvera, 2017; Vargas-Rueda et al., 2021). En este substrato se establece 81.66% de las especies registradas.
Por otra parte, la ocupación vertical del espacio por parte de la flora epífita es altamente diversa, una característica propia del BMM (Rzedowski, 1978; CONABIO, 2010). En el polígono estudiado este contingente de plantas representa una proporción de 0.18, bastante superior al de otros BMM del país como Zongolica, Veracruz (Pe=0.12; Castillo-Hernández y Flores-Olvera, 2017); Lolotla, Hidalgo (Pe=0.09; Ponce-Vargas et al., 2006) y Tenango de Doria, Hidalgo (Pe=0.06; Alcántara-Ayala y Luna-Vega, 1997).
Esta relación entre epífitas y el total de plantas ayuda a explicar tanto la biodiversidad local derivado de las condiciones especiales de humedad que favorece la ocupación de este substrato (Zotz y Schutlz, 2008; Sanger y Kirkpatrick, 2017), como el tipo de forófitos amigables existentes (Dislich y Mantovani, 2016). Por ejemplo, en el BMM de Avándaro, Estado de México, López-Pérez et al. (2011) reportaron 22 spp. (5.6%), vs. 99 spp. (18.4%) en Xicopetec. Demuestra claramente cómo la diferencia de la humedad atmosférica juega un papel en la estructura de la diversidad propias del BMM, donde ciertas familias comunes (p.ej., familias como Bromeliaceae, Polypodiaceae, Piperaceae y Orchidaceae) tienen diferencias en su presencia taxonómica y de abundancia. El diagrama ombrotérmico de Avándaro muestra un déficit hídrico de los meses de noviembre a abril (López-Pérez et al., 2011). Este factor físico puede ayudar a explicar la diferencia en la diversidad de este grupo funcional, puesto que, en Xicotepec, no existe tal decremento anual. Lo anterior, aunado a la presencia de elementos de agua superficiales y la topografía accidentada, que generan zonas con humedad ambiental muy alta en Xicotepec, permite la presencia no solo de mayor diversidad de las familias antes mencionadas, sino también de taxones de grupos más dependientes de la humedad, como Cyatheaceae, Gesneriaceae y Hymenophyllaceae, ausentes en BMM más estacionales.
Formas de vida
Los espectros de FV como elementos de interpretación climo-dinámica y de impacto son muy aceptados en el mundo (Cain, 1950; Leuschner y Ellenberg, 2017; Di Biase et al, 2021). Sin embargo, en México existen muy pocos trabajos que los contemplen (Frías-Castro et al., 2013). Rzedowski (1978) indicó la universalidad de este instrumento de análisis de formaciones vegetales mexicanas vs. de otras partes en el mundo. En general, en México los hemicriptófitos están bien representados en el clima templado, pero deprimidos en clima cálido vs. lo contrario a fanerófitos arbóreos. Los terófitos lo están en las zonas áridas y ambientes secundarios y los caméfitos en la zona alpina y pastizales de diferente índole. Las desviaciones teóricas de un espectro permiten entonces una interpretación de impacto (Pausas y Austin, 2001; López-Pérez et al., 2011).
El espectro de FV del área de BMM de Xicotepec tiene parecido al de otros BMM (Fig. 5), donde la FV más abundantes son hemicriptófitos, fanerófitos y caméfitos (considerando a las plantas epífitas) (López-Pérez et al., 2011; Rzedowski, 1978). La presencia de hemicriptófitos y caméfitos (104 y 189 spp., respectivamente; equivalentes a hierbas perennes o subarbustos en general) no presentan abundancias altas en zonas donde el dosel se encuentra conservado. Sin embargo, como una de las propiedades de expresión de los bosques templados (Rzedowski, 1978), las hemicriptófitas son de mayor abundancia y riqueza florística en las porciones del norte y este del área de estudio, donde el estrato arbóreo no está consolidado por tener frontera con ambientes antrópicos como el pastoreo.
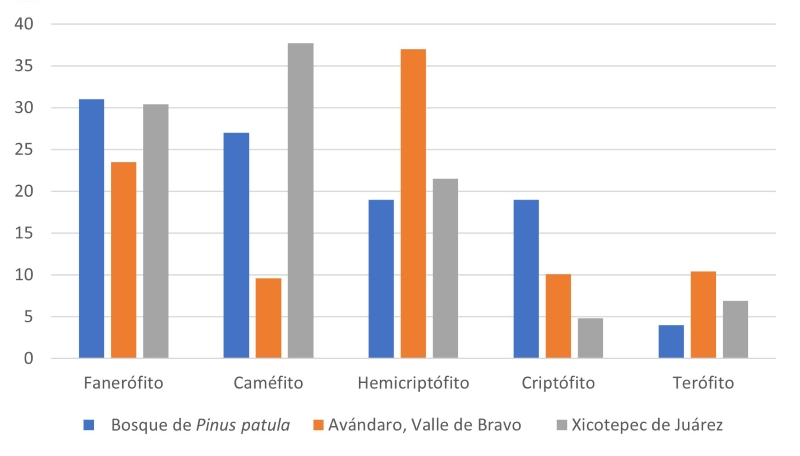
Figura 5: Espectro de formas de vida (en porcentaje) reportados en bosque de Pinus patula Schltdl. & Cham. (Rzedowski, 1978), Avándaro, Valle de Bravo (López-Pérez et al., 2011) y Xicotepec de Juárez (presente estudio).
Por lo tanto, la expresión en el espectro de formas de vida de Xicotepec se ve desviada de la normalidad para esta formación vegetal donde hemicriptófitos y fanerófitos escaposos deben predominar (al igual que caméfitos epífitos) (Mueller-Dombois y Ellenberg, 1974; Rzedowski, 1978; Vidal y Reif, 2011; Di Biase et al., 2021). Parte de la explicación de dicha desviación sucede por el impacto antrópico local, que ha sido históricamente importante. Así, un contingente de especies terófitos, hemicriptófitos (herbáceas de ciclo anual y algunas perennes) y caméfitos (subarbustos y algunas herbáceas no epifitas) sobrerrepresentadas están ligadas a zonas abiertas de potreros y veredas (Grime, 2006). Otra forma de vida abundante son los fanerófitos cespitosos (equivalente a arbustos), probablemente debido a la existencia de una extensa línea de borde de bosque, donde suelen dominar con apenas unas cuantas especies arbóreas juveniles de rápido crecimiento como Liquidambar L. y melastomatáceas como Miconia xalapensis (Bonpl.) M.Gómez.
Instrumentos de conservación
Se encontraron 177 especies (Apéndice) coincidentes con las enumeradas en listados de especies sensibles al impacto antrópico, de las cuales destacan: Ceratozamia mexicana Vovides, Avendaño, Pérez-Farr. & Gonz.-Astorga (Apéndice I CITES y Amenazada (A) en la NOM-059-SEMARNAT-2010); Quercus delgadoana S.Valencia, Nixon & L.M.Kelly y Urera martiniana V.W. Steinm. (Endangered (EN) en la Lista Roja de la IUCN) y Alsophila firma (Baker) D.S.Conant En peligro de extinción (P) según la NOM-059-SEMARNAT-2010 (SEMARNAT, 2019). Resulta paradójica la nominación de Nephrolepis cordifolia (L.) C.Presl, contemplada en la NOM-059-SEMARNAT-2010 (SEMARNAT, 2010) en un estado de peligro de extinción ya que es introducida (Tejero-Díez y Torres-Díaz, 2012) y, aunque en la zona de estudio no se comporta como invasora, en otras localidades como Huauchinango, Puebla se ha observado desplazando a la flora local (Tejero-Díez, obs. pers.).
Este conjunto de especies en protección suele ser superior al de otros lugares similares (Castillo-Hernández y Flores-Olvera, 2017; López-Pérez et al., 2011), a excepción del Parque Nacional Cañón del Río Blanco, donde 270 especies se encuentran en alguna categoría de los mismos instrumentos utilizados en este estudio (Vargas-Rueda et al., 2021). Si bien la nominación de especies en listas de prevención se puede considerar deficiente y controvertido, p.ej. el caso del párrafo anterior (Giraudo et al., 2011), son un claro indicador, junto con la consideración de las especies endémicas (siguiente párrafo), del valor biológico del área de estudio (Hobohm y Barker, 2023).
Distribución
De las 536 especies determinadas, 77 son endémicas al país, mientras que fisiográficamente seis especies se encuentran restringidas únicamente a la SMOr, sin haber sido reportadas para el estado de Puebla (Rodríguez-Acosta et al., 2014) (Apéndice). De estas destaca la familia Asteraceae con dos especies: Cirsium lappoides Sch. Bip y Verbesina olsenii B.L. Turner. Las demás familias cuentan con una especie solamente: Woodwardia martinezii Maxon ex Weath. (Blechnaceae), Quercus delgadoana (Fagaceae), Eugenia xilitlensis McVaugh (Myrtaceae) y Urera martiniana (Urticaceae).
Cabe destacar el hallazgo de 59 especies novedosas para el estado de Puebla (Apéndice; Rodríguez-Acosta et al., 2014; Villaseñor, 2016; ). Se reporta la familia Balanophoraceae con Helosis cayennensis (Sw.) Spreng., una planta parásita de raíz, previamente conocida para Veracruz e Hidalgo en la misma región fisiográfica del Carso Huasteco y otros estados (Martínez-Pérez y Acevedo-Rosas, 1995). De un modo similar destaca Voyria flavescens Griseb. Desde luego, este alto número de novedades es en parte debido a la ausencia de estudios florísticos locales.
Por otra parte, la presencia de vegetación inducida de importancia comercial como el café o plantas ornamentales, aunado a la cercanía con el poblado de Xicotepec, auspició el hallazgo de 33 especies exóticas. Si se toma en cuenta la zona de estudio en su extensión total, se puede considerar que este conjunto de especies tiene un efecto aditivo a la diversidad. Sin embargo, es cierto que las plantas invasoras se pueden encontrar de manera recurrente en zonas secundarias, donde el cambio en la estructura de la comunidad y la constante presión ejercida por la actividad humana favorecen su presencia, disminuyendo la diversidad en estos sitios (Vilà et al., 2011).
Este estudio reporta un gran número de especies para una localidad con BMM situada en la Sierra Norte de Puebla. Si bien es un resultado que se esperaba por la relación especial de spp./ha que presenta este tipo de bosque, las presiones antrópicas a las que está sujeto la llevan a considerarla como crítica para la conservación. La presencia de especies alóctonas y un espectro de FV que muestra elevado porcentaje de hábitos impropios a la estructura vegetal impoluta contrastan con la elevada riqueza de la flora, ausencia de plagas forestales, sistema florístico estructural original y un contingente de especies evaluadas como sobresalientes en la conservación. Estas últimas destacan la importancia de considerar la localidad de estudio como un sitio de reservorio de flora o Área Natural Protegida local o estatal, o hasta un parque urbano natural. Actualmente los terrenos están “protegidos” por ser de propiedad privada.
Contribución de autores
JDTD concibió, planeó y financió el proyecto además de vigilar la determinación de ejemplares y el escrito. ARS y JFE realizaron la determinación taxonómica de los ejemplares. ARS se encargó de la redacción del escrito y cartografía con la ayuda de JDTD y JFE. Todos los autores colaboraron en el trabajo de campo, en la revisión y aprobación del escrito final.











 nueva página del texto (beta)
nueva página del texto (beta)