Introducción
La familia Cactaceae es endémica de América con aproximadamente 2000 especies en todo el continente. Se distribuye del norte de Canadá hasta el sur de la Patagonia Argentina, y empezando a nivel del mar en dunas costeras con límite máximo a 5100 metros de altitud en Perú (Palacios, 2010), abarcando desde la isla Fernando de Noronha al este, incluso el archipiélago de Galápagos en el oeste (Barthlott y Hunt, 1993). Únicamente la especie epífita Rhipsalis baccifera (Sol.) Stearn ocurre en África tropical, Madagascar, islas del Océano Índico y Sri Lanka, y probablemente ha sido dispersada del Nuevo Mundo a estas áreas, por las aves y por el hombre (Anderson, 2001). Representantes de la familia se pueden encontrar en hábitats diversos, desde desiertos extremadamente secos e inclusive los bosques húmedos tropicales (Hoffmann y Walter, 2005). En consecuencia, la gran diversidad de hábitats ha dado lugar a una enorme variabilidad en formas y tamaños, permitiendo que los cactus sean hermosos, o al menos notables para aquellos que los observan (Anderson, 2001).
Cabe señalar que en el Perú la familia Cactaceae está representada por 40 géneros y 262 especies y subespecies de cactáceas (Ostolaza, 2019). Por su parte, Arakaki et al. (2006) han reconocido la existencia de 199 especies y subespecies, y seis géneros endémicos para el Perú. Las cactáceas peruanas están distribuidas en casi todos los ecosistemas, tanto en los desiertos costeros, vertiente occidental, puna y valles interandinos, como en el bosque tropical amazónico (Calderón Moya-Méndez et al., 2004). La mayoría de los taxones endémicos ocupan las regiones Matorral Desértico y Mesoandina, desde el nivel del mar hasta 4000 metros de altitud (Arakaki et al., 2006). No obstante, Brako y Zarucchi (1993) dieron a conocer que la familia Cactaceae está representada por 43 géneros y alrededor de 250 especies, principalmente con formas de crecimiento arbustivo-columnares.
De otra parte, la germinación de las semillas es un proceso multifactorial que también depende tanto de factores intrínsecos como ambientales (Taiz y Zeiger, 2010), siendo el agua, el oxígeno y la temperatura los factores más importantes (Bradford, 2002). El agua es necesaria para la hidratación de los tejidos, el oxígeno para facilitar la respiración aeróbica, y una temperatura adecuada, para iniciar los procesos fisiológicos (Milberg et al., 2000). En la germinación de semillas también participan las fitohormonas como la auxina bajo la forma de ácido indol acético y ácido giberélico (Bhatla y Lal, 2018).
Es pertinente indicar que la luz es una señal ambiental importante que puede afectar y controlar diferentes procesos fisiológicos en las plantas (Baskin y Baskin, 1998); entre ellos el tiempo de germinación de las semillas, así como el crecimiento y supervivencia de las plántulas (Pons, 2000). Los requerimientos de luz en la germinación de las semillas son variables entre especies, ya que pueden necesitar pocos segundos, largos períodos de iluminación continua o pulsos secuenciales intermitentes (Bewley et al., 2013). El dónde y cuándo germinar (control de la germinación) puede estar influenciado por la cantidad y calidad de la luz disponible, y por la capacidad de la semilla para percibirla (Fenner y Thompson, 2005).
Por otra parte, las plantas, en función de su respuesta a la luz para germinar, pueden clasificarse de la siguiente forma: las que requieren luz para germinar, las que requieren oscuridad para germinar y las que presentan un gran porcentaje de semillas neutras a la luz (Luna y Moreno, 2010; Bhatla y Lal, 2018; Baczek-Kwinta, 2022). Por ende, las semillas denominadas como fotoblásticas positivas son aquellas que no germinan en la oscuridad y constituyen el 70% de las especies vegetales, la germinación en fotoblásticas negativas es inhibida por la luz y representa el 25% de las especies, y el 5% restante de las especies es constituido por fotoblásticas neutras (Come, 1970; Baskin y Baskin, 2014). Particularmente las semillas fotoblásticas positivas requieren de una breve exposición a la luz roja para germinar (Bhatla y Lal, 2018). Por tanto, el fotoblastismo es modulado por un fotorreceptor denominado fitocromo. Las funciones que realiza el fitocromo en las semillas consisten en inducir la dormancia cuando las condiciones lumínicas son desfavorables para el establecimiento de las plantas. También está involucrado en la ruptura de la dormancia en semillas, aunque este último también está relacionado con la reversibilidad de la luz rojo/rojo lejano (Fenner y Thompson, 2005; Donohue et al., 2007; Azcón-Bieto y Talón, 2008)
Perú es considerado como uno de los principales centros de riqueza a nivel de géneros en cactáceas, pero existen pocos estudios realizados referente a la modulación de la luz en la germinación de semillas de cactáceas peruanas; la mayoría de los trabajos pioneros de fotoblastismo en cactáceas han sido realizados en México. Por ejemplo, Flores et al. (2006), cuando evaluaron el efecto de la luz en la germinación de semillas de 28 especies de cactáceas del Desierto Chihuahuense, determinaron que las semillas que tenían un peso menor a un miligramo respondieron como fotoblásticas positivas. Resultados similares dieron a conocer Loza-Cornejo et al. (2008), cuando investigaron la germinación de seis especies de cactus columnares (Pachycereeae), obteniendo una correlación positiva entre la masa de semillas y la velocidad de germinación. Además, Flores et al. (2011) investigaron 136 especies de cactus de diferentes países, concluyendo que la masa de semillas estaba relacionada con la dependencia de la luz y que las especies de cactáceas con semillas con un mayor peso son más indiferentes a la luz, en comparación con las especies que presentan masa menor. Sin embargo, Rojas-Aréchiga et al. (2013) indicaron que encontraron un resultado diferente, y no detectaron una relación entre la masa de semillas y la dependencia de la luz en 54 especies de cactus de la tribu Cacteae.
Por otra parte, Ortega-Baes et al. (2010), en estudios de la germinación de semillas de varias especies de cactáceas, comprobaron la existencia de un bajo porcentaje de germinación, o nula germinación en respuesta a la luz, demostrando que la baja germinación de las semillas se debía al estado de dormancia fisiológico de la semilla. Para lograr la germinación es necesario romper la quiescencia de las semillas (Rojas-Aréchiga y Vázquez-Yanes, 2000). Se considera la dormancia en la semilla como una adaptación para aumentar las probabilidades de germinación en un lugar seguro y en un tiempo adecuado, y poder tener éxito en el establecimiento de una plántula (Baskin y Baskin, 2014). También se ha comprobado que algunas especies de cactáceas para germinar requieren de un período de postmaduración de las semillas y poder romper la dormancia, como fue observado en Turbinicarpus lophophoroides (Werderm.) Buxb. & Backeb. y T. pseudopectinatus (Backeb.) Glass & R.A. Foster (Flores et al., 2008). Además, se considera que el fotoblastismo positivo tambien está asociado con la filogenia, y la respuesta de la germinación de semillas de cactáceas podría estar relacionado con las condiciones de su hábitat y microhábitat (Santini et al., 2017).
De otra parte, en Perú la conservación de los cactus está amenazada principalmente por la expansión de áreas agrícolas, actividades mineras, la construcción de carreteras, la expansión urbana y el aumento de la población, ocasionando la fragmentación y destrucción de los hábitats. El objetivo de este estudio fue evaluar la modulación que ejerce la luz en la germinación de semillas de cactáceas peruanas. En ese sentido, nuestra hipótesis fue que cuando las semillas de cactáceas son inducidas por la luz, la respuesta en la germinación está asociada también con la masa y el estado de dormancia de las semillas, así como con la condición particular de cada especie.
Materiales y Métodos
Colecta de frutos y procesamiento de semillas
En los departamentos Ancash, Apurímac, Arequipa y Huánuco, en Perú (Cuadro 1), se colectaron frutos de las siguientes especies de cactáceas: Austrocylindropuntia floccosa (Salm-Dyck) F. Ritter, Armatocereus mataranus subsp. ancashensis (F. Ritter) Ostolaza, Browningia candelaris (Meyen) Britton & Rose, Corryocactus aureus (Meyen) Hutchison, Corryocactus brevistylus Britton & Rose, Cumulopuntia ignescens (Vaupel) F. Ritter, Espostoa lanata subsp. ruficeps (F. Ritter) G.J. Charles, Haageocereus platinospinus (Werderm. & Backeb.) Backeb., Lobivia maximiliana subsp. westii (Hutchison) Rausch ex G.D. Rowley, Opuntia macbridei Britton & Rose, Trichocereus cuzcoensis Britton & Rose, Trichocereus. santaensis Rauh & Backeb., Tunilla soehrensii (Britton & Rose) D.R. Hunt & Iliff y Weberbauerocereus weberbaueri (K. Schum. ex Vaupel) Backeb. (Fig. 1).
Cuadro 1: Formas de crecimiento, procedencia, masa de semillas (g) y tiempo promedio de germinación (días) de 14 especies y subespecies de cactáceas procedentes de cuatro departamentos del Perú. Masa de semillas (n=40) y tiempo promedio de germinación (n=5) representan la media ± desviación estándar. Promedios con letras iguales en las columnas (*) son estadísticamente similares (p<0.05), por la prueba de comparación de medias de Tukey (α=0.05).
| Tribu | Especies | Formas de crecimiento | Procedencia | Masa de semillas (g) | Tiempo promedio de germinación (días) |
|---|---|---|---|---|---|
| Browningieae | Armatocereus mataranus subsp. ancashensis (F. Ritter) Ostolaza | arborescente | Ancash | 0.2±0.00e | 20.8±0.45a |
| Browningieae | Browningia candelaris (Meyen) Britton & Rose | arborescente | Arequipa | 0.0±0.00g | 11.2±1.79bc |
| Notocacteae | Corryocactus aureus Hutchison | arbustivo | Arequipa | 0.03±0.0009ij | 10.2±1.92e |
| Notocacteae | Corryocactus brevistylus (K. Schum. ex Vaupel) Britton & Rose subsp. brevistylus | arbustivo | Arequipa | 0.03±0.001j | 11.2±1.79bcde |
| Opuntioideae | Austrocylindropuntia floccosa (Salm-Dyck) F. Ritter | cespitoso | Apurímac | 1.53±0.0001a | 13.2±2.12b |
| Opuntioideae | Cumulopuntia ignescens (Vaupel) F. Ritter | cojín denso | Arequipa | 0.5±0.00c | 15.2±0.45cde |
| Opuntioideae | Opuntia macbridei Britton & Rose | arbustivo | Huánuco | 0.62±0.00b | 15.6±0.55de |
| Opuntioideae | Tunilla soehrensii (Britton & Rose) D.R. Hunt & Iliff | postrado | Arequipa | 0.42±0.00d | 10.2±0.84e |
| Trichocereeae | Espostoa lanata subsp. ruficeps (F. Ritter) G.J. Charles | arbustivo | Ancash | 0.01±0.00k | 11.8±1.64cde |
| Trichocereeae | Haageocereus platinospinus (Werderm. & Backeb.) Backeb. | postrado | Arequipa | 0.02±0.0008j | 12.2±1.10de |
| Trichocereeae | Lobivia maximiliana subsp. westii (Hutchison) Rausch ex G.D. Rowley | globosa | Apurímac | 0.03±0.00hi | 13.4±0.89de |
| Trichocereeae | Trichocereus cuzcoensis Britton & Rose | arborescente | Arequipa | 0.04±0.00hi | 11.2±1.30de |
| Trichocereeae | Trichocereus santaensis Rauh & Backeb. | arbustivo | Ancash | 0.15±0.00f | 12.4±1.95e |
| Trichocereeae | Weberbauerocereus weberbaueri (K. Schum. ex Vaupés) Backeb. | arbustivo | Arequipa | 0.03±0.0001k | 10.0±0.71e(*) |

Figura 1: A. Armatocereus mataranus subsp. ancashensis (F. Ritter) Ostolaza; B. Browningia candelaris (Meyen) Britton & Rose; C. Corryocactus aureus Meyen; D. Corryocactus brevistylus Britton & Rose; E. Austrocylindropuntia floccosa (Salm-Dyck) F. Ritter; F. Cumulopuntia ignescens (Vaupel) F. Ritter; G. Opuntia macbridei Britton & Rose; H. Tunilla soehrensii (Britton & Rose) D.R. Hunt & Iliff; I. Espostoa lanata subsp. ruficeps (F. Ritter) G.J. Charles; J. Haageocereus platinospinus (Werderm. & Backeb.) Backeb.; K. Lobivia maximiliana subsp. westii (Hutchison) Rausch ex G.D. Rowley; L. Trichocereus cuzcoensis Britton & Rose; M. Trichocereus santaensis Rauh & Backeb.; N. Weberbauerocereus weberbaueri (K. Schum. ex Vaupel) Backeb., procedentes de Perú en los departamentos Ancash, Apurímac, Arequipa y Huánuco.
Además, en los lugares de colecta se obtuvieron muestras de plantas, de preferencia en estado reproductivo, y se fotografiaron con una cámara digital Canon modelo EOS R10 18-150 IS STM (Canon Inc., Tokio, Japón). La identificación taxonómica de los especímenes se realizó con la ayuda de una especialista en la familia Cactaceae del Herbario Sur Peruano (HSP), Arequipa, Perú. La confirmación de la identidad y las autorías de las especies fueron verificadas en la base de datos de International Plant Names Index (IPNI, 2023).
De cada especie fueron colectados 10 frutos maduros de diferentes individuos. La extracción, limpieza y secado de las semillas se realizó de acuerdo con los procedimientos indicados por Arredondo (2002) y Reyes (2013). El contenido de humedad de las semillas de cada especie fue reducido utilizando un desecador con silicagel Isolab (Berlín, Alemania), hasta lograr obtener una humedad estable de 15%. Finalmente, las semillas fueron almacenadas en bolsas trilaminadas hasta el inicio de los experimentos.
Masa de semillas
Previamente las semillas fueron limpiadas y separadas libre de daños físicos; la viabilidad de las semillas fue determinada con base en su densidad por la prueba líquida con inmersión de semillas en agua destilada, y por la prueba de tetrazolio de la actividad enzimática (Camacho Morfín, 2011). Las semillas se pesaron en una balanza analítica (A&D-HR-250AZ, Seúl, Corea del Sur). Por cada una de las 14 especies, se pesaron 50 semillas con cinco repeticiones.
Tiempo promedio de germinación
El tiempo promedio de germinación es el tiempo que necesitan las semillas para germinar (González-Zertuche y Orozco-Segovia, 1996). Esta variable se calculó utilizando la ecuación:
Donde: T=tiempo promedio de germinación, ti=número de días después de la siembra, ni=número de semillas germinadas el día i.
Germinación de semillas en condiciones controladas
Es necesario precisar que antes de instalar el experimento se realizaron ensayos preliminares de germinación de las 14 especies de cactus en condiciones de iluminación y oscuridad. Del total de especies, Armatocereus mataranus subsp. ancashensis, Austrocylindropuntia floccosa, Cumulopuntia ignescens, Opuntia macbridei y Tunilla soehrensii obtuvieron un bajo porcentaje de germinación. Luego, en un segundo ensayo preliminar, las semillas de estas cinco especies recibieron un pretratamiento de escarificación física mediante un lijado de la testa de las semillas, lo que permitió una ligera mejora en la germinación. En tal sentido, solamente las semillas de las cinco especies de cactus con dormancia física recibieron un pretratamiento. Este consistió en una escarificación física de lijado de la testa de la semilla utilizando una lija de textura fina (ASALITE No. 180, Lima, Perú) para facilitar la imbibición de las semillas (Baskin y Baskin, 1998).
El experimento se realizó en condiciones de laboratorio mediante un diseño experimental aleatorizado. La germinación de semillas de las 14 especies de cactáceas fue evaluada en dos condiciones de luz (con iluminación y en oscuridad). La unidad experimental fue una placa de Petri con medio sólido de agar bacteriológico al 1% y semillas. A cada placa Petri se le agregaron 25 semillas con cinco repeticiones por cada tratamiento y especie.
La incubación de las semillas se realizó utilizando una cámara de crecimiento (Vision modelo VS-3DM, Seúl, Corea del Sur) programada por 30 días, a una temperatura mínima de 18 °C y máxima de 25 °C. La temperatura y fotoperiodo fueron programados de acuerdo con las recomendaciones de Nobel (1988) y Gurvich et al. (2008), que indican que 25 °C es la temperatura más adecuada para la germinación de semillas de agaves y cactus, con un fotoperíodo de 12 horas luz y 12 horas de oscuridad permanente. Las unidades experimentales del tratamiento de oscuridad consistieron en que las placas de Petri con las semillas de las 14 especies de cactus fueron cubiertas con doble capa de papel de aluminio. Su evaluación fue realizada en una cámara con luz verde (EFEC-002, Lima, Perú).
La germinación fue registrada diariamente por cada tratamiento y especie. Se consideró una semilla como germinada cuando la emergencia de la radícula alcanzó 2 mm de longitud (ISTA, 1996). El éxito de la germinación fue medido como porcentaje de semillas germinadas (G) durante el periodo de evaluación (Ranal y Santana, 2006). La germinación se expresó como el número de semillas germinadas (g) en relación con el número total de semillas por repetición (n=25), que fue calculada mediante la ecuación:
Cálculo del índice de germinación relativa a la luz (GRL)
Este cálculo da a conocer los requerimientos de luz para la germinación de semillas (Milberg et al., 2000). Esta variable se calculó mediante la siguiente ecuación:
En donde, GL=% germinación de tratamientos con iluminación y GO=% germinación en oscuridad permanente. Este índice fue calculado solo para aquellas especies que obtuvieron un porcentaje de germinación igual o mayor a 50%. El GRL representa un rango de valores que van desde 0 (germinación solo en oscuridad) a 1 (germinación solo en luz). Las especies con valores de GRL superior a 0.75 se consideran como fotoblásticas positivas, mientras valores de GRL menor a 0.25 se consideran fotoblásticas negativas. Las especies con valores de GRL entre 0.25 y 0.75 se clasificaron como indiferentes a la luz (Milberg et al., 2000).
Análisis estadístico
El análisis estadístico se realizó de acuerdo con el diseño experimental. Previamente todos los datos se transformaron en arco seno (Zar, 1999), luego se procedió con el análisis varianza (ANOVA) de una sola vía con un nivel de significancia p<0.05. Cuando las variables obtuvieron diferencias significativas, se realizó la prueba de comparación múltiple de medias de Tukey (α=0.05). La estimación de la correlación entre germinación de semillas y masa de semillas, tiempo promedio de germinación y masa, e índice relativo de germinación a la luz con masa se calculó mediante correlación de Pearson, con una probabilidad de p<0.001. Los cálculos fueron efectuados con el programa estadístico Infostat v. 2008 (Balzarini et al., 2011; Di Rienzo et al., 2015).
Resultados
Masa de semillas
Al realizar el cálculo de la desviación estándar y el análisis de comparación múltiple de medias por el método de Tukey, Austrocylindropuntia floccosa obtuvo el mayor valor de masa de semillas de las 14 especies evaluadas, con una masa de 1.53±0.0001 gramos (Cuadro 1). El menor valor de masa de semillas fue registrado en Espostoa lanata subsp. ruficeps, obteniendo el valor de 0.01±0.00 gramos (Cuadro 1).
Hay una correlación negativa de germinación de semillas con la masa de semillas (r=-0.505, p≤0.001; Fig. 2A). Se observa que se obtuvo un mayor porcentaje de germinación en semillas de cactus con menor masa, que fueron inducidas con un tratamiento de iluminación.
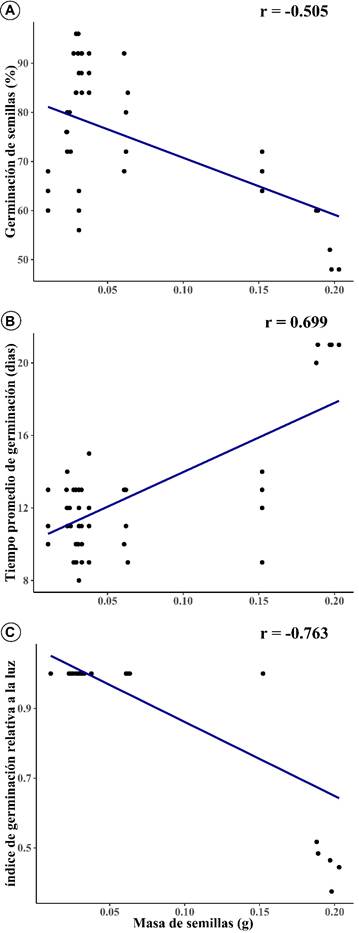
Figura 2: A. correlación de Pearson de masa de semillas (g) y germinación de semillas; B. masa de semillas y tiempo promedio de germinación de semillas (días); C. masa de semillas con índice de germinación relativa a la luz, con valores significativo a una probabilidad de p<0.0001.
De otra parte, el análisis de correlación mostró una asociación positiva significativa del tiempo promedio de germinación con masa de semillas (r=0.699, p≤0.001; Fig. 2B). Las semillas de cactáceas que presentan un menor peso germinan en menor tiempo, en comparación con las semillas de cactus con mayor peso, que requieren de un mayor tiempo para lograr la germinación. Hay una asociación negativa significativa del índice de germinación relativa a la luz con masa de semillas (r = -0.763, p≤0.001; Fig. 2C). Las semillas de cactáceas con menor masa consiguen valores de índice de germinación relativa a la luz (IGL) muy cercanas a 1. En cambio, los valores de IGL de las semillas de cactus de mayor masa se alejan de 1.
Tiempo promedio de germinación
Al realizar el cálculo de desviación estándar y el análisis de comparación múltiple de medias por el método de Tukey (α=0.05), Armatocereus mataranus subsp. ancashensis requirió de un tiempo de 20.80±0.45 días (Cuadro 1), para lograr la germinación de más de 50% de semillas. A partir de los 20.80±0.45 días transcurridos ya no se observaron más semillas germinadas en las unidades experimentales. El menor tiempo promedio de germinación fue registrado en la germinación de semillas de Weberbauerocereus weberbaueri, logrando germinar a los 10.00±0.71 días (Cuadro 1), luego de haber iniciado el experimento.
Germinación de semillas
De las 14 especies estudiadas, el análisis de comparación múltiple de medias por Tukey (α=0.05) mostró que las semillas de Weberbauerocereus weberbaueri con tratamiento de iluminación obtuvieron el más alto porcentaje de germinación (90.4%). Sin embargo, en esta especie con el tratamiento sin iluminación no se obtuvo ninguna germinación (Cuadro 2). Cabe mencionar que de todas las especies evaluadas solamente las semillas de Armatocereus mataranus subsp. ancashensis y Austrocylindropuntia floccosa germinaron con tratamiento de iluminación y en condiciones de oscuridad. Armatocereus mataranus subsp. ancashensis en condiciones de oscuridad obtuvo el mayor porcentaje de germinación, alcanzando 64%; en tanto Austrocylindropuntia floccosa con tratamiento de oscuridad alcanzó 32.80% de germinación (Cuadro 2), lo que demuestra que ambas especies son fotoblásticas neutras.
Cuadro 2: Germinación de semillas (%) de 14 especies de cactáceas de Perú procedentes de los departamentos de Ancash, Apurímac, Arequipa y Huánuco, evaluadas con tratamientos de luz y oscuridad. Promedios con letras iguales en las columnas (*) son estadísticamente similares (p<0.05), por la prueba de comparación de medias de Tukey (α=0.05).
| Especies | Germinación de semillas (%) | |
|---|---|---|
| con luz | en oscuridad | |
| Weberbauerocereus weberbaueri (K. Schum. ex Vaupés) Backeb. | 90.40a | 0.00c(*) |
| Corryocactus aureus Meyen | 89.60ab | 0.00c |
| Trichocereus cuzcoensis Britton & Rose | 87.20ab | 0.00c |
| Corryocactus brevistylus Britton & Rose | 84.80abc | 0.00c |
| Browningia candelaris (Meyen) Britton & Rose | 79.20bcd | 0.00c |
| Haageocereus platinospinus (Werderm. & Backeb.) Backeb. | 75.20cde | 0.00c |
| Trichocereus santaensis Rauh & Backeb. | 68.80de | 0.00c |
| Espostoa lanata subsp. ruficeps (F.Ritter) G.J. Charles | 64.80ef | 0.00c |
| Lobivia maximiliana subsp. westii (Hutchison) Rausch ex G.D. Rowley | 58.40ef | 0.00c |
| Armatocereus mataranus subsp. ancashensis (F. Ritter) Ostolaza | 53.60g | 64.00a |
| Cumulopuntia ignescens (Vaupel) F. Ritter | 36.00h | 0.00c |
| Tunilla soehrensii (Britton & Rose) D.R. Hunt & Iliff | 32.00h | 0.00c |
| Austrocylindropuntia floccosa (Salm-Dyck) F. Ritter | 28.00hi | 32.80b |
| Opuntia macbridei Britton & Rose | 18.40i | 0.00c |
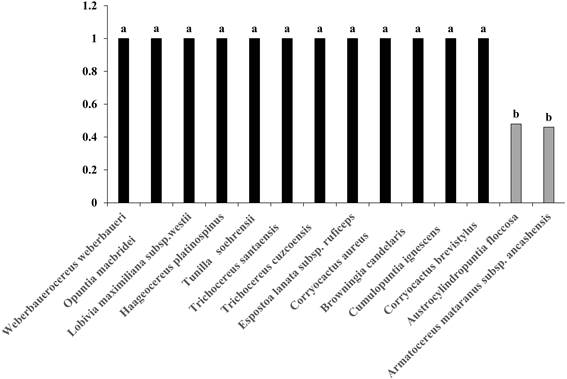
Índice de germinación relativa a la luz
Cuando se realizó el análisis de comparación múltiple de medias por Tukey (α=0.05), de las 14 especies de cactus evaluadas 12 obtuvieron el valor de 1 de índice de germinación relativa a la luz (GRL) (Fig. 3). Por lo tanto, las semillas de Haageocereus platinospinus, Lobivia maximiliana subsp. westii, Trichocereus cuzcoensis, Trichocereus santaensis, Weberbauerocereus weberbaueri, Browningia candelaris, Corryocactus aureus, Corryocactus brevistylus, Espostoa lanata subsp. ruficeps, Cumulopuntia ignescens, Opuntia macbridei y Tunilla soehrensii son fotoblásticas positivas. Por otra parte, Armatocereus mataranus subsp. ancashensis obtuvo un valor de 0.46 de GRL y Austrocylindropuntia floccosa 0.48 (Fig. 3), por lo que las semillas de estas dos especies responden de forma indiferente o neutra a la luz.
Discusión
De las 14 especies evaluadas, en la subfamilia Opuntioideae, tribu Opuntioideae, Austrocylindropuntia floccosa obtuvo el valor más alto de masa (1.53 gramos) de todas las especies evaluadas. Cumulopuntia ignescens, Opuntia macbridei y Tunilla soehrensii obtuvieron un mayor valor de masa que el resto. La masa en las semillas es un factor importante, ya que a mayor masa de la semilla es probable que la respuesta en la germinación sea fotoblástica neutra, porque a mayor masa de semillas tendrá menor dependencia a la luz (Flores et al., 2016).
Asimismo, se ha observado en estas especies que la germinación mejoró con un pretratamiento de escarificación mecánica con lijado de la testa, considerando que las semillas en estas especies son relativamente más grandes. Cabe mencionar que Cumulopuntia ignescens, Opuntia macbridei y Tunilla soehrensii germinaron únicamente con tratamiento de iluminación, obteniendo 36, 32 y 18.40 por ciento de germinación, respectivamente, en comparación con Austrocylindropuntia floccosa que germinó tanto en tratamiento de luz como en oscuridad.
Contrastando nuestros resultados con otros trabajos realizados en la tribu Opuntioideae, como por ejemplo el de Flores et al. (2011), cuando evaluaron la germinación de Cylindropuntia imbricata (Haw.) F.M. Knuth consiguieron 47% de germinación con tratamiento de iluminación y 73% de germinación con tratamiento en oscuridad. Reyes-Corral et al. (2022) en Cylindropuntia leptocaulis (DC.) F.M. Knuth lograron 13.30% de germinación en un tiempo promedio de germinación de 27.7 días; en contraste con Cylindropuntia spinosior (Engelm.) F.M. Knuth que presentó los valores más bajos de porcentaje de germinación (3.30%) en tiempo medio de germinación de 4.60 días. En Opuntia macbridei alcanzamos 18.40% de germinación. Flores et al. (2011) en Opuntia sulphurea G. Don. obtuvieron 5% de germinación con tratamiento de iluminación y 0% en oscuridad, mientras que Opuntia Engelm. tuvo 12% de germinación con tratamiento de iluminación y 0% en oscuridad. Olvera-Carrillo et al. (2003) en Opuntia tomentosa lograron un 20% de germinación con tratamiento de iluminación y 0% en oscuridad. González-Cortés et al. (2018), cuando evaluaron la germinación de Opuntia engelmannii Salm-Dyck y Opuntia microdasys Lehm. con pretratamiento de semillas lijado de testa y luego remojarlas en peróxido de hidrógeno durante 24 horas, alcanzaron un 82.50% y 67.50% de germinación, respectivamente, mientras que O. rastrera F.A.C. Weber alcanzó 72.50% de germinación con semillas lijadas. Opuntia megacantha Salm-Dyck consiguió el mayor porcentaje de germinación (100%). Del análisis de estos trabajos se observa que en los experimentos de germinación con iluminación y con pretratamiento de escarificación mejora la germinación de semillas, pero el tiempo promedio de germinación es muy variable, lo que coincide con nuestros resultados.
En la subfamilia Cactoideae, tribu Browningieae, Armatocereus mataranus subsp. ancashensis, con pretratamiento de escarificación de lijado de la testa de la semilla, fue la que requirió el mayor tiempo promedio de germinación (20.80 días). Asimismo, las semillas de este taxon germinaron tanto con tratamiento de luz como en oscuridad. Además, es necesario resaltar que con tratamiento en oscuridad obtuvo un mayor porcentaje de germinación (64%) que con el tratamiento con luz. Sin embargo, Rojas (2023) al evaluar la germinación de esta subespecie con iluminación reportó 67.40% de germinación. En efecto, cuando las semillas germinan en condiciones de iluminación y en oscuridad, se les conoce como semillas indiferentes o neutras (Rojas-Aréchiga y Batis, 2001). En las cactáceas se han reportado la presencia de semillas fotoblásticas positivas e indiferentes (Rojas-Aréchiga et al., 2013). En el banco de semillas del suelo, cuando las semillas indiferentes a la luz se entierran a poca profundidad pueden ser capaces de germinar a pocos milímetros de la superficie del suelo donde se mantiene la humedad por un periodo más prolongado, y también les permite una protección a las altas temperaturas y de los depredadores (Rojas-Aréchiga y Batis, 2001).
Browningia candelaris requirió de un tiempo promedio de 11.20 días para la germinación. Germinaron solamente con el tratamiento de iluminación con 79.20%, y el valor de 1 del índice de germinación relativa a la luz; en consecuencia, las semillas de esta especie son fotoblásticas positivas. En la tribu Notocacteae fueron evaluados Corryocactus aureus y Corryocactus brevistylus, y coincidentemente ambas especies obtuvieron una masa de 0.03 gramos. Sin embargo, Corryocactus aureus obtuvo un porcentaje de germinación de 89.60%, mayor que Corryocactus aureus (84.80%), y ninguna de estas dos especies germinaron en condiciones de oscuridad. Jara-Peña et al. (2018) informaron que las semillas de Corryocactus brevistylus son fotoblásticas positivas, y el mayor número de semillas germinadas se obtuvo solamente con el tratamiento de iluminación (control) y con tratamiento de iluminación más 200 ppm de ácido giberélico; con el tratamiento en oscuridad no consiguió ninguna germinación. Sin embargo, Flores et al. (2011) al evaluar la germinación de Corryocactus brevistylus con el tratamiento de iluminación consiguieron 85% de germinación y con tratamiento en oscuridad 1% de germinación, y el valor de GRL de 0.98.
Por su parte, Larrea-Alcázar y Pablo López (2008) evaluaron la germinación de Corryocactus melanotrichus en condiciones de laboratorio (16-25 °C) y con iluminación de luz natural, y con pretratamiento de semillas con escarificación mecánica (lijado) e inmersión de semillas en soluciones ácidas. Las semillas germinaron rápidamente durante la primera semana, y en todos los tratamientos aumentaron la capacidad germinativa: 28.50% (control) y con escarificación mecánica (45%) y con soluciones ácidas 65%, respectivamente.
De la tribu Trichocereeae fueron evaluadas las semillas de Espostoa lanata subsp. ruficeps, Haageocereus platinospinus, Lobivia maximiliana subsp. westii, Trichocereus cuzcoensis, Trichocereus santaensis y Weberbauerocereus weberbaueri. En esta tribu las masas de las semillas obtuvieron valores entre 0.01 (Espostoa lanata subsp. ruficeps) y 0.15 gramos (Trichocereus santaensis). Pues bien, los argumentos para explicar la germinación de las semillas en respuesta a la luz han ido cambiando con el tiempo. Flores et al. (2006) informaron que las semillas de cactáceas que requerían luz tenían tamaños pequeños, considerando, que tiempo atrás, había pocos estudios que traten sobre la masa de semillas y el fotoblastismo en cactáceas. Posteriormente, Flores et al. (2011) concluyeron que en las cactáceas, el fotoblastismo positivo está asociado con la forma de vida y la masa de semillas
Referente a la germinación de semillas, en la tribu Trichocereeae, Weberbauerocereus weberbaueri es la especie que obtuvo el más alto porcentaje de germinación (90.40%), seguida de Trichocereus cuzcoensis (87.20%), Haageocereus platinospinus (75.20%), Trichocereus santaensis (68.80%), Espostoa lanata subsp. ruficeps (64.80%) y Lobivia maximiliana subsp. westii (58.40%), respectivamente. Las semillas de las seis especies y subespecies de esta tribu germinaron solamente con el tratamiento de iluminación, y también coincide que estas especies y subespecies estudiadas consiguieron el valor de 1 de GRL. Esta respuesta de germinación nos indica un fotoblastismo positivo. Sin embargo, Flores et al. (2011) consiguieron algunas diferencias de GRL entre taxones de Cacteae, Pachycereeae y Trichocereeae; estos tenían mayores valores GRL que Notocacteae, pese a que nosotros logramos valores altos de GRL en las tribus de Trichocereeae y Notocacteae. Por su parte, Flores et al. (2011) en Espostoa melanostele (Vaupel) Bullock alcanzaron 94% de germinación en condiciones de iluminación, ninguna germinación en oscuridad y el valor de 1 de GRL. Entre tanto, Villanueva (2018), cuando evaluó la germinación de semillas de cuatro especies de cactus en condiciones de 12 horas de iluminación, alcanzó el mayor porcentaje de germinación en Espostoa melanostele con 95%, seguida de Melocactus peruvianus Vaupel con 93%, Haageocereus pacalaensis Backeb. con 83% y Neoraimondia arequipensis (Meyen) Backeb. con 83%, respectivamente. Flores et al. (2011) en Espostoa melanostele obtuvo 95% de germinación. En Haageocereus acrantus (Vaupel) Backeb. consiguieron 79% de germinación, en Haageocereus pseudomelanostele (Werderm. & Backeb.) Backeb. 91%, en Haageocereus pseudomelanostele subsp. auriespinus (Rauh & Backeb.) Ostolaza 83% de germinación. Estas tres especies obtuvieron un valor de GRL de 1, y germinaron únicamente con tratamiento de iluminación (Flores et al., 2011). En este sentido, la luz suele favorecer la germinación, y la exposición prolongada de semillas a la oscuridad reduce la sensibilidad a la luz. En cactáceas que habitan en ambientes hostiles, una respuesta rápida a la exposición a la luz es potencialmente ventajosa para el establecimiento de las plántulas (Yang y Pritchard, 2022). Considerando luego del éxito en la germinación de las semillas, la siguiente etapa vital es el establecimiento de plántulas en donde la luz favorece este proceso.
Lindow-López et al. (2018), cuando investigaron los efectos de temperaturas constantes y alternantes en la germinación de semillas fotoblásticas positivas de seis especies de cactus nativas de Argentina, notaron que las semillas de las especies evaluadas no germinaron en oscuridad, independientemente de los regímenes de temperatura. A una temperatura constante, Cereus hankeanus F.A.C. Weber, Trichocereus atacamensis Phil., Trichocereus terscheckii J. Parm. y Parodia aureicentra Backeb. mostraron una mayor proporción de germinación máxima que Echinopsis ancistrophora Speg. y Gymnocalycium saglionis F. Cels. Estos resultados coinciden con la germinación obtenida en Trichocereus cuzcoensis y Trichocereus santaensis, en la cual las semillas de estas dos especies germinaron solamente en condiciones de iluminación. Un resultado similar también fue obtenido por Ortega-Baes y Rojas-Aréchiga (2007) en semillas de Trichocereus terscheckii que germinaron en el rango de temperatura entre 15 a 35 °C, y los porcentajes máximos de germinación obtuvieron con luz blanca, sin registrar ninguna germinación en condiciones de oscuridad. Ortega-Baes et al. (2010) en Trichocereus candicans (Gillies ex Salm-Dyck) Britton & Rose registró 82% de germinación, en Echinopsis thelegona (F.A.C. Weber) H. Friedrich & G.D. Rowley 93%, y en Haageocereus pseudomelanostele subsp. auriespinus 83%. Estas tres especies obtuvieron valor de GRL de 1 y germinaron únicamente en tratamiento de iluminación (Flores et al., 2011).
Conclusiones
La mayor masa de semillas fue obtenida en Austrocylindropuntia floccosa (1.53 g) y la menor masa se obtuvo en Espostoa lanata subsp. ruficeps con 0.01 gramos. Armatocereus mataranus subsp. ancashensis requirió del mayor tiempo promedio de germinación necesitando 20.80 días, y Weberbauerocereus weberbaueri fue la especie que menos tiempo promedio de germinación requirió, germinando en 10 días. De las 14 especies evaluadas, 12 especies son fotoblásticas positivas, que son: Haageocereus platinospinus, Lobivia maximiliana subsp. westii, Trichocereus cuzcoensis, Trichocereus santaensis, Weberbauerocereus weberbaueri, Browningia candelaris, Corryocactus aureus, Corryocactus brevistylus, Espostoa lanata subsp. ruficeps, Cumulopuntia ignescens, Tunilla soehrensii y Opuntia macbridei. De otra parte, Armatocereus mataranus subsp. ancashensis y Austrocylindropuntia floccosa son fotoblásticas neutras.











 nueva página del texto (beta)
nueva página del texto (beta)