Introducción
La interacción entre el suelo, las plantas y los microorganismos es un componente esencial para la sostenibilidad y productividad agrícola. Las bacterias benéficas que habitan la rizosfera y la endosfera de las plantas desempeñan un papel importante en la promoción del crecimiento vegetal al ser utilizadas como bioestimulantes. Las bacterias promotoras del crecimiento vegetal (PGPB, por sus siglas en inglés) son microorganismos que inciden en el metabolismo vegetal mejorando la disponibilidad de nutrientes, incrementan la fertilidad de los suelos agrícolas y favoreciendo el crecimiento y rendimiento de las plantas. Estas bacterias incluyen géneros como Klebsiella, Acinetobacter, Bacillus y Pseudomonas, los cuales han demostrado tener un potencial significativo como promotores del crecimiento de plantas (De Souza, Ambrosini y Passaglia, 2015).
Las PGPB emplean una amplia gama de mecanismos de acción, entre ellos se incluye la fijación de nitrógeno, la solubilización de fósforo, la producción de reguladores de crecimiento o la liberación de hormonas como auxinas y citoquininas (Ramakrishna, Yadav y Li, 2019). Estas funciones microbianas no solo mejoran la nutrición de las plantas, sino que también aumentan la calidad y fertilidad del suelo, promoviendo un ecosistema agrícola más saludable y productivo. Se ha descubierto que la aplicación de cepas PGPB puede incidir en el crecimiento y rendimiento de cultivos, además, ayuda a reducir la dependencia de fertilizantes químicos, contribuyendo a prácticas agrícolas sostenibles (Kong et al., 2019).
El maíz (Zea mays L.) es uno de los cultivos más importantes a nivel mundial y México es reconocido como su centro de origen y diversificación. Las razas criollas de maíz en México no solo tienen una gran importancia económica, sino también social y agrícola, debido a su adaptabilidad y resistencia a diversas condiciones ambientales. La aplicación de biofertilizantes formulados a partir de PGPB en cultivos de maíz ha mostrado efectos significativamente positivos, incluyendo el incremento en el rendimiento del cultivo, la mejora en la calidad del suelo, y la protección de las plantas contra daños ocasionados por la salinidad. Estudios recientes han destacado el impacto beneficioso de cepas bacterianas específicas en el crecimiento y la productividad del maíz (Rodríguez-Hernández et al., 2019). Las técnicas moleculares avanzadas, como la amplificación del gen 16S rRNA y huellas genómicas ERIC-PCR (Enterobacterial Repetitive Intergenic Consensus), han permitido una identificación más precisa y una comprensión más profunda de las bacterias PGPB. Estas tecnologías han facilitado el aislamiento y caracterización de cepas bacterianas con alto potencial biofertilizante, desempeñando un papel fundamental en la mejora de la productividad agrícola y en la sostenibilidad de los sistemas agroecológicos (Gamalero, Bona y Glick, 2022).
El objetivo de este trabajo fue identificar taxonómicamente cepas bacterianas rizosféricas y endofíticas fijadoras de nitrógeno asociadas al cultivo de maíz mediante el uso del gen 16S rRNA y huellas genómicas ERIC-PCR y evaluar sus cualidades de promoción de crecimiento vegetal.
Materiales y Métodos
Sitio experimental y caracterización fisicoquímica del suelo agrícola
Muestras de suelo agrícola a granel (suelo inicial sin planta) se obtuvieron en septiembre de 2023 en la parcela ubicada en el Ejido Palo Alto, municipio de Berriozábal, Chiapas, a 1100 m de altitud y con coordenadas geográficas de 16° 48’ 16.1” N, 93° 22’ 13.0” O según el USGS (2024). El sitio experimental presenta un clima cálido subhúmedo (Awo) a cálido húmedo (Am), con un rango de temperatura que oscila entre 22 y 28 °C y, con un rango de precipitación de 900 a 2000 mm (INEGI, 2021). El muestreo de suelo se llevó a cabo con la finalidad de realizar determinaciones fisicoquímicas para conocer el estado inicial del sitio experimental. Las muestras de suelo a granel se recolectaron a una profundidad de 0-30 cm, seleccionando cinco puntos aleatorios distribuidos en la parcela, con el objetivo de asegurar que la muestra obtenida fuera representativa de toda la extensión de la parcela (Mendoza y Espinoza, 2017). El pH, conductividad eléctrica (CE), capacidad de intercambio catiónico (CIC) y la temperatura se determinaron in situ utilizando un medidor multiparamétrico portátil HANNA® modelo HI-9828 (HANNA Instruments, Limena, Italy). (Rincón-Molina et al., 2019). La materia orgánica y el nitrógeno total se determinaron con un analizador elemental Flash 2000 (Thermo Scientific®, USA). El fósforo total se determinó con el método de solubilización de HNO3/HClO4.
Obtención de suelo rizosférico y granos de maíz
Para la obtención de muestras de suelo rizosférico de plantas de maíz, se realizó inicialmente la colecta de las plantas. El diseño de muestreo empleado fue un muestreo aleatorio simple, mediante el cual se seleccionaron cinco plantas completas, incluyendo las raíces, siguiendo la metodología de extracción descrita por Schafer, Hallett y Johnson (2014). Estas plantas se ubicaron en cinco puntos seleccionados al azar dentro de un área mínima en la parcela experimental. Las raíces fueron agitadas vigorosamente para eliminar el suelo a granel y, posteriormente, se limpió cuidadosamente la fina capa de suelo adherida a la superficie radicular utilizando una brocha estéril, según lo recomendado por Clemmensson-Lindell y Persson (1992).
Para la obtención de granos de maíz, se seleccionaron 10 mazorcas de forma aleatoria de las mismas plantas utilizadas para las muestras de suelo rizosférico. Las mazorcas fueron transportadas al laboratorio en hieleras para preservar su integridad. Los granos se extrajeron utilizando pinzas de disección estériles, seleccionando cinco granos al azar de cada mazorca, lo que resultó en un total de 50 granos. El proceso de extracción se realizó con extremo cuidado, asegurando que el pedicelo de los granos no sufriera fracturas, a fin de evitar la entrada de agentes de desinfección al interior del grano.
Aislamiento y cultivo de bacterias
Se llevó a cabo el aislamiento de bacterias asociadas a la rizosfera y endófitas. Para el procesamiento de las muestras de suelo rizosférico, se pesó 1.0 g de muestra de suelo, se colocó en un matraz que contenía 100 mL de H2O destilada estéril y se dejó en agitación a 120 rpm durante 24 h. Se realizaron diluciones seriadas de las muestras en tubos de ensayo hasta una dilución de 10-7. Alícuotas de 100 μL de las diluciones 10-5 a 10-7 fueron inoculadas en tubos de ensayo que contenían medio NFb semisólido pH 6.8 (Baldani et al., 2014) y, tubos con medio nutritivo semisólido (3.0 g L-1 de extracto de carne, 5.0 g L-1 de peptona de gelatina, 5.0 g L-1 de agar bacteriológico). Los tubos se incubaron a 30 °C de 3 a 5 días.
Con respecto al aislamiento de endófitos, los granos de maíz se desinfectaron durante 5 min con etanol (70%) y después con hipoclorito de sodio (1.5%) durante 10 min, seguidos de lavados con agua destilada estéril (Rincón-Molina et al., 2022). Para determinar la efectividad del método de desinfección, se tomaron alícuotas de 100 μL del agua utilizada en el último lavado y se inocularon en placas con medio PY-Ca2+ (5.0 g L-1 de peptona de caseína, 10 mL L-1 de 0.94 M CaCl2 y, 3.0 g L-1 de extracto de levadura pH 6.8) a 30 °C por 72 h (Rincón-Rosales, Lloret, Ponce y Martínez, 2009). Los granos de maíz fueron macerados en morteros esterilizados previamente y las muestras fueron inoculadas en tubos de ensayo que contenían medio NFb semisólido y tubos con medio nutritivo semisólido, se incubaron a 30 °C de 3 a 5 días.
Posteriormente, se analizó el cambio de coloración y crecimiento bacteriano. Los tubos que presentaron cambio de coloración fueron inoculados en placas con medio NFb para comprobar el crecimiento de bacterias fijadoras de nitrógeno (Baldani et al., 2014). Las placas se incubaron a 30 °C durante 72 h. Las colonias crecidas en cajas que presentaron cambio de coloración fueron trasladadas a medio PY-Ca2+ hasta su purificación.
La morfología celular de las cepas aisladas de las muestras de rizosfera y endófitas fue examinada por microscopía de luz visible (Zeiss® PS7, Alemania). Se determinó la reacción Gram utilizando un kit comercial (Merck®, Alemania), de acuerdo con las especificaciones del fabricante.
Identificación molecular de cepas bacterianas
Se realizó la extracción de ADN total bacteriano para cada cepa obtenida utilizando el kit comercial DNA Isolation Kit for Cells and Tissues (Roche®) siguiendo las especificaciones del fabricante (López-Fuentes et al., 2012). La calidad y cantidad del ADN extraído se verificaron mediante electroforesis en gel de agarosa al 1% y con el espectrofotómetro UV-Vis de microvolumen NanoDrop One de Thermo Scientific®.
Utilizando el ADN total de cada cepa bacteriana, se obtuvieron patrones moleculares con la técnica de reacción en cadena de polimerasa de secuencias consenso repetitivas intergénicas de enterobacterias (ERIC-PCR, por sus siglas en inglés), utilizando los cebadores ERIC1 y ERIC2, como se describe en Versalovic, Koeuth y Lupski (1991). Los patrones genómicos se identificaron después de la separación de los productos de PCR por electroforesis en gel de agarosa al 1.5% y se analizaron con el software GelCompar II (Applied Maths®). Los índices de riqueza (d) y diversidad (H) (índice de Shannon-Weaver) se calcularon con base en el número total de bacterias aisladas de la rizosfera y de tejidos vegetales de las plantas de maíz con respecto a los patrones genómicos obtenidos (Pereira, Nesci y Etcheverry, 2009). Se llevó a cabo la Reacción en Cadena de la Polimerasa (PCR, por sus siglas en inglés) para amplificar el gen 16S rRNA con la ayuda del kit comercial HIGH Pure PCR Template Preparation Kit (Roche®). Se utilizaron los cebadores universales 27F (5′-AGAGTTTGATCCTGGCTCAG-3′) y 1492R (5′-TACGG- YTACCTTGTTACGACTT-3′). El protocolo de amplificación fue de acuerdo con lo comentado por Rincón-Molina et al. (2020).
Los productos de PCR fueron purificados y secuenciados en Macrogen® (Seúl, Corea). Las secuencias se editaron con el programa Bioedit Sequence Alignment Editor®. Todas las secuencias se compararon utilizando la herramienta de análisis BLAST de la base de datos del Centro Nacional de Información Biotecnológica (NCBI, por sus siglas en inglés) (Rincón-Molina et al., 2022).
Pruebas PGPB
Se realizaron pruebas para evaluar la capacidad de las cepas bacterianas aisladas como promotoras del crecimiento vegetal, centrándose en su capacidad para la fijación de nitrógeno, la solubilización de fosfato y la producción de sideróforos.
Para la prueba de reducción de acetileno, que se realiza para evaluar la capacidad de las cepas bacterianas de fijar nitrógeno, se inocularon viales con medio mínimo libre de nitrógeno con cada una de las cepas obtenidas. Se empleó un inóculo bacteriano del género Klebsiella spp. como control positivo y se incubaron durante 24 h a 35 °C. Posteriormente, se preparó un vial con carburo de calcio, al que se le inyectó 0.1 mL de agua milli-Q® para inducir la reacción exotérmica y producir gas acetileno. A los viales inoculados se les retiró 0.4 mL de aire con una jeringa para inyectar el gas acetileno, seguido de una incubación adicional de 24 horas a 35 °C. La reducción de acetileno a etileno, un indicador indirecto de la actividad de fijación de nitrógeno, fue medida mediante cromatografía de gases utilizando un cromatógrafo de gases Varian® 3300 (Rincón-Molina et al., 2020).
La evaluación cualitativa para la solubilización de fosfato inorgánico se evaluó en placas con medio de crecimiento enriquecido con fosfato tricálcico [Ca3(PO4)2] como fuente de fósforo, según lo descrito por Gen-Jiménez et al., (2023). Las colonias bacterianas solubilizadoras de fósforo fueron reconocidas por la presencia de halos después de haber sido incubadas a 28 ºC durante 3 a 5 días.
La capacidad de producir sideróforos se determinó cualitativamente a partir del ensayo CAS-agar (Schwyn y Neilands, 1987). Se inoculó cada cepa y se incubó de 3 a 5 días a 28 °C. La formación de halos amarillos-anaranjados alrededor de las colonias indicaron la capacidad para producir sideróforos (Rincón-Molina et al., 2020).
Resultados y Discusión
El análisis fisicoquímico de las muestras de suelo a granel obtenidas de la parcela experimental mostró un pH de 7.71±0.22, una baja CE (0.113±0.26 dS m-1), un valor alto de CIC (52.79±1.54 Cmol kg-1). Se determinó una moderada cantidad de materia orgánica (8.19±0.16%). Por otra parte, la cantidad de nitrógeno total (0.42±1.7%), fósforo disponible (6.81±1.8 mg kg-1) y potasio disponible (0.42±0.02 Cmol kg-1) se encontró en muy bajas cantidades. Adicionalmente, se determinó que el suelo a granel está compuesto en un 14.2% de arena, 65.8% de arcilla y 20% de limo. Diferentes estudios han demostrado que los suelos agrícolas en Chiapas presentan variaciones significativas en sus propiedades fisicoquímicas dependiendo del uso del suelo y la topografía. Por ejemplo, en los Altos de Chiapas, los suelos presentan una baja disponibilidad de nutrientes y una tendencia hacia la acidez (León-Nájera, Gómez, Hernández y Alvarez, 2006; Martínez-Soto, Yañez, Cantú, González y Marmolejo, 2022). Un pH de 7.71 señala que el suelo es moderadamente alcalino, lo que puede limitar la disponibilidad de micronutrientes clave para el desarrollo de las plantas, como el hierro (Fe), manganeso (Mn), zinc (Zn) y cobre (Cu) (Gupta, Kening y Liang, 2008). En suelos alcalinos, la presencia de metales como el aluminio (Al) y el hierro (Fe) puede estar limitada, lo que afecta la absorción de estos nutrientes por las plantas (Riaz et al., 2020; Martínez-Soto et al., 2022). El elevado valor de CIC identificado en este estudio indica una gran capacidad del suelo para retener nutrientes, lo que representa un factor favorable para su fertilidad. Un valor alto de CIC se asocia típicamente con una mayor presencia de arcilla, componentes que aumentan la capacidad del suelo para retener cationes esenciales como el calcio (Ca), magnesio (Mg) y potasio (K) (Yang et al., 2024). Un pH ligeramente alcalino puede limitar la disponibilidad de ciertos micronutrientes, pero esto no necesariamente contradice los beneficios de una alta CIC. En suelos con alta CIC, los macronutrientes esenciales suelen estar más disponibles. La menor disponibilidad de micronutrientes puede corregirse mediante prácticas de manejo adecuadas, como la adición de quelatos de hierro o el uso responsable de fertilizantes específicos (Osman, 2013; Havlin, 2020). Es importante señalar que la materia orgánica es crucial para la fertilidad del suelo y la salud de los cultivos. El contenido moderado de materia orgánica en el suelo de la parcela experimental es un indicador positivo para el cultivo de maíz, ya que sugiere que el suelo tiene buena retención de agua y de nutrientes, lo que es crucial para el crecimiento saludable de las plantas, especialmente en condiciones de cultivo intensivo (Fageria, 2012; Ankenbauer y Loheide, 2017; Minasny y McBratney, 2018; Lal, 2020). Por otro lado, es importante considerar la disponibilidad de otros nutrientes esenciales como el nitrógeno, fósforo y potasio, que se encontraron en bajas cantidades en el análisis del suelo. El nitrógeno es un nutriente esencial para el crecimiento de las plantas, involucrado en la síntesis de proteínas y la fotosíntesis (Fathi, 2022). La baja cantidad de nitrógeno total en el suelo puede estar relacionada con una mineralización deficiente de la materia orgánica, un proceso clave que libera nitrógeno disponible para las plantas. Esta deficiencia en la mineralización podría deberse a condiciones ambientales no óptimas, como temperatura, humedad o niveles de oxígeno inadecuados, así como a una baja actividad microbiana, lo que limita la descomposición de la materia orgánica y, por tanto, la liberación de nitrógeno (Ma et al., 2020; Kirsten et al., 2021). De igual manera, el fósforo es vital para la transferencia de energía en las plantas y el desarrollo de las raíces (Fathi y Afra, 2023). La baja cantidad de fósforo disponible puede deberse a la inmovilización en suelos arcillosos. Estudios indican que estos suelos tienen la capacidad de fijar fósforo, formando compuestos insolubles que las plantas no pueden absorber (Islam et al., 2024). En cuanto a la baja cantidad de potasio disponible en el suelo de acuerdo con el análisis realizado en este estudio, puede deberse a la continua extracción de este nutriente por cultivos anteriores sin una adecuada reposición mediante fertilización. En Chiapas, se ha documentado que muchos suelos presentan bajas concentraciones de potasio intercambiable, lo que puede afectar negativamente el rendimiento del maíz (Gómez et al., 2022). Además, en suelos con alta CIC, el potasio puede competir con otros cationes, como calcio y magnesio, por los sitios de adsorción en las partículas de arcilla, reduciendo su disponibilidad para las plantas (Appel, Ma, Rhue y Reve, 2003; Rakhsh, Golchin, Al Agha y Alamdari, 2017). Esta competencia, junto con posibles procesos de lixiviación en suelos arcillosos, puede limitar la cantidad de potasio accesible para el crecimiento óptimo de los cultivos.
El análisis fisicoquímico del suelo de la parcela experimental revela que, según las cantidades de materia orgánica y la CIC, existe un buen potencial para la retención de nutrientes y agua, pero las bajas cantidades de nitrógeno total, fósforo y potasio disponibles indican deficiencias significativas que limitarían la fertilidad del suelo y, en consecuencia, la productividad del cultivo de maíz. El pH ligeramente alcalino puede reducir la disponibilidad de ciertos micronutrientes esenciales, complicando aún más la situación nutricional del suelo. En suelos arcillosos como el estudiado, que tienen una alta capacidad de retención de nutrientes, pero también una tendencia a inmovilizar fósforo es crucial implementar prácticas de manejo que incluyan la adición de insumos agrícolas específicos para corregir estas deficiencias. Por lo tanto, aunque el suelo tiene un buen potencial debido a su estructura y capacidad de retención, requiere un manejo cuidadoso y la suplementación adecuada de nutrientes esenciales para mejorar su fertilidad y optimizar su capacidad para soportar un cultivo de maíz productivo. La investigación de microorganismos de la rizosfera y endófitos de una amplia diversidad de plantas, especialmente con potencial como PGPB, ha cobrado relevancia en los últimos años, dado su potencial para mejorar la productividad agrícola de manera sostenible (Rincón-Molina et al., 2020; Saad, Kandil y Mohammed, 2020; Ercole et al., 2021; Fernández et al., 2023; Agunbiade, Fadiji, Agbodjato y Babalola, 2024). En este estudio, se aislaron y cultivaron microorganismos de la rizosfera y tejidos vegetales de maíz con el objetivo de identificar cepas con cualidades probióticas vegetales. Un total de 46 cepas bacterianas fueron aisladas de cultivos de maíz, usando medio de cultivo NFb y medio nutritivo, con la finalidad de aislar bacterias fijadoras de nitrógeno. De los aislados bacterianos, 28 cepas pertenecieron a la rizosfera (Cuadro 1) y 18 cepas endófitas fueron aisladas de los granos de maíz (Cuadro 2). En relación con los aspectos fenotípicos, los aislados presentaban morfología celular correspondiente a bacilos, cocos y cocobacilos. Dentro de los aislados, las bacterias gram negativas se encontraron en mayoría. En cuanto al aspecto y color, las cepas aisladas tuvieron aspecto seco a mucoso y presentaron coloración blanca, amarilla y crema. La eficacia del medio NFb en la selección de bacterias promotoras del crecimiento vegetal ha sido ampliamente documentada en la literatura científica. Investigaciones realizadas han demostrado la eficacia del medio NFb para aislar bacterias diazotróficas de diversos cultivos, incluyendo maíz y otros cereales (Döbereiner, Reis, Paula y Olivares, 1993; Weber et al., 1999). Estos estudios destacan la capacidad del medio para seleccionar cepas bacterianas que no solo fijan nitrógeno, sino que también poseen otros atributos beneficiosos como la producción de fitohormonas y la solubilización de fósforo.
Table 1: Relative abundance (%) according to ERIC group classification in rhizosphere.
| Rizósfera | ||
| Grupo | Cepa | Abundancia relativa |
| % | ||
| 1 | MC1 | 3.6 |
| 2 | MC2 | 3.6 |
| 3 | MC3 | 3.6 |
| 4 | MC4, MC24 | 7.1 |
| 5 | MC5, MC17 | 7.1 |
| 6 | MC6, MC7 | 7.1 |
| 7 | MC9 | 3.6 |
| 8 | MC11, MC19 | 7.1 |
| 9 | MC12 | 3.6 |
| 10 | MC13, MC27, MC28 | 10.7 |
| 11 | MC14 | 3.6 |
| 12 | MC15 | 3.6 |
| 13 | MC16-A, MC16-B | 7.1 |
| 14 | MC18 | 3.6 |
| 15 | MC20, MC22 | 7.1 |
| 16 | MC21, MC26 | 7.1 |
| 17 | MC23-A | 3.6 |
| 18 | MC25 | 3.6 |
| 19 | MC23-B | 3.6 |
| Total de cepas | 28 | 100 |
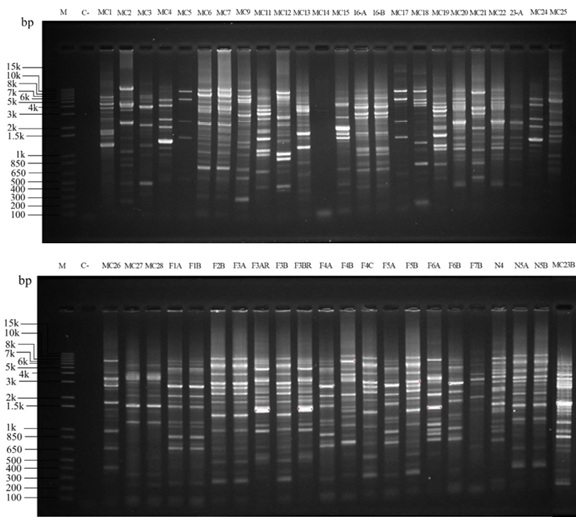
La riqueza y diversidad de aislados bacterianos se determinó con la técnica ERIC-PCR, que, tras obtener el ADN genómico de cepas puras, generó patrones genómicos de diferentes tamaños (Figura 1). Los perfiles genómicos ERIC agruparon a 46 cepas bacterianas aisladas de la rizosfera y tejidos vegetales de las plantas de maíz dentro de 26 grupos diferentes. Los índices de riqueza (d) y diversidad (H) fueron más altos en la rizosfera (d: 5.40, H: 6.60) que en los tejidos vegetales (d: 2.08, H: 3.70). Con respecto a la diferencia entre la cantidad de aislados según la sección de la planta, se ha evidenciado que las zonas más cercanas a las raíces (la rizosfera) o en el interior de estas, habitan una mayor diversidad de bacterias y que pueden colonizar la endosfera (Maldonado-Mendoza y Morales Ruíz, 2021).
El análisis de las secuencias del gen 16S rRNA de 22 cepas representativas reveló que los aislados pertenecían a 12 géneros bacterianos. Los géneros bacterianos presentes en la rizosfera son diversos e incluyen especies como Pseudacidovorax, Acinetobacter, Massilia, Klebsiella, Delftia, Pseudomonas, Ochrobactrum, Stenotrophomonas y Comamonas. Muchas de estas especies han sido identificadas como potenciales promotores del crecimiento vegetal (PGPB), exhibiendo capacidades tales como solubilización de fosfato, fijación de nitrógeno, fitorremediación, síntesis de hormonas vegetales y producción de biopelículas (Cuadro 3) (Han et al., 2005; Carcaño-Montiel, Ferrera, Pérez, Molina y Bashan, 2006; Pang et al., 2016; Pandey, Pathak y Dave, 2016; Zheng, Bi, Hao, Zhou y Yang, 2017; Wedage, Aberathne, Harischandra y Gunawardana, 2019; Morales-Guzmán et al., 2020; Lau y Chang, 2024). Además, se ha reportado que algunas de estas bacterias han sido empleadas en procesos de biorremediación y biodegradación de contaminantes ambientales y compuestos orgánicos, destacando su potencial aplicabilidad en contextos industriales y medioambientales (Cuadro 3) (Verma, Singh, Chowdhury y Tripathi, 2004; Pandey et al., 2016; Sanclemente, Yacumal y Patiño, 2017).
Table 3: Molecular characteristics of bacterial strains isolated from maize cultivation.
| Grupo ERIC | Cepa | Especie similar BLAST-NCBI | Similitud genética (%) | Fuente de aislamiento | Cualidades biológicas | Referencia |
| 1 | MC1 | Pseudacidovorax intermedius OsEnb_ALM_A3 | 99.81 | Rizosfera | Competente en nodulación con identidad no rizobiana, capaz de secretar IAA, celulasas y proteinasas al medio extracelular, formación de biopelículas. | Wedage, Aberathne, Harischandra y Gunawardana (2019) |
| 2 | MC2 | Acinetobacter calcoaceticus R1-1 | 98.57 | Rizosfera | Biorremediación por degradación de hidrocarburos lineales. Cepa con cualidades PGPB en cultivos de maíz y pepino. | Pandey et al. 2016; Sanclemente, Yacumal y Patiño (2017) |
| 3 | MC3 | Massilia phosphatilytica 12-OD1 | 95.63 | Rizosfera | Solubiliza fosfatos | Zheng, Bi, Hao, Zhou y Yang (2017) |
| 4 | MC4 | Acinetobacter baylyi PKS61 | 96.79 | Rizosfera | Inocua, posee capacidad para degradar varios compuestos aromáticos y con potencial biotecnológico. | (Metzgar et al., 2004; Fischer, Bleichrodt y Gerischer, 2008;Santala et al., 2011) |
| 6 | MC6 | Klebsiella sp. A8-KP4 | 96.57 | Rizosfera | Fijadora de N2 y productora de sustancias reguladoras del crecimiento. | Carcaño-Montiel, Ferrera, Pérez, Molina y Bashan (2006) |
| 7 | MC9 | Delfia tsuruhatensis AD1 | 99.04 | Rizosfera | Cepa con características PGPB en cultivos de arroz y potencial agente de biocontrol contra patógenos de las plantas. | Han et al. (2005) |
| 8 | MC19 | Pseudomonas putida JC186 | 99.50 | Rizosfera | Producción de IAA, solubilización de fosforo inorgánico en trigo | Pang et al. (2016) |
| 9 | MC12 | Ochrobactrum sp. KT49 | 95.55 | Rizosfera | Tolerante a metales pesados, utilizada en biorremediación de aguas contaminadas, con cualidades PGPB. | Verma, Singh, Chowdhury y Tripathi (2004) |
| 10 | MC13 | Stenotrophomonas maltophilia HH21 | 98.86 | Rizosfera | Biorremediación de suelos/degradación de pesticidas | Estrada-Gamboa et al. (2023) |
| 12 | MC15 | Pseudomonas putida TA7 | 98.02 | Rizosfera | Cualidades PGPB con potencial aplicación industrial y medioambiental | Benedetti (2014†) |
| 13 | MC16-B | Stenotrophomonas maltophilia SW20 | 97.34 | Rizosfera | Biodegradación de compuestos orgánicos y solubiliza fosfato | Morales-Guzman et al. (2020) |
| 15 | MC20 | Pseudomonas taiwanensis GN1026 | 95.57 | Rizosfera | Solubiliza fosfato | Torres-Rubio, Valencia, Bernal y Martínez (2000) |
| 16 | MC26 | Comamonas terrigena MRHB1-156 | 96.58 | Rizosfera | Biorremediación y tolerancia a metales pesados | Lau y Chang (2024) |
| 17 | MC23-A | Pseudomonas putida E13 | 97.68 | Rizosfera | Aplicada en biodegradación de contaminantes ambientales y la síntesis de productos químicos de valor añadido (biocatálisis) | Kivisaar (2020) |
| 18 | MC25 | Pseudomonas mediterranea S58 | 99.51 | Rizosfera | Propiedades PGPB | Gu, Wang, Xia y Wei (2020) |
| 1 | F1A | Stenotrophomonas geniculata W10-6 | 99.47 | Endosfera | Tolerante a metales pesados | Zhang, Song, Zhang y Wang (2024) Wang et al. (2023) |
| 2 | F2B | Pantoea dispersa CHEN_B2 | 99.91 | Endosfera | Propiedades PGPB | Yang, Yi y Xia (2023) |
| 3 | F3AR | Brucella pseudogrignonensis H324 | 98.19 | Endosfera | Producción de sideróforos, movilización de fosforo y degradación de celulosa | Feigl et al. (2024) |
| 4 | F4B | Brucella pseudogrignonensis IILSFSC124 | 99.14 | Endosfera | Producción de sideróforos, movilización de fosforo y degradación de celulosa | Feigl et al. (2024) |
| 5 | F6A | Brucella pseudogrignonensis IILSFSC124 | 99.14 | Endosfera | Producción de sideróforos, movilización de fosforo y degradación de celulosa | Feigl et al. (2024) |
| 6 | F7B | Mycetocola reblochoni LMG23020 | 99.79 | Endosfera | Potencial biotecnológico en la producción de quesos | Bora et al. (2008) |
| 7 | N4 | Pantoea vagans Y-4 | 100 | Endosfera | Genes involucrados en la biosíntesis de carotenoides y terpenoides. Producción de A. giberélico, IAA y A. benzoico. Síntesis de rebaudiósido A | Simlat, Ptak, Jaglarz, Szewczyk, Dziurka y Gurgul (2023) |
† Benedetti, I. (2014). Design of standardized molecular tools to analyze regulatory properties and biotechnological applications of the soil bacterium Pseudomonas putida. Tesis para obtener el grado de Doctor en Ciencias. Universidad de Madrid. Disponible en http://hdl.handle.net/10486/664721
† Benedetti, I. (2014). Design of standardized molecular tools to analyze regulatory properties and biotechnological applications of the soil bacterium Pseudomonas putida. Thesis for the degree of Doctor of Science. Autonomous University of Madrid. Available in http://hdl.handle.net/10486/664721
Para las cepas bacterianas aisladas de la endosfera se identificaron cuatro géneros distintos: Stenotrophomonas, Pantoea, Brucella y Mycetocola. Estos géneros han sido asociados previamente con características relevantes PGPB. Entre las funciones destacadas se incluye la producción de sideróforos, la tolerancia a metales pesados con aplicaciones en fitorremediación, la movilización de fósforo y la degradación de celulosa (Morales-Guzmán et al., 2020; Estrada-Gamboa, Umaña, Sancho y Orozco, 2023; Kumar et al., 2023; Feigl et al., 2024). Además, se ha informado sobre su capacidad para sintetizar hormonas vegetales, tales como el ácido giberélico, el ácido indolacético (IAA) y el ácido benzoico, contribuyendo así a la promoción del crecimiento y desarrollo de las plantas hospederas (Cuadro 3) (Simlat, Ptak, Jaglarz, Szewczyk, Dziurka y Gurgul, 2023; Yang, Yi y Xia, 2023). Con respecto a la frecuencia de los aislados, destaca la presencia de dos grupos, Pseudomonas y Stenotrophomonas, con mayor abundancia, cuyas cualidades biológicas destacan la capacidad de producir algunos metabolitos que favorecen a la planta bajo diferentes condiciones de estrés biótico y abiótico, tolerancia a metales pesados, presentar actividades de promoción de crecimiento vegetal como fijación de nitrógeno, solubilizar fosfatos, además, de la eficacia en la inoculación de las semillas para aumentar el rendimiento de granos de maíz (Lizárraga-Sánchez, Leyva, Sánchez, Quiroz y Maldonado, 2015).
Los resultados de la prueba de reducción de acetileno, solubilización de fosfato y producción de sideróforos se presentan en el Cuadro 4. De las 46 cepas aisladas, ocho mostraron capacidad para la fijación biológica de nitrógeno, diez evidenciaron halos de solubilización de fosfato tras cinco días de inoculación, y 17 cepas demostraron capacidad para la producción de sideróforos. Dentro de estas cepas, las que pertenecen a los géneros Klebsiella, Pantoea y Brucella mostraron resultados positivos en las tres pruebas realizadas, lo que sugiere una capacidad multifuncional como promotoras del crecimiento vegetal.
Table 4: Results of the PGPB assays for the 46 isolated strains.
| Cepa | ARA* | SOL Pβ | SID° | Fuente de aislamiento |
| MC1 | + | - | + | Rizosférico |
| MC2 | - | + | - | Rizosférico |
| MC3 | + | - | + | Rizosférico |
| MC4 | - | + | - | Rizosférico |
| MC5 | - | - | - | Rizosférico |
| MC6 | + | + | + | Rizosférico |
| MC7 | + | - | - | Rizosférico |
| MC9 | - | - | + | Rizosférico |
| MC11 | - | - | - | Rizosférico |
| MC12 | - | - | - | Rizosférico |
| MC13 | - | - | + | Rizosférico |
| MC14 | - | - | - | Rizosférico |
| MC15 | - | - | + | Rizosférico |
| MC16-A | - | - | - | Rizosférico |
| MC16-B | - | - | + | Rizosférico |
| MC17 | - | - | + | Rizosférico |
| MC18 | - | - | + | Rizosférico |
| MC19 | - | + | + | Rizosférico |
| MC20 | - | + | - | Rizosférico |
| MC21 | - | - | - | Rizosférico |
| MC22 | - | - | - | Rizosférico |
| MC23-A | - | + | + | Rizosférico |
| MC23-B | - | + | - | Rizosférico |
| MC24 | - | - | - | Rizosférico |
| MC25 | - | - | - | Rizosférico |
| MC26 | - | - | + | Rizosférico |
| MC27 | - | - | - | Rizosférico |
| MC28 | - | - | - | Rizosférico |
| F1A | + | - | + | Endófito |
| F1B | - | - | - | Endófito |
| F2B | + | + | + | Endófito |
| F3A | - | - | - | Endófito |
| F3AR | - | - | - | Endófito |
| F3B | - | - | - | Endófito |
| F3BR | - | - | - | Endófito |
| F4A | - | - | - | Endófito |
| F4B | + | + | + | Endófito |
| F4C | - | - | - | Endófito |
| F5A | - | - | - | Endófito |
| F5B | - | - | - | Endófito |
| F6A | - | - | - | Endófito |
| F6B | - | - | - | Endófito |
| F7B | + | - | + | Endófito |
| N4 | - | + | + | Endófito |
| N5A | - | - | - | Endófito |
| N5B | - | - | - | Endófito |
+ = actividad positiva; - = actividad negativa. *ARA = prueba de reducción de acetileno; βSOL P = solubilización de fosfatos; °SID = Producción de sideróforos.
+ = positive activity; - = negative activity. *ARA = acetylene reduction assay; βSOL P = phosphate solubilization activity; °SID = siderophore production.
Los géneros Pantoea y Klebsiella han sido estudiados ampliamente por su rol en la promoción del crecimiento de las plantas, atribuible principalmente a su capacidad para fijar nitrógeno y producir sideróforos. Estas bacterias también pueden solubilizar fosfatos, contribuyendo a una mayor disponibilidad de nutrientes para las plantas hospedadoras (Rana et al., 2020; Duran-Bedolla, Garza, Rodríguez, Aguilar y Barrios, 2021; Sharma, Gang, Schumacher, Buck y Saraf, 2021; Timofeeva, Galyamova y Sedykh, 2023). Por otro lado, el género Brucella, aunque mayormente conocida como patógeno animal, incluye cepas que han demostrado ser beneficiosas para las plantas al promover su crecimiento mediante la fijación de nitrógeno y la producción de sideróforos (Khanna, Raj, Kumar y Wati, 2022; Sun, Shahrajabian y Soleymani, 2024).
De igual manera, las bacterias del género Pseudomonas exhibieron la capacidad de producir sideróforos y solubilizar fosfatos. Aunque no mostraron capacidad para fijar nitrógeno, su habilidad para aumentar la disponibilidad de nutrientes esenciales en el suelo las convierte en posibles candidatas para mejorar la salud y el rendimiento de los cultivos (Li et al., 2017; Timofeeva et al., 2023). Además, los géneros Massilia, Mycetocola y Stenotrophomonas demostraron la capacidad de producir sideróforos y fijar nitrógeno (Ryan et al., 2009; Ghosh, Chatterjee y Mandal, 2020; Peta, Raths y Bücking, 2021; Tuesta-Popolizio, Velázquez, Rodriguez y Contreras, 2021; Kumar et al., 2023; Martins et al., 2024). Esta combinación de habilidades puede contribuir significativamente a la mejora de la disponibilidad de nutrientes para las plantas, incrementando así la productividad agrícola en diversos sistemas de cultivo. Estos hallazgos subrayan la importancia de explorar y caracterizar cepas bacterianas con capacidades promotoras del crecimiento vegetal, para desarrollar estrategias biotecnológicas que optimicen el rendimiento agrícola sostenible. Es fundamental evitar el uso de géneros bacterianos relacionados con cepas patógenas, para asegurar la eficiencia en la promoción del crecimiento vegetal, la seguridad y salud de los cultivos, del medio ambiente y de los seres humanos (García-Fraile et al., 2017; Flores-Félix et al., 2024).
Conclusiones
Los hallazgos obtenidos en este estudio revelan una notable diversidad de bacterias rizosféricas y endofíticas con potencial promotor del crecimiento vegetal (PGPB) en el cultivo de maíz en Chiapas, México. Las cepas aisladas mostraron capacidades relevantes, como la fijación biológica de nitrógeno, la solubilización de fosfatos y la producción de sideróforos, lo que subraya su posible aplicación en la mejora de la nutrición vegetal y la sostenibilidad agrícola. Además, la caracterización genética mediante huellas genómicas ERIC-PCR y secuenciación del gen 16S rRNA permitió identificar una rica diversidad microbiana, destacando a los géneros Klebsiella, Acinetobacter, Pseudomonas y Stenotrophomonas como los más prominentes. Estos resultados sugieren que las interacciones de estas bacterias con el maíz pueden desempeñar un papel crucial en la optimización del uso de nutrientes y en la promoción de un desarrollo más eficiente del cultivo. La diversidad microbiana observada y la capacidad multifuncional de algunas de las cepas aisladas, como aquellas del género Klebsiella, evidencian su potencial para futuras aplicaciones biotecnológicas en el diseño de bioinoculantes dirigidos a mejorar la sostenibilidad de los sistemas de producción de maíz. Este estudio aporta información valiosa sobre la microbiota asociada al maíz y contribuye en el estudio para el futuro desarrollo de estrategias de biofertilización más eficientes y específicas. Por último, es importante mencionar que, antes de considerar la aplicación de algunas cepas bacterianas como biofertilizantes, es crucial comprobar su naturaleza y asegurar su seguridad y eficacia. Este proceso implica realizar estudios exhaustivos para determinar no solo su capacidad para promover el crecimiento vegetal, sino también su inocuidad para las plantas, el suelo, y el medio ambiente.











 nueva página del texto (beta)
nueva página del texto (beta)