ANTECEDENTES
La sepsis se define como la existencia posible o documentada de una infección junto con manifestaciones sistémicas de infección, de acuerdo con la Guía de Recomendaciones Internacionales de la Campaña para Sobrevivir a la Sepsis 2012.1 Por sepsis severa entendemos, en términos generales, el proceso infeccioso que conlleva a disfunción orgánica. En muchas ocasiones el término sepsis y sepsis severa se usan como sinónimos.2
En términos estadísticos, en Estados Unidos, 2% de los pacientes admitidos en un hospital cumplen con el diagnóstico de sepsis severa; de éstos, la mitad son admitidos en la unidad de terapia intensiva, lo que representa 10% de las admisiones en esta unidad. El número de casos por año sobrepasa 75,000, por causas adquiridas en la comunidad e intrahospitalarias.2 A pesar de los cuidados intensivos, la mortalidad de los pacientes con sepsis es de 25 a 30% y con sepsis severa de 40 a 70%.3
El hemocultivo es el estudio de primera línea en pacientes con sospecha de infección; el objetivo principal de los hemocultivos consiste en confirmar bacteremia;3 además permite no sólo establecer la causa infecciosa de un episodio de bacteremia, sino que con base en los resultados, hacer modificaciones en el tratamiento antimicrobiano establecido y otorga un valor pronóstico.4
En las Recomendaciones Internacionales de la Campaña para Sobrevivir a la Sepsis 2012 se recomienda, como parte del abordaje diagnóstico, la obtención de dos hemocultivos (una muestra percutánea y otra mediante cada dispositivo de acceso vascular; esta última muestra en pacientes con catéteres permanentes >48 horas), antes de iniciar el tratamiento antimicrobiano, en un lapso no mayor a 45 minutos.1
No obstante, a pesar de saber que los hemocultivos constituyen un parteaguas en el diagnóstico y tratamiento de pacientes con sepsis, está bien establecido en la bibliografía que la sensibilidad en el diagnóstico de bacteremias es baja, con crecimiento en cultivos <10%;5 en otras palabras, los hemocultivos son positivos en únicamente una tercera parte de los casos.2
La posibilidad de aislar un microorganismo depende de múltiples factores, entre ellos, las características del paciente, el microorganismo causal, la enfermedad de base y sospechada y el método del procesamiento de hemocultivo seleccionado (manual o automatizado).6
La principal causa de sepsis la constituyen los procesos neumónicos, que ocupan más de la mitad de los casos, seguidos de los focos intraabdominales e infecciones del aparato urinario.2 Dos tercios de los casos de sepsis son de origen nosocomial y son más susceptibles los pacientes expuestos a procedimientos invasivos, ya sean quirúrgicos o que requieren vigilancia invasiva mediante catéteres arteriales o venosos, ventilación mecánica invasiva o catéteres vesicales.3 Los catéteres representan el foco de infección en aproximadamente 20% de los casos de sepsis nosocomial.3
El porcentaje de microorganismos aislados depende de las poblaciones de microorganismos que maneja cada hospital e incluso cada unidad del hospital. En un estudio retrospectivo en Estados Unidos, los microorganismos grampositivos y los hongos fueron los responsables del mayor número de casos de sepsis.7 Entre los microorganismos grampositivos, Staphylococcus aureus y Streptococcus pneumoniae son los más aislados; mientras que Escherichia coli, especies de Klebsiella y Pseudomonas aeruginosa están en el grupo de los gramnegativos.2 En un estudio más reciente, de 2009, que incluyó 14,000 pacientes de 75 países, los microorganismos gramnegativos se aislaron en 62%, los grampositivos en 47% y los hongos en 19%.2
En el estudio de Munson y colaboradores, los seis microorganismos aislados con mayor frecuencia incluyeron: Staphylococcus aureus en 20%, Escherichia coli en 14%, estafilococo coagulasa negativo en 13%, enterococo en 12%, Pseudomonas aeruginosa en 6% y Klebsiella pneumoniae en 5%.8 Mientras que en el estudio de Ruiz-Giardin y su grupo, realizado en 2015, los microorganismos más frecuentes fueron: enterobacterias en 47%, Staphylococcus en 15%, Staphylococcus aureus en 8%, infecciones polimicrobianas en 5%, Enterococcus sp en 5%, bacilos gramnegativos no fermentadores en 4%, Streptococcus pneumoniae en 2.5%, Candida sp en 2% y Streptococcus agalactiae, en 1%.9 Más de 300 especies de bacterias se han relacionado con sepsis.3
El propósito de este artículo es determinar la tasa de hemocultivos positivos en el Hospital Ángeles Pedregal de la Ciudad de México, así como describir los microorganismos encontrados con mayor frecuencia y sus resistencias.
MATERIAL Y MÉTODO
Estudio retrospectivo, observacional y descriptivo, en el que se revisaron todos los hemocultivos realizados en el hospital citado, de enero a diciembre de 2015.
Se incluyeron los resultados de hemocultivos y no se excluyó ningún estudio. Se analizaron los resultados positivos, negativos, microorganismos encontrados y antibiograma, que fueron diferentes para los organismos grampositivos y gramnegativos.
El análisis descriptivo se realizó con el programa Statistical Package for the Social Sciences 22 (SPSS 22) y se elaboraron gráficas de barras para mostrar los resultados.
RESULTADOS
De la muestra total (1,598 hemocultivos), 1,035 (65%) eran de pacientes hospitalizados y 563 (35%), de pacientes externos, con edad promedio general de los pacientes de 57.6±20.42 años. Al considerar variable de interés el resultado positivo o negativo de los hemocultivos, 213 (13%) de los participantes en el estudio tuvieron hemocultivos positivos; de éstos, 120 (56%) fueron de pacientes hospitalizados y 93 (44%), de pacientes externos; 69 (34%) pacientes resultaron con organismos grampositivos y 136 (66%) con gramnegativos. Al suponer que nuestra variable de interés se aproxima a una distribución binomial (n,p, debido a que cada paciente representa un ensayo Bernoulli), al ajustar el parámetro p obtuvimos una probabilidad de éxito de 13%.
Entre los hemocultivos positivos para organismos gramnegativos, 92 (43%) resultaron positivos para Escherichia coli, de los que 35 (16%) fueron organismos resistentes (BLEE). El organismo que siguió en frecuencia fue Burkholderia cepacia, con 13 hemocultivos positivos (6%).
Mientras que en los hemocultivos positivos para grampositivos, el organismo más frecuente fue Staphylococcus epidermidis, en 19 hemocultivos (9%), seguido de Staphyloccocus aureus, en 13 hemocultivos (6%) y posteriormente, Enterococcus faecalis, encontrado en 10 hemocultivos (5%). Figura 1
Además de revisar si el hemocultivo era positivo o negativo y del microrganismo que se logró aislar, se realizó una base de datos de los antibiogramas. Se dividieron para organismos grampositivos y para gramnegativos.
Los microrganismos gramnegativos resultaron con resistencia alta a las quinolonas, en especial a ciprofloxacino, en segundo lugar a moxifloxacino y por último a levofloxacino. Otros antibióticos a los que resultaron resistentes en la mayor parte de los cultivos fueron: trimetoprim/sulfametoxazol, ceftriaxona, ampicilina y clindamicina. De modo contrario, mostraron buena sensibilidad a los carbapenémicos, sobre todo a piperacilina/ tazobactam y a amikacina (Figura 2).
TMP/SMX: trimetoprim/sulfametoxazol; PIP/TAZO: piperacilina/tazobactam; AMP/SULB: ampicilina/sulbactam.
Figura 2 Frecuencia de resistencia de acuerdo con el antibiograma de organismos gramnegativos.
En el antibiograma para organismos grampositivos encontramos gran resistencia a las quinolonas, en primer lugar, de nuevo a ciprofloxacino, posteriormente a levofloxacino y por último a moxifloxacino; otros antibióticos a los que resultaron resistentes fueron: penicilina, ampicilina y eritromicina. De modo contrario, mostraron gran sensibilidad a vancomicina, linezolid y tetraciclina (Figura 3).
DISCUSIÓN
En nuestro estudio se encontró una probabilidad de éxito de obtener un resultado positivo en un hemocultivo de 13%, discretamente mayor al reportado en la bibliografía revisada, en la que el crecimiento de microorganismos es menor a 10%.5
En la bibliografía se comenta que el mejor momento para tomar un hemocultivo es 2 horas con 30 minutos antes del pico febril; sin embargo, es muy difícil predecir el momento en el que un paciente tendrá fiebre, por lo que la recomendación es tomar dos hemocultivos en 24 horas, con diferencia de tiempo de 30 a 90 minutos, o al mismo tiempo, si el sitio de punción es diferente, cuando el paciente requiere el inicio del tratamiento antimicrobiano inmediato.10
En pacientes en los que se toman los hemocultivos en pico febril y ya están en tratamiento antimicrobiano, el porcentaje de resultados positivos es muy bajo, por lo que cuestiona la utilidad en este contexto.10
En la evidencia recolectada hasta el momento se establece que el hecho de que el paciente tenga fiebre en el momento de la extracción de sangre no es ni más sensible ni más específico para la existencia de bacteriemia.11 El tiempo para la recolección de las muestras de sangre para hemocultivo es de acuerdo con la conveniencia y debe insistirse en la importancia del volumen adecuado para procesar el hemocultivo, de la obtención de un número adecuado de hemocultivos y de usar una técnica aséptica estricta con la finalidad de evitar falsos positivos por contaminación.11
El porcentaje de hemocultivos negativos fue de 87% y el hecho de que los hemocultivos resultaran negativos fue consecuencia de varias circunstancias, entre las que destacan: contaminación, tiempo de recolección inadecuado, volumen sanguíneo insuficiente o por administración de antimicrobianos previa a la toma de la muestra.12
Por contaminación entendemos el crecimiento de microorganismos en los hemocultivos que no se encuentran en ese momento en la sangre y por ende no son los responsables del cuadro de sepsis. La tasa estimada de contaminación de hemocultivos es de 0.6 a 6%,13 lo que implica no sólo errores en el tratamiento del paciente, sino un incremento en los gastos de la atención médica. Por ello, en la última década se han determinado tres áreas de enfoque como reto en la disminución de contaminación de hemocultivos: detección de contaminantes, prevención y optimización del uso de hemocultivos.13
Las claves para la detección de hemocultivos contaminados son: identificación del microorganismo, número de conjuntos de cultivos positivos, número de botellas positivas de cada conjunto, tiempo de crecimiento, cantidad de crecimiento bacteriano, datos clínicos y de laboratorio y fuente del cultivo.13
La identificación del microorganismo es el predictor más importante para saber si se trata de contaminación del hemocultivo o de una bacteremia real. Ciertos microorganismos han demostrado ser contaminantes; los más frecuentes son: especies de Corynebacterium, especies de Bacillus, Propionibacterium, especies de Micrococcus, S. viridans, enterococos, C. perfingens y estafilococo coagulasa negativo, que en ciertas circunstancias pueden ser causantes reales de cuadros de bacteremia; en particular el caso del estafilococo coagulasa negativo, que puede provocar bacteremia incluso en 26% de pacientes con dispositivos protésicos y catéteres venosos centrales.
De acuerdo con las bases de datos, pocos sugieren contaminación, debido a que únicamente tres hemocultivos resultaron positivos para más de un microorganismo y fueron del mismo paciente; los tres hemocultivos resultaron positivos para Escherichia coli y Proteus mirabilis. Entre las especies conocidas que pueden ser contaminantes y no la causa real de bacteremia, encontramos cuatro hemocultivos positivos. En pacientes previamente sanos tienen poca relevancia, pero en pacientes inmunodeprimidos deben tener mayor importancia clínica y no deben menospreciarse. Entre ellos están: Streptococcus viridans, Staphyloccocus warneri, Enterobacter amnigenus y Peptostreptococcus micros.1
La mayor parte de las bacteremias son provocadas por un microorganismo, pero de 6 a 21% pueden ser polimicrobianas en pacientes de riesgo alto; por lo que un hemocultivo con crecimiento en más de un microorganismo no siempre se trata de contaminación.13
El número de conjunto de hemocultivos positivos también nos ayuda a descartar contaminación; en una bacteremia real, múltiples conjuntos de hemocultivos resultarán positivos y es por esta razón que para incrementar el valor predictivo positivo deben tomarse al menos dos conjuntos de hemocultivos. Otra manera de descartar contaminación es mediante la susceptibilidad antimicrobiana; de tal forma que si la susceptibilidad del microorganismo es idéntica en los diferentes hemocultivos descarta el hecho de que se trate de contaminación.13
El tiempo en el que crece un microorganismo mediante técnicas automatizadas debe considerarse por los médicos cuando ocurre en las primeras 12 horas después de la incubación, pues diversos autores han descrito la relación directa que existe entre el tiempo de crecimiento y la carga bacteriana. Esto explicaría por qué los hemocultivos contaminados tienen un crecimiento más lento: de 3 a 5 días.9,14
También debe considerarse el contexto de los pacientes, porque los que recibieron tratamiento antimicrobiano previo a la toma del hemocultivo también tendrán un retraso en el crecimiento, debido a la reducción de la carga bacteriana. Por esto, ningún agente patógeno debe ignorarse.9 Cuando el paciente no ha recibido tratamiento antimicrobiano y en el hemocultivo se reporta crecimiento en las primeras 14 horas, sugiere que el foco infeccioso es endovascular.9
Desde el decenio de 1990 se ha intentado estandarizar la toma y procesamiento adecuados de los hemocultivos para evitar falsos negativos o positivos. Entre las recomendaciones del Colegio Americano de Médicos y el Instituto de Estándares Clínicos y de Laboratorio de Estados Unidos (CLSI) destacan:
Toma de muestra para hemocultivo
Se prefiere toma por venopunción, debido a que está demostrado que tiene mejor valor predictivo positivo, de 73%, en comparación con las muestras por accesos vascular, 63%;15 además, las muestras arteriales no mejoran el tiempo de diagnóstico y las muestras tomadas por acceso intravascular tienden a reportar tasas elevadas de contaminación.16 De requerir alguna toma de acceso intravascular, debe compararse con una muestra tomada por venopunción.17
Cuando el hemocultivo se toma de un acceso vascular y resulta positivo existen tres posibilidades: bacteremia, colonización del catéter o contaminación.13 La colonización se refiere a los microorganismos que crecen en la superficie del catéter; esta colonización puede o no progresar a bacteremia e incluso 25% de los accesos vasculares están colonizados de manera habitual por estafilococo coagulasa negativo.18
El tiempo de recolección de las muestras en apariencia no está relacionado con el aislamiento de los microorganismos, por lo que está autorizada la recolección de múltiples muestras simultáneas o con un corto periodo entre ellas.19
Deben tomarse, de ser posible, de 2 a 4 conjuntos por venopunción de sitios diferentes, con un volumen mínimo de 20 a 40 mL en adultos, porque está demostrado que un volumen menor de recolección y la toma de varias muestras de un mismo sitio de punción disminuyen la sensibilidad de la prueba y dificultan la interpretación de los resultados.17,20 21 22
Previo a realizar la toma de muestra por venopunción se requiere adecuada antisepsia; se ha evaluado una gran cantidad de antisépticos para la piel y se ha aprobado el uso de tintura de yodo, yodo povidona, peróxido de cloro, alcohol etílico y clorhexidina.19 Algunos expertos recomiendan preparar el sitio de punción con alcohol etílico, permitir que se oree y realizar un segunda preparación utilizando tintura de yodo o yodo povidona 10%.23 Independientemente del antiséptico que se desee usar, es importante considerar el tiempo que requiere para tener el efecto máximo; como ejemplo, la tintura de yodo requiere 30 segundos para su efecto máximo.24
Una vez recolectadas las muestras de hemocultivo, los especímenes deben enviarse al laboratorio lo más pronto posible. Deben permanecer a temperatura ambiente máximo por un par de horas.19
Técnicas de laboratorio para hemocultivo
En casi todas las instituciones, las muestras para hemocultivo entran a un protocolo de incubación en un dispositivo de vigilancia continua. Existen múltiples marcas, pero trabajan de manera similar; las muestras para hemocultivo son incubadas en un periodo establecido por el usuario y tienen una señal acústica o visual en caso de detectar desarrollo de microorganismos.17
Previo a la recolección de sangre se recomienda desinfectar con alcohol la tapa de la botella.25 Las botellas contienen una mezcla de medio de cultivo, anticoagulante y, en muchos casos, resinas y mezclas de carbón vegetal con la finalidad de disminuir el efecto de los antimicrobianos y tóxicos. De manera habitual se realizan combinaciones de medios de cultivo para tratar de aislar un gran número de microorganismos; estas combinaciones incluyen fórmulas que cubren microorganismos aerobios y anaerobios; en casos particulares existen fórmulas para micobacterias y levaduras.17
La incubación se realiza durante cinco días, tiempo suficiente para el aislamiento de una gran cantidad de patógenos; sin embargo, algunos microorganismos, como Legionella, Brucella, Bartonella o Nocardia spp requieren más tiempo de incubación; en particular, las micobacterias spp deben incubarse por cuatro semanas.17
En el Hospital Ángeles Pedregal de la Ciudad de México se cuenta con un protocolo para la toma de hemocultivos, mismo que puede encontrarse en el Manual de prevención y control de infecciones. Protocolo para el cuidado del paciente con catéter vascular central. Cuarta revisión, 2014, que establece dos procedimientos: uno para la toma de hemocultivos por punción periférica y otro para la toma de hemocultivo de acceso vascular.
Toma de muestra periférica con técnica cerrada, utilizando equipo con vacutainer
Los pasos para realizarla son:
Colocarse cubrebocas y gorro.
Seleccionar el sitio de venopunción para la toma.
Lavarse las manos.
Colocarse los guantes.
Colocar torniquete con ayuda de otra persona.
Realizar asepsia de la piel, de preferencia con gluconato de clorhexidina.
Limpiar el tapón de goma de los frascos con toallitas con alcohol, antes de puncionar y esperar a que seque.
Insertar la aguja, sin tocar o palpar el sitio de la venopunción, después de la asepsia.
En adultos, extraer de 8 a 10 mL de sangre y distribuirla en los frascos, previa asepsia del tapón; realizar cambio de aguja para cada frasco. En niños y neonatos extraer 1 a 3 mL por frasco.
Mezclar suavemente los frascos mediante la técnica de inversión.
Membretar los frascos con los datos completos del paciente, especificando la hora y que la toma se realizó por punción.
Colocar un parche en el sitio de punción.
Retirar el equipo y dejar al paciente en posición cómoda.
Realizar la disposición final de los residuos.
Enviar de inmediato la muestra al laboratorio de microbiología. Estas muestras no deben refrigerarse.
Toma de muestra a través de un acceso vascular
Está indicada cuando se sospecha bacteremia relacionada con tratamiento intravascular o cuando no es posible realizar la toma por punción.
Material y equipo
Cubrebocas, gorro y guantes estériles.
Jeringas de 3, 5, 10 y 20 cm.
Agujas de 20x32 G.
Gasa estériles.
Solución antiséptica (alcohol, yodo o gluconato de clorhexidina).
Frascos para hemocultivo.
Campo estéril.
Jeringa de 10 mL con agua inyectable.
Técnica
Colocarse cubrebocas y gorro.
Lavarse las manos.
Colocarse los guantes.
Realizar asepsia antes de acceder a la vía.
Colocar los campos estériles.
Extraer la sangre y distribuirla en los frascos, previa asepsia del tapón y cambio de aguja.
Descontaminar el tapón de goma con alcohol, antes de puncionar y esperar a que seque.
Realizar cambio de aguja entre la punción de un frasco y otro.
Lavar el catéter con solución salina.
Mezclar suavemente los frascos mediante la técnica de inversión.
Membretar los frascos con los datos completos del paciente, especificando la hora de la toma de catéter central.
Retirar el material restante y dejar al paciente en posición cómoda.
Realizar la disposición final de los residuos.
Enviar de inmediato la muestra al laboratorio de microbiología. Estas muestras no deben refrigerarse.
La técnica abierta (sin vacutainer) no es una buena práctica debido a que incrementa el riesgo de contaminación, además de que aumenta costos al procedimiento, puesto que requiere bata y campos estériles.
Aislamiento, identificación y pruebas de susceptibilidad
Al tornarse un hemocultivo positivo por la técnica usada, el siguiente paso es realizar una tinción de Gram; además se realizan resiembras que permitan la identificación del microorganismo y la susceptibilidad en las siguientes 24 a 48 horas.17
Interpretación de hemocultivos positivos
El resultado positivo en un hemocultivo representa, en ciertas ocasiones, un dilema para los médicos debido a que debe correlacionarse con la clínica para intentar determinar si el resultado es secundario a la enfermedad con la que cursa el paciente o constituye un falso positivo por contaminación.
Existen ciertas características que incrementan la validez de nuestros resultados: 1) obtener el mismo microorganismo en dos hemocultivos tomados en dos sitios de venopunción diferentes;172) desarrollo de microorganismos específicos: estafilococo, Streptococcus pneumoniae, Enterobacteriacea, Pseudomonas aeruginosa y Candida albicans. Corynebacterium spp y Propinebacterium spp siempre representan contaminación.17
Métodos de identificación rápida y pruebas de susceptibilidad de hemocultivos positivos
Es evidente la importancia que tiene identificar a la brevedad al microorganismo en pacientes en estado crítico, para tomar decisiones en relación con el tratamiento a iniciar. En los sistemas modernos de incubación para la identificación de la mayor parte de microorganismos en hemocultivos positivos, el tiempo promedio es de 12 a 36 horas, a las que se agregan 48 a 72 horas para la identificación bioquímica y susceptibilidad antimicrobiana; de tal manera que el tiempo promedio de identificación es de 3 a 5 días, lo que significa un retraso en el inicio del tratamiento apropiado.17 Esto ha provocado que se desvíe la atención en búsqueda de nuevas técnicas de identificación más rápida del microorganismo; entre ellos, los métodos moleculares: ensayos de amplificación de ADN y microarreglos de ADN.
CONCLUSIONES
En el Hospital Ángeles Pedregal de la Ciudad de México, los microorganismos aislados con mayor frecuencia fueron gramnegativos, lo que corrobora la teoría de que esto dependerá de las poblaciones de microorganismos de cada hospital. Por mucho, el microorganismo aislado con mayor frecuencia fue Escherichia coli, con 92 hemocultivos positivos (43%), de los que 35 (16%) fueron organismos resistentes (BLEE). El siguiente aislado con más frecuencia fue Burkholderia cepacia, en 13 hemocultivos positivos (6%). También se registraron organismos grampositivos, de los que el más frecuente fue Staphylococcus epidermidis, en 19 hemocultivos (9%), seguido por Staphyloccocus aureus, en 13 hemocultivos (6%) y posteriormente Enterococcus faecalis, encontrado en 10 hemocultivos (5%).
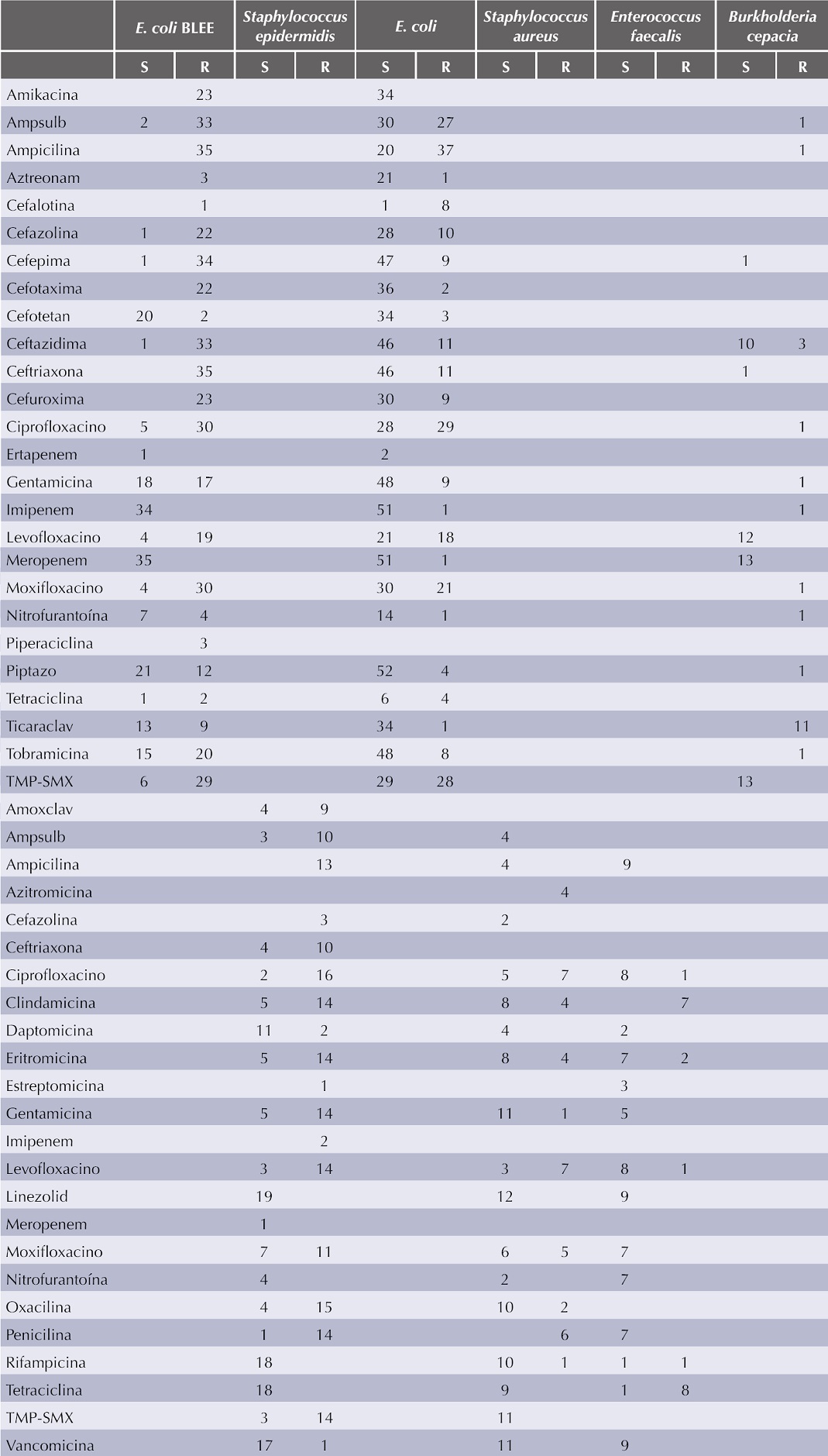
Es relevante la importante resistencia que se mostró a las quinolonas, que son indicadas con mucha frecuencia contra la infección de las vías urinarias, que en la mayor parte de los casos es causada por Escherichia coli. Otros tratamientos comúnmente indicados son trimetoprim-sulfametoxazol y ceftriaxona, que también mostraron alta resistencia. Vale la pena considerar lo anterior, en especial en pacientes que no responden al tratamiento y tener en cuenta que mostraron sensibilidad a otros antibióticos, como carbapenémicos, piperacilina-tazobactam y amikacina. En el Cuadro 1 se expone de manera detallada el número total de hemocultivos sensibles y resistentes a los diferentes antibióticos de los microorganismos aislados más frecuentes.











 nueva página del texto (beta)
nueva página del texto (beta)