Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Salud mental
versión impresa ISSN 0185-3325
Salud Ment vol.34 no.5 México sep./oct. 2011
Artículo original
Estructura del sueño y funciones ejecutivas en niños con depresión
Sleep architecture and executive functions in children with depression
Jesús Antonio Moo Estrella,1 Matilde Valencia Flores,2,3 Rosa Elena Ulloa Flores,4 Feggy Ostrosky Solís,2 Isabel Reyes Lagunes2
1 Universidad Autónoma de Yucatán.
2 Universidad Nacional Autónoma de México.
3 Hospital Nacional de Ciencias Médicas y Nutrición Salvador Zubirán.
4 Hospital Psiquiátrico Infantil Juan N. Navarro.
Correspondencia:
Jesús Moo Estrella.
Facultad de Psicología, Universidad Nacional Autónoma de México, Universidad 3000, Copilco Universidad, Coyoacán, 04360, México, D.F.
E.mail: jmestre@uady.mx
ABSTRACT
Sleep disturbance is a common complaint in depression. However, objective data in relation to the architecture of sleep associated with depression in childhood have been inconsistent. The objective measurement of sleepiness and executive functions is little known in depressive children. The objective of this study was to determine the differences in the sleep architecture, daytime sleepiness and executive functions in children with and without depression.
Method
The participants were 20 children with an average of 10.5 (SD=1.5) years old; nine were girls. Ten met the diagnostic criteria for major depression and ten were control. There were no differences by sex and age between groups with and without depression (p>.05). The instruments were: Schedule for Affective Disorders and Schizophrenia for School–Age Children–Present and Lifetime version (K–SADS–PL), the Children Depression Inventory, and the Battery of Executive Frontal Functions. Also, there were two consecutive nights of polysomnographic recording and Multiple Sleep Latency Test (MSLT).
Results
No differences were found in the architecture of sleep, sleep efficiency was greater than 90% in both groups and the indexes of initiation and sleep maintenance did not show statistically significant differences. There were no differences in daytime sleepiness, sleep onset latency in the MSLT was 22.8 (SD=6.4) minutes for the group with depression and 23.7 (SD=4.1) for the control. The executive functions showed differences in tasks involving: visual–motor and impulse control, working memory and identification of the risk–benefit ratio.
Conclusions
The results suggest that prefrontal structures are more vulnerable to depression than the structures that regulate the circadian and homeostatic sleep.
Key words: Sleep architecture, daytime sleepiness, executive functions, depression, children.
RESUMEN
La alteración del sueño es una queja común en la depresión. Sin embargo, los datos objetivos sobre las alteraciones en la estructura del sueño asociadas a la depresión infantil han sido inconsistentes. Por otro lado, el estudio objetivo de la somnolencia y las funciones ejecutivas en niños con depresión es poco conocida. El objetivo fue conocer si existen diferencias en la estructura del sueño, la somnolencia diurna y las funciones ejecutivas en niños con y sin depresión.
Método
Participaron 20 niños con promedio de 10.5 (DE=1.5) años de edad, de los cuales 45% fueron niñas. Diez cumplieron los criterios diagnósticos de depresión mayor y 10 fueron controles. No hubo diferencias por sexo y edad entre los grupos (p>.05). Los instrumentos fueron: La entrevista Schedule for Affective Disorders and Schizophrenia for School–Age Children–Present and Lifetime version (K–SADS–PL), el Inventario de Depresión Infantil, y la Batería de Funciones Frontales y Ejecutivas. Asimismo, se realizaron dos noches consecutivas de registro polisomnográfico y la Prueba de Latencias Múltiples a Sueño (PLMS).
Resultados
No se encontraron diferencias en la estructura del sueño, la eficiencia del sueño fue mayor al 90% en ambos grupos y no hubo diferencias en los índices de inicio y continuidad del sueño, así como en las diferentes etapas de sueño. Tampoco se obtuvieron diferencias en la somnolencia diurna, la latencia al inicio de sueño en la PLMS fue de 22.8 (DE=6.4) minutos para el grupo con depresión y 23.7 (DE=4.1) para el control. Las funciones ejecutivas mostraron diferencias en tareas que implican: control visomotor y de impulsos, memoria de trabajo e identificación de la relación riesgo–beneficio.
Conclusiones
Los resultados sugieren que las estructuras prefrontales son más vulnerables a la depresión que las estructuras que regulan el ritmo circadiano y homeostático del sueño.
Palabras claves: Estructura del sueño, somnolencia diurna, funciones ejecutivas, depresión, niños.
INTRODUCCIÓN
La alteración del sueño es común en la depresión.1–3 El 70% de los niños con depresión informa de problemas para dormir4 y el porcentaje es mayor (96%) cuando se suma el autoinforme de los niños con el informe de sus padres.5 Por su parte, los datos sobre las alteraciones objetivas del sueño en la depresión infantil, particularmente de la estructura del sueño, han sido inconsistentes. Los cambios en la estructura del sueño han sido descritos con más frecuencia en adultos y adolescentes,6,7 que en niños.8–11 Los cambio en la estructura del sueño asociados a la depresión incluyen: aumento de la latencia del inicio del sueño, aumento de los despertares, reducción de la etapa tres de sueño, disminución de la latencia del sueño de movimiento oculares rápidos (MOR) e incremento de la duración del sueño MOR al principio de la noche,12 así como menor eficiencia del sueño.13,14
Por su parte, durante el día, una queja importante de sueño asociada a la depresión, que se reporta por el impacto negativo sobre el funcionamiento en general del individuo, es la somnolencia diurna excesiva (SDE).15–17 En la población infantil la SDE puede ocurrir en 15% de los niños18 y 32% de los adolescentes.19 Aunque no se han mostrado suficientes datos para determinar la prevalencia de SDE en la depresión infantil, los reportes en adultos indican que puede estar asociada en 50% de los casos.20–22 Asimismo, los estudios de autoinforme indican que existe una correlación entre los síntomas de depresión y la SDE.23 No obstante, los estudios entre la depresión y la SDE empleando medidas objetivas como la Prueba de Latencia Múltiples a Sueño (PLMS) son poco conocidos. Al respecto, los pacientes con depresión generalmente no muestran niveles altos de somnolencia en la PLMS.12
Las funciones cognitivas suelen alterarse en los casos de depresión. Los circuitos involucrados tanto en los procesos afectivos como cognitivos de la depresión incluyen regiones límbicas, temporales, frontales y en especial prefrontales,24–27 las cuales están relacionadas con la percepción, reconocimiento y control de las emociones.28–31 Las funciones cognitivas asociadas a estas regiones que se alteran en los casos de depresión incluyen: la atención, concentración, memoria de trabajo y las funciones ejecutivas.32 Estas últimas involucran funciones relacionadas con la inhibición, solución de problemas y planeación.33
Los datos previos indican que la depresión modifica el sueño, usualmente disminuyendo el tiempo necesario para dormir o generando múltiples despertares. Asimismo, la continua alteración del sueño repercute adversamente sobre el funcionamiento diurno. Las repercusiones pueden manifestarse mediante la SDE, y las alteraciones neuropsicológicas. No obstante, la bibliografía sobre las alteraciones objetivas del sueño asociadas a la depresión infantil, en particular de la estructura del sueño, es limitada.
De la misma forma, la investigación en relación con los efectos de los cambios en la estructura del sueño asociados a la depresión sobre el funcionamiento diurno en niños y adolescentes es escasa. Conocer los efectos de la estructura del sueño sobre el funcionamiento diurno en niños con depresión permite aportar datos para comprender la compleja interacción entre el sueño y la depresión. Bajo este marco, se propuso conocer si existen diferencias en la estructura del sueño y sus efectos sobre la somnolencia diurna y las funciones ejecutivas en niños con depresión.
MÉTODO
Participantes
La muestra estuvo constituida por 20 niños, de los cuales 10 cumplieron los criterios diagnósticos de depresión mayor según el DSM IV TR34 y 10 fueron controles sin alteraciones en el estado de ánimo. Los criterios de inclusión para el grupo con depresión fueron: edad entre 8 y 13 años, puntuación ≥19 en el inventario de depresión infantil,35 primer episodio depresivo y virgen a tratamiento. Se excluyeron niños que presentaron comorbilidad con: trastorno por déficit de atención e hiperactividad (TDAH), trastornos generalizados del desarrollo, psicosis, trastornos neurológicos primarios o abuso de sustancias. Los criterios de inclusión para el grupo control fueron: niños sin diagnóstico de depresión, calificación <19 en el Inventario de Depresión Infantil35 y sin diagnóstico de trastornos neurológicos o psiquiátricos.
De la muestra total, nueve fueron mujeres y 11 hombres, la edad promedio fue 10.5 (DE=1.5) años. El promedio de años de estudio los ubicó en quinto grado de primaria (M=5.1, DE=1.5). No hubo diferencias entre los grupos en la distribución por sexo (X2=1.81, p=.78), promedio de edad (t=.712, p=.48) y años de estudio (t=.149, p=.88).
Instrumentos
Entrevista Schedule for affective disorders and schizophrenia for school–age children–present and lifetime version (K–SADS–PL)
La entrevista K–SADS–PL36 es un instrumento diseñado para evaluar la psicopatología de niños y adolescentes transversal y longitudinalmente. En formato de entrevista semi–estructurada, permite el diagnóstico de los trastornos de acuerdo con los criterios del Manual Diagnóstico y Estadístico de los Trastornos Mentales.34 La entrevista fue realizada a los niños y sus padres. La estructura del K–SADS–PL, comprende una entrevista introductoria para el tamizaje de los posibles trastornos presentes en el niño y cinco suplementos: trastornos afectivos, psicóticos, de ansiedad, conducta, abuso de sustancias y otros trastornos. Para el presente estudio se utilizó la versión al español K–SADS–PL,37 que cuenta con niveles de confiabilidad interevaluador de buenos (k=.76) a excelentes (k=1) para los diferentes diagnósticos.
Inventario de depresión infantil
Se empleó el Inventario de Depresión Infantil35 (CDI, por sus siglas en inglés) para medir la sintomatología de depresión. El CDI es un cuestionario autoaplicable que deben completar los niños y adolescentes anotando la frecuencia con la que han experimentado cada síntoma en las últimas dos semanas. En su estudio de validez se encontró que el punto de corte ≥19 es útil para considerar la presencia de la sintomatología depresiva.35
Batería de funciones frontales y ejecutivas
La batería de Funciones Frontales y Ejecutivas integra quince pruebas validadas en la población mexicana, incluyendo el grupo de edad con el que se trabajó en este estudio.38 Las pruebas se agrupan con base en el criterio anátomo–funcional en las siguientes áreas:
Fronto–orbital–medial (FOM): Laberintos atravesar paredes, Stroop forma A (aciertos, errores, tiempo). Prueba de juego de cartas (porcentaje de cartas de riesgo, puntaje total). Clasificación de cartas (errores de mantenimiento). Stroop forma B (aciertos, errores, tiempo).
Prefrontal dorsolateral (PFDL): Memoria de trabajo; Visoespacial secuencial (aciertos, errores, perseveraciones). Señalamiento autodirigido (aciertos, tiempo, perseveraciones). Ordenamiento alfabético. Resta consecutiva (100–7–7… y 40–3–3…) y Suma consecutiva (1+5+5…). Ejecutivas; Laberintos (errores de planeación y tiempo). Clasificación de cartas (perseveraciones, tiempo y aciertos). Clasificación semántica (total categorías, puntaje total). Fluidez verbal (aciertos, perseveraciones). Torre Hanoi de tres y cuatro aros (número de movimientos y tiempo). Prefrontal anterior (PFA): Clasificación semántica total de categorías abstractas. Refranes (aciertos, tiempo). Metamemoria número de errores negativos y positivos.
La puntuación normalizada de la batería de funciones frontales y ejecutivas tiene una media de 100 y una desviación estándar de 15; la interpretación de la puntuación total, así como de cada área, permite clasificar la ejecución de siguiente manera: normal alto (116 en adelante), normal (85–115), alteraciones leves a moderadas (70–84) y alteraciones severas (menos de 69).
Procedimiento
Los niños con depresión fueron seleccionados en la consulta de primera vez del Hospital Psiquiátrico Infantil Juan N. Navarro (HPIJNN) y del Centro de Servicios Psicológicos (CSP) de la Facultad de Psicología de la Universidad Nacional Autónoma de México. Se les entregó por escrito cartas de participación voluntaria y consentimiento informado a los niños y sus tutores aprobados por el comité de ética del HPIJNN. El grupo control fue obtenido de escuelas primarias previo al tamizaje con el CDI para incluir niños sin síntomas de depresión. El diagnóstico de depresión fue realizado con la entrevista clínica K–SADS–PL.37 Tanto al grupo con depresión como el control siguieron el mismo proceso para los estudios polisomnográficos y la PLMS, las cuales se describen a continuación.
Polisomnografía
Se realizaron dos noches de registro polisomnográfico (PSNG) consecutivas en el Laboratorio de Trastornos del Dormir de la Facultad de Psicología de la Universidad Nacional Autónoma de México, empleando los estándares técnicos internacionales para el registro del sueño.39 Los parámetros empleados fueron: el electroencefalograma (EEG), tomando como referencia el sistema internacional 10–2040 para la colocación de los electrodos, de los cuales se colocaron 16 distribuidos en las regiones: Fp1, Fp2, F7, F3, FZ, F4, F8, T3, C3, Cz, C4, T4, T5, T6, O1 y O2, referidos contralateralmente a mastoides M1 y M2. También se registraron el electrooculograma (EOG) izquierdo y derecho, electromiograma (EMG) de mentón, EMG de tíbiales, electrocardiograma en derivación II (ECG), esfuerzo respiratorio de tórax y abdomen, medición de flujo por cánula nasal y oximetría de pulso. Se usó la unidad de trabajo polisomnógrafo marca Embla N7000 (32 canales de referencia y ocho canales bipolares). Los registros se iniciaron cuando los participantes se fueron a dormir siguiendo su horario habitual y se detuvieron cuando despertaron espontáneamente. La estadificación de las etapas de sueño y calificación de eventos respiratorios y de movimiento se realizó con base en los estándares de la AASM.39
Prueba de latencias múltiples a sueño (PLMS)
Se realizaron cuatro PLMS en el trascurso del día posterior a la segunda noche de registro PSNG. La primera prueba inició dos horas después de concluir el registro PSNG; las siguientes, se realizaron en el trascurso del día manteniendo el intervalo de dos horas entre cada prueba. En cada PLMS, en un cuarto oscuro y sonoamortiguado se indicó al participante ponerse cómodo, con los ojos cerrados y no oponer resistencia a dormirse. Asimismo, en cada prueba se les dio 30 minutos de oportunidad para iniciar el sueño. La latencia a sueño se definió como el tiempo transcurrido entre el momento de apagar las luces y la aparición de la primera época de sueño no MOR. A partir de la primera época de sueño se les permitió dormir 15 minutos antes de concluir la prueba.
La batería de funciones ejecutivas fue aplicada entre la segunda y la tercera PLMS, y el tiempo promedio para responder la batería fue de 45 min. Los datos fueron analizados con el paquete estadístico SPSS V. 18. El nivel alfa mínimo aceptado para cada prueba estadística fue ≤ .05.
RESULTADOS
Los síntomas característicos de acuerdo con la entrevista K–SADS–PL en el grupo con depresión fueron: ideación suicida 70%, irritabilidad y enojo 60% y cambios de apetito o peso 60%; los síntomas: afecto depresivo, alteraciones del sueño, culpa, sensibilidad al rechazo y autodesprecio estuvieron presentes en 30% de los casos.
Estudio polisomnográfico
En el análisis comparativo (t Student) de la estructura del sueño entre el grupo con y sin depresión (cuadro 1) no se encontraron diferencias estadísticamente significativas (p>0.05). Cabe mencionar que en los dos grupos la eficiencia del sueño fue mayor a 90%; la etapa N2 ocupó cerca de la mitad del tiempo (45%), seguida de la etapa N3 (23% en el grupo con depresión y 21.5% en el control) y el sueño MOR (18% en el grupo con depresión y 15% en el control). La latencia al sueño MOR fue mayor a dos horas y no se encontraron diferencias entre los grupos (depresión =128.3 DE =31.6 minutos, controles =131.1 DE =31). No obstante, en el cuadro 1 también se puede ver que en el informe subjetivo no se encontraron diferencias en el número de horas dormidas entre semana, pero sí en el fin de semana, donde el grupo con depresión informó dormir menos que el grupo control. De igual forma, el 56% del grupo con depresión informó de dificultades para iniciar el sueño, es decir, acostarse y no poder dormir y 20% en el grupo control.
Por otra parte, al tomar el subgrupo de casos de depresión que presentaron los síntomas más característicos en esta muestra, los cuales fueron pensamientos recurrentes de muerte e ideación suicida, se encontró que éste, comparado con el que no presentó estos síntomas (U de Mann–Whitney), tuvo más episodios de sueño MOR (M=5.35, DE=1.10 y M=3.83, DE=.76, respectivamente, U=1.50, p=.03), no obstante que la duración de cada episodio de sueño MOR fue menor en el grupo que presentó los síntomas de ideación suicida (M = 25.35, DE=2.95 vs. M=20.82, DE=1.43, U=1.0, p=.017).
PLMS
Respecto a la PLMS, no se encontraron diferencias entre los grupos (p>.05). La latencia al inicio de sueño fue poco más de 20 minutos (depresión M=22.8, DE=6.4 minutos, control M=23.7, DE=4.1) y el tiempo total de sueño para el grupo con depresión fue de 5.1 (DE=4.2) minutos y para el control 6.2 (DE=3.1).
En relación con el sueño MOR, en el grupo con depresión dos participantes niñas presentaron esta etapa, con una latencia promedio de 3.17 (DE=0.47) minutos después de iniciado el sueño y permanecieron en esta etapa 10 (DE=3.53) minutos en promedio. Una niña tuvo sueño MOR sólo en la primera PLMS y la otra en las tres primeras de las cuatro PLMS.
Por su parte, en el grupo control sólo una niña tuvo sueño MOR, que ocurrió en la primera PLMS en un tiempo de 2.5 minutos iniciado el sueño y permaneció 10 minutos en esta etapa.
Funciones ejecutivas
El desempeño de cada grupo en las áreas de las funciones ejecutivas se puede ver en la figura 1. En el análisis comparativo (t de Student) entre el grupo con depresión y el control no se encontraron diferencias en las áreas (p>0.05). Los dos grupos se ubicaron en cada área dentro de una desviación estándar alrededor de la media normativa de la prueba.
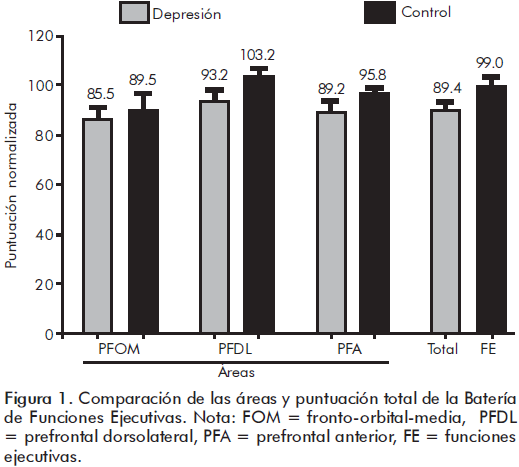
El perfil comparativo entre el grupo con depresión y el control en la prueba de funciones ejecutivas y frontales se puede ver en las figuras 2 y 3. En el área PFDL se encontró una diferencia significativa (t(19) =2.78, p=.013) en la prueba de ordenamiento alfabético (memoria de trabajo), en la cual el grupo con depresión obtuvo la puntuación más baja (M=8.22, DE=2.54 vs. M=11.50, DE=2.60). En el área PFA, se encontró una diferencia significativa (t(17) =3.18, p=.01) en el tiempo empleado para responder la prueba de refranes (control de impulsos), en la cual el grupo con depresión tardó menos tiempo (M=13.66 DE=1.36 vs. M=10.66 DE=.68) de acuerdo con las puntuaciones estandarizadas. Por su parte, en el área PFOM se observaron diferencias (t(17) =2.41, p=.027) en la prueba de laberintos (control visomotor), en la cual el grupo con depresión tuvo la puntación más baja (M=5.44, DE=3.77 vs. M=9.50, DE=3.54), y en la prueba de juego de cartas (t(17) =2.28, p=.036) en la cual el grupo con depresión obtuvo la puntación más alta en la evitación de cartas de riesgo (M=12.67, DE=2.65 vs. M=10, DE=2.45).
Correlación entre la estructura del sueño y las funciones ejecutivas
Se realizaron correlaciones entre las funciones ejecutivas y la estructura del sueño (r de Pearson) en cada grupo. Se encontró que en el grupo con depresión la dimensión FOM obtuvo una correlación positiva tanto en la eficiencia (r=.70, p=.35) como en el tiempo total de sueño (r=.68, p=.46). Por su parte, en el grupo control no se encontraron correlaciones entre la estructura del sueño y las dimensiones de las FE.
DISCUSIÓN
Se confirman hallazgos previos de que no hay diferencias en la estructura del sueño entre el grupo con y sin depresión.11 No obstante, el grupo con depresión informó dormir menos horas el fin de semana. Las diferencias en la medición subjetiva del sueño encontrada en este estudio y reportada en estudios previos3,41 parece que no es perceptible en la medición de la estructura del sueño. Es posible que los cambios electroencefalográficos que explican las quejas subjetivas de sueño en los niños con depresión requieran un análisis más específico como la micro–estructura del sueño. El patrón cíclico alternante del sueño (CAPS),42 el análisis de los husos del sueño43 y el metabolismo cerebral durante el sueño44 pueden ser alternativas que contribuyan a comprender la relación entre el sueño y los síntomas clínicos de la depresión infantil. Por su parte, en el análisis de la PLMS no se encontraron diferencias entre los grupos. Los datos sobre la medición objetiva de la somnolencia diurna en niños con depresión es desconocida. No obstante, nuestros datos al respecto apoyan los resultados encontrados en adultos con depresión en quienes no se han reportado diferencias en la PLMS.
Los procesos neuroquímicos asociados con los trastornos del estado del ánimo incluyen las alteraciones en el funcionamiento de la serotonina, dopamina, noradrenalina, glutamato, GABA, glucocorticoides y péptidos.45 No obstante, el sistema colinérgico cumple un papel central en los casos de depresión con alteraciones del sueño. La sobreactivación de este sistema, además de aumentar los síntomas de la depresión, también modifica la estructura del sueño, acortando la latencia al sueño MOR y aumentando su densidad como se ha reportado en los casos de depresión con la administración de agonistas colinérgicos.46 Estudio posteriores podrían analizar la participación del sistema colinérgico que permita comprender los cambios reportados en la estructura del sueño en adultos pero no en los niños con depresión. Por ejemplo, conocer si los cambios reportados en los adultos puede ser resultado de la hipersensibilidad desarrollada en este sistema, resultado de varios episodios de depresión, como se ha propuesto en el modelo estrés diátesis de la depresión.47
En cuanto a las funciones ejecutivas, los resultados indican que los niños con depresión obtienen puntuaciones diferentes en funciones específicas relacionadas a tareas de: control visomotor y de impulsos, memoria de trabajo e identificar la relación riesgo–beneficio. Las dos primeras tareas concuerdan con los síntomas conductuales de la depresión.
En la depresión infantil, la impulsividad e irritabilidad aparecen con mayor frecuencia que en los adultos.48 De la misma forma, el control visomotor y de impulsos medidos a través de la prueba de laberintos ha mostrado correlaciones significativas en niños y adolescentes,49 pero no en adultos con depresión.50 Probablemente, estas tareas cognitivas sean más sensibles a ser alteradas en los niños con trastornos afectivos, ya que las estructuras neurocognitivas aun no presentan un grado avanzado de desarrollo necesario para ver los síntomas de depresión como típicamente reportan los adultos (culpa, desesperanza, estado de ánimo depresivo, entre otros).48 En la relación riesgo–beneficio los resultados apoyan la hipótesis de que los deprimidos aprenden a identificar las respuestas de riesgo más rápido que los no deprimidos.51,52 Probablemente, porque las personas deprimidas están más atentas a los estímulos negativos.53 Los resultados sugieren que sujetos normales se comportan como si estuvieran esperando el éxito en tanto que los deprimidos como si estuvieran esperando el fracaso; los deprimidos parecen estar más atentos a los castigos.
La alteración en las funciones ejecutivas, pero no en el sueño en la depresión infantil, puede explicarse en función del neurodesarrollo. En este sentido, actualmente se conoce que las áreas prefrontales suelen completar su desarrollo hasta la etapa adulta,54 en tanto que las estructuras cerebrales que regulan el ritmo circadiano y la homeostasis del sueño se consolidan en los primeros años de vida.55,56 Probablemente las estructuras cerebrales que aún no han sido consolidadas en la infancia como las prefrontales sean más vulnerables a la depresión que las estructuras subcorticales que regulan las funciones del sueño, las cuales ya han sido consolidadas. La correlación entre el tiempo total de sueño y la eficiencia del sueño con el área PFOM en el grupo con depresión resalta la importancia del papel que cumple el sueño sobre las funciones cognoscitivas y en particular en los casos con depresión. Por ejemplo, estudios previos han mostrado un incremento de la inteligencia fluida de 6.1 puntos por cada hora de sueño recuperada.57 Estos datos sugieren que incrementar la eficiencia de sueño en los niños con depresión, incrementaría los efectos benéficos relacionados con el funcionamiento cognitivo del tratamiento de base.
Limitaciones
El estudio tiene varias limitaciones que deben ser consideradas. Primero, el tamaño de la muestra, pues el reducido número de casos en cada grupo podría comprometer la potencia estadística de los resultados. Asimismo, no permitió incluir análisis sobre los posibles efectos relacionados con el sexo y edad de los participantes. Estudios posteriores podrían corroborar nuestros datos con muestras más grandes con el fin de obtener un adecuado balance entre los errores tipo I y II. De igual forma, en estudios futuros se recomienda incluir el análisis de acuerdo con la gravedad de los síntomas de depresión y el número de episodios recurrentes; asimismo, incluir otros marcadores del sueño como la potencia del sueño MOR y el análisis espectral de las ondas delta. No obstante las limitaciones, nuestros resultados permiten hacer una primera aproximación del estudio PSNG en niños con diagnóstico de depresión en México.
CONCLUSIONES
No se encontraron cambios en la macroestructura del sueño y la somnolencia en niños con depresión, pero sí en funciones ejecutivas que implican: control visomotor y de impulsos, memoria de trabajo e identificar la relación riesgo–beneficio. El tiempo total de sueño y la eficiencia del sueño se correlacionaron positivamente con la puntuación obtenida en el área PFOM en el grupo con depresión. Los resultados sugieren en primer lugar que las estructuras prefrontales son más vulnerables a la depresión que las estructuras que regulan el ritmo circadiano y homeostático de sueño. En segundo lugar, resaltan la importancia del papel que cumple el sueño sobre las funciones cognoscitivas y en particular en los casos con depresión.
REFERENCIAS
1. Ivanenko A, Crabtree VM, Obrien LM, Gozal D. Sleep complaints and psychiatric symptoms in children evaluated at a pediatric mental health clinic. J Clin Sleep Med 2006;15(1):42–48. [ Links ]
2. Lofthouse N, Gilchrist R, Splaingard M. Mood–related sleep problems in children and adolescents. Child Adolesc Psychiatr Clin N Am 2009;18(4):893–916. [ Links ]
3. Bertocci MA, Dahl RE, Williamson, DE, Iosif AM et al. Subjective sleep complaints in pediatric depression: A controlled study and comparison with EEG measures of sleep and waking. J Am Acad Child Adolesc Psychiatry 2005;44:1158–1166. [ Links ]
4. Liu X, Buysse DJ, Gentzler AL, Kiss E et al. Insomnia and hypersomnia associated with depressive phenomenology and comorbidity in childhood depression. Sleep 2007;30:83–90. [ Links ]
5. Lofthouse N, Fristad M, Splaingard M, Kelleher K. Child reports of sleep problems associated with early–onset bipolar spectrum disorders. J Family Therapy 2007;1:114–123. [ Links ]
6. Rao U, Dahl RE, Ryan ND, Birmaher B et al. Heterogeneity in EEG sleep findings in adolescent depression: unipolar versus bipolar clinical course. J Affective Disorders 2002;70:273–280. [ Links ]
7. Rao U, Chen LA. Characteristics, correlates, and outcomes of childhood and adolescent depressive disorders. Dialogues Clin Neurosci 2009;11:45–62. [ Links ]
8. Ivanenko A, Johnson K. Sleep disturbances in children with psychiatric disorders. Seminars Pediatric Neurology 2008;15:70–78. [ Links ]
9. Forbes E, Michele A. Bertocci M, Alice M et al. Objective sleep in pediatric anxiety disorders and major depressive disorder. J Am Acad Child Adolesc Psychiatry 2008;47:148–155. [ Links ]
10. Arana–Lechuga Y, Núñez–Ortiz R, Terán–Pérez G, Castillo–Montoya C et al. Sleep–EEG patterns of school children suffering from symptoms of depression compared to healthy controls. World J Biol Psychiatry 2008;9: 115–120. [ Links ]
11. Emslie GJ, Armitage R, Weinberg WA, Rush AJ et al. Sleep polysomnography as a predictor of recurrence in children and adolescents with major depressive disorder. Int J Neuropsychopharmacol 2001;4:159–168. [ Links ]
12. American Academy of Sleep Medicine. The international classification of sleep disorders, diagnostic and coding manual. Segunda edición. Westchester: American Academy of Sleep Medicine; 2005. [ Links ]
13. Armitage R, Hoffmann R. Sleep electrophysiology of major depressive disorders. Current Review Mood Anxiety Disorders 1997;1:139–151. [ Links ]
14. Benca R, Obermeyer W, Thisted R, Gillin C. Sleep and psychiatric disorders: A meta–analysis. Arch Gen Psychiatry 1992;49:651–668. [ Links ]
15. Kotagal S. Hypersomnia in children: interface with psychiatric disorders. Child Adolesc Psychiatr Clin N Am 2009;18(4):967–977. [ Links ]
16. Reséndiz M, Valencia Flores M, Santiago V, Castaño V et al. Somnolencia diurna excesiva: causas y medición. Rev Mex Neuroci 2004;5:147–155. [ Links ]
17. Velten–Schurian K, Hautzinger M, Poets CF, Schlarb AA. Association between sleep patterns and daytime functioning in children with insomnia: the contribution of parent–reported frequency of night waking and wake time after sleep onset. Sleep Med 2010;11(3):281–288. [ Links ]
18. Calhoun SL, Vgontzas AN, Fernandez–Mendoza J, Mayes SD et al. Prevalence and risk factors of excessive daytime sleepiness in a community sample of young children: the role of obesity, asthma, anxiety/depression, and sleep. Sleep 2011;34:503–507. [ Links ]
19. Moo Estrella JA, Pérez Benítez H, Solís–Rodríguez F, Arankowsky–Sandoval G. Evaluation of depressive symptoms and sleep alterations in college students. Arch Medical Research 2005;36:393–398. [ Links ]
20. Mume CO. Excessive daytime sleepiness among depressed patients. Libyan J Med 2010;5:4626–doi:10.4176/091024. [ Links ]
21. Laxhmi–Chellappa' S, Fontenele Araújo J. Excessive daytime sleepiness in patients with depressive disorder. Rev Bras Psiquiatr 2006 28(2):126–129. [ Links ]
22. Jiménez Genchi A, Flores Flores G, Zavaleta Ramírez P, Nenclares Portocarrero A. Evaluación de la somnolencia en pacientes deprimidos empleando la Escala de Somnolencia de Epworth. PSIQUIS 2008;17(6):182–190. [ Links ]
23. Fava M. Daytime sleepiness and insomnia as correlates of depression. J Clin Psychiatry 2004;65:27–32. [ Links ]
24. Zalsman G, Oquendo MA, Greenhill L, Goldberg PH et al. Neurobiology of depression in children and adolescents. Child Adolesc Psychiatr Clin N Am 2006;15:843–868. [ Links ]
25. Caetano SC, Fonseca M, Hatch JP, Olvera RL et al. Medial temporal lobe abnormalities in pediatric unipolar depression. Neurosci Lett 2007;427: 142–147. [ Links ]
26. DelBello MP, Adler CM, Strakowski SM. The neurophysiology of childhood and adolescent bipolar disorder. CNS Spectr 2006;11:298–311. [ Links ]
27. Serene JA, Ashtari M, Szeszko PR, Kumra S. Neuroimaging studies of children with serious emotional disturbances: a selective review. Can J Psychiatry. 2007;52:135–145. [ Links ]
28. Scheuerecker J, Frodl T, Koutsouleris N, Zetzsche T et al. Cerebral differences in explicit and implicit emotional processing and fMRI study. Neuropsychobiology 2007;56:32–39. [ Links ]
29. Forbes EE, May CJ, Siegle GJ, Ladouceur CD et al. Reward–related decision–making in pediatric major depressive disorder: an fMRI study. J Child Psychol Psychiatry 2006;47:1031–1040. [ Links ]
30. Pavuluri MN, O'Connor MM, Harral E, Sweeney JA. Affective neural circuitry during facial emotion processing in pediatric bipolar disorder. Biol Psychiatry 2007;62:158–167. [ Links ]
31. Leibenluft E, Rich BA, Vinton DT, Nelson EE et al. Neural circuitry engaged during unsuccessful motor inhibition in pediatric bipolar disorder. Am J Psychiatry 2007;164:52–60. [ Links ]
32. Andrew SD. The neuropsychological basis of childhood psychopathology. Psychology in the Schools 2006;43:503–513. [ Links ]
33. Fossati P, Ergis AM, Allilaire JF. Executive functioning in unipolar depression: a review. Encephale 2002;28:97–107. [ Links ]
34. American Psychiatric Association. Diagnostic criteria from DSM–IV–TR. Washington; 2000. [ Links ]
35. Kovacs M. Inventario de depresión infantil (CDI). Madrid: TEA Ediciones; 2004. [ Links ]
36. Kaufman J, Birmaher B, Brent D, Rao U et al. Schedule for affective disorders and schizophrenia for school–age children–present and lifetime version (K–SADS–PL): initial reliability and validity data. J Am Acad Child Adolesc Psychiatry 1997;36:980–988. [ Links ]
37. Ulloa RE, Ortiz S, Higuera F, Nogales I et al. Estudio de fiabilidad interevaluador de la versión en español de la entrevista Schedule for affective disorders and schizophrenia for school–age children–present and lifetime version (K–SADS–PL). Actas Esp Psiquiatr 2006;34:36–40. [ Links ]
38. Flores J, Ostrosky–Solís F. Batería de funciones frontales y ejecutivas. Rev Neuropsicología, Neuropsiquiatría Neurociencias 2008;8:141–158. [ Links ]
39. American Academy of Sleep Medicine. The AASM Manual for the scoring of sleep and associated events: Rules, terminology and technical specifications. Westchester: Autor; 2007. [ Links ]
40. Jasper HH. The 10–20 electrode system of the international federation. Electroencephalogr Clin Neurophysiol 1958;10:370–375. [ Links ]
41. Moo Estrella JA, Castaño Meneses A, Gil Aldeco D, Rodríguez Pérez V et al. Los hábitos y problemas relacionados con el dormir como factores de riesgo para la depresión infantil. Congreso Nacional para la Investigación y Medicina del Sueño, Jalisco. Veracruz; 2009. [ Links ]
42. Terzano MG, Parrino L, Smerieri A et al. Atlas, rules, and recording techniques for the scoring of cyclic alternating pattern (CAP) in human sleep. Sleep Med 2002;3:187–199. [ Links ]
43. Lopez J, Hoffmann R, Armitage R. Reduced sleep spindle activity in early–onset and elevated risk for depression. J Am Acad Child Adolesc Psychiatry 2010;49:934–943. [ Links ]
44. Brody AL, Saxena S, Mandelkern MA, Fairbanks LA et al. Brain metabolic changes associated with symptom factor improvement in major depressive disorder. Biol Psychiatry 2001;50:171–178. [ Links ]
45. Drevets WC, Price JL, Furey ML. Brain structural and functional abnormalities in mood disorders: implications for neurocircuitry models of depression. Brain Struct Funct 2008;213(1–2):93–118. [ Links ]
46. Gillin JC, Sitaram N, Duncan WC. Muscarinic supersensitivity:a possible model for the sleep disturbance of primary depression? Psychiatry Res 1979;1:17–22. [ Links ]
47. Sadek N, Nemeroff C. Actualización en neurobiología de la depresión. Revista Psiquiatría Uruguay 2000;64:462–485. [ Links ]
48. Ginicola MM. Children's unique experience of depression: Using a developmental approach to predict variation in symptomatology. Child Adolescent Psychiatry Mental Health 2007;1:9–doi:10.1186/1753–2000–1–9. [ Links ]
49. Kerr J, Beer J. Specific and diversive curiosity and depression in junior high school students of divorced and nondivorced parents. Psychol Rep 1992;71:227–231. [ Links ]
50. Gass CS, Ansley J, Boyette S. Emotional correlates of fluency test and maze performance. J Clinical Psychology 1994;50(4):586–590. [ Links ]
51. Smoski MJ, Lynch TR, Rosenthal MZ, Cheavens JS et al. Decision–making and risk aversion among depressive adults. J Behav Ther Exp Psychiatry 2008;39(4):567–576. [ Links ]
52. Garon N, Moore C, Waschbusch DA. Decision making in children with ADHD only, ADHD–anxious/depressed, and control children using a child version of the Iowa Gambling Task. J Atten Disord 2006;9:607–619. [ Links ]
53. Elliott R, Sahakian BJ, Michael A, Paykel ES et al. Abnormal neural response to feedback on planning and guessing tasks in patients with unipolar depression. Psychological Medicine 1998;28:559–571. [ Links ]
54. Zelazo PD, Craik FIM, Booth L. Executive function across the life span. Acta Psychologica 2005;115:167–183. [ Links ]
55. Huang W, Ramsey KM, Marcheva B, Bass J. Circadian rhythms, sleep, and metabolism. J Clin Invest 2011;121:2133–2141. [ Links ]
56. Franken P, Dijk DJ. Circadian clock genes and sleep homeostasis. Eur J Neurosci 2009;29:1820–1829. [ Links ]
57. Geiger A, Achermann P, Jenni OG. Association between sleep duration and intelligence scores in healthy children. Dev Psychol 2010;46:949–954. [ Links ]
Nota
Editores invitados: Rosa Elena Ulloa Flores, Francisco de la Peña Olvera, Lino Palacios Cruz.














