Introducción
Tamaulipas es el principal productor de sorgo en México, con el 60 % del total nacional. En el 2023 se cultivaron 806 mil hectáreas con una producción de 2.3 millones de toneladas y un rendimiento promedio de 2.8 t ha -1. La productividad del cultivo es baja pues 73 % del sorgo en Tamaulipas se cultiva en condiciones de temporal, con promedios del rendimiento de 2.6 t ha -1, lejos del rendimiento del sorgo (más de 6 t ha -1) cultivado con riego en otras regiones de México (SIAP, 2024). Bajo las condiciones del temporal tamaulipeco ocurren frecuentemente períodos intermitentes de sequía y de altas temperaturas, que afectan el crecimiento y desarrollo del cultivo, así como el rendimiento y calidad de la producción. El estrés ambiental incrementa la incidencia y daños por enfermedades y plagas (Díaz-Franco y Montes-García, 2008).
Una de las enfermedades más importantes del sorgo en Tamaulipas es la pudrición carbonosa del tallo, cuyo agente causal es el hongo Macrophomina phaseolina. El hongo infecta principalmente tallos y raíces de la planta y causa el síntoma típico de ‘pudrición carbonosa’ o ‘tizón cenizo’ debido a la producción de microesclerocios y micelio (Little et al., 2023). La preponderancia de la enfermedad y de las condiciones favorables para su desarrollo ha generado el interés en la producción de germoplasma de sorgo resistente tanto al estrés ambiental (sequía y altas temperaturas) como a la pudrición carbonosa, con el objetivo de incrementar la producción en la región (Williams-Alanís et al., 2009; 2021; Montes-García et al., 2020; 2021). Considerando que la mayor proporción de la superficie sembrada con sorgo se cultiva en condiciones de temporal y que los insumos que se utilizan para su producción en estas condiciones son escasos (Alejandro-Allende et al., 2020), es conveniente desarrollar, evaluar y proponer alternativas económicas, no contaminantes y efectivas en el control de las enfermedades y plagas del cultivo
Las estrategias de biocontrol de enfermedades como opción de manejo están disponibles, de manera que si ofrecen resultados favorables podrían extrapolarse a la producción comercial del sorgo en Tamaulipas (Ángeles-Núñez et al., 2018). Las opciones que se han manejado en el caso de M. phaseolina, son diversas (Márquez et al., 2021; Rajput et al., 2023). Una de ellas, quizá la más utilizada en sorgo y otros cultivos, son los hongos del género Trichoderma spp. que utilizan mecanismos variados como antibiosis, micoparasitismo, competencia, promoción del crecimiento vegetal, mejoramiento de la tolerancia del hospedante al estrés abiótico y la activación del sistema de defensa contra patógenos como M. phaseolina. Además, producen compuestos volátiles y no volátiles y/o sideróforos para desarrollar su biocontrol (Shahriar et al., 2022, Rubayet y Bhuiyan, 2023; Rajpu et al., 2023). Martínez-Salgado et al. (2021) reportaron que T. koningiopsis (T-K11) mostró la mayor tasa de crecimiento y de inhibición del crecimiento de M. phaseolina (71%) in vitro; así como la mayor producción de cacahuate (Arachis hypogaea) (1.60±0.01 t ha−1) y menores daños por pudrición carbonosa en campo. Arispe-Vázquez et al. (2024) observaron la mayor inhibición del crecimiento de M. pseudophaseolina por cepas de T. reesei en plantas de chile cultivadas en invernadero.
Otra opción, cuya aplicación en el manejo de M. phaseolina no se ha reportado, es el hongo Aspergillus flavus. Aunque es conocido que el hongo produce aflatoxinas con potencial carcinogénico en humanos y afecta la calidad y la productividad de diversos cultivos, en contraparte se reportan aislamientos que de manera natural no producen aflatoxinas (atoxigénicos) y que, además, compiten por espacio y nutrimentos con los aislamientos productores de aflatoxinas durante el desarrollo de los cultivos, reduciendo la contaminación por aflatoxinas. La cepa AF36 de A. flavus es una estrategia de control biológico por exclusión competitiva de hongos aflatoxigénicos en algodonero (Cotty y Bayman, 1993). King et al. (2011) y Rangel-Muñoz et al. (2022) indican que AF36 controla la infección por hongos toxígenos en algodonero (Gossypium hirsutum), maíz (Zea mays) o cacahuate. También en frutales como pistache (Pistacia vera) y almendro de España (Prunus dulcis), la cepa AF36 de A. flavus reduce significativamente la contaminación por aflatoxinas (García-López et al., 2018, 2024).
Finalmente, está la opción de los agentes químicos detoxificantes que suprimen o reducen la adsorción, incrementan la excreción o modifican el modo de acción de sustancias como las micotoxinas, debido a que éstas se adhieren al compuesto por adsorción química. Un caso sobresaliente son los aluminosilicatos de calcio y sodio (HSCAS), usados con éxito en algunos cultivos (Habschied et al., 2021; Hassan y Afzal, 2022; Aloui et al., 2023). La aplicación foliar o al suelo de silicatos de sodio reduce la infección por M. phaseolina en soya (Rajput et al., 2023). Tampoco hay reportes previos del uso de HSCAS en el cultivo del sorgo para el manejo de M. phaseolina. El objetivo de este trabajo fue evaluar el efecto de tratamientos biológicos (hongos T. koningiopsis cepa T808 y A. flavus cepa AF36; y el agente quelante aluminosilicato de calcio y potasio, Kuali®), en el desarrollo de M. phaseolina en sorgo cultivado en invernadero, bajo condiciones de déficit hídrico.
Híbridos de sorgo. El estudio incluyó dos híbridos de sorgo, el P-8282 de Pioneer® y el RB-Patrón® del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP). P-8282 se distingue por su adaptación al noreste de México, su tolerancia al acame y a la sequía (Pioneer-Dupont, 2017); RB-Patrón es tolerante a las altas temperaturas y sequía, así como a la infección por M. phaseolina en el norte de Tamaulipas (Williams- Alanís et al., 2004).
Tratamientos biológicos. En el estudio se evaluaron tres estrategias de biocontrol: 1) la cepa AF36 de A. flavus (Syngenta®; Arizona, EUA); 2) la cepa T808 de T. koningiopsis (Hernández-Mendoza et al., 2011) y 3) el agente quelante de aflatoxinas Kuali (Azul Natural®; Durango, México. https://azulnatural.net/products/), a base de aluminosilicato de calcio y potasio. En todos los casos, la forma de aplicación y las dosis usadas se basaron en las instrucciones de los fabricantes. Tanto T808 como AF36 se inocularon al momento de la siembra del sorgo, mientras que Kuali se aplicó al follaje de las plantas a los 15 días después de la siembra (dds) (solución de Kuali/aceite mineral estéril 5:1 p/v).
Inoculación de M. phaseolina. El inóculo de M. phaseolina se preparó a partir de la cepa HMP5, aislada de soya (Glycine max) en Altamira, México y con alta virulencia en plantas de frijol (Phaseolus vulgaris), sorgo (Sorghum bicolor) y soya (Glycine max) (Mayek- Pérez et al., 2002). La cepa se creció en medio Papa-Dextrosa-Agar (PDA) a 30 °C durante siete días en oscuridad. Los microesclerocios y micelio se ‘rasparon’ de las placas completamente colonizadas y se preparó una solución en agua desionizada estéril. A los tratamientos correspondientes se aplicó una concentración de 105 unidades formadoras de colonia por unidad experimental al momento de la siembra del sorgo, junto a las semillas (De la Peña-Devesa et al., 2009).
Niveles de humedad. Los tratamientos se sembraron bajo dos condiciones de humedad: riego y déficit hídrico. En riego, la humedad se mantuvo a capacidad de campo desde la siembra hasta concluir los experimentos; en déficit hídrico el riego se suspendió a los 25dds hasta alcanzar el punto de marchitez permanente. Las plantas se mantuvieron en esa condición durante tres días y se aplicó un riego de recuperación a capacidad de campo. En el resto de los experimentos, las plantas se mantuvieron bajo condiciones de riego normal (Mayek-Pérez et al., 2002).
Las semillas de los híbridos de sorgo se desinfestaron en una solución de hipoclorito de sodio 1 % durante 2.5 min. Las semillas se enjuagaron con agua desionizada estéril y se secaron con papel estéril; luego, se sembraron en charolas de plástico de 36 cavidades que contenían sustrato estéril (Topsoil®; Marisville, EUA) a razón de seis semillas por cavidad. Los 20 tratamientos evaluados resultaron de la combinación de los factores y niveles considerados: dos híbridos de sorgo x dos niveles de humedad (riego, déficit hídrico) x 5 tratamientos de inoculación (tres de biocontrol: T808, AF35, Kuali más dos testigos: los híbridos sin inoculación con ningún agente de control y los híbridos inoculados con HMP5). Los tratamientos presentaron un arreglo factorial en parcelas subdivididas y se aleatorizaron en un diseño experimental completamente al azar con seis repeticiones. Las parcelas grandes correspondieron a los híbridos de sorgo, las medianas a los niveles de humedad y las chicas a los tratamientos de biocontrol. La unidad experimental fue una cavidad con seis semillas. El experimento se repitió dos veces.
Altura de planta. La variable se midió a los 10, 16, 22, 28, 34 y 40 dds en tres plantas de cada unidad experimental; se utilizó una regla y se midió la altura a partir de la base de las plantas en el suelo y hasta el ápice de las hojas.
Severidad de la pudrición carbonosa. En las mismas fechas de evaluación de la altura de planta se cuantificó la severidad de la pudrición carbonosa en las plantas de una unidad experimental por tratamiento. Las plantas se lavaron previamente con agua desionizada estéril. La severidad se evaluó con la escala de Abawi y Pastor-Corrales (1990) que incluye nueve valores (del 1 al 9, donde 1=sin síntomas visibles y 9=75 % o más de los tejidos con lesiones, decaimiento de la raíz y crecimiento extenso del hongo).
Peso seco de biomasa. Las plantas a las que se evaluó la severidad de M. phaseolina se utilizaron para estimar el peso seco de la raíz, de la parte aérea y total. Las plantas se colocaron en sobres de papel y se secaron en un horno de aire forzado a 60 °C durante cinco días (FX5, Shel-Lab; Cornelius, OR, EUA). Posteriormente, se determinó el peso seco en una balanza analítica (BP 2100S, Sartorius; Göttingen, Alemania).
Los datos de las variables medidas se sujetaron al análisis de la varianza (ANVA). En los casos que se detectaron diferencias significativas, se calcularon los valores de la diferencia mínima significativa honesta (DMSH, p=0.05) de Tukey para la comparación de promedios entre tratamientos (Martínez-Garza, 1988). El análisis estadístico se realizó con el programa SAS versión 9.0 para Windows (SAS Institute; Cary, NC, EUA; https://www.sas.com/es_mx/home.html.
Experimento 1. El ANVA detectó diferencias significativas (p<0.05) entre niveles de inoculación para todas las variables medidas; entre híbridos y niveles de humedad sólo para altura de planta en la primer evaluación, mientras que para la sexta evaluación se detectaron diferencias significativas (p<0.05) entre híbridos, niveles de humedad y de inoculación para severidad de pudrición carbonosa; entre híbridos para altura de planta y peso seco de tallo; entre niveles de humedad para peso seco de tallo y de raíz. Las interacciones simples y triples no mostraron diferencias significativas (p>0.05) en la primera evaluación para ninguna variable, pero si se detectaron diferencias significativas en todas las variables medidas para la mayoría de las interacciones en la sexta evaluación (datos no incluidos).
En la primera evaluación el híbrido P-8282 exhibió mayor altura de planta (5.6 cm), mientras que la menor altura de planta se detectó en condiciones de riego (5.1 cm). Entre tratamientos biológicos el testigo absoluto no registró daños por M. phaseolina (1.0) y también exhibió la mayor altura de planta (5.9 cm). La aplicación de T808 mostró el menor peso seco de tallo (16 mg), mientras que el tratamiento con M. phaseolina exhibió mayor peso seco de raíz (30 mg). Para la sexta evaluación, RB-Patrón presentó los mayores daños por pudrición carbonosa (6.0), que se tradujo en el menor crecimiento de las plantas (menores promedios en altura de planta, peso seco de tallo y peso seco de raíz). La sequía incrementó el daño por pudrición carbonosa y redujo, además, el crecimiento del sorgo en cuanto a la altura de planta, peso seco de tallo y de raíz. Por su parte, la cepa T808 redujo la severidad de la pudrición carbonosa hasta 4.6, mientras que los otros tratamientos biológicos exhibieron valores de severidad mayores a 6.0 (Cuadro 1).
La interacción triple (híbridos x humedad x tratamientos biológicos) mostró una amplia variación en respuestas, pues la severidad de M. phaseolina pasó de un valor de 1 a 9 y, por ello, se redujo la acumulación de biomasa seca total, pues los valores no fueron mayores de 200 mg por unidad experimental. Los tratamientos biológicos con menores daños por pudrición carbonosa fueron Kuali en RB-Patrón bajo riego y T808 en RB-Patrón bajo déficit de humedad (Figura 1A).
Experimento 2. El ANVA detectó diferencias significativas (p<0.05) entre híbridos para las variables severidad de M. phaseolina, altura de planta y peso seco de tallo (primera evaluación); para los pesos secos de tallo y de raíz (sexta evaluación). Entre niveles de humedad hubo diferencias significativas (p<0.05) sólo para la severidad de la pudrición carbonosa (primera evaluación); mientras que en la sexta evaluación se detectaron diferencias (p<0.05) en todas las variables medidas. Entre tratamientos biológicos se observaron diferencias significativas (p<0.05) para severidad de pudrición carbonosa en ambas fechas de evaluación y para altura de planta sólo en la primera medición de la variable. Las interacciones simples y triples no mostraron diferencias significativas (p>0.05) en la primera evaluación en ninguna variable, pero si se detectaron diferencias significativas (p<0.05) en todas las variables medidas para todas las interacciones, en la sexta medición de variables (datos no incluidos).
El híbrido RB-Patrón mostró mayor severidad de daño (1.4) en comparación con P- 8282 que exhibió un valor de 1; sin embargo, también presentó los mayores promedios en altura de planta y peso seco de tallo en la primera medición y los menores pesos secos de tallo y de raíz en la sexta evaluación. Los mayores daños por pudrición carbonosa se observaron en plantas bajo déficit hídrico en comparación con plantas bajo riego: 1.4 vs 1.0 en la primera medición y 2.8 vs 2.0 en la segunda, respectivamente. El déficit hídrico redujo la altura de planta en 10 % y la acumulación de biomasa al final del experimento entre 35 y 40 %. En la primera medición, el testigo no mostró daños por M. phaseolina pero si la mayor altura de planta. En contraste, en la sexta evaluación los menores daños por pudrición carbonosa correspondieron a T808 (2.2), mientras que los otros tratamientos biológicos presentaron valores de severidad mayores a 2.7 (Cuadro 2). La interacción triple (híbridos x humedad x tratamientos biológicos) mostró menor variación en la respuesta a M. phaseolina, con valores de severidad de 1 a 4; por ello, la acumulación de biomasa seca total fue más alta que la observada en el experimento 1 (valores de hasta 1800 mg por unidad experimental). Los tratamientos biológicos con los menores daños por pudrición carbonosa fueron Kuali, AF36 y T808 en el híbrido P-8282 con déficit hídrico; así como T. koningiopsis cepa T808 en RB-Patrón con riego (Figura 1B).
Cuadro 1 Comparación de medias de los efectos principales para severidad de daño por M. phaseolina, altura de planta y acumulación de biomasa en sorgo. Primera y sexta evaluaciones en el experimento 1.
| Tratamiento | Primera evaluación (10 dds) | Sexta evaluación (40 dds) | ||||||
|---|---|---|---|---|---|---|---|---|
| Severidad de daño | Altura planta (cm) | Peso seco tallo (mg) | Peso seco raíz (mg) | Severidad de daño | Altura planta (cm) | Peso seco tallo (mg) | Peso seco raíz (mg) | |
| Híbridos | ||||||||
| Pioneer 8282 | 1.0 | 5.6 | 19 | 18 | 4.6 | 7.3 | 78 | 60 |
| RB-Patrón | 1.3 | 5.1 | 20 | 20 | 6.0 | 6.8 | 66 | 54 |
| DMS | 0.3NS | 0.3** | 2NS | 2NS | 1.3** | 0.4** | 8** | 11NS |
| Humedad | ||||||||
| Riego | 1.0 | 5.1 | 18 | 20 | 2.6 | 7.2 | 84 | 63 |
| Déficit hídrico | 1.3 | 5.6 | 20 | 20 | 8.0 | 6.9 | 59 | 50 |
| DMS | 0.3NS | 0.3** | 2NS | 2NS | 1.3** | 0.4NS | 8** | 11** |
| Inoculación | ||||||||
| *M. phaseolina* | 1.0 | 4.9 | 22 | 30 | 6.9 | 6.9 | 62 | 50 |
| AF36 | 2.1 | 5.3 | 21 | 2 | 6.7 | 7.1 | 82 | 56 |
| T808 | 1.2 | 4.8 | 16 | 19 | 4.2 | 6.7 | 68 | 58 |
| Kuali | 1.0 | 5.5 | 20 | 18 | 7.9 | 7.1 | 71 | 67 |
| Testigo | 1.0 | 5.9 | 19 | 15 | 1 | 7.4 | 70 | 51 |
| DMS | 0.6** | 0.7** | 4** | 4** | 2.6** | 0.8NS | 18NS | 25 NS |
Cuadro 2 Comparación de medias de los efectos principales para severidad de daño por M. phaseolina, altura de planta y acumulación de biomasa en sorgo. Primer y sexto evaluaciones en el experimento 2.
| Tratamiento | Primera evaluación (10 dds) | Sexta evaluación (40 dds) | ||||||
|---|---|---|---|---|---|---|---|---|
| Severidad de daño | Altura planta (cm) | Peso seco tallo (mg) | Peso seco raíz (mg) | Severidad de daño | Altura planta (cm) | Peso seco tallo (mg) | Peso seco raíz (mg) | |
| Híbridos | ||||||||
| Pioneer 8282 | 1.0 | 10.6 | 105 | 14 | 2.3 | 17.3 | 720 | 360 |
| RB-Patrón | 1.4 | 11.4 | 88 | 15 | 2.5 | 17.2 | 586 | 223 |
| DMS | 0.3** | 0.3** | 10** | 2NS | 0.4NS | 0.6NS | 77** | 43** |
| Humedad | ||||||||
| Riego | 1.0 | 11.1 | 103 | 15 | 2.0 | 18.1 | 801 | 367 |
| Déficit hídrico | 1.4 | 10.9 | 90 | 13 | 2.8 | 16.5 | 513 | 221 |
| DMS | 0.3** | 0.3NS | 10NS | 2NS | 0.4** | 0.6** | 77** | 43** |
| Inoculación | ||||||||
| *M. phaseolina* | 1.4 | 10.9 | 99 | 15 | 3.0 | 16.5 | 550 | 313 |
| AF36 | 1.8 | 10.6 | 92 | 13 | 2.7 | 17.7 | 742 | 315 |
| T808 | 1.6 | 10.7 | 88 | 15 | 2.2 | 16.8 | 634 | 238 |
| Kuali | 1.2 | 11.1 | 105 | 15 | 2.8 | 16.7 | 629 | 288 |
| Testigo | 1.0 | 11.6 | 97 | 15 | 1 | 18.0 | 700 | 335 |
| DMS | 0.4** | 0.7** | 25NS | 4NS | 0.7** | 1.6NS | 195NS | 109NS |
En ambos experimentos se observó que los mayores daños por pudrición carbonosa ocurrieron en el híbrido RB-Patrón, particularmente cuando se cultivó en condiciones de deficiencia hídrica; esto derivó en la menor acumulación de biomasa seca. Ambas condiciones de estrés, solas o combinadas (hongo/déficit de humedad), afectan negativamente el crecimiento y la acumulación de biomasa seca en los híbridos de sorgo (Perumal et al., 2020; Marquez et al., 2021; Little et al., 2023), particularmente durante la fase vegetativa del desarrollo de la especie, que fue el periodo que se estudió en este trabajo. La sequía reduce el crecimiento de la parte aérea y de las raíces del sorgo, así como la acumulación de biomasa seca debido a la reducción de la extensibilidad de la pared y la turgencia celular (Queiroz et al. 2019; Abreha et al., 2022).
Severidad de m. Phaseolina
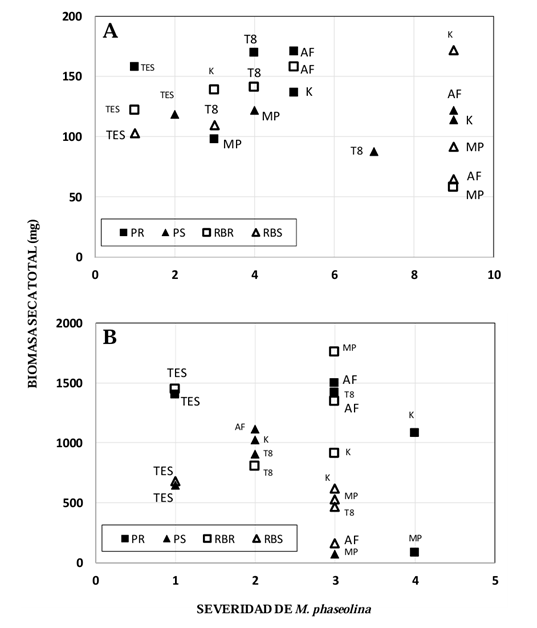
Figura 1 Relación entre la severidad de la pudrición carbonosa y la biomasa seca total acumulada en la sexta evaluación en sorgo cultivado en invernadero. (A) Experimento 1, (B) Experimento 2. PR=Pioneer 8282/Riego; PS=Pioneer 8282/Déficit hídrico; RBR=RB Patrón/Riego; RBS=RB Patrón/Déficit hídrico.
En general, el tratamiento con T. koningiopsis cepa 808 tuvo los mejores resultados de control de M. phaseolina en términos de los menores daños por pudrición carbonosa y el mayor crecimiento y acumulación de biomasa seca. Las combinaciones de Kuali con RB- Patrón bajo riego y T808 con RB-Patrón bajo déficit de humedad, aunque con acumulación de biomasa intermedia (experimento 1) también ofrecieron resultados promisorios; mientras que en el experimento 2 las mejores respuestas de biocontrol se obtuvieron con Kuali, AF36 o T808 en combinación con P-8282 bajo déficit hídrico y T808 con RB-Patrón bajo riego. Además, ciertas combinaciones específicas de tratamientos de biocontrol (T. koningiopsis, A. flavus atoxigénica, Kuali) exhibieron porcentajes de reducción de la severidad de la pudrición carbonosa en sorgo, así como la reducción de los efectos en el crecimiento y acumulación de biomasa seca.
Los reportes del efecto de cepas de T. harzianum, T. viride, T. asperellum o T. koningiopsis en la supresión del crecimiento in vitro y de los daños causados en campo por diversos hongos fitopatógenos, entre ellos M. phaseolina; así como en diversos cultivos, entre ellos en sorgo, han sido constantes y con resultados similares (Yassin et al., 2021). Aislamientos del género Trichoderma y, en específico, cepas de T. koningiopsis han mostrado efectos positivos en sorgo, tanto mejorando su respuesta al estrés abiótico como en la defensa contra la infección de patógenos como M. phaseolina (Bhutada y Shinde, 2023; Kubiak et al., 2023; Rubayet y Bhuiyan, 2023; Rajpu et al., 2023). Por ejemplo, en cacahuate cultivado en Puebla, México Martínez-Salgado et al. (2021) reportaron que K. koningiopsis presentó la mayor tasa de crecimiento y la mayor inhibición del crecimiento de M. phaseolina (71 %) in vitro; así como la mayor producción de cacahuate (1.60±0.01 t ha−1) y los menores daños por pudrición carbonosa en campo. Ruangwong et al. (2021) señalaron que T. koningiopsis contiene azetidina, 2-feniletanol y etil-hexadecanoato, compuestos asociados con la antibiosis y la supresión del crecimiento micelial de M. phaseolina reportados por Martínez-Salgado et al. (2021).
Aunque autores como Quiroz et al. (2008) observaron que cepas de Aspergillus sp. podrían constituirse como una opción en el control biológico de hongos como M. phaseolina, no recomendaron su aplicación en campo dado que se conoce la capacidad productora de aflatoxinas y de otras micotoxinas en las especies del género. Sin embargo, los resultados de Almeyda-León et al. (2020) son promisorios pues, a partir de 312 aislados obtenidos de suelos cultivados y no cultivados, identificaron 212 morfotipos fúngicos y de ellos tres morfotipos inhibieron el crecimiento de M. phaseolina en más del 60 %. Dos de esos morfotipos se identificaron como Aspergillus sp. y el otro como Penicillium sp. Los resultados demostraron que naturalmente ocurren cepas de hongos con una potencial actividad antagónica contra M. phaseolina. Entonces, los hongos del género Aspergillus nativos de suelos cultivados o no cultivados de México son potencialmente aptos para aplicarse en estrategias de control biológico de M. phaseolina en sorgo, solo que se debe asegurar la condición atoxigénica de las cepas con potencial para inhibir el desarrollo de la pudrición carbonosa en sorgo cultivado en el noreste de México.
En el caso del agente secuestrante fabricado con base en aluminosilicato de calcio y potasio (HSCAS), aunque en menor medida, también mostró resultados que permiten sugerir la necesidad de evaluaciones posteriores en campo que permitan definir si tiene posibilidades de usarse en la producción comercial de sorgo en el norte de Tamaulipas. Los aluminosilicatos se han evaluado y aplicado, con éxito, en el manejo de las aflatoxicosis derivadas del hongo A. flavus, particularmente en la industria de los alimentos balanceados que utilizan granos de sorgo y de maíz que, de estar contaminados con aflatoxinas, serían un importante problema de salud para el ganado y, posteriormente, para el consumidor de los productos de ese ganado, como la carne y la leche (Peng et al., 2018).
El siguiente paso es extender estas evaluaciones al ciclo biológico completo del cultivo, en varios sitios experimentales en el norte de Tamaulipas y corroborar lo observado en condiciones controladas. Los resultados son promisorios en ese sentido, pues este es el primer reporte que cuyos resultados indican que, tanto la cepa AF36 de A. flavus como el agente secuestrante Kuali muestran efectos positivos en el biocontrol de M. phaseolina en el patosistema que integra con el sorgo en condiciones de temporal.
El reto en el corto plazo es definir el modo de acción los microorganismos antagonistas o del agente secuestrante en el caso de M. phaseolina en sorgo, lo que permitirá avanzar en el desarrollo de biopesticidas potenciales a partir del establecimiento de las interacciones en sistemas dinámicos (agente de biocontrol-fitopatógeno, agente de biocontrol-planta o agente de biocontrol-planta-fitopatógeno). Además de comprobar las propiedades antagónicas y fitosanitarias del hongo, deberá evaluarse su toxicidad en los humanos y al medio ambiente. También, es importante poner atención en los métodos de tratamiento o aplicación tanto a suelo, como a planta o semillas; la formulación y la fermentación en gran escala de los biopesticidas. Una limitante es transferir efectivamente los resultados del laboratorio al campo, aunque el reto más importante para desarrollar productos biológicos es el generar conciencia pública sobre la eficacia y seguridad de los bioproductos basados en Trichoderma sp. (Navi y Yang, 2020; Kubiak et al., 2023; Kumar et al., 2023).
El híbrido de sorgo RB-Patrón mostró los mayores daños por pudrición carbonosa en comparación con P-8282, así como el menor crecimiento (altura de planta: 10 %) y acumulación de biomasa seca (entre 35-40 %). El déficit hídrico incrementa la severidad de la pudrición carbonosa y reduce el crecimiento del sorgo La cepa T808 de T. koningiopsis redujo la severidad de la pudrición carbonosa (valor del 4.6) mientras los otros tratamientos biológicos exhibieron valores de severidad mayores a 6.0.
La interacción triple (híbridos x humedad x tratamientos biológicos) mostró resultados variables, pues los tratamientos biológicos con los menores daños por pudrición carbonosa fueron Kuali, AF36 y T808 en el híbrido P-8282 con déficit hídrico; así como T808 en RB- Patrón con riego. Estos tratamientos deberán evaluarse en condiciones de campo para confirmar la viabilidad de su aplicación en la producción comercial de sorgo en el norte de Tamaulipas.











 texto en
texto en 


