Introducción
Los cultivos de hortalizas en áreas tropicales y subtropicales dependen en gran medida del control adecuado de nematodos agalladores (Sikora y Fernández, 2005; Ulloa et al., 20l6), especialmente contra Meloidogyne spp. los cuales son difícil de controlar, debido a su amplia gama de hospedantes, altas tasas de reproducción y su tipo de parasitismo (Manzanilla et al., 2004; Guerrero-Abad et al., 2021).
En general, M. incognita induce la formación de agallas (hipertrofia e hiperplasia) en la raíz, lo cual bloquea el flujo de agua y nutrimentos. Por el mal funcionamiento del sistema vascular, disminuye el crecimiento de las plantas, lo que causa clorosis, marchitez, caída de flores, frutos y pérdidas en la producción (Hernández et al., 2011). El manejo de estos nematodos se basa en la aplicación de nematicidas organofosforados y carbamatos (Marbán y Manzanilla, 2012). Sin embargo, por su toxicidad y persistencia ambiental existe la tendencia de evaluar alternativas de control compatibles con la salud de los agroecosistemas (Xie et al., 2015), como con Trichoderma spp. antagonistas de patógenos de la raíz (Szabó et al., 2013).
La eficiencia de Trichoderma spp. para regular poblaciones de parásitos radicales como los nematodos, depende principalmente del origen de la cepa, la interacción con el hospedante, la capacidad para adaptarse al ambiente donde se incorporan y del tipo de parasitismo del nematodo (Zhang et al., 2014). La investigación sobre el uso de microorganismos antagonistas cada vez es mayor (Hallman et al., 2009; Corazon-Guivin et al., 2024).
De los microorganismos que parasitan a los nematodos, los hongos son particularmente atractivos ya que han mostrado su potencial (Martínez-Canto et al., 2023). Trichoderma spp. son micoparásitos activos que han sido considerados para el biocontrol de hongos causantes de enfermedades foliares y radicales (Martínez-Canto et al., 2021; Natsiopoulos et al., 2024). Por lo anterior, el objetivo de este estudio fue evaluar en condiciones protegidas, la aplicación individual y en combinación de dos especies de Trichoderma en Capsicum chinense para controlar a Meloidogyne incognita.
Materiales y Métodos
El presente estudio se realizó en condiciones protegidas (invernadero) y en el laboratorio de Fitopatología perteneciente al Tecnológico de Nacional de México/Campus Conkal, ubicado en la Avenida Tecnológico S/N, localizado entre los paralelos 21°02’ y 21°08’ latitud norte y los meridianos 89°29’ y 89°35’ longitud oeste.
Establecimiento del experimento. Se utilizaron plántulas de 45 días de germinadas de chile habanero cv. Izamal (rojo en su madurez final), se trasplantaron en bolsas de 5 kg de capacidad, que contenían sustrato compuesto por suelo, bocashi y rocas volcánicas en proporción de 6:3:1. Las bolsas se establecieron en un diseño experimental de bloques completos al azar, en un invernadero tipo túnel el cual tuvo una cubierta de techo con plástico y paredes cubiertas con malla antiáfidos. Se establecieron cinco tratamientos: 1) T. asperellum (Ta13-17), 2) T. erinaceum (Te10-15), 3) combinación de T. asperellum (Ta 13-17) y T. erinaceum (Te10-15), se consideraron dos testigos; 4) Vydate® (i. a Oxamil 24% de síntesis química) en dosis de 2 mL L-1 de agua, al momento del trasplante y 5) testigo, solo plantas sin el control del nematodo.
Obtención cepas Trichoderma spp. e inoculación en plantas de chile. Las cepas de Trichoderma que se evaluaron, fueron proporcionadas por el Cepario Fúngico del Laboratorio de Fitopatología perteneciente al Campus Conkal, las cuales fueron identificadas como T. asperellum (Ta13-17) (Celis-Perera et al., 2021) y T. erinaceum (Te10-15) (Martínez et al., 2021). Para su uso, se reactivaron en medio de cultivo papa dextrosa agar (PDA) y se incubaron a 28 °C durante 15 días. Después se preparó el inóculo fúngico (1x103 esporas mL-1). Previo al trasplante, este inóculo se aplicó por separado y en combinación al suelo, posteriormente se realizaron dos inoculaciones a los ocho y 15 días después del trasplante.
Obtención del inóculo de Meloidogyne incognita e inoculación en plantas. A partir de poblaciones establecidas de M. incognita en condiciones protegidas en el cultivo de Solanum lycopersicum, se extrajeron raíces agalladas, las cuales se diseccionaron para la obtención de masas de huevos del nematodo, para su posterior desinfestación y obtención de los huevos del nematodo, la desinfestación se realizó con hipoclorito de sodio al 2 % durante dos minutos; inmediatamente después, se realizaron lavados sucesivos con agua potable usando tamices de malla con número 45, 100, 200, 325 y 400 (Ayoub, 1980). La inoculación de huevos del nematodo se realizó al sustrato indicado contenido en bolsas de 5 kg, cada una de estas fue inoculada con 500 huevos larvados (Martínez et al., 2023).
Variables de estimación de control de M. incognita . Para estimar la efectividad de los tratamientos, se consideraron las variables de severidad de agallamiento y de reproducción, evaluadas a los 56, 90, 122 y 137 días después del trasplante (ddt). Para la severidad, se utilizó una escala de índice de agallamiento de seis clases (Taylor y Sasser, 1978). Los puntos medios de cada clase se utilizaron para realizar mediante parámetros epidemiológicos, los siguientes análisis: Área Bajo la Curva del Progreso de la Enfermedad (ABCPE), tasa de infección aparente mediante el parámetro inverso de b (1/b) con el modelo de Weibull y la severidad final mediante el parámetro de Yfinal (Pennypacker et al., 1980; Campbell y Madden, 1990).
Para el efecto de tratamientos en la reproducción de M. incognita, se contabilizaron huevos y hembras por gramo de raíz; se realizaron fragmentaciones de raíces de chile habanero y se homogenizaron y se tomaron dos gramos. Posteriormente, se licuó un gramo durante 10 s, con 20 mL de cloro y 30 mL de agua potable y se filtró con tamices de malla con número 45, 100, 200, 325 y 400. Finalmente, se realizó la colecta de huevos y, fueron lavados con agua corriente. Para su contabilización se realizó con ayuda de una cámara cuenta nematodos con un microscopio compuesto utilizando el objetivo de 4X. El otro gramo de raíz, se tiñó con fucsina ácida previamente preparada, que consistió en colocar 1 g de raíz en un frasco, se añadieron 2 mL de fucsina ácida con 50 mL de agua potable para su tinción con calor a punto de ebullición; después que se enfrió se lavó con agua potable para quitar el exceso de la solución de fucsina, al final se colocó glicerina para su conservación y posterior evaluación. En un microscopio estereoscópico se separaron y contabilizaron las hembras a partir de las raíces teñidas (Moo et al., 2018; Martínez et al., 2023).
Variables Agronómicas. En cada uno de los cuatro muestreos realizados (56, 122, 137 días ddt), se estimaron las variables asociadas con la productividad del cultivo como la altura de la planta, se inició con la extracción de las plantas de la bolsa, en donde se separó la parte aérea y raíz. Con un flexómetro se midió desde el ápice de la planta hasta la base del tallo; peso seco foliar de tallo y hojas, éstas fueron depositadas en bolsas de papel estraza, se colocaron en una estufa de secado a 50 °C durante 10 días, hasta que las muestras tuvieron peso constante. Para la variable peso seco de raíz, se realizó mediante lavados de raíces, después de evaluar la severidad de la enfermedad se procedió al secado de raíces, de la misma manera las variables de peso seco de tallo y hojas. El volumen de raíces, se calculó por desplazamiento volumétrico de agua con una probeta de 1000 mL. El rendimiento, se obtuvo de ocho cortes durante el ciclo del cultivo, se determinó: peso del fruto, diámetro polar y ecuatorial.
Análisis de resultados. Los análisis epidemiológicos y de reproducción del nematodo, así como las variables agronómicas, se analizaron con el paquete estadístico de SAS ver. 9.4 para Windows. Con las variables de reproducción del nematodo, se hicieron análisis de varianzas (ANDEVAS) en las fechas de muestreo indicada. Las comparaciones de medias se realizaron con el método de Tukey (p≤0.05).
Resultados y Discusión
Efecto de control microbiano de M. incognita en chile habanero. Durante el primer muestreo a partir de los 56 ddt, el tratamiento de la combinación de T. asperellum (Ta13- 17) y T. erinaceum (Te10-15), permitió el menor índice de agallamiento y así se mantuvo hasta el último muestreo (137 ddt) con una disminución del 86.17 %, seguido de T. asperellum (Ta13-17) con 65.26 %, mientras que el tratamiento testigo sin inoculantes fúngicos, se observaron los mayores daños del nematodo durante las evaluaciones con un promedio de 29.88 % (Figura 1). Resultados también confirmados por Moo-Koh et al. (2018), mostraron que la interacción entre dos cepas de T. citrinoviride (Th33-58) y T. harzianum (Th33-59) ejercieron una reducción del 83 % en la severidad del daño radical. También Affokpon et al. (2011) reportaron menor índice de agallamiento con T. asperellum (T-12), a las nueve semanas en comparación con el testigo sin inoculación fúngica.
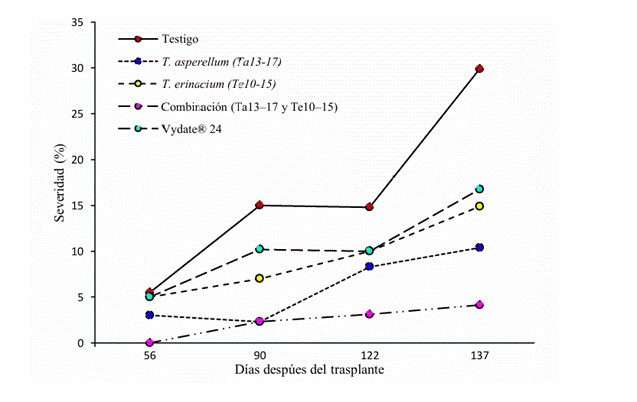
Figura 1 Curvas del progreso del índice de agallamiento en el cultivo orgánico de C. chinense, durante el período de 56, 90, 122 y 137 días después del trasplante.
Efecto del control microbiano en los parámetros epidemiológicos. El ABCPE en los tratamientos, mostró en la combinación T. asperellum (Ta13-17) y T. erinaceum (Te10-15) menor progreso de la enfermedad con 138.19 unidad % día-1; seguido del tratamiento individual de T. asperellum con 376.94 unidad % día-1. Lo que significó que durante el ciclo del cultivo en estos dos tratamientos se mejoró el control de la enfermedad con respecto al testigo. En un manejo integrado de nematodos agalladores (Naccobus aberrans y M. incognita), con biosolarización y T. viride se mantuvo 457 unidad % día-1 (Magallanes, 2021), lo que evidenció también que una acumulación de materia orgánica en asociación con organismos antagónicos y saprofitos puede disminuir la población de M. incognita (Pérez et al., 2019). La enfermedad se pudo caracterizar y ajustar al modelo de descripción Weibull con el cual se estimó la tasa de infección aparente mediante el inverso de su parámetro b-1 (Pennypeker et al., 1980). Al respecto, los tratamientos que permitieron menores tasas de infección aparente (velocidad de la enfermedad) fueron: el tratamiento de la combinación T. asperellum (Ta13-17) / T. erinaceum (Te10-15), tratamiento con Vydate®, y T. erinaceum, lo que demostró que los intervalos de aplicación fueron los adecuados para el control de la enfermedad. En contraste, el tratamiento que mayor intensidad de enfermedad mostró fue el testigo, sin control del nematodo (Cuadro 1). Al final del experimento el parámetro de Yfinal, mostró que la combinación Ta13-17 y Te10-15 fue la que mejor controló la enfermedad al permitir un 4.13 % de severidad final, lo cual superó (p≤0.01) al resto de los tratamientos ya que estos permitieron al menos un 30 % de severidad de la enfermedad (Cuadro 1). El efecto antagónico de Trichoderma spp. en el control del nematodo, está asociado con sus mecanismos de acción en la producción de metabolitos secundarios como viridina, gliotoxina, gliovirina, que inhiben no solo el crecimiento de hongos, si no la eclosión de huevos e inmovilización de estadios juveniles de nematodos (Zin y Badaluddin et al., 2020) (Cuadro 1).
Cuadro 1 Efecto de tratamientos en el control de M. incognita estimado con parámetros epidemiológicos en el cultivo orgánico de C. chinense.
| Tratamiento | ABCPE (unidad % día -1) | Tasa de la infección aparente 1/b (unidad % día -1) | r2 (ajuste del modelo Weibull) | Yfinal (%) |
|---|---|---|---|---|
| *T. asperellum* (Ta13-17) | 376.94 c z | 0.0076 ab | 0.97 | 10.38 ab |
| *T. erinaceum* (Te10-15) | 778.25 b | 0.0072 b | 0.91 | 14.88 ab |
| Combinación | 138.19 c | 0.0044 c | 0.93 | 4.13 b |
| Testigo | 1202.63 a | 0.0091 a | 0.90 | 29.88 a |
| Vydate® | 815.75 b | 0.0074 b | 0.90 | 16.75 ab |
| DMS* | 293.86 | 0.0016 | - | 11.56 |
ZMedias con letras iguales no son estadísticamente diferencias (Tukey, ≤0.05). *Diferencia Mínima Significativa (P≤0.05).
Número de huevos por gramo de raíz licuada. La combinación (Ta13-17 y Te10-15) a los 56 días después del trasplante, no presentó huevos, y se mantuvo un control de esta variable con un porcentaje de disminución con respecto al testigo con 81 % a los 122 días después del trasplante y, 77 % a los 137 días después del trasplante (Cuadro 2). Moo Koh et al. (2018) evaluaron la interacción T. simmonsii (Th 09-06) / T. harzianum (Th33-59) y consiguieron un 59.3 % en la reducción de huevos. El tratamiento solo con T. asperellum causó una disminución de número de huevos de 37.65 % a los 137 días después del trasplante, también cuando se aplicó T. asperellum cepa Ta.90 en plantas de tomate, disminuyeron en el número de huevos del 50 % (Hernández et al., 2015). La disminución de huevos es una consecuencia del parasitismo detectado en ootecas y huevos, lo que ratifica el efecto observado bajo condiciones in vitro en dónde T. asperellum FbMi6 mostró una actividad de inhibición sobre la eclosión de los huevos y la mortalidad de juveniles de M. incognita (Saharan et al., 2023).
Cuadro 2 Efecto de tratamientos en número de huevos de M. incognita en el cultivo orgánico de C. chinense.
| Tratamiento | Número de huevos por gramo de raíz licuada | |||
|---|---|---|---|---|
| 56 ddty | 90 ddt | 122 ddt | 137 ddt | |
| *T. asperellum* (Ta13-17) | 70.25 bc z | 86.50 b | 1214.25 a | 1361.75 ab |
| *T. erinaceum* (Te10-15) | 105.75 bc | 491.75 ab | 1372.25 a | 1487.25 ab |
| Combinación | 0.00 c | 55.50 b | 335.25 a | 495.25 b |
| Testigo | 394.25 a | 944.25 a | 1787.00 a | 2184.25 a |
| Vydate® | 302.25 ab | 843.75 ab | 1540.25 a | 1554.50 ab |
| DMS* | 233.81 | 822.92 | 1978.01 | 1530.49 |
yddt: Días después del trasplante. Z Medias con letras iguales no son estadísticamente diferencias (Tukey, ≤ 0.05). *Diferencia Mínima Significativa (P≤0.05).
Número de hembras por gramo de raíz teñida. A los 90 días después del trasplante, el tratamiento con T. asperellum (Ta13-17) disminuyó un 75 % respecto al tratamiento testigo. Mismo efecto mostró el tratamiento con la combinación T. asperellum (Ta13-17) /T. erinaceum (Te10-15) en número de hembras por gramo de raíz teñida y, así se mantuvo el control de reproducción del nematodo hasta los 122 días después del trasplante. Al final del cultivo, es decir 137 días después del trasplante, con la combinación (Ta13-17 y Te10- 15), el número de hembras por gramo de raíz teñida se disminuyó un 77.31 y un 73.65 % en relación al testigo y al Vydate®, respectivamente (Cuadro 3). En otro estudio, en el cultivo de tomate las interacciones (combinaciones) de T. simmonsii (Th09-06) / T. harzianum (Th33-59), T. virens (Th27-08) / T. harzianum (Th33-59) y T. virens (Th 43- 13) / T. ghanense (Th26-52) tuvieron una disminución del 90.1, 88.1 y 31.5 %, respectivamente (Moo-Koh et al., 2018). Al final del cultivo, el tratamiento individual de T. asperellum (Ta13-17) causó una disminución de reproducción del 43.81 % en comparación con el tratamiento testigo.
Cuadro 3 Efecto de tratamientos en el número de hembras de M. incognita en cultivo orgánico de C. chinense.
| Número de hembras por gramo de raíz teñida | ||||
|---|---|---|---|---|
| Tratamiento | 56 ddty | 90 ddt | 122 ddt | 137 ddt |
| *T. asperellum* (Ta 13-17) | 4.50 abz | 4.50 a | 25.75 a | 27.25 ab |
| *T. erinaceum* (Te 10-15) | 11.25 a | 13.25 a | 29 a | 35.25 ab |
| Combinación | 0 b | 4.50 a | 6.25 a | 11 b |
| Testigo | 8.50 ab | 18 a | 41.77 a | 48.5 a |
| Vydate® | 7.50 ab | 37 a | 32.50 a | 41.75 ab |
| DMS* | 10.98 | 33.79 | 35.65 | 34.43 |
yddt: días después del trasplante. Z Medias con letras iguales no son estadísticamente diferencias (Tukey, ≤0.05). *Diferencia Mínima Significativa (P≤0.05).
Se ha planteado también que las propiedades de Trichoderma, radica en la habilidad para parasitar diferentes estadios de vida de M. incognita (Sharon et al., 2011). En particular con T. asperellum, mejora la tolerancia de las plantas infectadas por nematodos, al fortalecer las características bioquímicas y fisiológicas, sobre todo la producción de metabolitos secundarios como compuestos fenólicos, que dificulta la reproducción del nematodo (Saharan et al., 2023).
Efecto de control microbiano en el cultivo. En las variables agronómicas, aunque no hubo diferencias estadísticas significativas entre tratamientos; en la altura de la planta, biomasa foliar y volumen radicular se estimó mayor efecto con la combinación de Trichoderma (cepas: Ta13-17 y Te10-15), con promedios de 30.85 cm, 95.49 g y 55.06 cm3 en su orden, que cuando se estimó el efecto correspondiente a la aplicación individual de las cepas de Trichoderma spp. El tratamiento con menor efecto en altura fue con el tratamiento Vydate® con un promedio de 23.64 cm. Es notorio que el tratamiento de la combinación de Trichoderma (cepas: Ta13-17 y Te10-15) tuvo un efecto favorable en diámetro de tallo (Cuadro 4). La aplicación de cepas de Trichoderma spp., estudiadas como antagonistas de M. incognita, al suprimir la población de nematodos y disminuir el índice de agallamiento, tuvieron una tendencia en mejorar el crecimiento del cultivo, lo que se reflejó en las variables agronómicas del chile habanero. Cuando hay una promoción del crecimiento tiene lugar una interacción específica con Trichoderma y la producción del ácido indolacético, que se refleja en mayor producción de biomasa vegetal (Contreras et al., 2009; Martínez et al., 2011). Sin embargo, esto no sucede cuando el hospedante establece una interacción con un patógeno. En cambio, los microorganismos de biocontrol, como Trichoderma, destinan los recursos a la activación de mecanismos de defensa, conocidos como resistencia sistémica inducida, a través de las vías del ácido jasmónico, el ácido salicílico o el etileno, a lo que se atribuye lo ocurrido en el presente estudio (Hermosa et al., 2013; Nawrocka et al., 2013).
Cuadro 4 Efecto de tratamientos en el control de M. incognita en las variables agronómicas del cultivo orgánico de C. chinense.
| Tratamiento | Altura de la planta (cm) | Diámetro del tallo(mm) | BiomasaFoliar (g) | Volumen Radicular(cm³) |
|---|---|---|---|---|
| *T. asperellum* (Ta 13-17) | 28.84±2.68 a | 7.84±0.82 ab | 81.9±13.54 a | 48.94±6.3 a |
| *T. erinaceum* (Te 10-15) | 26.76±1.36 a | 7.16±0.75 ab | 88.43±15.96 a | 49.31±8.35 a |
| Combinación | 30.85±3.14 a | 7.96±0.71 a | 95.49±11.83 a | 55.06±7.05 a |
| Testigo | 30.41±1.26 a | 7.47±0.67 ab | 76.41±11.46 a | 40.88±6.24 a |
| Vydate® | 23.64±2.94 a | 6.72±0.82 b | 79.88±12.83 a | 44.38±7.76 a |
| DMS* | 9.32 | 1.23 | 52.26 | 16.00 |
ZMedias con letras iguales no son estadísticamente diferencias (Tukey, ≤0.05). *Diferencia Mínima Significativa (P≤0.05).
Efecto de tratamientos en la producción de frutos, mediante el control de M. incognita en el cultivo orgánico de C. chinense. Los resultados de rendimiento y tamaño de frutos fueron de ocho cortes realizados, los análisis de varianza mostraron diferencias significativas entre los tratamientos (p≤0.01). Los tratamientos con mayor producción fueron los inoculados con Trichoderma spp. Los tratamientos con T. asperellum (Ta13-17) y la combinación (cepas: Ta13-17 y Te10-15), no solo superaron al tratamiento testigo sin inoculante fúngico, también fueron mejores al tratamiento con el nematicida Vydate®. En el primer caso se tuvo un rendimiento de 244.78 g planta -1, en el segundo 231.08 g planta -1. El mejor tamaño de fruto se determinó en el tratamiento de T. erinaceum (Te10-15) (Cuadro 5). Algunos estudios sugieren que los antagonistas microbianos también pueden reducir el rendimiento de los cultivos debido a la competencia fúngica (Meyer et al., 2001) y la interacción con hongos en los cultivos (Harman, 2006) o la supresión de raíces, lo que debe considerarse en próximos estudios de biocontrol. Sin embargo, este efecto se evidenció en este estudio (Cuadro 5).
Cuadro 5 Efecto de tratamientos en el rendimiento de frutos en el cultivo de C. chinense.
| Tratamiento | Rendimiento (g planta-1) | Número de frutos | DiámetroEcuatorial(cm) | Diámetro Polar(cm) |
|---|---|---|---|---|
| *T. asperellum* (Ta 13-17) | 244.78±20.95 a | 23.59±1.85 a | 2.89±1.02 b | 4.63±1.64 b |
| *T. erinaceum* (Te 10-15) | 210.4±17.65 ab | 20.97±1.69 a | 4.51±1.16 a | 11.23±3.97 a |
| Combinación | 231.08±18.41 a | 18.94±1.27 ab | 2.89±1.02 b | 3.94±1.39 b |
| Testigo | 121.85±11.88 c | 12.91±1.29 b | 2.94±1.04 b | 3.94±1.39 b |
| Vydate® | 151.93±15.78 bc | 17.59±1.81 ab | 3.05±1.08 b | 4.79±1.69 b |
| DMS* | 66.47 | 6.18 | 0.45 | 1.13 |
ZMedias con letras iguales no son estadísticamente diferencias (Tukey, ≤0.05). *Diferencia Mínima Significativa (P≤0.05).
Conclusiones
Los tratamientos que incluyeron inoculaciones con T. asperellum (Ta13-17) mejoraron el control de M. incognita con una disminución del 65.26 % en la severidad, al igual que el tratamiento con la combinación de Trichoderma (cepas: Ta13-17 y Te10-15) que redujo un 86.17 %. En las variables de reproducción del nematodo se disminuyeron del 75 al 85 % en número de huevos por gramo de raíz licuada y hembras por gramo de raíz teñida a los 122 días después del trasplante del cultivo. Al igual que en el rendimiento, estos mismos tratamientos aumentaron en un 40 al 50 % la producción de frutos por planta con respecto al testigo. El ABCPE y la tasa de infección aparente mediante el modelo de Weibull, explicaron una disminución significativa en el índice de agallamiento con la aplicación individual de T. aperellum (Ta13-17); sin embargo, cuando se combinó con T. erinaceum (Te10-5) causaron menor formación de agallas.











 texto en
texto en 


