Introducción
Los plátanos y bananos (Musa spp.) son el cuarto cultivo más importante del mundo, solo por debajo del arroz, el trigo y el maíz (FAOSTAT, 2024). Esta fruta está disponible todo el año y se cultiva en 135 países en regiones tropicales y subtropicales. Aunque el banano representa una fuente significativa de ingresos en la región de latinoamérica, solo 15 % de la producción se exporta como fruta fresca, ya que la mayoría de la cosecha se realiza en pequeñas fincas o traspatios para el consumo nacional o los mercados locales (FAOSTAT, 2024).
Los plátanos y bananos son afectados por varios patógenos en todo el mundo, un ejemplo es la marchitez por Fusarium, causada por el hongo Fusarium oxysporum (Fo), esta enfermedad es especialmente preocupante. El complejo específico de F. oxysporum f. sp. cubense (Foc), constituido al menos por cuatro razas, es considerada una de las enfermedades más destructivas para este cultivo (van Westerhoven et al., 2022). Foc produce tres tipos de esporas asexuales: macroconidios, microconidios y clamidosporas, que desempeñan funciones en la dispersión, infección, la reproducción y la supervivencia (Pegg et al., 2019). Cuando Foc invade una plantación es difícil de controlar, ya que el patógeno permanece en el suelo durante largos periodos (Maryani et al., 2019). Así, la alternativa más efectiva para controlar la enfermedad es el reemplazo de cultivares susceptibles por cultivares resistentes al patógeno.
En el pasado, casi todas las plantaciones comerciales del mundo cambiaron sus variedades susceptibles por genotipos del subgrupo Cavendish (genoma AAA). El reciente surgimiento de Foc Raza 4 Tropical (Foc R4T), capaz de infectar a miembros del subgrupo Cavendish, se ha convertido en la principal amenaza a la industria del plátano y el banano. Esto es más problemático porque, hoy en día, los mercados demandan principalmente frutos del clon ‘Enano Gigante’ del subgrupo Cavendish y no hay otros genotipos de banano resistentes disponibles (Ordoñez, 2018). En México, cerca de 40 mil hectáreas del cultivar ‘Gros Michel’ se vieron devastadas a mediados de la década de 1950 debido a Foc raza 1, lo que obligó a reemplazarlas por clones resistentes del subgrupo ʻCavendishʼ, como ʻEnano Giganteʼ. Por ejemplo, hace una década, el estado de Nayarit tenía 3 mil ha de cultivos de ʻManzanoʼ y 3.5 mil ha de ʻGros Michelʼ. La producción de plátanos y bananos en México está concentrada en 16 estados, con Chiapas, Tabasco, Colima y Veracruz como los productores principales, representando 72.5 % del área sembrada, 75.3 % del volumen producido y 66.3 % del valor de la producción del cultivo. El volumen obtenido en 2023 fue de 2,642,338 de toneladas, 1.9 % más que la producción del año anterior (SIAP, 2024).
El conocimiento de la diversidad genética de las poblaciones de hongos fitopatógenos y de su modo de reproducción es relevante para los programas de mejoramiento genético de cultivos y para reducir el impacto de la enfermedad (McDonald y Linde, 2002). En el caso de Foc, presenta una estructura genética relativamente diversa para un hongo de reproducción asexual (Martínez-de la Parte et al., 2024). La información genética del patógeno puede usarse para diseñar prácticas de manejo efectivas contra la enfermedad, así como para programas de mejoramiento para desarrollar cultivares de banano resistentes o tolerantes, y para fines de cuarentena en un país o ubicación geográfica determinados (Magdama et al., 2020; van Westerhoven et al., 2022; Chittarath et al., 2022; Baruah et al., 2025). En México, a pesar del aumento sostenido de plantaciones de plátano y banano, la información sobre la diversidad y estructura genética de Foc es escasa. Esta investigación presenta el primer análisis en donde se estudian aislamientos de Fo de diferentes regiones usando marcadores SSR como un acercamiento preliminar para justificar estudios más a fondo sobre la diversidad de Foc.
El muestreo se realizó directamente sobre plantas de Musa de las variedades ‘Pisang Awak’ (ABB), ‘Manzano’ (AAB) y ‘Pera’ (ABB) afectadas por la marchitez por Fusarium en cinco regiones productoras de plátano de México: en los estados de Colima, Michoacán, Jalisco, Nayarit y Yucatán (Cuadro 1). En cada plantación muestreada se recolectaron pseudotallos de plantas de seis a ocho meses de edad, con síntomas de marchitez por Fusarium. Los haces vasculares decolorados se cortaron en 2 a 4 fragmentos y se almacenaron en una bolsa de papel. En el laboratorio, se obtuvieron cultivos monospóricos utilizando cultivos mediante el protocolo propuesto por Mostert et al. (2017). La morfología y las características culturales de los aislados de Fo se determinaron según lo descrito por Leslie y Summerell (2006). Se obtuvieron 96 cultivos monospóricos, los cuales fueron almacenados en glicerol esterilizado al 15 % (v/v) a -80 °C. No se realizaron pruebas adicionales para verificar la identidad del aislamiento como F. oxysporum f. sp. cubense. Para la extracción del ADN genómico de los 96 cultivos monospóricos de Fo, se siguió el protocolo de Möller y Bahnweg (1992). Se analizaron seis loci SSR para la caracterización de haplotipos. Los oligonucleótidos usados aparecen en el Cuadro 2. Dado que estos SSR fueron sugeridos para estudiar la estructura de Fo (Bogale et al., 2005), no necesariamente se debe asumir que este trabajo se enfocó en aislamientos de Foc, así como en sus razas, excepto la raza 4 (Foc R4T), la cual no ha sido reportada de forma oficial en México. Los ciclos de PCR se realizaron según lo especificado por Bogale et al. (2005). Los productos PCR se analizaron por electroforesis en gel de agarosa al 1.5 % y luego se tiñeron en bromuro de etidio y se documentaron en un sistema ChemiBis MF-2 (Bio-Imaging Systems, Neve Yamin, Israel). Se construyó una matriz binaria para los seis loci y un total de 96 aislamientos.
Cuadro 1 Sitios de recolección de muestras para el aislamiento de F. oxysporum en plantaciones comerciales de banano en cinco estados mexicanos.
| Código del aislamiento | Municipio | Estado | Cultivar | Localización geográfica | Altitud (msnm) |
|---|---|---|---|---|---|
| ACM1 | Silk (AAB) | 18°53´23”N, 104° 0´ 0” O | 11 | ||
| ACM2 | Silk (AAB) | 18°53´23”N, 104° 0´ 0” O | 11 | ||
| ACP1 | Bluggoe (ABB) | 18° 54´ 52”N, 103° 59´38” O | 11 | ||
| ACP2 | Bluggoe (ABB) | 18° 54´ 52”N, 103° 59´38” O | 11 | ||
| ACM3 | Armería | Colima | Silk (AAB) | 18°54´5”N, 103°54´31”O | 11 |
| ACM4 | Silk (AAB) | 18°54´5”N, 103°54´31”O | 11 | ||
| ACM10 | Silk (AAB) | 18°53´10”N, 103°59´37”O | 11 | ||
| ACP11 | Bluggoe (ABB) | 18°55´24”N, 103°57´49”O | 11 | ||
| ACP15 | Bluggoe (ABB) | 18°55´24”N, 103°57´49”O | 11 | ||
| ACM13 | Silk (AAB) | 18°55´34”N, 103°58´2”O | 11 | ||
| TCM1 | 18°55´3”N, 103°5´ 13´´O | 40 | |||
| TCM2 | 18°55´3”N, 103°5´ 13´´O | 40 | |||
| TCM8 | 18°48´44”N, 103°42´49” O | 69 | |||
| TCM9 | Tecomán | Colima | Silk (AAB) | 18°48´44”N, 103°42´49” O | 69 |
| TCM10 | 18°48´44”N, 103°42´49” O | 69 | |||
| TCM11 | 18°48´44”N, 103°42´49” O | 69 | |||
| TCM12 | 18°48´44”N, 103°42´49” O | 69 | |||
| TCM13 | 18°50´ 54´´N, 163°99´ 28´´ O | 27 | |||
| TCM14 | 18°50´ 54´´N, 163°99´ 28´´ O | 27 | |||
| TCM15 | 18°50´ 54´´N, 163°99´ 28´´ O | 27 | |||
| TCM16 | 18°50´ 54´´N, 163°99´ 28´´ O | 27 | |||
| TCM1 | 18°58´2”N, 103° 50´33” O | 62 | |||
| MCP1 | Bluggoe (ABB) | 18°57´0”N, 104°3´40”O | 22 | ||
| MCT3 | Pisang awak (ABB) | 109°02´48”N, 104°06´35”O | 70 | ||
| MCT4 | Pisang awak (ABB) | 109°02´48”N, 104°06´35”O | 70 | ||
| MCT5 | Pisang awak (ABB) | 109°02´48”N, 104°06´35”O | 70 | ||
| MCT6 | Pisang awak (ABB) | 109°02´48”N, 104°06´35”O | 70 | ||
| MCM7 MCM9 | Manzanillo | Colima | Silk (AAB) Silk (AAB) | 109°0´52”N, 104°9´22”O 109°0´52”N, 104°9´22”O | 21 21 |
| MCM10 | Silk (AAB) | 109°0´52”N, 104°9´22”O | 21 | ||
| MCM11 | Silk (AAB) | 109°0´52”N, 104°9´22”O | 21 | ||
| MCM13 | Silk (AAB) | 19°00´46”O, 104°09´25”O | 21 | ||
| MCM14 | Silk (AAB) | 19°00´46”O, 104°09´25”O | 21 | ||
| MCM15 | Silk (AAB) | 19°02´21”N, 104°14´08”O | 16 | ||
| SNM1 | Silk (AAB) | 21°32´25”N, 105°07´51”O | 325 | ||
| SNP1 | Bluggoe (ABB) | 21°32´32”N, 105°08´01”O | 206 | ||
| SNM2 | Silk (AAB) | 21°32´32”N, 105°08´05”O | 206 | ||
| SNM3 | Silk (AAB) | 21°32´32”N, 105°08´05”O | 206 | ||
| SNM4 | Silk (AAB) | 21°32´41”N, 105°08´05”O | 206 | ||
| SNM5 | Silk (AAB) | 21°32´44”N, 105°08´12”O | 206 | ||
| SNM5.2 | Silk (AAB) | 21°32´44”N, 105°08´12”O | 206 | ||
| SNM6 | Silk (AAB) | 21°32´44”N, 105°08´12”O | 206 | ||
| SNM7 SNM8 | San Blas | Nayarit | Silk (AAB) Silk (AAB) | 21°32´44”N, 105°08´12”O 21°32´44”N, 105°08´17”O | 206 206 |
| SNM9 | Silk (AAB) | 21°32´44”N, 105°08´17”O | 206 | ||
| SNM10 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| SNT1 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| SNT2 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| SNT3 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| SNT4 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| SNT5 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| SNT6 | Pisang awak (ABB) | 21°26´36”N, 105°11´20”O | 33 | ||
| AYP1 | Bluggoe (ABB) | 20°15´53”N, 89°21´37”O | 32 | ||
| AYP2 AYM1 | Akil | Yucatán | Bluggoe (ABB) Silk (AAB) | 20°5´55”N, 89°21´37”O 20°15´52”N, 89°2´37”O | 32 32 |
| AYM2 | Silk (AAB) | 20°15´52”N, 89°21´22”O | 32 | ||
| OYM4 | Silk (AAB) | 20°13´38”N, 89°27´32”O | 49 | ||
| OYM5 OYM6 | Oxkutzcab | Yucatán | Silk (AAB) Silk (AAB) | 20°13´38”N, 89°27´32”O 20°13´14”N, 89°26´30”O | 49 49 |
| OYM7 | Silk (AAB) | 20°13´38”N, 89°27´32”O | 49 | ||
| OYM8 | Silk (AAB) | 20°13´38”N, 89°27´32”O | 49 | ||
| OYM9 | Silk (AAB) | 20°13´38”N, 89°27´32”O | 49 | ||
| OYP3 | Bluggoe (ABB) | 20°13´38”N, 89°27´32”O | 49 | ||
| OYM10 | Silk (AAB) | 20°16´42”N, 89°22´52”O | 32 | ||
| OYM11 | Silk (AAB) | 20°16´42”N, 89°22´52”O | 32 | ||
| OYM12 | Silk (AAB) | 20°16´42”N, 89°22´52”O | 32 | ||
| OYM13 | Silk (AAB) | 20°16´42”N, 89°22´52”O | 32 | ||
| OYM14 | Silk (AAB) | 20°16´42”N, 89°22´52”O | 32 | ||
| CMM1 | 18°40´41”N, 103°40´29”O | 21 | |||
| CMM2 | 18°40´43”N, 103°40´31”O | 21 | |||
| CMM3 | 18°40´22”N, 103°41´22”O | 29 | |||
| CMM4 | 18°39´57”N, 103°41´27”O | 29 | |||
| CMM5 | Coahuayana | Michoacán | Silk (AAB) | 18°44´04”N, 103°40´01”O | 27 |
| CMM6 | 18°44´04”N, 103°40´01”O | 27 | |||
| CMM7 | 18°42´59”N, 103°42´03”O | 27 | |||
| CMM8 | 18°42´59”N, 103°42´03”O | 27 | |||
| CMM9 | 18°42´59”N, 103°42´03”O | 27 | |||
| RJP1 | Silk (AAB) | 19°10´30.42´´N 104°36´01.13´´O | 12 | ||
| RJP2 | Silk (AAB) | 19°10´30.22´´N, 104°36´01.25´´O | 12 | ||
| RJP3 | Silk (AAB) | 19°10´30.22´´N, 104°36´01.57´´O | 12 | ||
| RJP4 | Silk (AAB) | 19°10´30.04´´N, 104°36´01.74´´O | 12 | ||
| RJP5 | Silk (AAB) | 19°10´29.93´´N, 104°36´02.17´´O | 12 | ||
| RJP6 | Silk (AAB) | 19°10´29.83´´N 104°36´02.41´´O | 12 | ||
| RJP7 | Silk (AAB) | 19°10´39.42´´N 104°36´07.12´´O | 12 | ||
| RJP8 | Silk (AAB) | 19°10´38.67´´N 104°36´06.60´´O | 12 | ||
| RJP9 | Silk (AAB) | 19°10´38.38´´N 104°36´05.71´´O | 12 | ||
| RJP10 RJP11 | El Rebalse | Jalisco | Silk (AAB) Bluggoe (ABB) | 19°10´38.86´´N 104°36´07.77´´O 19°10´38.66´´N 104°36´06.80´´O | 12 14 |
| RJM12 | Bluggoe (ABB) | 19°10´39.20´´N 104°36´09.30´´O | 14 | ||
| RJM13 | Bluggoe (ABB) | 19°10´38.68´´N 104°36´09.20´´O | 14 | ||
| RJM14 | Bluggoe (ABB) | 19°11´15.86´´N, 104°35´29.56´´O | 14 | ||
| RJM15 | Bluggoe (ABB) | 19°11´16.26´´N, 104°35´29.50´´O | 14 | ||
| RJM16 | Bluggoe (ABB) | 19°11´17.05´´N, 104°35´17.05´´O | 14 | ||
| RJM17 | Bluggoe (ABB) | 19°11´17.35´´N, 104°35´27.92´´O | 14 | ||
| RJM18 | Bluggoe (ABB) | 19°11´17.72´´N, 104°35´26.70´´O | 14 | ||
| RJM19 | Bluggoe (ABB) | 19°11´21.94´´N, 104°35´09.52´´O | 14 | ||
| RJM20 | Bluggoe (ABB) | 19°11´21.83´´N, 104°35´08.53´´O | 14 |
Cuadro 2 Información de los oligonucleótidos de repetición de secuencia simple (SSR) usados para analizar la diversidad genética de aislamientos de Fusarium oxysporum (modificado de Bogale et al., 2005).
| Oligonucleótido | x Secuencia (5´-3´) | Temperatura de empalme (°C) |
|---|---|---|
| G1/ MV15 | R: CTCGTCCTTTGCGAATGACC | 58 |
| G: ACCACCTCGGTGATGGTGAGACGG | ||
| R: CAAGCCGCTCTCCACGGCGAAGGCG | ||
| MB18 | F: GGTAGGAAATGACGAAGCTGAC | 57 |
| R: TGAGCACTCTAGCACTCCAAAC | ||
| R: CGTCCTCAAGAGCAGCGAC |
x F: forward, R: reverse
Los aislamientos totales se organizaron en tres grupos para mejorar la robustez del análisis y facilitar la interpretación de datos. Así, consideramos a los aislamientos de Colima, Jalisco y Michoacán como una población única por su continuidad regional y la falta de barreras ecológicas aparentes. Los aislamientos de Nayarit integran la segunda población, y los de Yucatán son la tercera población. Después, con base en la proximidad geográfica y las rutas de comercio de frutas y propágulos de plátano, estas se asignaron adicionalmente a dos regiones: (i) el este de México (muestras de Yucatán) y (ii) el occidente de México (aislamientos de Nayarit, Colima, Jalisco y Michoacán). El número y la frecuencia de los haplotipos se calcularon en POPGENE. Con estos datos, por medio del índice de similitud de Morisita en el paquete Vegan de R (Oksanen et al., 2019), se estimó la semejanza genética de las poblaciones. Con los datos del haplotipo, también se realizó un análisis molecular de varianza (AMDEVA) para evaluar la diferenciación genética entre regiones (FCT), entre poblaciones en cada región (FSC) y entre todas las poblaciones incluidas en el análisis (FST). Se realizó el AMDEVA en ARLEQUIN v. 3.5 con el uso de 1000 permutaciones. Además, para ilustrar las relaciones entre haplotipos y su distribución y frecuencia entre poblaciones, se generó una red de expansión mínima. La estructura genética se infirió mediante el análisis de componentes principales y la factorización matricial dispersa no negativa (sNMF) en LEA (Frichot y François, 2015). Se seleccionó el número óptimo de K con el uso de un criterio de entropía cruzada basado en la predicción de genotipos enmascarados para evaluar el error en la estimación de la ascendencia.
Los resultados de la caracterización cultural mostraron que el desarrollo del tamaño de la colonia tuvo un rango de 8.7 a 9.8 mm por día en un medio PDA a 28 °C. Después de siete días de cultivo, todos los aislamientos presentaron micelio blanco algodonoso, que podía ser plano o aéreo, de forma circular o irregular, con una coloración de violeta claro a violeta oscuro en la superficie superior. En el reverso de la placa de Petri, el color de las colonias variaba de naranja a rojo oscuro. Las monofiálides tuvieron un promedio de 3 a 5 septos, unicelulares o bicelulares, con microconidios ovalados de 5-15 × 2.5-3.5 μm. Los macroconidios eran de 23.5-47.8 × 3.3-4.8 μm, falciformes, con tres a cuatro septos (Leslie y Summerell, 2006). Estas características son típicas de Fusarium oxysporum. Por otra parte, los análisis moleculares, mostraron que todos los loci analizados fueron polimórficos en los 96 aislamientos mexicanos de Fusarium oxysporum. Se detectaron 16 haplotipos, de los cuales el más frecuente y común fue el H16 (Figura 1). El resto se encontró ampliamente disperso o restringido a una o dos poblaciones.
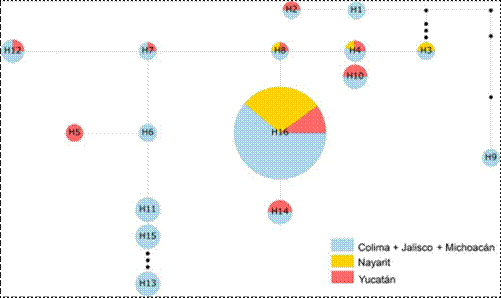
Figura 1 Una red de expansión mínima de 16 haplotipos encontrados en las poblaciones estudiadas de Fusarium oxysporum. Los pequeños puntos negros a lo largo de las ramas representan haplotipos ausentes. El H dentro de los círculos corresponde al identificador del haplotipo, el color indica el tipo de población y el tamaño del círculo representa la frecuencia del haplotipo.
Las diferencias genéticas entre las tres poblaciones analizadas no fueron significativas (Cuadro 3, Figura 2), ni entre regiones (Cuadro 4).
Cuadro 3 Disimilitud entre las poblaciones muestreadas de Fusarium oxysporum.
| Población | Colima, Jalisco y Michoacán | Nayarit | Yucatán |
|---|---|---|---|
| Colima, Jalisco and | – | – | – |
| Michoacán Nayarit | 0.097 | – | – |
| Yucatán | 0.000 | 0.255 | – |
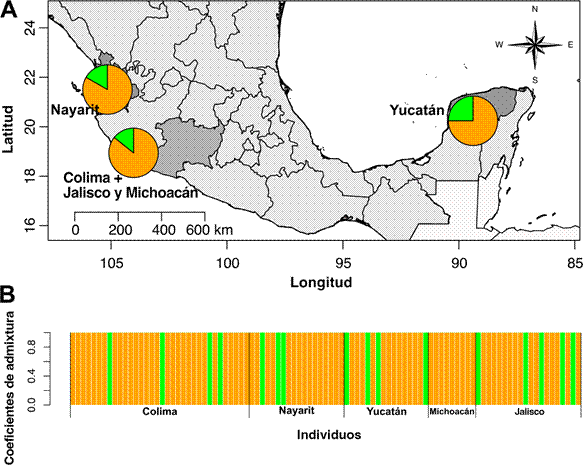
Figura 2 Análisis de la estructura genética de aislamientos de Fusarium oxysporum de diferentes localidades con base en la factorización matricial dispersa no negativa (sNMF). (A) Estructura poblacional para K = 2, representada en el mapa utilizando los valores promedio del coeficiente de ascendencia para cada población estimada. (B) Probabilidad de asignación grupal de cada individuo muestreado.
Cuadro 4 Análisis molecular de varianza (AMDEVA) con base en haplotipos asociados a 96 aislamientos de Fusarium oxysporum de Colima, Jalisco, Michoacán, Nayarit y Yucatán, agrupados en dos regiones (este y oeste de México).
| Fuente de variaciónX | d.f. | Suma de cuadrados | Componentes de varianza | Variación(%) | FI | P |
|---|---|---|---|---|---|---|
| Entre regiones | 1 | 0.921 | -0.00145 | -0.19 | -0.00188 | 0.66960 ± 0.019 |
| Entre poblaciones al interior de regiones | 1 | 1.012 | 0.00888 | 1.15 | 0.01150 | 0.21114 ± 0.014 |
| Entre poblaciones | 94 | 71.778 | 0.76359 | 99.04 | 0.00964 | 0.23460 ± 0.011 |
| Total | 96 | 73.711 | 0.77103 | – | – | – |
xd.f., grados de libertad; FI, índice de fijación; P, significancia.
Según estos resultados, las poblaciones mexicanas de Fo son genéticamente similares (Cuadros 3 y 4). Al analizar poblaciones ecuatorianas de Foc, Magdama et al. (2020) concluyeron que también integran un único linaje clonal. En este estudio se detectaron varios haplotipos de Foc, pero solo uno era dominante (Figura 1). Esto puede estar relacionado a la baja tasa de variabilidad de Foc como organismo asexual en comparación con organismos que se reproducen de forma sexual, tales como Pseudocercospora fijiensis (Manzo-Sánchez et al., 2019; McDonald y Linde, 2002). Estos resultados también concuerdan con Bentley (1998), quien detecta solo un linaje de Foc en poblaciones mexicanas (linaje VIII). El mismo autor describe que este linaje es único en Centroamérica, pero no asignó un código de grupo de compatibilidad vegetativa (VCG). Por otra parte, Ordoñez (2018) especifica que el VCG 0124 hallado en México corresponde al complejo de grupo de compatibilidad 0124/5/8/20, cuyos miembros a nivel mundial se habían identificado como pertenecientes a las razas 1, 2 y 4. El VCG de Foc hallado en México nos permite plantear la hipótesis de que el patógeno en este país es una mezcla entre cepas nativas e introducidas. Si esto es cierto, las actividades humanas son responsables de la diseminación del linaje clonal.
El hongo Fusarium oxysporum f. sp. cubense es un patógeno genéticamente diverso con una distribución cosmopolita. Está compuesto de cuatro razas, de las cuales tres infectan a plátanos y bananos (Ploetz, 2015; Pegg et al., 2019; Martinez-de la Parte et al., 2024; Baruah et al., 2025). Asimismo, se han reconocido más de 24 grupos de compatibilidad vegetativa (Koening et al., 1997; Ordoñez, 2018; Maryani et al., 2019), y se han detectado al menos nueve linajes filogenéticamente agrupados en dos clados (Bentley et al., 1998; Czislowski et al., 2018; O’Donnell et al., 1998; Pegg et al., 2019). Debido a que Foc se reproduce de forma preferentemente asexual, su diversidad genética está agrupada en linajes clonales (Bentley et al., 1998; Pegg et al., 2019). Esta diversidad puede enriquecerse por eventos parasexuales en los que puede ocurrir una transferencia horizontal de genes (Czislowski et al., 2018; Fourie et al., 2009; Ma et al., 2010; Vlaardingerbroek et al., 2016). Así, la estructura genética de Foc (o la ausencia de esta) corresponde a lo que se espera para un organismo que se reproduce de manera preferentemente asexual (McDonald y Linde, 2002). De hecho, la diversidad genética de este patógeno (la mayoría de los VCGs) se concentra en su centro de origen, y solo unos pocos VCGs se encuentran dispersos por el mundo (Bentley et al., 1998; Koening et al., 1997; Mostert et al., 2017), lo cual explica la ausencia de una estructura genética detectable en las poblaciones muestreadas.
¿Por qué Foc es diverso y cosmopolita a nivel mundial, pero puede tener una estructura genética restrictiva a nivel local? Tres explicaciones posibles: una es que el patógeno se había dispersado de manera efectiva debido al intercambio de materiales contaminados (rizomas o hijuelos) (Ploetz, 2015). Otra explicación es que se trata de un complejo
polifilético, por lo que es posible que las cepas nativas hayan convergido parasíticamente con la introducción de Musa spp. (Gurr, 2011). La tercera posibilidad es que, efectivamente, Musa spp. pudo haberse dispersado junto con algunos linajes clonales de Foc que intercambiaron información genética mediante mecanismos parasexuales o quizá sexuales con linajes nativos locales (Ordoñez, 2018). En México no se conocen las dinámicas de dispersión de Foc (Ordoñez, 2018), aunque Foc, sobre todo la raza 1, está ampliamente distribuido en el territorio.
En conclusión, la morfología cultural de los aislamientos monospóricos de Fo fue consistente con lo reportado en la literatura para Fo. A pesar de la diversidad de haplotipos encontrada (16), H16 fue el más frecuente, mientras que los haplotipos restantes pueden estar distribuidos de manera amplia o local, pero con baja frecuencia. No se encontraron diferencias genéticas significativas entre las poblaciones estudiadas ni agrupadas por regiones. Por lo tanto, estos resultados, obtenidos mediante el uso de seis marcadores SSR, sugieren que las poblaciones analizadas constituyen una única metapoblación.











 texto en
texto en 


