Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista mexicana de fitopatología
versión On-line ISSN 2007-8080versión impresa ISSN 0185-3309
Rev. mex. fitopatol vol.42 no.spe Texcoco 2024 Epub 06-Jun-2025
https://doi.org/10.18781/r.mex.fit.2024-28
Articles
Control in vitro de Neopestalotiopsis sp. aislada de fresa empleando Trichoderma y fungicidas comerciales
1Universidad Politécnica de Guanajuato. Ingeniería Agroindustrial. Avenida Universidad Sur # 1001, Comunidad Juan Alonso. C.P. 38496. Cortázar, Guanajuato, México
2Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP), Campo Experimental Bajío. Carretera San Miguel de Allende-Celaya, km. 6.5. C.P. 38110. Celaya, Guanajuato, México
3Universidad Politécnica de Guanajuato. Ingeniería Agroindustrial. Avenida Universidad Sur # 1001, Comunidad Juan Alonso. C.P. 38496. Cortázar, Guanajuato, México
4INIFAP, Campo Experimental Valle de México. Carretera Los Reyes-Texcoco, km 13.5, C.P. 56120. Coatlinchan, Texcoco, México.
5Universidad de Guanajuato, Campus Celaya-Salvatierra, Departamento de Ingeniería Agroindustrial, Prolongación Río Lerma s/n, Col. Suiza. C.P. 38060. Celaya, Guanajuato, México
6Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP), Campo Experimental Bajío. Carretera San Miguel de Allende-Celaya, km. 6.5. C.P. 38110. Celaya, Guanajuato, México
7Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP), Campo Experimental Bajío. Carretera San Miguel de Allende-Celaya, km. 6.5. C.P. 38110. Celaya, Guanajuato, México
8Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP), Campo Experimental Bajío. Carretera San Miguel de Allende-Celaya, km. 6.5. C.P. 38110. Celaya, Guanajuato, México
Antecedentes/Objetivo.
El hongo Neopestalotiopsis sp. es un patógeno emergente que puede ocasionar pérdidas superiores al 70 % en el cultivo de fresa. Debido a esta situación, se busca implementar métodos de control de bajo impacto ecológico. El objetivo de este trabajo fue evaluar el efecto inhibitorio de cepas de Trichoderma sp. y de fungicidas empleados en el Bajío de Guanajuato, México, sobre el crecimiento de Neopestalotiopsis sp. Materiales y Métodos. El patógeno se aisló de plantas de fresa sintomáticas. Se realizó la caracterización morfológica y de patogenicidad del aislado. Las cepas de Trichoderma se obtuvieron de la colección biológica del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias Campo Experimental Bajío (CEBAJ) y se confrontaron en cultivos duales con el patógeno, se determinó el porcentaje de inhibición del crecimiento radial (PICR) a las 120 h. Además, se evaluó el efecto de cinco fungicidas comerciales, que se agregaron al medio de crecimiento, sobre el diámetro de crecimiento del hongo.
Resultados.
Se obtuvo PICR en un intervalo de 63 al 70 %. El mecanismo de parasitismo de Trichoderma fue por enrollamiento, adhesión y lisis a las hifas del patógeno. La cepa T1 fue la que presentó mayor potencial para el control del patógeno, seguido de T5 y T7. Tres fungicidas comerciales, Tebuconazol (100 mL 100 L-1), Extracto de Canela y Neem (500 mL 100 L-1), y el Ácido Peracético (25 mL 100 L-1) inhibieron completamente el crecimiento del hongo.
Conclusión.
Estos resultados contribuyen al conocimiento sobre el control de Neopestalotiopsis sp. con la aplicación de Trichoderma y los productos autorizados en México.
Palabras Clave: Inhibición de crecimiento fúngico; microorganismos benéficos; patógenos de fresa; Extracto de Canela-Neem; Ácido Peracético
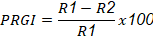 Background/Objective. The fungi Neopestalotiopsis sp. is an emerging pathogen that can cause losses of more than 70 % of production in strawberry crops. Due to this situation, is necessary to evaluate and implement control methods with low ecological impact. The objective of this work was evaluated the inhibitory growth of Neopestalotiopsis sp. using antagonist strains of Trichoderma sp. and fungicides used locally in the Bajio of Guanajuato, México.
Background/Objective. The fungi Neopestalotiopsis sp. is an emerging pathogen that can cause losses of more than 70 % of production in strawberry crops. Due to this situation, is necessary to evaluate and implement control methods with low ecological impact. The objective of this work was evaluated the inhibitory growth of Neopestalotiopsis sp. using antagonist strains of Trichoderma sp. and fungicides used locally in the Bajio of Guanajuato, México.
Materials and Methods.
The pathogen was isolated in strawberry symptomatic plants. The morphological and pathogenicity characterization of the isolate was carried out. The Trichoderma strains were obtained from the biological collection of the National Forestry, Agricultural and Livestock Institute (INIFAP), Bajio Experimental Field (CEBAJ), and were confront in dual cultures with the pathogen, the percentage of radial growth inhibition (PRGI) was calculated at 120 h. In addition, five commercial fungicides were added to the growth medium and was calculated the growth diameter of the fungus.
Results.
The PRGI by Trichoderma were observed in a range of 63 to 70 %. The mechanisms of parasitism for Trichoderma were curling, adhesion and lysis to the pathogen hypha. The T1 strain was the greatest potential for controlling the pathogen, followed by T5 and T7. Three fungicides, Tecobenazole (100 mL 100 L-1), Cinnamon and Neem extract (500 mL 100 L-1), and Peracetic Acid (25 mL 100 L-1) had 100 % inhibited of fungal growth.
Conclusion.
These results contribute to the knowledge on the control of Neopestalotiopsis sp. with the application of Trichoderma and the authorized products in Mexico
Keywords: Growth inhibition; beneficial microorganisms; pathogens strawberry; Cinnamon-Neem Extract; Peracetic Acid
Introducción
El cultivo de fresa (Fragaria x ananasa) tiene gran importancia económica para México y actualmente ocupa el tercer lugar como proveedor de fresa en el mundo, con un valor de la producción mayor de 15,400 millones de pesos (SIAP, 2024). No obstante, existen patógenos que pueden disminuir la producción y ocasionar pérdidas económicas como la enfermedad de la secadera ocasionada por especies del género Neopestalotiopsis, una de ellas de reciente introducción y que puede ocasionar mermas superiores al 70 % de la producción. La sintomatología incluye pudrición de raíz, corona y manchas foliares (Rebollar-Alviter et al., 2020), y en los frutos se presentan lesiones de aproximadamente 2-4 mm que se extienden hasta causar pudrición y momificación (Goldenhar y Pate, 2021). Debido a la escasa información del patógeno, se han estudiado estrategias de control en campo como prácticas culturales, control químico y biológico (Rebollar- Alviter et al., 2020). Se ha indicado que para el control de este patógeno se pueden emplear agentes antagónicos de los géneros Trichoderma, Bacillus y Pseudomonas (Zhang et al., 2024; Amrutha y Vijayaraghavan, 2018). En particular el efecto antagónico de Trichoderma se debe a la acción de enzimas, que pueden degradar la pared celular, quitina, proteínas y lípidos (Pandey et al. 2022). Además, produce metabolitos secundarios como policétidos, péptidos no ribosomales, terpenoides, pironas, antibiótico entre otros, los cuales funcionan como inhibidores del crecimiento; además, puede actuar como micoparásito, competir por espacio o por nutrientes (Mukherjee et al., 2012). En el caso del control con agroquímicos, aunque existen productos autorizados para emplearse en fresa (COFEPRIS, 2024), ya sea como molécula sintética o extractos vegetales, no es precisa la información para el control de Neopestalotiopsis. En este sentido, el objetivo de este trabajo fue evaluar el efecto inhibitorio de cepas de Trichoderma sp. sobre el crecimiento de este Neopestalotiopsis sp. aislada de fresa, y el control con fungicidas comerciales que se emplean en algunas localidades del Bajío de Guanajuato. La información que se generó muestra la importancia del uso de Trichoderma y fungicidas comerciales efectivos para reducir el crecimiento de este patógeno en la producción de fresa.
Materiales y métodos
Las cepas de Trichoderma sp. fueron proporcionadas por el Laboratorio de Microbiología Agrícola del Área de Transformación del Campo Experimental Bajío (CEBAJ) del Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias y previamente aisladas de diferentes sustratos y lugares de México (Cuadro 1). La reactivación se realizó en Papa Dextrosa Agar (PDA) a 26±2 °C.
Cuadro 1 Datos de identificación, sustrato de aislamiento y procedencia de cepas de Trichoderma sp. empleadas en el control biológico de Neopestalotiopsis sp.
| Nombre de la cepa | Sustrato | Lugar de procedencia |
|---|---|---|
| 8L9 | Lixiviado | Talea de Castro, Oaxaca, México |
| 1752 | Suelo agrícola | Santiago Coltzingo, Puebla, México |
| 1S1 | Composta | Palma Sola, Veracruz |
| THP | Suelo agrícola | San José de Pantoja, Valle de Santiago, Guanajuato, México |
| 675, T1, T2, T3, T4, T5, T6, T7 | Suelo agrícola, cultivo de plátano | Piedra Parada, Veracruz |
Aislamiento de Neopestalotiopsis sp. en fresa y caracterización morfológica
En julio de 2022 se aisló Neopestalotiopsis sp. de plantas sintomáticas de fresa var. San Andrés del invernadero de hortalizas del CEBAJ. Se colectaron hojas, frutos y tallos que se depositaron en bolsas de plástico para su traslado al laboratorio. Se cortaron trozos de tejido de aproximadamente 1 cm2 y se desinfestaron con NaClO 5% durante 60 segundos. Se lavaron tres veces con agua estéril, el material vegetal se dejó secar sobre una toalla de papel estéril. Posteriormente se sembró en cajas Petri desechables que contenían PDA y amoxicilina (30 mg 1000 µL-1), se incubaron a 26±2°C. Una vez que el patógeno esporuló, se tomó un acérvulo con una aguja de disección y se suspendió en 1000 µL de agua estéril, a continuación, la solución se homogenizó en vórtex y se tomaron 100 µL para sembrar por extensión en placa. La incubación se realizó a 26±2 °C por 24 h. Pasado este tiempo y bajo el microscopio estereoscópico se tomaron conidios germinados y se llevaron a medio PDA para la obtención de colonias monospóricas, las que se incubaron a 26±2 °C. La caracterización morfológica de Neopestalotiopsis sp. se realizó basándose en la descripción a nivel género con las características descritas por Maharachchikumbura et al. (2012) y Maharachchikumbura et al. (2014).
Pruebas de patogenicidad
Para comprobar la patogenicidad del aislado, se sembró el hongo y se dejó crecer por cinco días. Con ayuda de un sacabocado se tomaron cinco discos de 5 mm de medio invadido y se colocaron en la corona de la fresa. Este procedimiento se realizó en 15 macetas con plantas sanas de fresa var. San Andrés. Adicionalmente, se colocaron dos discos en hojas y tallos para corroborar la patogenicidad del hongo. Las plantas se regaron cada 48 h y se cubrieron con una bolsa de polietileno para alcanzar una humedad relativa > 90 %. Se observó la sintomatología que se presentó después de la inoculación (di).
Actividad antagónica de Trichoderma sobre Neopestalotiopsis sp.
Para determinar la actividad antagónica se empleó la metodología de cultivo dual descrita por Correa et al. (2007), que indica colocar un disco del patógeno y otro del hongo antagonista en lados opuestos, a 1 cm del borde de la caja Petri (90 x 15 mm). La prueba se realizó con ocho repeticiones en medio PDA libre de antibiótico. Se emplearon discos de 5 mm de diámetro de cultivo con micelio del patógeno y de las cepas de Trichoderma sp. previamente crecidos en PDA por cinco días, al patógeno se le dio ventaja de crecimiento de tres días. La incubación se realizó a 26±2 °C. Cada ocho horas se midió el crecimiento radial del patógeno hasta llegar a las 120 h. El porcentaje de inhibición del crecimiento radial (PICR) se obtuvo a partir del crecimiento de cada patógeno en el cultivo dual, junto con sus respectivos testigos, empleando la fórmula utilizada por Suárez et al. (2008):
𝑃𝐼𝐶𝑅 =
𝑅1 − 𝑅2
𝑅1
𝑋100
Donde PICR=porcentaje de inhibición de crecimiento radial; R1=crecimiento radial (mm) del patógeno sin Trichoderma, R2=crecimiento radial (mm) del patógeno con Trichoderma.
Adicionalmente, se evaluó la capacidad antagónica de los aislados seleccionados según la escala de Bell et al. (1982), donde Clase 1: el agente antagónico coloniza completamente al fitopatógeno y cubre totalmente la superficie del medio; Clase 2: el agente antagónico coloniza las dos terceras partes de medio de cultivo, limitando el crecimiento del fitopatógeno; Clase 3: el agente antagónico y el patógeno colonizan cada uno la mitad de la superficie, el crecimiento es similar, Clase 4: el fitopatógeno coloniza las dos terceras partes de la superficie del medio de cultivo y limita el crecimiento del agente antagónico, y Clase 5: el fitopatógeno coloniza completamente el medio del cultivo y crece sobre el agente antagónico. Se analizó el PICR mediante un análisis de varianza (ANOVA) con un diseño completamente al azar. La comparación múltiple de medias se realizó con el método de Tukey (p< 0.05). Los datos se analizaron con el Programa R versión 4.4.0.
Micoparasitismo
Para observar la presencia de parasitismo de las cepas de Trichoderma hacia Neopestalotiopsis se usó la técnica de microcultivos duales. En los ensayos se evaluaron 15 cepas de Trichoderma contrapuestas con el patógeno Neopestalotiopsisis, se realizaron tres repeticiones. Los microcultivos se prepararon con un portaobjetos a los que se les aplicó una capa de medio (16 g agar bacteriológico + 10 g PDA para 1 L), libre de antibiótico, para las confrontaciones se emplearon discos de 5 mm de diámetro del micelio del patógeno y de Trichoderma previamente crecidos en PDA por cinco días. En un extremo del portaobjetos se colocó un disco del patógeno, con una diferencia de 24 h, esto debido a que el crecimiento del patógeno presentó un crecimiento más lento en comparación con Trichoderma. En el extremo equidistante se colocó un disco de Trichoderma. Las preparaciones se incubaron a 26±2 °C. Cuando ambos hongos entraron en contacto (aproximadamente 24 h), se retiró el portaobjetos de la caja Petri y con ayuda de una tira de cinta adhesiva transparente se tomó una muestra de micelio, se agregó una gota de azul de algodón para poder observar bajo el microscopio y determinar el tipo de parasitismo de las cepas de Trichoderma.
Pruebas de inhibición de crecimiento de Neopestalotiopsis con fungicidas comerciales
Se determinó el efecto de inhibición sobre crecimiento del patógeno de cinco productos comerciales: el fungicida de contacto Captan (Captan 50®), el fungicida sistémico Tebuconazol (Folicur®), el fungicida sistémico Carbendazim (Agrosys®), Extracto de Canela y Neem (Nymeria®), Ácido Peracético (Microclean®) y un fungicida orgánico a base de cítricos de venta local. Cada fungicida se evaluó en tres concentraciones (Cuadro 2), que se eligieron considerando las recomendaciones de fabricante en la ficha técnica, se utilizó en una concentración mínima, una intermedia y la máxima recomendada. Se realizaron cinco repeticiones por cada concentración más un control. Las pruebas se realizaron en cajas Petri con PDA libre de antibióticos. Los fungicidas se incorporaron al medio cuando presentó una temperatura de 45-50 °C. Al centro de cada caja se colocó un disco de 5 mm del medio de crecimiento de Neopestalotiopsis, crecido previamente por cinco días en PDA. Cada 8 h se determinó el diámetro de crecimiento hasta llegar a las 120 h. El control se estableció en PDA sin fungicida. Las pruebas se realizaron con cinco repeticiones. Para el análisis estadístico los datos se acomodaron en un diseño completamente al azar. Estos datos se analizaron en un ANOVA utilizando el Programa de R versión 4.4.0. Se realizó la comparación múltiple de medias con el método de Tukey (p≤0.05).
Cuadro 2 Fungicidas evaluados en la inhibición del crecimiento de Neopestalotiopsis sp.
| Fungicida | Dosis (L-1) |
|---|---|
| Captan | 2 g (A), 3 g (B), 4 g (C) |
| Tebuconazol | 1 mL (D), 2.5 mL (E), 3.75 mL (F) |
| Carbendazim | 4 mL (G), 5 mL (H), 6 mL (I) |
| Extracto de Canela y Neem | 5 mL (J), 10 mL (K), 15 mL (L) |
| Ácido Peracético | 0.25 mL (M), 0.50 mL (N), 0.75 mL (O) |
| Fungicida orgánico a base de cítricos | 5 mL (P), 7.5 mL (Q), 10 mL (R) |
Nota: Las letras en el paréntesis se usarán para referir el tratamiento aplicado.
Resultados y discusión
Identificación de síntomas en plantas de fresa
Se observaron síntomas en plantas según lo documentado por Rebollar-Alviter et al. (2020): tizón en hojas, muerte regresiva de los brotes, pudrición y deformación de frutos, achaparramiento de plantas, así como pudrición de la raíz y la corona (Figura 1). Estos síntomas son similares entre especies de Neopestalotiopsis. Al respecto, Baggio et al. (2021) menciona que los tejidos más afectados por N. rosae son la raíz y cuello de la raíz, aunque tienen una baja incidencia en frutos y hojas. De la misma forma, autores como Obregón et al. (2018) indicaron que N. clavispora muestra síntomas en hojas en las que manifiestan zonas intervenales necróticas de color rojizo que comienzan en los márgenes y van avanzando conforme se hace senescente el tejido. Según los autores, la raíz y el cuello de esta también se ve afectado lo que finalmente provoca la muerte de la planta. La especie N. clavispora causa tizón en el cáliz y en el receptáculo de fresa (Shi et al., 2022).
Identificación del agente causal
Después de ocho días de crecimiento, las colonias en medio PDA presentaron textura algodonosa, micelio color blanco que fue tornándose a salmón y márgenes concéntricos. Cuando el cultivo tuvo seis días se formaron masas negras de esporas (Figura 2). A los 12 días se produjeron acérvulos globosos de color negro en el medio de crecimiento y sobre el tejido los estromas presentaron forma irregular (Figura 2). Los conidios presentaron tres células centrales de color oscuro y dos basales hialinas, con tres apéndices apicales (Figura 2). La morfología del patógeno coincidió con las características de género descritas por Maharachchikumbura et al. (2014); sin embargo, de acuerdo con algunas características señaladas por Maharachchikumbura et al. (2012), el aislado de Neopestaloptiopsis de este estudio podría tratarse de N. rosae, especie que fue confirmada presente en cultivo de fresa en México (Rebollar-Alviter et al., 2020).
Patogenicidad de Neopestaloptiosis sp.
Las plantas inoculadas con el aislado presentaron síntomas 24 h di (Figura 3), donde inicialmente se observaron pequeñas manchas marrones de 2 mm en hojas, después de 56 h di se observó tizón de hojas, necrosis en tallo y debilitamiento de la planta (Figura 3). Después de 168 h di los daños se encontraron muy avanzados, el tallo presentó necrosis en aproximadamente 70 % del tallo y ablandamiento total. Las manchas presentes en las hojas abarcaron más del 80 % de la superficie foliar (Figura 3). La sintomatología coincidió con la documentada por Rebollar Alviter et al. (2020) y Gilardi et al. (2019) en cultivo de fresa, tanto en hojas como en fruto.
Actividad antagónica de Trichoderma sobre Neopestalotiopsis
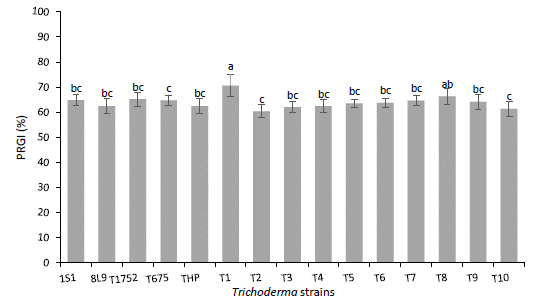
El análisis estadístico indicó que existieron diferencias significativas (p < 0.05) en la inhibición del crecimiento entre las cepas evaluadas. De acuerdo con la comparación de medias se encontraron tres grupos de inhibición, la cepa T1 fue la que presentó el mayor PICR (70 %), mientras que las cepas T675, T2 y T10 fueron las que exhibieron menor inhibición (Figura 4). En general el PICR se mantuvo entre el 60 al 70 %, por lo que las cepas pueden considerarse con potencial para el control del patógeno. Al respecto Yao et al. (2023) tras un análisis de diferentes estudios indica que una cepa de Trichoderma puede considerarse con potencial en el control efectivo de la enfermedad cuando la inhibición de crecimiento supera el 50 %.

Figura 3 Síntomas en plantas de fresa causadas por Neopestalotiopsis sp. A) Tizón en hojas, B) Necrosis en tallo y C) Necrosis en cuello y raíz.
Algunos autores han evaluado el efecto de Trichoderma para el control de Neopestalotiopsis. Uno de los primeros trabajos fue el de Mora-Morales et al. (2020) quienes evaluaron in vitro el efecto antagónico de T. harzianum sobre Pestalotiopsis (Neopestalotiopsis sp.), sus resultados mostraron una PICR del 71.11 %. Otros autores como Amrutha y Vijayaraghavan (2018) evaluaron el efecto antagónico de T. asperellum contra Neopestalotiopsis clavispora aislada de fresa, determinaron en promedio 66 % de inhibición en el crecimiento del patógeno en pruebas in vitro; y una reducción de la enfermedad del 74 %. Los autores indicaron que para el manejo de la enfermedad con productos biológicos y químicos es necesario considerar las condiciones agroclimáticas para tener una mayor eficiencia en el control. En otro estudio realizado por Liu et al. (2024) en el que evaluaron el efecto antagónico de metabolitos volátiles y metabolitos de fermentación producidos por T. asperellum sobre el crecimiento de N. clavispora, determinaron inhibición de 79.67 y 69.84 %, respectivamente. También identificaron que, el efecto antagónico se debió a la competencia por el sustrato, producción de antimicóticos y parasitismo. Adicionalmente, indicaron que la aplicación de T. asperellum promovió el crecimiento de la fresa, la altura de la planta, la longitud de la raíz, el peso fresco total, el peso de la raíz, el peso fresco del tallo y el peso seco de la raíz. Por otra parte, Pandey et al. (2022) determinaron que T. reesei incidió en el crecimiento in vitro de Pseudopestalotiopsis theae, sus resultados mostraron una inhibición del 81.2 %. Cuando llevaron el experimento a plantas en condiciones de vivero la severidad de la enfermedad fue de entre 67.5 y 75 %. En este sentido los autores indicaron que T. reesei fue capaz de producir metabolitos volátiles y no volátiles con efecto inhibitorio, además en las plantas inoculadas con el antagonista encontraron acumulación de enzimas de defensa como polifenol oxidasa, peroxidasa, fenilalanina amonio liasa, β-1, 3-glucanasa, y quitinasa. De la misma forma, a los 45 di estas plantas mostraron aumento en la altura, diámetro del tallo, peso brotes y raíces.
Antagonismo de las cepas de Trichoderma
Según la escala de Bell et al. (1982), se encontraron niveles de antagonismos II y III (Cuadro 3, Figura 5), es decir en el tipo II las cepas de Trichoderma colonizaron las dos terceras partes de medio de cultivo, limitando el crecimiento del fitopatógeno; en el III, Trichoderma y el patógeno colonizaron cada uno la mitad de la superficie, el crecimiento fue similar entre las cepas (Cuadro 3). Diversos autores han indicado que Trichoderma posee diferentes mecanismos de antagonismo, destacando el micoparasitismo, competencia por espacio y alimento y la antibiosis (Álvarez et al., 2022). Uno de los principales es el micoparasitismo, pueden presentar estructuras en forma de ganchos, enrollamientos o apresorios alrededor del hospedante que le permiten penetrar al interior del patógeno y degradarlo (Mukherjee et al., 2022; Álvarez et al., 2022). Este mecanismo está acompañado por la secreción de enzimas como la quitina para degradar la pared celular del patógeno (Yao et al., 2023; Companioni-González et al., 2019).
En este estudio se encontraron los mecanismos de micoparasitimo: adhesión y enrollamiento de las cepas de Trichoderma a la hifa del patógeno, además de lisis de hifa, formación de ganchos y penetración del antagonista al patógeno (Figura 6).
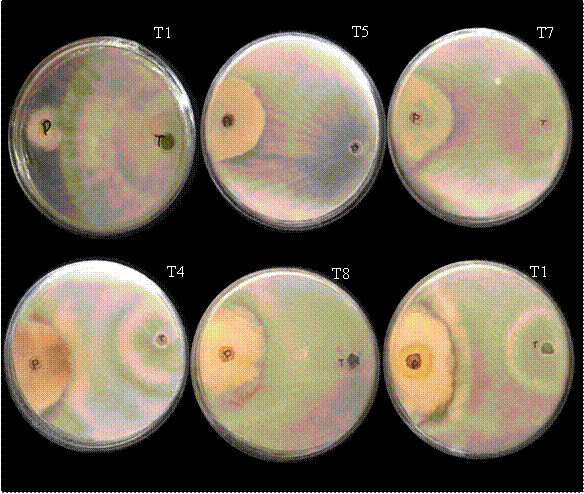
Figura 5 Confrontaciones de cepas de Trichoderma contra Neopestalotiopsis sp. Donde T = Trichoderma y P = patógeno. El número que se encuentra en la parte superior derecha corresponde a la identificación de la cepa de Trichoderma. Se observa que T1, T5 y T7 mantiene un nivel de antagonismo de II, mientras que T4, T8 y T10 un nivel III.
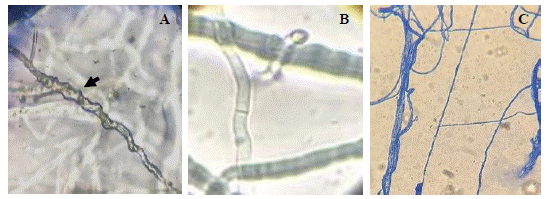
Figura 6 Mecanismos de parasitismo de Trichoderma sp frente a Neopestaloptiopsis sp. A) Enrollamiento, B) Formación de ganchos y C) Adhesión y lisis.
Cuadro 3 Nivel de antagonismo según Bell et al. (1982) y mecanismos de micoparasitismo.
| Nivel de antagonismo | Cepa | Mecanismo del micoparasitismo |
|---|---|---|
| II | 1S1, T175, T675, T5 | Adhesión, enrollamiento |
| II | 8L9, T3 | Enrollamiento, formación de ganchos |
| II | THP | Lisis, enrollamiento |
| II | T1, T2 | Adhesión |
| II | T3 | Enrollamiento, formación de ganchos |
| II | T6 | Adhesión, enrollamiento, formación de ganchos |
| II | T7 | Adhesión, penetración a hifa |
| III | T4, T8 | Enrollamiento |
| III | T9, T10 | Enrollamiento, formación de ganchos |
Evaluación de control de Neopestalotiopsis sp. empleando fungicidas comerciales
De acuerdo con el análisis estadístico, se encontraron diferencias significativas entre tratamientos. La comparación de medias indicó que el fungicida sistémico Tebuconazol, el Extracto de Canela y Neem, y el Ácido Peracético, en todas las concentraciones empleadas, fueron los productos que inhibieron el crecimiento de Neopestalotiopsis sp. en 100 % (Figura 7). El fungicida de contacto Captan inhibió el crecimiento del patógeno en 81, 83 y 86 %, siguiéndole el fungicida orgánico a base de cítricos con 52, 60 y 63 %; y el fungicida sistémico Carbendazim inhibió en un 28, 42 y 52 % con respecto al testigo.
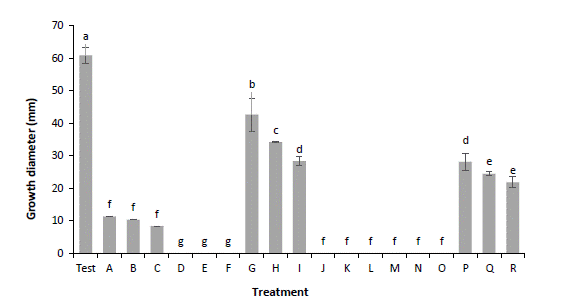
Figura 7 Crecimiento de Neopestalotiopsis sp en medio PDA con fungicidas comerciales. Test: testigo sin producto; A-C: Captán 200, 300 y 400 g 100 L-1; D-F: Tebuconazol 100, 250 y 375 mL 100 L-1; G-I: Carbendazim 400, 500 y 600 mL 100 L-1; J-L: Extracto de Canela y Neem 500, 1000 y 1500 mL 100 L-1; M-O: Ácido Peracético 25, 50 y 75 mL 100 L-1; P-R: Fungicida orgánico a base de cítricos 500, 750 y 1000 mL 100 L-1. 400 g y 600 mL 100 L-1 (p≤0.05).
Debido a las grandes pérdidas económicas que ha generado Neopestaloptiopsis se han realizado estudios para determinar el manejo de la enfermedad, al respecto Rebollar- Alviter et al. (2020) evaluaron el control in vitro de Neopestaloptiosis rosae empleando Captan y otros productos como Azoxistrobin, Fenopyroxad + Piraclostrobina, Piraclostrobina + Boscalid, Iprodiona, Difenoconazol, Prochloraz, Cyprodinil + Fludioxonil. Los resultados en cuanto a la inhibición en el crecimiento del patógenos sugirieron que Captan, Fludioxonil + Cyprodinil, Difenoconazol e Iprodion tuvieron el mayor efecto para el control de Neopestaloptiopsis. De la misma forma, Baggio et al. (2023) realizaron estudios para determinar la sensibilidad de patógeno frente a fungicidas comerciales, sus resultados indicaron que Captan, Thiram y Clorotalonil tuvieron mayor efectividad. Autores como Acosta-González et al. (2024) señalaron que, al aplicar fungicidas, principalmente Pidiflumetofen + Fludioxonil, Ciprodinil + Fludioxonil y Procloraz de forma preventiva, lograron la disminución de la incidencia y severidad de la enfermedad, también disminuyó la mortalidad de las plantas. Los autores indicaron que cuando los fungicidas se aplicaron de forma preventiva se consiguió una eficiencia del 99 al 100 %; sin embargo, cuando se usaron de forma curativa, es decir después que se expresaron los síntomas, la eficiencia fue de 0 al 37 %.
Por otro lado, productos a base de extractos vegetales como ajo, manzanilla, ruda, canela, tagetes, acacia, neem, chile, pimienta, agave, ruda, ricino, chicalote, pino, cítricos, gobernadora y otros, están autorizados en México como plaguicidas para el cultivo de fresa (COFEPRIS, 2024). Por lo tanto, son una alternativa importante para el manejo orgánico en este cultivo. Los resultados que se obtuvieron en este trabajo con el Extracto de Canela y Neem demostraron que puede aplicarse para inhibir el crecimiento del patógeno sin causar estragos ambientales a largo plazo. Otros autores como Darapanit et al. (2021) demostraron que extractos etanólicos a base de cúrcuma (Curcuma longa), jengibre (Zingiber officinale), zacate limón (Cymbopogon citratus), jamaica (Hibiscus sabdariffa) y clavo de olor (Syzygium aromaticum) inhibieron el crecimiento de cepas de Neopestalotiopsis y Pseudopestalotiopsis, principalmente los extractos de Cúrcuma y clavo de olor en concentraciones de 10,000 mg L-1. En general los extractos a base de plantas producen metabolitos secundarios como esteroides, alcaloides, taninos, terpenos, fenoles, flavonoides y resinas que presentan propiedades antimicrobianas (Lengai et al., 2020).
Conclusiones
El control in vitro obtenido con las 15 cepas de Trichoderma evaluadas se determinó por el PICR en un intervalo de 63 al 70 %. La cepa T1 fue la que presentó mayor porcentaje de inhibición en el crecimiento radial del patógeno. El nivel de antagonismo que se encontró fue clase II y clase III, con mecanismos de parasitismo de enrollamiento, adhesión a la hifa del patógeno y lisis. En el caso del control de crecimiento del patógeno con los fungicidas, se determinó 100 % de inhibición con Tebuconazol, Extracto de Canela y Neem y Ácido Peracético; los ingredientes activos Captan y Carbendazim tuvieron una inhibición del crecimiento del 86 y 52 % con las dosis 400 g y 600 mL 100 L-1, respectivamente. Los resultados de este estudio son referencia para el desarrollo de un manejo integral con aplicaciones preventivas y de control con Trichoderma sp. y productos orgánicos como alternativa a moléculas químicas, que contribuyen en la reducción de inóculo primario proporcionando una protección a las plantas una vez establecidas en campo.
References
Acosta-González, U. Leyva-Mir, S.G. Silva-Rojas, H.V. Rebollar-Alviter, A. 2022 Preventive and Curative Effects of Treatments to Manage Strawberry Root and Crown Rot Caused by Neopestalotiopsis rosae Plant Disease 108 1278-1288 10.1094/PDIS-05-23-0958-RE [ Links ]
Álvarez, P. Román, A. Tamayo, L. Guerra, L. Tuburcia, A. 2022 Efeito de Trichoderma harzianum e Trichoderma longibrachiaum no crescimento de Chionanthus pubescens, Eucalyptus cinerea e Cupressus macrocarpa em viveiro Revista Agraria Acadêmica 5 5 62-71 10.32406/v5n5/2022/62-71/agrariacad [ Links ]
Amrutha, P. Vijayaraghavan, R. 2018 Evaluation of Fungicides and Biocontrol Agents against Neopestalotiopsis clavispora causing leaf blight of strawberry (Fragaria x ananassa Duch.) International Journal of Current Microbiology and Applied Sciences 7 8 622-628 10.20546/ijcmas.2018.708.067 [ Links ]
Baggio, J.S. Forcelini, B.B. Wang, N.Y. Ruschel, R.G. Mertely, J.C. Peres, N.A. 2021 Outbreak of leaf spot and fruit rot in Florida strawberry caused by Neopestalotiopsis spp. Plant Disease 105 2 305-315 10.1094/PDIS-06-20-1290-RE [ Links ]
Baggio, S.J. Rebello, S.C. de Morais, B.M. Marin, V.M. Gama, B.A. Forcelini, B.B. Mertely, C.J. Peres, A.N. 2023 Efficacy of Single- and Multi-Site Fungicides Against Neopestalotiopsis spp. of strawberry Plant Disease 107 7 10.1094/PDIS-08-22-1929-RE [ Links ]
Bell, D. Well, H. Markham, C. 1982 In vitro antagonism of Trichoderma species against six fungal plant pathogens Phytopathology 72 379-382 10.1094/Phyto-72-379 [ Links ]
COFEPRIS, Comisión Federal para la Protección contra Riesgos Sanitarios 2024 Consulta de Registros Sanitarios de Plaguicidas, Nutrientes Vegetales y LMR https://siipris03.cofepris.gob.mx/Resoluciones/Consultas/ConWebRegPlaguicida.asp (consulta, enero 2024) [ Links ]
Companioni-González, B. Domínguez-Arizmendi, G. García-Velasco, R. 2019 Trichoderma: su potencial en el desarrollo sostenible de la agricultura Biotecnología Vegetal 19 4 237-248 [ Links ]
Correa, S. Mello, M. Ávila, Z. Minare, L. Pádua, R. Gomes, D. 2017 Cepas de Trichoderma spp. para el control biológico de Sclerotium rolfsii SAAC Fitosanidad 11 1 3-9 [ Links ]
Darapanit, A. Boonyuen, N. Leesutthiphonchai, W. Nuankaew, S. Piasai, O. 2021 Identification, pathogenicity and effects of plant extracts on Neopestalotiopsis and Pseudopestalotiopsis causing fruit diseases Scientific Reports 11 1 22606 10.1038/s41598-021-02113-5 [ Links ]
Gilardi, G. Bergeretti, F. Gullino, M.L. Garibaldi, A. 2019 First report of Neopestalotiopsis clavispora causing root and crown rot on strawberry in Italy Plant Disease 103 2959 10.1094/PDIS-03-19-0673-PDN [ Links ]
Goldenhar K Pate E 2021 Pest Alert: Neopestalotiopsis - an emerging strawberry disease in North America https://onfruit.ca/wp-content/uploads/2021/03/Pest-Alert-Neopestalotiopsis-.pdf (consulta, agosto 2023) [ Links ]
Lengai, G.M.W. Muthomi, J.W. Mbega, E.R. 2020 Phytochemical activity and role of botanical pesticides in pest management for sustainable agricultural crop production Scientific African 7 e00239 10.1016/j.sciaf.2019.e00239 [ Links ]
Liu, P. Yang, R. Wang, Z. Ma, Y. Ren, W. Wei, D. Ye, W. 2024 Biocontrol Potential of Trichoderma asperellum CMT10 against Strawberry Root Rot Disease Horticulturae 10 246 10.3390/horticulturae10030246 [ Links ]
Maharachchikumbura, S.S.N. Guo, L.D. Cai, L. Chukeatirote, E. Wu, W.P. Sun, X. Crous, P.W. Bhat, D.J. McKenzie, E.H.C. Bahkali, A.H. Hyde, K.D. 2012 A multi-locus backbone tree for Pestalotiopsis, with a polyphasic characterization of 14 new species Fungal Diversity 56 95-129 10.1007/s13225-012-0198-1 [ Links ]
Maharachchikumbura, S.S.N. Hyde, K.D. Groenewald, J.Z. Xu, J. Crous, P.W. Pestalotiopsis revisited Studies in Mycology 79 121-186 10.1016/j.simyco.2014.09.005 [ Links ]
Morales-Mora, L.A. Andrade-Hoyos, P. Valencia-de Ita, M.A. Romero-Arenas, O. Silva-Rojas, H.V. Contreras-Paredes, C.A. 2020 Characterization of strawberry associated fungi and in vitro antagonistic effect of Trichoderma harzianum Revista Mexicana de Fitopatología 38 3 434-449 10.18781/r.mex.fit.2005-7 [ Links ]
Mukherjee, M. Mukherjee, P.K. Horwitz, B.A. Zachow, C. Berg, G. Zeilinger, S. 2012 Trichoderma-plant-pathogen interactions: advances in genetics of biological control Indian Journal of Microbiology 52 4 522-529 10.1007/s12088-012-0308-5 [ Links ]
Mukherjee, P.K. Mendoza-Mendoza, A. Zeilinger, S. Horwitz, B.A. 2022 Mycoparasitism as a mechanism of Trichoderma-mediated suppression of plant diseases Fungal Biology Reviews 39 15-33 10.1016/j.fbr.2021.11.00 [ Links ]
Obregón, V.F. Meneguzzi, N.G. Ibañez, J.M. Lattar, T.E. Kirschbaum, D.S. 2018 First report of Neopestalotiopsis clavispora causing root and crown rot on strawberry plants in Argentina Plant Disease 102 9 1856 10.1094/PDIS-02-18-0330-PDN [ Links ]
Pandey, A.K. Kumar, A. Samota, M.K. Tanti, A. 2022 Trichoderma reesei as an elicitor triggers defense responses in tea plant and delays gray blight symptoms Pesticide Biochemistry and Physiology 188 105279 10.1016/j.pestbp.2022.105279 [ Links ]
Rebollar-Alviter, A. Silva-Rojas, H.V. Fuentes-Aragón, D. Acosta-González, U. Martínez-Ruiz, M. Parra-Robles, B.E. 2020 An emerging strawberry fungal disease associated with root rot, crown rot and leaf spot caused by Neopestalotiopsis rosae in Mexico Plant Disease 104 8 2054-2059 10.1094/PDIS-11-19-2493-SC [ Links ]
Shi, J. Zhang, X. Liu, Y. Zhang, Z. Wang, Z. Xue, C. Ma, Y. Wang, F. 2022 First Report of Neopestalotiopsis clavispora Causing Calyx and Receptacle Blight on Strawberry in China Plant Disease 106 4 1307 10.1094/PDIS-07-21-1376-PDN [ Links ]
SIAP, Servicio de Información Agroalimentaria y Pesquera 2024 Anuario Estadístico de la Producción Agrícola https://nube.siap.gob.mx/cierreagricola/ Consulta, enero 2024 [ Links ]
Suárez, C. Fernández, R. Valero, N. Gámez, R. Páez, A. 2008 Antagonismo in vitro de Trichoderma harzianum Rifai sobre Fusarium solani (Mart.) Sacc. asociado a la marchitez en maracuyá Revista Colombiana de Biotecnología 10 3 35-43 [ Links ]
Yao, X. Guo, H. Zhang, K. Zhao, M. Ruan, J. Chen, J. 2023 Trichoderma and its role in biological control of plant fungal and nematode disease Frontiers in Microbiology 14 10.3389/fmicb.2023.1160551 [ Links ]
Zhang, S. Wu, J. Chen, J. Jun, S. Yuan, Y. Dai, X. Wang, F. Ma, Y. 2024 The biological control effect of Bacillus cereus on strawberry leaf spot disease caused by Neopestalotiopsis clavispora Scientia Horticulturae 327 1 112841 10.1016/j.scienta.2024.112841 [ Links ]
Recibido: 10 de Julio de 2024; Aprobado: 23 de Diciembre de 2024











 texto en
texto en