Introducción
México ocupa el noveno lugar como productor mundial de jitomate (Solanum lycopersicum). En el ciclo agrícola 2018-2019 produjo un total de 938,009 t, siendo Sinaloa, el estado que encabezó la lista de productores a nivel nacional con 605,261 t (SIAP, 2020). Sin embargo, las plagas y enfermedades son los principales problemas que impactan a este cultivo (Jones et al., 2016).
Dentro de las enfermedades en jitomate, la raíz corchosa es escasamente estudiada a pesar de ser muy problemática; dicha enfermedad desarrolla lesiones de color café y raíces corchosas. En un inicio, la lesión es limitada y posteriormente se extiende progresivamente y rodea las raíces, desarrollando lesiones que van desde algunos milímetros hasta varios centímetros (Blancard, 2011). En este contexto, la enfermedad denominada raíz corchosa, es uno de los problemas más graves en los últimos años en predios agrícolas dedicados al cultivo de jitomate en México (Pardo, 1999; Martínez-Ruiz et al., 2016).
Aunque la enfermedad de raíz corchosa se observa a menudo en cultivos en invernadero, y su distribución se reportó principalmente en Europa (Schneider, 1966), Estados Unidos (Campbell et al., 1982), Líbano (Davet, 1973) y Chile (Olavarria, 1991); no hay suficientes estudios relacionados con el agente causal de la enfermedad (USDA, 2017).
De manera general, la raíz corchosa en jitomate esta asociada a Pseudopyrenochaeta lycopersici (sin. Pyrenochaeta lycopersici) como su agente causal (Golzar, 2009); sin embargo, en un estudio realizado en México, se demostró con base en datos morfológicos, análisis filogenéticos y pruebas de patogenicidad, que la raíz corchosa en campos de Sinaloa es causada por Setophoma terrestris y que, además, podía causar raíz rosada en el cultivo (López-López et al., 2020).
Según De Gruyter et al. (2010), S. terrestris y P. lycopersici comparten características morfológicas y genéticas muy similares, las cuales se diferenciaron taxonómicamente de acuerdo con análisis filogenéticos con datos de secuencias concatenadas de la región ITS y fragmentos del gen LSU (Valenzuela-López et al., 2018). Setophoma es un género de hongo que forma picnidios, los cuales son estructuras de reproducción asexual. El picnidio puede tener forma globosa a subglobosa, así como setas (de allí el origen del prefijo del género “seto”), con un cuello ostiolar alrededor. Dentro de los picnidios se encuentran las esporas denominados conidios, que son hialinos, cilíndricos, aseptados y principalmente gutulados (De Gruyter et al., 2010).
Setophoma terrestris se ha estudiado mayormente en el cultivo de cebolla (Allium cepa), ya que es su principal hospedante, ocasionando la enfermedad conocida como raíz rosada, la cual es de importancia y alto impacto económico a nivel mundial. Este hongo primero ataca el sistema radical y progresivamente afecta a la planta hasta la muerte (Castillo y Plata, 2010). También se reportó causando daños a otros hospedantes como: canola (Brassica napus) en Canadá (Yang et al., 2017), calabacita (Curcubita maxima) en EE. UU. (Rivedal et al., 2018), así como plantas de ajo (Allium sativum) y de té (Camellia sinensis) en China (Liu et al., 2019; Zhang et al., 2019).
En un trabajo previo (López-López et al., 2020) se demostró por primera vez la naturaleza infecciosa de Setophoma terrestris en plantas de jitomate (S. lycopersicum) en México, con base a un solo aislado. El objetivo de este estudio fue caracterizar morfológica y molecularmente a los aislados fúngicos asociados a los síntomas de raíz corchosa y rosada en campos de jitomate de Culiacán, Sinaloa, así como evaluar su patogenicidad.
Materiales y Métodos
Recolección de muestras. Las muestras se recolectaron en cinco sitios (Figura 1), los cuales se encuentran distribuidos en cinco localidades dentro del Valle de Culiacán, así como en los límites de Navolato, Sinaloa, con producción intensiva de jitomate de crecimiento indeterminado en etapa de producción (tres meses de edad). Estos sitios tenían antecedentes de presencia de raíz corchosa y rosada en jitomate. En algunas plantas en etapa de cosecha, se observaron diferentes tipos de síntomas en el área foliar; como clorosis y reducción del crecimiento. Por ello, se hizo un muestreo dirigido de acuerdo a los síntomas mencionados. También, se revisaron las raíces de las plantas mediante su extracción y observación de daños a lo largo de las mismas. Una vez confirmados los síntomas relacionados a la enfermedad en el cultivo, se recolectaron 15 muestras de raíces de jitomate enfermas por cada sitio. Los lugares de colecta fueron invernaderos de tipo casa sombra de aproximadamente 5 ha cada una. Finalmente, se colocaron en bolsas de plástico y se trasladaron a las instalaciones del Laboratorio de Fitopatología, de la Coordinación Culiacán del CIAD para su análisis.
Aislamiento, purificación y conservación de hongos. Las raíces enfermas se sumergieron en agua potable para eliminar el exceso de suelo sin lastimar el tejido
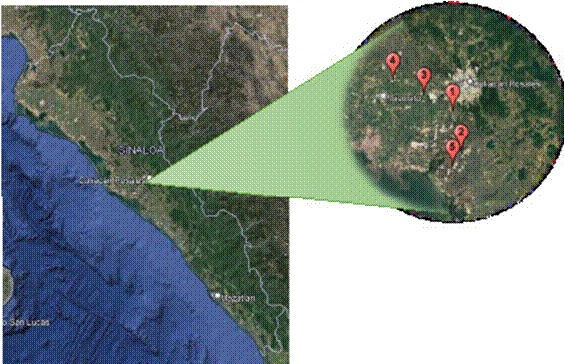
Figura 1 Localización de los sitios de recolección de plantas con síntomas de raíz corchosa en agrícolas con producción de jitomate en el valle de Culiacán, Sinaloa. Sitio 1 (24°42’56.58”N, 107°26’42.86”O), Sitio 2 (24°35’21.67”N, 107°24’56.50”O), Sitio 3 (24°46’2.77”N, 107°32’51.30”O), Sitio 4 (24°48’47.44”N, 107°39’26.19”O) y Sitio 5 (24°32’34.07”N, 107°26’44.93”O).
vegetal. Posteriormente, a partir de lesiones necróticas desarrolladas en las raíces de jitomate, se cortaron fragmentos de 5 mm de longitud, luego se desinfestaron en la superficie mediante inmersión en una solución de hipoclorito de sodio al 2 % durante 2 minutos, se enjuagaron en agua destilada estéril y se colocaron en placas Petri con medios de cultivo papa dextrosa agar acidificado (APDA) y jugo V8 agar acidificado (V8A), y se incubaron a 25 ºC en oscuridad continua. Posteriormente, se realizó la transferencia de los aislados fúngicos a nuevas placas Petri con V8A y después de 10 días en incubación a 25 ºC, se purificaron los aislados mediante la técnica de cultivos monospóricos (Crous et al., 2019). El cuál consistió en colocar los picnidios sobre portaobjetos y los conidios se observaron bajo el microscopio compuesto, a partir de estos conidios, se obtuvieron cultivos monospóricos en placas Petri con medio V8A y a los 7 días después de la siembra se observó el crecimiento de micelio color rosa. La conservación de los aislados fúngicos se realizó colocando discos de 4 mm de diámetro a partir de colonias con cinco días de crecimiento y se preservaron a temperatura ambiente en tubos estériles de 2 mL conteniendo agua destilada estéril para resguardarse en la colección de cepas del Laboratorio de Fitopatología en CIAD, Unidad Culiacán.
Caracterización morfológica. Con la finalidad de estimular la producción de estructuras asexuales, se colocaron aproximadamente tres raíces de jitomate en cámaras húmedas a temperatura de 20 ºC. A los 30 días, se retiraron y se observaron en el microscopio estereoscópico, localizando los picnidios y colocándolos en portaobjetos con agua destilada estéril para su observación y caracterización.
La caracterización morfológica de los aislados se realizó usando claves y descripciones reportadas por De Gruyter et al. (2010). Para ello, se cultivó el hongo en cajas Petri con medio V8A por un periodo de 10 días. Los aislados que no formaron picnidios en el medio V8A, se estimularon mediante el método descrito por Clerjeau (1973), el cual consiste en colocar raíces de plántulas de melón (Cucumis melo) sobre el micelio del hongo de interés con 5-7 días de crecimiento y posteriormente incubar nuevamente a temperatura ambiente (25-30 ºC) por 15 a 20 días para la producción artificial de picnidios. Una vez que estos se obtuvieron, se examinaron las características de los picnidios, conidios y setas en un microscopio compuesto (Zeiss®, Alemania) con cámara digital integrada (AxioCam) y se realizaron 50 mediciones de cada una de las diferentes estructuras fúngicas asexuales de cada aislado.
Extracción de ADN, amplificación por PCR y secuenciación. La extracción de ADN total se realizó a partir de colonias fúngicas de siete días de edad, cultivadas en medio V8A. El micelio de cada aislado se raspó con un portaobjetos estéril, se maceró en un mortero estéril usando nitrógeno líquido y se transfirió a un tubo de microcentrífuga de 1.5 mL con 500 µL de solución de Bromuro de hexadeciltrimetilamonio, CTAB (Tris 100 mM, pH 8; 20 mM de EDTA, pH 8; NaCl, 1.4 M y 3 % de CTAB), se mezcló con vórtex por 10 s y se incubó por 60 min a 65 °C. Se agregaron 700 µL de cloroformo-alcohol isoamílico (24:1v/v), se pasó por vórtex por 10 s y se colocó en una centrífuga 5810 R (Eppendorf®, EE. UU.) a 13000 g durante 10 min. Después, el sobrenadante se transfirió a un tubo de microcentrífuga de 1.5 mL y se agregó 700 µL de isopropanol. Los tubos se mezclaron por inversión de cuatro a cinco veces y se dejaron a -20 °C durante 10 min, luego se centrifugó a 13000 g durante 10 min para precipitar el ADN. Posteriormente, se realizaron dos lavados del precipitado con 500 µL de etanol al 70 %, centrifugando a 13000 g por 5 min y desechando el sobrenadante en cada vez. Enseguida, se dejó secar la pastilla de ADN colocando los tubos invertidos sobre papel secante por no más de 15 min para permitir la evaporación del etanol y finalmente, se resuspendió el ADN en 100 µL de agua estéril libre de DNAsa y RNAsa. La calidad y concentración del ADN se evaluó en un espectrofotómetro Q 3000 UV (Quawell, EE. UU.) y electroforesis en geles de agarosa al 1 %, considerando adecuado el ADN con valores de pureza (relación de A260/280) entre 1.8 y 2.0 y concentración (A260) de aproximadamente 2.0 µg µL-1, así como bandas íntegras de alto peso molecular, respectivamente. El ADN se almacenó a -20 °C para su uso posterior.
La amplificación de la región ITS del DNAr y la subunidad larga (LSU) se realizó mediante la reacción en cadena de la polimerasa (PCR) en punto final. La región ITS (ITS1-5.8S-IT2) se amplificó usando los iniciadores ITS1 (TCCGTAGGTGAACCTGCGG) e ITS4 (TCCTCCGCTTATTGA TATGC) con 480 pb aproximadamente (White et al., 1990), mientras que la banda amplificada del gen LSU (incluyendo los dominios D1 y D2) se realizó mediante una PCR anidada usando los iniciadores PM3 (Takamatsu y Kano, 2001) /TW14 (Mori et al., 2000) y NL1/ TW14 (Mori et al., 2000) para la primera y segunda reacción, respectivamente. La mezcla de reacción se preparó a un volumen final de 25 µL, conteniendo amortiguador de PCR 1X, 2.5 mM de MgCl2, 0.5 mM de dNTPs, 1 µM de cada iniciador, 1U de ADN polimerasa (Promega®, EE. UU.) y 100 ng de ADN. La PCR se realizó bajo las siguientes condiciones de termociclado (termociclador C-1000, Bio-Rad®, EE.UU.): desnaturalización inicial de 95 ºC por 5 min, 35 ciclos de 95 ºC por 30 s, 54 ºC por 30 s, 72 ºC por 30 s, con una extensión final de 72 ºC por 10 min. Para la amplificación del gen 28S se usó las mismas condiciones de termociclado excepto por la temperatura de alineamiento, la cual fue de 52 ºC. Los productos amplificados se analizaron por electroforesis en gel de agarosa al 1 %, teñido con bromuro de etidio. La electroforesis se realizó a 90 V por 40 min y los resultados se visualizaron en un transiluminador M-26X en un sistema de imágenes GelDoc-ItTM 300 (UVP®, EE. UU.). Los productos de PCR se purificaron mediante el kit DNA Clean & Concentrator (Zymo Research®, EE. UU), de acuerdo con las recomendaciones del fabricante y se secuenciaron en la empresa Macrogen (www.macrogen.com) en Seúl, Corea del Sur.
Análisis filogenético. La calidad de las secuencias de nucleótidos y el método de ensamblaje se realizaron utilizando el Paquete Staden (Staden et al., 2000). Las secuencias se limpiaron y las generadas a partir de la región del ITS y la subunidad grande (LSU) del ARNr se alinearon con secuencias de diferentes especies del género Setophoma obtenidas del GenBank y a partir de datos de referencia publicados (De Gruyter et al., 2010; Liu et al., 2019) (Cuadro 1). Se generaron alineamientos múltiples de secuencias utilizando ClustalW tal como se implementó en MEGA 11 (Tamura et al., 2021) y se mejoraron manualmente para permitir la máxima similitud entre el conjunto de datos. Las estimaciones filogenéticas bayesianas se infirieron con MrBayes 3.2.6 (Ronquist et al., 2012) implementado en el clúster CIPRES (https://www.phylo.org/portal2/home.action) y seleccionando el modelo de sustitución nucleotídica que mejor se ajustó a los datos de esta investigación,
Cuadro 1 Información de los aislados fúngicos y números de acceso del GenBank de especies de Setophoma usadas en el análisis filogenético.
| Taxon | Código de colección | Hospedante | País | No. de acceso LSU | No. de acceso ITS |
|---|---|---|---|---|---|
| Setophoma antiqua | LC6594 | Camellia sinensis | China | MK511947 | MK511909 |
| LC6595 | C. sinensis | China | MK511948 | MK511910 | |
| S. chromolaenae | CBS 135105x | Chromolaena odorata | Brasil | KF251747 | KF251244 |
| S. cyperi | CBS 141450x | Cyperus sphaerocephala | Sudáfrica | KX228337 | KX228286 |
| S. endophytica | CGMCC 3.19528 | C. sinensis | China | MK511956 | MK511931 |
| LC3164 | C. sinensis | China | MK511957 | MK511932 | |
| S. longinqua | LC6593x | C. sinensis | China | MK511946 | MK511908 |
| S. poaceicola | MFLUCC 16-0880x | - | Tailandia | KY550386 | KY568988 |
| Setophoma | CGMCC 3.19526 | Carbonatita en cueva | China | MK511965 | MK511944 |
| S. sacchari | MFLUCC 12-0241 | Saccharum officinarum | Tailandia | KJ476147 | KJ476145 |
xaislados ex-tipo. Los números de acceso de las secuencias generadas en este estudio se destacan en negrita.
CBS: Colección de aislados en Centraal bureauvoor Schimmelcultures, Fungal Biodiversity Centre, Utrecht, Países Bajos; IMI: Colección de aislados de CABI Europe UK Centre, Egham, Reino Unido; CPC: Colección de trabajo de Pedro W. Crous, alojada en CBS. CGMCC: Centro General de Recolección de Cultivos Microbiológicos de China, Instituto de Microbiología, Academia de Ciencias de China, Beijing, China; LC: Colección de trabajo de Lei Cai, alojada en el Instituto de Microbiología, Academia China de Ciencias, Beijing, China; MUCL: Mycothèque de l’Université catholique de Louvain, Louvain-la-Neuve, Bélgica.
de acuerdo con el criterio de información de Akaike (AIC) obtenido con MrModeltest 2.3 (Nylander, 2004). El número de generaciones fue de 10.000.000 y las probabilidades posteriores se calcularon después de descartar el primer 25 % de las iteraciones. Los árboles filogenéticos se visualizaron con TreeView (Page, 1996).
Pruebas de patogenicidad. La patogenicidad de siete aislados fúngicos se determinaron mediante la inoculación en la raíz principal de plántulas de jitomate cv. 8444 de 30 días de edad. Se utilizaron 10 plantas por cada uno de los aislados, además de 10 plantas no inoculadas que se sirvieron como control. Se utilizaron discos de V8A de 4 mm de diámetro con crecimiento activo del hongo por aislado, los cuales se colocaron sobre una herida previamente realizada con un palillo de madera (mondadiente). El disco micelial se sujetó a la herida de la raíz usando papel Parafilm® (EE. UU.). En las plantas testigo, se realizó la herida y se colocó un disco con medio de cultivo V8A sin crecimiento fúngico. Las plantas se mantuvieron en un invernadero a temperatura de 20-35 ºC durante 30 días. Posteriormente, se extrajeron las raíces inoculadas y se reaislaron los hongos en medio V8A. Una vez desarrollado el micelio, se consideraron las características morfológicas y culturales como son pigmentación del medio V8A, así como los caracteres cualitativos y cuantitativos de setas, picnidios y conidios de acuerdo a lo descrito previamente. La prueba se repitió dos veces.
Resultados y Discusión
Se observaron síntomas de clorosis y senescencia de hojas, así como reducción del crecimiento de plantas de jitomate (Figuras 2A-C) en una incidencia que varió de 10 a 20 % en los cinco diferentes campos agrícolas comerciales muestreados en el valle de Culiacán, Sinaloa, México. Las raíces sintomáticas desarrollaron lesiones de color café oscuro, hinchadas y con textura corchosa (Figura 2D-E) y rosada (Figura 2F). Estos síntomas en el área foliar y sistema radical concuerdan con los reportados por López-López et al. (2020); mientras que el mismo agente causal afectaron plantas de jitomate reportados en Brasil, Canadá, EE. UU. y Venezuela (Farr y Rossman, 2022). Asimismo, estos síntomas se registraron en otros hospedantes, como en cebolla china (Allium fistulosum) en China (Luong et al., 2008). De manera similar, los síntomas de la enfermedad de raíz corchosa y rosada en jitomate coinciden con los descritos para S. terrestris en cebolla (Schwartz y Mohan, 2008).
La sintomatología de raíz rosada puede ser similar a la causada por Pseudopyrenochaeta lycopersici, la cual se registró en un amplio número de hospedantes como sorgo (Sorghum), maíz (Zea mays), caña de azúcar (Saccharum officinarum) (Sprague, 1950), césped (Cynodon dactylon) (Conners, 1967), puerro (Allium porrum) (Hall et al., 2007), melón (Cucumis melo), calabacita (Curcubita pepo), trigo (Triticum) y espinaca (Spinacia oleracea) (USDA, 1960) y en árboles de sauce (Salix) (Pfleger y Vaughn, 1972). Por otra parte en el cultivo de jitomate lo han reportado en Australia (Golzar, 2009), África (Testen et al., 2019) Alemania (ValenzuelaLópez et al., 2018) y en Estados Unidos como patógeno asociado a la pudrición café de la raíz del jitomate (Vrisman et al., 2017).

Figura 2 Síntomas de raíz corchosa y rosada en jitomate. A-C) Clorosis, crecimiento deficiente y senescencia en plantas. D-F) Lesiones en la raíz de color café oscuro, hinchadas, con textura corchosa y rosada.
Aislamiento e identificación morfológica. De las 15 muestras (plantas) de raíces de jitomate con síntomas de raíz corchosa y rosada por sitios, se trabajaron con siete aislados fúngicos, provenientes de los cinco sitios previamente señalados en el mapa con sus respectivas coordenadas en el Valle de Culiacán. La técnica que funcionó para el aislamiento de los hongos fue colocar secciones de tejidos infectados en cámara húmeda para la estimulación de los picnidios en los tejidos de las raíces a temperatura de 4 ºC (Gilchrist-Saavedra et al., 2005).
Los aislados obtenidos corresponden a Setophoma terrestris, y las colonias fueron de color rosa anverso y reverso, con crecimiento radial (80 mm) a los 7 días de crecimiento (Figuras 3A-B). Dichas características de crecimiento del hongo en medio V8A fueron similares a las reportadas por De Gruyter et al. (2010).
La examinación morfológica de las estructuras asexuales mostraron picnidios globosos a obpiriformes, de color negro a café oscuro (Figura 3C) y de 142-220 × 104-140 µm. Se observó la presencia de setas de color café oscuro, septadas, de 52-114 × 2-8 µm y que rodeaban el cuello ostiolar (Figura 3D). Los conidios fueron hialinos, cilíndricos, de 2-8 × 1-3 µm, y con dos gútulas muy características en sus extremos (Figuras 3E-F). Todos los caracteres morfológicos observados coincidieron con los reportados por otros autores (Koenning et al., 2007; Wiriyajitsomboon, 2015; Yang et al., 2017; Rivedal et al., 2018; Zhang et al., 2019) (Cuadro 2). A pesar de que algunas mediciones fueron variables entre sí, estos datos no son contundentes para diferenciar entre una u otra especie, por lo cual se requieren de herramientas moleculares y análisis filogenéticos para la confirmación a nivel de especie.
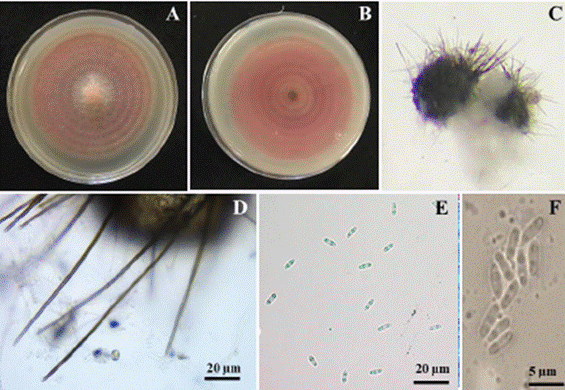
Figura 3 Colonias y estructuras de reproducción asexual de Setophoma terrestris. A) Colonia de S. terrestris en medio V8A con 7 días de crecimiento. B) Crecimiento de colonia en el reverso de la placa. D) Picnidio. D) Setas. E-F) Conidios gutulados.
Cuadro 2 Medidas de estructuras asexuales en aislados de Setophoma terrestres obtenidos en plantas de jitomate.
| Setas (µm) | Picnidio (µm) | Conidio (µm) | Referencia |
|---|---|---|---|
| yNA | yNA | 4.5-5.5 × 1.8-2.3 | Koenning et al., 2007 |
| ≈ 100-120 | ≈ 200 | ≈ 4-5 | Wiriyajitsomboon, 2015 |
| ≈ 100 | ≈ 300 | ≈ 5 | Yang et al., 2017 |
| yNA | yNA | 5.0 × 2.0 | Rivedal et al., 2018 |
| 55-150 | 160-230 | 4.0-5.0 × 1.5-2.0 | Zhang et al., 2019 |
| 68-84 × 2-3 | 237-345 × 105-250 | 5-7 × 2-3 | López-López et al., 2020 (CCLF01) |
| 52-114 × 3-6 | 150-183 × 133-156 | 6-7 × 2-3 | zCCLF02 |
| 60-108 × 2-5 | 142-160 × 124-132 | 6-8 × 2-3 | zCCLF03 |
| 46-102 × 3-5 | 200-233 × 110-130 | 4-6 × 2-3 | zCCLF04 |
| 55-106 × 3-4 | 220-231 × 105-133 | 2-3 × 1-1.5 | zCCLF05 |
| 67-90 × 2.5-4 | 216-255 × 104-140 | 3-4 × 1-2 | zCCLF06 |
| 90-107 × 3-8 | 175-180 × 140-155 | 5-8 × 2-3 | zCCLF07 |
| 60-101 × 3-5 | 160-175 × 137-153 | 5-6 × 2-3 | zCCLF08 |
yNA: No aplica / No se reportaron
zLas mediciones generadas en este estudio se destacan en negrita en referencias.
Respecto a los rangos de valores morfométricos, se observó que los siete aislados de S. terrestris de este estudio se distribuyeron en tres grupos de acuerdo a medidas ascendentes: grupo 1 integrado por el aislado CCLF05, grupo 2 por CCLF06 y CCLF04, y por último el grupo 3 con los aislados CCLF07, CCLF08, CCFL02 y CCLF03. Es importante mencionar que en el grupo 3, también se encuentra el aislado (CCLF01) reportado previamente en otro estudio en Sinaloa, México (LópezLópez et al., 2020).
Por su parte, Luong et al. (2008) identificaron a S. terrestris como agente causal de raíz rosada en cebolla utilizando características de la colonia y observaron el pigmento rosa en el medio de cultivo, así como las setas en los picnidios y conidios típicos de este género en algunas raíces rosadas. Además, observaron grandes gútulas en los conidios de sus aislados, las cuales coinciden con las reportadas en este estudio. Estas mismas características microscópicas en los conidios fueron descritas por De Gruyter y Boerema (2002).
Similarmente, Ikeda et al. (2012) identificaron como agente causal de raíz rosada en calabacita a S. terrestris y obtuvieron dos aislados que formaron picnidios de color café a negro oscuro, de forma subglobosa a globosa y con cuello ostiolar con setas alrededor. Estas setas se observaron de forma cilíndrica y de color café a café oscuro, y sus medidas fueron 104-262 × 3.5-6.9 µm. Estas características y medidas coinciden con las obtenidas en este estudio.
Por otra parte, las medidas pueden tener ligeras diferencias entre los aislados y lo antes señalado se puede deber a múltiples factores ambientales que afectan el desarrollo del patógeno, tal como lo mencionaron Burton et al. (1997), haciendo una relación con los síntomas de la enfermedad en melón y sandía e identificando al agente causal con base a estructuras morfológicas y analisis de secuencias ITS. A diferencia de nuestros aislados, los picnidios reportados por Duarte y Barreto (2015), no cuentan con las típicas setas alrededor del ostíolo, señalando que este atributo no es un carácter genérico. Asimismo, las características que comparten los hongos P. lycopersici y S. terrestris son muy similares a diferencia que, en P. lycopersici las setas de sus picnidios son superiores a 200 µm de longitud, mientras que S. terrestris regularmente oscilan desde 50-150 µm aproximadamente (De Gruyter, 2010).
Análisis filogenético. Las secuencias alineadas correspondientes a la región ITS y la subunidad mayor (LSU), resultaron en una longitud total de 1,345 nucleótidos. El análisis filogenético generado con MrBayes basado en el conjunto de datos (Figura 4) mostraron que todos los aislados obtenidos en este estudio se agruparon con la especie Setophoma terrestris, con un soporte alto de probabilidad posterior (1.0).
Por otra parte, en el análisis filogenético se observaron dos agrupamientos, los cuales en su mayoría aborda todos los aislados con un 0.88 de probabilidad posterior, excepto por el aislado CCLF05, el cual se agrupó de manera separada y presentó la mayor diferencia filogenética. Asimismo, con lo previamente mencionado y de acuerdo a la morfometría se agrupo en un solo grupo. Con base en esto, se pudo comprobar nuevamente que Pseudopyrenochaeta lycopersici, no es la especie responsable de causar la enfermedad conocida como raíz corchosa y rosada en Sinaloa, México.
El análisis filogenético de este estudio concuerda con la identidad molecular reportada por Rivedal et al. (2018), quienes utilizaron la región ITS, encontrando que el ADN de todos sus aislados mostraron una similitud del 99 % con Setophoma terrestris. Asimismo, esas secuencias también se compararon con las reportadas por De Gruyter et al. (2010), obteniendo resultados similares. Por otra parte, Duarte y Barreto (2015) utilizaron el mismo criterio de análisis de inferencia bayesiana, pero como la diferencia que se apoyaron únicamente en secuencias LSU, mientras que en este trabajo se analizaron secuencias concatenadas ITS y LSU. Esto es de gran importancia ya que en estos años se ha demostrado y avalado que estos géneros son muy cercanos entre sí y se distinguen únicamente al realizar análisis filogenéticos con secuencias concatenadas (De Gruyter et al., 2010). Dicha información es de gran importancia, ya que el género Phoma ha crecido para adaptar a más de 3000 especies que forman picnidios con conidios hialinos y septados (Aveskamp et al., 2008), reevaluando así varios estudios relacionados con este género al identificarse correctamente (Boerema et al., 2004).
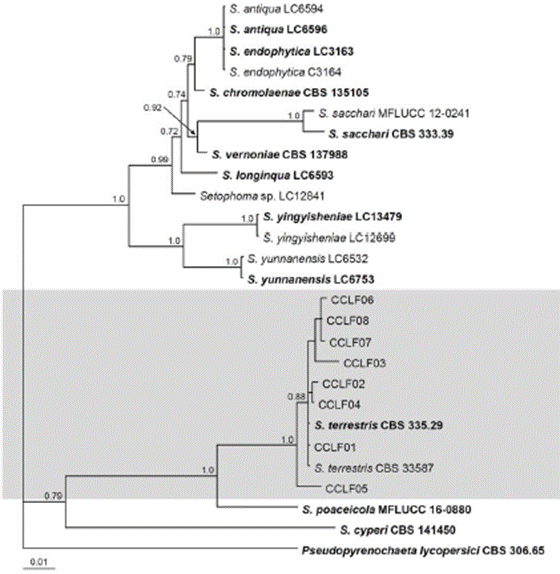
Figura 4 Árbol Bayesiano obtenido con datos combinados de secuencias ITS y LSU. El árbol muestra las relaciones filogenéticas de las especies de Setophoma. Los valores de probabilidad posterior Bayesiana por encima de 0.70 se muestran en los nodos. La especie Pseudopyrenochaeta lycopersici se utilizó como grupo externo y la barra de escala indica el número de cambios esperados por sitio.
Pruebas de patogenicidad. Treinta días después de la inoculación, las hojas mostraron amarillamiento (Figuras 5A-B). Las raíces de jitomate inoculadas mostraron textura corchosa y coloración rosada (Figura 5C), los cuales fueron similares a los síntomas observados en campo. De los reaislamientos, se obtuvieron colonias (Figura 5D) y estructuras fúngicas idénticas a las del hongo inoculado, lo que

Figura 5 Pruebas de patogenicidad en plantas de jitomate. A-B) Plantas de jitomate variedad 8444 inoculadas con S. terrestris y mostrando síntoma de amarillamiento. C) Síntoma de raíz corchosa a los 30 días después de la inoculación con S. terrestris. D) Colonia obtenida del reaislamiento in vitro de S. terrestris.
confirmó la patogenicidad de los siete aislados inoculados, mientras que las raíces de las plantas control permanecieron asintomáticas.
Los resultados de las pruebas de patogenicidad de este estudio, concuerdan con los reportados por Zhang et al. (2019), quienes observaron síntomas típicos de raíz rosada en ajo. Asimismo, este patógeno también se ha encontrado causando daño a otros hospedantes como: canola (Brassica napus) en Canadá (Yang et al., 2017), calabacita (Curcubita maxima) en EE. UU. (Rivedal et al., 2018), planta del té (Camellia sinensis) en China (Liu et al., 2019).
Los síntomas observados en las pruebas de patogenicidad del estudio llevado a cabo por Zhang et al. (2019), mostraron que S. terrestris causó clorosis, marchitez y muerte en plantas de ajo en un lapso de 40 días, dato similar a lo descrito por López-López et al. (2020), y que a su vez concuerda con los resultados en este estudio. Esto demuestra que Pseudopyrenochaeta lycopersici no es el agente causal de la raíz corchosa en campos de jitomate en Sinaloa, México, como se estuvo considerando por mucho tiempo.
Por otra parte, se comprobó que S. terrestris es un patógeno de lento crecimiento y desarrollo, ya que en las pruebas de patogenicidad de Rivedal et al. (2018) mostraron síntomas de raíz rosada a las 12 semanas después de la inoculación en calabaza de invierno, mientras que en nuestras pruebas fue de 4 semanas, esto pudiera deberse a que la relación patógeno-hospedante es diferente. De manera similar, Yang et al. (2017) utilizaron discos miceliales de S. terrestris en Canola, observando a los 21 días síntomas de raíz corchosa y rosada, lo cual concuerda con el tiempo aproximado en este estudio. El tiempo que tarda el patógeno en colonizar el tejido vegetal puede verse afectado por las condiciones en las que se encuentre, es decir, después de multiples reactivaciones en medios de cultivo su tasa de crecimiento varia (de Gruyer y Borema, 2002), posiblemente perdiendo así el grado de virulencia original de cada aislado, y por consecuencia, retrasar la visibilidad de los síntomas de la enfermedad en estudio.
Conclusiones
De acuerdo con la caracterización morfológica, identificación molecular y pruebas de patogenicidad, se confirmó que Setophoma terrestris es el agente causal de la enfermedad conocida como raíz corchosa y rosada en campos agrícolas de jitomate distribuidos en Culiacán, Sinaloa. El análisis morfológico mostró que en Setophoma terrestres se observaron picnidios de 142-220 × 104-140 µm, setas de color café oscuro de 52-114 × 2-8 µm y conidios de 2-8 × 1-3 µm. Asimismo, se obtuvieron tres agrupamientos de los aislados donde se observaron variaciones de valores morfométricos y filogenéticos. Los síntomas que presentaron las plantas de jitomate infectadas fue corchosis y raíz rosada, así como, disminución de cantidad de raíces.











 texto en
texto en 


