Introducción
Las bacterias asociadas a plantas sobreviven como epífitas o endófitas (Agrios, 2005), y en la mayoría de los casos, realizan funciones que mantienen el balance del sistema como la fijación de nitrógeno y el antagonismo contra fitopatógenos (Arauz, 2011; Nion y Toyota, 2015; Compant et al., 2019; Hashem et al., 2019). Estas bacterias comparten nicho con las bacterias fitopatógenas que utilizan las plantas como fuente de nutrientes y se han especializado en evadir sus defensas y en consecuencia invadir los tejidos de la planta hospedera (Vidaver y Lambrecht, 2004; Agrios, 2005; Kannan y Bastas, 2015).
En Costa Rica, se han reportado varios géneros como patógenos de plantas ornamentales y follajes como Erwinia, Pectobacterium, Pseudomonas, Xanthomonas, Burkholderia y el complejo de especies de Ralstonia solanacearum (Arauz, 2011; Quesada-González y García-Santamaría, 2014; Cubero-Agüero et al., 2021; López, 2021; Vidaurre-Barahona et al., 2021). La infección causada por estas bacterias puede manifestarse como manchas en frutos (Pseudomonas syringae y Xanthomonas campestris), cancros (Erwinia y Pseudomonas) marchitamiento (Ralstonia solanacearum) y pudrición blanda (Pectobacterium carotovorum y Dickeya dadanti) (Vidaver y Lambrecht, 2004; Agrios, 2005; Arauz, 2011; Bellincampi et al., 2014). La variedad de síntomas y de hospederos hacen a estos patógenos responsables de daños severos en cultivos y, por ende, en la economía del sector agrícola. Adicionalmente, estas enfermedades son más graves y frecuentes en zonas tropicales y subtropicales, donde las condiciones de calor y humedad son ideales para su desarrollo, y no hay disminución del inóculo por efecto de las bajas temperaturas del invierno (Arauz, 2011; Kannan y Bastas, 2015; Miller et al., 2022). Por lo tanto, el combate de estos patógenos es vital para conservar la productividad de los agroecosistemas; sin embargo, pocas sustancias son eficaces o se encuentran disponibles para mitigar la pérdida de la cosecha (Stockwell y Duffy, 2012), entre las que se encuentran los antibióticos.
Actualmente, los antibióticos de mayor uso a nivel mundial son la estreptomicina, oxitetraciclina, penicilina, ácido oxonólico y gentamicina (McManus et al., 2002; Mann et al., 2021; Miller et al., 2022), de los cuáles la estreptomicina y oxitetraciclina son aprobados para la agricultura en Estados Unidos, a diferencia de la Unión Europea y otros países desarrollados donde no son permitidos (Miller et al., 2022), debido a su importancia para el uso médico (WHO, 2019). La aplicación de antibióticos es el método más utilizado para el manejo de enfermedades bacterianas en algunos países de bajo o mediano ingreso (PBMI) (Miller et al., 2022), tal es el caso en Latinoamérica y el Caribe donde son usados sin restricción a pesar del riesgo de desarrollo de resistencia (Rodríguez et al., 2006; Rodríguez et al., 2008; MSP, 2018; Taylor y Reeder, 2020), y con resultados variables en el combate de enfermedades bacterianas en los cultivos (McManus et al., 2002; Stockwell y Duffy, 2012), ya que, aunque las bacterias fitopatógenas tienen habilidad de penetrar en los tejidos vegetales y multiplicarse (Sundin et al., 2016), la mayoría de las formulaciones son aplicadas en la parte aérea, de manera que su absorción, translocación y eficiencia son reducidas (McManus et al., 2002; Agrios, 2005). Por ejemplo, la absorción de oxitetraciclina en cítricos vía foliar es muy limitada, por lo que se recurre a la inyección al tronco para el combate de Candidatus Liberibacter asiaticus en este cultivo (Killiny et al., 2020).
Los bactericidas y antibióticos son los compuestos más utilizados para el control de bacterias fitopatógenas en Costa Rica (Ramírez-Muñoz et al., 2014; DuránQuirós et al., 2017; Blanco-Meneses et al., 2023), entre los que se encuentran la oxitetraciclina, la gentamicina, así como mezclas de estos con estreptomicina (gentamicina y oxitetraciclina en Agri-Gent Plus 4 y 8, estreptomicina y oxitetraciclina en Agry-mycin 16.5) (Rodríguez et al., 2006; Galt, 2009; MSP, 2018). La ausencia de un sistema de registro integrado en el país limita controlar el uso eficiente de estos productos en humanos, animales y vegetales (MSP, 2018). De la Cruz et al. (2008) determinaron que el consumo de antibióticos en el cultivo de Cucumis melo, Citrullus lanatus y Oriza sativa en el Distrito de riego Arenal-Tempisque fue de 7.4-155.0 g ha-1 al año tanto para estreptomicina como oxitetracilina; otros estudios indican que existe variabilidad entre productores en las dosis, frecuencia de uso y período de carencia (tiempo de suspensión de la aplicación antes de la cosecha) (Durán-Quirós et al., 2017; Blanco-Meneses et al., 2023).
Los antibióticos pueden permanecer activos en la superficie de la planta al menos una semana (Stockwell y Duffy, 2012), lo que aunado a su uso frecuente puede generar bacterias resistentes (Silbergeld et al., 2008; Alós, 2014; FAO, 2021). Al respecto, Rodríguez et al. (2006; 2008) identificaron bacterias epífitas resistentes a gentamicina y oxitetraciclina en muestras de lechuga (Lactuca sativa) y en suelos agrícolas, así como determinantes genéticos de resistencia, lo que implica una diseminación de bacterias resistentes entre los diferentes ambientes y/o una transferencia horizontal de genes de resistencia. No obstante, no se ha estudiado la presencia de bacterias fitopatógenas resistentes a antimicrobianos en el país por lo que este estudio tuvo como objetivo analizar la diversidad de una colección de bacterias aisladas a partir de lesiones provenientes de diferentes cultivos con síntomas de infección bacteriana en Costa Rica y evaluar su resistencia a los antibióticos estreptomicina, oxitetraciclina y gentamicina, utilizados para el manejo de enfermedades bacterianas de plantas en este país.
Materiales y Métodos
Aislamientos bacterianos. Se analizaron 116 bacterias Gram negativas pertenecientes a la colección del Laboratorio de Microbiología Ambiental del Centro de Investigación en Biología Celular y Molecular. Las bacterias se aislaron durante el 2006 al 2009 de muestras provenientes de diferentes zonas agrícolas de Costa Rica. Se consideró tejido de la zona de avance de lesiones en plantas que presentaron síntomas asociados con patógenos bacterianos. En el Cuadro 1 se presenta información pertinente respecto al cultivo, tipo de tejido, síntoma observado y sitio de colecta.
Cuadro 1 Características de colecta de aislados bacterianos establecida a partir de síntomas de 19 cultivos en diferentes zonas de Costa Rica entre 2006 al 2009.
| Planta hospedera | Nombre común | Nº de muestras | Tejido | Síntomas observados | Sitio de colecta | Nº de aislamientos |
|---|---|---|---|---|---|---|
| Apium graveolens | Apio | 3 | Tallo | Pudrición blanda (Figura 1D) | Cartago | 6 |
| Bactris gasipaes | Palmito | 3 | Hoja | Necrosis | Limón | 6 |
| Brassica oleracea var. botrytis | Coliflor | 2 | Hoja | Mancha | Heredia | 5 |
| Brassica oleracea var. capitata | Repollo | 6 | Hoja | Necrosis angular (Figura 1H), Mancha, Pudrición blanda | Heredia, Cartago | 25 |
| Capsicum annuum | Chile dulce | 2 | Fruto | Pudrición blanda (Figura 1E) | Cartago | 9 |
| Cucumis melo | Melón | 1 | Fruto | Pudrición blanda | Guanacaste | 5 |
| Cucurbita pepo | Zapallo | 1 | Fruto | Pudrición blanda (Figura 1G) | Cartago | 3 |
| Curcuma longa | Cúrcuma | 2 | Raíz | Pudrición blanda | Guanacaste | 4 |
| Daucus carota | Zanahoria | 1 | Raíz | Pudrición blanda | Alajuela | 1 |
| Dracaena massangeana | Dracaena | 2 | Tallo | Pudrición blanda (Figura 1F) | Alajuela | 7 |
| Ficus carica | Higo | 1 | Hoja | Mancha | Alajuela | 1 |
| Lactuca sativa | Lechuga Boston | 2 | Hoja | Mancha (Figura 1A) | Cartago | 5 |
| Lactuca sativa var. capitata | Lechuga Iceberg | 6 | Tallo y Hoja | Pudrición blanda (Figura 1B), Mancha | Cartago | 11 |
| Mangifera indica | Mango | 2 | Fruto | Mancha (Figura 1I) | Alajuela | 4 |
| Musa paradisiaca | Banano | 5 | Tallo y Corona | Pudrición blanda, Necrosis del tallo | Limón | 12 |
| Ornithogalum arabicum | Ornamental | 1 | Hoja | Pudrición blanda | Alajuela | 2 |
| Phaseolus vulgaris | Frijol | 2 | Hoja | Mancha | Heredia | 3 |
| Solanum lycopersicum | Jitomate | 3 | Fruto y Hoja | Manchas del fruto y hoja, Pudrición blanda de fruto | Alajuela, Cartago | 6 |
| Solanum tuberosum | Papa | 1 | Raíz | Pudrición blanda | Cartago | 1 |
| Total | 46 | 116 |

Figura 1 Síntomas de infección bacteriana de los que fueron aisladas las bacterias de la colección analizada en este estudio. A. Mancha de la hoja en Lechuga Boston, B. Pudrición blanda en Lechuga Iceberg, C. mancha necrótica en Jitomate. D. Pudrición blanda en Apio. E. Pudrición blanda en Chile dulce. F. Pudrición blanda en Dracaena. G. Pudrición blanda en Zapallo. H. Necrosis angular en Repollo. L. Mancha del fruto en Mango.
Identificación de la colección de bacterias mediante análisis del gen ARN 16S ribosomal. Cada bacteria se inoculó en 3 mL de caldo nutritivo, se incubó por 2448 horas a 30 °C, y el crecimiento obtenido fue centrifugado por 5 min a 10000 r.p.m, hasta obtener la biomasa. Se extrajo el ADN contenido en esta biomasa siguiendo el protocolo de extracción reportado por Fontecha (2003). Posteriormente, se realizó la amplificación del gen ARNr 16S utilizando cebadores universales: 27F (AGAGTTTGATCMTGGCTCAG) y 1492R (TACGGYTACCTTGTTAC-GACTT) (Weisburg et al., 1991). Cada reacción de PCR se llevó a cabo en 50 μL de mezcla con 0.8 μL (200 μM) de cada dNTPs (Thermo Scientific), 2.5 μL (1.25 mM) de MgCl2 (Thermo Scientific), 2.0 μL (0.4 μM) de cada cebador, 0.5 U de Taq ADN polimerasa (Thermo Scientific), 5.0 μL de buffer con KCl y sin MgCl2 1X (Thermo Scientific) y ~10 ng de ADN genómico. Se amplificaron las reacciones con el programa y condiciones reportadas por Fontecha (2003): Etapa de desnaturalización a 94 ºC por 4 min, seguida por 34 ciclos compuestos de desnaturalización a 94 ºC por 30 segundos, hibridización a 50 ºC por 30 s y extensión a 72 ºC por 90 s, y por último una extensión a 72 ºC por 10 min. Los productos de PCR fueron visualizadas en un gel de agarosa al 1 %. Los productos de amplificación fueron purificados utilizando el kit Wizard PCR Preps DNA Purification System (Promega, Madison, Wisconsin, Estados Unidos) según las instrucciones del fabricante y fueron secuenciados en un equipo ABI PRISM 3130 con el kit BigDye® Terminator v3.1 Cycle Sequencing RR-100 (Applied BioSystems) o, alternativamente, en la compañía Macrogen (Corea). Las secuencias resultantes fueron ensambladas utilizando el software BioEdit Sequence Alignment Editor Versión 7.2 (Hall, 1999). La búsqueda de homología se realizó utilizando la base de datos BLASTN del NCBI (National Center for Biotechnology Information) para encontrar similitudes con secuencias depositadas en el GenBank (Altschul et al., 1997), y utilizando una extensión de EzbioCloud (Yoon et al., 2017) cuya base de datos almacena secuencias del gen del ARNr 16S de cepas de referencia y con asignaciones taxonómicas válidas y publicadas.
Análisis filogenético. Las secuencias se alinearon utilizando ClustalX (Larkin et al., 2007) en el programa MEGA (Tamura et al., 2013), y se realizó el análisis con secuencias de cepas tipo de referencia y Bacillus subtilis (NR112116) como grupo externo. Las distancias evolutivas se calcularon mediante la inferencia de Neighbour joining y se evaluó la topología del árbol realizando 1,000 remuestreos. El árbol fue visualizado utilizando la herramienta ITOL (https://itol.embl.de.com). Las secuencias obtenidas se depositaron en la base de datos GenBank del NCBI bajo el bioproyecto PRJNA898399.
Identificación de aislamientos por sistema semiautomatizado Biolog™. Se utilizó el sistema Biolog™ para la identificación de aislamientos que no presentaron resultados concluyentes en la identificación molecular. Este sistema compara las reacciones redox de 95 fuentes de carbono y otras sustancias con la base de datos que incluye bacterias ambientales entre ellas fitopatógenas. Para esto se sembraron los cultivos de bacterias de 24 horas de cada aislamiento en las placas de identificación siguiendo las instrucciones del fabricante. Las lecturas se realizaron 24 h después y se documentó la identificación más cercana según el software del equipo Biolog.
Perfil de susceptibilidad a antibióticos y determinación de la concentración mínima inhibitoria (CMI). Se analizó la susceptibilidad a los antibióticos estreptomicina, gentamicina y tetraciclina con el método de difusión en agar de KirbyBauer, usando mono-discos impregnados con cantidades estándar de antibióticos comerciales (Oxoid), 10 mg en el caso de estreptomicina y gentamicina y 30 mg para la tetraciclina. Los discos se colocaron sobre cultivos de cada aislamiento en el medio de cultivo Muller-Hinton, y posteriormente se midió el halo de inhibición de crecimiento (Sánchez y Guerrero, 2006), que se comparó con los puntos de corte únicos arbitrarios basados en las recomendaciones para bacterias de origen clínico de las mismas familias taxonómicas descritas a continuación: Resistente a Tetraciclina (≤ 14 mm), intermedio (15-18 mm), sensible (≥19 mm). Resistente a Gentamicina (≤ 12 mm), intermedio (13-14 mm), sensible (≥ a 15 mm). Resistente a Estreptomicina (≤ 11 mm), intermedio (entre 12-14 mm), sensible (≥15 mm), que corresponden a los cortes para Pseudomonas aeruginosa, Acinetobacter sp. y enterobacterias (NCCLS, 2000). Se utilizaron como controles las cepas E. coli (ATCC-25922) y Pseudomonas aeruginosa (ATCC-15442). A los aislamientos categorizados como resistentes e intermedios se les determinó la CMI de estreptomicina, gentamicina y oxitetraciclina utilizando el método epsilométrico E-test (AB Biodisk, Solna, Suecia), que consta de una tira sólida con una escala de lectura en la parte superior y una gradiente exponencial de antimicrobiano en la parte inferior que cubre concentraciones adecuadas para determinar la CMI (Alippi et al., 2013). Se siguió el protocolo reportado por Lang y García (2004), utilizando como medio de cultivo agar LB e incubando a una temperatura de 30 °C. Después del periodo de incubación se documentó el resultado de las concentraciones mínimas.
Relación fitopatogenicidad-resistencia a antibióticos. Con el fin de analizar si existe relación entre la resistencia a los tres antibióticos y la fitopatogenicidad de las bacterias analizadas, se utilizaron los datos de la reacción de hipersensibilidad (RH) (Cuadro 2), previamente generados (Herrera, 2009); para ello, se inocularon suspensiones de 24 horas de cada aislamiento en hojas de Nicotiana tabacum mediante la técnica de impresión, planteada por Trigiano et al. (2004). Se tomó como una RH negativa los niveles 0 a 2, desde la ausencia de reacción hasta un halo de clorosis mínimo sin presencia de necrosis, y una reacción positiva desde clorosis intensa con necrosis (nivel 3), hasta el desarrollo de la necrosis típica de RH delimitada por los haces vasculares o nervaduras (nivel 4), o necrosis que se extiende fuera de esa área (nivel 5).
Resultados
Identificación de la colección de bacterias mediante análisis del gen ARN 16S y análisis filogenético. Se logró obtener 90 secuencias con la calidad necesaria para su identificación molecular, y los 26 aislamientos restantes se identificaron utilizando el Sistema Biolog ™ (Cuadro 2). Los 116 aislamientos se agruparon en
Cuadro 2 Identificación y niveles de resistencia a estreptomicina, tetraciclina y gentamicina de aislamientos bacterianos pertenecientes a la colección de bacterias asociadas a síntomas de infección en cultivos colectados de 2006-2009 en Costa Rica.
| Código | Hospedero | Sínt.a | Tejido | RHb | Identificación de cepas (ARN 16S y BiologTM) | CMIc (µg mL-1) | ||
|---|---|---|---|---|---|---|---|---|
| EST | TET | GEN | ||||||
| MA-6 | Apium graveolens | PB | tallo | 0 | Pseudomonas protegens CHA0T | >1024* | ||
| MA-7 | Apium graveolens | PB | tallo | 2 | Pseudomonas capeferrum WCS358T | 512* | - | |
| MA-15 | Apium graveolens | PB | tallo | 1 | Pseudomonas arauntiaca (Biolog)* | - | ||
| MA-16 | Apium graveolens | PB | tallo | 2 | Serratia marcescens ATCC 13880T | 512* | ||
| MA-79 | Apium graveolens | PB | tallo | 2 | Pseudomonas capeferrum WCS358T | - | ||
| MA-86 | Apium graveolens | PB | tallo | 2 | Pseudomonas koreensis Ps 9-14T | 128* | 24 | |
| MA-50 | Bactris gasipaes | N | hoja | 4 | P. stewartii sp. indologenes LMG 2632T | |||
| MA-52 | Bactris gasipaes | N | hoja | 5 | Stenotrophomonas maltophilia ATCC 19861T | 12 | 12 | |
| MA-53 | Bactris gasipaes | N | hoja | 2 | Stenotrophomonas maltophilia ATCC 19861T | 12 | ||
| MA-54 | Bactris gasipaes | N | hoja | 5 | Stenotrophomonas maltophilia ATCC 19861T | 12 | 24 | 256 |
| MA-55 | Bactris gasipaes | N | hoja | 2 | Providencia rettgeri DSM 4542T | 12 | - | |
| MA-65 | Bactris gasipaes | N | hoja | 5 | P. stewartii sp. indologenes LMG 2632T | 12 | 12 | |
| MA-30 | Brassica oleracea var. botrytis | M | Hoja | 0 | Serratia marcescens ATCC 13880T | |||
| MA-95 | Brassica oleracea var. botrytis | M | Hoja | 5 | Pseudomonas protegens CHA0T | - | ||
| MA-110 | Brassica oleracea var. botrytis | M | Hoja | 2 | Stenotrophomonas maltophilia (Biolog) | - | ||
| MA-142 | Brassica oleracea var. botrytis | M | Hoja | 0 | Stenotrophomonas rhizophila DSM 14405 | >1024 | ||
| MA-143 | Brassica oleracea var. botrytis | M | Hoja | 0 | Acinetobacter lactucae NRRLB-41902T | 12* | - | 32 |
| MA-9 | Capsicum annuum | PB | fruto | 2 | Pseudomonas maumuensis COW77T | |||
| MA-10 | Capsicum annuum | PB | fruto | 2 | Serratia marcescens ATCC 13880T | 16* | >256 | - |
| MA-11 | Capsicum annuum | PB | fruto | 2 | Pantoea vagans LMG 24199T | - | ||
| MA-14 | Capsicum annuum | PB | fruto | 1 | Acinetobacter lactucae NRRL B-41902T | |||
| MA-19 | Capsicum annuum | PB | fruto | 5 | Pantoea anthophila LMG 2558T | >1024 | - | |
| MA-33 | Capsicum annuum | PB | fruto | 4 | Pseudomonas punonensis CECT 8089 | - | >256 | |
| MA-90 | Capsicum annuum | PB | fruto | 4 | Pseudomonas fragi ATCC 4973T | |||
| MA-120 | Capsicum annuum | PB | fruto | 4 | Raoultella terrigena ATCC 33257T | >256 | ||
| MA-140 | Capsicum annuum | PB | fruto | 5 | Pseudomonas protegens CHA0T | - | - | 12 |
| MA-128 | Cucumis melo | PB | fruto | 2 | Klebsiella pneumoniae DSM 30104T | |||
| MA-129 | Cucumis melo | PB | fruto | 1 | Pseudomonas sp. (Biolog) | - | ||
| MA-130 | Cucumis melo | PB | fruto | 5 | Pseudomonas protegens CHA0T | 12 | 12 | |
| MA-131 | Cucumis melo | PB | fruto | 1 | Pseudomonas protegens CHA0T | 12 | ||
| MA-132 | Cucumis melo | PB | fruto | 3 | Achromobacter marplatensis LMG 26685T | >1024 | 12 | |
| MA-2 | Curcuma longa | PB | Raíz | 4 | E. cloacae subsp. dissolvens LMG 2683T | - | 12 | |
| MA-8 | Curcuma longa | PB | Raíz | 1 | Serratia marcescens (Biolog) | - | ||
| MA-38 | Curcuma longa | PB | Raíz | 0 | Enterobacter huaxiensis 090008T | - | ||
| MA-61 | Curcuma longa | PB | Raíz | 2 | Pseudomonas fragi ATCC 4973T | >1024* | ||
| MA-4 | Dracaena massangeana | PB | Tallo | 2 | Psychrobacter alimentarius JG-100T | 12 | ||
| MA-27 | Dracaena massangeana | PB | Tallo | 1 | Pantoea vagans LMG 24199T | |||
| MA-42 | Dracaena massangeana | PB | Tallo | 2 | Pseudomonas putida NBRC 3738T | 48* | ||
| MA-43 | Dracaena massangeana | PB | Tallo | 2 | Comamonas koreensis KCTC 12005T | 12 | - | |
| MA-88 | Dracaena massangeana | PB | Tallo | 0 | Pseudomonas fluorescens (Biolog) | - | ||
| MA-89 | Dracaena massangeana | PB | Tallo | 2 | Pantoea vagans LMG 24199T | - | ||
| MA-136 | Dracaena massangeana | PB | Tallo | 0 | Pantoea agglomerans (Biolog) | |||
| MA-59 | Ficus carica | M | hoja | 0 | O. pseudogrignonensis CCUG 30717T | - | 96 | |
| MA-5 | Lactuca sativa var. capitata | PB | hoja | 0 | Pseudomonas putida (Biolog) | |||
| MA-13A | Lactuca sativa var. capitata | PB | tallo | 4 | Pectobacterium aroidearum SCRI 109T | 12 | ||
| MA-13B | Lactuca sativa var. capitata | M | hoja | 4 | Pseudomonas capeferrum WCS358T | 96 | ||
| MA-14C | Lactuca sativa var. capitata | PB | tallo | 5 | Stenotrophomonas maltophilia ATCC 19861T | - | 48 | |
| MA-17 | Lactuca sativa var. capitata | PB | hoja | 1 | Pseudomonas azotoformans LMG 21611T | |||
| MA-23A | Lactuca sativa var. capitata | M | hoja | 3 | Pantoea vagans LMG 24199T | 12 | ||
| MA-224 | Lactuca sativa var. capitata | M | hoja | 4 | Pseudomonas oryzihabitans NBRC 102199T | 12 | ||
| MA-43A | Lactuca sativa var. capitata | PB | hoja | 4 | Raoultella terrigena ATCC 33257T | 12 | ||
| MA-82 | Lactuca sativa var. capitata | PB | hoja | 1 | Pseudomonas extremorientalis KMM 3447T | - | 24 | |
| MA-60 | Lactuca sativa var. capitata | PB | hoja | 1 | Pseudomonas sp. (Biolog) | |||
| MA-84 | Lactuca sativa var. capitata | PB | hoja | 2 | Pseudomonas putida (Biolog) | - | ||
| MA-40 | Lactuca sativa | M | hoja | 1 | Pseudomonas fragi ATCC 4973T | 32* | ||
| MA-44 | Lactuca sativa | M | hoja | 2 | Pseudomonas punonensis CECT 8089T | - | >256 | - |
| MA-49 | Lactuca sativa | M | hoja | 4 | Pseudomonas cichorii ATCC10857T | |||
| MA-111 | Lactuca sativa | M | hoja | 0 | Serratia marcescens ATCC 13880T | - | >256 | |
| MA-112 | Lactuca sativa | M | hoja | 2 | Pantoea vagans LMG 24199T | - | 128 | |
| MA-115 | Mangifera indica | M | fruto | 2 | Erwinia billingiae CIP 106121T | |||
| MA-124 | Mangifera indica | M | fruto | 2 | Pseudomonas putida NBRC 3738T | |||
| MA-125 | Mangifera indica | M | fruto | 0 | Pseudomonas sp. (Biolog) | |||
| MA-127 | Mangifera indica | M | fruto | 1 | Pseudomonas putida (Biolog) | |||
| MA-24 | Musa paradisiaca | PB | Tallo | 1 | Pseudomonas sp. (Biolog) | |||
| MA-51 | Musa paradisiaca | N | Tallo | 1 | Pseudomonas sp. (Biolog) | - | 12 | |
| MA-68 | Musa paradisiaca | PB | Tallo | 2 | Acinetobacter sp. (Biolog) | |||
| MA-72 | Musa paradisiaca | PB | Tallo | 1 | Pseudomonas sp. (Biolog) | - | - | |
| MA-77 | Musa paradisiaca | N | Tallo | 2 | Aeromonas caviae (Biolog) | - | 12 | |
| MA-87 | Musa paradisiaca | PB | Tallo | 0 | Serratia marcescens ATCC 13880T | >1024 | >256 | |
| MA-97 | Musa paradisiaca | PB | Tallo | 2 | Pseudomonas sp. (Biolog) | - | 12 | |
| MA-101 | Musa paradisiaca | PB | Tallo | 2 | Pseudomonas protegens CHA0T | 12 | ||
| MA-117 | Musa paradisiaca | PB | Tallo | 1 | Achromobacter spanius LMG 5911T | - | ||
| MA-118 | Musa paradisiaca | PB | Tallo | 4 | Pseudomonas protegens CHA0T | - | >256 | - |
| MA-119 | Musa paradisiaca | PB | Tallo | 1 | Pseudomonas putida NBRC 3738T | 12 | - | |
| MA-139 | Musa paradisiaca | N | Tallo | 1 | Pseudomonas sp. (Biolog) | - | - | - |
| MA-1 | Ornithogalum arabicum | PB | hoja | 0 | Psycrobacter faecalis Iso-46T | - | ||
| MA-13 | Ornithogalum arabicum | PB | hoja | 1 | Pseudomonas putida NBRC 3738T | 24* | - | - |
| MA-37 | Phaseolus vulgaris | M | hoja | 4 | Pseudomonas syringae ATCC 19304T | 24* | ||
| MA-70 | Phaseolus vulgaris | M | hoja | 5 | Pseudomonas syringae ATCC 19304T | |||
| MA-81 | Phaseolus vulgaris | M | hoja | 1 | Pseudomonas azotoformans DSM 18862T | - | ||
| MA-12 | Solanum tuberosum | PB | Raíz | 0 | Psychrobacter aquaticus CMS 56T | - | ||
| MA-18 | Brassica oleracea var. capitata | PB | hoja | 3 | Sphingobacterium kitahiroshimense 10CT | 12 | - | 256 |
| MA-22 | Brassica oleracea var. capitata | N | hoja | 2 | Psychrobacter pulmonis CECT 5989T | |||
| MA-23 | Brassica oleracea var. capitata | M | hoja | 2 | Pseudomonas sp. (Biolog) | |||
| MA-26 | Brassica oleracea var. capitata | N | hoja | 1 | Pseudomonas moraviensis CCM 7280T | - | ||
| MA-28 | Brassica oleracea var. capitata | N | hoja | 0 | Serratia marcescens ATCC 13880T | - | >256 | |
| MA-29 | Brassica oleracea var. capitata | N | hoja | 0 | Serratia marcescens (Biolog) | - | >256 | |
| MA-32 | Brassica oleracea var. capitata | PB | hoja | 1 | Pantoea vagans LMG 24199T | - | - | 256 |
| MA-34 | Brassica oleracea var. capitata | N | hoja | 1 | Pseudomonas protegens CHA0T | 48* | 24 | |
| MA-35 | Brassica oleracea var. capitata | M | hoja | 1 | Serratia marcescens ATCC 13880T | >256 | ||
| MA-36 | Brassica oleracea var. capitata | PB | hoja | 5 | Pantoea vagans LMG 24199T | |||
| MA-39 | Brassica oleracea var. capitata | N | hoja | 1 | Psycrobacter faecalis Iso-46T | |||
| MA-41 | Brassica oleracea var. capitata | N | hoja | 2 | Pseudomonas capeferrum WCS358T | >1024* | - | - |
| MA-46 | Brassica oleracea var. capitata | M | hoja | 0 | Pseudomonas saponiphila DSM 975T | |||
| MA-48 | Brassica oleracea var. capitata | M | hoja | 0 | Pseudomonas laurylsulfativorans AP3_22T | - | - | |
| MA-57 | Brassica oleracea var. capitata | M | hoja | 1 | Serratia marcescens ATCC 13880T | - | >256 | |
| MA-76 | Brassica oleracea var. capitata | M | hoja | 1 | Serratia marcescens (Biolog) | - | ||
| MA-85 | Brassica oleracea var. capitata | M | hoja | 4 | Pseudomonas protegens CHA0T | - | ||
| MA-91 | Brassica oleracea var. capitata | N | hoja | 4 | Psychrobacter pulmonis CECT 5989T | 24 | ||
| MA-96 | Brassica oleracea var. capitata | M | hoja | 2 | Pseudomonas hunanensis LVT | - | 18 | |
| MA-98 | Brassica oleracea var. capitata | N | hoja | 2 | Carnobacterium inhibens DSM 13024T | - | >256 | |
| MA-103 | Brassica oleracea var. capitata | M | hoja | 0 | Serratia marcescens ATCC 13880T | 32* | 16 | |
| MA-104 | Brassica oleracea var. capitata | M | hoja | 4 | Escherichia hermannii CIP 103176T | - | >1024 | |
| MA-105 | Brassica oleracea var. capitata | M | hoja | 1 | Pseudomonas fluorescens (Biolog) | 24* | ||
| MA-106 | Brassica oleracea var. capitata | N | hoja | 1 | Acinetobacter johnsonii CIP 64.6T | - | >256 | |
| MA-107 | Brassica oleracea var. capitata | M | hoja | 3 | Stenotrophomonas rhizophila DSM 14405T | 12 | ||
| MA-31 | Solanum lycopersicum | M | hoja | 1 | Pseudomonas fulva (Biolog) | >1024* | ||
| MA-56 | Solanum lycopersicum | N | fruto | 2 | Pseudomonas fulva 12-XT | >1024* | ||
| MA-74 | Solanum lycopersicum | PB | fruto | 3 | Dickeya oryzae ZYY5T | >1024 | ||
| MA-83 | Solanum lycopersicum | N | fruto | 1 | Pseudomonas sp. (Biolog) | >1024* | ||
| MA-113 | Solanum lycopersicum | M | hoja | 3 | Serratia marcescens ATCC 13880T | - | - | - |
| MA-141 | Solanum lycopersicum | M | hoja | 2 | Serratia marcescens ATCC 13880T | - | >256 | - |
| MA-3 | Daucus carota | PB | Raíz | 1 | Pseudomonas azotoformans LMG 21611T | 32* | ||
| MA-20 | Cucurbita pepo | PB | fruto | 0 | Klebsiella michiganensis W14T | 48 | ||
| MA-75 | Cucurbita pepo | PB | fruto | 1 | Pseudomonas corrugata (Biolog) | -* | ||
| MA-80 | Cucurbita pepo | PB | fruto | 2 | Pseudomonas protegens CHA0T | 16* | ||
a Síntomas. Tipo de lesión en tejido vegetal de donde se aisló la bacteria. M: Mancha, N: Necrosis, PB: Pudrición blanda
b RH: Reacción Hipersensible. Datos tomados de Herrera (2009)
c Determinación de Concentración Mínima Inhibitoria utilizando e-Test (Solna). EST: Estreptomicina, TET: Tetraciclina, GEN:Gentamicina
* Tomado de Méndez (2010).
20 géneros bacterianos, de los cuáles la mayoría se clasificaron como Pseudomonas (48 %), seguido por Serratia (12 %), Pantoea (9 %), Stenotrophomonas (6 %) y Psychrobacter (5 %). Los otros 15 géneros representaron menos de un 5 % de abundancia del total de la colección, 10 de estos con solamente un representante (Cuadro 2). Se identificaron un total de 55 especies bacterianas, pertenecientes la mayoría al filo Proteobacteria (53 especies), específicamente a la clase Gamaproteobacteria, con un aislamiento de Alfaproteobacteria (Ochrobactrum) y Betaproteobacteria (Achromobacter). Se obtuvo además un aislamiento del filo Bacteroidetes (Sphingobacterium) y uno de Firmicutes (Carnobacterium).
Los aislamientos del género Pseudomonas se obtuvieron a partir de la mayoría de los cultivos analizados (Cuadro 2), a excepción de las muestras de Ficus carica (higo), Bactris gasipaes (palmito) y Solanum tuberosum (papa), y provienen de todos los sitios excepto uno. Dentro de este género, se identificaron patógenos de plantas reconocidos como P. syringae, P. cichorii, P. corrugata y P. orizihabitans además de otras 18 especies de origen ambiental. Los aislamientos de Serratia marcescens se recuperaron a partir de muestras de Apium graveolens (apio), Musa paradisiaca (banano), Capsicum annuum (chile dulce), Brassica oleracea var. botrytis (coliflor), Curcuma longa (cúrcuma), Lactuca sativa (lechuga Boston), Brassica oleracea var. capitata (repollo) y Solanum lycopersicum (jitomate), de las provincias de Cartago, Limón, Heredia y Guanacaste. Mientras Pantoea, con especies patógenas como P. anthophila, P. stewartii, P. agglomerans y P. vagans, fueron obtenidos de diversos cultivos como chile dulce, lechuga Iceberg y Boston, repollo, palmito y Dracaena massangeana (dracaena), también en las mismas provincias. Los aislamientos de Stenotrophomonas, siguiente género en abundancia de la colección, se encontraron en palmito, coliflor, repollo y lechuga en las provincias de Cartago, Limón y Heredia, con la mayoría de estas cepas clasificadas como S. malthophilia (Cuadro 2). Además, se identificaron fitopatógenos Gram negativas de Dickeya oryzae, Enterobacter cloacae subsp. dissolvens y Pectobacterium aroidearum en muestras de jitomate, cúrcuma y lechuga Boston, respectivamente. Las relaciones filogenéticas entre las secuencias de los aislamientos y secuencias de referencia obtenidas de bases de datos curadas como EzbioCloud (Yoon et al., 2017) se presentan en la Figura 2.
Perfil de susceptibilidad a antibióticos y determinación de la concentración mínima inhibitoria (CMI). Para efectos de este estudio, se consideró resistentes los aislamientos clasificados como resistentes o intermedios por la prueba de Kirby-Bauer, que además presentaron una CMI ≥ 12 ng mL-1 (Figura 3) (Miernik y Rzeczycka, 2007; Rodríguez et al., 2008). Se utilizó esta concentración basada en la recomendación para patógenos humanos entéricos, no entéricos y anaerobios según la guía CLSI (2017), ya que es superior a la CMI intermedia para estos grupos
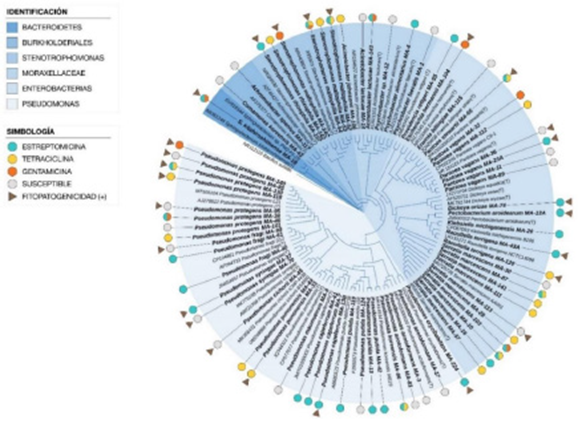
Figura 2 Cladograma construido con el método del vecino más cercano a partir de 70 secuencias parciales del gen ARNr 16S de bacterias aisladas de lesiones en plantas y secuencias de cepas de referencia. Se evaluó la topología del árbol realizando 1 000 remuestreos y se utilizó la secuencia de Bacillus subtilis como grupo externo. Los símbolos en el exterior del árbol indican los aislamientos clasificados como resistentes a Estreptomicina, Tetraciclina y Gentamicina y sus combinaciones (círculos) y aquellos con Reacción hipersensible positiva (triángulos).
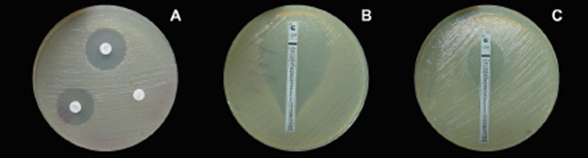
Figura 3 A. Halos que demuestran la sensibilidad a los antibióticos en discos (Oxoid) de gentamicina y tetraciclina y resistencia a estreptomicina (ausencia de halo) en la prueba de difusión en disco Kirby Bauer. B. Bacteria con una CMI de 0.25 µg mL-1 para gentamicina, determinada por el método epsilométrico (E-test). C. Bacteria con una CMI de 32 µg mL-1 para el mismo antibiótico.
bacterianos. Según esta clasificación, se observó la presencia de bacterias resistentes a los antibióticos estudiados en muestras provenientes de todos cultivos con excepción de mango y papa (Cuadro 3). La mayor proporción de aislamientos resistentes fueron identificados en las muestras de jitomate (83.3 %), palmito (83.3%) y lechuga Boston (80 %) (Figura 4). Los aislamientos obtenidos de repollo, banano, chile dulce y lechuga Iceberg presentaron los mismos fenotipos de resistencia a estreptomicina, tetraciclina y gentamicina, además de resistencias múltiples como estreptomicina-tetraciclina (Estr-Tet) (chile dulce y banano), y estreptomicina-gentamicina (Estr-Gent) en repollo. En el caso del palmito, se aisló la mayor cantidad de bacterias con resistencia múltiple Estr-Tet y Estr-Tet-Gent (Cuadro 3, Figura 4). Otro cultivo que presentó bacterias resistentes a los tres antibióticos analizados fue la lechuga Iceberg, cuyas muestras provienen de diferentes fincas de la provincia de Cartago. La resistencia múltiple también fue observada en muestras de coliflor (Estr-Gent), apio y melón (Estr-Tet), mientras que cultivos como jitomate, lechuga Boston y cúrcuma se les detectó aislamientos resistentes a estreptomicina y tetraciclina.
Se encontró resistencia a estreptomicina en bacterias aisladas de todos los cultivos excepto higo. Para este antibiótico, todos los aislamientos provenientes de jitomate y cúrcuma tuvieron una CMI máxima de >1024 µg mL-1, los de apio una CMI de 128 a >1024 µg mL-1 y en el caso de repollo, banano, melón y coliflor, de 12 a >1024 µg mL-1, chile dulce de 16 a >1024 µg mL-1 y lechuga Iceberg de 12 a 96 µg mL-1. Los demás cultivos presentaron bacterias con CMI entre 12 y 48 µg mL-1. La resistencia a tetraciclina se detectó en bacterias provenientes de 10 de los 19 cultivos y aislamientos de repollo, banano, chile dulce, lechuga Boston y zanahoria tuvieron la CMI máxima de >256 µg mL-1. A pesar de encontrarse con menor frecuencia, los aislamientos resistentes a gentamicina tuvieron CMI de 256 en el palmito, 16 a 256 en el repollo y de 12 a 48 µg mL-1 en banano, chile dulce y coliflor (Cuadro 2). Dentro de los géneros que tuvieron una mayor cantidad de aislamientos resistentes, se encuentran Pseudomonas, Serratia, Pantoea y Stenotrophomonas, todos con miembros fitopatógenos y saprófitos caracterizados por su identificación molecular y la reacción de hipersensibilidad (Figura 2 y 5).
El género Pseudomonas fue detectado en muestras de 16 de los 19 cultivos de los que fue aislada la colección bacteriana, donde se identificaron 56 aislamientos de este género, de los cuáles 30 tuvieron una CMI mayor a 12 µg mL-1 (Cuadro 3), por lo que se consideraron resistentes. Se observaron cinco de los seis fenotipos de resistencia estudiados, siendo la resistencia a estreptomicina predominante, con un rango de 12 a >1024 µg mL-1 con el 65% de los aislamientos con CMI mayor a 32 µg mL-1, y cuatro de las bacterias con niveles máximos de CMI (>1024 µg mL-1). En lo que respecta a la resistencia a tetraciclina, tres de los 11 aislamientos resistentes presentaron >256 µg mL-1 de CMI (máxima). Solamente dos bacterias tuvieron resistencia a gentamicina (CMI de12 a 24 µg mL-1) (Cuadro 2).
Cuadro 3 Géneros bacterianos identificados y frecuencia de bacterias resistentes a los antibióticos Estreptomicina (Estr), Tetraciclina (Tetra) y Gentamicina (Gent).
| Filo | Clase | Género | Nº de aislamientos | Aislamientos con CMI (E-test) ≥ 12 µg mL-1 | Estr | Tet | Gent | Estr-Tet | Estr-Gent | Estr-Tet-Gent | Nº (%) de resistentes |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Proteobacteria | AlfaProteobacteria | Ochrobactrum | 1 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 1 (100.0 %) |
| Proteobacteria | BetaProteobacteria | Achromobacter | 2 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 1 (100.0 %) |
| Proteobacteria | GamaProteobacteria | Acinetobacter | 4 | 0 | 1 | 0 | 0 | 1 | 0 | 0 | 2 (50.0 %) |
| Proteobacteria | GamaProteobacteria | Aeromonas | 1 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 1 (100.0 %) |
| Proteobacteria | BetaProteobacteria | Comamonas | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 1 (100.0 %) |
| Proteobacteria | GamaProteobacteria | Dickeya | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 1 (100.0 %) |
| Proteobacteria | GamaProteobacteria | Enterobacter | 2 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 1 (50.0 %) |
| Proteobacteria | GamaProteobacteria | Erwinia | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Proteobacteria | GamaProteobacteria | Escherichia | 1 | 0 | 0 | 1 | 0 | 0 | 0 | 0 | 1 (100 %) |
| Proteobacteria | GamaProteobacteria | Klebsiella | 2 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 1 (50.0 %) |
| Proteobacteria | GamaProteobacteria | Pantoea | 11 | 2 | 1 | 1 | 1 | 0 | 0 | 0 | 5 (45.0 %) |
| Proteobacteria | GamaProteobacteria | Pectobacterium | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 1 (100 %) |
| Proteobacteria | GamaProteobacteria | Providencia | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 1 (100 %) |
| Proteobacteria | GamaProteobacteria | Pseudomonas | 56 | 17 | 8 | 1 | 3 | 1 | 0 | 0 | 30 (53.6 %) |
| Proteobacteria | GamaProteobacteria | Psychrobacter | 6 | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 2 (33.3 %) |
| Proteobacteria | GamaProteobacteria | Raoultella | 2 | 1 | 1 | 0 | 0 | 0 | 0 | 0 | 2 (100.0 %) |
| Proteobacteria | GamaProteobacteria | Serratia | 14 | 1 | 6 | 0 | 2 | 1 | 0 | 0 | 10 (71.4 %) |
| Proteobacteria | GamaProteobacteria | Stenotrophomonas | 7 | 1 | 2 | 1 | 1 | 0 | 1 | 0 | 6 (85.7 %) |
| Bacteroidetes | Sphingobacteriia | Sphingobacterium | 1 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 1 (100 %) |
| Firmicutes | Bacilli | Carnobacterium | 1 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 1 (100 %) |
| TOTAL | 116 | 28 | 23 | 5 | 8 | 4 | 1 | 69 | |||
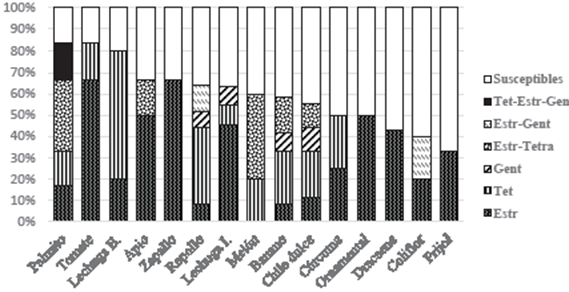
Figura 4 Proporción de bacterias resistentes (CMI ≥ 12 µg mL-1) a los bactericidas Estreptomicina (Estr), Tetraciclina (Tet) y Gentamicina (Gent) y sus combinaciones en los hospederos analizados que presentaron más de un aislamiento.
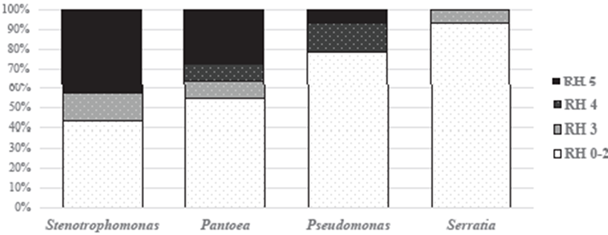
Figura 5 Tipos de Reacción de Hipersensibilidad (RH) en los géneros bacterianos más frecuentemente observados en muestras de cultivos con síntomas asociados a bacterias. Se considera bacteria fitopatógena los aislamientos con RH entre 3 y 5 (Herrera, 2009). Los niveles de RH de 0 a 2 se muestran de manera conjunta e indica no patogenicidad
Diez de las 14 aislamientos clasificados como Serratia mostraron resistencia (Cuadro 3), provenientes de seis de los ocho cultivos de los que se aislaron (repollo, jitomate, chile, lechuga Boston, apio y banano). La resistencia comúnmente observada fue para tetraciclina, donde ocho aislamientos resistentes presentaron CMI máxima para este antibiótico. Se detectaron también tres cepas resistentes a estreptomicina (CMI de 12 a 512 µg mL-1) y una a gentamicina (16 µg mL-1). Bacterias clasificadas como Stenotrophomonas mostraron CMI de 12 a >1024 µg mL-1 a estreptomicina, entre 12 y 24 a tetraciclina, y de 48 a >256 gentamicina, con solamente un aislamiento (MA-110) susceptible a los tres antibióticos. Cinco de las 11 bacterias identificadas en el género Pantoea presentaron resistencia, con valores máximos solo para estreptomicina en el caso de MA-19 (chile dulce) (Cuadro 2, 3).
Relación fitopatogenicidad-resistencia a antibióticos. De acuerdo con los datos reacción de hipersensibilidad reportados por Herrera (2009), el 73 % de las bacterias de esta colección se clasificaron como no patógenas de plantas o RH negativa, ya que no presentaron clorosis ni necrosis alrededor del punto de inoculación (niveles de 0 a 2). Al comparar la taxonomía de los aislamientos con esa clasificación, se observó una mayor proporción de aislamientos con RH positiva (niveles 3 a 5) en los géneros Stenotrophomonas (57.2 %) y Pantoea (45.5 %), Pseudomonas (21.4%) y Serratia (7.1 %), aunque algunas de las especies que presentaron esta reacción no corresponden a especies fitopatógenas reconocidas, sino especies de origen ambiental como es el caso de P. protegens, P. fragi y P. punonensis (Cuadro 2).
Al comparar la calificación del grado de patogenicidad con el número de cepas resistentes identificadas en cada categoría de RH (Figura 6), se encontró que el 45 % de esta población con RH negativa, presentó resistencia a alguno de los antibióticos estudiados, aunque la proporción fue menor a la encontrada en los aislamientos patógenos (RH +), en los que las bacterias resistentes representaron un 70 a un 83 %, correspondientes al nivel 3 y 5, respectivamente. Resistencia a los tres antibióticos fueron detectadas en todos los niveles de fitopatogenicidad, y una bacteria con RH 5 (Stenotrophomonas malthopilia MA-54), fue la única a la que se le detectó resistencia a los 3. En el nivel de mayor patogenicidad se detectó mayor proporción de bacterias con resistencia múltiple.
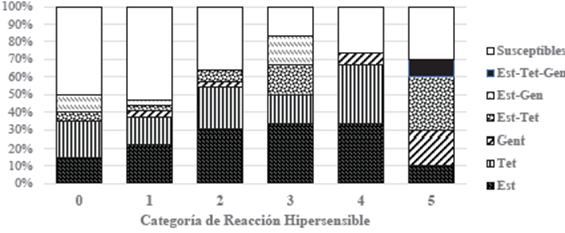
Figura 6 Proporción de cepas resistentes a los antibióticos estudiados de acuerdo con la escala de RH (niveles 0 a 5) determinada por Herrera (2009). En el eje Y se indica el porcentaje de aislamientos susceptibles dentro de cada categoría.
Discusión
La diversidad de síntomas relacionados a enfermedades de plantas de origen bacteriano aumenta la dificultad de manejo en sistemas agrícolas (Aráuz, 2011). Más aún, algunos síntomas como manchas de frutos y hojas y pudrición blanda son compartidos por patógenos diferentes, haciendo necesaria la identificación en laboratorio por diferentes metodologías, ya que una adecuada identificación temprana permite un mejor control de la enfermedad (Kannan et al., 2022). Por otro lado, la parte aérea de las plantas está predominantemente colonizada por una comunidad bacteriana diversa, tanto en forma de epífitas en la superficie de la planta como de endófitos en el tejido vegetal. Mientras que algunas bacterias asociadas a las plantas promueven su crecimiento, otras pueden ser patógenos de plantas o inclusive de humanos (Lindow y Brandl, 2003; Jackson et al., 2013). Al respecto Jackson et al. (2013), al analizar la composición de la comunidad bacteriana de hortalizas de hoja verde mediante pirosecuenciación, identificó once filos diferentes, donde las Gamaproteobacterias, Betaproteobacterias y Bacteroidetes fueron los linajes dominantes. Estos filos coinciden con lo observado en este estudio, en el cual se encontraron los mismos grupos de Proteobacterias, además de Alfaproteobacterias. De los géneros identificados, Pseudomonas, Serratia, Pantoea, Stenotrophomonas, Klebsiella y Enterobacter son bacterias Gram negativas que tienen especies de patógenos en plantas. Es importante recordar que estos aislamientos provienen de la zona del borde de la lesión y que debido al proceso de aislamiento en el cual la muestra es desinfestada con hipoclorito antes de la disección, pueden aislarse también bacterias endófitas y oportunistas. Para poder discriminar los patógenos de plantas en esta colección, Herrera (2009) utilizó la técnica de reacción hipersensible (RH) en la planta indicadora Nicotiana tabacum. Esta técnica, que consiste en la inoculación de bacterias en el envés de las hojas de plantas para evaluar la capacidad fitopatogénica de las bacterias (Zurbriggen et al., 2010), se caracteriza por la muerte de células cercanas al punto de reconocimiento del patógeno y la aparición de clorosis y necrosis delimitada en las hojas (Bellincampi et al. 2014).
En este estudio los géneros encontrados con mayor abundancia presentaron aislamientos clasificados como fitopatógenos, además de representantes saprófitos.
La diversidad de especies de Pseudomonas en el ecosistema del suelo influye tanto en el crecimiento de las plantas y su patogenicidad (Kumar et al., 2017), esto debido a su versatilidad metabólica y plasticidad genética. Esta diversidad y capacidad metabólica puede ser la causa de que en esta investigación Pseudomonas fuese aislada a partir de 16 de los 19 cultivos analizados. P. syringae, la especie que ocupa el primer lugar en la lista de Mansfied et al. (2012) de las 10 principales especies bacterianas patógenas de plantas, fue identificada en este estudio, junto con P. cichorii, P. corrugata y P. orizihabitants (Höfte y De Vos, 2007; Pauwelyn et al., 2013; Li et al., 2021). A pesar de que en otras especies de Pseudomonas no identificadas en esta colección se ha reportado resistencia natural a los aminoglucósidos (Krahn et al., 2012), se encontró un amplio rango de CMI para estreptomicina, con más de la mitad de los aislamientos con CMI mayores a 32 µg mL-1 para estreptomicina y la mayoría susceptible a gentamicina. Debido a la ubicuidad de este género en diferentes ambientes y su utilización como biofertilizante y biocontrolador, es importante estudiar si los genes que confieren resistencia están presentes en el cromosoma o en determinantes de transferencia horizontal de genes, en aislamientos de este género.
Serratia marcescens es una especie bacteriana genéticamente variable que se encuentra en diferentes entornos, incluyendo agua, suelo, plantas y como patógeno oportunista en humanos y animales (Besler y Little, 2017). Esta especie ha sido asociada tanto con infecciones nosocomiales en el ámbito médico como con enfermedades en plantas. Por ejemplo, cepas de S. marcescens han sido identificadas como causantes de la enfermedad de la vid amarilla de las cucurbitáceas y de la pudrición blanda en frutos de chile (Zhang et al., 2005; Gillis et al., 2017). En este estudio 14 aislamientos de S. marcescens de diferentes hospederos presentaron alta similitud a la secuencia de la cepa tipo S. marcescens ATCC 13880(T) aislada de un tanque de tratamiento de aguas residuales, por lo que su papel en la planta hospedera debe estudiarse con un mayor detalle. Esta especie presentó en 10 de 13 de aislamientos una CMI ≥ 12 µg mL-1, y su nivel de resistencia fue el máximo para tetraciclina, y en un amplio rango para estreptomicina, con solo un aislamiento resistente a gentamicina. Estos hallazgos concuerdan con un estudio realizado en Costa Rica donde aislamientos de Serratia obtenidos a partir de suelos aplicados con gentamicina y tetraciclina, fueron resistentes a tetraciclina y sensibles a gentamicina (Rodríguez et al., 2007). A pesar de que S. marcescens presenta resistencia natural a los aminoglicósidos (Sandner-Miranda et al., 2018), la mayoría de los aislamientos analizados en este estudio fueron susceptibles a la estreptomicina y gentamicina, y algunas cepas presentaron CMI máximas para tetraciclina por lo que se hace necesario un mayor estudio de sus determinantes de resistencia.
El género Pantoea comprende bacterias con diversas funciones en las plantas, incluyendo su papel como fitopatógenos, endófitos y epifitos (Doni et al., 2021). Dentro de los patógenos de plantas se han identificado P. citrea, P. ananas, P. eucalypti, P. stewartii, P. agglomerans, P. vagans y P. antophila (Schaad et al., 2001; Brady et al., 2009) estas cuatro últimas identificadas en este estudio. En particular, Pantoea stewartii sp. indologenes MA-65, aislada de lesiones en hojas de palmito, es el agente causal de la bacteriosis del palmito que afectó a las plantaciones en Costa Rica en la década de 2000 (Mora-Urpí et al., 2008). En este estudio, aislamientos clasificados como patógenos por análisis filogenético y de fitopatogenicidad presentaron resistencia a estreptomicina y tetraciclina.
Especies del género Stenotrophomonas tiene representantes endófitos, y que se utilizan como agentes de biocontrol en la agricultura sostenible (Berg y Martinez, 2015). S. maltophilia se considera un patógeno oportunista emergente en el ámbito clínico, con resistencia natural a aminoglucosidos, aunque en menor medida a la gentamicina (Antón et al., 2005; Berg y Martinez, 2015). En un estudio realizado en Costa Rica se encontró que los aislamientos de Stenotrophomonas sp. provenientes de plantas de lechuga presentaban resistencia a varios antibióticos, incluyendo tetraciclina y gentamicina (Rodríguez et al., 2007). En este trabajo se observó que la mayoría de los aislamientos mostraron resistencia a los antibióticos evaluados con CMI entre 12-24 µg mL-1 para tetraciclina y estreptomicina, con excepción de MA-142 que tuvo un CMI máximo (>1024 µg mL-1) para estreptomicina y gentamicina. Entre los aislamientos resistentes se encuentran bacterias con un alto nivel de patogenicidad, las cuáles fueron recuperadas a partir de palmito (Cuadro 2), adicionalmente, el aislamiento MA-54 fue el único de la colección resistente a los tres antibióticos estudiados (Cuadro 2). Al presentar resistencia intrínseca, es importante realizar un análisis detallado en los aislamientos de S. maltophilia ante la posible presencia de genes de resistencia asociados a elementos móviles en el caso de la estreptomicina y tetraciclina.
La mayoría de las bacterias fitopatógenas identificadas filogenéticamente y mediante la prueba de RH no han sido descritas en Costa Rica, a excepción de los aislamientos de Erwinia billingiae MA-115 y Raoultella terrigena, que fueron sometidos a pruebas de patogenicidad en plantas de mango y chile dulce respectivamente (cultivos de los que fueron aislados), y al comprobarse su virulencia por los Postulados de Koch, fueron descritos como fitopatógenos (Vidaurre-Barahona et al., 2021; Cubero et al., 2021). En esta colección de bacterias de taxonomía diversa, se observó que las bacterias con RH positiva, consideradas patógenas de plantas, presentaron una proporción más alta de resistencia (Figura 4). Esto podría deberse a su adaptación para sobrevivir en las partes superficiales y los tejidos vegetales, donde están más expuestas a los antimicrobianos aplicados en las hojas (Stockwell y Duffy, 2012).
La resistencia a los antibióticos estudiados en el 60 % de los aislamientos, puede ser resultado del uso de productos en los cultivos de donde se obtuvieron las bacterias. Es importante considerar que el criterio de 12 µg mL-1 utilizado para definir la resistencia en este estudio es más alto que la concentración mínima inhibitoria (CMI) para bacterias susceptibles, pero más baja que la CMI para bacterias patógenas resistentes en humanos. Sin embargo, este criterio se ha utilizado en estudios previos en diferentes entornos, al considerarse que los microorganismos ambientales están expuestos a concentraciones mucho más bajas que las bacterias clínicas, pero también pueden desarrollar resistencia en el entorno natural (Popowska et al., 2012; Sandegren, 2014; Nogrado et al., 2021). La menor cantidad de bacterias resistentes a gentamicina observada (10 de 116), puede ser resultado de un menor uso de este antibiótico, o por motivos intrínsecos a la molécula y la persistencia en condiciones ambientales.
La presencia de bacterias resistentes en el 90 % de los hospederos analizados, los cuáles constituyen un conjunto diverso de plantas, genera preocupación por el estado actual de resistencia a esos antibióticos, ya que estos aislamientos fueron colectados entre 2006 y 2009. Los cultivos con mayor presencia de bacterias resistentes y fenotipos de resistencia a los tres antibióticos estudiados fueron el repollo, banano, lechuga Iceberg, palmito y chile dulce, los cuales pueden estar relacionados con un manejo más agresivo de las enfermedades bacterianas que afectan a estos cultivos, como la mancha angular en repollo causada por Xanthomonas campestris, el marchitamiento (Ralstonia solanacearum) en banano, las manchas foliares causadas por especies de Pseudomonas en lechuga, la bacteriosis (P. stewartii) en palmito, o la pudrición blanda común en hortalizas en climas tropicales (Bhat et al., 2010). La alta proporción de bacterias resistentes de la colección asociadas a síntomas en cultivos, encontradas en 16 de los 19 cultivos de diversas regiones del país, puede derivarse de un amplio uso agrícola de antibióticos como la tetraciclina, estreptomicina y gentamicina, sin una regulación, dosis y registros adecuados, fenómeno común también en otros países latinoamericanos. Estos hallazgos proporcionan una base para investigar la evolución de la resistencia a los antimicrobianos en bacterias fitopatógenas y no patógenas presentes en vegetales destinados al consumo humano en Costa Rica, y evidencia la necesidad de realizar estudios más detallados debido a su impacto en el control de enfermedades en los cultivos y en las comunidades microbianas asociadas.
Conclusiones
El análisis de los 116 aislamientos de una colección proveniente de síntomas de pudrición blanda, necrósis y manchas de hojas, tallos, frutos de 19 cultivos, mostraron la presencia de 20 géneros de los cuales Pseudomonas (48 %), Serratia (12 %), Pantoea (9 %) y Stenotrophomonas (6 %), fueron los más abundantes, con Pseudomonas como el género con mayor número de especies y aislamientos observados. Entre las bacterias fitopatógenas presentes en la colección se identificaron Pseudomonas syringae, P. cichorii, P. corrugata, Pantoea stewartii subsp. indologenens, P. anthophila, Dickeya oryzae, Enterobacter cloacae subsp. dissolvens y Pectobacterium aroidearum, que estuvieron entre el 23 % de aislamientos positivos para la RH. Según las condiciones del estudio se detectó resistencia al menos uno de los tres antibióticos en el 60 % de los aislamientos evaluados siendo la resistencia a estreptomicina la más frecuente. La resistencia se observó en bacterias aisladas de 17 de las especies vegetales, donde el jitomate, palmito, lechuga, apio, zapallo y repollo mostraron la mayor proporción de aislamientos resistentes, lo que sugiere un mayor riesgo en la producción de estos alimentos a seleccionar bacterias resistentes a antibióticos. La información obtenida indica la necesidad de una mayor regulación en la venta y uso de productos antimicrobianos para mitigar los efectos de estas sustancias en el medio ambiente, los animales y las personas.











 texto en
texto en 


