Introducción
Con más de 600 000 ha y una producción superior a los 8 millones de t en 2021, México se ubica como uno de los principales productores de cítricos. La derrama económica generada alcanzó cerca de 35 millones de pesos (SIAP, 2022), lo que demuestra la importancia de esos cultivos en el sector económico del país. Su pro- ducción se encuentra distribuida en 24 de los 32 estados que conforman el país; desde la península de Yucatán, hasta Tamaulipas por el Golfo de México; y desde Chiapas, hasta Sonora y la península de Baja California por el Pacífico (Salcedo- Baca et al., 2010; García-Ávila et al., 2021). Sin embargo, en el mundo los cítricos enfrentan una amplia problemática fitosanitaria; que, a diferencia de otros cultivos, en ellos ocurren casos exitosos de control biológico clásico. E.g., en México, la escama algodonosa de los cítricos (Icerya purchasi) mediante la catarinita Rodolia cardinalis y la mosca prieta (Aleurocanthus woglumi), regulada por el parasitoide Encarsia perplexa, entre otras (Trevor et al., 2013).
Lo anterior hace que los cítricos sean un cultivo especial, pues a diferencia de otros donde el control químico es base fundamental del manejo de plagas, en cítri- cos los plaguicidas deben ser utilizados con mayor cuidado. Su abuso pudiera per- turbar el equilibrio ecológico logrado, y eventualmente favorecer el resurgimiento de plagas de importancia (Qureshi y Stansly, 2009) como las arriba mencionadas.
En los últimos años se han registrado nuevas invasiones de plagas exóticas en México, donde destaca el “psílido asiático de los cítricos”, Diaphorina citri (Hemiptera: Leviidae), que junto con Trioza erytreae (Hemiptera: Triozidae), es uno de los vectores de Candidatus Liberibacter asiaticus (CLas), agente causal de la enfermedad Huanglongbing (HLB). Después de la introducción del psílido en 2002, el HLB fue registrado por primera vez en 2009 en Yucatán; desde enton- ces, la enfermedad se ha distribuido a diferentes regiones hasta cubrir 24 estados citrícolas (García-Ávila et al., 2021). Los riesgos de la presencia del patosistema
D. citri-CLas en la citricultura mexicana (Salcedo-Baca et al., 2010) motivaron al desarrollo de estrategias de manejo integrado, donde destaca el control químico, y de manera complementaria, el biológico (García-Ávila et al., 2021).
En México, el psílido cuenta con una amplia diversidad de enemigos naturales (EN), incluido uno de sus parasitoides primarios, Tamarixia radiata (Hymenopte- ra: Eulophidae) (Cortez-Mondaca et al., 2010; Mora-Aguilera, 2013). Este insecto se encuentra ampliamente distribuido en las zonas citrícolas de México; sin embar- go, los niveles de parasitismo son insuficientes (3-26 %) para la regulación natural de la plaga y de CLas (Halbert y Manjunath, 2004; García-Ávila et al., 2021). Para potenciar el control biológico (CB) de D. citri y reducir el riesgo de dispersión de CLas, el gobierno mexicano ha hecho esfuerzos para establecer un programa de control biológico inundativo (CBI) mediante el parasitoide T. radiata en las regio- nes citrícolas del país (García-Ávila et al., 2021). Aunque la literatura científica señala la importancia de la conservación de EN en el manejo de D. citri, son pocos los estudios desarrollados en el mundo (Qureshi y Stansly, 2009; Irvin et al., 2021; Irvin y Hoddle, 2021), mientras que en México la investigación documentada es incipiente (Godoy-Ceja y Cortez-Madrigal, 2018).
Bajo el supuesto de que el manejo integrado de plagas (MIP) debe descansar en la conservación de EN, y el empleo de insecticidas solo cuando la población plaga alcance un umbral económico (UE), el objetivo del presente escrito es analizar el estatus del manejo del patosistema D. citri-CLas en el mundo, pero particularmente en México. Con base en ello, proponer estrategias de conservación que puedan ir más allá del control biológico de D. citri; es decir, la regulación de otros fitófagos de los cítricos (incluidas plagas).
El agroecosistema citrícola en México
Los cítricos cultivados son originarios del Sureste asiático, donde evoluciona- ron por alrededor de 8 millones de años (Ibanez et al., 2015). Conocer el centro de origen de un cultivo es primordial para el manejo de plagas exóticas, pues eventual- mente se requerirá la exploración e importación de EN desde su lugar de origen. A través de su historia productiva, los cítricos en México han sido frecuentemente afectados por diversas plagas exóticas, varias de ellas reguladas exitosamente me- diante programas de control biológico clásico (Trevor et al., 2013).
La producción citrícola en México se localiza en 24 de los 32 estados del país (García-Ávila et al., 2021), regiones con amplias diferencias edafoclimáticas y cul- turales, relacionadas ambas con el diseño y manejo del agroecosistema, incluido el patosistema D. citri-CLas. Así, los vientos y la dispersión de las huertas marcaron la diferencia en la intensidad del HLB entre las regiones citrícolas del Pácifico mexicano y la Península de Yucatán (Mora-Aguilera, 2013).
Al igual que otros productores, los citricultores mexicanos tienen características distintivas entre ellos, por lo que debería considerarse su tipología; entendida como la caracterización de productores con base en superficie, tecnología y nivel educa- tivo, entre otras (Rosales-Martínez et al., 2018). Lo anterior facilitaría la imple- mentación de diversos programas; e.g., la conservación de EN. Así, la situación so- cioeconómica y cultural de pequeños productores induce a establecer plantaciones con diferentes características; e.g., grados de diversificación; desde plantaciones con tolerancia de malezas y asociación con otros cultivos (Península de Yucatán); hasta los policultivos, como el sistema café-plátano-cítrico practicado en algunas regiones del estado de Veracruz (Aguilar et al., 2014). Lo anterior contrasta con los monocultivos extensivos en diferentes regiones del país (e.g. Huimanguillo, Tabasco). Son modelos agrícolas contrastantes en diseño y manejo; por ejemplo, el uso de plaguicidas, aspecto determinante para la implementación de estrategias de Control Biológico por Conservación (CBPC) (Gurr y You, 2016).
Aunque existen plantaciones con sistemas de riego, la mayor parte de la citri-
cultura mexicana (63 %) es de temporal (García-Ávila et al., 2021). No obstante, algunas regiones reúnen condiciones favorables para la prevalencia de EN; e.g., en Rovirosa, Quintana Roo, la alta humedad relativa favoreció el desarrollo de epizootias naturales del hongo Hirsutella citriformis en D. citri (Mora-Aguilera et al., 2017), lo que sugiere que los hongos entomopatógenos (HEPs) pudieran ser una herramienta clave para el manejo del complejo D. citri-CLas en esas regiones.
El patosistema cítrico-Diaphorina citri-CLas
En 2002 se introdujo a México D. citri, actualmente distribuido en todas las zo- nas citrícolas del país (García-Ávila et al., 2021). Además de los daños directos que causa en los cítricos, D. citri es vector de α-Proteobacterias, G-negativas del género Candidatus Liberibacter spp. agente causal del HLB (Galdeano et al., 2020). Se en- cuentran involucradas tres especies: CL. africanus, CL. americanus y CL. asiaticus. Esta última es la más prevalente en el mundo (Thakuria et al., 2023). Los daños y pérdidas por HLB son variables entre país, región y hospedero; así, en Brasil las pérdidas en naranja dulce fluctuaron del 17.5-42 %; mientras que, en México las pérdidas varian de acuerdo con el cultivo y región; desde 17 % para limón persa en Yucatán, hasta 62 % para limón mexicano en Colima (Mora Aguilera et al., 2014). En un escenario de baja intensidad del HLB en México, se estiman pérdidas de 1.84 millones de t de cítricos; o sea, el 25 % de la producción nacional, con pérdidas de 4 millones de jornales (Salcedo et al., 2010).
La idea de “epidemia” como un desequilibrio entre poblaciones puede aplicar- se al patosistema cítricos-D. citri-CLas, donde el conocimiento de su biología y ecología puede ser la diferencia entre el éxito o fracaso de programas de manejo. Como guía se pudiera aplicar el concepto de “sistema epidemiológico”, concebido éste como un sistema abierto de n-factores que opera en tiempo y espacio para determinar la incidencia de una epidemia (Figura 1) (Mora-Aguilera et al., 2017).
Para D. citri, la temperatura optima fluctua entre 25-28 ºC y su desarrollo se detiene entre los 10 y 33 oC (Liu y Tsai, 2000). Las hembras dejaron de ovipositar cuando la temperatura se mantuvo durante cinco días a 34 °C; una vez se redujo la temperatura, los adultos nuevamente iniciaron la ovipostura (Skelley y Hoy, 2004). Por su parte, CLas no tolera temperaturas >35 °C (Thakuria et al., 2023). El nú- mero de huevos por hembra de D. citri fue menor cuando la humedad relativa se mantuvo por debajo de 40 % (Skelley y Hoy, 2004).
Por otro lado, la humedad tiene un efecto indirecto en D. citri, pues favorece la prevalencia de HEPs que reducen las poblaciones del insecto (Aubert, 1987). Una interacción entre precipitaciones pluviales leves y altas temperaturas, favorecieron indirectamente las poblaciones de D. citri al inducir mayor brotación foliar en los árboles, aspecto correlacionado directamente con las poblaciones del vector e inci- dencia del HLB (Leong et al., 2020). El viento es otro factor clave en la dispersión de D. citri y CLas. Se ha documentado que el psílido puede volar hasta 2.4 km en ausencia de viento. En presencia de vientos, algunas estimaciones sugieren que el insecto pudiera dispersarse hasta 4 km (Mora-Aguilera, 2013) e incluso 470 km (Stelinski, 2019). Bajo ese escenario, las corrientes de viento fue uno de los factores que favorecieron la rápida dispersón del HLB en México (Mora et al., 2013).
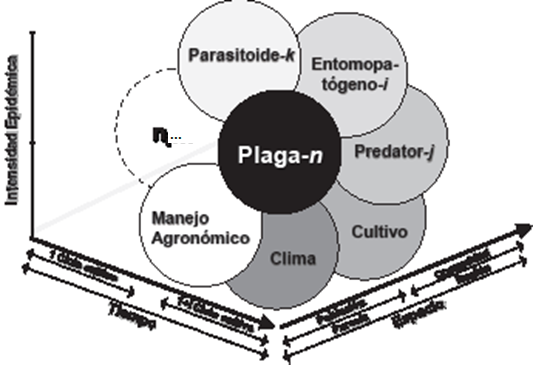
Figura 1 Sistema Epidemiológico definido por la interacción de factores determinantes de un proceso epidé- mico: especie plaga, entomopatógeno, depredador (predator) y parasitoide, cultivo, manejo agro- nómico, clima, y algún otro factor específico (ni) y los cuales operan a distintos niveles espacio-temporal (Tomado de Mora-Aguilera et al., 2017).
Los adultos hibernantes de D. citri, especialmente las hembras, sobreviven por más tiempo (8-9 meses) y congregan en el envés de las hojas. Las ninfas son se- dentarias, pero las recién emergidas pueden migrar hacia brotes vecinos o moverse dentro del mismo brote, pero nunca hacia hojas maduras (Yang et al., 2006). Un aspecto de interés para el manejo ecológico del vector y CLas es que tanto machos como hembras se aparean múltiples veces con diferentes parejas, y existen eviden- cias de que la hembra emite una feromona sexual para atraer a su pareja (Wenninger y Hall, 2008). La producción de huevos en D. citri es variable; e.g., en función del hospedero. Así, Tsai y Liu (2000) obtuvieron una media de 857.9 huevos en toronja, mientras que Nava et al. (2007) registraron 348.4 huevos en Murraya paniculata.
Los huevos de D. citri son depositados exclusivamente en brotes vegetativos y las ninfas solo se desarrollan en ellos; así, su fluctuación poblacional se correlacionó positivamente con esos periodos fenológicos (Leong et al., 2020). El mayor daño de D. citri suele ocurrir con la brotación foliar de otoño (Yang et al., 2006; Godoy- Ceja y Cortez-Madrigal, 2018). Bajo condiciones tropicales como la India, pueden ocurrir hasta nueve generaciones. Con base a temperatura, días favorables al psilido y superficie plantada, estimaciones para México sugieren desde 15 hasta 34 genera- ciones anuales (Díaz-Padilla et al., 2014). Diaphorina citri es fuertemente atraído por el color amarillo (Patt et al., 2015).
La relación D. citri-CLas es de tipo propagativo-circulativo (Galdeano et al., 2020) y una vez adquirido el patógeno, el insecto permanece infectivo durante su vida; sin embargo, no se ha registrado transmisión transovarial (Halbert y Manjuna- th, 2004). De acuerdo con Inoue et al. (2009), los insectos que adquieren la bacteria en estado adulto muestran una pobre eficiencia como vectores; en cambio, los que adquieren el patógeno en estado ninfal son más eficientes como vectores. La baja concentración de bacterias en el insecto adulto fue causa de la baja transmisión a la planta; en cambio, cuando el psílido se alimenta en estado ninfal en una planta enferma, la concentración de la bacteria incrementa significativamente y se trans- mite hasta en 67 % de las plantas sanas. El periodo de incubación de CLas en el hospedero puede ser hasta de seis meses (Aleman et al., 2007).
Se ha comprobado que CLas requiere de aminoácidos que obtiene de la planta hospedera y de D. citri. Existen amplias evidencias de que CLas puede manipular el comportamiento y desempeño del vector, y así incrementar la transmisibilidad y dispersión del patógeno. Lo anterior ocurre tanto dentro del vector, como por intermediación de la planta infectada. Los vectores positivos tienen mayor ferti- lidad, fecundidad, y tasa de desarrollo; en cambio, la sobrevivencia se reduce. De cualquier modo, CLas favorece el incremento de poblaciones positivas de D. citri (Yamada et al., 2019).
Otros aspectos interesantes de la relación cítrico-D. citri-CLas es que los insec- tos adultos positivos muestran mayor capacidad de vuelo que los psilidos negati- vos. Su preferencia por los volátiles en plantas enfermas es evidente; sin embargo, una vez infectados, los insectos se dispersan hacia plantas sanas (Yamada et al., 2019); lo anterior, y el hecho de que las hembras evitan brotes infestados por el in- secto, favorece la dispersión de la enfermedad. El psilido se distribuye, primero en agregados; después, en forma aleatoria y luego, nuevamente en agregados (Leong et al., 2020). La manipulación por CLas llega incluso hasta el apareamiento; e.g., los machos de D. citri mostraron mayor atracción por hembras positivas que por las sanas. También, el parasitoide T. radiata es mayormente atraído por plantas enfermas (Yamada et al., 2019).
El sistema inmune del psílido también es alterado por CLas. En adultos posi- tivos, la concentración de oxidasas y esterasas se reduce significativamente. Estas enzimas son fundamentales para la detoxificación de insecticidas; por tanto, insectos positivos son más susceptibles a insecticidas; incluso, a los HEPs (Yamada et al., 2019). Lo anterior tiene implicaciones prácticas en la conservación de EN; por ejemplo, utilizar HEPs, o dosis mínimas de insecticidas dirigidas a insectos positi- vos; así, se causaría menor daño a los EN.
Al igual que otros vectores, el sistema inmune de D. citri es incompleto; así, los endosimbiontes asociados al insecto contribuyen con la producción de metabolitos de defensa contra invasores; e.g., CLas y EN (Yamada et al., 2019). Al respecto, en psílidos positivos se incrementó la producción de “diaphorin”, un policétido que tiene efectos tóxicos para insectos; y por lo tanto, pudiera limitar la actividad de algunos EN del psílido, como el coccinélido Harmonia axyridis (Galdeano et al., 2020). No se registraron investigaciones que diluciden esas interacciones; e.g., niveles de parasitismo de T. radiata en psílidos positivos.
Para D. citri se han registrado 59 especies hospederas de la familia Rutaceae (Halbert y Manjunath, 2004). Además, el psílido puede alimentarse en Celtis spp. y Solanum tuberosum (Stelinski, 2019). Recientemente se reportó la planta Cor- dia myxa (Boraginaceae) como hospedera de D. citri (Arshad et al., 2019), lo que sugiere que el psílido (y probablemente CLas) pudiera tener hospederas no regis- tradas previamente, particularmente en regiones de reciente introducción del com- plejo D. citri-CLas.
Mediante injertos se demostró la susceptibilidad a CLas de casi todos los cítri- cos cultivados. Citrus sinensis suele ser la especie más susceptible, mientras que
aurantiifolia la más tolerante (Thakuria et al., 2023). Especies ornamentales de Murraya spp. son también hospederas de CLas. Aunque M. paniculata puede fun- cionar como hospedero puente en la diseminación de CLas, la excepcional dilución de la bacteria después de cinco meses sugiere que esa especie es poco importante como hospedera de CLas (Damsteegt et al., 2010). En contraste, M. koenigii fue tolerante a CLas, por lo que se sugiere su empleo como planta trampa (Beloti et al., 2018).
También, mediante Cuscuta spp. se logró transmitir CLas a plantas fuera de la familia Rutaceae; e.g., Catharanthus roseus (Apocynaceae) y diferentes plantas solanáceas. En Pithecillobium lucidum (Fabaceae) se registró CLas aun cuando no se registraron psilidos (Thakuria et al., 2023). En adición, en Cleome rutidos- perma (Cappraceae), Pisonia aculeata (Nyctaginaceae) y Trichostigma actandrum (Phytolaccaceae) se detectó CLas mediante PCR, sin registros de psílidos ni sínto- mas del HLB (Brown et al., 2014).
En el 2010 se registraron adultos de D. citri en tricomas glandulares de Si- cydium tamnifolium (Cucurbitaceae) sobre plantas de M. paniculata en Chetumal, Q.R., México. La especie se distribuye solo por la vertiente del Golfo de México y Chiapas (Lira, 2004). Aunque se desconoce su papel como hospedera de D. citri, esas observaciones preliminares sugieren que S. tamnifolium pudiera aprovecharse como planta trampa para D. citri y otras plagas. Sin embargo, es necesario dilucidar los pros y contras de su uso; e.g., interferencia con el control biológico, interferen- cia con el cultivo, probable reservorio de plagas, economía.
Manejo de Diaphorina citri-CLas
Una vez que CLas infecta a su hospedante es difícil eliminarlo, aun cuando numerosos estudios demuestran posibilidades de control; por ejemplo, mediante control cultural, químico y biológico; termoterapia, inductores de defensa, y ma- nipulación genética para la resistencia (Thakuria et al., 2023). Sin embargo, en la práctica el manejo del HLB incluye medidas preventivas; entre otras, producción de plantas sanas (Yang et al., 2006), erradicación de plantas enfermas y control legal (García-Ávila et al., 2021); pero fundamentalmente mediante el control del vector (Yang et al., 2006; García-Ávila et al., 2021). Aunque se propone el manejo integrado de D. citri, la mayor atención se centra en control químico (Qureshi y Stansly, 2007; Parra y Coelho, 2019), y el biológico solo de manera complementa- ria (Etienne et al., 2001; Salcedo-Baca et al., 2010). Sin embargo, cuando está pre- sente CLas en huertas comerciales, el control químico es el recomendado (Parra y Coelho, 2019; García-Ávila et al., 2021). Después de la introducción del complejo Dcitri-CLas en Brasil, las aplicaciones de insecticidas se incrementaron >600 % (Parra et al., 2016). Visto así, el control químico pudiera tener un impacto detri- mental en el ambiente y en las poblaciones de EN (Qureshi y Stansly, 2009; Monzó y Stansly, 2020). Para vectores de enfermedades el UE es prácticamente ausencia de plaga. E.g., la tasa de transmisión de CLas por adultos de D. citri a plantas de Citrus depressa se estimó en 8.5 % cuando se introdujo un adulto por planta, con un período de acceso a la inoculación de dos semanas (Ukuda-Hosokawa et al., 2015). Se han propuesto solo algunos UE para su control; así, en Florida se sugieren cinco adultos y tres ninfas/brote (Halbert y Manjunath, 2004); ó, 0.2-0.7 adultos/brote y
0.2 adultos/trampa (Monzo y Stansly, 2015). En México, un UE propuesto es un adulto/trampa (Yzquierdo-Álvarez, 2021).
Diaphorina citri cuenta con un amplio abanico de EN, tanto depredadores, pa- rasitoides como entomopatógenos (Yang et al., 2006; Qureshi y Stansley, 20007), los que presumiblemente deberían reducir también la incidencia y prevalencia de la enfermedad.
Entomófagos. En el mundo se tienen registros de 95 especies de artrópodos (arác- nidos e insectos) dentro de nueve ordenes y 23 familias (Kondo et al., 2015), con un impacto variable en D. citri. Por ejemplo, en Arabia Saudita el Orden Araneae con- tribuyó hasta con 33.6 % en la reducción del vector (Halbert y Manjunath, 2004). En Florida, los depredadores contribuyen hasta con 100 % del control de D. citri (Quereshi et al., 2009). Incluyen especies de Araneae, Hemerobiidae, Syrphidae y Anthocoridae; aunque destacaron los coccinélidos, H. axyridis, Olla v-nigrum y Cycloneda sanguinea (Michaud, 2004). En Colombia se registraron 16 especies de EN de seis familias y cinco ordenes que inciden en D. citri (Kondo et al., 2015). Contrariamente, las altas aplicaciones de insecticidas en Brasil limitaron el impacto de los depredadores en el CB del psílido (Parra et al., 2016). En México se registran 20 especies de entomófagos incluidos en las familias Coccinellidae, Chrysopidae, Anthocoridae y Vespidae, con mayor prevalencia de las dos primeras. También, se han aislado de D. citri HEPs como Beauveria bassiana e Hirsutella citriformis (Cuadro 1).
La mayor atención en control biológico de D. citri ha sido mediante la introduc- ción de sus parasitoides, T. radiata y Dyaphorencyrtus aligarhensis (Hymoptera:
Cuadro 1 Enemigos naturales asociados a D. citri en huertas citrícolas de México.
| Familia/Especie | Referencia |
|---|---|
| Coccinellidae | |
| H. axyridis | Mora-Aguilera, 2013 |
| O. v-nigrum | |
| C. sanguinea | Cortez-Mondaca et al., 2010 |
| Chilocorus cacti | Mora-Aguilera, 2013 |
| Hippodamia convergens | |
| Scymnus sp. | |
| Arawana sp. | Lozano-Contreras y Jasso-Argumedo, 2012 |
| Azya orbigera | |
| Delphastus sp. | |
| Zagloba sp. | |
| Chrysopidae | |
| Ceraeocrhysa sp. | Lozano-Contreras y Jasso-Argumedo, 2012 |
| C. cubana | |
| C. claveri | |
| C. valida | |
| C. everes | |
| Chrysoperla rufrilabris | Cortez-Mondaca et al., 2010 |
| Ch. comanche | |
| Chrysoperla sp. | Mora-Aguilera, 2013 |
| Anthocoridae Orius spp. | Cortez-Mondaca et al., 2011 |
| Eulophidae T. radiata | |
| Encyrtidae Diaphorencyrtus spp. | |
| Globorotallidae H. citriformis | Mora-Aguilera et al., 2017 |
| Clavicitaceae B. bassiana |
Encyrtidae) (Halbert y Manjunath, 2004), aunque la mayor atención se ha centrado en el primero. Sin embargo, sus niveles de parasitismo han sido variables; desde 28.9-36.4 % en Taiwan (Chiu et al., 1988), hasta 100 % en la isla Reunión, Francia (Etienne et al., 2001).
En Florida, T. radiata es un factor de mortalidad poco importante de D. citri, con niveles < 20 % en primavera-verano; aunque en otoño alcanza niveles del 39-56 % (Quereshi et al., 2009). En Puerto Rico, Pluke et al. (2008) reportaron niveles de parasitismo del 70-100 %; mientras que, en Sinaloa, México se registró hasta 59.6 % de parasitismo natural (Cortez-Mondaca et al., 2010). La eficiencia de T. radiata es fuertemente limitada por la presencia de hiperparasitoides (Aubert, 1987), uso de plaguicidas (Diniz et al., 2020), ausencia de hospederos en periodos críticos (Leong et al., 2020), y ausencia de néctar y polen (Irvin y Hoddle, 2021).
Dada la variabilidad en el parasitismo de T. radiata, el mayor esfuerzo se ha centrado en la cría y liberación masiva (Parra et al., 2016; Flores y Ciomperlik, 2017; García-Ávila et al., 2021). Sin embargo, en huertos comerciales la estrategia es incompatible con los plaguicidas (Diniz et al., 2020). Así, el control biológico solo se practica en huertos de traspatio, zonas urbanas y en plantaciones abando- nadas, con evidencias científicas de reducir la incidencia de D. citri y del HLB en huertas comerciales (Parra et al., 2016; Diniz et al., 2020; García-Ávila et al., 2021). E.g., en Texas, EE. UU. después de liberar T. radiata se redujo el vector en
> 91 % (Flores y Ciomperlik, 2017). En países como Brasil se alcanzaron niveles de parasitismo del 72.5 % después de la liberación del parasitoide (Parra et al., 2016). En México se menciona que el parasitismo natural de T. radiata (3-26 %) se incrementó hasta 85 % después de liberaciones masivas (García-Ávila et al., 2021).
Hongos entomopatógenos. Destacan las especies H. citriformis, B. bassiana (Pa- dulla y Alves, 2021), Isaria fumosorosea (Gallou et al., 2016) y Metarhizium ani- sopliae (Ayala-Zermeño et al., 2015). Sin embargo, solo H. citriformis, B. bassiana e I. fumosorosea (=Paecilomyces fumosoroseus) se han aislado del insecto (Halbert y Manjunath, 2004; Meyer et al., 2008; Mora-Aguilera et al., 2017). Los HEPs han sido mayormente evaluados como estrategia inundativa (i.e. aspersión); en Brasil, su empleo en campo alcanzó niveles de 57.8 y 96.1 % de mortalidad, lo que estu- vo directamente relacionado con la humedad, e inversamente con la temperatura (Saldarriaga-Ausique et al., 2017).
En México, los HEPs constituyen una herramienta importante contra D. citri y CLas en huertas comerciales de cítricos (García-Ávila et al., 2021). Después de evaluar Cordyceps bassiana, M. anisopliae e I. fumosorosea en Colima, México, la mayor mortalidad en ninfas (60 %) y adultos (50 %) se obtuvo con C. bassiana (Lezama-Gutiérrez et al., 2012). En condiciones de campo I. javanica (=fumosoro- sea) alcanzó una mortalidad del 66-81.8 % (Gallou et al., 2016).
Los HEPs pueden también colonizar los tejidos de las plantas. Bamisile et al. (2021) determinaron la capacidad endofítica de B. bassiana e I. fumosorosea, don- de solo el primero colonizó los tejidos de cítricos. Siete días después de inoculados, la mortalidad en adultos de D. citri fue de 10-15 %, y mostró una reducción signi- ficativa de huevecillos depositados por hembras alimentadas en plantas tratadas.
Más allá del control biológico del patosistema D. citri-HLB: la conservación de enemigos naturales
Existe la idea de que, una vez establecido CLas, el control biológico (CB) de
D. citri es irrelevante para el manejo del HLB (Helbert y Manjunath, 2004; Yang et al., 2006), y esto pudiera ser cierto cuando se piensa el CB que emula al control químico; es decir, reducir drásticamente la población plaga. Sin embargo, si igno- ramos el paradigma convencional y atomístico del control de plagas y del control biológico inundativo (CBI) derivado de él, podremos visualizar un fenómeno na- tural de autorregulación de poblaciones; tan poderoso, que el control biológico por conservación (CBPC) debería considerase como base del MIP.
El CBPC incluye todas aquellas medidas dirigidas a la modificación del ambien- te y al manejo de plaguicidas para favorecer la conservación e incremento de EN (Gurr y You, 2016). El CBPC es la estrategia más importante del CB, pero también la menos atendida (Cortez-Madrigal y Gutiérrez-Cárdenas, 2023). Lo anterior debi- do a que el paradigma agrícola moderno se ha diseñado con fines productivistas, no para la conservación de organismos benéficos. Diversas estrategias son planteadas para su conservación; entre otras, el manejo de plaguicidas; dispositivos para la conservación e incremento de parasitoides in situ (Kehrli et al., 2005); provisión de alimento alterno como néctar, polen (Gurr y Wratten, 1999; Gurr y You, 2016) y hospederos alternos (Cortez-Madrigal y Gutiérrez-Cárdenas, 2023).
Cuando en un cultivo falta alimento alternativo para EN, éstos se desplazan a lugares donde lo puedan obtener, lo que desfavorece la presencia de poblaciones funcionales de EN (Cortez-Madrigal y Gutiérrez-Cárdenas, 2023); o que su pre- sencia se retrase tanto, que el CB llega a ser ineficiente (Doutt y Nakata, 1973). La situación anterior puede modificarse mediante un rediseño del agroecosistema que favorezca el establecimiento permanente de parasitoides, depredadores y ento- mopatógenos antes de que arribe la plaga; pero no solo de EN conformados por insectos y ácaros, sino también del conjunto de organismos que participan en la au- torregulación de poblaciones en los ecosistemas; esto es, el CBPC desde una visión amplia: “más allá del control biológico” (Cortez-Madrigal y Gutiérrez-Cárdenas, 2023).
Aunque se ha demostrado el valor económico del CBPC en la regulación pobla- cional de D. citri (Monzó y Stansly, 2020), pocos estudios se han documentado (Irvin et al., 2021; Irvin y Hoddle, 2021). Algunas estrategias de conservación de EN evaluadas en D. citri o en plagas relacionadas, son: flora nectarífera, hospederos alternos de EN, dispositivos para la conservación e incremento de parasitoides in situ, dispositivos para la conservación, y la autodiseminación de entomopatógenos. A diferencia del CB clásico e inundativo, el CBPC suele ser más barato; incluso, puede potenciar las otras dos estrategias del CB. Se ha argumentado, por ejemplo, que las fallas de diversos programas de CB clásico se debe, probablemente, a la ausencia de hospederos alternos que sostuvieran en determinados periodos a los EN recientemente introducidos (Gurr y Wratten, 1999). ¿Podría ser el caso de T.
radiata?
Si las condiciones del agroecosistema fuesen favorables para el establecimiento de EN, el control biológico inundativo también se pudiera potenciar con un menor número de liberaciones. A la propuesta que integra el CB clásico, inundativo y por conservación, se le ha denominado “control biológico integrado” (Gurr y Wratten, 1999). Los cítricos en México pudieran ser un primer modelo de control biológico integrado.
Potenciando el control biológico de D. citri
Inclusión y conservación de plantas nectaríferas. Debido a las condiciones im- perantes del cultivo, el parasitoide T. radiata esta necesariamente ausente de los cítricos durante gran parte del año. Una estrategia para su conservación sería la inclusión de plantas nectaríferas para atraer poblaciones de EN. Sin embargo, no todas las especies nectaríferas son igualmente atractivas, por lo que se requieren estudios particulares. Así, Irvin et al. (2021), después de evaluar cuatro especies de plantas con flores en la conservación de Allograpta obliqua (Diptera: Syrphidae), solo dos fueron atractivas para el importante depredador de D. citri en California. Se registraron 2.5 veces más depredadores y 3.5 veces más oviposturas en huertas con presencia de plantas florales, que en las que no las tuvieron.
Cuando el parasitoide T. radiata se alimentó con néctar de Fagopyrum escu- lentum, su sobrevivencia se incrementó significativamente y las hembras tuvieron cinco veces más huevos que las alimentadas con otras fuentes de azucares. Así, la adición de plantas nectaríferas en huertas citrícolas pudiera potenciar la eficiencia de T. radiata (Irvin y Hoddle, 2021). Al respecto, en el noroeste de Michoacán, México, de más de 27 especies de plantas fanerógamas evaluadas, solo 24 de ellas registraron parasitoides. Destacan plantas anuales como Stevia serrata; arbustos, como Senecio salignus y Budleja sp.; árboles como Thouinia villosa; y trepadoras como Serjania racemosa. En las flores de esas plantas se registraron >14 Familias de himenópteros parasíticos (Datos sin publicar).
La adición de néctar y polen por si sola no garantiza la prevalencia de EN en los agroecosistemas. Si faltan presas u hospederos para EN; éstos, como entomófagos que son, serán incapaces de completar su ciclo biológico, o se alejarán en busca de alimento, particularmente los parasitoides como T. radiata. La conservación de hospederos alternos es entonces fundamental para la permanencia de EN junto a los agroecosistemas.
Conservación de hospederos alternos. Un ejemplo cercano a D. citri fue el con- trol biológico de T. erytreae con el parasitoide T. dryi en Isla Trinidad. Trioza easto- pi se alimenta en la maleza Litsea chinensis (Lauraceae) y funciona como hospede- ro alterno del parasitoide, el que logró incrementarse y controlar exitosamente a la plaga (Duran-Vila y Bové, 2015).
La especie Asclepias curassavica (Apocynaceae) hospeda fitófagos especialis- tas (>9), incluidos los órdenes Hemiptera, Lepidoptera, Diptera, Coleoptera, y la subclase Acarina. Incluye especies como Aphis nerii, Danaus plexippus (Lepidop- tera: Nymphalydae), Euchaetes antica (Lepidoptera: Erebidae), Liriomyza ascle- piadis (Diptera: Agromyzidae) y el ácaro Eotetranychus typhae (Tetranychidae), entre otros (Figura 2) (Cortez-Madrigal et al., 2016).

Figura 2 Aphis nerii en Asclepias curassavica y algunos enemigos naturales asociados. A) Pseudodorus clavatus, B) Cycloneda sanguínea, C) Adulto de Oligota, D) Adulto de Chamaemyiidae, E) Momias y adultos de Lyci- phlebus testaceipes.
En condiciones de campo de la Cienega de Chapala, Michoacán, los fitófagos especializados de A. curassavica reclutaron más de 20 especies de EN en huertas de cítricos; incluidos parasitoides de huevos, áfidos y minadores; así como una am- plia diversidad de depredadores, incluidas las familias Coccinellidae, Syrphidae, Chamaemyiidae, Chrysopidae, Staphylinidae, Cecidomyiidae; y en los órdenes Thysanoptera, Hemiptera, y ácaros de la familia Phytoseiidae, entre otros (Figura
2) (Cortez-Madrigal et al., 2016). De los coccinélidos registrados, O. v-nigrum,
H. convergens y C. sanguinea son depredadores importantes de D. citri (Michaud, 2004; Cortez-Mondaca et al., 2010).
Estudios desarrollados en cítricos registraron una reducción importante de pla- gas del cultivo del limón persa Citrus x latifolia en donde se incorporó la planta A. curassavica; entre ellas, D. citri. Una explicación dada fue la abundancia de EN reclutados por A. curassavica, principalmente de las familias Coccinellidae, Syr- phidae, Chamaemyiidae y Chrysopidae (Godoy-Ceja y Cortez-Madrigal, 2018).
La mariposa monarca resultó ser un importante hospedero del parasitoide de huevos Trichogramma pretiosum (Trichogrammatidae), con parasitismo múltiple por huevo. En la región de estudio, T. pretiosum estuvo presente durante gran parte del año (Cortez-Madrigal et al., 2016), lo que pudo explicar la baja incidencia de larvas de lepidópteros plaga en cítricos (Godoy-Ceja y Cortez-Madrigal, 2018).
Dispositivos para conservar parasitoides in situ . El objetivo es conservar in situ parasitoides de plagas sésiles o de baja movilidad. En recipientes con aberturas de emergencia y mallas selectivas, se deposita material vegetal infestado por la plaga, de modo que permitan la emergencia solo del parasitoide (Kehrli et al., 2005). Otra modificación incluye jaulas que cubran plantas completas, adaptadas con aberturas de emergencia con malla selectiva (Desurmont et al., 2022) como la mencionada antes.
Para la conservación de T. triozae (Hymenoptera: Eulophidae), parasitoide de la paratrioza de las solanáceas (Bactericera cockerelli; Hemiptera: Triozidae), se determinó que una abertura de malla de 500 µm permitió hasta un 89 % de emer- gencia de parasitoides y retuvo los psílidos adultos (Figura 3). En condiciones de campo del cultivo de jitomate, el dispositivo favoreció >80 % de parasitismo de la paratrioza (Datos sin publicar).
Ese mismo dispositivo con modificaciones menores pudiera potenciar el control biológico de D. citri. Por ejemplo, mediante el diseño y uso de jaulas como las arriba descritas que cubran plantas de Murraya spp. con poblaciones de D. citri y
T. radiata. Las características vegetativas de M. paniculata hace que la planta se utilice en programas de cría masiva de T. radiata para su posterior liberación en campo (Parra et al., 2016; García-Ávila et al., 2021). Además de T. radiata, el em- pleo de los dispositivos pudiera también conservar HEPs del psílido. Por ejemplo, en periodos de estiaje y ausencia de brotación en cítricos de Yucatán, México, los setos de M. paniculata fue donde se registró prevalencia de H. citriformis (Cortez- Madrigal et al., 2013).

Figura 3 Diferentes tipos de malla evaluadas en la emergencia selectiva de Tamarixia triozae, parasitoide de Bactericera cockerelli como modelo para implementar con D. citri y su parasitoide. A) Mallas de 700 x 700 µm, B) 700 x 900 µm, C) 500 µm.
Dispositivos para la conservación y autodiseminación de HEPs. Algunos auto- res sugieren el uso de la técnica de autodiseminación de HEPs para el manejo de D. citri (Avery et al., 2010). Sin embargo, se han implementado pocos estudios. Así, Patt et al. (2015) evaluaron dispositivos de color amarillo cebados con esporas de
I. fumosorosea en condiciones de invernadero. Después de 24 h, el 55 % de adul- tos fueron infectados con el entomopatógeno; cuando los cadáveres micosados se expusieron a ninfas sanas, >90 % de ellas fueron infectadas. Las blastosporas en la trampa mostraron viabilidad hasta por 20 días, la que se redujo cuando las trampas se expusieron directamente al sol. En otro estudio mediante tarjetas amarillas im- pregnadas con esporas del mismo hongo, la mortalidad de adultos fue <40 %; cuan- do se añadieron volátiles de los cítricos a las tarjetas, la mortalidad se incrementó en 23 % (Moran et al., 2011).
En especies de hongos como H. citriformis, con bajo potencial para utilizarse de manera inundativa, la autodiseminación pudiera favorecer la conservación y desa- rrollo temprano de epizootias. En diferentes partes del mundo ocurren epizootias de H. citriformis en poblaciones de D. citri, con mortalidades variables; desde 75 % en Florida (Hall et al., 2012), hasta 92 % en Rovirosa, Quintana Roo, México (Mora-Aguilera et al., 2017).
La autodiseminación de HEPs pudiera favorecerse por el comportamiento de D. citri; entre otros, el apareamiento con múltiples parejas (Wenninger y Hall, 2008), la preferencia de los machos por hembras positivas para copular, mayor capacidad de vuelo de adultos positivos (Yamada et al., 2019) y la atracción por trampas de color (Moran et al., 2011), entre otras. Adicionalmente, el posible desarrollo de una feromona sexual (Wenninger et al., 2008) del insecto pudiera potenciar la técnica de autodiseminación.
Análisis y perspectivas
A pesar de los pronósticos catastróficos desde la aparición del HLB en 2009 (Salcedo-Baca et al., 2010), los esfuerzos emprendidos en México han evitado los peores impactos de la enfermedad en la citricultura mexicana. Sin embargo, ocho años después de su aparición la enfermedad continúa su dispersión, y en 2017 ya se tenían registros en los 24 estados citrícolas del país (García-Ávila et al., 2021). Lo anterior demuestra que la citricultura nacional siempre estará en permanente riesgo por la presencia del patosistema D. citri-CLas. Recientes estudios señalan que al- gunos citricultores mexicanos han optado por cambiar de cultivo, lo que significará una reducción considerable en la producción citrícola nacional (Granados-Ramírez et al., 2018).
Es claro que la investigación sobre el patosistema D. citri-CLas no ha con- cluido. Se requieren estrategias que reduzcan costos fitosanitarios, donde el CBPC tiene un importante papel que jugar. La presente revisión evidencia la ausencia de estudios y programas enfocados a la conservación de EN para D. citri, aun cuando se demuestra la importancia para su manejo (Qureshiy y Stansly, 2009; Irvin et al., 2021;). E.g., se ha estimado que en huertas sin programas efectivos de CBPC, las pérdidas anuales estimadas pudieran alcanzar los 2 000 USD/ha (Monzó y Stansly, 2020). Como referencia, el costo en aplicación de insecticidas en cítricos de Florida alcanzó los 3 000 USD/ha (García-Ávila et al., 2021). Por lo tanto, la viabilidad a largo plazo de las estrategias hasta ahora implementadas para el manejo del HLB deberían reconsiderarse (Monzó y Stansly, 2020).
Las estrategias aquí planteadas para programas de CBPC en cítricos son senci- llas, y no perturbarían las medidas ya implementadas para el manejo del patosiste- ma D. citri-CLas. Un trabajo a futuro es evaluar especies de Murraya en la conser- vación de T. radiata mediante el diseño y uso de jaulas selectivas durante períodos de ausencia de ninfas de D. citri en cítricos. Además de proteger al parasitoide de aplicaciones de plaguicidas, se adelantarían sus poblaciones para sincronizarlas con el inicio de poblaciones de ninfas en cítricos. Otros estudios demuestran la factibilidad de modificar la secuencia de aparición plaga-EN en los agroecosis- temas, por la de EN-plaga, lo que se sabe potencia el CB (Doutt y Nakata, 1973; Jacas y Urbaneja, 2010).
Existen numerosas especies de plantas que albergan fitófagos especializados que pudieran funcionar como presas alternas de depredadores en cítricos; es decir, con bajo riesgo de convertirse en plagas; un ejemplo es la familia Apocynaceae (=Asclepiadaceae). En México, la familia está ampliamente distribuida con >300 especies en el país (Juárez-Jaimes et al., 2007), de modo que existe un alto poten- cial para incluirlas en programas de CBPC de D. citri. Además de A. curassavica, las especies A. linaria, A. angustifolia y Mandevilla foliosa han registrado pobla- ciones de A. nerii, D. plexippus y chinches de la familia Lygaeidae. Incluso, plantas tolerantes a CLas, como M. koenigii, pudieran funcionar como planta trampa de D. citri y albergar EN; entre otros, T. radiata.
En conjunto con hospederos alternos, la aportación de néctar y polen es funda- mental para el reclutamiento e incremento de la amplia diversidad de depredadores que inciden en D. citri (Kondo et al., 2015). La inclusión de plantas nectaríferas en cítricos para la conservación de EN de D. citri es un aspecto pobremente estudiado (Irvin et al., 2021; Irvin y Hoddle, 2021). Estudios pioneros en México como los aquí descritos, pudieran utilizarse como punto de partida para el manejo del pato- sistema, principalmente en plantaciones jóvenes donde la ausencia de floración es evidente. A la par, debe investigarse que las plantas acompañantes no sean hospe- deras de D. citri y de otras plagas importantes.
La atracción que presenta D. citri por el color amarillo abre posibilidades para utilizar trampas cebadas con entomopatógenos, y aprovechar al mismo insecto para su autodiseminación. La baja cantidad de inóculo utilizado y el bajo efecto en or- ganismos no blanco señalan a la autodiseminación como una herramienta de utili- dad en programas de CBPC del complejo D. citri-CLas. Una ventaja a destacar en vectores es el poder adelantar epizootias en la población (en bajas poblaciones), lo que presumiblemente retrasaría la dispersión e incidencia del HLB. Sin embargo, se requieren estudios epidemiológicos de campo y laboratorio que identifiquen las condiciones bióticas y abióticas que favorecen el desarrollo de epizootias; e.g., la caracterización de HEPs, donde se incluya entre otros, la velocidad de germinación a diferente temperatura y humedad. Existe la idea generalizada de que los HEPs requieren de alta humedad para su desarrollo (>90 %; Tanada y Kaya, 1993); sin embargo, para su germinación y muerte del hospedero pudiera ser suficiente 53 % de humedad (Hastuti et al., 1999).
Lo anterior abre posibilidades para identificar aislamientos más virulentos en
ambientes adversos; por ejemplo, en regiones citrícolas con baja humedad macro- ambiental, pero condiciones microambientales favorables para los HEPs (e.g. riego). Sorprendentemente, de 28 artículos relacionados con HEPs en D. citri, ninguno aborda estudios relacionados con la respuesta de aislamientos a la hume- dad.
Queda pendiente la evaluación de otros EN, como los nematodos entomopató- genos (NEPs). Observaciones preliminares demostraron que la especie Heterorha- bditis indica infecta y mata adultos de D. citri (datos sin publicar). Sin embargo, la aspersión de NEPs en follaje ha dado resultados incipientes, por lo que la pregunta entonces sería ¿Cómo pudieran aplicarse para D. citri? Una posible estrategia sería el uso de trampas atrayentes cebadas con juveniles de NEPs. La rapidez con la que mata a su hospedero hace de esos organismos una herramienta atractiva para el control de vectores de enfermedades como D. citri.
La amplia diversidad del agroecosistema cítrico en México se plantea como una limitante en el manejo regional del patosistema D. citri-CLas (Mora-Aguilera, 2013). Sin embargo, el manejo local de plantaciones pequeñas y dispersas de cí- tricos, incluidas rutáceas ornamentales, ha demostrado ser también exitoso en el manejo de la enfermedad (Uechi et al., 2019). Esas experiencias deberían consi- derarse para su implementación en programas de CBPC en México e incentivar a productores a favorecer la diversificación del cultivo; por ejemplo, mediante ba- rreras rompevientos, una estrategia ya recomendada para reducir la dispersión del vector y del HLB (Stelinski, 2019). Si las barreras seleccionadas fuesen árboles con potencial nectarífero, su efecto sería doble: como barreras, y como atrayentes de EN y polinizadores.
En suma, el aprovechamiento exitoso y sustentable de EN en programas de CBPC requiere de estudios ecológico/epidemiológicos. Es necesario visualizar a los EN como parte importante de comunidades con cadenas tróficas sofisticadas, lo que resulta en complejos sistemas de interacciones ecológico-epidemiológicas. El cultivo y la vegetación espontánea como primer nivel trófico tiene un rol integrador importante de esas cadenas tróficas, donde convergen entomófagos-entomopató- genos-fitófagos-fitopátógenos. Así, emergen complejas interacciones positivas y negativas en cada nivel trófico y los correspondientes beneficios (+) o perjuicios (-) para las especies consumidoras. E.g., el complejo depredador-parasitoide-entomo- patógeno (D-P-E) asociado con Toxoptera citricida favorece (+) indirectamente a
D. citri, y por tanto a CLas al suprimir la competencia por brotes vegetativos entre ambas plagas. Finalmente, todo el complejo D-P-E de D. citri y T. citricida favore- ce (+) la salud de los cítricos en general (Figura 4) (Mora et al., 2017).
Conclusiones
La principal estrategia de control de D. citri y CLas es mediante insecticidas, y el control biológico inundativo de T. radiata y algunas especies de HEPs de manera complementaria. Aunque ocurren epizootias naturales de hongos en D. citri, son pocos los estudios ecológicos/epidemiológicos que coadyuvan a la selección de aislamientos de HEPs con mayor racionalidad. Pocos estudios se han desarrollado para expandir su empleo en forma endofítica y mediante autodiseminación.

Figura 4 Sistema trófico fitosanitario en dos especies de cítricos (limón persa y naranja dulce) y la limo- naria M. paniculata, los que son infestados diferencialmente con dos especies plaga-vector (D. citri y T. citricida) y dos patógenos (Citrus tristeza virus y Candidatus Liberibacter asiaticus). Tomado de Mora et al. (2017).
Los depredadores de D. citri son reconocidos como uno de sus principales regu- ladores, incluso superior a T. radiata en diferentes partes del mundo; sin embargo, su amplia diversidad ha sido pobremente aprovechada en el manejo del patosiste- ma, principalmente por la interferencia del control químico y la simplicidad ecoló- gica del cultivo.
Es evidente la ausencia de estudios sobre control biológico por conservación de
D. citri, aun cuando se menciona reiteradamente su importancia. Su implementa- ción pudiera potenciar, no solo el control biológico de D. citri-CLas, sino también la autorregulación de plagas de cítricos en general. Se requiere de un mayor esfuer- zo y entendimiento por todos los sectores involucrados: instituciones, gobierno, investigadores, técnicos, productores y sociedad en general. El reto es grande, pero la amplia diversidad de regiones y sistemas de producción citrícola en México pu- diera favorecer lo que sería una primera aproximación a la idea del control biológi- co integral: por conservación, clásico e inundativo.











 texto en
texto en 


