Introducción
Los insectos de la subfamilia Scolytinae son comúnmente conocidos como escarabajos descortezadores y ambrosiales (Atkinson, 2017).
La mayoría de las especies de Scolytinae se desarrollan en los tejidos de plantas leñosas recientemente cortadas, lesionadas o deterioradas que están en proceso de morir. Algunas especies, en cambio, se encuentran únicamente en frutas o semillas maduras, ya sea antes o después de que caigan al suelo (Wood, 2007). La función ecológica de estas especies es contribuir a la descomposición de la madera, el transporte de microorganismos simbióticos o facilitar el acceso a microorganismos descomponedores (Raffa et al., 2015). Las especies de Scolytinae capaces de matar árboles son pocas; sin embargo, pueden generar un impacto significativo en la composición de especies, la estructura de edad, la densidad, la acumulación de desechos maderables e incluso el balance global de carbono (Kurz et al., 2008; Lindgren & Raffa, 2013).
Las trampas diseñadas para capturar insectos varían según el propósito de su uso, las especies objetivo y los hábitats en los que se implementan. Estas trampas se emplean para estudiar la diversidad de insectos, detectar o predecir nuevas invasiones de insectos plaga en el tiempo y el espacio (Werle et al., 2011); además, delimitar el área de infestación y monitorear los niveles poblacionales de plagas establecidas.
La información obtenida a través de estas trampas es fundamental para la toma de decisiones sobre la implementación de medidas de control o la evaluación de la eficacia de un programa de manejo de plagas (Epsky et al., 2008; Cardé, 2021). Para la captura de Scolytinae, los modelos de trampas más utilizados son de embudo múltiple Lindgren y tipo panel (Steininger et al., 2015; Kendra et al., 2019; Laureano-Ahuelicán et al., 2023). No obstante, estas trampas presentan la desventaja de ser costosas, por lo que una alternativa viable es el uso de trampas artesanales.
Diversos estudios han comprobado la eficiencia del alcohol etílico y metílico para la captura de especies de Scolytinae (Rangel et al., 2012; Lázaro-Dzul et al., 2023; Aguilar-Castillo et al., 2023).
El objetivo del presente estudio fue determinar la eficiencia de cuatro trampas artesanales, cebadas con atrayente, para la captura de Scolytinae presentes en la zona de manglar de la “Laguna del Carpintero”, en Tampico, Tamaulipas, México.
Materiales y métodos
Área de estudio. El estudio se realizó de noviembre a diciembre de 2021 en el manglar de la “Laguna del Carpintero”, Tampico, Tamaulipas, México, ubicado en las coordenadas 22° 14' 06.4" N y 97° 51' 17.9" O. Las especies presentes son Avicennia germinans L., 1764 (Acanthaceae), Laguncularia racemosa L. Gaertn. f., 1807 (Combretaceae), Conocarpus erectus L., 1758 (Combretaceae) y Rhizophora mangle L., 1753 (Rhizophoraceae).
Trampas artesanales. Se diseñaron y elaboraron cuatro tipos de trampas utilizando botellas PET de 1, 1.5 y 2.5 L de capacidad (Fig. 1), se tomó como referencia los modelos reportados por Barrera et al. (2008) y Quispe-Condori et al. (2015): trampa 1, botella de 1 L, con una ventana lateral de 11 cm de ancho por 15 cm de alto, con un dispositivo liberador y colector de plástico de 50 ml de capacidad, colocado en la boca de la botella (Fig. 1A); trampa 2, botella de 1.5 L con una ventana de 8 cm de ancho por 4 cm de alto, además, tres cuartas partes de la botella fueron pintadas con aerosol negro (Fig. 1B); trampa 3 botella de 1 L, con una ventana de 11 cm de ancho por 15 cm de alto. En la parte superior de la botella, se colocó un plato de plástico para evitar alteraciones en la recolecta causadas por el sol, la lluvia y los residuos de hojarasca. Esta trampa fue pintada con aerosol negro (Fig. 1C); trampa 4, botella de 2.5 L con tres ventanas laterales de 10 cm de ancho por 8 cm de alto, con tres cuartas partes de la botella pintadas con aerosol negro (Fig. 1D).

Figura 1 Diseños de trampas para captura de Scolytinae. Donde: A) = Trampa 1, B) = Trampa 2, C) = Trampa 3 y D) = Trampa 4.
En las tres últimas trampas, el dispositivo liberador de los compuestos atrayentes consistió en un frasco de 35 ml de capacidad, al cual se le realizaron tres perforaciones de 3 mm de diámetro en la parte superior. Los frascos fueron sujetados al interior de cada trampa mediante alambre, y como líquido conservador se utilizó una solución de agua con jabón. Las trampas se cebaron con etanol al 96 %, metanol al 99%, etanol + metanol (1:1) y vinagre de manzana + etanol (1:1). De cada trampa se tuvo cuatro repeticiones en las cuales se asigno un tipo de atrayente, dando un total de 16 tratamientos (Cuadro 1).
Cuadro 1 Tratamientos evaluados según la combinación de trampa y atrayente.
| Tratamiento | Tipo De Atrayente | Tipo De Trampa/Repetición |
| T1 | Etanol | Trampa 1R1 |
| T2 | Metanol | Trampa 1R2 |
| T3 | Etanol + Metanol (1:1) | Trampa 1R3 |
| T4 | Vinagre de manzana + Etanol (1:1) | Trampa 1R4 |
| T5 | Etanol | Trampa 2R1 |
| T6 | Metanol | Trampa 2R2 |
| T7 | Etanol + Metanol (1:1) | Trampa 2R3 |
| T8 | Vinagre de manzana + Etanol (1:1) | Trampa 2R4 |
| T9 | Etanol | Trampa 3R1 |
| T10 | Metanol | Trampa 3R2 |
| T11 | Etanol + Metanol (1:1) | Trampa 3R3 |
| T12 | Vinagre de manzana + Etanol (1:1) | Trampa 3R4 |
| T13 | Etanol | Trampa 4R1 |
| T14 | Metanol | Trampa 4R2 |
| T15 | Etanol + Metanol (1:1) | Trampa 4R3 |
| T16 | Vinagre de manzana + Etanol (1:1) | Trampa 4R4 |
Las trampas se colocaron a 1.5 m del nivel del suelo y se dispusieron de manera lineal, con una distancia de 20 m entre cada una. La recolecta de insectos se realizó cada siete días, y los frascos con el atrayente se cambiaron cada 15 días, los insectos recolectados fueron transportados en recipientes de polietileno con alcohol etílico al 70 %. En laboratorio con ayuda de un microscopio estereoscópico Carl Zeiss® se separaron los especímenes de Scolytinae de otros grupos, y la identificación taxonómica se llevó a cabo mediante el uso de claves taxonómicas (Wood, 2007; Pérez-De La Cruz et al., 2009a; Pérez-Silva et al., 2021), las identificaciones se compararon con material depositado en la Colección de Insectos del Colegio de Postgraduados, Campus Montecillo, México (CEAM).
Análisis estadístico. La frecuencia de capturas de Scolytinae se dividió por especie, y los cuatro diseños de trampas artesanales se separaron por tratamiento, con base en cada combinación de trampa y atrayente (Cuadro 1). Después, para determinar el grado de asociación entre la frecuencia del número de capturas de cada especie de Scolytinae con los tratamientos se utilizó el Análisis de Correspondencia (AC). Los datos de frecuencia fueron sometidos a un análisis de estadística descriptivo con el fin de calcular el número promedio, número mínimo y máximo, número total y el porcentaje de insectos capturados por especie en función de la trampa y el atrayente.
Resultados
Se registraron 408 Scolytinae, se determinaron cuatro géneros y diez especies; de los cuales, 396 especímenes pertenecieron al género Hypothenemus; de donde se identificaron siete especies, H. seriatus presentó la menor abundancia, con tan solo dos registros, mientras que, H. birmanus fue la más abundante con 237 registros. De los géneros Coccotrypes, Microcorthylus y Xyleborus se obtuvo el registro de las especies C. cyperi, M. minimus y X. volvulus; de la especie M. minimus se recolectaron 10 ejemplares, y de la especie C. cyperi y X. volvulus se recolectó un sólo ejemplar (Cuadro 2). Además, se registraron 38 especímenes de Cerambycidae, 44 de Staphylinidae, 17 de Bostrichidae, 9 de Cleridae, 4 de Anthribidae, 39 especímenes del orden Díptera y 5 de Lepidóptera.
Cuadro 2 Especies de Scolytinae recolectadas en el ecosistema de mangle en Tampico, Tamaulipas.
| Subfamilia | Género | Especie | Total | % |
| Scolytinae | Coccotrypes | Coccotrypes cyperi (Beeson)* | 1 | 0.2 |
| Hypothenemus | Hypothenemus birmanus (Eichhoff) | 237 | 58.1 | |
| Hypothenemus crudiae (Panzer) | 119 | 29.2 | ||
| Hypothenemus obscurus (F.)* | 20 | 4.9 | ||
| Hypothenemus eruditus Westwood* | 10 | 2.5 | ||
| Hypothenemus interstitialis (Hopkins) | 4 | 1.0 | ||
| Hypothenemus javanus (Eggers) | 4 | 1.0 | ||
| Hypothenemus seriatus (Eichhoff) | 2 | 0.5 | ||
| Microcorthylus | Microcorthylus minimus Schedl | 10 | 2.5 | |
| Xyleborus | Xyleborus volvulus (F.) | 1 | 0.2 |
*Nuevos registros para Tamaulipas, México.
La mayor captura se registró en el tratamiento cuatro (T13) que correspondió a la combinación Trampa 4 + Etanol con un total de 103 especímenes (Cuadro 3). En el número de insectos recolectados entre los cuatro tipos de trampas se registraron diferencias estadísticamente significativas (p = 0.000), siendo la Trampa 4 la que registró el número mayor de insectos (Fig. 2); de igual manera en el número de insectos recolectados por tipo de atrayente se observaron diferencias estadísticamente significativas (p =0.000, Fig. 3). El Etanol, Etanol+ Metanol y Vinagre de manzana + Etanol registraron el número mayor de insectos (promedios similares) en comparación con el Metanol. El número de especies por cada tratamiento fue variable, en el T6 y T10 únicamente se colectó a la especie H. crudiae, en el T1, T14 y T16 dos especies, en el T7 y T8 tres especies, en el T2, T3, T4, T9, T11, T12 y T13 cuatro especies, y en el T5 y T15 cinco especies (Cuadro 4).
Cuadro 3 Captura total de Scolytinae por cada tratamiento evaluado.
| Tratamiento | Total | % | Media | Mínimo | Máximo |
| T1 | 14 | 3.431372549 | 2.333333333 | 0 | 11 |
| T2 | 8 | 1.960784314 | 1.142857143 | 0 | 2 |
| T3 | 12 | 2.941176471 | 1.5 | 0 | 3 |
| T4 | 66 | 16.17647059 | 7.333333333 | 0 | 36 |
| T5 | 17 | 4.166666667 | 1.888888889 | 1 | 6 |
| T6 | 3 | 0.735294118 | 0.6 | 0 | 1 |
| T7 | 7 | 1.715686275 | 1 | 0 | 3 |
| T8 | 24 | 5.882352941 | 4 | 0 | 11 |
| T9 | 19 | 4.656862745 | 2.111111111 | 0 | 7 |
| T10 | 4 | 0.980392157 | 0.8 | 0 | 3 |
| T11 | 12 | 2.941176471 | 1.5 | 0 | 4 |
| T12 | 22 | 5.392156863 | 2.75 | 0 | 9 |
| T13 | 103 | 25.24509804 | 14.71428571 | 0 | 76 |
| T14 | 8 | 1.960784314 | 1.333333333 | 0 | 4 |
| T15 | 78 | 19.11764706 | 11.14285714 | 0 | 73 |
| T16 | 11 | 2.696078431 | 1.833333333 | 1 | 3 |
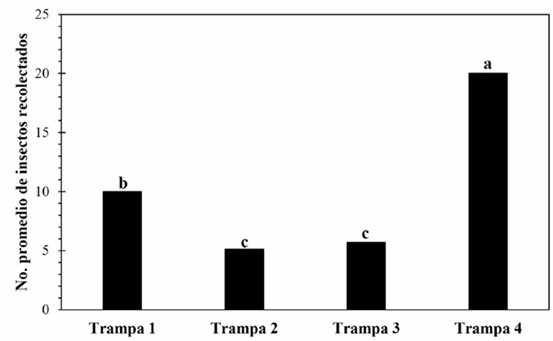
Figura 2 Análisis descriptivo del número promedio de insectos capturados por tipo de trampa en el área de estudio. Donde: La letra sobre la barra de datos representa una diferencia estadística, y las barras con la misma letra indican que los promedios de captura son estadísticamente iguales.
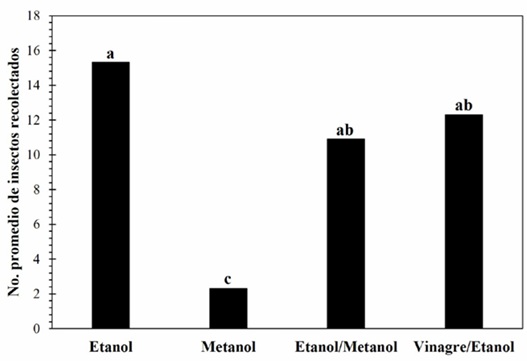
Figura 3 Análisis descriptivo del número promedio de insectos capturados por tipo de atrayente en el área de estudio. Donde: La letra sobre la barra de datos representa una diferencia estadística, y las barras con la misma letra indican que los promedios de captura son estadísticamente iguales.
Cuadro 4 Especies de Scolytinae recolectadas tratamiento.
| Tratamiento | Genero | Especie | Total | % | Media | Mínimo | Máximo |
| T1 | Hypothenemus | H. birmanus | 13 | 3.186275 | 6.5 | 2 | 11 |
| T1 | Hypothenemus | H. obscurus | 1 | 0.245098 | 1 | 1 | 1 |
| T2 | Hypothenemus | H. birmanus | 1 | 0.245098 | 1 | 1 | 1 |
| T2 | Hypothenemus | H. crudiae | 2 | 0.490196 | 1 | 1 | 1 |
| T2 | Hypothenemus | H. obscurus | 3 | 0.735294 | 1.5 | 1 | 2 |
| T2 | Microcorthylus | M. minimus | 2 | 0.490196 | 2 | 2 | 2 |
| T3 | Hypothenemus | H. birmanus | 4 | 0.980392 | 2 | 2 | 2 |
| T3 | Hypothenemus | H. crudiae | 2 | 0.490196 | 2 | 2 | 2 |
| T3 | Hypothenemus | H. obscurus | 4 | 0.980392 | 2 | 1 | 3 |
| T3 | Microcorthylus | M. minimus | 2 | 0.490196 | 2 | 2 | 2 |
| T4 | Hypothenemus | H. birmanus | 47 | 11.51961 | 15.66667 | 2 | 36 |
| T4 | Hypothenemus | H. crudiae | 14 | 3.431373 | 4.666667 | 1 | 11 |
| T4 | Hypothenemus | H. javanus | 4 | 0.980392 | 4 | 4 | 4 |
| T4 | Microcorthylus | M. minimus | 1 | 0.245098 | 1 | 1 | 1 |
| T5 | Hypothenemus | H. birmanus | 12 | 2.941176 | 2.4 | 1 | 6 |
| T5 | Hypothenemus | H. eruditus | 1 | 0.245098 | 1 | 1 | 1 |
| T5 | Hypothenemus | H. obscurus | 2 | 0.490196 | 2 | 2 | 2 |
| T5 | Hypothenemus | H. seriatus | 1 | 0.245098 | 1 | 1 | 1 |
| T5 | Microcorthylus | M. minimus | 1 | 0.245098 | 1 | 1 | 1 |
| T6 | Hypothenemus | H. crudiae | 3 | 0.735294 | 1 | 1 | 1 |
| T7 | Hypothenemus | H. birmanus | 2 | 0.490196 | 2 | 2 | 2 |
| T7 | Hypothenemus | H. crudiae | 4 | 0.980392 | 2 | 1 | 3 |
| T7 | Hypothenemus | H.interstitialis | 1 | 0.245098 | 1 | 1 | 1 |
| T8 | Hypothenemus | H. birmanus | 20 | 4.901961 | 10 | 9 | 11 |
| T8 | Hypothenemus | H. obscurus | 3 | 0.735294 | 3 | 3 | 3 |
| T8 | Xyleborus | X. volvulus | 1 | 0.245098 | 1 | 1 | 1 |
| T9 | Cocotrypes | C. cyperi | 1 | 0.245098 | 1 | 1 | 1 |
| T9 | Hypothenemus | H. birmanus | 13 | 3.186275 | 4.333333 | 1 | 7 |
| T9 | Hypothenemus | H. eruditus | 3 | 0.735294 | 3 | 3 | 3 |
| T9 | Microcorthylus | M. minimus | 2 | 0.490196 | 1 | 1 | 1 |
| T10 | Hypothenemus | H. crudiae | 4 | 0.980392 | 2 | 1 | 3 |
| T11 | Hypothenemus | H. birmanus | 5 | 1.22549 | 2.5 | 1 | 4 |
| T11 | Hypothenemus | H. eruditus | 3 | 0.735294 | 1.5 | 1 | 2 |
| T11 | Hypothenemus | H.interstitialis | 1 | 0.245098 | 1 | 1 | 1 |
| T11 | Hypothenemus | H. obscurus | 3 | 0.735294 | 3 | 3 | 3 |
| T12 | Hypothenemus | H. birmanus | 15 | 3.676471 | 7.5 | 6 | 9 |
| T12 | Hypothenemus | H. crudiae | 2 | 0.490196 | 1 | 1 | 1 |
| T12 | Hypothenemus | H. eruditus | 1 | 0.245098 | 1 | 1 | 1 |
| T12 | Hypothenemus | H. obscurus | 4 | 0.980392 | 2 | 2 | 2 |
| T13 | Hypothenemus | H. birmanus | 25 | 6.127451 | 8.333333 | 1 | 23 |
| T13 | Hypothenemus | H. crudiae | 76 | 18.62745 | 76 | 76 | 76 |
| T13 | Hypothenemus | H. eruditus | 1 | 0.245098 | 1 | 1 | 1 |
| T13 | Hypothenemus | H.interstitialis | 1 | 0.245098 | 1 | 1 | 1 |
| T14 | Hypothenemus | H. crudiae | 6 | 1.470588 | 2 | 1 | 4 |
| T14 | Microcorthylus | H. minimus | 2 | 0.490196 | 2 | 2 | 2 |
| T15 | Hypothenemus | H. birmanus | 73 | 17.89216 | 73 | 73 | 73 |
| T15 | Hypothenemus | H. crudiae | 2 | 0.490196 | 2 | 2 | 2 |
| T15 | Hypothenemus | H. eruditus | 1 | 0.245098 | 1 | 1 | 1 |
| T15 | Hypothenemus | H.interstitialis | 1 | 0.245098 | 1 | 1 | 1 |
| T15 | Hypothenemus | H. seriatus | 1 | 0.245098 | 1 | 1 | 1 |
| T16 | Hypothenemus | H. birmanus | 7 | 1.715686 | 1.75 | 1 | 3 |
| T16 | Hypothenemus | H. crudiae | 4 | 0.980392 | 2 | 1 | 3 |
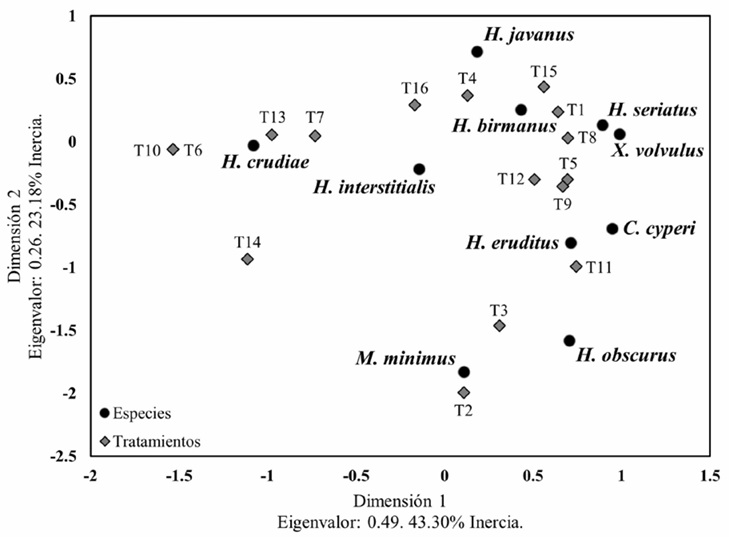
La frecuencia del número de capturas de cada especie de Scolytinae se asoció significativamente con los tratamientos evaluados (X 2 g.l. 135 = 466.24, p = 0.000, Fig. 4). La posición canónica de las especies H. crudiae e H. interstitialis mostraron una alta asociación con los tratamientos T6 (Trampa 2 con Metanol), T10 (Trampa 3 con Metanol) y T14 (Trampa 4 con Metanol). Mientras que, la posición canónica de las especies C. cyperi, H. eruditus, H. obscurus y M. minimus presentaron una fuerte asociación con los tratamientos T2 (Trampa 1 con Metanol), T3 (Trampa 1 con Etanol/Metanol), T5 (Trampa 2 con Etanol), T9 (Trampa 3 con Etanol), T11 (Trampa 3 con Etanol/Metanol) y T12 (Trampa 3 con Vinagre/Etanol). Por otro lado, la posición canónica de las especies H. birmanus, H. javanus, H. seriatus y X. volvulus exhibieron una alta asociación con los tratamientos T1 (Trampa 1 con Etanol), T4 (Trampa 1 con Vinagre/Etanol), T8 (Trampa 2 con Vinagre/Etanol) y T15 (Trampa 4 con Etanol/Metanol). Finalmente, la posición canónica de los tratamientos T7 (Trampa 2 con Etanol/Metanol), T13 (Trampa 4 con Etanol) y T16 (Trampa 4 con Vinagre/Etanol) no revelaron una asociación con las categorías de las especies, por lo que se puede inferir que estas combinaciones no son eficaces para la captura de Scolytinae.
Discusión
Por su bajo costo y eficacia, las trampas artesanales o elaboradas a mano son usadas ampliamente con fines de monitoreo y control de diversas especies dentro de la subfamilia Scolytinae en México y otros países, destacándose entre ellas, las trampas elaboradas de envases de plástico de refrescos embotellados (envases PET), ya que, dentro de sus ventajas, está la amplia disponibilidad, menor costo y la oportunidad de contribuir al reciclado de este tipo de materiales (Reding et al., 2010; Steininger et al., 2015; Lázaro-Dzul et al., 2023).
El diseño y la eficacia de las trampas para la captura de Scolytinae pueden estar influenciados por diversos factores ambientales y estructurales. En el presente estudio, se observaron diferencias significativas en el número de capturas entre los distintos diseños de trampas, lo que sugiere que la morfología y el área de captura juegan un papel importante en la atracción y retención de los insectos. Aunque aún se desconoce en gran medida cómo varía el espacio activo entre trampas con diferentes diseños, se ha documentado que factores meteorológicos y de comportamiento pueden limitar la eficiencia de captura, incluso si se incrementa dicho espacio (Allison & Redak, 2017).
Se ha reportado que la volatilización del atrayente debido a la radiación solar y la influencia del viento pueden afectar la efectividad de las trampas, disminuyendo el número de capturas, como se ha observado en estudios previos sobre la broca del café (Hypothenemus hampei) en El Salvador y Nicaragua (Dufour, 2008). Además, la dispersión de los compuestos volátiles se ve afectada por la difusión turbulenta, lo que genera columnas de olor intermitentes que pueden dificultar la orientación de los insectos hacia la fuente de atracción (Murlis et al., 1992; Kuenen & Cardé, 1994). En este estudio, a pesar de que las trampas no estuvieron directamente expuestas al sol, las corrientes de viento en la zona de estudio pudieron haber interferido en la difusión del atrayente, generando diferencias en la eficiencia de captura entre los tratamientos evaluados (trampas + atrayentes).
Otro factor determinante en la captura de insectos es la capacidad de retención y el área de superficie de la trampa. Estudios han demostrado que trampas de intercepción de vuelo con recipientes de recolección húmedos son más eficientes para capturar coleópteros barrenadores en comparación con aquellas con recipientes secos (Miller & Duerr, 2008; Graham & Poland, 2012; Allison et al., 2014). En este sentido, los resultados del presente estudio coinciden con estos hallazgos, ya que se corroboró la eficiencia de los recipientes húmedos en la recolección de insectos en los cuatro diseños de trampa evaluados.
En cuanto al área de superficie, las trampas con mayor superficie de silueta tienden a capturar un mayor número de insectos (Allison & Redak, 2017). En este estudio, la Trampa 4, fabricada con una botella de 2.5 L presentó la mayor captura de Scolytinae en comparación con las trampas 1, 2 y 3, que fueron elaboradas con botellas de menor capacidad (1-1.5 L). Estos resultados son consistentes con lo reportado por McIntosh et al. (2001), quienes encontraron que trampas con una mayor área de silueta incrementaron o mantuvieron el número de capturas en comparación con aquellas de menor tamaño. Sin embargo, estos resultados contrastan con los hallazgos de Mayfield y Brownie (2013), quienes determinaron que, en el caso de Xyleborus glabratus, un incremento excesivo en el diámetro de la trampa no necesariamente mejoró su atracción. Con relación al numero de ventanas laterales de las trampas, los resultados concordaron con lo reportado por Mendoza-Cervantes et al. (2021) quienes al utilizar trampas artesanales elaboradas de envases PET de tres ventanas, observaron su eficiencia para la captura de la especie, H. hampei. Sin embargo, difirieron de lo documentado por Moreno-Rodríguez et al. (2010), Steininger et al. (2015) y Lázaro-Dzul et al. (2023) quienes reportaron mayor eficiencia en la captura de Scolytinae, al utilizar trampas de envases PET con una sola ventana lateral.
En cuanto a los atrayentes, el etanol fue el compuesto más eficiente en la captura de especies de Scolytinae, lo cual concuerda con estudios previos que han demostrado su eficacia para atraer escarabajos barrenadores en ecosistemas forestales (Hulcr et al., 2008; Ranger et al., 2018). Este compuesto es liberado naturalmente por árboles estresados o en descomposición, convirtiéndolo en un atrayente ideal para el monitoreo de especies polífagas (Bouget et al., 2009; Reding et al., 2010; Steininger et al., 2015).
Asimismo, la combinación de metanol y etanol incrementó la atracción de ciertos Scolytinae, como se ha documentado en estudios previos sobre H. hampei (Moreno-Rodríguez et al., 2010; Uemura-Lima et al., 2010; Pereira et al., 2012). La mezcla de vinagre y etanol también resultó eficiente, coincidiendo con lo reportado por Mendoza-Cervantes et al. (2021), quienes encontraron que esta combinación es altamente efectiva para la captura de H. hampei.
En términos de abundancia por atrayente, el etanol permitió la captura del mayor número de especies (ocho en total), mientras que la especie X. volvulus solo fue recolectada con la mezcla de vinagre y etanol. Esto sugiere que el vinagre podría tener un efecto sinérgico con el etanol, mejorando la captura de ciertas especies. Estudios previos en México han reportado que el etanol es el atrayente más eficiente para la recolección de Scolytinae en diferentes ecosistemas (Gerónimo-Torres et al., 2015; Pérez-De La Cruz et al., 2009b; 2016).
Este estudio, documentó la abundancia de especies del género Hypothenemus, lo cual concuerda con estudios previos en manglares (Gerónimo-Torres et al., 2015; 2021) y en otros ecosistemas como selvas y agroecosistemas (Pérez-De La Cruz et al., 2016; Falcón-Brindis et al., 2018; Aguilar-Castillo et al., 2023). Además, la abundancia de este género se atribuye a su amplia distribución en zonas tropicales y subtropicales, así como a su capacidad de colonizar una gran variedad de tejidos vegetales y niveles de descomposición (Wood & Bright, 1992; Johnson et al., 2016). La especie H. birmanus fue la más abundante, debido a su preferencia por pecíolos y ramas pequeñas de plantas leñosas (Wood, 2007; Pérez-De La Cruz et al., 2009b). También ha sido reportada en asociación con diversas especies de mangle (Rhizophora mangle, Laguncularia racemosa y Avicennia germinans), lo que explica su presencia en la zona de estudio (Atkinson & Equihua, 1985; Atkinson, 2024). La segunda especie más abundante, H. crudiae, ocurre en ecosistemas de manglar y agroecosistemas de aguacate (Gerónimo-Torres et al., 2015; 2021; Lázaro-Dzul et al., 2020), lo cual se debe a su carácter polífago y su capacidad de habitar distintos tipos de tejidos vegetales (Atkinson & Equihua, 1985; Vega et al., 2015; Atkinson, 2024). Otras especies como M. minimus y X. volvulus han sido reportadas en manglares de Tabasco y Tamaulipas (Gerónimo-Torres et al., 2015; 2021; Lázaro-Dzul et al., 2021). Sin embargo, la baja abundancia de X. volvulus en este estudio contrasta con los registros de Tabasco, donde se encontró en mayor cantidad (Gerónimo-Torres et al., 2015; 2021). Estas diferencias pueden atribuirse a variaciones en la vegetación, disponibilidad de alimento, presencia de competidores y condiciones ambientales como temperatura y humedad (Rudinsky, 1962; Pérez-De La Cruz et al., 2009b).











 nueva página del texto (beta)
nueva página del texto (beta)