Introducción
Los roedores tienen diferentes interacciones ecológicas con sus ectosimbiontes. Entre estas destacan la foresia, el comensalismo y el parasitismo. La foresia es definida por Seeman y Walter (2023) como una simbiosis en la que una fase de vida de un animal de tamaño pequeño se adhiere a uno más grande con el fin de dispersarse. El comensalismo ocurre cuando un individuo se beneficia al asociarse con otro, el huésped, y este ni gana ni pierde (Walter & Proctor, 2013). Un parásito se puede definir como un organismo que vive dentro o sobre otro organismo del cual obtiene sus nutrientes (Bautista-Hernández et al., 2015).
Los roedores sinantrópicos Rattus rattus (Linnaeus, 1758) y Mus musculus Linnaeus, 1758, están asociados con grandes pérdidas económicas y productivas, por lo que son considerados una plaga importante a nivel global (Clapperton, 2006). Estos mamíferos pequeños causan daños materiales a las viviendas al roer cables eléctricos, paredes, tuberías de plomo, madera, presas de hormigón y otros materiales de construcción (Nowak, 1999; Bonnefoy et al., 2008). Así mismo, afectan a campos de cultivo y granjas al alimentarse de granos o productos almacenados, o bien, al contaminarlos con sus heces y orina (Pimentel et al., 2005).
Además, están involucrados con enfermedades zoonóticas actuando como huéspedes o reservorios intermediarios de agentes infecciosos, los cuales, pueden ser transmitidos por sus ectoparásitos (Himsworth et al., 2013). Bajo esta premisa, identificar los ectosimbiontes de roedores sinantrópicos nos proporciona un acercamiento a su papel potencial como vectores de agentes infecciosos, siendo los ectoparásitos generalistas los que tienen mayor relevancia en el ámbito médico-veterinario (Pimm, 1984).
En Yucatán, México, R. rattus y M. musculus, han sido registrados en áreas rurales, sub-urbanas y urbanas (Baak-Baak et al., 2016; Cigarroa-Toledo et al., 2016; Núñez-Corea, 2021, Panti-May et al., 2023). Baak-Baak et al. (2016, 2018) y Núñez-Corea (2021) han documentado ectosimbiontes de importancia médica en R. rattus y M. musculus capturados en domicilios, parques y zoológicos de Yucatán (Cuadro 1).
Cuadro 1: Registros previos de ectosimbiontes en dos especies de roedores sinantrópicos del estado de Yucatán, México. M=Mus musculus, R=Rattus rattus.
| Clase | Orden | Especie | Huésped | Lugar | |
| M | R | ||||
| Insecta | Psocodea | Polyplax spinulosa | Mérida*, Xkalakdzonot | ||
| Insecta | Psocodea | Liposcelis bostrychophila | x | Mérida | |
| Insecta | Siphonaptera | Ctenocephalides felis | x | Mérida | |
| Arachnida | Mesostigmata | Laelaps echidninus | x | Mérida**, Xkalakdzonot | |
| Arachnida | Mesostigmata | Ornithonyssus bacoti | x | x | Mérida |
| Arachnida | Mesostigmata | Androlaelaps fahrenholzi | x | Xkalakdzonot | |
| x | x | ||||
*Reporte en domicilios y parques. **Reporte en domicilios, parques y el Zoológico. M: M. musculus; R: R. rattus.
En comunidades costeras como Celestún, el estudio sobre la abundancia de estos mamíferos es escaso y no se conoce tampoco mucho sobre su fauna asociada. Es importante señalar que los roedores sinantrópicos viven en estrecha asociación con humanos, por lo que representan un riesgo para la salud pública.
Aunado a esto, en Mérida, Yucatán se encontró evidencia serológica para los virus Dengue, Apoi, fiebre amarilla, Modoc y encefalitis de San Luis en los roedores sinantrópicos R. rattus y M. musculus (Cigarroa-Toledo et al., 2016). El municipio de Celestún forma parte de la Reserva de la Biósfera Ría Celestún (RBRC); dada su importancia como un centro turístico, es necesario llevar a cabo estudios sobre la abundancia de roedores sinantrópicos y de sus ectosimbiontes.
Materiales y métodos
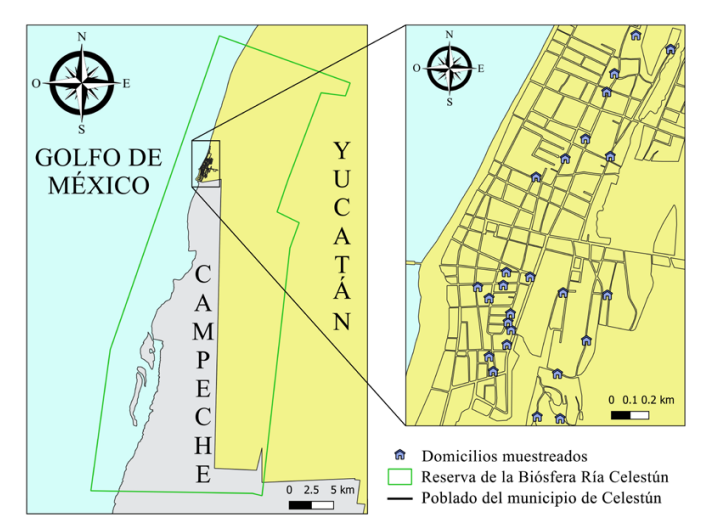
Área de estudio. El estudio se realizó en el municipio de Celestún, que pertenece a la Reserva de la Biosfera Ría Celestún, localizada en el extremo noroccidental de la Península de Yucatán. Tiene una superficie de 81,482.33 ha, ubicadas entre los municipios de Celestún y Maxcanú, en el estado de Yucatán, y Calkiní en el estado de Campeche (SEMARNAT, 2002). El comité de Ética y Comité Interno para el Cuidado y Uso de los Animales de Laboratorio del Centro de Investigaciones Regionales Dr. Hideyo Noguchi de la Universidad Autónoma de Yucatán aprobó los protocolos utilizados en el estudio (CEI-04-2023 y CICUAL-002-2023). Los roedores sinantrópicos fueron capturados mediante el permiso de colecta científica registrada con el número de bitácora 31/K5-0044/05/23 de la Secretaría de Medio Ambiente y Recursos Naturales, México.
Captura de roedores y extracción de ectoparásitos. La captura de roedores sinantrópicos se realizó dos veces al mes de julio a diciembre de 2023 en 25 domicilios del municipio de Celestún (Fig, 1). Para su captura, se cebaron trampas tipo jaula RatiplaxS, del número dos (9 cm x 25 cm x 13 cm) y tres (10 cm x 27.5 cm x 14.5 cm), con pan de harina y semillas de girasol (Helianthus annuus) o avena (Avena sativa) con esencia de vainilla comercial. Se colocaron tres trampas en cada domicilio durante tres noches consecutivas. Los roedores capturados fueron identificados siguiendo las descripciones contenidas en guías morfológicas (Emmons, 1990; Reid, 2009) y se procesaron siguiendo las indicaciones de la Norma Oficial Mexicana NOM-062-ZOO-1999, Especificaciones técnicas para la producción, cuidado y uso de los animales de laboratorio. Con el propósito de disminuir el estrés, previo al sacrificio, los especímenes se sedaron mediante una inyección de xilacina (IM dosis 1.5-2mg/kg); 10 minutos después, se sacrificaron empleando una sobredosis de pentobarbital vía intraperitoneal a una dosis 150 mg/kg. Posteriormente, se empleó el dislocamiento cervical para garantizar la muerte.
La extracción de ectosimbiontes en los roedores se realizó con peines y pinzas entomológicas bajo microscopio estereoscópico (Carl Zeiss Microlmaging GmbH®). Los ectosimbiontes recolectados fueron preservados en tubos tipo Eppendorf de 0.5 ml con alcohol al 70%. Para su identificación morfológica, los ácaros se aclararon con solución de lactofenol y se montaron en líquido de Hoyer en porta y cubreobjetos. Los ácaros se identificaron bajo microscopio de luz invertida (ZEISS ID 03) con la ayuda de claves taxonómicas (Fain et al., 1970; Bochkov, 2010; Masan & Fenda, 2010; Herrera-Mares et al., 2021). La pulga se montó con solución de polivinil lactofenol y se identificó siguiendo las características reportadas por Hii et al. (2015). Las especies de ácaros se fotografiaron con microscopía electrónica de barrido (MEB) en el Laboratorio Nacional de la Biodiversidad (LANABIO), Instituto de Biología, Universidad Nacional Autónoma de México. La metodología de MEB consistió en que los ácaros se fijaron en glutaraldehído al 2% y posteriormente se fijaron en buffer de cacodilato al 1%. Posteriormente, los ácaros se deshidrataron en una serie de concentraciones crecientes de etanol y se secaron hasta el punto crítico con CO2. En el siguiente paso, los ácaros se recubrieron con oro. Las micrografías de MEB se obtuvieron con un microscopio de barrido digital (Hitachi VP-SEM SU1510, Hitachi High Technologies America, Inc.).
Análisis de datos. Los parámetros ecológicos de prevalencia, abundancia e intensidad promedio se estimaron con el software Quantitative Parasitology on the Web (Reiczigel et al., 2019).
Prevalencia: Es expresada como el número de individuos de una especie de huéspedes infestados con una especie de parásito, entre el número de huéspedes examinados expresada en porcentaje (Bush et al., 1997).
Abundancia: Es el número total de una especie de parásito entre el total de huéspedes tanto infectados como no infectados (Margolis et al., 1982).
Intensidad promedio: Es el número total de parásitos de una especie particular encontrada en una muestra dividida entre el número de huéspedes infectados con ese parásito (Bush et al., 1997).
Resultados
De los 25 domicilios seleccionados, solo en uno no se detectó la presencia de roedores sinantrópicos. Se capturaron un total de 82 individuos, de los cuales, M. musculus fue más abundante seguido por R. rattus. En total se recolectaron 551 ectosimbiontes obtenidos de 45 roedores infestados, 42 M. musculus y 3 R. rattus (Cuadro 2). De estos huéspedes se identificaron seis taxones de artrópodos, cinco pertenecen a ácaros y uno a insectos. Ningún taxón fue compartido por ambos roedores.
Cuadro 2: Niveles de infestación de los ectosimbiontes registrados en dos especies de roedores sinantrópicos en Celestún, Yucatán, México. NE/RI= Número de ectosimbiontes/ roedores infestados, P (%)= Prevalencia en porcentaje, A= Abundancia, IP= Intensidad promedio.
| Clase | Orden | Especie de roedor/taxón de ectosimbionte | NE/RI | P (%) | A | IP |
| ; | Mus musculus n=59 | ; | ; | |||
| Arachnida | Sarcoptiformes | Listrophoridae* | 404/13 | 22.03 | 6.85 | 37.08 |
| Arachnida | Sarcoptiformes | M. musculinus | 9/3 | 5.10 | 0.15 | 3 |
| Arachnida | Trombidiformes | M. murismusculi | 46/16 | 27.12 | 0.78 | 2.88 |
| Arachnida | Trombidiformes | R. affinis | 49/10 | 16.95 | 0.83 | 4.9 |
| ; | ; | ; | ; | |||
| ; | ; | Rattus rattus n=23 | ; | ; | ||
| Arachnida | Mesostigmata | L. echidninus | 42/2 | 8.70 | 1.83 | 21 |
| Arachnida | Siphonaptera | C. felis | 1/1 | 4.30 | 0.04 | 1 |
Ectosimbiontes asociados a Mus musculus . El roedor sinantrópico M. musculus fue la especie que presentó la mayor riqueza de ectosimbiontes con cuatro taxones asociados. Siendo estos, la familia Listrophoridae y las especies Myocoptes musculinus (Koch, 1844), Myobia murismusculi (Schrank, 1781) y Radfordia affinis (Poppe, 1896). El mióbido R. affinis (Fig. 2) fue el más prevalente, mientras que, la familia Listrophoridae fue la más abundante y la que mayor intensidad promedio presentó. La menor prevalencia y abundancia correspondió al miocóptido M. musculinus y la menor intensidad promedio al mióbido M. murismusculi (Fig. 3).
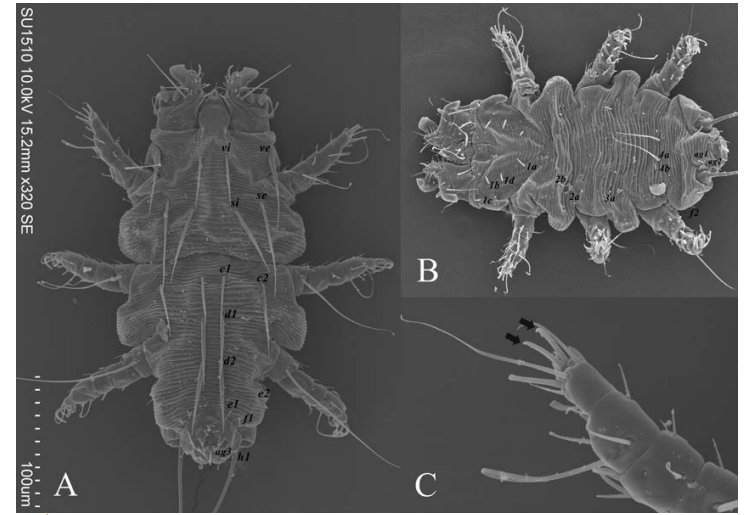
Figura 2 Ácaro Randfordia affinis Poppe, 1896 hembra. (A) Quetotaxia en vista dorsal, (B) Quetotaxia en vista ventral y (C) Pata II con dos uñas tarsales.

Figura 3 Ácaro Myobia murismusculi Schrank, 1781 hembra. (A) Quetotaxia en vista ventral, (B) Primer par de patas y (C) Pata II con una uña tarsal grande.
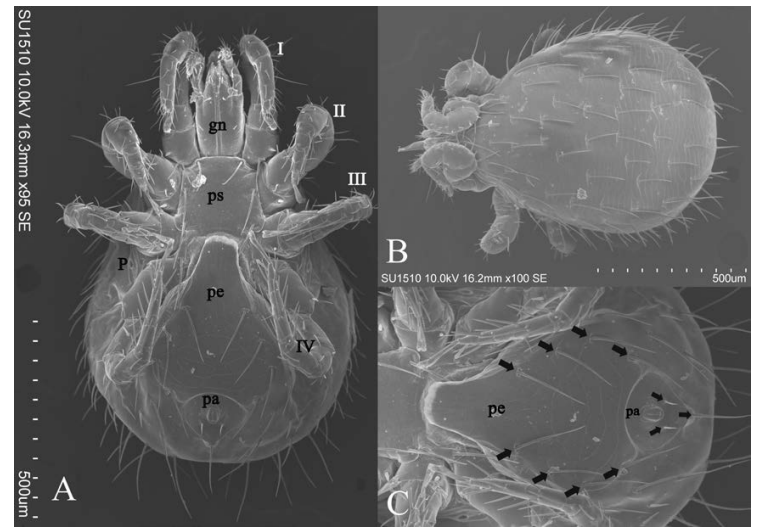
Ectosimbiontes asociados a Rattus rattus . El roedor R. rattus solo presentó dos taxones asociados, el ácaro mesostigmado Laelaps (Echinolaelaps) echidninus (Berlese, 1887) y la pulga Ctenocephalides felis (Bouché, 1835). La prevalencia, abundancia e intensidad promedio fue mayor en el ácaro L. echidninus (Fig. 4) y en C. felis (Fig. 5) fue menor.
al., 2014; Panti-May et al., 2015; Peniche-Lara et al., 2015; Cigarroa-Toledo et al., 2016; Solís-Hernández et al., 2016; Torres-Castro et al., 2016).
Figura 4 Ácaro Laelaps echidninus Berlese, 1878 hembra. (A) Vista ventral gn: Gnathosoma, I-IV: Patas, ps: Placa esternal, p: Peritrema, pe: Placa epigidial, pa: Placa anal, (B) Vista dorsal y (C) Placa epigidial con cuatro setas y placa anal con tres setas.
Discusión
Las especies de roedores M. musculus y R. rattus fueron comunes en los domicilios de Celestún. Cabe señalar que, los roedores sinantrópicos tienen un papel importante en salud pública debido a que pueden estar involucrados en el ciclo infectivo de enfermedades zoonóticas e inclusive actuar como reservorios naturales, huéspedes intermediarios y huéspedes de ectoparásitos vectores (Meerburg et al., 2009). En Yucatán, estudios realizados con pruebas moleculares y serológicas en M. musculus y R. rattus también han revelado la presencia de Leptospira interrogans, Leptospira kirschneri, Borrelia burgdorferi (sensu lato), Rickettsia typhi, Rickettsia felis, Toxoplasma gondii, Trypanosoma cruzi, Cysticercus fasciolaris, virus Dengue, virus Apoi, virus de la fiebre amarilla, virus Modoc y virus de la encefalitis de San Luis (Panti-May et al., 2013; Torres-Castro et al., 2014; Panti-May et al., 2015; Peniche-Lara et al., 2015; Cigarroa-Toledo et al., 2016; Solís-Hernández et al., 2016; Torres-Castro et al., 2016).
Los ácaros de la familia Listrophoridae pasan todo su ciclo de vida sobre el pelaje de sus huéspedes, tienen una amplia diversidad y comúnmente son ectosimbiontes de roedores (Fain, 1976; Sikora & Bochkov, 2012). Sobre M. musculus se han encontrado los géneros Prolistrophorus y Listrophorus (Wilson & Lawrence, 1967; Fain, 1973). En R. rattus se han encontrado los géneros Olistrophorus y Afrolistrophorus (Fain 1971, 1972). Sin embargo, ha sido poco estudiada en México. De los 20 géneros que se conocen cuatro (Listrophorus, Prolistrophorus, Geomilychus y Asiochirus) han sido registrados en el país (Fain, 1973; Fain & Estebanes, 1996; Vargas et al., 1999; Bochkov, 2010).
En relación con el ácaro miocóptido M. musculinus éste se describió por primera vez en roedores M. musculus en Alemania. Esta especie es común en roedores de laboratorio (Fain et al., 1970); sin embargo, se le ha encontrado también en ratones domésticos M. musculus (Bochkov, 2016) y otros autores la han referido en asociación con especies silvestres, tales como: Apodemus sylvaticus Linnaeus, 1758; Apodemus flavicollis Melchior, 1834; Peromyscus leucopus Rafinesque, 1818 y Peromyscus maniculatus Wagner, 1845 (Fain et al., 1970; Fain & Hyland, 1970; Haitlinger, 1986; Whitaker et al., 2007). Asimismo, Vilcins et al. (2009) reportan este ácaro en el marsupial Dasyurus maculatus Kerr, 1792. La presencia de esta especie en especies del género Apodemus y D. maculatus fue referida por Bochkov (2010) como un intento del ácaro por cambiar de huésped.
En México, se han registrado 41 especies de ácaros pertenecientes a la familia Myobiidae, los cuales, son ectosimbiontes de los órdenes Chiroptera, Dasyuromorphia, Didelphimorphia, Diprotodontia, Erinaceomorpha, Macroscelidea, Microbiotheria, Paucituberculata, Rodentia y Soricomorpha (Bochkov 2009; Sidorchuk et al., 2018). En particular, los géneros Myobia, Radfordia y Zacaltepetla incluyen especies que se relacionan directamente con pequeños roedores (Herrera-Mares et al., 2021). En el estado de Yucatán, solo se han referido ácaros mióbidos de los géneros Eudusbabekia e Ioannela, los cuales, son específicos de quirópteros (Whitaker & Morales-Malacara, 2005; Herrera-Mares et al., 2017; Herrera-Mares et al., 2021).
Schnaas et al. (1968) reportan por primera vez al ácaro R. affinis sobre ratones de laboratorio M. musculus. Así mismo, mencionan a la especie M. murismusculi, pero sin proporcionar datos sobre el lugar y huésped de recolecta. Además, ha sido encontrada sobre roedores M. musculus, Peromyscus gratus Merriam, 1898 y Baiomys taylori Thomas, 1887 (Hoffmann & López-Campos, 2000).
Respecto a estos ácaros, Maaz et al. (2018) obtuvieron resultados similares en cuanto a los parámetros ecológicos, la familia Listrophoridae fue más abundante, seguida por las familias Myobiidae y Myocoptidae; donde Myobiidae fue la de mayor prevalencia. Reeves y Cobb (2005) refirieron a M. murismusculi más prevalente respecto a R. affinis, sin embargo, M. musculinus tuvo una prevalencia mayor. La baja abundancia y prevalencia del ácaro miocóptido puede deberse a un desplazamiento por el mióbido M. murismusculi. Esto se ha observado en dos colonias de ratones de laboratorio donde los resultados para la colonia A fue contraria a la de la B (Bressan et al., 1997).
Actualmente, se sabe que ninguno de estos ácaros está asociado con la transmisión de patógenos. Sin embargo, Fain et al. (1970), mencionan la pérdida de pelo en roedores con altas infestaciones de ácaros miocóptidos. Asimismo, Watson (1961) observó que además de la pérdida de pelo, en algunos roedores infestados por M. musculinus y M. murismusculi se presentaba hinchazón de tejidos, pérdida de peso e incluso la muerte.
En Yucatán, el mesostigmado L. echidninus ha sido referido en asociación con R. rattus y M. musculus, aunque, en este último con una prevalencia muy baja (Baak-Baak et al., 2016; Núñez-Corea, 2021). Cabe destacar que los huéspedes R. rattus resultaron positivos por serología a la presencia de virus de la fiebre amarilla, virus Modoc y virus Apoi (Baak-Baak et al., 2016). Por otro lado, Baak-Baak et al. (2018) encontraron una relación entre la abundancia de este ácaro con el piojo Polyplax spinulosa Burmeister, 1839. Aunque en nuestro estudio el piojo P. spinulosa no fue recolectado. Además, L. echidninus es el vector principal del protozoario apicomplexa Hepatozoon muris que afecta a ratas y también se ha identificado el virus junin, el agente causal de la fiebre hemorrágica epidémica (Strandtmann & Wharton, 1958; Parodi et al., 1959). Kuo et al. (2020) lograron identificar en ácaros L. echidninus fragmentos de los genes gltA y ompB, los cuales, están relacionados con especies de bacterias del género Rickettsia del grupo de las fiebres manchadas. Este ácaro puede alimentarse de humanos y puede no presentar preferencia por un huésped específico (Wharton & Cross 1957).
La única especie de insecto encontrada fue la pulga C. felis que es considerada como oportunista debido a la amplia gama de hospederos en los que se ha encontrado (Rust, 2017). En Yucatán, se ha reportado principalmente en gatos y perros domésticos (Zavala-Velázquez et al., 2002; Peniche-Lara et al., 2018). Baak-Baak et al. (2016) identificaron a la pulga C. felis sobre el roedor sinantrópico R. rattus en Mérida. Más tarde, Peniche-Lara et al. (2015) refirió a C. felis sobre el roedor endémico Peromyscus yucatanicus Allen & Chapman (1897) en el municipio de Oxkutzcab, Yucatán. Asimismo, en el estado de Yucatán, se ha identificado ADN de Rickettsia typhi en la pulga C. felis y es el vector principal de Rickettsia felis (Zavala-Velazquez et al., 2002; Peniche-Lara et al., 2015). No obstante, C. felis es el vector principal de Bartonella henselae, y es el hospedero intermediario del cestodo Dipylidium caninum Linnaeus (1758) que afecta a perros (McElroy et al., 2010; Beugnet et al., 2014). El mesostigmado L. echidninus se ha documentado en Yucatán con baja abundancia, mientras que, las prevalencias reportadas han sido similares, siendo la menor de 8.16 % y la mayor 10.67% (Baak-Baak et al., 2016; Núñez-Corea, 2021). En este estudio, se recolectaron muchos ejemplares de pocos roedores, por lo que la intensidad promedio fue alta. Se sabe que estos ácaros tienen este comportamiento cuando sus huéspedes principales son poco abundantes (Thomas, 1956). En cuanto a C. felis, Baak-Baak et al. (2016) reportaron una prevalencia menor, pero con una abundancia mayor a la obtenida en este estudio. El tamaño, peso y densidad corporal del huésped influyen en la riqueza y abundancia de las pulgas, por lo que en roedores los parámetros ecológicos suelen ser bajos (Bitam et al., 2010; Clark et al., 2018; Kessy et al., 2024).
Los ácaros listrophoridos, R. affinis, M. murismusculi y M. musculinus se reportan por primera vez en el estado de Yucatán. Debido a la alta especificidad que tienen estos ácaros, son un punto clave para investigar la relación huésped-ectosimbionte en cuanto a la evolución paralela, coevolución y relaciones filogenéticas (Fain, 1994; Herrera-Mares et al., 2021). En cuanto a los ectoparásitos L. echidninus y C. felis, estos presentan importancia médico-veterinaria por lo que es importante conocer su distribución y rango de huéspedes, ya que, se sabe que pueden participar en la transmisión de enfermedades zoonóticas. Adicionalmente, se sugiere el monitoreo en animales silvestres, sinantrópicos, domésticos y de crianza principalmente en áreas rurales y suburbanas como las áreas naturales protegidas.
Como parte del estudio se emitieron recomendaciones a los moradores de las viviendas para evitar la presencia de roedores, entre las cuales, se sugirió el ordenamiento de la basura en los patios, el correcto almacenamiento de granos, cubrir los orificios que pudieran funcionar como madrigueras y la higiene en el interior de los domicilios.











 nueva página del texto (beta)
nueva página del texto (beta)