INTRODUCCIÓN
La vigilia y el sueño son dos estados esenciales que, en el humano, así como en otras especies, se alternan durante el día y la noche, acompañándose de actividad, el primero; y de reposo, el segundo. Estos procesos están regulados por interacciones entre diversas regiones del cerebro y sus sistemas de neurotransmisión1. En esta revisión exploramos los mecanismos neurobiológicos subyacentes a estos estados, en particular, el involucro de los endocannabinoides y de las orexinas en la regulación de la vigilia y el sueño, y su potencial involucro en el abuso de sustancias.
La palabra sueño deriva de latín somnus: sueño y de somnium: imaginaciones, y hace alusión al estado fisiológico de quietud e inconsciencia reversible de duración variable que el humano exhibe con recurrencia circadiana; es decir, cada 24 horas. El sueño es un estado en el que se ausenta la consciencia, definiendo sucintamente consciencia como la capacidad del sujeto de percibir e interactuar voluntariamente con su medio interno y con su entorno.
Cuando la consciencia desaparece, la capacidad de respuesta voluntaria a la estimulación externa consecuentemente también desaparece, aunque se conserva la respuesta a estímulos significativos para el durmiente, como escuchar su nombre, la alerta sísmica o el llanto de su hijo. En los casos en que dichos estímulos se manifiestan, tienen el potencial de despertar al individuo del sueño, provocando una respuesta consciente a estos estímulos.
El sueño también se acompaña de procesos autonómicos dinámicos, como cambios en la frecuencia respiratoria y cardíaca.
El tono muscular se reduce hasta desaparecer durante la fase de sueño de movimientos oculares rápidos (sMOR)2,3. Asimismo, hay cambios en la liberación de hormonas, v. gr., aumento de las hormonas melatonina, del crecimiento, prolactina y reducción del factor liberador de corticotropina (CRF), de la corticotropina y del cortisol.
También hay cambios en la actividad eléctrica cerebral que reflejan las diferentes fases de sueño por las que transita un sujeto a lo largo de una noche.
CARACTERÍSTICAS POLISOMNOGRÁFICAS DE LAS FASES DE SUEÑO Y SU ALTERNANCIA A LO LARGO DE LA NOCHE
Es importante señalar que no dormimos de la misma manera a lo largo de toda la noche. De manera general, dividimos al sueño en dos fases principales: el sueño sin movimientos oculares rápidos (sNMOR) y el sueño de movimientos oculares rápidos (sMOR). A lo largo de la noche hay una alternancia cíclica de estos dos estados: sNMOR-sMOR. En la fase de sMOR ocurren las ensoñaciones4, aunque algunos investigadores creen que hay ensoñaciones también en las fases de sNMOR. En todo caso, los eventos cognitivos durante el sNMOR tienen características diferentes a las que llamamos ensoñaciones.
El sNMOR se compone de tres fases:
La fase N1, que es la transición entre la vigilia y el sueño, dura entre 5-10 minutos y se caracteriza por cursar con una relajación progresiva de los músculos sin llegar a la atonía. El sujeto tiene los párpados cerrados; sin embargo, podemos observar movimientos oculares lentos a los que llamamos pendulares. La actividad eléctrica cerebral, registrada con el electroencefalograma (EEG), se observa más lenta respecto a la actividad registrada en vigilia, expresando ondas alfa (8.0-13.0 Hz) y theta (4.0-7.5 Hz), además de ondas agudas del vertex. Puede haber sacudidas musculares repentinas (mioclonías) y el sujeto puede despertar fácilmente de esta fase.
La fase N2, se expresa en varios brotes por noche de sueño y cada brote dura entre 10 y 25 minutos. En total, constituye aproximadamente el 50% del sueño nocturno. En esta fase se produce una mayor relajación muscular, el EEG muestra grafoelementos llamados “husos del sueño” o ritmo sigma y “complejos K”. La frecuencia cardíaca y la temperatura corporal disminuyen. No hay movimientos oculares.
La fase N3, llamada también sueño profundo, sueño de ondas lentas, sueño sincronizado o sueño delta, se expresa en brotes de alrededor de 20-40 minutos. Se considera, junto con el sMOR, la fase de sueño más profunda y reparadora. Se caracteriza porque en el EEG predominan ondas cerebrales lentas, denominadas ondas delta (0.5-4.0 Hz)5. En el adulto joven, esta fase se expresa en la primera parte de la noche y desaparece en la segunda parte.
Por otro lado, el sMOR tiene una duración aproximada de 10 minutos en el primer brote, que ocurre aproximadamente 90 minutos después de iniciado el sueño. La duración de los brotes de sMOR va incrementándose a lo largo de la noche y hacia la mañana puede llegar a tener hasta 40 minutos de duración. En esta fase, la actividad eléctrica cerebral es semejante a la de la vigilia, constituida por ondas beta (13.5-30.0 Hz). Además, se caracteriza porque los ojos se mueven rápidamente, y porque hay atonía muscular. Asimismo, la frecuencia cardíaca, la presión arterial y la temperatura corporal se vuelven erráticas y como ya mencionamos, durante esta fase es donde se dan principalmente las ensoñaciones4,6-8.
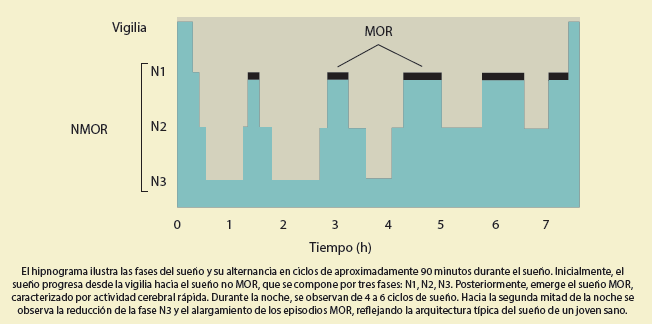
Cada ciclo sNMOR-sMOR dura aproximadamente 90 minutos, repitiéndose de 4 a 6 veces por noche en un adulto joven. A medida que avanza la noche y se aproxima la mañana, los periodos de sMOR se alargan y las fases de sueño profundo (N3) desaparecen (figura 1 ). En el sNMOR, especialmente en la fase de sueño profundo, la tasa metabólica disminuye, permitiendo que las neuronas se deshagan de productos de desecho como radicales libres, a través del sistema glinfático, liberando al cerebro de estos productos y de otros más cuya acumulación es potencialmente tóxica. Esta fase de sueño también se asocia a la consolidación de la memoria declarativa5,7. El sMOR, es esencial para la maduración y remodelación neuronal asociada al aprendizaje, procesamiento de información y regulación del estado de ánimo; asimismo, se ha asociado a consolidación de memoria no declarativa o procedimental9 y a la formación de nuevas estrategias para la solución de problemas10.
El hipnograma ilustra las fases del sueño y su alternancia en ciclos de aproximadamente 90 minutos durante el sueño. Inicialmente, el sueño progresa desde la vigilia hacia el sueño no MOR, que se compone por tres fases: N1, N2, N3. Posteriormente, emerge el sueño MOR, caracterizado por actividad cerebral rápida. Durante la noche, se observan de 4 a 6 ciclos de sueño. Hacia la segunda mitad de la noche se observa la reducción de la fase N3 y el alargamiento de los episodios MOR, reflejando la arquitectura típica del sueño de un joven sano.
El término vigilia, deriva del latín vigilare, que se refiere a la “acción de estar despierto o en vela”, y hace alusión al estado durante el cual el sujeto interacciona con su entorno voluntariamente, es decir, está consciente. En esta fase, el sujeto exhibe conductas orientadas a objetivos, con una actividad motora coordinada y propositiva, y manifiesta respuestas a estímulos generados internamente o en el entorno11. Durante la vigilia, el EEG se compone de ondas de frecuencias rápidas y de baja amplitud, denominadas ondas alfa (8.0-13.0 Hz) y ondas beta (13.5-30.0 Hz), asociadas a un procesamiento cognitivo activo. Asimismo, hay tono muscular sostenido de fondo, pero que cambia con diversos grados de actividad.
EL MODELO DE LOS DOS PROCESOS PARA LA OCURRENCIA DEL SUEÑO
¿Qué cambios neurofisiológicos y neuroquímicos propician el sueño? Esta es una pregunta cuya respuesta es pertinente, ya que nos ayuda a entender cómo ocurre el sueño y cómo la alteración de estos mecanismos evita la expresión normal del sueño, favoreciendo patologías y propiciando la ausencia de salud y de bienestar del individuo. Uno de los modelos explicativos sobre los mecanismos que subyacen a la ocurrencia del ciclo vigilia-sueño es el de los dos procesos cerebrales, el cual propone un componente homeostático (proceso S) y un componente circadiano (proceso C)12.
El proceso C
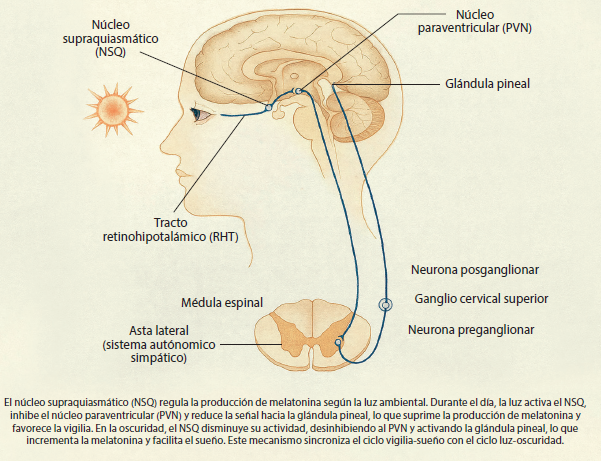
Está regulado por el núcleo supraquiasmático (NSQ). Este núcleo está ubicado en la parte anterior del hipotálamo (figura 2), y se comporta como el “reloj maestro” del cuerpo, generando un ritmo de actividad-inactividad para diversos procesos fisiológicos, incluyendo el ciclo vigilia-sueño. El NSQ establece un ritmo circadiano, de circa: alrededor y diem: día, del ciclo vigilia-sueño. Es decir, la actividad del NSQ está sincronizada con el ciclo de luz-oscuridad que es ocasionado por la rotación de la tierra. Los humanos y prácticamente todas las especies animales se ajustan al ciclo luz-oscuridad para dormir.
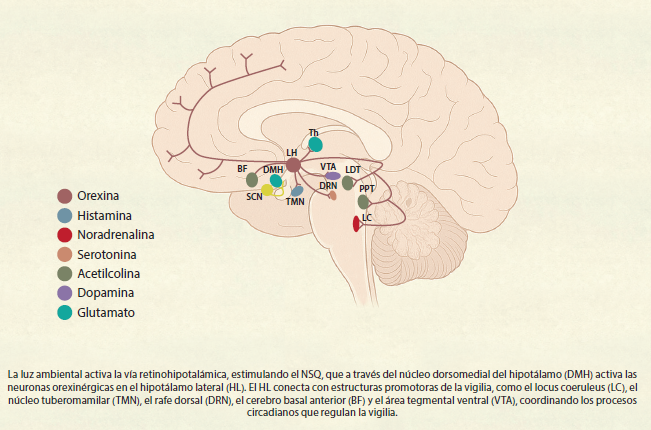
Algunos animales duermen durante la noche y forrajean durante el día, mientras que otros duermen durante la luz y forrajean durante la noche. El NSQ recibe información sobre la luminosidad ambiental directamente de la retina a través del tracto retino-hipotalámico (TRH)13. Este tracto está formado por los axones de las células ganglionares productoras de melanopsina de la retina14 que activan a las células del NSQ por medio de glutamato. La activación del NSQ tiene varias consecuencias neurofisiológicas, incluyendo la activación de sistemas cerebrales promotores de la vigilia, como son las neuronas glutamatérgicas del núcleo hipotalámico dorsomedial (NHDM), las cuales activan a las neuronas hipocretinérgicas/orexinérgicas, cuyos axones están conectados con las neuronas de los núcleos locus coeruleus (LC, noradrenérgico), tuberomamilar (TMN, histaminérgico), rafe dorsal (RDN, serotoninérgico), núcleos del cerebro basal anterior (BF, colinérgicos), el área tegmental ventral (ATV, dopaminérgicos) y otros (figura 3)15. Asimismo, el NSQ promueve la inhibición de la producción de melatonina por la glándula pineal, al inhibir al núcleo paraventricular hipotalámico (PVN). El PVN, cuando está libre de la inhibición del NSQ, es decir en la noche, activa a las neuronas de la asta lateral de la médula espinal torácica superior, las cuales activan a las neuronas del ganglio cervical superior, cuyas neuronas activan a las células de la glándula pineal, promoviendo que la glándula libere melatonina. A su vez, esta hormona reduce la actividad del NSQ, facilitando, de esta manera, el inicio del sueño (figura 2). Así que, durante la noche, cuando la actividad del NSQ desciende, consecuentemente se reduce la actividad de los sistemas promotores de la vigilia, facilitando la actividad en los sistemas promotores del sueño y promoviendo la liberación de melatonina. Todo ello participa en la generación del sueño.
La actividad de las neuronas del NSQ, principalmente GABAérgicas, depende de la expresión de ciertos genes, v. gr., BMAL1 / BMAL2, CLOCK, CRY1/ CRY2 y PER1 / PER2 / PER3 que regulan y controlan su propia transcripción y traducción, oscilando en un ciclo de 24 horas. Esta dinámica expresión de los genes mantiene el ritmo circadiano incluso en ausencia de señales externas, como la luz solar16. El proceso C, ha ayudado al humano a adaptarse a los ciclos ambientales. Gracias a este sistema los seres humanos y diversos otros animales, optimizan el uso de energía y regulan la fisiología del cuerpo17. Los ritmos circadianos no solo son importantes para la regulación del ciclo vigilia-sueño, también lo son para la regeneración celular, la regulación hormonal, la ingestión de alimento y el funcionamiento del cerebro incluyendo los procesos cognitivos.
El proceso S
Este proceso considera la acumulación de sustancias promotoras de sueño durante la vigilia, como la adenosina, que aumenta la presión del sueño o necesidad para dormir. La adenosina es un producto del metabolismo de la adenosina trifosfato (ATP), principal molécula de energía en las células. Las evidencias experimentales indican que se acumula en el cerebro durante las horas de vigilia y termina promoviendo el sueño, presuntamente cuando alcanza un umbral de concentración en algunas regiones cerebrales18. Así que, a medida que la adenosina se acumula, la presión por dormir aumenta, al activar neuronas GABAérgicas de la región hipotalámica llamada área preóptica medial (mPOA) y ventrolateral (vlPO). Las neuronas GABAérgicas inhiben a las neuronas de todos los núcleos promotores de la vigilia, ya mencionados en la sección de vigilia, lo que incluye a las neuronas hipocretinérgicas/orexinérgicas6,11,12.
LOS NEUROTRANSMISORES EN LA REGULACIÓN DEL CICLO SUEÑO-VIGILIA
Neurotransmisores, como la acetilcolina (ACh), la dopamina (DA), la noradrenalina (NA), la serotonina (5-HT), la histamina (Hi) y los péptidos hipocretina/orexina, trabajan juntos para mantener la vigilia. La liberación de ACh cortical es mayor durante la vigilia y el sMOR y menor durante el sNMOR19. La 5-HT se libera a partir de neuronas de los núcleos del rafe, en particular del núcleo de rafé dorsal. La NA se libera a partir de neuronas del LC. Las células noradrenérgicas del LC inhiben al sMOR, promueven la vigilia y activan diversas regiones cerebrales como el tálamo, el hipotálamo, el cerebro basal anterior y la corteza cerebral. La histamina se libera a partir de neuronas del núcleo TMN del hipotálamo posterior. La actividad de los diferentes neurotransmisores y estructuras que regulan la vigilia está orquestada por la actividad de las hipocretinas/orexinas. Los cuerpos celulares de las neuronas productoras de hipocretinas/orexinas están localizados en el hipotálamo lateral y se comunican con todas las regiones cerebrales que regulan el alertamiento, esta actividad es crucial para mantener la vigilia y prevenir el sueño, particularmente cuando las demandas del medio exigen estar despierto (figura 3).20
OTRAS MOLÉCULAS QUE REGULAN EL CICLO SUEÑO-VIGILIA
La cortistatina
Esta molécula es un péptido cuya expresión parece restringirse a neuronas corticales, de allí su nombre y por su parecido bioquímico con la somatostatina21. Este péptido aumenta su concentración al final del periodo de vigilia y la reduce al final del periodo de sueño. Asimismo, la cortistatina aumenta significativamente durante la privación de sueño total por 24 h, pero se reduce con 8 h de recuperación de sueño22. Su administración exógena induce sueño en la rata, regula la memoria23 y la percepción del dolor24.
El péptido intestinal vasoactivo (VIP) y la colecistocinina (CCK)
Son dos neuropéptidos que aumentan eficientemente el sMOR. Asimismo, proteínas originalmente descritas como mediadoras de la respuesta proinflamatoria, como la interleucina 1beta (IL-1beta) y el factor de necrosis tumoral alfa (TNF alfa) son proteínas que aumentan el sNMOR25.
En resumen, el ciclo vigilia-sueño es orquestado por una compleja interacción entre el ritmo circadiano (proceso C) regulado por el NSQ y el proceso homeostático (proceso S) mediado por moléculas que se acumulan durante la vigilia, como la adenosina y la cortistatina, que aumentan su concentración conforme la vigilia avanza y producen un aumento de la presión del sueño. Cuando el sujeto duerme se reduce la concentración de estas moléculas, presuntamente a través del sistema glinfático, facilitando la generación de vigilia acompañada de una sensación subjetiva de descanso26. La interacción de estos dos procesos no es tan simple, como hemos mencionado arriba, debemos considerar el concurso de otros neurotransmisores y hormonas, particularmente aquellos cuya desregulación afectan el sueño y facilitan la adicción a sustancias.
CONCLUSIONES
El ciclo vigilia-sueño constituye un proceso biológico complejo y fundamental para el mantenimiento de la homeostasis cerebral y sistémica. A lo largo de este trabajo hemos revisado los mecanismos fisiológicos y neuroquímicos que regulan los estados de vigilia y sueño, destacando que su equilibrio depende de una intrincada interacción entre diferentes núcleos cerebrales, neurotransmisores, neuropéptidos y factores circadianos.
Los hallazgos expuestos reafirman que el sueño no debe entenderse como un estado pasivo, sino como un proceso activo y dinámico que involucra funciones críticas como la consolidación de la memoria, la plasticidad sináptica, la regulación emocional y la eliminación de metabolitos neurotóxicos. Asimismo, la vigilia no constituye únicamente la contraparte del sueño, sino un estado organizado en el que la consciencia y la interacción con el entorno se sostienen gracias a un delicado balance neuroquímico27.
Otro aspecto central del sueño es su regulación mediante dos procesos -el circadiano (C) y el homeostático (S). La influencia del núcleo supraquiasmático y su sincronización con los ciclos luz-oscuridad se complementa con la acumulación de moléculas promotoras del sueño, como la adenosina, constituyendo un sistema adaptativo que optimiza la eficiencia energética y la regulación fisiológica sincronizada a las señales ambientales de luz-oscuridad. No obstante, como se ha mostrado, este modelo se complejiza al integrar la participación de moléculas adicionales como la cortistatina, el péptido intestinal vasoactivo, la colecistocinina y citoquinas proinflamatorias.
De manera complementaria, es importante señalar que esta revisión constituye la primera parte de un análisis más amplio sobre los sistemas neurobiológicos que regulan la vigilia y el sueño, y como estos sistemas neurobiológicos también juegan un papel fundamental en el abuso de sustancias28. Esta segunda parte profundizará en los mecanismos mediante los cuales los sistemas de endocannabinoides29, y de orexinas30 contribuyen a la regulación de diversas funciones fisiológicas, incluyendo la arquitectura del sueño, así como su participación en la instalación de trastornos del sueño y su papel en la respuesta a reforzadores como drogas de abuso y en el desarrollo de abuso de sustancias31.











 nueva página del texto (beta)
nueva página del texto (beta)