INTRODUCCIÓN
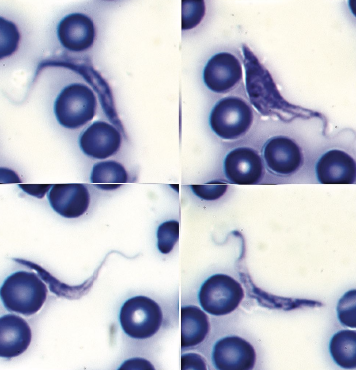
La enfermedad de Chagas, o tripanosomiasis americana, es una enfermedad cuyo agente etiológico es Trypanosoma cruzi, que es transmitido de forma natural por vectores. Según estimaciones de la Organización Mundial de la Salud (OMS), entre 6 y 7 millones de personas están infectadas en el mundo, con aproximadamente 30,000 casos nuevos y 12,000 muertes anuales1,2. Por sus características de distribución regional, es endémica en 21 países de América Latina, con mayor incidencia en áreas rurales y cinturones de pobreza de zonas urbanas y suburbanas. Por lo anterior, se considera una enfermedad tropical desatendida, olvidada o de la pobreza. Se calcula que aproximadamente 75 millones de habitantes se encuentran en riesgo de infección3; además, además, debido a los altos índices migratorios, la enfermedad se ha extendido a regiones no endémicas, como ocurre en América del Norte, Europa e incluso Asia2,4.
México es un país endémico, con una estimación de 4.06 millones de personas infectadas, cifra superior a los 1.1 millones de casos estimados en años anteriores5-7. Se han identificado 31 especies de triatominos en el territorio mexicano, de las cuales 29 han sido reportadas como infectadas con T. cruzi, lo que coloca al 88% de la población en riesgo de infección vectorial7. Entre 2010 y 2023, la Secretaría de Salud reportó un promedio anual de 783 casos, con mayor incidencia en los estados de Veracruz (17.8%), Yucatán (10.3%), Oaxaca (10.5%), Morelos (9.2%), Chiapas (8.1%), Jalisco (5.9%), Estado de México (5.2%)8,9.
En el país existe un subregistro de casos debido a la falta de acceso de la población al diagnóstico y al tratamiento, como ocurre en la mayoría de los países endémicos, donde existe desconocimiento de la enfermedad tanto por parte de la población como del personal de salud. Se estima que la prevalencia de la infección en menores de 18 años es del 1.51%, lo que confirma la transmisión activa y convierte a la enfermedad en un problema de salud pública vigente6,7.
Enfermedad de Chagas en menores de 18 años
La enfermedad crónica en edad pediátrica ha sido poco conocida debido a que la mayoría de los estudios y casos reportados se desarrollaron en adultos. La primoinfección parasitaria ocurría usualmente en la infancia, especialmente en regiones endémicas, donde la convivencia con el transmisor formaba parte de la vida cotidiana y no se identificaba como fauna nociva.
Las principales vías de transmisión en niños fueron la vectorial y la denominada materno-fetal o vertical, que ocurría principalmente de forma transplacentaria o durante el parto10,11. Aunque el modo de transmisión tenía valor epidemiológico, no modificaba el diagnóstico, tratamiento o seguimiento de estos casos12.
La historia natural de la enfermedad en población pediátrica siguió el mismo patrón que en el adulto, con una fase aguda y otra crónica, que podía ser asintomática o sintomática10.
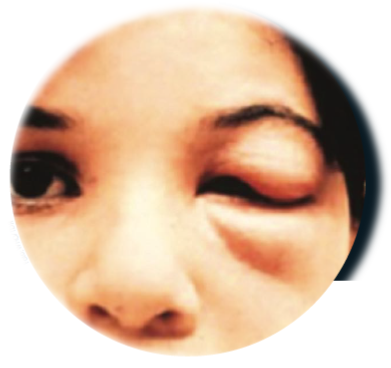
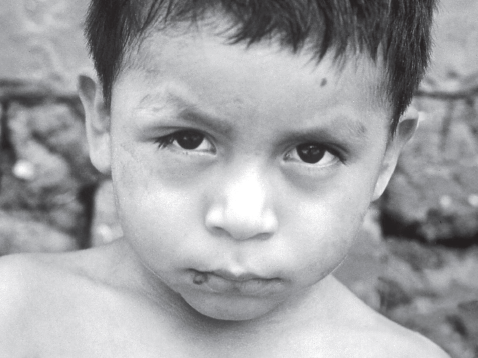
La fase aguda fue generalmente asintomática o con síntomas leves o inespecíficos en el 5% de los casos; cuando la transmisión era vectorial, los síntomas iniciaban entre 7 y 10 días después de la infección; cuando era por transfusión sanguínea, entre los 20 y 40 días posteriores. En esta fase, el signo de Romaña-Mazza se consideraba patognomónico y formaba parte del complejo oftalmoganglionar que se presentaba cuando el parásito ingresaba al organismo cerca de la mucosa ocular; se caracterizaba por edema bipalpebral unilateral, violáceo, con prurito leve y adenopatías preauriculares, submaxilares o retroauriculares. Cuando penetraba en otra región del cuerpo, se denominaba chagoma de inoculación, que consistía en una lesión nodular subcutánea violácea con adenitis regional; ambos con duración de 2 a 3 semanas. Las manifestaciones sistémicas eran variables e inespecíficas; la fiebre era lo más frecuente y usualmente poco elevada, sin características especiales. Podía acompañarse de astenia, mialgias, artralgias y hepatoesplenomegalia.
Menos del 1% de estos casos desarrollaban formas graves en la fase aguda, principalmente niños desnutridos, con otras morbilidades o inmunocomprometidos. Las complicaciones incluían meningoencefalitis, miocarditis, pericarditis e incluso pancarditis, con evolución generalmente fatal13. En México, en 2011 se reportaron dos casos de infecciones agudas en San Luis Potosí, ambos con signo de Romaña y fiebre, que evolucionaron favorablemente después del diagnóstico temprano y tratamiento con benznidazol14.
En años recientes, se han reportado casos de complicaciones durante la fase aguda en pacientes pediátricos con evolución fatal, debido a una desregulación de la respuesta del sistema inmune ante la infección, aunado a otros factores donde se describió que, a menor edad, mayor era el riesgo de aparición de estas complicaciones.
En Brasil, un masculino de 2 años y 10 meses presentó fiebre persistente, cefalea, vómito, dolor abdominal y erupción cutánea generalizada, y falleció a los 75 días con diagnóstico de “paro cardiorrespiratorio” por miocarditis15. Otro caso, también en Brasil, fue el de una lactante de 22 meses de edad con edema bipalpebral, anasarca, fiebre, vómito, diarrea y exantema generalizado de 13 días de evolución; en el frotis sanguíneo se confirmó la presencia de T. cruzi, se inició tratamiento con benznidazol y, a los 26 días, falleció16. En Venezuela, una niña de 2 años de edad con diagnóstico inicial de neumonía fue ingresada a un hospital donde le diagnosticaron pericarditis, ascitis, hepatoesplenomegalia y derrames pleural y pericárdico; el frotis sanguíneo resultó positivo para T. cruzi y falleció a los 17 días17.
Respecto a escolares y adolescentes, en Brasil se reportó el caso de dos hermanos masculinos: uno de 9 años, que a los 21 días del inicio de los síntomas se complicó con disnea, anasarca, hepatomegalia y derrame pleural izquierdo, y murió a los cinco días por insuficiencia respiratoria; el otro, de 16 años de edad, evolucionó con hipotensión, disnea, taquicardia, cardiomegalia y derrame pericárdico, presentó falla cardíaca y falleció a los nueve días18. Otro paciente del sexo masculino de 6 años presentó derrame pericárdico derecho con cardiomegalia progresiva y falleció a los 27 días. La necropsia confirmó el diagnóstico de miocarditis por enfermedad de Chagas19.
La mayoría de los casos que cursaron esta fase aguda sobrevivieron aun sin tratamiento y evolucionaron a la cronicidad inicialmente asintomática (sin patología demostrable)5,10.
La fase crónica se presentó en forma asintomática (sin patología demostrada) o sintomática (con patología demostrada). La forma asintomática pudo durar entre 5 y hasta 20 años, y se caracterizó por presentar parasitemia muy baja, por lo que el diagnóstico empleaba métodos serológicos. Esta fase afectó al 35 % de los infectados, personas que sufrieron daño cardíaco o en otros órganos (principalmente en esófago y colon)5,20.
La fase crónica sintomática afectó también al 35 % de los infectados21. La enfermedad de Chagas fue la causa de miocardiopatía infecciosa más frecuente del mundo, comprometió varios tejidos cardíacos y las alteraciones cardiovasculares fueron variadas. Predominó el daño cardíaco caracterizado por insuficiencia cardiaca progresiva y cardiomegalia, además de alteraciones en la contractilidad. Cuando el daño no fue extenso, las anormalidades fueron mínimas o ausentes, y el trazo electrocardiográfico (ECG) pudo ser normal por un tiempo, hasta que los mecanismos de compensación propios del órgano fueron incapaces de contrarrestar la insuficiencia cardiaca. Cuando el tratamiento antiparasitario se administró en esta fase o previamente, fue eficaz y con muy buen pronóstico.
El aumento de áreas de contracción anormal originó el inicio de la disnea progresiva; si el daño fue severo, se manifestó como una disfunción segmentaria o global, con dilatación cavitaria y, por ende, con alteraciones de la función ventricular con insuficiencia. La disnea fue el síntoma más frecuente, aunque también se presentaron palpitaciones, taquicardia y algias precordiales22-25.
Los trastornos autonómicos fueron descritos desde 1911 por Chagas y Villela. Actualmente, se consideró característico en esta cardiopatía las alteraciones del ritmo, extrasístoles ventriculares y bloqueos de rama. La fibrilación auricular fue menos frecuente, pero de pronóstico grave por causar tromboembolismo. La muerte se presentó por insuficiencia progresiva del miocardio, que finalizó en asistolia, o en forma súbita por arritmias ventriculares19,26,27.
Las alteraciones cardíacas en edad pediátrica fueron variadas y la información disponible resultó escasa. En un estudio realizado en menores de 18 años, se analizaron 37 casos seropositivos con sintomatología compatible con la enfermedad, clasificados en tres grupos: Grupo 1 (12 casos), sin alteraciones en el ECG; Grupo 2 (11 casos), con alteraciones en el ECG o ECO; y Grupo 3 (14 casos), con alteraciones cardiológicas severas. En estos casos, los síntomas se presentaron en el 70 % de los pacientes; la disnea fue lo más frecuente en los tres grupos (59%), seguida de dolor precordial (51%), palpitaciones (43%) y taquicardia (16%). En el ECO, las alteraciones encontradas fueron hipertrofia septal y/o de pared posterior (38%), fracción de eyección del ventrículo izquierdo (FEVI) < 57% (14%) e hipertensión pulmonar (11%)23. En el ECG, todos los casos del Grupo 2 presentaron bloqueo incompleto de rama derecha; y en el Grupo 3, 12 mostraron bloqueo completo o incompleto de rama derecha del haz de His, hipertrofia de ventrículo izquierdo o de aurícula derecha, arritmia y bradicardia sinusal.
Existe un metaanálisis donde se concluyó que las alteraciones electrocardiográficas en niños y adolescentes fueron las mismas que en los adultos, con mayor frecuencia los bloqueos incompletos o completos de rama derecha, del fascículo anterior izquierdo y aurículo-ventriculares. Se ha descrito que la muerte fue más rápida en los casos pediátricos23,28,29.
En la patogénesis de las lesiones, se desarrollaron varios mecanismos de respuesta a la infección. En los casos que vivieron en áreas endémicas, las reinfecciones por convivencia con el vector favorecieron la cronicidad y progresión de las lesiones. En las pruebas de ECO destacaron la hipertrofia septal y de pared posterior, originadas por el proceso inflamatorio y la consecuente fibrosis, debido a la respuesta inmune tipo IV, activación de células T de memoria y reclutamiento de mononucleares al sitio de inflamación. Cuando se presentó incremento en la respuesta proinflamatoria con baja expresión de los antagonistas, se favoreció la cronicidad con progresión de las lesiones30.
La hipertrofia ocasionó motilidad anormal de las cavidades con deterioro de la función cardiaca, lo que explicó los valores anormales en el tiempo de relajación isovolumétrica y de la fracción de expulsión del ventrículo izquierdo. En algunos casos, se presentó hipertensión pulmonar, debida al deterioro funcional del órgano y a las alteraciones en la circulación microvascular, con formación de trombos plaquetarios, característico en esta enfermedad. Las alteraciones de conducción y ritmo que se presentaron en los trazos del ECG se debieron a lesión parasimpática causada por la fibrosis miocárdica presente en las taquiarritmias (taquicardia o fibrilación ventricular), principales causas de muerte súbita en adultos crónicos; esta fibrosis bloqueó el impulso cardiaco, lo que disminuyó la velocidad de conducción31-34.
Tratamiento antiparasitario
La OPS, con el propósito de fomentar el diagnóstico y tratamiento adecuados de la enfermedad, recomendó el tratamiento tripanocida para todos los pacientes diagnosticados, ya sea en fase aguda o crónica; estrategia que se consideró la intervención más efectiva para combatir la enfermedad. Los medicamentos continuaron siendo el benznidazol (actualmente con presentación pediátrica) y el nifurtimox35.
El tratamiento erradicó la infección y previno complicaciones sistémicas, ya que se comprobó que, cuanto más temprano se diagnosticó y trató la enfermedad, mayor fue la posibilidad de alcanzar la seronegativización, principal criterio de cura12.
Se estimó que solo el 1% de los infectados recibió tratamiento y seguimiento adecuados, debido a las múltiples barreras de acceso a la salud, la falta de diagnóstico o la falta de disponibilidad de los medicamentos1.
Con objeto de resaltar los desafíos significativos en la sospecha, el diagnóstico y el manejo de la enfermedad en población pediátrica, se documentó un caso clínico desde la inoculación del parásito en la fase aguda hasta el fallecimiento en la fase crónica sintomática.
CASO CLÍNICO
Paciente del sexo masculino de 13 años, proveniente del municipio de San Antonio, San Luis Potosí, residente de zona rural en vivienda tipo “choza” (varas y palmas, con piso de tierra), con una sola habitación para ocho personas. Se identificaron ejemplares de Triatoma dimidiata, que fueron mostrados; se refirió convivencia frecuente con estos insectos tanto dentro como fuera del domicilio. La madre reportó que el menor había sido picado en más de 10 ocasiones. No presentaba antecedentes transfusionales y contaba con esquema de vacunación completo.
A la edad de 5 años y 4 meses, acudió al Centro de Salud acompañado de su madre por presentar fiebre y edema bipalpebral izquierdo con eritema conjuntival. Fue referido al Hospital de Ciudad Valles, donde le realizaron lavado ocular con aparente remisión del cuadro. Quince días después fue hospitalizado por fiebre no cuantificada, tos, exantema macular puntiforme y hepatoesplenomegalia, con sospecha de paludismo. Le administraron antihistamínicos y se tomaron muestras sanguíneas para frotis y gota gruesa. Cinco días después fue dado de alta, asintomático y sin los resultados de la prueba sanguínea.
A los 6 años y 8 meses, presentó dolor precordial con fiebre no cuantificada, hiporexia, hipodinamia y disnea, por lo que acudió nuevamente al hospital. A la exploración física mostró polipnea, cianosis peribucal, tiros intercostales, dolor a la palpación de hemitórax izquierdo y hepatomegalia de 3 a 4 cm por debajo del reborde costal. La auscultación pulmonar reveló hipoventilación, y la cardíaca, un chasquido en diástole. Los estudios de laboratorio fueron normales. La radiografía de tórax mostró cardiomegalia grado 3 con condensación basal izquierda; el estudio ECG reveló hipertrofia auricular y ventricular izquierdas, por lo que se estableció el diagnóstico de miocardiopatía dilatada y enfermedad de Chagas en fase crónica, debido a la confirmación de Trypanosoma cruzi en el frotis y gota gruesa del año anterior, además de la serología positiva. Fue internado durante cinco días y dado de alta con tratamiento antiparasitario con nifurtimox, ácido acetilsalicílico y furosemida. La sintomatología disminuyó, con persistencia de la disnea a medianos esfuerzos, tos, hepatomegalia y bradicardia.
A partir de ese momento y hasta los 10 años, presentó cuadros bronquiales recurrentes, bradicardia y desnutrición significativa. A la exploración física se detectó soplo holosistólico grado II, arritmia y hepatomegalia. A los 13 años, durante el sueño, presentó hemiparesia izquierda con cefalea, mareo y vómito; se le diagnosticó EVC y fue referido al Instituto Nacional de Cardiología (INC).
En el INC, el ecocardiograma mostró insuficiencias mitral, tricuspídea y pulmonar leves; disfunción del ventrículo izquierdo con fracción de eyección (FEVI) del 34%, y bloqueo auriculoventricular Mobitz II, con episodios aislados de taquicardia auricular. Se programó colocación de marcapasos bicameral, que fue retrasada debido a taquicardia ventricular sostenida que evolucionó a fibrilación ventricular, requiriendo reanimación cardiopulmonar durante 20 minutos y ventilación mecánica durante seis días. Posteriormente, durante la colocación del marcapasos, presentó nuevamente fibrilación ventricular y asistolia, lo que requirió maniobras de resucitación cardiopulmonar. Finalmente, se completó la colocación del marcapasos.
La resonancia magnética de corazón mostró dilatación global de cavidades, disfunción sistólica biventricular, insuficiencia mitral moderada, insuficiencia tricuspídea severa y trombo en orejuela izquierda. La resonancia magnética de cráneo confirmó enfermedad vascular isquémica de la arteria cerebral media derecha, por lo que el paciente fue referido a rehabilitación física.
El paciente se recuperó de la hemiparesia y se estabilizó, por lo que a los dos meses de hospitalización fue dado de alta con los diagnósticos de cardiomiopatía restrictiva, insuficiencia mitral, tricuspídea y pulmonar leves, con fracción de eyección del 34% y bloqueo sinoauricular Mobitz I. Fue catalogado como Clase funcional II con insuficiencia cardíaca en tratamiento. A los tres meses, al presentarse a su primera cita de control, falleció al regresar a su comunidad.
DISCUSIÓN Y CONCLUSIONES
La enfermedad de Chagas continuó siendo una de las principales causas de miocarditis infecciosa en países endémicos, afectando tanto a adultos como a menores de edad. El caso presentado resaltó las consecuencias del diagnóstico y tratamiento tardíos. La infección fue confirmada un año después de la toma de la muestra, lo que ocasionó un retraso significativo en la intervención médica, por lo que la progresión del daño evolucionó hacia una cardiopatía severa.
Otro aspecto crítico en la evolución del paciente fue la falta de sospecha clínica inicial, lo que llevó a un manejo inadecuado y, en consecuencia, al deterioro progresivo de la función cardíaca, con fracción de eyección ventricular izquierda muy reducida (34%), así como la presencia de trombos intracavitarios que evidenciaron el compromiso cardíaco severo, manifestaciones frecuentes en esta cardiopatía en fases crónicas avanzadas. La miocardiopatía observada en este paciente mostró un patrón restrictivo, poco común en comparación con la forma dilatada típica de la enfermedad. Diversos estudios sugirieron que la cardiopatía restrictiva se relaciona con daño miocárdico severo, con alteraciones en la motilidad y disfunción diastólica36-38. El evento vascular cerebral (EVC) observado en este paciente, debido a tromboembolismo, se ha asociado frecuentemente con la fase crónica de la enfermedad, con una incidencia reportada del 60% para el tromboembolismo periférico y entre el 15 y el 70% para el intracavitario36,39,40.
Se destacaron otros factores que contribuyeron al deterioro de este caso y que dependieron de una historia clínica adecuada, del acceso al diagnóstico y tratamiento, así como de una referencia oportuna a atención médica especializada. La convivencia con el vector fue un factor de riesgo importante, por lo que una historia clínica detallada, una exploración dirigida y la toma de muestras tanto en la fase aguda como en la crónica resultaron esenciales para detectar la enfermedad de forma oportuna. La intervención tardía tuvo repercusiones adversas, ya que el tratamiento se inició cuando los niveles de anticuerpos ya se habían reducido y solo fueron detectados mediante western blot41.
La carencia de servicios especializados en la región de origen del paciente fue determinante en su deterioro. Además, el requerimiento de viajar a diferentes altitudes sobre el nivel del mar probablemente contribuyó a su fallecimiento posterior a la cita de control.
Resulta crucial implementar campañas educativas en zonas rurales con acceso limitado a servicios de salud, con el apoyo de la Secretaría de Salud, así como propiciar la colaboración entre especialistas en el manejo y seguimiento de estos pacientes para mejorar su pronóstico.
Finalmente, se destacó la necesidad de fortalecer la vigilancia epidemiológica y la capacidad diagnóstica en áreas endémicas, así como optimizar los procesos de referencia y contrarreferencia, además de garantizar el acceso efectivo al tratamiento.











 nueva página del texto (beta)
nueva página del texto (beta)