Introducción
La enfermedad de Chagas, causada por el protozoo Trypanosoma cruzi (T. cruzi), sigue siendo un importante problema de salud pública en América Latina. Se calcula que más de 6 millones de personas en la región están infectadas, siendo la transmisión vectorial la vía de infección más frecuente. En México, la enfermedad es endémica en varias regiones. Sin embargo, el conocimiento sobre las mujeres embarazadas con enfermedad de Chagas y la transmisión vertical sigue siendo limitado. La transmisión congénita está adquiriendo mayor relevancia, especialmente en países donde el control vectorial y el riesgo de transmisión por transfusiones se han reducido de manera significativa.
El diagnóstico de la enfermedad de Chagas congénita es complejo ya que la mayoría de los casos son asintomáticos. La detección temprana es fundamental, dado que los recién nacidos con infección por T. cruzi pueden ser tratados con éxito y curados si el diagnóstico se realiza oportunamente. Además, los recién nacidos y los niños pequeños presentan una baja incidencia de efectos adversos.1,2 La identificación precoz de la transmisión vertical es esencial para prevenir la progresión silenciosa de la enfermedad crónica, que a menudo se inicia en la infancia y puede conducir posteriormente a complicaciones graves, como insuficiencia cardiaca y muerte en la adolescencia o en la adultez temprana. Por ello, el cribado de la enfermedad de Chagas en mujeres embarazadas durante el control prenatal y en el momento del parto no solo ofrece una valiosa oportunidad para detectar infecciones congénitas, sino que también permite estudiar a otros familiares potencialmente expuestos e iniciar un tratamiento temprano.
En mujeres embarazadas, la enfermedad de Chagas se diagnostica habitualmente mediante pruebas serológicas, que detectan anticuerpos específicos contra T. cruzi. No obstante, las pruebas serológicas no son adecuadas para el diagnóstico de la infección en recién nacidos debido a la persistencia de anticuerpos maternos hasta por 6 meses después del parto. Por ello, se recomiendan métodos parasitológicos (detección de parásitos vivos en sangre) o técnicas moleculares, como la reacción en cadena de la polimerasa (PCR), para el diagnóstico de la infección neonatal. El diagnóstico de la enfermedad de Chagas congénita debe confirmarse mediante la persistencia de resultados positivos por PCR, pruebas parasitológicas o serológicas a los 8 meses de edad.2
Una de las principales barreras para la detección prenatal efectiva en México es la falta de un tamizaje sistemático, en parte debido a las disparidades regionales en el acceso a los servicios de salud, lo cual ha dado lugar a un subregistro significativo, a un seguimiento limitado y a una detección insuficiente de los recién nacidos expuestos.3 Además, los métodos diagnósticos actuales muestran una sensibilidad limitada.
Con el fin de comprender mejor la carga de las infecciones por T. cruzi durante el embarazo en México, realizamos una revisión de la literatura sobre la enfermedad de Chagas en mujeres embarazadas en distintos estados del país, publicada entre 2006 y 2024.3-10 Cuando estuvo disponible, también se incluyó información sobre los recién nacidos de madres seropositivas.
Además de la revisión de la literatura sobre la enfermedad de Chagas en mujeres embarazadas en México, se reportan datos clínicos, así como las complicaciones y comorbilidades descritas en 22 pacientes embarazadas infectadas por T. cruzi que recibieron atención prenatal en el Hospital General de México.11 En estos casos, el diagnóstico serológico se realizó mediante pruebas de inmunoensayo enzimático (ELISA), incluyendo tanto un kit ELISA comercial como un ELISA desarrollado in situ basado en un aislado mexicano de T. cruzi.11 Se discuten las posibles causas de las discrepancias observadas entre ambas pruebas diagnósticas ELISA.
Material y métodos
Se realizó una revisión de los estudios publicados sobre mujeres embarazadas con enfermedad de Chagas en México entre 2006 y 2024. También se analizaron datos de 22 (de 150) mujeres embarazadas procedentes de zonas endémicas de Chagas en México, diagnosticadas de infección por T. cruzi y que recibieron atención prenatal en el Hospital General de México.11 Las zonas endémicas se seleccionaron con base en información del sistema nacional de vigilancia (Sistema Nacional de Vigilancia Epidemiológica). Todas las participantes completaron un cuestionario sobre comorbilidades y complicaciones de embarazos previos. El protocolo del estudio fue aprobado por el Comité de Ética de la Universidad Nacional Autónoma de México (UNAM) (proyecto número 139-2017) y por el Comité de Ética del «Hospital General de México» (aprobación n.º HGM-DG-114-DI-2019). Los datos del cuestionario fueron analizados en el presente estudio.
El diagnóstico de la infección por T. cruzi en las 22 mujeres embarazadas se realizó mediante pruebas serológicas, incluyendo un ELISA desarrollado in situ basado en un aislado mexicano de T. cruzi y una prueba ELISA recombinante comercial Accutrack Chagas Micro ELISA (Laboratorio Lemos, Buenos Aires, Argentina), basada en antígenos recombinantes de parásitos sudamericanos de T. cruzi. El ELISA in situ utilizó antígenos derivados de una cepa mexicana de T. cruzi (TBAR/MX/0000/Querétaro). Tal como se describió en un estudio previo,11 los parásitos de T. cruzi (fase epimastigote) se lisaron mediante sonicación y se centrifugaron a 30.600 × g durante 1 h a 4 °C. El contenido proteico se analizó en los sobrenadantes, y los ensayos ELISA se realizaron utilizando 0,6 μg de antígeno por pozo, siguiendo los protocolos estándar.11 Los valores de densidad óptica (DO) se calcularon restando el valor de corte a la DO media obtenida de 3 muestras séricas replicadas. Las muestras se clasificaron como positivas cuando los valores de DO superaron el valor de corte en, como mínimo, un 10%, negativas cuando estuvieron al menos un 10% por debajo del valor de corte, e indeterminadas cuando se encontraron dentro del 10% del valor de corte. El valor de corte se estableció según la siguiente fórmula: 3 veces la desviación estándar de la muestra más la DO media del control negativo.
Resultados
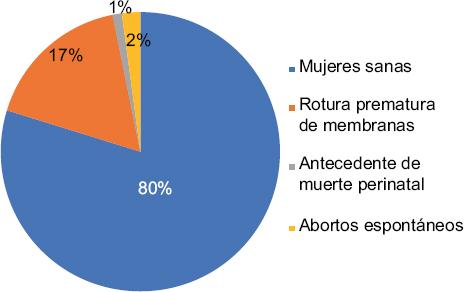
La revisión de la literatura sobre la enfermedad de Chagas durante el embarazo en México incluyó un total de 4.616 mujeres embarazadas, de las cuales 188 (4.1%) dieron positivo para infección por T. cruzi. Aunque el 80% de estas mujeres reportó embarazos sin complicaciones, el 17% presentó ruptura prematura de membranas (RPM), el 2% refirió abortos espontáneos y el 1%, muertes perinatales (Fig. 1). En cuanto a los resultados neonatales, se dispuso de datos de 2,298 recién nacidos, 30 de los cuales (1.3%) dieron positivo para enfermedad de Chagas. En los neonatos nacidos de madres seropositivas de distintos estados, se utilizaron > 2 pruebas diagnósticas para confirmar la enfermedad de Chagas (Chagas Stat-Pak, ELISA recombinante Wiener, PCR en sangre de cordón umbilical, microhematocrito y ELISA no comercial).
La evaluación clínica de estos neonatos reveló que el 87% estaba sano, el 7% presentó puntuaciones APGAR limítrofes, el 3% desarrolló síndrome de dificultad respiratoria y el 3% falleció por parada cardiaca (Fig. 2).
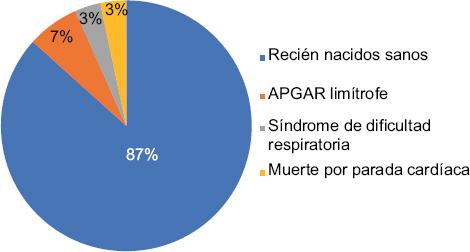
Figura 2 Revisión de las complicaciones médicas en recién nacidos de madres con enfermedad de Chagas.
La revisión de la enfermedad de Chagas en mujeres embarazadas en México reveló variaciones en la prevalencia entre distintos estados y diferencias en los métodos diagnósticos utilizados para detectar la infección por T. cruzi. Un estudio realizado en Yucatán reportó una seroprevalencia de entre el 0.8 y el 1.2% en mujeres embarazadas, mientras que en el estado de Guanajuato la prevalencia fue de l0.41%, dependiendo del método diagnóstico empleado. En estos estudios no se confirmaron casos de infección congénita en mujeres embarazadas seropositivas durante el seguimiento de los recién nacidos. Otro estudio realizado en Guanajuato (León) mostró una seroprevalencia del 4% en madres embarazadas y del 0.8% en recién nacidos. En otro estudio llevado a cabo en 2 comunidades mayas de Yucatán, se evaluaron 390 mujeres, 9 de las cuales dieron positivo para enfermedad de Chagas y 4 reportaron antecedentes de aborto espontáneo. Asimismo, en esta comunidad se estudiaron 685 pacientes pediátricos, 3 de los cuales dieron positivo para enfermedad de Chagas, sin reportarse alteraciones de salud en estos casos.
Se observaron tasas más elevadas de infección por T. cruzi en mujeres embarazadas en los estados de Chiapas, Oaxaca y Jalisco. En particular, un estudio realizado en Chiapas reportó una seroprevalencia materna del 2.04% entre 1 125 mujeres embarazadas. En la ciudad de Tapachula, Chiapas, se documentó una tasa de transmisión congénita del 22.2%, mientras que en Palenque la incidencia fue del 7.14%. Este estudio también informó que el 31.8% de las pacientes positivas para Chagas presentó ruptura prematura de membranas y el 9.1% tenía antecedentes de muerte perinatal.
En los estados de Oaxaca y Jalisco, la seroprevalencia reportada de mujeres embarazadas positivas para Chagas alcanzó el 4.4 y 12.02%, respectivamente. En estos estudios se detectaron varios casos confirmados de transmisión congénita mediante PCR y pruebas serológicas. En dichos estados, las pruebas confirmatorias de seguimiento en los neonatos se realizaron a los 2 años en el 20% de los pacientes de Oaxaca y en el 11,9% de los de Jalisco. El análisis de las comorbilidades asociadas mostró que 14 de 67 pacientes positivas para Chagas en Jalisco y 9 de 35 en Oaxaca presentaron RPM. Otro estudio realizado en Veracruz y Chiapas reportó una seroprevalencia del 4.1% en mujeres embarazadas, aunque no se confirmaron infecciones congénitas en los recién nacidos. Estos hallazgos sugieren una variabilidad geográfica significativa en la prevalencia de la enfermedad de Chagas en mujeres embarazadas en México. Además, la falta de tamizaje sistemático durante el embarazo y el seguimiento posnatal inadecuado para la posible transmisión congénita pueden contribuir al subregistro de casos.
Junto con los hallazgos de la revisión de la literatura sobre embarazo y enfermedad de Chagas en México, se presentan datos recopilados en el área de maternidad del Hospital General de México. El estudio mostró que 22 de 150 mujeres embarazadas (14.6%) dieron positivo (11.3%) o indeterminado (3.3%) para enfermedad de Chagas en pruebas serológicas basadas en antígenos derivados de una cepa mexicana de T. cruzi. Se debe mencionar que 16 de las 22 pacientes seropositivas o indeterminadas reportaron antecedentes de complicaciones y comorbilidades, siendo la más frecuente el aborto espontáneo, presente en 8 pacientes (50%) (Tabla 1, Fig. 3A). La segunda comorbilidad más frecuente fue la diabetes gestacional (37%) (Fig. 3B). Se debe mencionar que 3 de las 6 pacientes con enfermedad de Chagas y diabetes gestacional habían experimentado al menos 1 aborto, y una de ellas reportó 2 abortos previos (Tabla 1).
Tabla 1 Comorbilidades y comparativas de cada una de las pacientes embarazadas con enfermedad de Chagas atendidas en el Hospital General de México
| ID | Diabetes gestacional | Abortos espontáneos | RPM | SUA | Antecedente de muerte perinatal | Hipertensión gestacional | Preeclampsia | Oligohidramnios | Quiste ovárico | Obesidad |
|---|---|---|---|---|---|---|---|---|---|---|
| FRLM | X | |||||||||
| AVFA | X | |||||||||
| RHH | X | |||||||||
| CGEA | X | |||||||||
| FVY | X | X | X | |||||||
| ARE | X | X | ||||||||
| OLHA | X | |||||||||
| GMM | X | |||||||||
| BMBV | X | X | ||||||||
| OBMA | X | X | ||||||||
| VZFV | X | X | X | |||||||
| ORVV | X | X | X | X | ||||||
| CRLN | X | X | ||||||||
| GNV | X | X | ||||||||
| TNE | X | |||||||||
| CGAR | X | X | X |
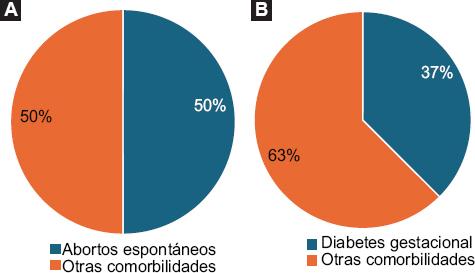
Figura 3 Comorbilidades y complicaciones más frecuentes en pacientes embarazadas con Chagas del Hospital General de México. A: porcentaje de abortos espontáneos frente a otras comorbilidades. B: porcentaje de diabetes gestacional frente a otras comorbilidades.
Otras comorbilidades fueron el sangrado uterino anormal, la obesidad, la RPM, los antecedentes de muerte perinatal, la hipertensión gestacional, la preeclampsia, el oligohidramnios y el quiste ovárico (Tabla 1).
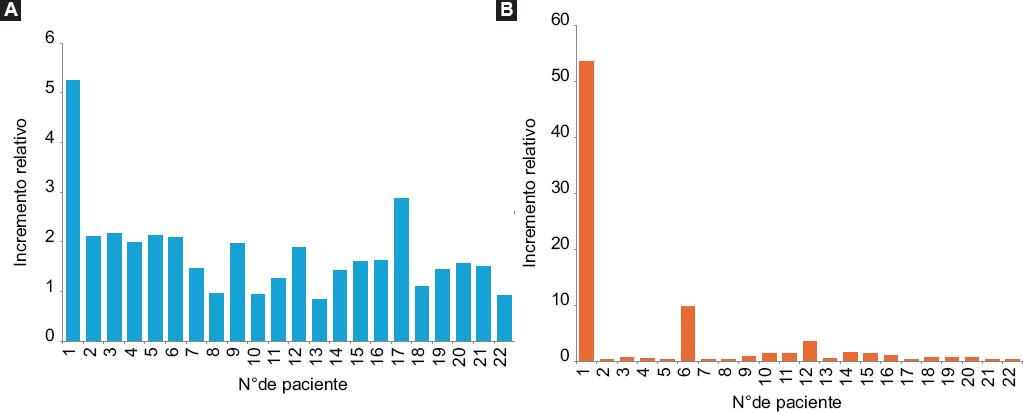
Se observó una discrepancia notable al comparar la prueba comercial Accutrack Chagas Recombinant Micro ELISA con el ELISA desarrollado in situ, basado en antígenos de una cepa local de T. cruzi. De las 22 pacientes que dieron positivo o indeterminado con el ELISA in situ (Fig. 4A), solo 2 también dieron positivo a la prueba Accutrack Recombinant ELISA (Fig. 4B). En ambos ensayos se realizó normalización de los datos, y los resultados se expresaron como incrementos relativos (Tabla 2). Para el ELISA in situ, los valores ≤ 1.1 se consideraron indeterminados y los valores ≥ 1.2, positivos. Para la prueba Accutrack Recombinant ELISA, el umbral de positividad se fijó en 4,0. El incremento relativo de los valores ELISA obtenidos con ambas pruebas para cada paciente se presenta individualizadamente en la Tabla 2 y la Fig. 4. Se debe mencionar que 1 de las 2 pacientes que dieron positivo en ambas pruebas era una mujer embarazada originaria de Colombia, posiblemente infectada con una cepa distinta de T. cruzi. La única paciente mexicana que dio positivo en ambas pruebas serológicas presentaba títulos muy altos de anticuerpos (Tabla 2, Fig. 4).
Tabla 2 Incremento relativo (entre paréntesis) por encima del umbral tras la normalización a uno, utilizando el ensayo ELISA con antígeno propio (in-house) o el ELISA recombinante comercial Accutrack. Se muestran el No y el ID de cada paciente
| Paciente positivo para Trypanosoma cruzi | ELISA con antígeno propio (in-house) | ELISA recombinante Accutrack |
|---|---|---|
| 1 (FRLM) | Pos (5.24) | Pos (53.6) |
| 2 (AVFA) | Pos (2.10) | Neg (0.30) |
| 3 (RHH) | Pos (2.16) | Neg (0.55) |
| 4 (LBKC) | Pos (1.99) | Neg (0.42) |
| 5 (CGEA) | Pos (2.13) | Neg (0.25) |
| 6 (FVY) | Pos (2.09) | Pos (9.66) |
| 7 (ARE) | Pos (1.47) | Neg (0.30) |
| 8 (CPDR) | Ind (0.97) | Neg (0.25) |
| 9 (OLHA) | Pos (1.96) | Neg (0.83) |
| 10 (GMM) | Ind (0.95) | Neg (1.25) |
| 11 (BMBV) | Pos (1.27) | Neg (1.33) |
| 12 (OBMA) | Pos (1.88) | Neg (3.50) |
| 13 (VZFV) | Ind (0.84) | Neg (0.50) |
| 14 (GSKM) | Pos (1.42) | Neg (1.58) |
| 15 (ORVV) | Pos (1.61) | Neg (1.33) |
| 16 (GML) | Pos (1.63) | Neg (1.06) |
| 17 (CRLN) | Pos (2.87) | Neg (0.25) |
| 18 (CCFJ) | Ind (1.10) | Neg (0.66) |
| 19 (GNV) | Pos (1.45) | Neg (0.66) |
| 20 (TNE) | Pos (1.57) | Neg (0.66) |
| 21 (CTCG) | Pos (1.51) | Neg (0.25) |
| 22 (CGAR) | Ind (0.92) | Neg (0.25) |
ELISA: ensayo inmunoenzimático; Ind: indeterminado; Neg: negativo; Pos: positivo.
Discusión
Los estudios longitudinales sobre la enfermedad de Chagas en mujeres embarazadas siguen siendo escasos en México, y el tamizaje rutinario de la enfermedad no está incluido en las pruebas prenatales estándar en la mayor parte del país. Actualmente, la detección comienza de manera incipiente en regiones de alto riesgo.
En el presente estudio se revisaron los datos publicados sobre la enfermedad de Chagas en mujeres embarazadas en México, poniéndose el énfasis en la transmisión congénita y complicaciones maternas y neonatales asociadas. En total, 4,616 mujeres embarazadas fueron incluidas en los estudios revisados, 188 de las cuales (4.1%) dieron positivo para Trypanosoma cruzi, principalmente en los estados de Chiapas, Oaxaca y Jalisco. Se evaluaron 2,298 recién nacidos, 30 de los cuales dieron positivo para transmisión congénita (1.3%).
La revisión reveló que existe una relación estrecha entre la enfermedad de Chagas materna y la RPM, una complicación que no se reconoce tradicionalmente como desenlace de la infección por T. cruzi durante el embarazo. Aunque la mayoría de los neonatos con Chagas congénito fueron asintomáticos al nacimiento, el 3% presentó signos clínicos como síndrome de dificultad respiratoria y parada cardiaca y el 7%, puntuaciones APGAR bajas. Aunque estas complicaciones se han descrito en el Chagas congénito, la relación causal directa con la infección por T. cruzi no ha podido demostrarse.
Se debe mencionar que el 50% del grupo de mujeres embarazadas con enfermedad de Chagas atendidas en el Hospital General de México tenía antecedentes de abortos previos, lo cual coincide con lo descrito en la literatura. Aunque los mecanismos no terminan de entenderse, se ha propuesto la participación de placentitis e invasión del trofoblasto conducentes a afectación placentaria.12-14
También se observó una alta incidencia de la diabetes gestacional en pacientes embarazadas con Chagas (37%). La diabetes gestacional se define como cualquier grado de intolerancia a la glucosa reconocido por primera vez durante el embarazo. Esta comorbilidad resulta preocupante debido a los riesgos maternos y fetales asociados.
Aunque no se ha establecido una relación clara entre la enfermedad de Chagas y la diabetes, estudios experimentales en modelos murinos han demostrado que la infección por T. cruzi puede inducir inflamación pancreática, alteración de la arquitectura de los islotes y parasitismo de las células β pancreáticas, lo cual podría conducir a disfunción metabólica. Se han descrito alteraciones similares en ratones infectados y en humanos.15-17 La diabetes gestacional también aumenta el riesgo de desarrollar diabetes mellitus tipo 2 (DMT2) en etapas posteriores de la vida.18 Aún no está claro si la diabetes gestacional es un precursor de la DMT2 en mujeres predispuestas, en quienes los desafíos metabólicos alterados propios del embarazo podrían conducir a riesgos adicionales para su desarrollo. Además de los cambios metabólicos asociados al embarazo, las pacientes con enfermedad de Chagas crónica también pueden presentar alteraciones metabólicas similares.15,19 Otra posible causa de los cambios metabólicos inducidos por la infección de la placenta por Trypanosoma cruzi es la reducción de la expresión del transportador de glucosa (GLUT1), el principal transportador de glucosa localizado en el sincitiotrofoblasto, lo cual provoca una alteración del eje glucosa-insulina-GLUT1 materno y fetal, lo cual podría modificar los niveles plasmáticos de insulina.20,21 En este sentido, la combinación de diabetes gestacional y enfermedad de Chagas podría incrementar aún más el riesgo de avance a DMT2. Aunque la enfermedad de Chagas no se ha reconocida oficialmente como un factor de riesgo para la diabetes, la posibilidad de un vínculo causal justifica una mayor investigación, lo cual resulta especialmente relevante en México, donde la DMT2 representa un importante problema de salud pública. En consecuencia, el cribado oportuno de DMT2 en mujeres embarazadas con enfermedad de Chagas y diabetes gestacional podría prevenir complicaciones futuras.
No obstante, el diagnóstico de la enfermedad de Chagas en zonas rurales continúa siendo un desafío, por lo que son esenciales métodos de cribado simplificados. Un abordaje prometedor es el uso de gotas de sangre seca para el cribado neonatal. Este método, implementado por la Secretaría de Salud de México, resulta particularmente valioso en áreas rurales o remotas con acceso limitado a laboratorios clínicos. El protocolo emplea pruebas serológicas basadas en ELISA sobre sangre obtenida mediante punción digital y depositada en papel filtro. Las muestras se secan al aire, se almacenan en bolsas selladas a 4 °C y posteriormente se eluyen en placas de microtitulación con tampón para la realización de pruebas ELISA convencionales.
Esta estrategia se está implementando a través de la Red Nacional de Laboratorios Estatales de Salud Pública como parte de la Estrategia Nacional para la Interrupción de la Transmisión de la Enfermedad de Chagas, en conjunto con el programa nacional de control vectorial. La iniciativa se centra en áreas de alta endemicidad, lo cual permite un diagnóstico temprano. Estudios pioneros en Nicaragua han demostrado la viabilidad y fiabilidad de este abordaje.22 La implementación sistemática del cribado prenatal no solo facilita el tratamiento temprano de madres y recién nacidos, sino que también contribuye a prevenir la transmisión continua, incluso en regiones con un control vectorial exitoso.
Uno de los problemas persistentes que dificultan los estudios sobre la enfermedad de Chagas es la falta de herramientas diagnósticas con alta sensibilidad y especificidad. El estudio realizado en el "Hospital General de México" puso de manifiesto discrepancias importantes entre los ensayos ELISA basados en diferentes antígenos de T. cruzi. El ELISA desarrollado in situ utilizó antígenos derivados de una cepa mexicana de T. cruzi perteneciente al linaje I predominante en México. En cambio, el ELISA comercial Accutrack emplea antígenos del linaje II, prevalente en Sudamérica. Las variaciones antigénicas específicas de linaje, las diferencias en virulencia y los distintos comportamientos epidemiológicos de los parásitos de diferentes linajes probablemente contribuyan a las variaciones en el rendimiento diagnóstico de las distintas pruebas.23
Nuestro estudio mostró claramente diferencias relevantes al comparar ambos ensayos ELISA. El ELISA in situ, basado en antígenos de T. cruzi aislado en México (linaje I), evidenció que las 22 pacientes presentaban respuestas de anticuerpos por encima de los valores de corte. En cambio, cuando las mismas pacientes fueron analizadas mediante el ELISA recombinante Accutrack (linaje II), solo 2 dieron positivo: una procedente de Colombia y otra paciente mexicana con títulos elevados de anticuerpos.
No sorprende que la paciente colombiana tuviera una positividad elevada (incremento relativo de 53,6 veces) en el ELISA Accutrack, que utiliza antígenos de cepas sudamericanas del linaje II. La segunda paciente positiva con el kit Accutrack fue una paciente mexicana con niveles altos de anticuerpos (incremento relativo de 9,66 veces). Como esta fue la única paciente mexicana que dio positivo con el kit Accutrack con títulos altos de anticuerpos, podría especularse con que este ensayo comercial presenta una baja sensibilidad para la detección de infecciones por T. cruzidel linaje I.
Estos resultados ponen de manifiesto la urgente necesidad de contar con herramientas diagnósticas mejoradas, adaptadas a los linajes de T. cruzi presentes en México. El desarrollo de pruebas serológicas que empleen antígenos específicos de linaje permitirá mejorar la precisión diagnóstica y la vigilancia epidemiológica, sobre todo, en mujeres embarazadas con riesgo de transmisión congénita. El uso de pruebas inadecuadas podría dar lugar a resultados falsamente negativos, privando a los recién nacidos infectados de un tratamiento oportuno y perpetuando la transmisión no detectada de la enfermedad.
Conclusiones
La enfermedad de Chagas durante el embarazo y la subsiguiente transmisión congénita de infecciones por T. cruzi son una vía de transmisión silenciosa pero significativa, que contribuye a la persistencia sostenida de la enfermedad de Chagas en México. Aunque diversos estudios han documentado su ocurrencia, la magnitud real del problema sigue siendo incierta, lo cual resalta la necesidad de realizar un cribaje sistemático y un seguimiento posnatal integral. Para un diagnóstico serológico preciso, resulta esencial incorporar antígenos derivados de los linajes de T. cruzi circulantes en México.
Además, las mujeres embarazadas diagnosticadas de enfermedad de Chagas deben someterse a cribados de diabetes gestacional y a seguimiento ante un posible avance de la DMT2. El avance en las herramientas diagnósticas y la garantía de su disponibilidad en regiones endémicas son pasos críticos tanto para el control de la transmisión congénita como para mejorar los desenlaces de salud materna y neonatal.











 nueva página del texto (beta)
nueva página del texto (beta)