Introducción
El síndrome de fragilidad es una condición clínica geriátrica caracterizada por una disminución progresiva de la reserva fisiológica, lo que conlleva un incremento significativo en la vulnerabilidad frente a factores estresores físicos, psicológicos o sociales. Este estado se ha asociado consistentemente con un mayor riesgo de caídas, discapacidad, hospitalización, institucionalización y mortalidad en personas adultas mayores.1
En 2001, Fried et al.1 propusieron un modelo fenotípico operativo de fragilidad basado en cinco criterios: pérdida de peso involuntaria, debilidad muscular, lentitud en la marcha, fatiga y bajo nivel de actividad física. La presencia de tres o más de ellos define clínicamente la fragilidad.1 Este enfoque ha sido ampliamente validado y continúa siendo uno de los más utilizados en contextos clínicos y de investigación.
De manera paralela, Rockwood et al.2 desarrollaron el Índice de Fragilidad (Frailty Index), un modelo acumulativo que evalúa múltiples déficits clínicos, funcionales y sociales, permitiendo una valoración más integral y adaptable a distintos escenarios clínicos.
Ambos modelos han sido aplicados en estudios poblacionales, intervenciones comunitarias y programas de atención geriátrica integral.3 No obstante, el abordaje tradicional del síndrome ha sido históricamente neutro al sexo, sin considerar las diferencias biológicas y sociales entre hombres y mujeres.
Las evidencias recientes sugieren que las mujeres tienen mayor prevalencia de fragilidad, pero los hombres presentan desenlaces clínicos más graves, incluyendo una mortalidad más alta.4-6 Este fenómeno ha sido denominado «paradoja sexo-fragilidad» y evidencia la necesidad de incorporar la perspectiva de género en la evaluación y el manejo del síndrome.
Asimismo, se han descrito mecanismos fisiopatológicos divergentes según el sexo. En las mujeres predominan los factores hormonales, emocionales y metabólicos, mientras que en los hombres destacan la sarcopenia, la inmunosenescencia y la vulnerabilidad neuromuscular.6-11 Factores como la calidad del sueño, el envejecimiento epigenético, la composición corporal y la inflamación crónica también muestran trayectorias distintas por sexo.12-15
Objetivo
Este artículo tiene como objetivo analizar la evidencia científica más actual sobre el síndrome de fragilidad en adultos mayores, con énfasis en las diferencias entre hombres y mujeres en términos de prevalencia, fisiopatología, manifestaciones clínicas y respuesta a las intervenciones terapéuticas. La finalidad es proponer un abordaje diferenciado y basado en la evidencia que permita optimizar la atención geriátrica.
Método
Se llevó a cabo una revisión narrativa de la literatura científica disponible entre marzo y abril de 2025, centrada en el síndrome de fragilidad y sus diferencias por sexo. La búsqueda bibliográfica se realizó en las bases de datos PubMed/MEDLINE, Cochrane Library, SciELO y ScienceDirect, utilizando descriptores MeSH ("frailty", "frailty phenotype", "sex differences", "gender disparities", "older adults", "sarcopenia", "sleep", "nutrition", "epigenetic clocks", "frailty index", "inflammaging") y operadores booleanos.
Los criterios de inclusión fueron:
- Artículos originales, revisiones sistemáticas o metaanálisis.
- Población ≥ 60 años.
- Análisis de diferencias por sexo.
- Uso de criterios operativos de fragilidad (Fried, Rockwood u otros validados).
- Publicaciones en inglés o español entre 2001 y 2025, con texto completo disponible.
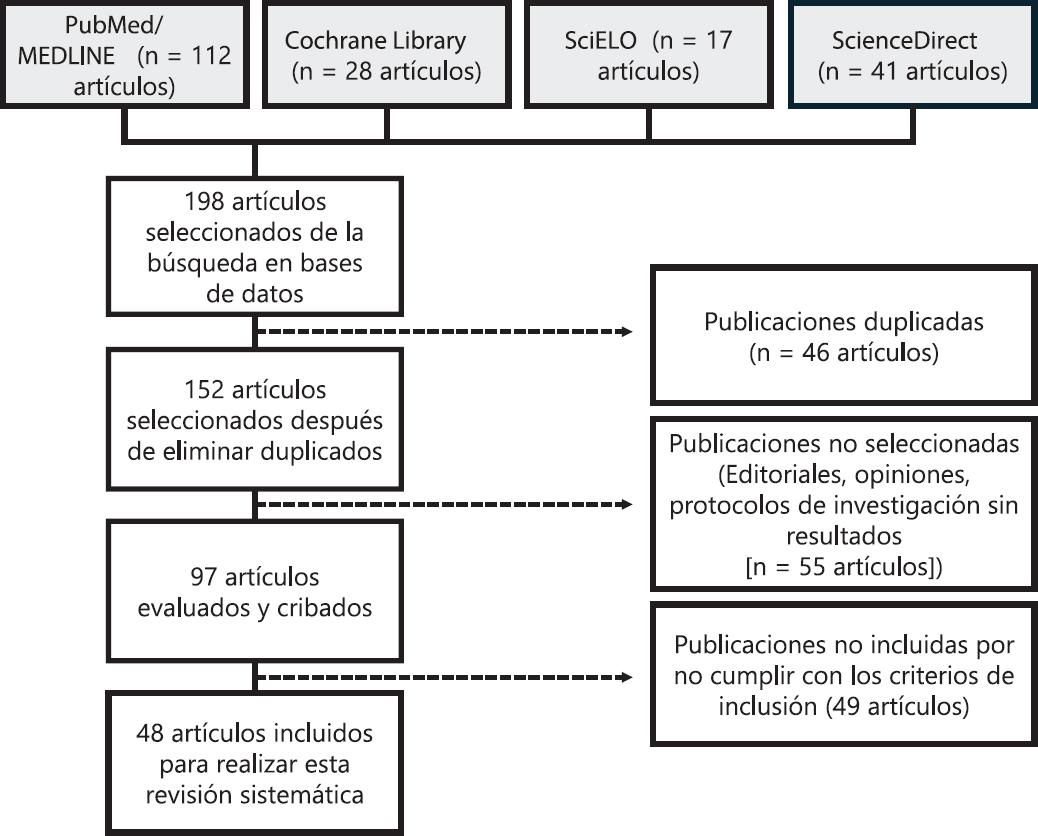
Se excluyeron los artículos duplicados, los editoriales, las opiniones, los protocolos sin resultados y los estudios centrados exclusivamente en el cuidado y la atención del adulto mayor. Tras su cribado y lectura crítica se incluyeron 48 artículos, de los cuales el 75% fueron publicados entre 2019 y 2025 (Fig. 1).
Experiencia del grupo
Esta revisión se fundamenta en la experiencia acumulada del grupo de trabajo en el ámbito clínico, docente e investigativo del envejecimiento funcional, con especial énfasis en la evaluación y el manejo del síndrome de fragilidad. A lo largo de varios años se ha trabajado con poblaciones geriátricas en contextos tanto hospitalarios como comunitarios, integrando un enfoque sensible al sexo en la práctica clínica. Las observaciones incluidas reflejan los hallazgos propios y las concordancias con la evidencia internacional sobre las diferencias por sexo en la manifestación y la evolución del síndrome.
Prevalencia
La prevalencia del síndrome de fragilidad en las personas mayores de 65 años oscila entre el 10% y el 27% en todo el mundo, dependiendo de la localización geográfica, del método diagnóstico utilizado y de las características de la población estudiada.16 El estudio original de Fried et al.1 reportó una prevalencia del 6.9% en adultos mayores estadounidenses, con mayor frecuencia en las mujeres, las personas afrodescendientes y la población con bajo nivel socioeconómico.
En Asia, la prevalencia puede alcanzar valores significativamente mayores; por ejemplo, en Corea del Sur se ha reportado una tasa del 23.1% en personas mayores.17 En contraste, datos del estudio longitudinal inglés (ELSA) mostraron que, aunque las mujeres desarrollaban más criterios de fragilidad con el tiempo, los hombres presentaban unas tasas de mortalidad más altas6. El estudio CHARLS, en China, evidenció una brecha de género creciente en la prevalencia de fragilidad entre 2011 y 2018.5
En México, los estudios basados en la Encuesta Nacional sobre Salud y Envejecimiento (ENASEM) indican que las mujeres presentan una prevalencia de fragilidad mayor que los hombres, incluso después de ajustar por factores socioeconómicos y funcionales.16 Además, se ha observado una asociación significativa entre el acortamiento de los telómeros y la fragilidad: las mujeres frágiles presentaron una probabilidad 3.1 veces mayor de tener telómeros cortos, mientras que para los hombres esta probabilidad fue de 4.6 veces.8
Factores como el estado civil, el nivel educativo y el entorno residencial también contribuyen a las diferencias de género en la fragilidad. Los estudios longitudinales confirman que las mujeres tienden a acumular más componentes del fenotipo de fragilidad, mientras que los hombres presentan mayor mortalidad asociada a este síndrome.8,16
Relevancia clínica
El síndrome de fragilidad constituye un predictor independiente de múltiples desenlaces adversos en los adultos mayores, incluyendo caídas, fracturas, deterioro funcional, hospitalización, institucionalización y mortalidad.1,2,18 También se ha asociado con mayor riesgo de reacciones adversas a medicamentos, complicaciones posquirúrgicas y pobre respuesta a tratamientos convencionales.2
Desde una perspectiva de salud pública, la detección temprana de la fragilidad permite la implementación de estrategias costo-efectivas, como programas de ejercicio multicomponente, intervenciones nutricionales y rehabilitación funcional19. Los estudios han demostrado que estos modelos integrales de atención pueden reducir las hospitalizaciones y preservar la autonomía funcional.20
Aunque la prevalencia es mayor en las mujeres, diversos estudios indican que los hombres frágiles presentan peores desenlaces clínicos. Por ejemplo, en una cohorte asiática, la tasa de mortalidad fue del 48.6% en los hombres frágiles, en comparación con el 22.0% en las mujeres.5 En un estudio realizado en Italia se documentó una asociación más fuerte entre fragilidad y hospitalización por infecciones en los hombres (hazard ratio [HR]: 2.32), frente a las mujeres (HR: 1.55).6
Este patrón clínico sugiere que las mujeres tienden a vivir más años con fragilidad leve o moderada, mientras que los hombres con fragilidad suelen experimentar un deterioro funcional más rápido y grave.6 Tales diferencias subrayan la necesidad de diseñar estrategias terapéuticas adaptadas a las características biológicas y funcionales específicas de cada sexo.
Factores biológicos y hormonales
La fragilidad es el resultado de alteraciones multisistémicas que involucran a los sistemas endocrino, neuromuscular, inmunitario y metabólico. Estas alteraciones presentan perfiles diferentes en los hombres y las mujeres.
Hormonas sexuales
En las mujeres, la disminución de estrógenos con la menopausia favorece un estado proinflamatorio basal y un deterioro del metabolismo óseo, aumentando el riesgo de fragilidad.8 Se ha reportado que unos valores elevados de interleucina (IL) 6 y de proteína C reactiva se asocian con lentitud y debilidad muscular en las mujeres posmenopáusicas.9
En los hombres, el descenso progresivo de la testosterona relacionado con la edad se vincula con pérdida de masa muscular, sarcopenia, disminución de la densidad ósea y síntomas depresivos, todos ellos factores asociados a la fragilidad.15 Aunque algunos estudios han explorado el uso de la testosterona como marcador o indicador de intervención terapéutica, su aplicación clínica continúa siendo objeto de debate.10,15
Composición corporal
Los hombres frágiles suelen presentar bajo peso corporal, menor índice de masa muscular y caquexia, lo que incrementa el riesgo de mortalidad funcional.11 En contraste, las mujeres frágiles frecuentemente exhiben obesidad abdominal, resistencia a la insulina y disfunción metabólica, incluso en ausencia de una pérdida ponderal significativa.6,12
Inflamación y biomarcadores
Los estudios han identificado perfiles inflamatorios específicos en las mujeres frágiles, caracterizados por la presencia de oxilipinas como TxB2 y 7-HDoHE. Estos compuestos se relacionan con estrés oxidativo, disfunción mitocondrial y activación plaquetaria, y podrían utilizarse como biomarcadores de estratificación del riesgo y como guía para intervenciones nutricionales o farmacológicas.13,21
Inmunosenescencia
La inmunosenescencia, el deterioro progresivo de la función inmunitaria con la edad, ocurre en ambos sexos, pero parece más pronunciada en los hombres. Estos muestran menor resiliencia frente a las infecciones y el estrés fisiológico, lo que podría explicar su mayor vulnerabilidad clínica.14,22 En contraste, la multiparidad podría conferir a las mujeres ciertos beneficios inmunitarios a largo plazo, aunque esto sigue bajo estudio.6,15
Factores genéticos
Los factores genéticos y epigenéticos desempeñan un papel determinante en la susceptibilidad al síndrome de fragilidad y en su evolución, con diferencias entre hombres y mujeres.
Uno de los biomarcadores más estudiados es el acortamiento de los telómeros, considerado un indicador de envejecimiento biológico. En un estudio realizado en población mexicana, las personas mayores frágiles presentaron telómeros significativamente más cortos, con una odds ratio de 3.1 en las mujeres y de 4.6 en los hombres, lo que sugiere una mayor vulnerabilidad biológica masculina frente al proceso de fragilidad.8
Además, se han identificado polimorfismos en genes proinflamatorios, como el de la IL-10, que aumentan la susceptibilidad a desarrollar fragilidad. Estos polimorfismos parecen tener un efecto más pronunciado en las mujeres, lo que podría estar relacionado con una respuesta inmunitaria diferencial de tipo genético.9
Los estudios que han utilizado relojes epigenéticos han revelado que, aunque las mujeres tienden a acumular más componentes del fenotipo de fragilidad, los hombres presentan una aceleración más marcada del envejecimiento biológico. Esta aceleración se asocia con mayor incidencia de enfermedades metabólicas, inflamación crónica y menor supervivencia.9
Factores psicosociales
Los determinantes psicosociales son fundamentales en la expresión y la progresión de la fragilidad, y muestran marcadas diferencias por sexo. Las mujeres mayores tienden a mantener redes sociales más activas, lo que actúa como factor protector frente al aislamiento. No obstante, presentan mayor prevalencia de síntomas depresivos, los cuales se asocian con fatiga, lentitud y peor percepción del estado de salud.4,23 En contraste, los hombres suelen experimentar un mayor grado de soledad tras eventos críticos como la viudez o el retiro laboral, lo que repercute negativamente en su funcionalidad y autoestima.4
Un análisis de las redes sociales en adultos mayores mexicanos evidenció que la fragilidad femenina se asocia con soledad, dependencia funcional y mala calidad del sueño, mientras que en los hombres se relaciona con caídas frecuentes y presencia de ideación suicida.24 Estos hallazgos enfatizan la necesidad de integrar la evaluación emocional y relacional en la atención geriátrica, adaptándola al contexto psicosocial de cada sexo.
Estado nutricional
La nutrición es un componente esencial en la génesis y la evolución de la fragilidad. Tanto la malnutrición como la sobrealimentación pueden influir negativamente en la reserva funcional del adulto mayor.25
En mujeres institucionalizadas se ha observado que la pérdida dentaria, la ausencia de prótesis funcionales y la malnutrición están fuertemente asociadas con mayor riesgo de fragilidad.26 Además, algunos perfiles metabólicos específicos, como unos niveles elevados de oxilipinas proinflamatorias, reflejan un estado de estrés oxidativo crónico y activación plaquetaria que contribuyen al deterioro funcional femenino.13
Por otro lado, los hombres frágiles tienden a presentar pérdida de masa magra, bajo índice de masa corporal y deficiente ingesta proteica, lo que exacerba la sarcopenia y acelera el deterioro físico.21
Estos hallazgos refuerzan la necesidad de incorporar estrategias nutricionales diferenciadas por sexo, considerando no solo el aporte calórico y proteico, sino también el estado inflamatorio y metabólico de base.
Calidad del sueño
Las alteraciones del sueño han sido reconocidas como un factor de riesgo importante para la fragilidad,27 mostrando patrones distintos según el sexo. En las mujeres, tanto el sueño corto (≤ 6 horas) como el sueño prolongado (≥ 9 horas) se han asociado con mayor prevalencia de fragilidad. Estas alteraciones afectan negativamente la fuerza muscular, la velocidad de marcha y el equilibrio, facilitando la progresión del síndrome.17,27 En estudios realizados en población mexicana, el insomnio, la baja calidad del sueño y el sueño fragmentado se identificaron como predictores significativos de fragilidad en las mujeres.17,27 En los hombres, aunque la asociación no siempre es estadísticamente significativa, el sueño prolongado se ha vinculado con debilidad muscular y baja actividad física.17
Dado que el sueño influye en la inflamación sistémica, el estado de ánimo y la recuperación funcional, su evaluación debe integrarse en la valoración geriátrica, especialmente en las mujeres mayores que viven solas.
Intervenciones terapéuticas y preventivas
El abordaje del síndrome de fragilidad debe ser proactivo, multidimensional y adaptado a las características biológicas, funcionales y psicosociales de cada persona.20,28,29 Las intervenciones deben considerar las diferencias por sexo para maximizar su eficacia.
Ejercicio físico
La intervención más respaldada es el ejercicio multicomponente, que incluye entrenamiento de fuerza, resistencia, equilibrio y movilidad.30-32 Se ha demostrado que mejora la velocidad de la marcha, la fuerza muscular y la calidad de vida en las personas mayores.32
En las mujeres, estos programas son especialmente útiles para contrarrestar la obesidad abdominal y el deterioro funcional asociado a la menopausia.31 En los hombres, la efectividad del ejercicio es más notoria en la mejora de la sarcopenia y la recuperación funcional, con beneficios adicionales sobre la integridad cerebral, según estudios de neuroimagen.11,33
Nutrición y suplementación
La suplementación con proteínas, vitamina D, calcio y ácidos grasos omega-3 ha demostrado eficacia en la preservación de la masa muscular y ósea.20,26 Las mujeres posmenopáusicas con perfiles inflamatorios elevados pueden beneficiarse especialmente del consumo de antioxidantes y ácidos grasos poliinsaturados. En los hombres, la intervención nutricional debe priorizar la prevención de la sarcopenia grave y la optimización del estado anabólico.26
Soporte psicosocial
El fortalecimiento de las redes sociales mediante intervenciones comunitarias y terapias grupales ha mostrado ser eficaz en la reducción del aislamiento y del deterioro emocional en las mujeres.11 En los hombres, es crucial implementar estrategias de soporte durante eventos críticos, como la viudez, para mitigar el riesgo de declive funcional y emocional.4
Calidad del sueño
Las terapias conductuales enfocadas en la higiene del sueño han demostrado mayor eficacia en las mujeres, especialmente en aquellas con insomnio o sueño fragmentado.17 La inclusión de la evaluación y el tratamiento del sueño en programas integrales de prevención debe ser una prioridad, dado su impacto en la función física, la inflamación y la salud mental.
Intervenciones farmacológicas
Aunque aún está bajo investigación, los tratamientos hormonales, como la terapia de reemplazo con testosterona en los hombres con hipogonadismo y con estrógenos en las mujeres posmenopáusicas, han mostrado resultados preliminares prometedores en cuanto a fuerza muscular y composición corporal. No obstante, su uso clínico requiere más estudios longitudinales y análisis de riesgo-beneficio individualizados.15,33
Discusión
El síndrome de fragilidad ha evolucionado desde una descripción funcional a una condición clínica con implicaciones predictivas y terapéuticas claras. Existen múltiples modelos conceptuales para evaluar la fragilidad, destacando el fenotipo de Fried y el índice de acumulación de déficits. Ambos han demostrado su utilidad, aunque capturan dimensiones distintas de la vulnerabilidad geriátrica.1,34-36
Uno de los hallazgos más consistentes es la paradoja sexo-fragilidad: las mujeres presentan mayor prevalencia y viven más años con fragilidad, y en cambio los hombres tienen menor prevalencia, pero mayor riesgo de hospitalización, deterioro funcional grave y discapacidad asociada.4,5,28 Esta paradoja refleja no solo diferencias biológicas, sino también sociales, conductuales y culturales.
Desde un enfoque fisiopatológico, en las mujeres predominan los mecanismos inflamatorios crónicos, la obesidad abdominal, la polifarmacia y los trastornos del ánimo; en los hombres, destacan la sarcopenia, la inmunosenescencia y el deterioro neuromuscular acelerado.14,21,22 Las diferencias hormonales y epigenéticas también influyen en cómo se manifiesta y progresa el síndrome. Mientras que las mujeres acumulan más componentes del fenotipo, los hombres muestran un envejecimiento biológico más acelerado, medido por telómeros cortos y relojes epigenéticos.8,9
Estas diferencias no son solo académicas, sino que tienen consecuencias directas en la práctica clínica. Por ejemplo, los hombres se benefician más de intervenciones centradas en la fuerza muscular y la movilidad funcional, mientras que las mujeres requieren abordajes más integrales que incluyan el abordaje de la depresión, soporte social, nutrición y sueño.10-12
El presente análisis también confirma que las estrategias universales de detección y tratamiento pueden ser ineficaces si no se consideran las diferencias por sexo. Las guías clínicas recientes recomiendan integrar la variable sexo/género en la evaluación geriátrica integral, y adaptar el manejo según las trayectorias clínicas predominantes en cada grupo.4,20
Desde la perspectiva de salud pública, la atención diferenciada permite priorizar recursos, diseñar programas más efectivos y reducir desigualdades. Este enfoque también es clave para mejorar la calidad de vida, la autonomía funcional y la satisfacción con el cuidado en las personas mayores.
Si bien la mayoría de los estudios coinciden en la existencia de diferencias por sexo, aún falta incorporar sistemáticamente esta variable en los ensayos clínicos, los registros poblacionales y los sistemas de salud. Se requieren más estudios longitudinales que evalúen la interacción de sexo biológico, género sociocultural y fragilidad a lo largo del tiempo.
En suma, el reconocimiento de las diferencias sexuales en la fragilidad, además de enriquecer la comprensión clínica del fenómeno, mejora la efectividad de las intervenciones y contribuye a una atención geriátrica más justa y precisa.
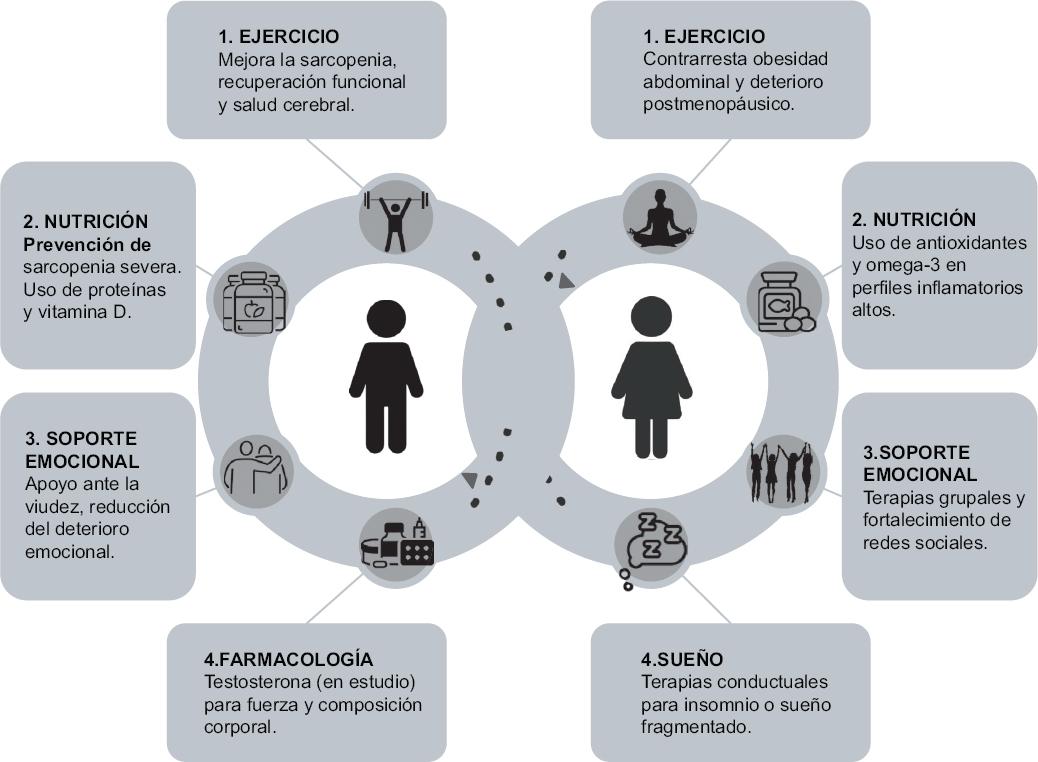
Considerando la evidencia disponible sobre las diferencias de género, es fundamental adaptar las estrategias preventivas y terapéuticas a las particularidades de cada sexo (Fig. 2).
En los hombres mayores se recomienda:
- Fomentar activamente el uso regular de servicios de salud preventiva, considerando su menor adherencia espontánea a los controles médicos.
- Incrementar las estrategias preventivas centradas en la salud cardiovascular desde edades más tempranas (mediana edad).
- Proporcionar educación nutricional temprana enfocada en la prevención de la inflamación sistémica crónica y de la sarcopenia.
- Desarrollar y fortalecer redes de soporte social, especialmente durante transiciones críticas, como la viudez.
En las mujeres mayores se recomienda:
- Realizar un manejo temprano y riguroso del sobrepeso y la obesidad abdominal tras la menopausia.
- Aumentar la vigilancia y el manejo oportuno de las secuelas derivadas de complicaciones obstétricas y ginecológicas previas.
- Implementar programas estructurados de actividad física dirigidos específicamente a prevenir y tratar la sarcopenia.
- Proporcionar soporte social activo y específico para mujeres mayores que viven solas, mitigando el aislamiento social y psicológico (Fig. 2).
Conclusión
El conocimiento actual sobre fragilidad en adultos mayores destaca la importancia crucial de incorporar la dimensión del sexo en la evaluación clínica y en la implementación de estrategias de salud pública. El síndrome de fragilidad es una condición multifactorial con diferencias de género significativas en su prevalencia, manifestaciones y desenlaces clínicos; mientras que las mujeres presentan mayor fragilidad, los hombres experimentan peores resultados en términos de mortalidad.
Es necesario fortalecer la evidencia sobre tratamientos diferenciales específicos. Los datos actuales son suficientes para recomendar explícitamente estrategias adaptadas según el sexo en la prevención y el manejo de este síndrome. Estas diferencias enfatizan la importancia de un enfoque personalizado en su diagnóstico y manejo. Reconocer las diferencias entre hombres y mujeres permitirá realizar una detección temprana, junto con estrategias preventivas y terapéuticas, lo cual es clave para reducir el impacto y mejorar la calidad de vida en la población de edad avanzada, así como guiar decisiones clínicas más acertadas y personalizadas, optimizando la calidad asistencial y la eficiencia de las intervenciones dirigidas a la población mayor.











 nueva página del texto (beta)
nueva página del texto (beta)