Introducción
El dengue es una enfermedad viral transmitida por mosquitos, causada por cuatro serotipos distintos del virus del dengue: DENV-1, DENV-2, DENV-3 y DENV-4. Cada uno de estos serotipos puede causar la enfermedad, y la infección por un serotipo no confiere inmunidad contra los otros, lo que significa que una persona puede infectarse hasta cuatro veces en su vida, cada vez con un serotipo diferente. La infección por el virus del dengue puede manifestarse como una enfermedad febril leve o evolucionar hacia formas más graves, como el dengue hemorrágico y el shock, que pueden ser fatales.1
La situación global actual del dengue en América Latina, y específicamente en México, refleja una carga significativa de morbilidad y mortalidad. En todo el mundo, el dengue es la enfermedad viral transmitida por mosquitos más prevalente, con aproximadamente 390 millones de infecciones anuales.2,3 En América Latina, la incidencia de dengue ha aumentado, con un cambio notable en la epidemiología, pues ahora afecta más a los niños, como se ha observado, por ejemplo, en Brasil y Colombia.3
En México, al igual que en otros países de la región, el dengue sigue siendo endémico y los esfuerzos de control se ven desafiados por factores como la resistencia a los insecticidas y la expansión urbana.3 En México, todos los serotipos del virus del dengue están presentes y cocirculan, lo que complica el control de la enfermedad y aumenta el riesgo de dengue grave, en especial en individuos que han sido infectados previamente por un serotipo diferente.4,5 Además, se ha observado un resurgimiento del serotipo DENV-3, que no había circulado en la región durante una década, y se ha asociado con un aumento en la gravedad de los casos. Por otro lado, el serotipo DENV-2 también ha sido identificado como un factor de riesgo significativo para el desarrollo de dengue grave.6
La diversidad genética y la evolución de los serotipos del virus del dengue en México han sido objeto de estudio, revelando la presencia de diferentes genotipos y la emergencia de nuevas líneas genéticas, lo que puede influir en la epidemiología de la enfermedad y en la respuesta inmunitaria de la población.7 Durante el brote de 2012-2013, los serotipos DENV-1 y DENV-2 fueron predominantes, con la identificación de genotipos específicos que contribuyeron a la diseminación del virus en regiones costeras y destinos turísticos.8
En cuanto a la mortalidad, aunque el dengue grave es menos frecuente, sigue siendo una preocupación significativa debido a su potencial para causar brotes epidémicos y sobrecargar los sistemas de salud.3,9 La coinfección con SARS-CoV-2 ha complicado aún más la situación, aumentando las tasas de hospitalización.3
En los últimos 5 años, la mortalidad por dengue en América Latina ha mostrado grandes variaciones, influenciada por factores como la urbanización, el cambio climático y la pandemia de COVID-19. En Brasil, por ejemplo, se ha observado un aumento de los casos sospechosos y de las muertes por dengue, con un incremento del 20% en los casos reportados en las primeras semanas de 2024 en comparación con todo el año 2023.10 Este aumento puede estar relacionado con la interrupción de las medidas de control vectorial durante la pandemia de COVID-19, lo que permitió un resurgimiento de la transmisión del dengue.11
En Ecuador, aunque la tasa de mortalidad hospitalaria por dengue no mostró cambios significativos entre 2015 y 2022, se observó un aumento en las hospitalizaciones por dengue en los últimos años, lo que sugiere un incremento en la carga de la enfermedad.4 En Colombia, la mortalidad por dengue ha variado, con tasas que oscilan entre el 0.07% y el 0.16% en diferentes años, reflejando la naturaleza endémica y la circulación de los cuatro serotipos del virus.12
En México, la mortalidad por dengue ha mostrado una correlación significativa con los casos de fiebre del dengue y de dengue hemorrágico, siendo las regiones costeras del sureste, el suroeste y el oeste las más afectadas.13 La urbanización y el cambio climático han facilitado la expansión del vector, complicando los esfuerzos de control y aumentando la incidencia de casos graves y mortales.14
La respuesta inmunitaria frente al dengue es compleja y multifactorial, involucrando tanto la respuesta humoral como la celular. Las vacunas contra el dengue buscan inducir una respuesta inmunitaria equilibrada que neutralice el virus y prevenga la enfermedad grave. Los estudios han demostrado que las vacunas pueden inducir una sólida respuesta de células T CD8+ específicas para el dengue, lo cual es fundamental para eliminar las células infectadas.15 Sin embargo, la generación de anticuerpos neutralizantes es igualmente importante, aunque puede conllevar el riesgo de enfermedad del dengue grave en individuos previamente infectados debido al fenómeno de potenciación dependiente de anticuerpos. Este fenómeno, bien documentado en la literatura científica, plantea un desafío en el diseño de vacunas contra el dengue.16
La implementación de programas de vacunación, combinados con campañas de vacunación de recuperación, ha mostrado potencial para reducir significativamente la carga del dengue en países endémicos.17 Sin embargo, la eficacia a largo plazo y el impacto poblacional de la vacuna dependen de factores como la seroprevalencia y la intensidad de transmisión en cada región.17,18
Las implicaciones de las vacunas contra el dengue para la salud pública son significativas. Una vez disponibles vacunas seguras y eficaces, se podría reducir drásticamente la carga de la enfermedad en los países endémicos. Los estudios han demostrado la eficacia de la vacuna TAK-003 en la prevención de casos graves de dengue.19 En los últimos años, se han desarrollado diversas vacunas tetravalentes contra el dengue, diseñadas para conferir protección contra los cuatro serotipos del virus, como Dengvaxia® (CYD-TDV), la cual representa un avance importante en la prevención de la enfermedad. Esta vacuna ha demostrado eficacia en la prevención del dengue virológicamente confirmado y del dengue grave en ensayos clínicos en América Latina y Asia.18,20 No obstante, su uso está recomendado principalmente en individuos que ya han estado expuestos al dengue, debido a que en las personas seronegativas puede aumentar el riesgo de dengue grave. La Organización Mundial de la Salud (OMS) recomienda su uso en poblaciones en las que al menos el 70% de los destinatarios previstos son seropositivos para el dengue.21
Estos avances han generado un gran interés en la comunidad científica y en la salud pública, ya que ofrecen la posibilidad de prevenir de manera eficaz esta enfermedad. Sin embargo, la eficacia y la seguridad de estas vacunas aún son objeto de investigación. Es crucial considerar factores como la cobertura vacunal, la vigilancia epidemiológica y la integración de las vacunas en los programas de inmunización existentes. Además, la eliminación del dengue requerirá un enfoque multidisciplinario que combine la vacunación con medidas de control del vector y educación de la población.
La prevención de casos graves de dengue es una prioridad de salud pública. La vacunación podría desempeñar un papel fundamental en la reducción de la carga de la enfermedad, en especial en regiones altamente endémicas. No obstante, es imprescindible contar con evidencia científica sólida sobre la eficacia y la seguridad de estas vacunas antes de su implementación a gran escala. Los estudios han mostrado resultados prometedores en cuanto a inmunogenicidad y seguridad de las vacunas tetravalentes, pero se requieren más investigaciones para evaluar su eficacia en la prevención de la enfermedad clínica.19,22
El presente estudio tiene como objetivo evaluar la eficacia de las vacunas tetravalentes contra el dengue en la prevención de casos graves de la enfermedad a través de una revisión sistemática de ensayos clínicos aleatorizados controlados con placebo. Específicamente, se busca responder a la siguiente pregunta de investigación: ¿cuál es la eficacia de la vacuna tetravalente contra el dengue en la prevención de casos graves de dengue en comparación con placebo, en diferentes poblaciones y contextos geográficos?
Método
Se llevó a cabo una revisión sistemática siguiendo las directrices PRISMA 2020 en las bases de datos PubMed, Scopus y Web of Science para identificar estudios relevantes. Con la adaptación de descriptores (DeCS y MeSH) se utilizaron las siguientes palabras clave: (Tetravalent vaccine OR dengue vaccine) AND (Dengue prevention OR dengue severity) AND (Clinical trial OR randomized controlled trial). La búsqueda se limitó a estudios publicados en inglés desde enero de 2019 hasta noviembre de 2024, para garantizar la inclusión de los hallazgos más recientes.
Criterios de inclusión
Se incluyeron ensayos clínicos aleatorizados controlados con placebo que evaluaran la eficacia de vacunas tetravalentes contra el dengue en poblaciones adultas residentes en áreas endémicas. Los estudios debían reportar como resultado primario la incidencia de dengue grave, definido según los criterios de la OMS.
Criterios de exclusión
Se excluyeron estudios con diseños metodológicos diferentes, aquellos que no reportaron la incidencia de dengue grave como resultado principal y los realizados en poblaciones no endémicas o pediátricas.
Pregunta de investigación
Siguiendo el sistema PICO, en el contexto de este estudio, la P (población) se refiere a individuos en riesgo de sufrir dengue que residen en áreas endémicas, la I (intervención) corresponde a la administración de la vacuna contra el dengue, la C (comparación) considera los resultados de aquellos que recibieron la vacuna frente a un grupo que recibió un placebo, y la O (resultado [outcome]) se enfoca en la prevención de casos graves de dengue, es decir, se evalúa la eficacia de la vacuna para reducir la incidencia de la enfermedad. La pregunta de investigación fue la siguiente: «¿cómo son la inmunogenicidad y la seguridad de la vacuna tetravalente contra el dengue en la prevención de casos graves de dengue en comparación con placebo, en diferentes poblaciones y contextos geográficos?»
Extracción de datos
Dos revisores independientes realizaron la selección de estudios de manera independiente, utilizando los criterios de inclusión y exclusión establecidos. Se resolvieron las discrepancias mediante consenso o consultando a un tercer revisor.
Se diseñó un formulario de extracción de datos para recopilar información relevante de cada estudio, incluyendo características de los participantes (edad, sexo y seroprevalencia previa), diseño del estudio, intervención (tipo de vacuna, dosis y esquema de vacunación), resultados (eficacia y seguridad) y metodología (aleatorización, cegamiento y análisis estadístico).
Resultados
En la búsqueda en PubMed, Scopus y Web of Science se identificaron 277 artículos relacionados con la eficacia de las vacunas tetravalentes contra el dengue. Tras aplicar los criterios de inclusión y exclusión, se seleccionaron nueve ensayos clínicos aleatorizados para su revisión completa. Finalmente, se eligieron seis estudios que cumplían con los criterios establecidos, excluyendo tres debido a la presencia de población pediátrica (Figura 1).
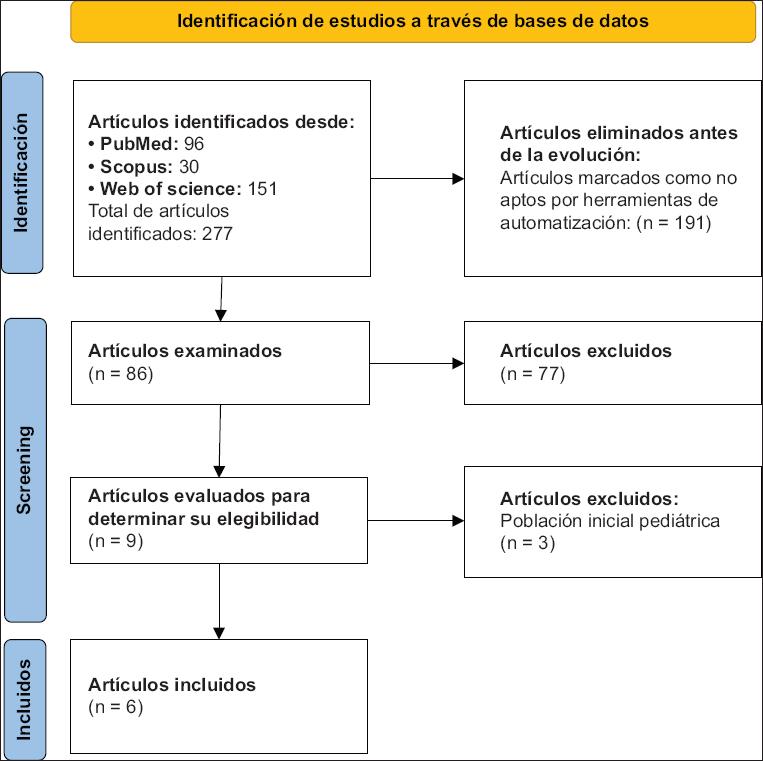
Figura 1 Diagrama PRISMA que muestra la identificación inicial mediante la matriz de búsqueda y posteriormente la eliminación por métodos de automatización, año y tipo de artículo. En el cribado se seleccionaron y se eliminaron artículos por la lectura de los títulos y resúmenes; de los seleccionados se excluyeron tres por no cumplir con los criterios de la investigación, y finalmente se seleccionaron seis artículos para ser incluidos en la revisión.
Así, esta revisión incluyó seis ensayos clínicos aleatorizados, sumando un total de 24,249 participantes, en los cuales se evaluaron resultados clínicos como la incidencia de dengue grave, la seropositividad y la respuesta inmunitaria a las vacunas TV003 y TV005 (Tabla 1).
Tabla 1 Estudios incluidos en la revisión
| N.º | Título, autores y nivel de evidencia | Población | Intervención | Resultados |
|---|---|---|---|---|
| 1 | Título: Safety and immunogenicity of a synthetic nanoparticle-base T cell priming peptide vaccine against dengue in healthy adults in Switzerland: a double-blind, randomized, vehicle-controlled, phase 1 study Autores: Miauton et al. Nivel de evidencia: 1b |
Población de 26 pacientes aleatorizados para recibir PepGNP-Dengue dosis baja (n = 10), vehículo-GNP* dosis baja (n = 3), PepGNP-Dengue dosis alta (n = 10) o vehículo-GNP* dosis alta (n = 3) *GNP sin péptidos (vehículo-GNP) |
Recibir dos dosis subcutáneas de PepGNP-Dengue (0.05 ml) o vehículo-GNP (0-5 ml) según grupo de dosis baja o alta, con un intervalo de 21 días Dos participantes no recibieron la segunda vacunación: uno debido a que retiró el consentimiento (grupo de dosis baja de PepGNP-Dengue) y otro por un eritema de grado 3 en el lugar de la inyección (grupo de dosis alta de vehículo-GNP) |
Resultado primario: en general, el 60% y el 10% de los participantes en los grupos PepGNP-Dengue de dosis baja y alta, respectivamente, presentaron al menos un marcador positivo de células T CD8 + (CD107a + CD25 + o CD137 + CD69 + ) en cualquier momento. PepGNP-Dengue indujo un aumento estadísticamente significativo de CD137 + CD69 + CD8 + activado por PepGNP-Dengue el día 90 en comparación con el valor inicial en el grupo de dosis baja ( + 0.0318%, intervalo de confianza del 95%: 0.0088-0.1723, prueba de Friedman p = 0.046). En términos de respondedores a la vacuna, PepGNP-Dengue dosis baja indujo un mayor número de respondedores que PepGNP-Dengue dosis alta el día 21 para CD137 + CD69 + CD8 + (5/10 [50%] vs. 0/10 [0%], prueba de Fisher p = 0.033) Resultado secundario: los participantes vacunados con PepGNP-Dengue (dosis baja y alta) presentaron un aumento de T CD8 + específicas para dengue, D-dext + CD8 + en el día 35 (n = 16, + 4.64/105 CD8 + , intervalo de confianza del 95%: 0.09-35.12, prueba de Friedman p = 0.024), específicamente subconjuntos Tcm y TemRA ( + 1.34/105 CD8 + , intervalo de confianza del 95%: 0.1-7.34, p = 0.024 y + 0,8/105 CD8 + , intervalo de confianza 95%: 0.19-5.13, p = 0.014, respectivamente). La funcionalidad de las células T CD8 + D-dextr + se evaluó mediante el expresión de CXCR3, con un aumento significativo en CXCR3 + CD8 + Tcm específico para dengue en el grupo PepGNP-Dengue en el día 35 ( + 1.335/105 CD8 + [0.1-7.34], prueba de Friedman p = 0.0106) |
| 2 | Título: Safety and immunogenicity of different formulations of a tetravalent dengue purified inactivated vaccine in healthy adults from Puerto Rico: final results after 3 years of follow-up from a randomized, placebo-controlled phase I study Autores: Diaz et al. Nivel de evidencia: 1b |
Población de 79 pacientes aleatorizados para recibir placebo (n = 16), 1 μg + aluminio (n = 16), 1 μg + AS01E (n = 15), 1 μg + AS03B (n = 16) o 4 μg + aluminio (n = 16) | Recibir dos dosis subcutáneas de una vacuna inactivada purificada tetravalente contra el dengue en investigación, formulada con diferentes sistemas adyuvantes (1 μg/serotipo/dosis adyuvada con aluminio, 1 μg/serotipo/dosis adyuvada con AS01E, 1 μg/serotipo/dosis adyuvada con AS03B con y 4 μg/serotipo/dosis adyuvada con aluminio) o placebo, con un intervalo de 1 mes | Resultado primario: la vacunación con vacuna de virus inactivados purificada tetravalente contra el dengue resultó segura e inmunógena por más de 3 años después de la vacunación en un adulto en comparación con el placebo Resultado secundario: los porcentajes de respondedores tetravalentes en 36-38 meses tras la dosis fueron del 78.6% (intervalo de confianza del 95%: 49.2-95.3) en el grupo de 1 μg + aluminio, del 92.9% (intervalo de confianza del 95%: 66.1-99.8) en el grupo de 4 μg + aluminio, del 92.3% (intervalo de confianza del 95%: 64.0-99.8) en el grupo de 1 μg + AS01E, del 100% (intervalo de confianza del 95%: 73.5-100) en el grupo de 1 μg + AS03B y del 93.8% (intervalo de confianza del 95%: 69.8-99.8) en el grupo que recibió placebo |
| 3 | Título: Safety and immunogenicity of a single dose of a tetravalent dengue vaccine with two different serotype-2 potencies in adults in Singapore: a phase 2, double-blind, randomised, controlled trial Autores: Tricou et al. Nivel de evidencia: 1b |
Población total de 351 pacientes aleatorizados para recibir alta dosis de vacuna tetravalente contra el dengue HD-TDV (n = 176) o vacuna tetravalente contra el dengue TDV (n = 175) | Recibir una dosis de 0.5 ml de HD-TDV o TDV | Resultado primario: tanto en el grupo de HD-TDV como en el de TDV se observó un aumento de la media geométrica de los títulos de anticuerpos (GMT) en el día 15, con la GMT más alta medida en el día 30. Los títulos de anticuerpos se mantuvieron por encima de los valores basales durante todo el ensayo para ambas vacunas. En la población general del ensayo no se observaron diferencias sustanciales en las GMT entre los dos grupos de vacunas, excepto frente al DENV-2, para el que la respuesta fue mayor en el grupo HD-TDV que en el grupo TDV (8640 frente a 1993 en el día 30) Resultado secundario: los resultados de este ensayo sugieren una respuesta inmunitaria más equilibrada con la nueva formulación TDV en comparación con la formulación temprana HD-TDV, y apoyan la elección de la nueva formulación para la evaluación de eficacia de fase 3 |
| 4 | Título: Safety and durable immunogenicity of the TV005 tetravalent dengue vaccine, across serotypes and age groups, in dengue-endemic Bangladesh: a randomised, controlled trial Autores: Walsh et al. Nivel de evidencia: 1b |
Población total de 192 pacientes aleatorizados para recibir vacunación (n = 144) o placebo (n = 48) | Recibir una dosis de 0.5 ml de vacuna contra el dengue TV005 | Resultado primario: tras una única dosis de TV005, la mayoría (87%) de los participantes con contacto previo con dengue mostraron respuestas sólidas frente a los cuatro serotipos, lo que sugiere que para esta población (al igual que en nuestros otros estudios), TV005 provoca respuestas de anticuerpos homotípicos frente a los serotipos restantes que nunca han infectado al individuo, aumenta los anticuerpos frente a todos los serotipos observados previamente y promueve una protección duradera frente a todos los serotipos Resultado secundario: tras la vacunación con TV005, los voluntarios de todas las edades (n = 142) fueron seropositivos para la mayoría de los serotipos, con 118 (83%) seropositivos para DENV-1, 141 (99%) para DENV-2, 137 (96%) para DENV-3 y 124 (87%) para DENV-4; en general, al día 180 |
| 5 | Título: Long-term efficacy and safety of a tetravalent dengue vaccine (TAK-003): 4·5-year results from a phase 3, randomised, double-blind, placebo-controlled trial Autores: Tricou et al. Nivel de evidencia: 1b |
Población total de 23,401 participantes seleccionados, de los cuales 20,099 fueron asignados aleatoriamente para recibir vacuna tetravalente contra el dengue TAK-003 (n = 13,401) o placebo (n = 6698) | Administrar dos dosis subcutáneas de TAK-003 (0-5 ml) o placebo (0-5 ml) con un intervalo de 3 meses | Resultado primario: de los 20,071 participantes que recibieron la primera vacunación, 18,257 (91.0%) completaron la parte 3 del ensayo. Durante aproximadamente 57 meses después de la primera dosis se notificaron 9698 (en el grupo de placebo) y 17,978 (en el grupo TAK-003) enfermedades febriles. Se detectó dengue confirmado serológicamente en 560 (5-8%) de las 9698 enfermedades febriles notificadas en el grupo placebo y en 447 (2.5%) de las 17,978 enfermedades febriles notificadas en el grupo TAK-003, de las cuales 142 (25%) de 560 y 46 (10%) de 447 requirieron hospitalización. Se detectaron proporcionalmente menos casos de dengue confirmado por serología durante los últimos 18 meses (placebo: 57 de 560; TAK-003: 55 de 447), con tasas de hospitalización similares a las observadas en el conjunto del estudio Resultado secundario: TAK-003 demostró eficacia y seguridad a largo plazo contra los cuatro serotipos en individuos previamente expuestos, y contra DENV-1 y DENV-2 en individuos sin dengue |
| 6 | Título: A phase 1, double-blind, randomized, placebo-controlled study to evaluate the safety and immunogenicity of a tetravalent live attenuated dengue vaccine in adults Autores: Russell et al. Nivel de evidencia: 1b |
Poblacion total de 200 adultos sanos, hombres y mujeres, entre 18 y 50 años de edad, expuestos (n = 160) o no (n = 40) al flavivirus Se inscribieron de 5 lugares de estudio diferentes (tres en los Estados Unidos y dos en Puerto Rico) | Ensayo clínico de fase I, aleatorizado, doble ciego y controlado con placebo, en el que los participantes fueron asignados aleatoriamente en una proporción 2:2:1 a recibir dos dosis de 0.5 ml de una de las dos formulaciones activas de la vacuna (TV003 o TV005) o un placebo. La primera dosis se administró en el día 1 y la segunda a los 6 meses | Resultado primario: el estudio evaluó la inmunogenicidad de las formulaciones de TV003 y TV005 contra el dengue utilizando la prueba de neutralización por reducción de virus al 60% (VRNT60). Se observó una alta seropositividad en los participantes, en especialmente en aquellos sin antecedentes de infección por dengue, de los cuales el 92.6% mostraron seropositividad tras la primera dosis de TV003. En el grupo de TV003 se registraron aumentos significativos en la media geométrica de los títulos de anticuerpos (GMT) de VRNT60 para todos los serotipos de dengue, con GMT de 64.5 para DENV-1, 100 para DENV-2, 45.3 para DENV-3 y 30.2 para DENV-4 a los 28 días de la vacunación. Aunque se observaron incrementos mínimos en las GMT tras la segunda dosis, los niveles se mantuvieron por encima de los valores iniciales durante 1 año, con GMT de 58.7 para DENV-2 a los 180 días. Además, se documentó un 25% de viremia detectable en los participantes tras la vacunación, lo que sugiere que la replicación del virus vacunal es un indicador de la eficacia de la inmunización Resultado secundario: los hallazgos del estudio respaldan el uso de las formulaciones TV003 y TV005 como opciones efectivas para la prevención del dengue, destacando la capacidad de TV003 para inducir una respuesta inmunitaria más robusta en individuos sin exposición previa al virus. En el grupo de TV003, el 100% de los participantes alcanzaron seropositividad para DENV-2 tras la primera dosis, en comparación con el 64% observado en estudios previos con la formulación TV005. La durabilidad de la respuesta inmunitaria se evidenció por los niveles sostenidos de GMT, que mostraron una disminución mínima del 10% en los títulos de VRNT60 desde el día 28 hasta el día 180. Tales resultados sugieren que estas vacunas podrían ser fundamentales en estrategias de salud pública para combatir el dengue, señalando la necesidad de estudios adicionales que evalúen la seguridad y la eficacia en poblaciones más amplias y diversas, incluyendo diferentes grupos etarios y demográficos |
El análisis de los datos reveló que la formulación TV003 mostró una alta seropositividad, alcanzando el 100% en el grupo sin antecedentes de infección por dengue tras la primera dosis, en comparación con el 64% observado en estudios previos con TV005 (Tabla 2).
Tabla 2 Hallazgos principales de cada estudio analizado
| Año | Autores | Vacuna | Seropositividad | Respuesta inmunitaria | Limitaciones |
|---|---|---|---|---|---|
| 2024 | Miauton et al. | PepGNP-Dengue | 60% (dosis baja), 10% (dosis alta) | Aumento células T CD8 + | Tamaño de muestra pequeño |
| 2020 | Diaz et al. | Inactivada tetravalente | > 90% | Anticuerpos neutralizantes | - |
| 2019 | Tricou et al. | TAK-003 | - | - | - |
| 2024 | Walsh et al. | TV005 | 83-99% (según serotipo) | - | - |
| 2023 | Tricou et al. | TAK-003 | - | - | - |
| 2022 | Russell et al. | Viva atenuada tetravalente (TV003/TV005) | 92.6% (TV003) | Aumento de la media geométrica de los títulos de anticuerpos | - |
En términos de inmunogenicidad, se registraron aumentos significativos en la media geométrica de los títulos de anticuerpos (GMT) en la prueba de neutralización por reducción de virus al 60% (VRNT60) para todos los serotipos de dengue, destacando una GMT de 64.5 para DENV-1, de 100 para DENV-2, de 45.3 para DENV-3 y de 30.2 para DENV-4 a los 28 días de la vacunación.
En cuanto a la durabilidad de la respuesta inmunitaria, se observó que los niveles de GMT se mantuvieron por encima de los valores iniciales durante 1 año, con GMT de 58.7 para DENV-2 a los 180 días. Además, se documentó un 25% de viremia detectable en los participantes tras la vacunación, sugiriendo que la replicación del virus vacunal podría ser un indicador de la eficacia de la inmunización.
Los estudios también evaluaron la incidencia de dengue grave, encontrando que las vacunas tetravalentes, especialmente TV003, podrían ser fundamentales en estrategias de salud pública para combatir el dengue. Sin embargo, se destaca la necesidad de realizar estudios adicionales que evalúen la seguridad y la eficacia en poblaciones más amplias y diversas, incluyendo diferentes grupos etarios y demográficos.
A pesar de los hallazgos positivos asociados con el uso de las vacunas tetravalentes, se deben considerar varias limitaciones. La calidad metodológica de los estudios incluidos fue generalmente alta, pero la variabilidad en los diseños de los estudios y en las características de los participantes puede haber influido en los resultados. Además, la falta de datos sobre efectos a largo plazo y las distintas formulaciones de las vacunas en los estudios limitan la generalización de los hallazgos.
Discusión
Las formulaciones de las vacunas tetravalentes contra el dengue analizadas en el estudio incluyen diversos compuestos diseñados para inducir una respuesta inmunitaria robusta contra los cuatro serotipos del virus del dengue. Por ejemplo, la formulación TV003 se basa en una vacuna específicamente diseñada que incluye partículas similares a virus que imitan la estructura del virus del dengue, proporcionando una respuesta inmunitaria sin la necesidad de una infección activa. Esta formulación se caracteriza por su alta seropositividad, evidenciada por un 100% de respuesta inmunitaria en participantes sin antecedentes de infección. Por otro lado, la vacuna TV005, aunque también es tetravalente, logró una seropositividad algo inferior, alcanzando el 64% en estudios anteriores, lo que sugiere diferencias en la capacidad de inducción de respuesta inmunitaria entre ambas formulaciones. Otras vacunas mencionadas, como CYD-TDV y TAK-003, también utilizan diferentes estrategias de presentación de antígenos, incluyendo virus inactivados y tecnologías basadas en nanopartículas, para estimular una respuesta inmunitaria significativa en los receptores.
La revisión de los seis estudios revela un panorama prometedor en cuanto al desarrollo de vacunas tetravalentes contra el dengue. Cada estudio aporta valiosos datos sobre la seguridad, la inmunogenicidad y, en algunos casos, la eficacia de estas nuevas vacunas. Entre los estudios incluidos, el de Miauton et al.15 se centra en la inmunogenicidad de una vacuna basada en nanopartículas, demostrando una sólida respuesta inmunitaria celular. Por su parte, Diaz et al.23 evalúan diferentes formulaciones de una vacuna inactivada, resaltando la seguridad y la durabilidad de la respuesta inmunitaria. Tricou et al.19 comparan dos formulaciones de una misma vacuna, mientras que Walsh et al.24 exploran la eficacia en diferentes grupos de edad. El estudio de gran escala de Tricou et al.19 demuestra la eficacia a largo plazo de la vacuna TAK-003, y Laydon et al.25 utilizan un enfoque bayesiano para evaluar la eficacia de la vacuna CYD-TDV. Finalmente, Russell et al.22 evalúan la seguridad y la inmunogenicidad de una vacuna viva atenuada.
A pesar de las diferencias en los diseños y las poblaciones estudiadas, todos los estudios coinciden en la importancia de inducir una respuesta inmunitaria sólida y duradera contra los cuatro serotipos del virus del dengue. Sin embargo, es fundamental destacar las limitaciones de cada estudio, como el tamaño de muestra, la duración del seguimiento y la falta de datos sobre eficacia clínica en algunos casos. Además, se observa una cierta heterogeneidad en los resultados, lo que sugiere la necesidad de realizar más investigaciones para comprender mejor los factores que influyen en la eficacia de las vacunas.
Si bien los estudios analizados contribuyen a la comprensión de las vacunas contra el dengue, presentan limitaciones metodológicas que afectan la generalización y la interpretación de sus resultados, así como su comparabilidad directa.
Varios estudios, como el de Miauton et al.15, tienen tamaños muestrales relativamente pequeños, lo cual limita la potencia estadística para detectar efectos del tratamiento y aumenta la probabilidad de errores de tipo II, es decir, la posibilidad de no identificar un efecto real de la vacuna.26 Por ejemplo, un tamaño muestral reducido podría dificultar la detección de eventos adversos raros asociados a la vacunación.
La mayoría de los estudios citados cuentan con periodos de seguimiento relativamente cortos. Esto limita la capacidad para evaluar la durabilidad a largo plazo de la protección inducida por la vacuna y la aparición de eventos adversos tardíos.24 Estudios a largo plazo, como el de Tricou et al.19 con la vacuna TAK-003 a 4.5 años, son cruciales para una mejor comprensión de la protección sostenida.
Los estudios presentan diferencias en las poblaciones estudiadas, las definiciones de casos de dengue y los criterios de inclusión y exclusión. Esta heterogeneidad dificulta la comparación directa de resultados entre estudios y la realización de metaanálisis robustos.
La mayoría de los estudios se centran en la evaluación de la respuesta inmunitaria inducida por las vacunas, pero no evalúan directamente su eficacia clínica en términos de reducción de la incidencia de dengue grave y de las hospitalizaciones.19 Son necesarios más estudios como el de Walsh et al.24 que evalúen la eficacia clínica, para facilitar una toma de decisiones informadas sobre las políticas de vacunación.
La ausencia de análisis de costo-efectividad a gran escala limita la comprensión del impacto económico de la vacunación y dificulta la evaluación de su rentabilidad. Estos análisis son cruciales para la formulación de políticas de salud pública basadas en la evidencia.
Además de las limitaciones mencionadas, se podrían considerar otros aspectos como la posibilidad de sesgos metodológicos (sesgo de selección y sesgo de detección), la variabilidad genética del virus del dengue y su impacto en la eficacia de las vacunas, o la potencial interacción de las vacunas contra el dengue y otras vacunas.
Conclusiones
Las vacunas tetravalentes contra el dengue representan una herramienta prometedora para la prevención de esta enfermedad. Sin embargo, se necesitan más investigaciones para establecer recomendaciones definitivas para su uso en la práctica clínica. Se sugiere realizar metaanálisis para obtener una estimación global de la eficacia, así como estudios de costo-efectividad para evaluar el impacto económico de la vacunación. Además, es fundamental monitorear la seguridad de las vacunas a largo plazo y desarrollar estrategias de vacunación adecuadas para diferentes poblaciones y contextos geográficos.
En general, los resultados de esta revisión sistemática son alentadores y respaldan el desarrollo de vacunas tetravalentes contra el dengue. No obstante, se requiere una comprensión integral de estas limitaciones, lo cual es fundamental para interpretar adecuadamente los resultados de los estudios actuales y diseñar futuras investigaciones que aborden tales desafíos. Esto permitirá el desarrollo y la implementación de vacunas contra el dengue más eficaces y rentables, contribuyendo a la prevención de esta importante enfermedad.











 nueva página del texto (beta)
nueva página del texto (beta)


