Introducción
El dolor tras una toracotomía puede ser muy intenso. En este sentido, además del alto riesgo quirúrgico que existe en la actualidad, los pacientes también enfrentan complicaciones adicionales debido al dolor postoperatorio.1-4 Una analgesia inadecuada causa atelectasia e hipoxemia debido a la acumulación de secreciones por un esfuerzo respiratorio deficitario e incapacidad para toser de manera efectiva.5-7 Se necesitan dosis altas de analgésicos opiáceos para evitar una analgesia inadecuada. Además, el uso de opiáceos para aliviar el dolor de la toracotomía puede provocar efectos secundarios tales como náuseas, vómitos, depresión respiratoria, adicción y un tiempo de recuperación prolongado.1,2,5,8
La analgesia epidural torácica (AET) se utiliza ampliamente en casos de cirugía torácica porque proporciona un control efectivo del dolor postoperatorio de la pared torácica.7 No obstante, la administración de AET puede causar efectos no deseados, tales como punción dural, lesión medular, hematoma epidural y absceso epidural. También se pueden observar complicaciones asociadas al catéter epidural, y la tasa de fallo epidural se sitúa en el 32%.9-11
En los últimos años, con el uso generalizado de la ecografía en anestesia se han comenzado a definir los bloqueos de planos fasciales. Con ellos se pretende alcanzar los nervios en estas regiones administrando un anestésico local entre dos capas fasciales, en lugar de bloquear los nervios que inervan la región uno por uno o el plexo al que están unidos. Los bloqueos de planos más comúnmente aplicados al área torácica son el de los pectorales I y II, el del serrato anterior, el del erector de la columna (PEC) y el del romboides.12
El bloqueo del PEC es una técnica anestésica regional destinada a la pared torácica de un lado y produce un bloqueo sensorial en múltiples dermatomas.13 En este método, el anestésico local se administra en el plano fascial entre el músculo erector de la columna y la apófisis transversa, bloqueando los ramos dorsales de los nervios espinales que pasan por allí. Como el área de inyección está lejos de la pleura, los vasos sanguíneos principales y la médula espinal, en el bloqueo del PEC la posibilidad de complicaciones mayores es muy baja.13 No obstante, aunque no suele citarse en la literatura científica, pueden sobrevenir complicaciones tales como neumotórax, toxicidad sistémica secundaria al anestésico local, daño a los nervios de la pared torácica y propagación del anestésico local al área epidural.14,15
El objetivo principal de este estudio fue poner a prueba la hipótesis de que la AET reduce las puntuaciones de la escala visual analógica (EVA) más que el bloqueo del PEC en el primer minuto, a los 30 minutos y las 2, 6, 12 y 24 horas de postoperatorio en pacientes sometidos a toracotomía. También se evaluaron como medidas de resultado secundarias la espirometría inspiratoria (Triflow) medida simultáneamente con las puntuaciones EVA, las náuseas y los vómitos postoperatorios (NVPO), y los niveles de sedación.
Material y métodos
Este estudio observacional prospectivo se llevó a cabo entre octubre de 2022 y diciembre de 2022 en el Health Sciences University Training and Research Hospital. El estudio fue realizado en conformidad con la Declaración de Helsinki (1964). Se informó detalladamente a los sujetos voluntarios y se obtuvo su consentimiento. Tras la aprobación del comité de ética de nuestro hospital (aprobación N.° 216 con fecha 21-10-2022), el estudio fue registrado en www.clinicaltrials.gov (N.° de identificador de registro: NTC06011863).
Se incluyeron pacientes de 18 a 70 años, con estado físico I-III de la ASA (American Society of Anesthesiologists), sometidos a toracotomía.16
Los pacientes fueron valorados preoperatoriamente por un anestesiólogo. Se les dieron explicaciones detalladas sobre la intervención quirúrgica, la anestesia y el manejo del bloqueo para el alivio del dolor. Se obtuvo el consentimiento informado por escrito de todos los pacientes para el estudio y la publicación de sus datos. También recibieron formación sobre la EVA empleada para valorar el dolor postoperatorio, que va de 0 (sin dolor) a 10 (el peor dolor imaginable), y los ejercicios de respiración Triflow.17,18
El día de la cirugía, los pacientes fueron llevados al quirófano tras 8 horas de ayuno y monitorizados de acuerdo con las pautas de la ASA. Aproximadamente 30 minutos antes de la intervención se insertó una vía venosa en la región antecubital utilizando una cánula de 20 G.
Los pacientes del grupo AET recibieron analgesia epidural dirigida a nivel de T7-T8, mientras que los pacientes del grupo con bloqueo PEC recibieron dicho bloqueo a nivel de T5-T6 en el lado de la incisión quirúrgica.
Tras la limpieza preoperatoria del área, se alcanzó la zona epidural desde el nivel T7-T8 de la línea media de las vértebras torácicas con una aguja epidural de 18 G (Perifix®, B. Braun Melsungen AG, Melsungen, Alemania) utilizando la técnica de la gota colgante. Tras aplicar 2 ml de lidocaína al 2% (Aritmal®, Osel Pharmaceutical Industry and Trade Inc., Estambul, Turquía) y no observar efecto espinal alguno, se administró una mezcla de morfina y anestésico local consistente en 3-4 mg de clorhidrato de morfina (Morphine HCl®, Galen Pharmaceutical Industry and Trade Inc., Estambul, Turquía), 5 ml de bupivacaína al 0.5% (Buvasin 0.5%, 20 ml, Vem Ilac, Estambul, Turquía) y 2 ml de solución salina al 0.9%, a través de la aguja epidural en una sola intervención. Luego se retiró la aguja epidural y se cerró el área de aplicación.
Antes de inducir la anestesia, el paciente fue sentado en la mesa de operaciones y colocado en una posición inclinada hacia adelante. Se cumplieron las condiciones de asepsia y antisepsia.
La sonda de matriz lineal de ultrasonido (5-12 MHz, Mindray DP-50, China) se colocó primero en el plano sagital para visualizar la apófisis espinosa de la vértebra. Después, dicha sonda se movió aproximadamente 2-3 cm lateralmente desde el nivel de la apófisis espinosa T5-T6 del lado a intervenir y se giró 90° en sentido al plano longitudinal para poder visualizar la apófisis transversa. Para dar con la posición correcta de la sonda, se identificaron los músculos trapecio, romboides mayor y erector de la columna. Utilizando el abordaje en plano, se insertó una aguja SonoPlex de 22 G 50 mm o 22 G 80 mm (Pajunk, Geisingen, Alemania) a través de la piel en sentido craneocaudal (Figura 1A). Cuando la aguja estaba ya descansando sobre la apófisis transversa, el plano entre el músculo erector de la columna y la apófisis transversa quedó confirmado mediante hidrodisección con 5 ml de solución salina (Figura 1B). Posteriormente se inyectaron 20 ml de bupivacaína al 0.25% (2.5-3 mg/kg). El bloqueo del PEC se consideró exitoso cuando el anestésico local pudo difundirse linealmente hasta el nivel de T8-T9 (Figura 1C).
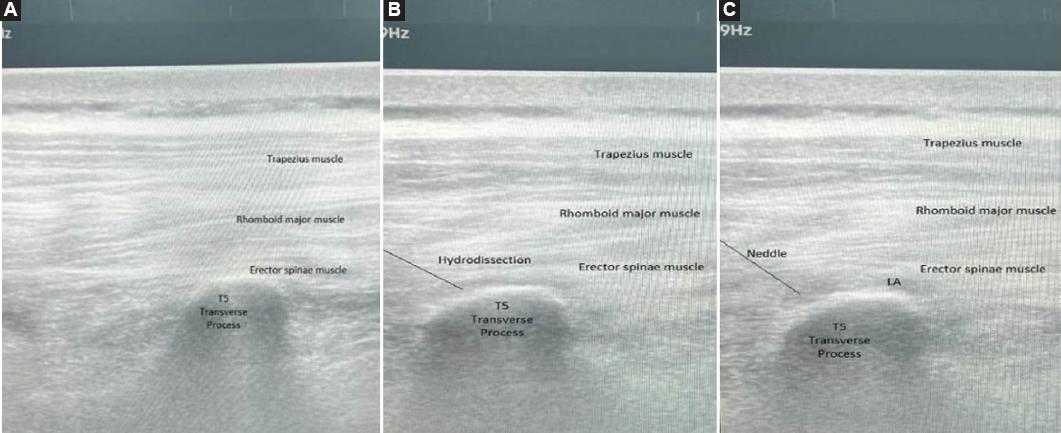
Figura 1 A: utilizando una sonda ecográfica de 5-12 MHz se identificó el músculo erector de la columna justo en la apófisis transversa de T5. B: a través de la aguja en este plano se practicó la hidrodisección. C: se inyectó lentamente el anestésico local, lo cual elevó el músculo erector de la columna de la apófisis transversa.
Los pacientes fueron colocados en posición supina. Para iniciar la anestesia, recibieron por administración intravenosa 0.1 mg/kg de midazolam (Zolamid®, Pharmaceutical Industry and Trade Inc., Ankara, Turquía), 2-3 mg/kg de propofol (Propofol® 2%, Fresenius Kabi, Bad Hamburg, Alemania), 2 μg/kg de fentanilo (Talinat®, Pharmaceutical Industry and Trade Inc., Ankara, Turquía) y 0.6 mg/kg de rocuronio (Curon®, Mustafa Nevzat Pharmaceutical Industry and Trade Inc., Estambul, Turquía). Después de lograr una relajación muscular adecuada, los pacientes fueron intubados con un tubo de doble luz de tamaño apropiado (35-37 Fr), aplicando además ventilación mecánica para que el nivel de dióxido de carbono al final de la espiración fuera de 30-35 mmHg.
Para mantener la anestesia general se utilizó una mezcla de 50% de oxígeno y 50% de aire, junto con sevoflurano (Sevoflurane® Liquit 100%, Queenborough Kent, Reino Unido) a una concentración del 2-2.5%. La mezcla se administró a razón de 3 l/min. Los requisitos adicionales de analgesia se abordaron administrando 1 μg/kg de fentanilo.
Cuando la presión arterial media aumentó un 20% o más, se procedió a administrar 1 μg/kg de fentanilo por vía intravenosa, registrándose asimismo la cantidad de opiáceo empleado durante la operación.
Todos los pacientes recibieron 1 g de paracetamol (Perfalgan®, Bristol-Myers Squibb, Itxassou, Francia) por vía intravenosa cada 8 horas en el postoperatorio. Cuando los valores de la EVA fueron ≥ 4, se administró 1 mg/kg de tramadol (Contramal®, Grunenthal GmbH, Alemania) por vía intravenosa. En los pacientes que no respondían a la administración de tramadol en un lapso de 30 minutos, se volvió a administrar 1 mg/kg de tramadol como dosis de rescate. Cuando la puntuación de NVPO fue > 1, se procedió a administrar 4 mg de ondansetrón intravenoso (Zofer®, Adeka, Estambul, Turquía).
Se registraron la edad, el sexo, el índice de masa corporal (IMC), el tipo de cirugía realizada, la duración de la intervención, la duración de la anestesia y el tiempo de estancia de los pacientes tanto en la unidad de cuidados intensivos (UCI) como en el hospital.
Tras la cirugía, los pacientes fueron extubados y seguidos primero en la sala de recuperación postanestésica y luego en la UCI de cirugía torácica. Se registraron las complicaciones tanto hemodinámicas como respiratorias con posterioridad a la intervención.
En la sala de recuperación, las puntuaciones EVA de los pacientes quedaron registradas a los 30 minutos y las 2, 6, 12 y 24 horas de postoperatorio. Si el paciente presentaba puntuaciones EVA ≥ 4, se procedió a administrar 100 mg de tramadol por vía intravenosa y se registró.
Paralelamente a las puntuaciones EVA, se sometió a una prueba de espirometría inspiratoria (Triflow) a todos los pacientes y se registró la tasa de flujo inspiratorio calculada según el número de bolas ascendentes (1 bola = 600 ml, 2 bolas = 900 ml, 3 bolas = 1200 ml). La ocurrencia de NVPO en los pacientes se valoró empleando una escala de 3 puntos, con puntuaciones de 0 (ninguno) a 2 (grave). Los pacientes con puntuaciones NVPO ≥ 1 recibieron una dosis de ondansetrón de 0.15 mg/kg por vía intravenosa.18 Los niveles de sedación se midieron utilizando una escala de 3 puntos (despierto = 0, somnoliento = 1, profundamente somnoliento = 2) en varios momentos de tiempo, incluyendo tras la extubación en la sala de recuperación postanestésica, durante los primeros 30 minutos postoperatorios y a las 2, 6, 12 y 24 horas, y se registraron como resultados secundarios.19
Análisis estadístico y cálculo del tamaño de la muestra
El cálculo del tamaño de la muestra para el estudio se realizó utilizando G*Power 3.1.9.4 software (Universidad de Kiel, Kiel, Alemania). Los parámetros empleados en el cálculo fueron un error alfa bilateral de 0.05, una potencia de 0.80 y un tamaño del efecto de 0.80. Basándose en un estudio previo y considerando una relación de asignación N2/N1 de 1, el número mínimo de pacientes requerido para el estudio se fijó en 42.20
Los análisis estadísticos se realizaron utilizando Statistical Package for the Social Sciences (SPSS 19, Chicago, IL, Estados Unidos de América). Se emplearon estadísticas descriptivas para expresar los datos numéricos como media y desviación estándar, mientras que los datos categóricos se expresaron como frecuencia y porcentaje. Se empleó la prueba χ2 para comparar datos categóricos entre grupos, y los resultados se describen como porcentajes. Para evaluar la normalidad de los datos numéricos se utilizó la prueba de Shapiro-Wilk. Para datos distribuidos normalmente se empleó la prueba t de Student, y para aquellos sin una distribución normal la prueba U de Mann-Whitney. Se consideraron estadísticamente significativos los valores de p < 0.05.
Resultados
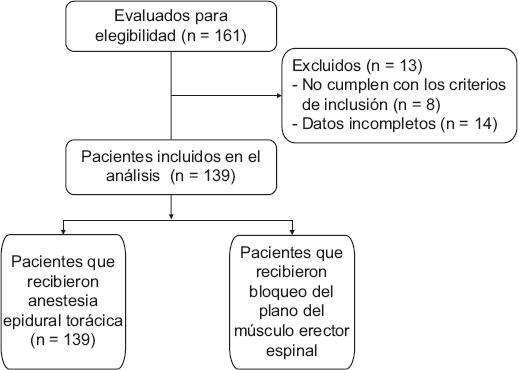
Se evaluaron 161 pacientes a efectos de elegibilidad y fueron excluidos ocho con infección, trastornos de la coagulación, obesidad mórbida (IMC > 35), alergia medicamentosa, antecedentes de dolor crónico, uso prolongado de opiáceos, antecedentes de enfermedad psiquiátrica o cirugía de emergencia (Figura 2). De los 153 pacientes restantes, 14 fueron excluidos debido a datos insuficientes durante el periodo de seguimiento (seis del grupo AET y ocho del grupo PEC). Al final quedaron 69 pacientes en el grupo AET y 70 pacientes en el grupo PEC. Los datos se obtuvieron de los registros médicos y las evaluaciones presenciales en el quirófano y en la UCI de cirugía torácica.
Del total de los sujetos, 57 eran mujeres y 82 eran hombres. La media de edad fue de 48.5 ± 17.4 años, y el IMC medio fue de 27.08 ± 3.40 kg/m². La duración media de la cirugía fue de 2.32 ± 0.57 horas y la de la anestesia fue de 3.27 ± 0.56 horas.
No se observaron diferencias significativas entre los dos grupos en cuanto a edad, sexo, IMC, duración de la cirugía, duración de la anestesia, estancia en la UCI y estancia hospitalaria (p = 0.41, 0.068, 0.87, 0.72, 0.60, 0.95 y 0.13, respectivamente) (Tabla 1).
Tabla 1 Comparación de las características demográficas y clínicas de los pacientes
| Características | Grupo AET (69) Media ± DE | Grupo PEC (70) Media ± DE | p |
|---|---|---|---|
| Edad (años) | 47.30 ± 17.28 | 49.76 ± 17.69 | 0.41 |
| IMC (kg/m²) | 27.03 ± 3.52 | 27.12 ± 3.30 | 0.87 |
| Sexo (mujer/hombre), n | 23/46 | 34/36 | 0.06 |
| Duración de la cirugía (h) | 2.31 ± 0.56 | 2.33 ± 0.59 | 0.72 |
| Duración de la anestesia (h) | 3.26 ± 0.55 | 3.27 ± 0.58 | 0.60 |
| Estancia en la UCI (días) | 1.35 ± 0.48 | 1.34 ± 0.47 | 0.95 |
| Estancia hospitalaria (días) | 4.13 ± 1.49 | 3.73 ± 1.19 | 0.13 |
AET: analgesia epidural torácica; DE: desviación estándar; IMC: índice de masa corporal: PEC: bloqueo del plano del músculo erector de la columna.
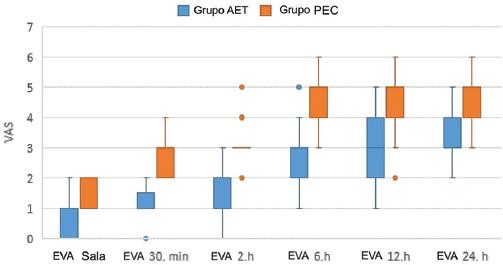
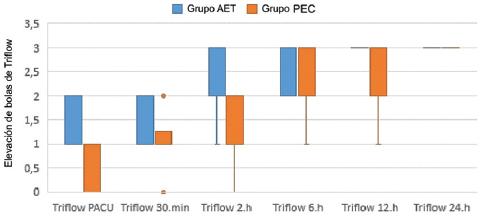
Al comparar los dos grupos según las puntuaciones en la escala EVA, se observó que el grupo AET obtuvo puntuaciones mucho más bajas que el grupo PEC, en la sala de recuperación postoperatoria, en el minuto 30 y a las 2, 6, 12 y 24 horas postoperatorias (p < 0.001). Además, el grupo AET obtuvo puntuaciones Triflow mucho más altas que el grupo PEC en la sala de recuperación postoperatoria, en el minuto 30 y a las 2, 6, 12 y 24 horas postoperatorias (p < 0.001) (Tabla 2).
Tabla 2 Comparación de las puntuaciones EVA y la capacidad respiratoria (Triflow) en el postoperatorio
| Parámetro | Grupo AET (69) Media ± DE | Grupo PEC (70) Media ± DE | p |
|---|---|---|---|
| EVA | |||
| Unidad de cuidados postoperatorios (sala de recuperación) | 0.49 ± 0.53 | 1.70 ± 0.46 | < 0.001٭ |
| 30 min | 1.13 ± 0.59 | 2.49 ± 0.53 | < 0.001٭ |
| 2 h | 1.18 ± 0.80 | 3.19 ± 0.49 | < 0.001٭ |
| 6 h | 2.20 ± 1.02 | 4.33 ± 0.79 | < 0.001٭ |
| 12 h | 3.01 ± 0.91 | 4.31 ± 0.91 | < 0.001٭ |
| 24 h | 3.74 ± 0.70 | 4.41 ± 0.75 | < 0.001٭ |
| Triflow | |||
| Unidad de cuidados postoperatorios (sala de recuperación) | 1.33 ± 0.47 | 0.34 ± 0.47 | < 0.001٭ |
| 30 min | 1.65 ± 0.48 | 1.10 ± 0.61 | < 0.001٭ |
| 2 h | 2.29 ± 0.48 | 1.53 ± 0.53 | < 0.001٭ |
| 6 h | 2.68 ± 0.46 | 2.14 ± 0.64 | < 0.001٭ |
| 12 h | 3.00 ± 0.00 | 2.41 ± 0.62 | < 0.001٭ |
| 24 h | 3.00 ± 0.00 | 2.80 ± 0.40 | < 0.001٭ |
AET: analgesia epidural torácica; DE: desviación estándar; EVA: escala visual analógica (1-10); PEC: bloqueo del plano del músculo erector de la columna.
Triflow: 1 bola = 600 ml, 2 bolas = 900 ml, 3 bolas = 1200 ml.
٭Estadísticamente significativo.
El uso de opiáceos intraoperatorios fue similar en ambos grupos. No obstante, en el postoperatorio, el consumo de opiáceos fue menor en el grupo AET que en el grupo PEC (p = 1.00 y < 0.001, respectivamente) (Tabla 3).
Tabla 3 Comparación del consumo de opiáceos intraoperatorios y postoperatorios
| Parámetro | Grupo AET (69) Media ± DE | Grupo PEC (70) Media ± DE | p |
|---|---|---|---|
| Fentanilo intraoperatorio (µg) | 100 ± 0 | 100 ± 0 | 1.00 |
| Tramadol postoperatorio (mg) | 147.8 ± 58.4 | 758.5 ± 207.4 | < 0.001٭ |
AET: analgesia epidural torácica; DE: desviación estándar; PEC: bloqueo del plano del músculo erector de la columna.
٭Estadísticamente significativo.
Al evaluar los efectos secundarios postoperatorios se observó que tanto las náuseas como los vómitos sobrevinieron, exclusivamente, en el grupo PEC; no obstante, esta disparidad no fue estadísticamente significativa (p = 0.527) (Tabla 4).
Tabla 4 Comparación de los efectos secundarios experimentados por los pacientes y la cantidad de analgésicos utilizados
| Efecto secundario | Grupo AET (69) n (%) | Grupo PEC (70) n(%) | p |
|---|---|---|---|
| Náuseas/vómitos | 4 (5.8) | 6 (8.57) | 0.52 |
| Hipotensión | - | - | - |
| Bradicardia | - | - | - |
| Prurito | - | - | - |
| Complicaciones respiratorias postoperatorias | - | - | - |
| Escala de sedación postoperatoria | 0 | 0 | - |
| Total | 4 (5.8) | 6 (8.57) | 0.52 |
AET: analgesia epidural torácica; PEC: bloqueo del plano del músculo erector de la columna.
Las puntuaciones obtenidas en la EVA y las evaluaciones Triflow de los grupos se ilustran en las figuras 3 y 4.
Discusión
En nuestro estudio evaluamos la efectividad del bloqueo del PEC y la AET en pacientes programados para toracotomía. Observamos que los pacientes que recibieron AET acompañada de una dosis baja de morfina tuvieron una menor intensidad de dolor postoperatorio y mayor capacidad respiratoria que los pacientes del grupo PEC.
En la actualidad, con el uso generalizado de la ecografía en anestesia, el interés en los bloqueos de planos fasciales ha ido en aumento. Primero, Forero et al.13 demostraron su efectividad al proporcionar analgesia completa aplicando un bloqueo del PEC a dos pacientes que desarrollaron dolor neuropático como resultado de una fractura patológica de costilla. Hamilton y Manickam21 confirmaron una analgesia efectiva con la aplicación continua de bloqueo del PEC en fracturas múltiples unilaterales de costillas en T6-T9. Asimismo, Fang et al.22 hallaron que ambos grupos tuvieron éxito en el control del dolor postoperatorio en pacientes sometidos a toracotomía que recibieron bloqueos paravertebral y del PEC.
En un caso reportado por Forero et al.23 se aplicó un bloqueo del PEC a nivel de T5 como técnica de rescate tras una AET fallida en un paciente con toracotomía, y el dolor se alivió por completo con la administración continua de un anestésico local. En otro estudio se logró un control exitoso del dolor aplicando un bloqueo del PEC tras una AET fallida en un caso similar de toracotomía.24
Pirsaharkhiz et al.25 descubrieron que el bloqueo del PEC tenía beneficios significativos en pacientes sometidos a toracotomía. También afirmaron que existe un alto riesgo de complicaciones asociadas a la anestesia epidural. En este sentido, concluyen que la técnica del bloqueo del PEC es más segura que los bloqueos epidurales y paravertebrales.25 Por su parte, Nagaraja et al.18 compararon la AET continua y el bloqueo bilateral continuo del PEC durante el perioperatorio y el postoperatorio. Encontraron que las puntuaciones EVA obtenidas durante las primeras 12 horas tras la cirugía fueron similares en los dos grupos, mientras que las obtenidas entre 12 y 48 horas posteriores fueron mucho más bajas en el grupo con bloqueo del PEC.18
Aunque los estudios son prometedores para los bloqueos de planos fasciales de la pared torácica, Marciniak et al.26 recomiendan aplicar abordajes multimodales para controlar el dolor en pacientes sometidos a toracotomía. Se afirma que el dolor asociado a los nervios simpáticos, vagales y frénicos que puede sobrevenir tras una toracotomía no puede aliviarse con bloqueos de planos, por lo que debe complementarse con analgésicos opiáceos o no opiáceos.26 Mijatovic et al.27 también tienen opiniones similares en su revisión de los métodos de analgesia en la realización de toracotomías. Basándose en lo anterior, Vilvanathan et al.28 aplicaron una combinación de bupivacaína y fentanilo a través de un catéter epidural torácico 20 minutos antes del final de la cirugía a un grupo de pacientes programados para toracotomía, y compararon la combinación de bloqueo intercostal único de bupivacaína y la infusión intravenosa de morfina con el otro grupo. Como resultado, las puntuaciones de dolor fueron estadísticamente más bajas en el grupo que recibió AET en las primeras 12 horas postoperatorias. También se observó que los resultados del grupo de bloqueo intercostal e infusión de morfina fueron similares a los del grupo que recibió AET. En este sentido, concluyen que los bloqueos de planos podrían ser una opción alternativa cuando la aplicación epidural no es viable.28 En otro estudio, Zengin y Alagoz29 aplicaron una combinación de bupivacaína, solución salina y morfina a través de un catéter epidural a un grupo de pacientes sometidos a toracotomía, mientras que en otro grupo aplicaron bupivacaína en el área paravertebral. Observaron que las puntuaciones EVA postoperatorias fueron mucho más bajas en el grupo que recibió AET.29 En este estudio, se vio que la adición de morfina a dosis bajas al anestésico local administrado por vía epidural torácica redujo notablemente el consumo de tramadol postoperatorio. Por otro lado, las puntuaciones en la EVA fueron más bajas y las capacidades respiratorias fueron más altas en los pacientes que recibieron AET. No hubo complicaciones ni fallos en la aplicación.
En nuestro estudio, se consideran limitaciones la incapacidad para evaluar el bloqueo sensorial al aplicar anestesia general inmediatamente después de la AET y los bloqueos del PEC, y la ausencia de un grupo de control.
Conclusiones
Como resultado, se concluye que se puede lograr una analgesia suficiente y efectiva con una sola aplicación al agregar morfina al agente anestésico local como AET en casos de toracotomía. No obstante, se ha determinado que el bloqueo del PEC podría ser un método alternativo en aquellos casos en los que no se puede aplicar AET por diferentes razones (coagulopatía, deformación anatómica, edad pediátrica, etc.).











 nueva página del texto (beta)
nueva página del texto (beta)