Introducción
México experimenta una transición epidemiológica caracterizada por disminución en la prevalencia de padecimientos infecciosos comunes e incremento de las enfermedades crónicas no transmisibles, entre las cuales destacan el cáncer y las enfermedades cardiovasculares de origen metabólico, como adiposopatía, dislipidemia, obesidad, hipertensión y diabetes tipo 2 (DT2).1,2 Estas entidades se han convertido en problemas significativos de salud pública y en las principales causas de muerte en el país. En 2023, el Instituto Nacional de Estadística y Geografía registró 189 289 fallecimientos atribuibles a enfermedades cardíacas y 110 174, a DT2.3
La diabetes incluye enfermedades metabólicas caracterizadas por hiperglicemia, que resultan de un defecto en la secreción o acción de la insulina, o ambos. Por su parte, la hiperglucemia crónica se asocia a daño, disfunción o falla de diversos órganos que puede llevar a la muerte.4,5 La Organización Mundial de la Salud estima que de los 422 millones de personas que viven con algún tipo de diabetes, entre 80 y 90 % padece DT2.6 En México, la prevalencia de esta enfermedad es de 18.3 %, constituye la primera causa de incapacidad prematura permanente y es responsable de 15.4 % de la mortalidad total en adultos, con lo que ocupa el segundo lugar después de las enfermedades cardíacas.3,7
La etiología de la DT2 es multifactorial, resultado de la compleja interacción entre factores ambientales y genéticos. En este sentido, se ha estimado que la heredabilidad de la DT2, la cual refleja la fracción de la enfermedad atribuible a factores genéticos, varía entre 26 y 73 %.8-10 Sin embargo, en México aún son escasos los estudios que estiman la heredabilidad de la DT2; en este sentido, Miranda Lora et al. analizaron 99 familias con miembros con diagnóstico de DT2 antes de los 19 años, en las cuales estimaron la heredabilidad de este padecimiento en 50 %.11
Diferentes estudios de genes candidato o amplios del genoma han identificado diversos loci asociados a esta patología; estos hallazgos han sido replicados principalmente en poblaciones de origen europeo y asiático.5,12,13 No obstante, este conocimiento no ha sido reproducible de manera consistente en poblaciones con una estructura genética diferente, como la mexicana.
Medicina de precisión
La culminación de la secuencia del genoma humano en 2003 marcó el inicio de una nueva era en la medicina, lo que ha generado grandes expectativas sobre cómo el conocimiento y las tecnologías derivadas de este proyecto podrían incrementar la comprensión de la etiopatogenia de las enfermedades y su aplicabilidad en la salud y la enfermedad.14 La Academia Nacional de Ciencias de Estados Unidos acuñó el término medicina de precisión y, más recientemente, salud de precisión. En ambos conceptos se pondera el uso de tecnologías ómicas como genómica, epigenómica, transcriptómica, farmacogenómica, proteómica y el exposoma, entre otras, para guiar con mayor exactitud un diagnóstico y tratamiento personalizado.15
En la actualidad, varios países están enfocados en secuenciar el genoma de sus poblaciones; un claro ejemplo es la iniciativa All of Us, un estudio que incluye a más de un millón de estadounidenses con el objetivo de vincular los datos genómicos, los registros médicos y las tecnologías digitales de salud recopilados a lo largo de más de una década. Recientemente, esta iniciativa ha presentado los resultados de la secuenciación del genoma completo de aproximadamente 100 000 estadounidenses, de los cuales alrededor de 50 % pertenece a minorías históricamente excluidas de estos estudios. Entre los principales resultados, se pudo brindar consejo genético preventivo a los participantes, contribuyendo a un nuevo paradigma de atención médica que sin duda impactará en su salud y en sus decisiones personales y médicas a lo largo de la vida.16
Así, en los últimos años han surgido otras iniciativas de medicina de precisión, como el UK Biobank, el 2025 France Genomic Medicine Initiative,17 el International Consortium for Personalised Medicine18 y la Japans Initiative on Rare and Undiagnosed Diseases,19 entre otras. Estas iniciativas engloban todas las ciencias ómicas que, en conjunto con métodos analíticos avanzados en bioinformática y datos clínicos masivos, están permitiendo no solo generar modelos de riesgo de padecer enfermedades complejas, sino también identificar el defecto responsable de entidades monogénicas, cáncer familiar y la predicción de la respuesta a medicamentos asociada a la variación genética individual. En conjunto, estos enfoques buscan establecer estrategias más precisas para el tamizaje poblacional, el diagnóstico temprano y el tratamiento personalizado, la estratificación y el monitoreo clínico desde las primeras manifestaciones bioquímicas o en etapas presintomáticas de la enfermedad, ganando cada vez más terreno en la práctica clínica. Sin embargo, el conocimiento ómico generado en una población no siempre es aplicable en otras, debido a las variaciones demográficas y adaptativas que sufren las poblaciones humanas a lo largo de su historia.
Esto abre la oportunidad de incidir en el manejo de las enfermedades y, en algunos casos, de guiar cambios significativos en el estilo de vida. Gracias a los avances en el desarrollo de tecnologías de nueva generación, la medicina genómica está impulsando nuevos enfoques en casi todas las especialidades médicas. A continuación, se discuten algunos ejemplos de las principales herramientas ómicas de medicina de precisión en DT2 (Figura 1).
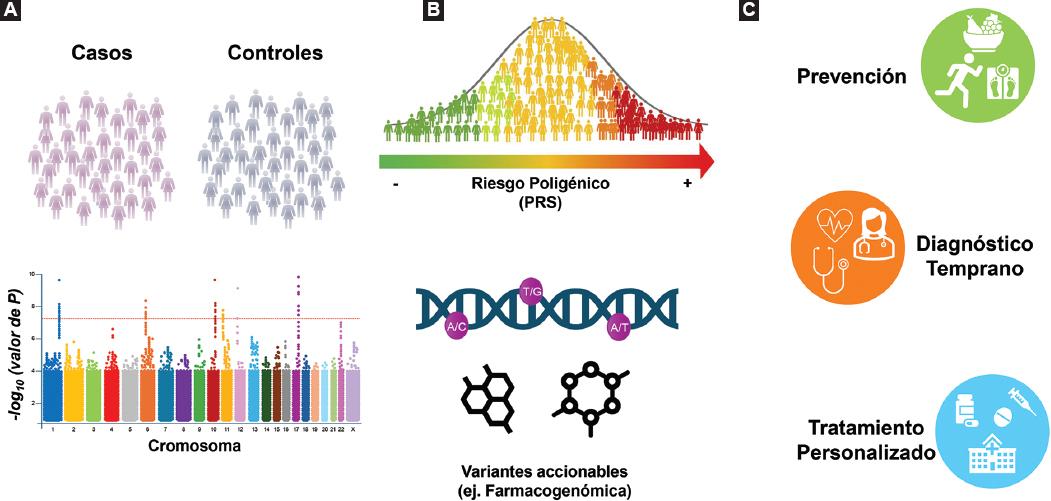
Figura 1 Implementación de medicina de precisión a partir de datos genómicos. A: los estudios de asociación comparan casos con alguna enfermedad (por ejemplo, DT2) y sujetos de control de una población, con el objetivo de identificar variantes que incrementan la probabilidad de padecer esa patología o que son accionables. B: las variantes pueden ayudar a determinar el riesgo genético individual para una enfermedad y a la estratificación de los individuos de acuerdo con este (PRS), o pueden incidir directa o indirectamente en la respuesta al tratamiento o a la aparición de sus efectos adversos (farmacogenómica). C: estas herramientas pueden ayudar a establecer estrategias de salud pública de medicina de precisión donde se ponderé la prevención, el diagnóstico más preciso y el tratamiento personalizado.
Estudios de asociación del genoma completo (GWAS) en diabetes tipo 2
Los GWAS analizan de manera simultánea la asociación de cientos de miles o millones de variantes genéticas con un fenotipo particular. Suelen incluir miles o decenas de miles de individuos afectados por una enfermedad o rasgo, así como sujetos sanos de control de la misma población. Actualmente, los GWAS han permitido identificar más de 60 000 variantes de un solo nucleótido (SNV, single nucleotide variant) asociadas a diferentes enfermedades, incluyendo DT2.20,21
En DT2, estos estudios han logrado identificar más de 500 SNV; algunas de ellas, como las variantes rs7903146 del gen TCF7L2 y la rs2237897 de KCNQ1, han sido replicadas de manera consistente. Por otro lado, también se han identificado variantes específicas para diferentes poblaciones.10,12,13 Históricamente, la población mexicana ha estado subrepresentada en este tipo de estudios. Durante la última década, como parte del consorcio SIGMA (Slim Initiative in Genomic Medicine for the Americas), se ha identificado un grupo de variantes propias o enriquecidas en la población de origen nativo americano, las cuales se encuentran asociadas a riesgo de desarrollar DT2. Un ejemplo de esto es el haplotipo compuesto por 18 SNV localizado en el gen SLC16A11,22 cuya frecuencia aproximada es de 30 % en población mestiza y 50 % en población indígena. En estudios in vitro en tejido hepático de pacientes mexicanos, se demostró que este haplotipo de riesgo induce una menor expresión del gen y los portadores tienen un receptor con una menor actividad, lo que se asocia a lipotoxicidad.23
Otra variante propia de la población mexicana es la p.E508K en el gen HNF1A. Aunque tiene una baja frecuencia (2 %), es exclusiva de población mexicana e incrementa el riesgo de DT2 en casi cinco veces (razón de momios = 4.96),24 alcanzando las mayores frecuencias en poblaciones mesoamericanas. Esto refleja la compleja estructura genética de la población mexicana, destacando la necesidad de incluir a grupos minoritarios en estudios genómicos.
Por otro lado, en el gen IGF2 se identificó la variante de protección rs149483638 (c.-3-1G>A), donde el alelo A se asocia a 20 % de reducción en el riesgo de desarrollar DT2. Esta variante afecta un sitio de corte y empalme entre los exones 1 y 2, causando la expresión de la isoforma 2 de esta proteína en hígado y tejido adiposo, lo que se relaciona con una reducción en los niveles de hemoglobina glicada. Esta variante tiene una frecuencia de 17 % en población mexicana y está ausente en otras poblaciones.25
A pesar de que se ha logrado identificar SNV de riesgo para DT2 en la población mexicana, lo que permite profundizar en el conocimiento de las bases genéticas de esta enfermedad, se requieren más estudios para determinar el espectro total de las variantes asociadas a DT2 en México, donde se han empezado a sumar esfuerzos como el Estudio Prospectivo de la Ciudad de México, que incluye la secuenciación de 10 000 genomas y 140 000 exomas, lo cual podría incrementar el conocimiento de la DT2 y sus comorbilidades en la población mexicana.26
Puntajes de riesgo poligénico
La integración del conocimiento genómico en herramientas que puedan transformarse en políticas públicas en materia de salud permitirá a los pacientes con enfermedades de origen multifactorial ser los principales actores de su bienestar, modificando factores ambientales, como el estilo de vida. Una alternativa cada vez más utilizada para la toma de decisiones clínicas, especialmente en el contexto de la detección temprana y la prevención de las enfermedades metabólicas, es la estimación probabilística, incluso desde el nacimiento, de la susceptibilidad individual basada en las variantes genéticas de riesgo o puntajes de riesgo poligénico (PRS, polygenic risk score). Los PRS se componen del conjunto de variantes asociadas a la predisposición genética para desarrollar una enfermedad en una población determinada. Para cada individuo, se suman sus alelos de riesgo, ponderados por su efecto (razón de momios), generando una puntuación de 0 a 100 %, que refleja la estimación precisa del riesgo genético de un individuo a padecer una enfermedad.27
La utilidad clínica de los PRS está en relación directa con la implementación de programas de intervención para reducir la probabilidad de desarrollar una enfermedad en las personas identificadas con alto riesgo.28 Un ejemplo de lo anterior son los estudios en individuos de ascendencia europea con alto riesgo poligénico de aterosclerosis (PRS ≥ 80 %), en quienes la intervención profiláctica con estatinas redujo en 44 % el riesgo relativo de sufrir una enfermedad coronaria y representó un ahorro de hasta $55 000 dólares por año de vida saludable del paciente.29 Con base en estos resultados, el acceso a las nuevas herramientas genómicas como los PRS debería incorporarse a la atención médica en países emergentes como México.
Estudios de farmacogenómica en población mexicana
Otra herramienta para medicina de precisión es la farmacogenómica, es decir, el uso de la información genómica que influye en la función de las proteínas encargadas de la absorción, metabolismo y eliminación de los fármacos, con el objetivo de personalizar la prescripción de los medicamentos. Las variantes genéticas influyen en la variabilidad interindividual de la farmacocinética y la farmacodinamia de los medicamentos, modificando su eficacia y efectos adversos.30
En la DT2, el adecuado control glucémico es crucial para prevenir las complicaciones asociadas; sin embargo, en México solo 36.1 % de los pacientes logra un control glucémico adecuado con las guías de tratamiento actuales.7 En este apartado se describirán algunos ejemplos de la farmacogenómica de los dos medicamentos más comunes para tratar la DT2 en la población.
La metformina es el tratamiento de primera elección para DT2. Dado que no se metaboliza, los estudios se han enfocado principalmente en los transportadores responsables de su absorción y eliminación, codificados por siete genes de la superfamilia SLC.31 La base de datos farmacogenómicos PharmGKB de los Institutos Nacionales de Salud de Estados Unidos reporta 19 variantes en genes SLC asociadas a cambios farmacocinéticos o efectos adversos de la metformina.30 Nuestro grupo de trabajo ha identificado que la variante p.L125F en el transportador MATE1, codificado por el gen SLC47A1, se asocia a cambios farmacocinéticos de la metformina y aumento de lactatemia, un efecto adverso potencialmente letal. La variante p.L125F muestra la frecuencia más alta del mundo en nuestra población: 16 % en mestizos y 27 % en indígenas mexicanos, aún más elevada en población maya de la península de Yucatán (34 %). Esta frecuencia contrasta con su ausencia en poblaciones europeas y africanas.32
La glibenclamida, perteneciente al grupo de las sulfonilureas, es otro medicamento utilizado como monoterapia para la DT2 en México, aunque su uso ha disminuido en los últimos años.33 Esta clase de fármacos inhibe los canales de potasio sensibles al ATP en células β pancreáticas, estimulando la secreción de insulina. En la plataforma PharmGKB, los genes con mayor número de variantes asociadas a la farmacocinética de las sulfonilureas son CYP2C9 y CYP2C19 (principales metabolizadores del fármaco), así como KCNJ11, ABCC8 y KCNQ1 (que codifican para canales de potasio). En la población nativa mexicana se han identificado diferencias étnicas en la frecuencia de los alelos de pérdida de función de CYP2C19.34 Adicionalmente, se ha reportado que los portadores de la variante p.A1369S en ABCC8 y de p.E23K en KCNJ11 tienen una respuesta diferencial a las sulfonilureas en pacientes mexicanos.35
Incluir el uso de variantes genéticas accionables en las guías ayudará a los médicos a brindar tratamientos personalizados y optimizar la terapia farmacológica, lo que ayudará a la disminución de los efectos adversos, los costos de atención y las complicaciones asociadas.
Retos para la implementación de la medicina de precisión en la práctica clínica
El desarrollo de las ciencias ómicas (especialmente la genómica) durante la última década ha traído consigo una nueva forma de entender el impacto de la variación genética, los perfiles de expresión, así como la función y cantidad de sus proteínas y metabolitos sobre la salud humana. La diversidad de esta primera generación de aplicaciones ómicas tiene el potencial de afectar directamente la atención clínica, la toma de decisiones para gestionar riesgos, la elección del tratamiento y el asesoramiento al paciente. Por otra parte, existen barreras que superar para la incorporación de estas tecnologías a la práctica clínica rutinaria, como los costos asociados, que en numerosos casos las hacen inaccesibles para los pacientes, al igual que su adopción por parte de los clínicos. Por lo anterior, se requiere la acción conjunta de científicos, clínicos, epidemiólogos, sector público y privado, tomadores de decisiones, entre otros, para generar políticas públicas de salud que se traduzcan en guías clínicas que incorporen la medicina de precisión para la prevención y tratamiento de la DT2 y otras patologías.
Conclusiones
La revolución genómica ha permitido profundizar en el conocimiento sobre la etiopatogénesis de diversas enfermedades, incluida la DT2. También ha subrayado la necesidad de investigar las distintas poblaciones humanas, ya que existen factores genéticos específicos de cada población que influyen en el desarrollo de esta y otras patologías. Aunque estos estudios aún son limitados en población mexicana, la generación de biobancos de datos clínicos y genómicos será fundamental para acelerar la traslación de la medicina genómica a la clínica, para el diagnóstico certero, la prevención y el tratamiento de distintas enfermedades en México.











 nueva página del texto (beta)
nueva página del texto (beta)


