Introducción
Las arilaminas N-acetiltransferasas (NAT) son isoenzimas importantes para la biotransformación de fármacos y sustancias químicas presentes en el ambiente; sin embargo, también participan en el metabolismo celular y en el desarrollo de cáncer.1,2 Ambas isoenzimas comparten una identidad de 81 % en su secuencia de nucleótidos, lo cual representa una similitud de 87 % en los aminoácidos. Las proteínas NAT se encuentran principalmente en el citosol y se componen de 289 aminoácidos, con un peso molecular aproximado de 33 kDa.3 A pesar del alto grado de identidad en la secuencia, los genes de NAT1 y NAT2 codifican isoenzimas con distintas especificidades de sustrato, distribución en tejidos y niveles de expresión durante el desarrollo. NAT1 se encuentra distribuida en la mayoría de los tejidos y tipos celulares, y preferencialmente acetila sustratos como ácido paraaminobenzoico, ácido p-aminosalicílico y p-aminobenzoilglutamato (arilaminas de cadena alquílica corta).4 NAT2 se detecta predominantemente en el hígado, intestino delgado y colon, y metaboliza sustratos como sulfametoxazol, isoniazida, procainamida y dapsona (arilaminas lipofílicas).5 Adicionalmente, por resultados de nuestro grupo de trabajo se muestra la presencia de NAT1 y NAT2 en linfocitos y monocitos humanos de sangre periférica de sujetos aparentemente sanos y con tuberculosis.6
Polimorfismos y NAT
Ambas isoenzimas se caracterizan por presentar más de un polimorfismo de un solo nucleótido (SNP) en sus respectivos genes, lo cual influye en la actividad de acetilación. Los SNP de NAT1 están asociados a efectos menores en la función de la acetilación, por lo que se ha reportado una menor variabilidad interindividual que la que presenta NAT2.7 Los SNP de NAT1 se relacionan principalmente con susceptibilidad a distintos tipos de cáncer, como el de mama, colón, vejiga o leucemia.8 Particularmente, el haplotipo NAT1*10 (anteriormente asignado como 1088 T > A, 1095 C > A y ahora como 215 T > A, 222 C > A) está relacionado con una actividad incrementada de NAT1 y con la formación de aductos de ADN, especialmente cuando se combina con fenotipos de acetilación lenta de NAT2.9 Nuestro grupo de investigación reportó la asociación genética entre los haplotipos de NAT1 y NAT2 con la leucemia linfoblásticas aguda,10 el cáncer infantil de mayor frecuencia, siendo los haplotipos NAT1*3 (razón de momios [RM] = 2.1) y NAT1*4 (RM = 1.92) de mayor riesgo en población infantil del estado de San Luis Potosí. Estos resultados son similares a los del estudio reportado por Krajinovic et al.,11 pero diferente a los de otras investigaciones de asociación genética en las que se encontró asociación del haplotipo NAT1*10 con la probabilidad de desarrollar cáncer, principalmente el de mama.
Los haplotipos de las familias NAT2*5, NAT2*6, NAT2*7 y NAT2*14 (acorde con los criterios del Arylamine N-acetyltransferase Gene Nomenclature Committee, http://nat.mbg.duth.gr/) muestran una actividad de acetilación disminuida y se presentan principalmente en población caucásica y africana. Respecto a los SNP de NAT2 se ha señalado que los fenotipos acetiladores rápidos y lentos están determinados por la herencia de un rasgo codominante.12 Estudios en poblaciones caucásicas y japonesas demuestran las diferencias geográficas en la incidencia de acetiladores lentos de isoniazida y sulfametazina en humanos,13 lo que deriva en que pueda cumplirse o no la meta terapéutica cuando las personas son medicadas con estos fármacos. De esta manera, el papel de los SNP de NAT y su utilidad en diversas áreas han sido demostrados.14-19 Se realizó la genotipificación de NAT2 de sujetos sanos de población mestiza mexicana del estado de San Luis Potosí para conocer su fenotipo acetilador. En este estudio se encontró 18.8 % de acetiladores rápidos, 45.4 % de acetiladores intermedios y 39.6 % de acetiladores lentos.6
En lo que concierne a NAT1, nuestro grupo de investigación es el primero en México en evaluar la frecuencia alélica y genotípica, así como su fenotipo de acetilación; en población de nuestro centro de trabajo10 se encontró mayor frecuencia del fenotipo rápido (72.8 %), después del intermedio (27.2 %) y no se identificaron casos del fenotipo lento.
Fisiología de las NAT
Las enzimas NAT transfieren grupos acetilo a partir de acetilcoenzima A hacia el grupo amino de una hidrazina arílica (isoniazida, hidralazina) o de una arilamina (aminas aromáticas), como paraaminosalicilato,20,21 mediante tres tipos de reacciones de acetilación: O−, N− y N, O−. El propósito de estas reacciones de acetilación es detoxificar el cuerpo humano de los xenobióticos que ingresan al organismo.
Como ya se mencionó, NAT2 ha sido la más estudiada y se asocia a fallas terapéuticas en el tratamiento contra la tuberculosis, debido a que metaboliza la isoniazida, produciendo el metabolito acetil isoniazida, el cual carece de actividad farmacológica.22,23 Por otra parte, esta enzima puede estar relacionada con alteraciones fisiopatológicas del metabolismo de la glucosa y ácidos grasos debido a que existen indicios de que la expresión genómica de NAT2 es sensible a los efectos de la insulina y la glucosa. En cultivos in vitro de hepatocitos humanos de la línea celular HepG2, se observó aumento de la expresión de NAT2 tras ser estimulados durante 24 horas con 5.5 mM de glucosa o 100 mM de insulina;24 mientras que en pacientes con diabetes mellitus tipo 2 se encontró incremento de la proteína de NAT2 y asociación positiva con los niveles de glucosa y hemoglobina glicosilada.25 Lo anterior sugiere que NAT2 pudiera tener algún papel en la modulación del metabolismo de la glucosa; sin embargo, falta determinar a qué nivel del metabolismo pudiera participar.
En contraste, se ha descrito que NAT1 disminuye el crecimiento celular26,27 debido a su posible regulación del gen P53, el principal gen supresor de tumor en nuestro genoma,28 y su influencia en el metabolismo de acetilcoenzima —promueve el crecimiento celular si se encuentra en altas concentraciones dentro de la célula—,2,29 aunque el mecanismo no se ha elucidado del todo.
Epigenética y NAT
La epigenética estudia las reacciones químicas y procesos que modifican la actividad del ADN, pero sin alterar su secuencia. Los tres mecanismos epigenéticos de regulación —metilación del ADN, modificación de las histonas y los ARN pequeños no codificantes microARN—, son reversibles, lo que resulta en un control dinámico de la expresión de genes.30
NAT1, enzima que inicialmente se consideraba detoxificante, ahora se propone que influye en la regulación del ciclo celular y constituye un factor clave en la regulación epigenética, debido a su participación en el metabolismo del folato. NAT1 acetila el metabolito p-aminobeozoilglutamato (pABAGlu),31,32 el cual inhibe la dihidrofolato reductasa, como consecuencia se inhibe el catabolismo del folato y la síntesis de S-adenosil metionina, cofactor importante en múltiples procesos de metilación, entre ellos la metilación del ADN y de histonas.1,33 Por lo anterior, se propone a NAT1 como un regulador epigenético,33 ya que al no presentar actividad enzimática, el epigenoma podría desestabilizarse. Por lo tanto, es de interés conocer los mecanismos de regulación de NAT1 y su influencia en cáncer. En tanto, al parecer en el humano NAT2 está más implicada en procesos metabólicos.
Estudio bioinformático de los genes de NAT1 y NAT2
Nuestro grupo de trabajo realizó un análisis bioinformático para explorar los sitios de metilación dentro de los promotores de los genes de NAT1 y NAT2 a través de la base de datos ENCODE® (https://www.encodeproject.org; https://epigenomegateway.wustl.edu/legacy). Por estudios in vitro con las líneas celulares Jurkat (leucemia del tipo T) y GM12878 (leucemia del tipo B) para el promotor del gen NAT1, se encontró que la región de interés no cuenta con el suficiente contenido de citocina-guanina para determinar que exista una isla CpG que influya en la expresión del gen. Sin embargo, en el promotor se encuentran sitios CpG que presentan metilación del ADN, los cuales, aunque no tengan influencia directa en la transcripción, pueden ser empleados como biomarcadores de correlación entre el grado de metilación y el desarrollo de cáncer.34 Para el caso del promotor de NAT2, en ENCODE se ha reportado una isla CpG a 3600 pb de la región codificante del gen; sin embargo, esta región se encuentra rodeada por retrotransposones, por lo que probablemente su influencia en la expresión del gen es baja. Por lo tanto, al igual que en NAT1, pueden existir sitios CpG que ayuden a predecir la susceptibilidad de desarrollar cáncer si se demuestra una correlación entre las dos variables.
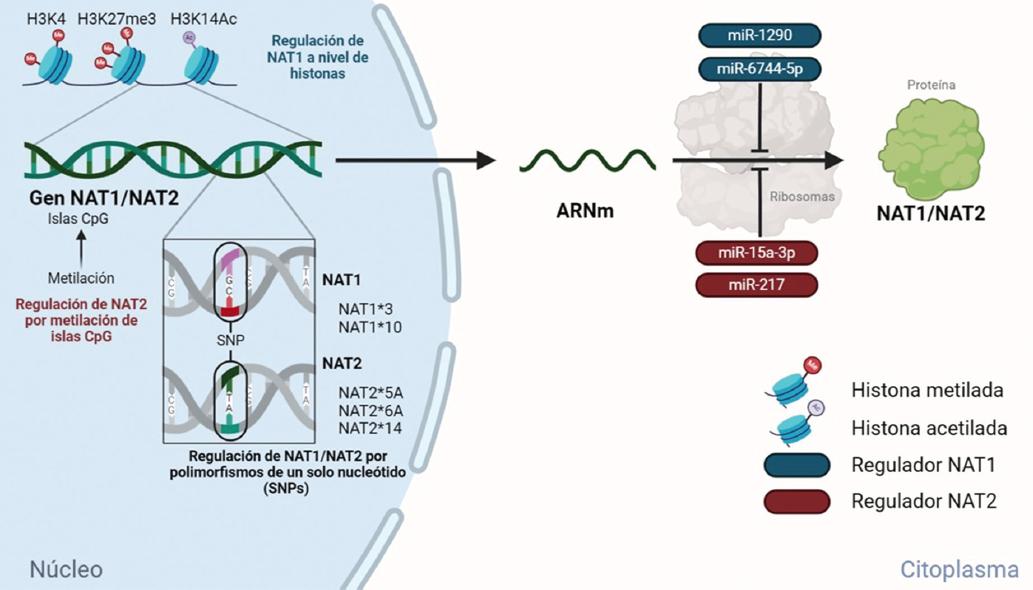
En lo que concierne a la modificación postraduccional de histonas, se realizó un estudio bioinformático en ENCODE, en el que se encontró que existe una fuerte interacción de lisina 4 trimetilada y 27 acetilada en histona H3 con el promotor de NAT1, principalmente en las líneas celulares Jurkat y GM12878. Para NAT2 se observó interacción en distintos sitios del gen con las colas de histonas y, a diferencia de las islas CpG, parece que la modificación de histonas desempeña un papel importante en la regulación de estos genes (Figura 1).
Cáncer y NAT1
Particularmente en cáncer, las regiones promotoras de cada gen pueden ser alteradas por metilación en las islas CpG o por desacetilación y metilación de histonas, en consecuencia se promueve la expresión de oncogenes y la disminución de genes supresores de tumores.35 Lo anterior apoya la propuesta de nuevas estrategias terapéuticas (epigenéticas) con el uso de fármacos para favorecer la expresión de los genes que se encuentran suprimidos. Se han reportado diversos ejemplos del uso de fármacos en fase I o II como el ácido valproico, tazemetostat, givinostat y vorinostat, este último para el tratamiento de linfoma cutáneo de células T.30
En experimentos in vivo, Xiao et al. reportaron que en células de pacientes con leucemia existe hipoacetilación general de H3 y H4 (generalmente asociada a baja expresión), mientras que predomina hipermetilación de H3 en lisina 4 (H3K4), que generalmente se relaciona con supresión de genes en ese estado.36
El primer estudio que reportó el control epigenético de NAT1 en tejido humano evaluó el estado de metilación de la región 5 proximal al codón de inicio en tejido mamario normal, maligno y benigno.37 En tejido de tumor maligno se demostró que las regiones de CpG en esa parte del gen presentaron menor metilación en comparación con tejido normal y de tumor benigno; además, la expresión de ARN mensajero (ARNm) fue 1000 veces mayor. El estudio demostró también que el gen de NAT1 se encuentra silenciado parcialmente por mecanismos de metilación en tejido mamario. Otro grupo de trabajo demostró que la resistencia a tamoxifeno en el tratamiento de cáncer mamario está relacionada con los niveles de metilación de NAT1 y afecta su expresión a nivel de ARNm. La hipermetilación de NAT1 confiere resistencia al tamoxifeno y los niveles de expresión de NAT1 son menores en los tumores resistentes al fármaco comparados con aquellos tumores sin resistencia.38
Por lo anterior, nuestro grupo de investigación estudió las posibles alteraciones a nivel de histona H3 en lisina 14 acetilada (H3K14Ac) y lisina 27 trimetilada (H3K27me3);39 encontró que las células mononucleares de niños con leucemia linfoblástica aguda presentan bajos niveles de acetilación (en H3K14Ac) para NAT1 en comparación con niños sanos; respecto al gen de NAT2, se observaron bajos niveles de acetilación (en H3K14Ac) y altos de metilación (en H3K27me3) en los mismos grupos de estudio. En el caso de NAT2, el trabajo de nuestro grupo es el primero que reporta niveles de alteración de histonas en cáncer.39 Sin embargo, a nivel de transcrito y proteína, solo NAT1 presentó alteraciones en su expresión, así como en su actividad enzimática; mientras que se detectaron niveles similares de expresión y actividad de NAT2 entre pacientes y sujetos de control.
Modulación de NAT mediante microARN
Distintos autores han reportado la regulación de NAT por sirtuínas o microARN (miARN) (Figura 1),39-41 pequeñas moléculas de ARN endógeno (de 20 a 25 nucleótidos) no codificantes que se unen directamente a la región 3-UTR de ARNm blanco, lo que les permite ser reguladores negativos de expresión génica.42 Desde su descubrimiento, los datos clínicos y biomédicos han mostrado evidencia del papel de los miARN en enfermedades humanas, como en cáncer y leucemias, categorizándolos como biomarcadores para el diagnóstico y pronóstico.43
Se ha descrito la relación de NAT1 con miR-1290 en cáncer de mama positivo para receptor de estrógenos y en leucemia linfoblástica aguda.39,41 El gen de NAT1 es blanco de este miARN, lo que induce una disminución de sus niveles de expresión. En modelos celulares de cáncer de mama luminal A, como la línea celular MCF-7, se ha estudiado también el efecto de pre-miR-1290 (precursor del miARN-1290) sobre NAT1, donde el incremento de los niveles de miARN-1290 mostraron una correlación negativa con los niveles de expresión de NAT1 a nivel de ARNm.44
En el mismo modelo celular se estudió el efecto de miR-6744-5p sobre la anoikis, la apoptosis que se induce cuando las células se desprenden de la matriz extracelular y de las células vecinas. Se demostró que la disminución de miR-6744-5p induce un aumento en la expresión de NAT1, lo que incrementa la motilidad, la resistencia a la apoptosis (anoikis) y la metástasis en esta línea celular de cáncer. Entre los posibles mecanismos por los cuales NAT1 podría contribuir a la resistencia a la apoptosis está causar daño al ADN por carcinogénesis química. Como enzima acetiladora, NAT1 participa en la conversión de 4-aminobifenilo en aducto de ADN, un compuesto cancerígeno que se ha asociado al consumo de carne roja.45
Por otra parte, NAT2 se ha asociado a daño hepático por isoniazida, cuyos metabolitos activos (AcHz) son hepatotóxicos. En modelos de ratón se ha evaluado el efecto de la modulación de NAT2 por hsa-miR-15a-3p. Se observó que la sobreexpresión de hsa-miR-15a-3p correlaciona con disminución de la expresión del ARNm de NAT2, reduciendo el daño hepático en los modelos murinos. Con lo anterior, hsa-miR-15a-3p participaría como modulador epigenético protector contra el daño hepático inducido por isoniazida.46 Interesantemente, en modelos de ratas Wistar con daño hepático no inducido por isoniazida, la inhibición de NAT2 mediante miR-217 disminuyó la proliferación de los hepatocitos al promover la apoptosis y la autofagia.47 Aún se desconoce el mecanismo por el que NAT2 participa en daño hepático de modelos no tratados con isoniazida, pero podría estar relacionado con las proteínas mitocondriales Bax y Bcl-2 y la caspasa 3, que modulan la proliferación y la apoptosis.
Lo anterior indica que estos miARN regulan las NAT; NAT1 está asociada a cáncer de mama y leucemia linfoblástica aguda, mientras que NAT2 se encuentra asociada a la función hepática, por lo que se consideran un posible blanco terapéutico al participar en el pronóstico de estas enfermedades, de ahí que sería importante determinar los mecanismos de regulación de NAT por miARN y su impacto en el metabolismo celular.
Actividad enzimática de las NAT
La expresión y actividad enzimática de NAT pueden estar reguladas a nivel genético, epigenético y postranscripcional. En ensayos in vitro de líneas celulares adicionando sustratos específicos se ha estudiado su actividad enzimática mediante cromatografía de líquidos:8,48,49 ácido paraaminobenzoico para NAT1 e isoniazida o sulfametoxazol para NAT2. Nuestro grupo de investigación implementó métodos para cuantificar sustratos y metabolitos por HPLC-UV/Vis.40
La actividad de NAT1 se encuentra disminuida en líneas celulares de leucemia (Jurkat y CEM),33 como se ha observado en investigaciones realizadas por nuestro grupo en niños con leucemia linfoblástica aguda,39 lo cual podría ser un factor pronóstico en los pacientes con esta neoplasia. En contraste, la actividad enzimática de NAT1 en el cáncer de mama se ha reportado variable en ensayos en líneas celulares (MCR-7, ZR-75-1, MDA-MB-231 y MDA-MB-436).33 Por ello, es importante elucidar los mecanismos celulares involucrados en la expresión de sus niveles en la proteína y en la actividad enzimática, para explicar este contraste, y comprender la relación en el ámbito genético y epigenético, y su papel en el crecimiento celular, así como su posible implicación en el control del epigenoma.
Conclusiones
Toda la información presentada demuestra que NAT1 y NAT2, ya sea en SNP, histonas, ARNm o actividad enzimática, tiene implicaciones en diversas patologías crónicas, como tuberculosis, leucemia linfoblásticas aguda o cáncer de mama. A partir de su descubrimiento, se consideraba a NAT1 y NAT2 como enzimas involucradas en el proceso de biotransformación de fármacos; actualmente, queda claro que su papel en la fisiología celular es más complejo y aún quedan mecanismos por investigar: en el caso específico de NAT1, elucidar su papel en el desarrollo de cáncer y en el metabolismo celular, con lo cual podría, incluso, llegar a ser considerada como un modulador epigenético. En tanto, NAT2 está involucrada principalmente en el metabolismo de la glucosa y la sensibilidad a la insulina.











 nueva página del texto (beta)
nueva página del texto (beta)