Introducción
La preeclampsia es una enfermedad multisistémica que afecta de 2 a 8 % de los embarazos en el mundo y es causa principal de morbilidad y mortalidad materna y perinatal.1 La preeclampsia tiene factores de riesgo conocidos, pero actualmente se recomienda aplicar pruebas de tamiz precoz para implementar medidas de prevención primaria, especialmente dirigidas a países de economías emergentes, donde la frecuencia de la preeclampsia y su impacto en salud son mayores.2 Estas pruebas de tamiz precoz de preeclampsia se basan en biomarcadores que pueden aplicarse como prueba única o en diversas combinaciones.3 Particularmente, la proteína plasmática A asociada al embarazo (PAPP-A, pregnancy-associated plasma protein A) es un biomarcador útil cuando no están disponibles otros, como el factor de crecimiento placentario o el Doppler pulsado de las arterias uterinas.2
PAPP-A en el primer trimestre es un marcador conocido de riesgo perinatal;4 es un producto de la placenta y la decidua que se secreta a la circulación materna durante el embarazo y tiene función de proteasa sobre la proteína de unión 4 para el factor de crecimiento similar a la insulina.5 Se le han descrito diversas funciones: en la placenta, promueve la invasión trofoblástica y regula la esteroidogénesis, así como el transporte de glucosa y aminoácidos en las vellosidades coriales.6 Esto explica por qué los niveles bajos de PAPP-A se asocian a eventos perinatales adversos.4 Además, a menores niveles de PAPP-A, el parto complicado con preeclampsia ocurre a edades gestacionales menores.3 Este comportamiento clínico es congruente con el modelo de riesgos en competencia para preeclampsia.7 Sin embargo, los algoritmos predictivos o calculadoras clínicas tienen un rendimiento inferior en poblaciones diferentes a las de su origen,8 excepto cuando se utilizan los valores de referencia de la población diana para los biomarcadores.9 Lo anterior ha sido probado en una población mexicana con acceso a múltiples biomarcadores,10 por lo que se justifica explorar la utilidad de PAPP-A en otras poblaciones mexicanas que no dispongan de otros biomarcadores.
El objetivo de este estudio fue explorar a pequeña escala el desempeño de PAPP-A como biomarcador precoz e independiente para predecir preeclampsia en una población mexicana conforme a valores de referencia locales; se utilizó un marco predefinido de riesgos en competencia.
Material y métodos
Se realizó un proyecto piloto con diseño de casos y controles anidados en una cohorte de embarazos de feto único incluidos durante el primer trimestre de la gestación, cuyo término fue atendido en un hospital regional. Para el estudio se obtuvo la aprobación del comité de ética de la sede, además de que se siguió la Declaración de Helsinki de la Asociación Médica Mundial para las investigaciones médicas en seres humanos. El reclutamiento fue consecutivo de abril de 2016 a junio de 2022 y todos los participantes otorgaron su consentimiento informado.
La preeclampsia se definió conforme a la Sociedad Internacional para el Estudio de la Hipertensión en el Embarazo11 y en el parto con preeclampsia se siguió el modelo de riesgos en competencia, en el cual el evento en estudio fue el tiempo al parto con preeclampsia, independientemente de la clasificación o severidad.7 Se midieron las concentraciones de PAPP-A (en mUI/mL mediante quimioluminiscencia) en sueros maternos obtenidos al reclutamiento en el primer trimestre. Los valores de referencia de la mediana poblacional local por edad de gestación se construyeron a partir de los controles mediante el método de Royston y Wright;12 la mediana se utilizó para estandarizar los valores absolutos de PAPP-A en múltiplos de la mediana (MoM).
El análisis estadístico se basó en el desempeño de PAPP-A como modelo de predicción13 para el desenlace de parto con preeclampsia,7 utilizando un marco predefinido de riesgos en competencia3,7 (los cálculos se describirán con detalle en otro documento y el código fuente está disponible para descarga desde https://doi.org/10.6084/m9.figshare.23304221.v1). De forma paralela, se calculó el desempeño del algoritmo en su formato original.3 El nivel de significación con fines de prueba fue α = 0.1 para el valor de p. El tamaño mínimo de muestra para la versión piloto se calculó en seis casos y seis controles (con base en la información disponible sobre la prueba en otras poblaciones3,10); se decidió concluir el reclutamiento al superar el mínimo de casos, por tratarse del evento menos frecuente en la cohorte de origen.
Resultados
Se incluyeron siete casos y 41 controles reclutados entre las siete y 13 semanas de gestación, la cual finalizó entre las 30 y 40 semanas. Los valores de referencia para la mediana local por gestación x resultaron ser los siguientes (Figura 1):
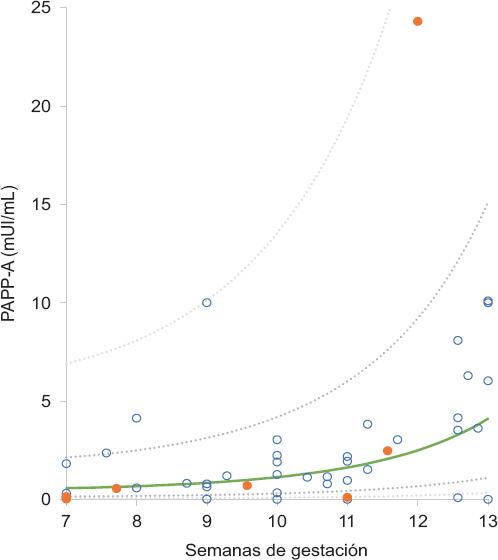
Figura 1 Gráfico de dispersión de la concentración sérica de la proteína plasmática A asociada al embarazo (PAPP-A), según la semana de gestación en que se midió en cada embarazo con preeclampsia (punto naranja) y sin preeclampsia (círculo azul); así como la mediana de referencia obtenida de la muestra poblacional (línea verde) y los percentiles 10, 25, 75 y 90 (líneas grises).
PAPP-A (mUI/mL) = 100.0003 × 2 0.0218x + 0.1135
El modelo de PAPP-A que resultó discriminante significativo fue el marco predefinido de riesgos en competencia centrado en razones de verosimilitud (LR, likelihood ratio) para preeclampsia en gestaciones de menos de 37 semanas y estas LR como clasificadores; tuvo un área bajo la curva de la característica operativa del receptor = 0.68 (IC 90 % = 0.52-0.84). Con una tasa de 20 % de resultados falsos positivos, la tasa de detección fue de 43 % para una LR = 3.5; mientras que con 15 % de resultados falsos positivos, la tasa de detección fue de 29 % para una LR = 46.1 (Figura 2, curva roja; los otros modelos no se presentan).
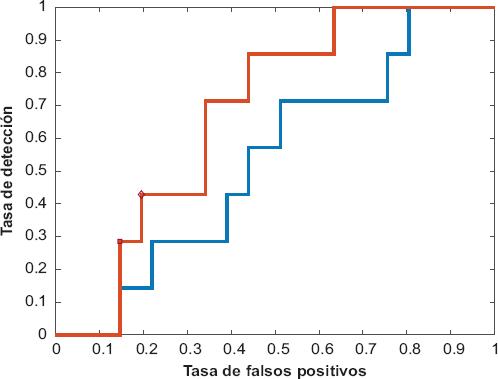
Figura 2 Áreas bajo las curvas de la característica operativa del receptor para la proteína plasmática A asociada al embarazo (PAPP-A), medida en el primer trimestre de la gestación como prueba discriminante para predecir parto con preeclampsia, según los múltiplos de la mediana (MoM) por valores de referencia locales (véase Figura 1), transformados a razones de verosimilitud positiva (LR) por un algoritmo predefinido adaptado desde una calculadora externa3 (https://doi.org/10.6084/m9.figshare.23304221.v1); el escenario fue preeclampsia antes de las 37 semanas (línea roja). Con una tasa de 20 % de resultados falsos positivos, la tasa de detección fue de 43 %, para una LR = 3.5 (rombo rojo); a 15 % de resultados falsos positivos, la tasa de detección fue de 29 % para una LR = 46.1 (cuadrado rojo). Adicionalmente se grafica el desempeño para el algoritmo en su formato original3 (línea azul).
Por el contrario, el algoritmo original para PAPP-A no mostró significación discriminativa con un área bajo la curva = 0.53 (IC 90 % = 0.34-0.73, Figura 2, curva azul).
Discusión
Se demostró a pequeña escala la validez de un método para implementar PAPP-A como biomarcador precoz e independiente de preeclampsia en el primer trimestre para población mexicana. La fortaleza del estudio radicó no solo en utilizar valores de referencia locales para PAPP-A, sino también en la asignación individual de LR para preeclampsia mediante metodología innovadora3,7 (véase https://doi.org/10.6084/m9.figshare.23304221.v1). Lo anterior tiene ventajas a nivel individual y de salud pública. Por un lado, el modelo permite probar el desempeño de diversos puntos de corte para seleccionar el óptimo para cada centro o programa de detección (una LR = 3.5 tiene mejor tasa de detección frente a una LR = 46.1, con menos resultados falsos positivos). Por otro lado, el valor de LR individualizado permite otorgar una atención médica personalizada y de precisión (Material Suplementario). Sin embargo, para hacer estas inferencias se requiere mejorar la confiabilidad de los estimados mediante una muestra de mayor tamaño; el resultado del estudio piloto justifica continuar esta línea de investigación. La combinación o comparación con otros marcadores escapa del alcance de esta investigación; no obstante, podrían abordarse en análisis futuros.
La utilidad de una prueba positiva estriba en la prevención primaria,2 porque la preeclampsia es causa importante de morbilidad y mortalidad materna y perinatal.1 Sin embargo, el asesoramiento individual sobre el resultado de una prueba de este tipo debe otorgarse bajo las consideraciones del ámbito perinatal:14 médicas o científicas, jurídicas y de derechos humanos, éticas y psicológicas.
Conclusión
PAPP-A en el primer trimestre del embarazo fue efectiva para predecir preeclampsia en la muestra estudiada. Deben usarse los valores de referencia de la población diana y el modelo de riesgos en competencia con mejor desempeño. Los algoritmos predictivos o calculadoras clínicas para preeclampsia tienen un rendimiento inferior en poblaciones diferentes a las de su origen cuando se aplican en su formato original.











 nueva página del texto (beta)
nueva página del texto (beta)


