Introducción
La osteoporosis se define como una enfermedad caracterizada por una baja masa ósea y un deterioro microarquitectural del tejido óseo que lleva a mayor fragilidad ósea y, en consecuencia, a un incremento en el riesgo de fracturas.1 Desde 1994, el diagnóstico de osteoporosis se ha definido por una densidad mineral ósea (DMO) 2.5 o más desviaciones estándar (DE) por debajo del valor medio de mujeres jóvenes, es decir, un T-score ≤ −2.5 DE.2 El rango de referencia para calcular el T-score tanto en hombres como en mujeres es la base de datos de la Tercera Encuesta Nacional de Examen de Salud y Nutrición (NHANES III) para mediciones del cuello femoral en mujeres blancas de 20 a 29 años en Estados Unidos, conforme a la recomendación de la Fundación Internacional de Osteoporosis, la Fundación Nacional de Osteoporosis y la Sociedad Internacional de Densitometría Clínica.3,4 El uso de umbrales diagnósticos basados en la DMO se adoptó ampliamente como criterio de inclusión para ensayos de intervención en osteoporosis,5 y posteriormente se consideraron umbrales de intervención.
Aunque la DMO constituye un componente central de la evaluación del riesgo de fractura, la precisión de la predicción del riesgo mejora cuando se consideran otros índices de riesgo de fractura, especialmente los que añaden información más allá de la proporcionada por la DMO. Se han desarrollado varios modelos de predicción de riesgo, y el más ampliamente utilizado es la herramienta de evaluación del riesgo de fractura FRAX®. En esta revisión, debatimos el papel que desempeña FRAX en el manejo de la osteoporosis, así como los desarrollos recientes para incorporar factores de riesgo adicionales en su uso.
Desarrollo de FRAX
FRAX es un algoritmo accesible en línea lanzado por primera vez en 2008 por el entonces Centro Colaborador de la Organización Mundial de la Salud para Enfermedades Metabólicas Óseas en Sheffield, Reino Unido.6,7 Calcula la probabilidad de fractura de cadera y de fractura osteoporótica mayor (FOM, cadera, columna vertebral, antebrazo distal o húmero proximal) a 10 años en mujeres posmenopáusicas y hombres de 40 años o más. El algoritmo integra edad, sexo, índice de masa corporal (IMC) y siete factores de riesgo clínicos (FRC) dicotomizados que comprenden fractura por fragilidad previa, historia parental de fractura de cadera, tabaquismo actual, uso de glucocorticoides orales (por más de tres meses), artritis reumatoide, consumo excesivo de alcohol (tres o más unidades por día) y otras causas de osteoporosis secundaria, para generar una probabilidad promedio de fractura a 10 años. La DMO del cuello femoral puede introducirse opcionalmente para mejorar la predicción. Tanto el riesgo de fractura como el riesgo de muerte se tienen en cuenta al generar la probabilidad de fractura. Esto es importante ya que las personas con un alto riesgo de muerte tienen una menor probabilidad de fractura que aquellas con una expectativa de vida más larga; además, algunos factores de riesgo afectan al riesgo de fractura y al riesgo de muerte, como el aumento de la edad, el bajo IMC, la baja DMO, el uso de glucocorticoides y el tabaquismo. Así, la probabilidad a 10 años en los ancianos es la probabilidad de vida restante.
El rendimiento de una herramienta de evaluación de riesgos puede evaluarse por el gradiente de riesgo: en FRAX, como el incremento del riesgo de fractura por cada DE de aumento en la puntuación de riesgo. La Tabla 1 muestra los gradientes de riesgo para la predicción de fracturas con el uso de solo FRC, solo DMO del cuello femoral y ambos. El uso de FRC más DMO y la inclusión de la edad mejoran la sensibilidad de la predicción de fracturas sin que influya negativamente en la especificidad.8 En general, el valor predictivo de FRAX es parecido al de otros motores de riesgo como la puntuación obtenida en el modelo Gail para cáncer de mama.9
Tabla 1 Gradientes de riesgo con el uso de la densidad mineral ósea del cuello femoral, factores de riesgo clínicos o ambos
| Edad (años) | Gradiente de riesgo | ||
|---|---|---|---|
| Solo DMO del cuello femoral | Solo FRC | FRC+DMO | |
| Fractura de cadera | |||
| 50 | 3.68 (2.61-5.19) | 2.05 (1.58-2.65) | 4.23 (3.12-5.73) |
| 60 | 3.07 (2.42-3.89) | 1.95 (1.63-2.33) | 3.51 (2.85-4.33) |
| 70 | 2.78 (2.39-3.23) | 1.84 (1.65-2.05) | 2.91 (2.56-3.31) |
| 80 | 2.28 (2.09-2.50) | 1.75 (1.62-1.90) | 2.42 (2.18-2.69) |
| 90 | 1.70 (1.50-1.93) | 1.66 (1.47-1.87) | 2.02 (1.71-2.38) |
| Otras fracturas osteoporóticas | |||
| 50 | 1.19 (1.05-1.34) | 1.41 (1.28-1.56) | 1.44 (1.30-1.59) |
| 60 | 1.28 (1.18-1.39) | 1.48 (1.39-1.58) | 1.52 (1.42-1.62) |
| 70 | 1.39 (1.30-1.48) | 1.55 (1.48-1.62) | 1.61 (1.54-1.68) |
| 80 | 1.54 (1.44-1.65) | 1.63 (1.54-1.72) | 1.71 (1.62-1.80) |
| 90 | 1.56 (1.40-1.75) | 1.72 (1.58-1.88) | 1.81 (1.67-1.97) |
Datos presentados como riesgo relativo por cambio de desviación estándar (intervalo de confianza de 95 %).8 Tabla reproducida con la amable autorización de Springer Science and Business Media. DMO: densidad mineral ósea; FRC: factores de riesgo clínicos.
El uso de solo FRC proporciona gradientes de riesgo comparables (1.4-2.1) al uso de solo DMO, si bien el mejor rendimiento (mayores gradientes de riesgo) se observa cuando se emplean ambos parámetros, particularmente en la predicción de fracturas de cadera (Tabla 1). Cabe destacar que existe una correlación débil, aunque significativa (r = −0.25) entre la puntuación FRAX sin DMO y la DMO del cuello femoral, lo que significa que las personas con altas probabilidades de fractura basadas únicamente en FRC suelen tener una DMO más baja.8,10 A modo de ilustración, las mujeres ≥ 75 años con probabilidades de FOM superiores a un umbral de 35 % con base únicamente en FRC tienen una DMO = −1 DE respecto a quienes están por debajo del umbral.11 Esto tiene una importancia obvia para la detección de casos en ausencia de acceso a DMO.
Validación y calibración de FRAX
FRAX ha sido validado en 11 cohortes independientes que no participaron en la síntesis del modelo. El uso de solo FRC o en conjunto con DMO dio gradientes de riesgo que diferían significativamente de la unidad en todas las cohortes de validación y eran comparables a los de las cohortes originales utilizadas para la construcción del modelo.8
Como las tasas de fractura y muerte específicas por edad difieren en las distintas regiones del mundo,12,13 los modelos de FRAX suelen calibrarse con la epidemiología de la fractura de cadera (preferentemente de fuentes nacionales; se pueden usar otros sitios si hay datos disponibles) y la mortalidad (generalmente derivada de datos de las Naciones Unidas) de cada país, con modelos actualmente disponibles para 84 naciones, que cubren más de 80 % de la población mundial. La herramienta parece estar bien calibrada cuando se ha analizado en estudios considerados representativos de poblaciones nacionales, de Reino Unido, Noruega, Israel, Japón, Taiwán y Canadá.14-20
FRAX está actualmente disponible en 35 idiomas y es fácilmente accesible a través de dos sitios web: https://frax.shef.ac.uk/frax/ y https://www.fraxplus.org, así como otras tecnologías como equipos de DMO, aplicaciones para teléfonos inteligentes y, en algunos países, en calculadoras de mano.
Uso de FRAX en la intervención y evaluación
Un objetivo importante de la evaluación del riesgo de fractura es que las intervenciones se dirijan adecuadamente a quienes tienen un alto riesgo de fractura. El uso de T-score de la DMO como único umbral para la intervención es subóptimo, ya que tiene baja sensibilidad pero alta especificidad para identificar a individuos con alto riesgo de fractura, de ahí que la mayoría de las fracturas por fragilidad ocurra en pacientes con valores de DMO por encima del umbral de osteoporosis.19 Además, el mismo umbral de T-score tiene un menor impacto en la probabilidad de fractura con el aumento de la edad, debido al creciente riesgo competidor de la muerte y la disminución de la DMO con la edad.20 En cambio, una fractura por fragilidad previa es un factor de riesgo altamente significativo en todas las edades.
Por último, las tasas de fractura difieren ampliamente de un país a otro, mucho más de lo que se puede explicar por variaciones en la DMO: un T-score correspondiente a una mujer de 65 años con una probabilidad de FOM a 10 años de 20 % varía de −4.6 en Venezuela a −2.0 en Islandia.21 Cuando los umbrales de intervención se basan solo en T-score, se niega el tratamiento adecuado a individuos con alto riesgo de fractura que no cumplen con la definición densitométrica de osteoporosis. Este problema se agrava aún más en algunos sistemas de salud que limitan el reembolso de los costos del tratamiento según criterios densitométricos22,23 y/o con relativa falta de acceso a métodos de densitometría ósea.
Para abordar estas limitaciones, los umbrales de intervención basados en las probabilidades de FRAX se han incorporado en más de 80 directrices de todo el mundo,24 aunque su aplicación ha sido heterogénea. Los umbrales de intervención fijos de probabilidad a 10 años ≥ 20 para FOM o ≥ 3 % para fracturas de cadera basados en análisis económicos (actualmente obsoletos)25 se utilizan en varias directrices, iniciadas originalmente por la Fundación Nacional de Osteoporosis de los Estados Unidos (ahora Fundación para la Salud Ósea y la Osteoporosis).26,27 No obstante, este abordaje constituye un problema en la proporción de la población apta para el tratamiento, tal como ilustra un estudio en mujeres posmenopáusicas japonesas: < 1 % de las mujeres menores de 60 años alcanzarían alguna vez un umbral de probabilidad de fractura ≥ 20 %, mientras que el uso de un umbral menos estricto, de 10 %, resultaría en que la mayoría de las mujeres > 65 años y más de 95 % de aquellas ≥ 75 años fueran tratadas.28 Por su parte, los umbrales basados en análisis de costo-efectividad también dependen del tiempo y del sistema de salud: los costos del tratamiento cambian con el tiempo y factores como el riesgo de fractura, el costo de la fractura, la disposición a pagar, entre otros, varían en los diferentes sistemas de salud.
El Grupo Nacional de Directrices de Osteoporosis del Reino Unido (NOGG) fue el primero en desarrollar directrices que incorporan umbrales de intervención dependientes de la edad.29,30 Dado que a las mujeres con una fractura por fragilidad se les puede recomendar tratamiento sin requerir una DMO para la toma de decisiones, este umbral de fractura la probabilidad de fractura específica de la edad equivalente a la de mujeres con IMC promedio y una fractura por fragilidad previa se estableció como el punto de decisión de intervención. Aunque este umbral aumenta con la edad, no guarda relación con abordajes de costo-efectividad para el establecimiento de umbrales, si bien se ha demostrado que es rentable en el contexto del Reino Unido.31
Los mismos umbrales dependientes de la edad también se aplican a los hombres, ya que la efectividad y rentabilidad de las intervenciones en hombres son, en general, similares a las de las mujeres con un riesgo equivalente.32 Estos criterios para los umbrales de intervención ha sido incorporado en disposiciones de Europa, Eurasia, Medio Oriente y América Latina.33-40 Los umbrales de NOGG fueron revisados posteriormente para aplanar el umbral a partir de los 70 años, ya que los umbrales anteriores requerían un mayor riesgo de fractura, particularmente de cadera, para que el tratamiento estuviera indicado en mujeres ≥ 70 años sin una fractura previa, en comparación con quienes calificaban solo por la fractura.41 Lo anterior resultó en parámetros híbridos tanto dependientes de la edad como criterios fijos para la intervención (Figura 1).42
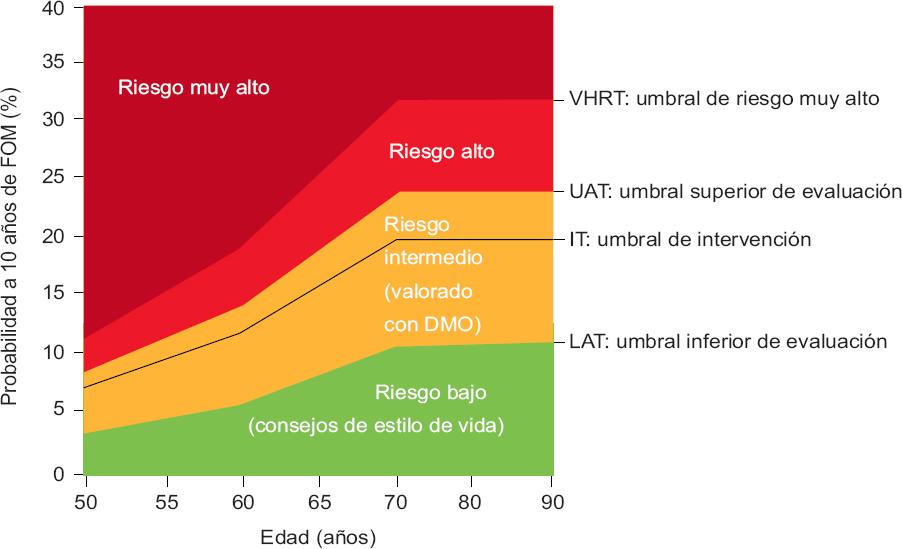
Figura 1 Umbrales de evaluación, intervención y riesgo del Grupo Nacional de Directrices de Osteoporosis del Reino Unido (NOGG) para la probabilidad de fractura osteoporótica mayor (FOM) en el Reino Unido según FRAX. En la evaluación sin DMO, se recomienda valorar la DMO en aquellos cuya probabilidad de fractura esté entre el umbral de evaluación superior (UAT) y el umbral de evaluación inferior (LAT). La intervención se recomienda si la probabilidad resultante supera el umbral de intervención (IT). El tratamiento se recomienda para individuos en las categorías de alto riesgo y muy alto riesgo, con tratamiento anabólico de primera línea recomendadas para aquellos en muy alto riesgo (ver texto).42 Reproducido con la amable autorización de Springer Science and Business Media.
Las guías de práctica clínica de NOGG también dan un ejemplo del uso de FRAX como puerta de entrada a la evaluación: delinea un umbral de evaluación superior (UAT, upper assessment thresholds), por encima del cual el paciente se considera en un riesgo suficientemente alto de fractura para ser considerado para tratamiento sin recurrir a la DMO; y un umbral de evaluación inferior (LAT, lower assessment thresholds), por debajo del cual el paciente corre un riesgo lo suficientemente bajo como para decidir no tratar sin la DMO. Con ello se enfoca el uso de la DMO en la categoría intermedia para guiar el tratamiento; posterior a la inclusión de la DMO, los pacientes con probabilidades de fractura que superen el umbral de intervención deberían recibir tratamiento (Figura 1).
Los abordajes para definir los umbrales de evaluación difieren según la disponibilidad (y reembolso) de la densitometría y la forma de dirigir el diagnóstico de la osteoporosis (por ejemplo, la búsqueda de casos en comparación con un cribado poblacional). En los criterios de NOGG, el UAT se ha establecido en 1.2 veces el umbral de intervención, ya que se encontró que era el punto de corte por encima del cual casi ninguna persona será reclasificada de alto a bajo riesgo con la adición de la DMO a FRAX.29 Con base en la búsqueda de casos, donde la evaluación va dirigida a individuos con FRC, el LAT se estableció en las probabilidades de fractura específicas de la edad de mujeres con un IMC medio sin FRC. En países con acceso muy limitado o nulo a métodos de densitometría, se puede usar FRAX sin DMO,43 ya que el uso de FRC per se proporciona gradientes de riesgo comparables a los de DMO.
Identificación de sujetos en riesgo muy alto
Más recientemente, la evidencia que demuestra una reducción más rápida del riesgo de fractura con el tratamiento anabólico en comparación con el tratamiento antirresortivo,44,45 así como el reconocimiento de que el riesgo de una fractura osteoporótica subsiguiente es particularmente alto inmediatamente después de una fractura índice y disminuye progresivamente con el tiempo (riesgo inminente),46,47 llevaron a la estratificación del riesgo alto para delinear una categoría de riesgo muy alto,48 en la que se puede considerar el uso de tratamiento anabólico de primera línea.49
El criterio para definir este umbral de riesgo muy alto varía, por ejemplo, las directrices del NOGG lo han establecido en 1.6 veces el umbral de intervención específico de la edad (Figura 1),42,50 y las guías de la Fundación Internacional de Osteoporosis y la Sociedad Europea de Aspectos Clínicos y Económicos de la Osteoporosis, la Osteoartritis y las Enfermedades Musculoesqueléticas en el UAT (1.2 veces el umbral de intervención).33 La Asociación Americana de Endocrinólogos Clínicos y el Colegio Americano de Endocrinología establecieron un umbral de riesgo muy alto, en 1.5 veces el umbral de intervención, es decir, una probabilidad de fractura de cadera de 4.5 % o una probabilidad de FOM de 30 %.26 En cambio, la definición adoptada por la Sociedad Endocrina de Estados Unidos es la presencia de múltiples fracturas vertebrales y un T-score de DMO de cadera o columna ≤ −2.5 DE.51
Cribado con FRAX
El papel que desempeña FRAX en el cribado poblacional se ha examinado en tres grandes estudios prospectivos aleatorizados de posibles estrategias de cribado poblacional,52-54 aunque con importantes diferencias en el diseño del estudio y criterios para los umbrales de intervención. Se observó que el uso del cribado basado en FRAX para identificar y tratar a individuos con alto riesgo de fractura logró una reducción en las fracturas de cadera en el ensayo de cribado para la prevención de fracturas en mujeres mayores (SCOOP) en el Reino Unido y en el estudio de Estrategia de Osteoporosis Estratificada por Riesgo en Dinamarca;52,53 en tanto, no se observó una diferencia significativa en las tasas de fractura en el Estudio de Osteoporosis SALT en los Países Bajos.54 Un metaanálisis de los tres estudios mostró una reducción de 20 % en las fracturas de cadera, y reducciones más pequeñas pero significativas en FOM y todas las fracturas osteoporóticas, aun cuando el tratamiento se dirigió solo a entre 11 y 18 % de los participantes en los grupos de cribado55 Además, se ha demostrado que el método utilizado en el ensayo SCOOP es altamente rentable y/o ahorrador de costos.56,57 Estos hallazgos proporcionan evidencia de que el cribado poblacional del riesgo de fractura es efectivo para reducir las fracturas.
Eficacia de la intervención estratificada por el riesgo basal de fractura
FRAX se ha aplicado predominantemente en análisis post-hoc de varios estudios de fase III de tratamiento de la osteoporosis para determinar las características de inclusión de los participantes y si la eficacia del tratamiento varía según el riesgo basal de fractura. Ranelato de estroncio,58 teriparatida,59,60 abaloparatida,61 zoledronato,62 la terapia hormonal menopáusica63 y raloxifeno mostraron una eficacia similar en una variedad de probabilidades de fractura,64 mientras que clodronato,65 denosumab,66 romosozumab67 y bazedoxifeno mostraron mayor reducción relativa del riesgo de fractura con mayores probabilidades basales de fractura.68
Los resultados anteriores implican que la intervención farmacológica, tradicionalmente basada en umbrales de DMO determinados en ensayos de intervención, es igualmente efectiva en pacientes seleccionados con base en FRAX en función únicamente de FRC, sin DMO. También avalan la opinión de las instituciones reguladoras de que los tratamientos deben dirigirse preferentemente a hombres y mujeres con alto riesgo de fractura; utilizar tratamientos que muestren una mayor eficacia con un mayor riesgo basal de fractura mejora el impacto presupuestario y la rentabilidad de la intervención. Finalmente, los hallazgos de una mayor eficacia a mayores probabilidades de fractura con algunas intervenciones tienen importantes implicaciones para la evaluación de tecnologías de salud y desafían el abordaje metaanalítico actual.
Abordando las limitaciones de FRAX y la introducción a FRAXplus®
FRAX fue diseñado para su uso en el entorno de la atención primaria, por lo que los FRC incluidos fueron cuidadosamente elegidos para limitar su número y complejidad, facilitar su registro e incluir solo contribuyentes bien validados e independientes al riesgo de fractura. Además, era importante que los factores identificados presentaran un riesgo susceptible de intervención, denominado reversibilidad del riesgo.8 Aunque apreciado por su simplicidad, una limitación importante por la que se ha criticado a FRAX es que en varios de los FRC identificados no se tiene en cuenta la respuesta a la exposición, como el mayor riesgo de fractura con el incremento de la dosis y duración de los glucocorticoides orales, el número de fracturas previas y la magnitud del consumo de tabaco y alcohol.24 También preocupa la falta de DMO de la columna lumbar (comúnmente recomendada en las directrices de tratamiento) y la ausencia de mediciones de las propiedades materiales o estructurales del hueso. Para abordar algunas de estas limitaciones, se han realizado análisis exploratorios en cohortes poblacionales para examinar el impacto de otros factores aparte de los incluidos en FRAX, con acceso a estos ajustes ahora a través de FRAXplus® (https://www.fraxplus.org). Se debe destacar que se ha demostrado que las probabilidades de FRAX no se ven afectadas en gran medida por el estatus socioeconómico,69 la variación en la composición corporal,70 la exposición a inhibidores de la aromatasa71 y el tratamiento concurrente para la osteoporosis.72
Fractura reciente por fragilidad
Se ha demostrado que el riesgo de una fractura osteoporótica subsiguiente es particularmente alto inmediatamente después de una fractura índice, y disminuye progresivamente con el tiempo.73-75 Este riesgo inminente también depende de la edad.46 El análisis de una cohorte poblacional de Reykjavik (Islandia) proporcionó un método para ajustar las estimaciones convencionales de FRAX de la probabilidad de fractura, utilizando una fractura previa de recencia incierta, para tener en cuenta el impacto de una fractura reciente conocida dentro de un intervalo de dos años.47 El efecto de la recencia también depende de la ubicación y es más acentuado en hombres y mujeres más jóvenes (Figura 2).
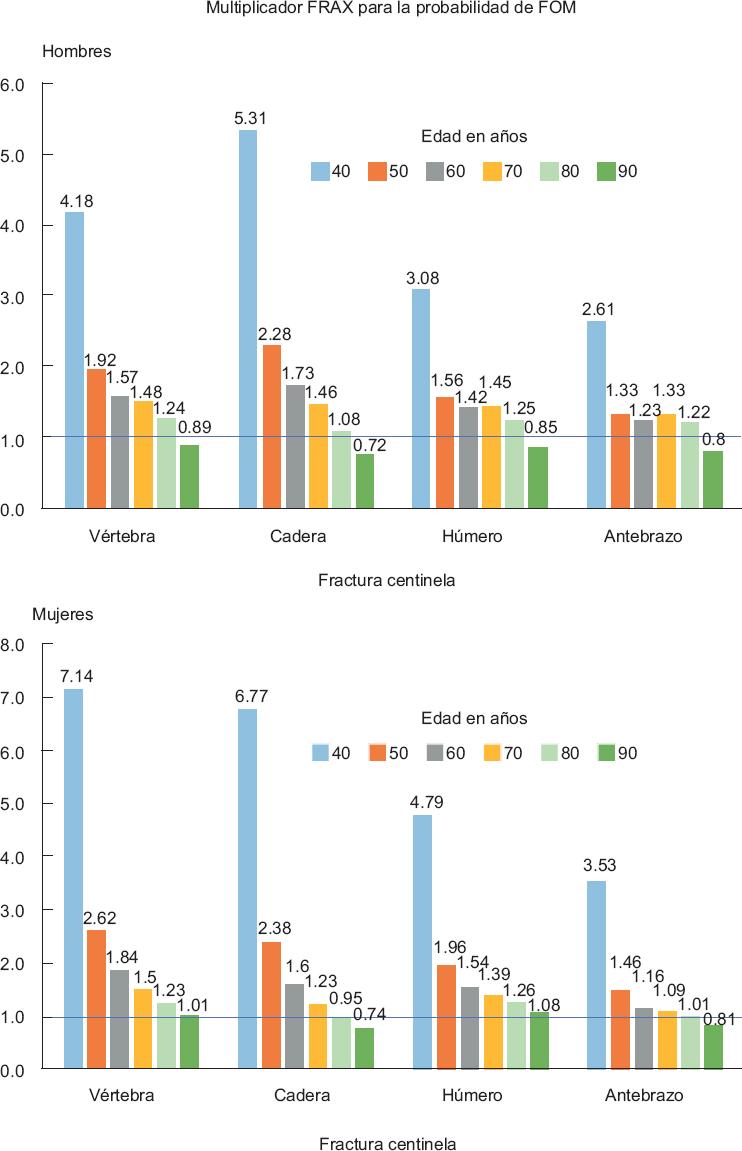
Figura 2 Relación de las probabilidades a 10 años de una fractura osteoporótica mayor por edad en hombres (panel superior) y mujeres (panel inferior). La relación es la probabilidad a 10 años de una fractura osteoporótica mayor (FOM) por una fractura reciente (dentro de los últimos 2 años) en los sitios mostrados, dividida entre la probabilidad a 10 años en cualquier sitio, independientemente de su recencia.47 Reproducido con la amable autorización de Springer Science and Business Media.
En los ancianos, se puede apreciar un ajuste a la baja en las probabilidades de fractura con una fractura reciente debido a que estas compiten con el riesgo incremental de muerte inmediatamente después de una fractura. Es importante señalar que, incluso cuando las proporciones de probabilidad caen por debajo de la unidad, los individuos con fractura reciente todavía tienen mayor probabilidad de fractura que aquellos sin fractura previa.
Número de fracturas previas
Un examen más detallado de la cohorte de Reykjavik también proporcionó datos para ajustar las probabilidades de fractura según el número de fracturas previas: como era de esperar, las probabilidades de fractura osteoporótica mayor y de cadera se incrementan con el número de fracturas pasadas.76 Las probabilidades a 10 años de fractura de cadera y de FOM se determinaron según el número de fracturas osteoporóticas previas durante un intervalo de 20 años a partir de los riesgos de muerte y fractura, y se derivaron proporciones de probabilidad en comparación con la probabilidad calculada para fractura previa independientemente del número de fracturas anteriores. Las proporciones nuevamente facilitaron los ajustes a las estimaciones convencionales de fractura de FRAX. Las medias de probabilidad según el número de fracturas previas para todos los escenarios fueron 0.95, 1.08, 1.21 y 1.35, para una, dos, tres y cuatro o más fracturas previas, respectivamente.76 El incremento en las probabilidades de fractura con el número de fracturas recientes disminuyó con la edad, pero no se afectó por el sexo.
Dosis de glucocorticoides orales
El impacto de la ingesta de glucocorticoides orales en las probabilidades de fractura en FRAX asume la exposición a una dosis media de glucocorticoides orales, aunque en realidad el riesgo de fractura depende tanto de la dosis como de la duración de la exposición.77,78 En un análisis de la Base de Datos de Investigación de Práctica General (GPRD) del Reino Unido, se llevaron a cabo comparativas entre la exposición a dosis bajas (< 2.5 mg/día de prednisolona o dosis equivalente), medias (2.5-7.5 mg/día) y altas (> 7.5 mg/día) de glucocorticoides orales, donde la dosis media se tomó como la exposición promedio.79 La exposición a dosis más altas de glucocorticoides se asoció a mayor riesgo de fractura. Se asumió que las dosis más altas de glucocorticoides probablemente estarían asociadas a mayor riesgo de mortalidad, ya sea directamente o como consecuencia de la gravedad de la enfermedad subyacente que hace necesaria la administración de dosis altas. Por lo tanto, el incremento en la probabilidad de fractura fue menor de lo predicho solo a partir de la razón de riesgo de fractura. Los resultados de este estudio proporcionaron la base para un simple ajuste aritmético de las estimaciones convencionales de FRAX en torno a la probabilidad de fractura en individuos expuestos a dosis altas de glucocorticoides orales: una revisión al alza de 15 % para la probabilidad de FOM y de 20 % para la de fractura de cadera (es decir, multiplicando la probabilidad de salida por 1.15 y 1.20 respectivamente).79
Diabetes mellitus tipo 2
La diabetes mellitus tipo 2 (DMT2) es un factor de riesgo de sufrir fracturas osteoporóticas; a pesar de estar asociada a una mayor DMO, FRAX subestima este riesgo.80,81 Se han propuesto varios ajustes para mejorar el rendimiento de FRAX en pacientes con DMT2: usar la entrada de artritis reumatoide como un sustituto para el efecto de DMT2; usar el ajuste de la puntuación del hueso trabecular; reducir la t-T del cuello femoral en 0.5 DE; o aumentar la entrada de edad en FRAX en 10 años. Aunque ninguno por sí solo fue óptimo para todos los resultados de fractura y duraciones de DMT2, se demostró que el uso de la entrada de artritis reumatoide era bastante eficaz para mejorar el rendimiento de FRAX en la predicción de FOM y fracturas de cadera,82 y resultó ser el de aplicación más simple en la clínica. Las probabilidades de FRAX también se pueden ajustar en función de la historia de DMT2, con una mayor duración de la enfermedad asociada a un mayor riesgo de fractura.82
Historial de caídas
El historial de caídas no se incorporó al modelo FRAX en el momento de su desarrollo por varias razones: falta de datos uniformemente fiables sobre el historial de caídas,83 evidencia insuficiente que avalara la contribución del riesgo de caídas a la predicción del riesgo de fractura,84-86 y preocupación por la posibilidad de que el riesgo de fractura atribuible al riesgo de caídas no fuese susceptible de tratamiento farmacológico.87 Desde entonces, ha quedado demostrado que, además de los FRC, la valoración del riesgo de caídas mejora la predicción de fracturas tanto de FRAX y DMO, independientemente del sexo.88,89
También ha quedado demostrado que las intervenciones dirigidas al hueso reducen el riesgo de fractura en pacientes con historial de caídas.62,63,90,91 Un informe previo del Grupo de Trabajo de Sociedad Internacional de Densitometría Clínica y la Fundación Internacional de Osteoporosis sugirió la aplicación de un factor de multiplicación de 1.3 a la probabilidad de fractura de cadera de FRAX por cada caída pasada (hasta cinco caídas).83 El análisis de la cohorte de Manitoba proporcionó datos para el ajuste de las probabilidades de FRAX con base en el número de caídas durante el año anterior y la edad (Tabla 2).92
Tabla 2 Razones de probabilidad para una fractura osteoporótica mayor y fractura de cadera en hombres y mujeres, según edad, número de caídas descritas, tanto en ausencia de entrada de la densidad mineral ósea en FRAX como cuando se incorpora la densidad mineral ósea
| Edad | Sin caídas | 1 caída | 2 caídas | ≥ 3 caídas | ||||
|---|---|---|---|---|---|---|---|---|
| FOM | FC | FOM | FC | FOM | FC | FOM | FC | |
| En ausencia de DMO | ||||||||
| 40 | 0.90 | 0.89 | 1.23 | 1.28 | 1.54 | 1.71 | 2.02 | 2.57 |
| 45 | 0.90 | 0.89 | 1.23 | 1.28 | 1.53 | 1.70 | 2.01 | 2.56 |
| 50 | 0.90 | 0.89 | 1.23 | 1.27 | 1.51 | 1.67 | 1.96 | 2.51 |
| 55 | 0.91 | 0.89 | 1.22 | 1.27 | 1.48 | 1.64 | 1.91 | 2.43 |
| 60 | 0.91 | 0.90 | 1.21 | 1.26 | 1.43 | 1.58 | 1.83 | 2.32 |
| 65 | 0.91 | 0.90 | 1.20 | 1.25 | 1.36 | 1.51 | 1.71 | 2.18 |
| 70 | 0.92 | 0.90 | 1.19 | 1.24 | 1.30 | 1.40 | 1.63 | 1.95 |
| 75 | 0.92 | 0.91 | 1.18 | 1.21 | 1.22 | 1.28 | 1.52 | 1.72 |
| 80 | 0.93 | 0.92 | 1.16 | 1.19 | 1.15 | 1.20 | 1.41 | 1.56 |
| 85 | 0.93 | 0.93 | 1.15 | 1.17 | 1.10 | 1.13 | 1.33 | 1.43 |
| 90 | 0.94 | 0.93 | 1.14 | 1.16 | 1.10 | 1.13 | 1.32 | 1.41 |
| Cuando se incorpora DMO | ||||||||
| 40 | 0.92 | 0.91 | 1.19 | 1.21 | 1.46 | 1.54 | 1.88 | 2.24 |
| 45 | 0.92 | 0.90 | 1.20 | 1.22 | 1.47 | 1.55 | 1.91 | 2.28 |
| 50 | 0.92 | 0.90 | 1.20 | 1.22 | 1.45 | 1.54 | 1.88 | 2.26 |
| 55 | 0.92 | 0.90 | 1.19 | 1.22 | 1.43 | 1.52 | 1.84 | 2.22 |
| 60 | 0.92 | 0.91 | 1.19 | 1.21 | 1.39 | 1.48 | 1.77 | 2.15 |
| 65 | 0.92 | 0.91 | 1.18 | 1.22 | 1.34 | 1.44 | 1.68 | 2.06 |
| 70 | 0.92 | 0.91 | 1.18 | 1.20 | 1.29 | 1.35 | 1.62 | 1.90 |
| 75 | 0.92 | 0.91 | 1.18 | 1.19 | 1.23 | 1.27 | 1.54 | 1.74 |
| 80 | 0.92 | 0.92 | 1.17 | 1.19 | 1.17 | 1.20 | 1.45 | 1.62 |
| 85 | 0.93 | 0.92 | 1.17 | 1.18 | 1.12 | 1.14 | 1.38 | 1.51 |
| 90 | 0.93 | 0.92 | 1.17 | 1.18 | 1.12 | 1.15 | 1.39 | 1.52 |
DMO: densidad mineral ósea; FC: fractura de cadera; FOM: fractura osteoporótica mayor. Tabla reproducida con la amable autorización de Springer Science and Business Media.92
Datos concurrentes sobre la DMO de la columna lumbar
Tal como se mencionó, la inclusión de la DMO del cuello femoral en el cálculo de FRAX mejora la predicción del riesgo de fractura más allá de los datos que proporcionan los FRC. El uso preferencial de la DMO del cuello femoral sobre las mediciones de otras localizaciones se relaciona principalmente con su amplia disponibilidad en las cohortes utilizadas para el desarrollo de FRAX. Además, la DMO del cuello femoral está asociada a un mayor gradiente de riesgo para fractura de cadera que las mediciones de la DMO en otros sitios esqueléticos, con una predicción similar o mejor de FOM cuando se hace un ajuste apropiado.93,94 No obstante, existen casos en los que puede ocurrir una gran discordancia en los T-scores del cuello femoral con las de la columna lumbar, y tener lo anterior en cuenta puede mejorar la precisión de la predicción del riesgo.95-97
El análisis de múltiples cohortes internacionales encontró que la discordancia en los T-scores de la DMO del cuello femoral y columna lumbar contribuye al riesgo de fractura con independencia de las probabilidades de FRAX que incorporan solo DMO del cuello femoral.98 En general, cuando el T-score de la DMO de la columna lumbar es menor que el T-score de la DMO del cuello femoral entre 1 y 2 DE, así como entre 2 y 3 DE, la probabilidad de FOM se incrementa 10 y 20 %, respectivamente, con una disminución correspondiente en la probabilidad de FOM cuando el T-score de la DMO de la columna lumbar es mayor que la del cuello femoral. Un ajuste más refinado de las diferencias en la DMO se incluye en FRAXplus.
Puntuación del hueso trabecular
La puntuación del hueso trabecular es una herramienta analítica que realiza mediciones novedosas de textura de nivel de gris en imágenes de densitometría de la columna lumbar, capturando así información relacionada con la microarquitectura trabecular.99 Una puntuación del hueso trabecular baja es un predictor de riesgo de fractura independientemente de FRAX y DMO del cuello femoral.100,101 Los datos de la cohorte de Manitoba se han utilizado para derivar un factor de ajuste para las probabilidades de FRAX al tener en cuenta la puntuación del hueso trabecular.102 La validez de este ajuste se exploró más a fondo en un metaanálisis de 14 cohortes (en el que se excluyó la cohorte de Manitoba), que mostró que la puntuación del hueso trabecular era un predictor significativo e independiente de fractura.103 Una revisión reciente confirma la contribución independiente de la puntuación del hueso trabecular a la predicción de fractura.99
Longitud del eje de la cadera
La longitud del eje de la cadera, definida como la distancia desde la base del trocánter mayor hasta el borde interno de la pelvis, se puede obtener de los informes de la densitometría. Una longitud del eje de la cadera más extensa que la media se asocia a un mayor riesgo de fractura de cadera con independencia del sexo, con datos de la cohorte de Manitoba que muestran un incremento relativo en la probabilidad de fractura de cadera de 4.7 % y una disminución de 3.8 % por cada milímetro que la longitud del eje de la cadera esté por encima y por debajo de la media específica para cada sexo, respectivamente.104
FRAXplus
Aunque algunos ajustes aritméticos para las estimaciones convencionales de FRAX de la probabilidad de fractura descritos se han simplificado para facilitar la aplicación clínica, los algoritmos basados en la web permiten que estos ajustes se realicen con mayor precisión y facilidad. FRAXplus (https://www.fraxplus.org) permite la modulación de la salida de FRAX para la recencia de la fractura osteoporótica, la alta exposición a glucocorticoides orales, la duración de la DMT2, el número de caídas en el año anterior, la información concurrente sobre la columna lumbar, la puntuación del hueso trabecular y la longitud del eje de la cadera. A nivel poblacional, la aplicación de estos ajustes podría resultar en la reclasificación de individuos en relación con los umbrales para la intervención, incluida la reclasificación entre alto y muy alto riesgo, afectando así las decisiones terapéuticas. Una advertencia importante para el uso de FRAXplus es que no existe una base de evidencia disponible para informar sobre la precisión de múltiples ajustes; una medida pragmática sería seleccionar el factor más dominante, es decir, el que probablemente tenga la mayor relevancia clínica para la probabilidad estimada.
Actualización de FRAX
Una actualización planificada de FRAX ha identificado 64 cohortes elegibles, que comprenden 2 138 428 participantes (69 % mujeres) seguidos durante aproximadamente 20 millones de personas-años, con 116 117 fracturas osteoporóticas mayores documentadas.109 La mayor población de análisis, la mayor representación de hombres y el mayor tiempo de seguimiento aumentarán la aplicabilidad general de la herramienta y mejorarán la caracterización de factores de riesgo clínicos existentes y nuevos para la fractura, con exploración de diferencias dependientes del sexo, efectos dependientes del tiempo, efectos de etnicidad (cuando sea posible) y términos de interacción. Se han completado dos metaanálisis y otros están en progreso.110,111
Conclusiones
FRAX, herramienta de evaluación del riesgo de fractura, proporciona algoritmos específicos por país para estimar la probabilidad individualizada a 10 años de FOM y fracturas de cadera con base en FRC y DMO, y mejora la toma de decisiones en el manejo de la osteoporosis en comparación con el uso de solo DMO. La relación entre las probabilidades de FRAX y la eficacia del tratamiento está bien establecida y se espera que influya aún más en las guías de tratamiento en el futuro. El sitio web FRAXplus facilita la consideración de escenarios clínicos importantes, donde los ajustes en las probabilidades de FRAX afectarán la evaluación y las decisiones de tratamiento.











 nueva página del texto (beta)
nueva página del texto (beta)


