ANTECEDENTES
Los errores innatos de la inmunidad se originan por mutaciones monogénicas que deben considerarse en el diagnóstico diferencial de pacientes con infecciones recurrentes o graves, alergias, autoinmunidad, enfermedades autoinflamatorias, insuficiencia de médula ósea y malignidad.12 Dentro de los errores innatos de la inmunidad, la deficiencia de anticuerpos es la más frecuente y de éstas la deficiencia selectiva de IgA es la más común.2345
La incidencia estimada de deficiencia selectiva de IgA varía de 1 en 300 a 700 sujetos norteamericanos caucásicos, en Brasil se reporta en donadores de sangre en 1 de cada 965, mientras que en Asia es de 1 en 18,000 casos.345 El antecedente familiar de deficiencia selectiva de IgA o inmunodeficiencia común variable (IDCV) es del 20 a 25% de los sujetos afectados de la misma familia. La prevalencia de deficiencia selectiva de IgA puede ser más alta en hombres.3 Estas variaciones apoyan la predisposición genética.4
La IgA es el isotipo más abundante producido en humanos, desempeña un papel decisivo en la respuesta inmunológica a nivel sistémico y de las mucosas, y aunque su función sérica en la respuesta inmune sistémica no se comprende completamente, existe un defecto fundamental en pacientes con deficiencia selectiva de IgA: incapacidad de los linfocitos B portadores de IgA para madurar en células plasmáticas secretoras de IgA, incluso se desconoce la razón de esta falla. El análisis de ligamiento genético indica que el locus HLA-DQ/DR supone el determinante hereditario más importante de susceptibilidad para padecer deficiencia selectiva de IgA.5
La causa molecular de la deficiencia selectiva de IgA no se ha descrito claramente. Los estudios genéticos implican una base multifactorial, que incluye contribuciones de diversos loci MHC y no MHC. En algunos casos las deleciones genéticas a gran escala, como el síndrome de deleción 18q, se han asociado con otras anomalías (deficiencia de IgG4) y manifestaciones autoinmunes (diabetes o tiroiditis).3
El diagnóstico de deficiencia selectiva de IgA se establece a partir de los 4 años de edad, con concentraciones de IgA menores de 7 mg/dL, e IgG e IgM normales, y se excluyen otras causas de hipogammaglobulinemia. Estos pacientes tienen respuesta normal de anticuerpos IgG vacunales.234
La mayoría de los pacientes con este tipo de inmunodeficiencia no manifiestan síntomas; sin embargo, algunos padecen infecciones recurrentes, malignidad, enfermedades autoinmunes y alergias, por lo que se sugiere vigilancia constante, debido a la posible ocurrencia de complicaciones.345
Diversos estudios indican que el diagnóstico de deficiencia selectiva de IgA debe confirmarse después de los 4 años de edad, porque la etapa de maduración de los plasmocitos culmina en este periodo.6
A continuación se informa el caso de un paciente con deficiencia selectiva de IgA, sugerente de la enfermedad desde los 2 años, con neumonía necrosante y hallazgos de laboratorio compatibles con la enfermedad.
REPORTE DE CASO
Paciente pediátrico de 4 años, de género masculino, con diagnóstico inicial sugerente de algún error innato de la inmunidad a partir de los 2 años y 9 meses de edad; antecedentes familiares: padres sanos, sin antecedentes de familiares con errores innatos de la inmunidad. Peso y talla bajos al nacimiento (2200 kg, percentil < 3; 43 cm, percentil <3), alimentación con leche materna y fórmula láctea hasta el año de vida; introducción de alimentos sólidos a los 6 meses, y esquema de vacunación completo. En la valoración inicial se encontraron peso, talla y perímetro cefálico adecuados para la edad y el género (peso/edad 92.8%, talla/edad 95.5%, peso/talla 100%).
A los 2 años de edad tuvo fiebre de 39°C de difícil control. Al cuarto día de persistencia del cuadro clínico, los estudios de laboratorio informaron trombocitosis y leucocitosis a expensas de neutrofilia; la radiografía de tórax reveló consolidación pulmonar izquierda; presentó exacerbación de los síntomas, con dificultad respiratoria y taquicardia, por lo que se decidió su ingreso hospitalario. La tomografía simple de tórax demostró bulas en el ápice izquierdo y derrame pleural ipsilateral. Al séptimo día continuó sin mejoría clínica, por lo que se practicó toracoscopia y decorticación, y se modificó el esquema de tratamiento, de ceftriaxona a vancomicina-meropenem. Se solicitó una nueva tomografía de tórax que reportó cavitación necrosante del lóbulo superior izquierdo, por lo que se realizó lobectomía.
El reporte histopatológico del tejido pulmonar advirtió infiltrados celulares y vasculares, compatibles con un proceso neumónico y necrosis (Figura 1 y 2). El cultivo de la biopsia pulmonar identificó Streptococcus salivarius y Streptococcus viridans. Luego de 18 días de hospitalización egresó por mejoría clínica.
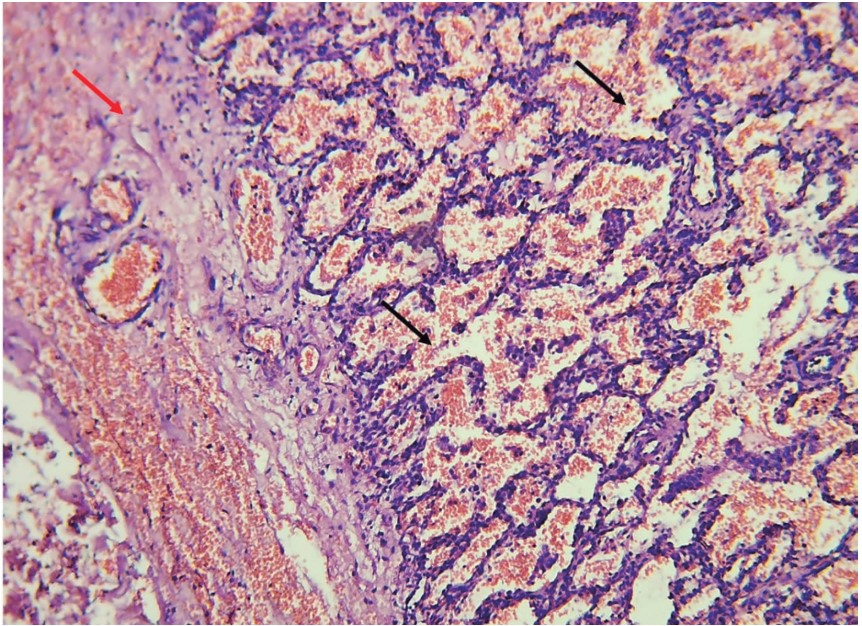
Figura 1 Figura 1. Imagen microscópica teñida con H&E en panorámica (4x) que muestra zonas periféricas del proceso neumónico. Observe los espacios alveolares con extensa hemorragia reciente (flechas negras), adyacente a una de engrosamiento pleural con congestión vascular (flecha roja).
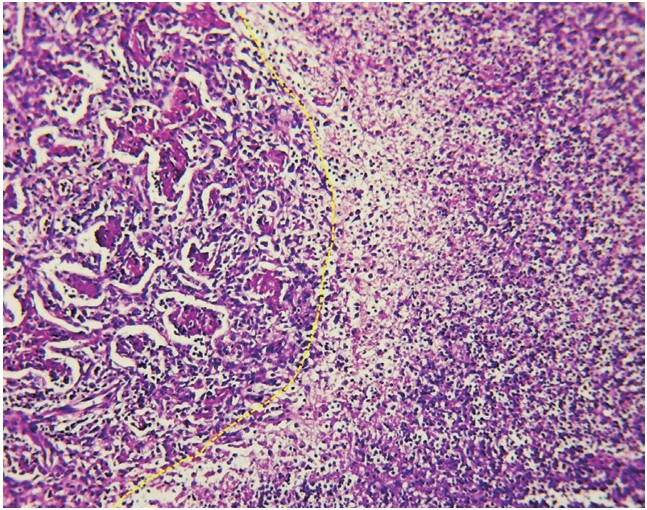
Figura 2 Figura 2. Imagen microscópica con H&E en seco débil (10x) en donde se puede apreciar una zona de transición del proceso neumónico entre zonas de neumonía en vías de organización (lado izquierdo) y zonas necrotizantes de la misma (lado derecho). Observe la pérdida de arquitectura alveolar en la zona necrótica y los agregados fibrinoides intraalveolares de la zona en organización.
En el seguimiento del paciente se identificaron datos clínicos de rinitis persistente. Se realizó el abordaje diagnóstico de errores innatos de la inmunidad. La determinación de inmunoglobulinas séricas reportó IgA por debajo de los valores de referencia para la edad, aunado a IgE elevada, IgG e IgM dentro de parámetros normales. Después de 5 meses de hospitalización se encontraron biometría hemática y subpoblaciones de linfocitos normales para la edad, persistencia baja de los valores de IgA, y disminución de ambos subtipos IgA1 e IgA2, e IgE persistentemente elevada.Cuadros1y2
Cuadro 1. Resultados de la determinación de inmunoglobulinas séricas y subclases
| Determinación de inmunoglobulinas | Hospitalización A los 2 años de edad | 5º mes de egreso | 4º año de vida | Valores de referencia | |
|---|---|---|---|---|---|
| IgA | mg/dL | 5 | <5 | 5.5 | 15 - 118 |
| IgD | mg/dL | 5.7 | - | - | 4.8 - 41 |
| IgE | UI/mL | 577.1 | 443 | 3 - 19.5 | |
| IgG | mg/dL | 864 | 948 | 369 - 1204 | |
| IgM | mg/dL | 103 | - | 35 - 80 | |
| Subclases de inmunoglobulinas | |||||
| IgA 1 | mg/L | 541 | 541 | 1670 - 3770 | |
| IgA 2 | mg/L | 55.5 | 55.5 | 255 - 969 | |
| IgG 1 | mg/L | 6,110 | 1940 - 8490 | ||
| IgG 2 | mg/L | 2,370 | 225 - 3000 | ||
| IgG 3 | mg/L | 185 | 186 - 853 | ||
| IgG 4 | mg/L | 63 | 5 - 784 | ||
Cuadro 2. Resultados de la determinación de subpoblaciones de linfocitos luego de la hospitalización
| Linfocito | Resultado | Valor de referencia | |
|---|---|---|---|
| Linfocitos T | % | 59.13 | 56 - 75 |
| CD3 + | cel/mL | 3,364 | 1,400 - 3,700 |
| Linfocitos T CD4 | % | 34.86 | 28 - 47 |
| CD3+/CD4+/CD8- | cel/mL | 1,983 | 700 - 2,200 |
| Linfocitos T CD8 | % | 17.88 | 16 - 30 |
| CD3+/CD4-/CD8+ | cel/mL | 1,017 | 490 - 1,300 |
| Relación CD4/CD8 | razón | 1.95 | 1.20 - 6.20 |
| Linfocitos B | % | 27.84 | 14 - 33 |
| CD19+ | cel/mL | 1,587 | 390 - 1,400 |
| CD20+ | cel/mL | 1,587 | 430 - 3,300 |
| NK | cel/mL | 10.68 | 4 - 17 |
| CD3-/CD16+/CD56+ | cel/mL | 608 | 130 - 720 |
Debido a la concentración alta de IgE sérica total y manifestación de síntomas nasales, se realizó la determinación de IgE específica para aeroalérgenos con la técnica de ImmunoCAP, con resultado positivo para caspa de perro 2.05 kUA/L y de gato 37.19 kUA/L (valores de referencia ≤ 0.1 kUA/L).
Se evaluó la respuesta del paciente para generar anticuerpos anti-polisacáridos para S. pneumoniae. Con esta prueba se midieron las concentraciones de IgG específica para cada serotipo de la vacuna polisacárida 23 valente y posteriormente se administró al paciente. Cuatro semanas después se midieron nuevamente los valores específicos de IgG y se obtuvo una respuesta adecuada, con elevación mayor del 50% de los anticuerpos IgG >1.3 mg/mL.Cuadro 3
Cuadro 3. Resultados de la medición de anticuerpos IgG específicos basales y posterior a la vacuna neumocócica polisacárida (PPSV23)
| Anticuerpos IgG, Streptococcus pneumoniae | ||||
|---|---|---|---|---|
| Serotipo | Resultados Antes de la prueba | Resultados después de la prueba | Valor de referencia | |
| 1 | mg/mL | 0.4 | 64 | >2.3 |
| 2 | mg/mL | <0.3 | 4.7 | >1.0 |
| 3 | mg/mL | 0.3 | 16.9 | >1.8 |
| 4 | mg/mL | <0.3 | >28.0 | >0.6 |
| 5 | mg/mL | 0.9 | 32.1 | >10.7 |
| 8 | mg/mL | 0.5 | 15.6 | >2.9 |
| 9N | mg/mL | 0.7 | 17.1 | >9.2 |
| 12F | mg/mL | <0.3 | 0.8 | >0.6 |
| 14 | mg/mL | 0.8 | 16.7 | >7.0 |
| 17F | mg/mL | 3.9 | 14.1 | >7.8 |
| 19F | mg/mL | 5.7 | >139.0 | >15.0 |
| 20 | mg/mL | 1.0 | 4.0 | >1.3 |
| 22F | mg/mL | <0.3 | 2.3 | >7.2 |
| 23F | mg/mL | 2.2 | 49.1 | >8.0 |
| 6B | mg/mL | 0.9 | 77.9 | >4.7 |
| 10A | mg/mL | <0.3 | 3.9 | >2.9 |
| 11A | mg/mL | <0.3 | 7.7 | >2.4 |
| 7F | mg/mL | <0.3 | 17.5 | >3.2 |
| 15B | mg/mL | <0.3 | 1.0 | >3.3 |
| 18C | mg/mL | <0.3 | 15.5 | >3.3 |
| 19A | mg/mL | 30.6 | 32.1 | >17.1 |
| 9V | mg/mL | <0.3 | 27.8 | >2.6 |
| 33F | mg/mL | 0.4 | 1.9 | >1.7 |
La nueva determinación de IgA sérica, llevada a acabo a los 4 años de edad, informó persistencia baja (5.5 mg/dL). Actualmente el paciente se encuentra con datos clínicos de rinitis alérgica, sin procesos infecciosos adicionales graves.
DISCUSIÓN
En el paciente de este estudio se inició el abordaje diagnóstico de errores innatos de la inmunidad desde los 2 años y 9 meses de edad, debido a una infección pulmonar grave, donde se aislaron patógenos de baja virulencia, además de enfermedad alérgica.
Hasta hace poco se calculaba que el 90% de los pacientes con deficiencia selectiva de IgA permanecen asintomáticos; sin embargo, un seguimiento a largo plazo de donantes de sangre con este tipo de deficiencia demostró que el 80% manifiestan síntomas por el resto de su vida.46
Se estima que un tercio de los pacientes sintomáticos con deficiencia selectiva de IgA experimentan infecciones recurrentes, por ejemplo: infecciones virales, otitis media, infecciones sinopulmonares y gastrointestinales.3 Las infecciones son más frecuentes en sujetos con deficiencia selectiva de IgA relacionadas con deficiencia de la subclase de IgG2.4 Además, tienen riesgo elevado de padecer enfermedades autoinmunes (lupus eritematoso sistémico, artritis), desórdenes hematológicos (neutropenia y trombocitopenia) y enfermedades gastrointestinales (enfermedad de Crohn, colitis ulcerativa y enfermedad celiaca). Los pacientes con deficiencia selectiva de IgA también tienen alto riesgo de malignidad gastrointestinal y linfoidea a futuro, incluso mayor prevalencia de alergias y asma, y se consideran pacientes de riesgo para sufrir reacciones anafilácticas a productos sanguíneos, debido a la posible ocurrencia de anticuerpos anti-IgA; sin embargo, el riesgo por individuo es poco claro y algunos centros realizan lavados al producto previo a la transfusión. Todas estas posibles complicaciones sugieren que estos pacientes deben mantenerse en vigilancia clínica e inmunológica estrecha a largo plazo.35
Respecto a la frecuencia de complicaciones, se ha encontrado que los pacientes inician con alergia (25-50%), autoinmunidad (5-30%), alteraciones gastrointestinales (enfermedad celiaca [2-3%]), malignidad (<2%) o infecciones recurrentes (40-90%).7 Un estudio emprendido en 330 pacientes pediátricos con IgA menor de 50 mg/L, que evaluó la frecuencia de enfermedades infecciosas, reportó neumonía (6%), sinusitis (17.5%) y otitis media (11.8%) entre las manifestaciones más frecuentes.4 Además, algunos pacientes sometidos a un estudio inmunológico más amplio manifestaron otro defecto humoral más grave: deficiencia de las subclases de IgG o inmunodeficiencia común variable.4, 7 Las alteraciones respiratorias son más comunes que las gastrointestinales, debido al aumento compensatorio de IgM secretora, principalmente en el conducto gastrointestinal que en el respiratorio.8
Se ha reportado que esta deficiencia puede desaparecer en la adolescencia en algunos pacientes, debido a la maduración tardía de los plasmocitos secretores de IgA.9 Aunque el mecanismo fisiopatológico no está bien dilucidado, se describe que puede ser producto de la reducción de la vida media o de alteraciones en la maduración de los plasmocitos secretores de IgA, defectos en el cambio de isotipo de inmunoglobulinas, ausencia de efecto de algunas citocinas (IL-21, IL-4, IL-10, TGFb), entre otros mecanismos propuestos.4, 7
La respuesta de anticuerpos para serotipos de S. pneumoniae se estudió en el caso aquí expuesto, porque la deficiencia selectiva de anticuerpos puede coexistir con la deficiencia selectiva de IgA, incluso puede ser una alternativa diagnóstica por la neumonía necrosante.
Si bien se ha descrito que el diagnóstico de deficiencia selectiva de IgA se establece a partir de los 4 años de vida, la complicación de una neumonía necrosante causada por bacterias de baja virulencia fue sugerente de la presencia de errores innatos de la inmunidad, pues el paciente comparte diversos criterios clínicos de la deficiencia selectiva de IgA, según la recopilación de datos en la bibliografía, y reporto valores de IgG e IgM normales, e IgE elevada con evidencia de enfermedad alérgica. Cuadro 4
Cuadro 4. Fenotipo clásico de inmunodeficiencia selectiva de IgA y fenotipo del caso expuesto
| Variables | Inmunodeficiencia selectiva de IgA | Paciente |
|---|---|---|
| Edad al momento del diagnóstico (4 años) | + | + |
| IgA < 7 mg/dL | + | + |
| IgG e IgM séricas normales o elevadas | + | + |
| IgE elevada | +/- | + |
| Alguna subclase de IgG disminuida | +/- | - |
| Población de linfocitos normales | + | + |
| Infecciones respiratorias frecuentes | +/- | + |
| Alteraciones gastrointestinales recurrentes | +/- | - |
| Enfermedad alérgica | +/- | + |
| Enfermedad autoinmune, malignidad | +/- | - |
Lo referente a la edad del diagnóstico, se sugiere esperar hasta los 4 años de edad en diferentes publicaciones; sin embargo, se sabe poco acerca de la carga de la enfermedad en niños con deficiencia de IgA menores de esta edad.10 Aunque el diagnóstico definitivo se establece a la edad mencionada, los pacientes con IgA por debajo de 7 mg/dL antes cumplir 4 años pueden persistir con concentraciones bajas de IgA.
Hasta el momento no existe tratamiento definitivo para la deficiencia selectiva de IgA, algunos pacientes con infecciones sinopulmonares recurrentes pueden beneficiarse de antibióticos profilácticos a largo plazo. La terapia de reemplazo con IgG aún se discute. La mayoría de los pacientes tienen mínima mejoría clínica. La evidencia de producción de anticuerpos alterada puede soportar su prescripción, incluso en pacientes con infecciones recurrentes que afectan negativamente su calidad de vida y en quienes fallan los tratamientos agresivos con antibióticos y profilaxis, o quienes sufren efectos adversos intolerables o hipersensibilidad a este tipo de fármacos.3
El seguimiento de pacientes que no manifiestan síntomas puede ser anual o bianual hasta los 10 años (fase de maduración del sistema inmune) y posteriormente cada 2 a 5 años; los estudios deben incluir hemograma, velocidad de sedimentación globular, determinación de inmunoglobulinas, subclases de IgG y anticuerpos anti-nucleares, y evaluar la respuesta de anticuerpos si la evolución del paciente lo indica, enfocándose en el despistaje de comorbilidades para el diagnóstico precoz, que minimice el riesgo de complicaciones.4
La deficiencia selectiva de IgA es una enfermedad de por vida; sin embargo, se han reportado casos excepcionales con recuperación espontánea, especialmente en pacientes jóvenes. Otros estudios no evidencian normalización de los valores de IgA en pacientes pediátricos o en donantes de sangre adultos con esta deficiencia, durante periodos de seguimiento que abarcan hasta 19 años.5
En la actualidad, el paciente de este caso se encuentra estable, los padres no aceptaron realizar el estudio genético, que aunque se realiza la secuenciación de exoma completo existe la posibilidad de no identificar la variante patológica que explique la deficiencia de IgA. Respecto a la neumonía necrosante grave, también puede manifestarse en pacientes con valores normales de inmunoglobulinas séricas.
El paciente no ha requerido tratamiento profiláctico con antibióticos ni de reemplazo con gammaglobulina; se mantiene en vigilancia clínica y con estudios de laboratorio anuales, debido a las posibles complicaciones que conlleva la enfermedad.
CONCLUSIONES
El personal médico debe considerar la deficiencia de IgA en niños pequeños como una condición clínicamente relevante. Las mediciones séricas de IgA deben formar parte de la evaluación diagnóstica de rutina en niños que sufren infecciones respiratorias recurrentes o graves. Los estudios pueden iniciar a partir de los dos años de edad y considerar a los pacientes portadores de deficiencia selectiva de IgA cuando se reporten concentraciones menores de 7 mg/dL y se hayan descartado otras alteraciones inmunológicas, como sucedió en nuestro caso. Se sugiere el seguimiento clínico e inmunológico estrecho, previniendo las posibles complicaciones a partir de su perfil.
















