Introducción
La insuficiencia hepática aguda es una entidad poco frecuente, la cual se presenta con rápido deterioro de la función hepática, asociado con presencia de coagulopatía y encefalopatía, en pacientes previamente sanos. En México carecemos de estadísticas epidemiológicas concretas; sin embargo, en los Estados Unidos se calculan más de 2,000 muertes anuales secundarias a insuficiencia hepática aguda. Dentro de las principales etiologías asociadas se encuentran: toxicidad asociada a fármacos, hepatitis virales, tóxicos, autoinmunes y asociadas a hipoperfusión hepática y estado de choque.1-5
Existen varias formas de clasificarla, pero la clasificación de O’grady es la más utilizada. El tratamiento va desde medidas farmacológicas y terapias de soporte extracorpóreo, pudiendo llegar hasta el trasplante hepático.6-11 Con el advenimiento de estas nuevas medidas de soporte hepático, se han realizado diversos estudios con la finalidad de evaluar su uso en comparación con las medidas farmacológicas.12-16
El tratamiento requiere de conocer la causa y de establecer rápido las medidas de soporte multiorgánico necesarias para evitar el riesgo de daño a otros órganos, como el inicio rápido de N-acetilcisteína y medidas antiamonio, como la necesidad de terapias de recambio plasmático de alto volumen con la finalidad de eliminar las sustancias que normalmente serian detoxificadas por el hígado y reponer algunas de las sustancias de síntesis hepática en caso de ser necesario, sin dejar de lado que pueden llegar a requerir de trasplante hepático.5,17-21
Material y métodos
En el estudio se incluyeron pacientes mayores de 18 años, que ingresaron a la Unidad de Cuidados Intensivos (UCI) con diagnóstico de falla hepática aguda. Se utilizó como herramienta la base de datos de la Unidad, donde se especifican: datos antropométricos, bioquímica sanguínea, diagnostico etiológico, escalas de falla hepática, mortalidad, días de estancia, días de uso de ventilación mecánica y uso de terapia extracorpórea. La base de datos abarca el período del 1 de enero de 2018 al 1 de septiembre de 2023. La terapia extracorpórea analizada fue plasmaféresis de alto volumen otorgada por la maquina Specta Optia Apheresis System (Terumo BCT ® ).
Diseño: estudio longitudinal, retrospectivo y analítico. Lugar donde se desarrolló el estudio: Unidad de Cuidados Intensivos Adultos. Población: pacientes con falla hepática aguda ingresados a la Unidad de Terapia Intensiva (UTI) en el periodo 2018-2023. Criterios de inclusión: pacientes de uno u otro sexo. Edades mayor o igual a 18 años y menor o igual a 60 años. Diagnóstico de falla hepática hiperaguda o aguda según la clasificación de O’Grady. Criterios de eliminación: pacientes con evidencia de infección crónica con virus HVB, HVC o HIV durante su hospitalización. Mujeres embarazadas. Criterios de exclusión: datos incompletos o dudosos en la base de datos.
Resultados
Se incluyeron un total de 20 pacientes. La media de edad fue 29.2 ± 8.7 años. Género masculino 12 (60%). Media de IMC 27 (3.6). Mediana de APACHE II 17.5 (rango 10-24.5), mediana de SOFA 7 (rango 6-9.7), mediana de KING COLLEGE 2 (rango 1-3), media de MELD SCORE 35.9 (6.9). Mediana de días UTI tres (rango 1-6.5), mediana de días ventilación mecánica 1.5 (rango 0-3). Media de creatinina 1.7 (0.57), mediana de lactato 7.61 (rango 2.7-10.7), mediana de bilirrubina 14.6 (rango 8.2-15.7), mediana de INR 4.7 (rango 2.9-6.8), más detalles en la Tabla 1.22
Tabla 1: Características generales de la población (N = 20).
| Características | n (%) |
|---|---|
| Género masculino | 12 (60) |
| Edad (años)* | 29.2 ± 8.7 |
| Índice de masa corporal* | 27 ± 3.6 |
| Escalas de severidad | |
| APACHE II‡ | 17.5 [10-24.5] |
| SOFA‡ | 7 [6-9.7] |
| KING COLLEGE‡ | 2 [1-3] |
| MELD SCORE* | 35.9 ± 6.9 |
| % MELD SCORE* | 65 ± 11.9 |
| Encefalopatía hepática‡ | 2.5 [0.25-4] |
| Días UTI‡ | 3 [1-6.5] |
| Días VM‡ | 1.5 [0-3] |
| Ventilación mecánica invasiva | 14 (70) |
| Vasopresor | |
| Norepinefrina | 18 (90) |
| Balance hídrico | |
| Neutro | 7 (35) |
| Positivo | 12 (60) |
| Negativo | 1 (5) |
| Creatinina* | 1.7 ± 0.57 |
| Lactato‡ | 7.61 [2.7-10.7] |
| Bilirrubina total‡ | 14.6 [8.2-15.7] |
| INR‡ | 4.7 [2.9-6.8] |
| DHL‡ | 542 [363-1,446] |
| TGO‡ | 1,527 [539-3,028] |
| TGP‡ | 2,706 [427-5,793] |
| Na* | 136 ± 6.5 |
| Diagnóstico de ingreso | |
| Falla hepática hiperaguda | 19 (95) |
| Falla hepática subaguda | 1 (5) |
| Etiología | |
| DILI | 4 (20) |
| Hepatitis A | 10 (50) |
| Hepatitis isquémica | 2 (10) |
| LLA | 1 (5) |
| Micetismo | 3 (15) |
| Soporte extracorpóreo | 8 (40) |
| Mortalidad a 30 días | 7 (35) |
| Trasplante | 1 (5) |
| LRA | 19 (95) |
| Traslado | 4 (20) |
| Tipo de terapia extracorpórea | |
| No aplica | 10 (50) |
| No | 2 (10) |
| Plasmaféresis | 8 (40) |
DHL = deshidrogenasa láctica. DILI = daño hepático inducido por medicamentos (drug-induced liver injury). INR = international normalized ratio (índice internacional normalizado). LLA = leucemia linfoblástica aguda. LRA = lesión renal aguda.
TGO = transaminasa glutamicooxalacética (o aspartato aminotransferasa [AST]). TGP = transaminasa glutamicopirúvica (o alanina aminotransferasa [ALT]).
UTI = Unidad de Terapia Intensiva. VM = ventilación mecánica.
* Valores expresados en media ± desviación estándar.
‡ Valores expresados en mediana y [rango intercuartil].
Se realizó un análisis bivariado entre mortalidad de acuerdo a la característica de la población. Se encontraron algunas variables con significancia, siendo las escalas de severidad, APACHE II con p = 0.024, SOFA con p = 0.010 para ambos grupos; la cifra de días UTI fue mayor para los sobrevivientes con mediana de 4.5 (rango 1-10.2), comparada frente al grupo de mortalidad mediana de 2 (rango 1-4), con p = 0.037, más detalles en la Tabla 2.
Tabla 2: Análisis bivariado entre mortalidad con las características dividido en dos grupos: supervivientes y mortalidad.
| Características | Supervivientes (N =13) n (%) |
Mortalidad (N = 7) n (%) |
p |
|---|---|---|---|
| Género masculino | 6 (60.0) | 6 (85.7) | 0.251 |
| Edad (años)* | 27.7 ± 5.5 | 31 ± 8.6 | 0.430 |
| Índice de masa corporal* | 26 ± 2.7 | 28 ± 5.1 | 0.336 |
| Escalas de severidad | |||
| APACHE II‡ | 13 [8.2-18.2] | 20.2 [11-26] | 0.024 |
| SOFA‡ | 7 [5.2-7.2] | 11 [6-18] | 0.010 |
| KING COLLEGE | |||
| 1 | 5 (38.4) | 2 (28.6) | 0.032 |
| 2 | 4 (30.7) | 1 (14.3) | |
| 3 | 4 (30.7) | 4 (57.1) | |
| MELD SCORE* | 36.5 ± 6.4 | 34 ± 8.8 | 0.010 |
| % MELD SCORE* | 55.6 ± 14.7 | 65 ± 5.0 | 0.009 |
| Encefalopatía hepática‡ | 2 [0-3] | 3 [1-4] | 0.037 |
| Días UTI‡ | 4.5 [1-10.2] | 2 [1-3] | 0.006 |
| Días VM‡ | 1.5 [0-4] | 2 [1-3] | 0.591 |
| Ventilación mecánica invasiva | 6 (46.1) | 6 (85.7) | 0.987 |
| Vasopresor | |||
| Norepinefrina | 13 (100) | 7 (100) | 0.243 |
| Balance hídrico | 0.218 | ||
| Neutro | 3 (23) | 1 (14.3) | |
| Positivo | 6 (46.1) | 6 (85.7) | |
| Negativo | 4 (30.7) | 0 (0.0) | |
| Creatinina* | 1.2 ± 0.70 | 3.1 ± 1.2 | 0.333 |
| Lactato‡ | 5.5 [2.3-9.7] | 4.4 [3.8-17] | 0.074 |
| Bilirrubina‡ | 12.1[10-32] | 9 [3.8-12.1] | 0.395 |
| INR‡ | 3.9 [2.3-8.1] | 3.5 [3-5.5] | 0.133 |
| DHL‡ | 462[310-995] | 562 [411-1,483] | 0.624 |
| TGO‡ | 1,809 [628-4,106] | 595 [527-2,647] | 0.778 |
| TGP‡ | 2,706 [523-5,380] | 1,898 [197-6,024] | 0.421 |
| Na* | 137 ± 5.8 | 138 ± 7.6 | 0.574 |
| Diagnóstico de ingreso | |||
| Falla hepática hiperaguda | 12 (92.3) | 7 (35.0) | 0.258 |
| Falla hepática subaguda | 1 (7.7) | 0 (0.0) | |
| Etiología | |||
| DILI | 3 (15.0) | 2 (10.0) | 0.150 |
| Hepatitis A | 8 (40.0) | 2 (10.0) | |
| Hepatitis I | 0 (0.0) | 2 (10.0) | |
| LLA | 1 (5.0) | 0 (0.0) | |
| Micetismo | 1 (5.0) | 1 (5.0) | |
| Soporte extracorpóreo | 5 (38.4) | 1 (14.3) | 0.018 |
| Trasplante | 1 (7.6) | 0 (0.0) | 0.452 |
| AKI | 9 (69.2) | 7 (100) | 0.790 |
| Traslado | 3 (30) | 7 (100) | 0.126 |
| Tipo de terapia extracorpórea | |||
| No aplica | 4 (30.7) | 5 (71.4) | 0.020 |
| No | 2 (15.3) | 1 (14.3) | |
| Plasmaféresis | 5 (38.4) | 1 (14.3) |
DHL = deshidrogenasa láctica. DILI = daño hepático inducido por medicamentos (drug-induced liver injury). INR = international normalized ratio (índice internacional normalizado). LLA = leucemia linfoblástica aguda. LRA = lesión renal aguda.
TGO = transaminasa glutamicooxalacética (o aspartato aminotransferasa [AST]). TGP = transaminasa glutamicopirúvica (o alanina aminotransferasa [ALT]).
UTI = Unidad de Terapia Intensiva. VM = ventilación mecánica.
* Valores expresados en media ± desviación estándar.
‡ Valores expresados en mediana y [rango intercuartil].
Destaca el que, a pesar de mayor incremento de enzimas hepáticas en el grupo que sobrevivió siendo para TGO la mediana de 1,809 (rango 628-4,106), comparado con el grupo de mortalidad 595 (rango 527-2,647), p = 0.778; la mediana para TGP fue de 2,706 (rango 523-5,380) para el grupo sobrevivientes, siendo la mediana 1,898 (rango 197-6,024) para el grupo de mortalidad, con p = 0.421; sin embargo, ninguna variable mostró significancia.
En nuestra cohorte, el grupo sobrevivientes utilizo en mayor porcentaje el soporte extracorpóreo con un 38.4%, en contraste con el grupo con mayor mortalidad en quienes sólo se usó en 14.3% (p = 0.018). Se deduce que los pacientes con mayor mortalidad no recibieron plasmaféresis y la muerte ocurrió de manera temprana entre los días uno a tres (p = 0.006). Dicha diferencia presentó significancia estadística en el análisis bivariado (Tabla 2).
Por último, se realizaron gráficos de Kaplan-Meier para mortalidad, no obteniendo significancia, probablemente por la limitada muestra de pacientes, resaltando que los pacientes que no se beneficiaron de la terapia de soporte alcanzaron la mediana de supervivencia al obtener 71% del puntaje MELD (o > 40 del valor) (Figura 1), con un log rank 0.049 (IC95% 63.8-78.1), siendo significativo.
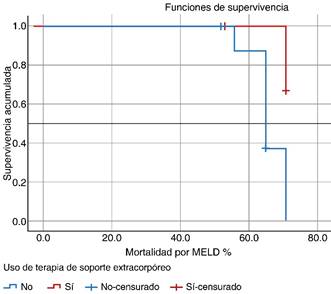
Figura 1: Análisis de supervivencia Kaplan Meier. El grupo que no uso la terapia de soporte extracorpóreo alcanzó la mediana de mortalidad al obtener 71% del puntaje MELD (o > 40 del valor), log rank 0.049 (IC95% 63.8-78.1), siendo significativo.
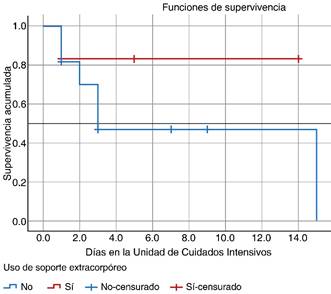
Figura 2: Análisis de supervivencia Kaplan Meier. El grupo que no uso la terapia de soporte extracorpóreo alcanzó la mediana de mortalidad en el día 2.8-3 de estancia en la Unidad de Cuidados Intensivos (UCI ), p = 0.271.
Aquellos pacientes que no tuvieron soporte extracorpóreo alcanzaron la mediana de supervivencia a los 2.8 días de estancia en UTI, p = 0.271 (Figura 2).
A pesar de la muestra pequeña, el resultado favorece a los pacientes con uso de soporte extracorpóreo con menor mortalidad en este padecimiento.
Discusión
El razonamiento detrás de las terapias de soporte hepático es el disminuir las manifestaciones asociadas a la acumulación de toxinas, restaurar la funcionalidad de la albúmina, redirigir la función hepática para la síntesis y promover la regeneración hepática. Con el objetivo real de mejorar la supervivencia libre de trasplante o funcionar como una terapia puente al mismo.23-26
Las revisiones sistemáticas y metaanálisis de ensayos clínicos aleatorizados han tratado de dilucidar cuál de las terapias extracorpóreas tiene el mejor perfil en cuanto a eficacia y seguridad. En 2020, Alshamsi y colaboradores incluyeron 25 ensayos clínicos aleatorizados con un total de 1,796 pacientes;17,27-30 encontraron que el soporte hepático se asoció con mejoría en la encefalopatía hepática (RR 0.71; IC95% 0.60-0.8) en pacientes con insuficiencia hepática aguda y crónica. Sin embargo, la eficacia y seguridad del soporte hepático extracorpóreo no está clara, dados la diversidad de modalidades, los costos y la disponibilidad. El estudio icónico de Larsen y asociados en 2016,31 que incluyó 182 pacientes, mostró evidencia de que el recambio plasmático con volúmenes de recambio mayores a un recambio plasmático terapéutico mejoraba la sobrevida libre de trasplante en pacientes con falla hepática aguda (IC95% 0.36-0.86; p = 0.0083). En nuestra cohorte, el grupo sobrevivientes utilizó en mayor porcentaje la plasmaféresis de alto volumen con 38.4%, en contraste con el grupo con mayor mortalidad en quienes solo se usó en 14.3% (p = 0.018), deduciendo que los pacientes con mayor mortalidad no recibieron plasmaféresis y además la muerte ocurrió de manera temprana entre los días uno a tres (p = 0.006).
En la revisión sistemática más reciente donde se incluyeron 343 pacientes con insuficiencia hepática aguda (IHA) (n = 174 Plex frente a n = 169 tratamiento estándar), el recambio plasmático en comparación con la terapia estándar se asoció significativamente con mayor supervivencia a 30 días (RR 1.41, IC95% 1.06-1.87, p = 0.02).32 Estos datos que concuerdan con nuestros resultados en población mexicana con falla hepática aguda de etiología diversa; puede entonces considerarse que el recambio plasmático es una buena opción de menor costo y disponible en la mayoría de hospitales del sector público y privado.
Conclusiones
La plasmaféresis de alto volumen es la mejor terapia de soporte hepático en la falla hiperaguda ya que aumenta la supervivencia libre de trasplanté, es además de bajo costo y alta disponibilidad en nuestro medio. Nuestro trabajo muestra que existe asociación con disminución en la mortalidad, debiendo considerar implementar su uso en los centros nacionales de referencia.















