Introducción
Las alteraciones de las condiciones ambientales acentuadas por el cambio climático pueden tener consecuencias importantes para la biodiversidad y el deterioro de los ecosistemas naturales (Gratani 2014). Las plantas por ser organismos sésiles están expuestas a múltiples factores bióticos y abióticos que determinan la composición genética de las poblaciones y su diferenciación, algunos de estos factores pueden ser el ensalitramiento de los suelos, fragmentación y destrucción del hábitat (Lienert 2004, Shahid et al. 2018). Al suceder esto, se pueden modificar los niveles de variación genética y su distribución entre y dentro de las poblaciones, favoreciendo (Young et al. 1993) o no esta cualidad (Fischer et al. 2000).
La expresión de la variación genética de una población puede diferir entre los rasgos foliares, de acumulación de biomasa, días a floración, forma, tamaño y color de fruto, entre otros, dependiendo de si están sujetos a selección natural o no y de cómo la selección varía espacialmente (Olsson y Ågren 2002). La diferenciación genética entre poblaciones puede ser impulsada por la selección natural o la deriva genética. La selección natural persiste en poblaciones donde sus individuos presentan diferencias fenotípicas y dichas diferencias son hereditarias y tienen un valor adaptativo. Por el contrario, la deriva genética produce cambios genéticos aleatorios, independientes de las presiones selectivas dadas las condiciones ambientales locales (Schmid y Guillaume 2017).
En las especies silvestres bajo condiciones naturales, sus individuos están en una continua interacción dinámica de adaptación con los factores en los que crece (Matesanz et al. 2020). El resultado de esta interacción adaptativa se traduce en la acumulación de la información genética que va guardando entre los miembros de su población, y que se va transmitiendo en las subsiguientes generaciones a través del tiempo (Romero-Higareda et al. 2022). De esta manera, aunque la población de individuos en una especie comparte características comunes y se pueden cruzar entre ellos, también es cierto que en cada una existen muchas variantes individuales ya que las presiones diferenciales de selección a través de condiciones contrastantes impulsan la evolución de los rasgos funcionales, lo que resulta en la diferenciación genética entre las poblaciones y la formación de ecotipos (Matesanz et al. 2020). Por lo que a partir de las colectas in situ de especies Capsicum es posible seleccionar genotipos que favorezcan los programas de mejoramiento cuando existe variación en sus rasgos (Pérez-Grajales et al. 2009). En las colectas, uno de los factores a revisar es la salinidad del suelo, y sus efectos en el crecimiento y desarrollo de las plantas (Chetelat et al. 2009).
Los estudios sobre efectos del ensalitramiento para investigar la variación fenotípica en poblaciones de Capsicum, son poco comunes, a pesar de que México cuenta con una superficie degrada por este fenómeno de 22.3 millones de hectáreas (Etchevers-Barra et al. 2023). Al respecto, Félix-Lizárraga et al. (2023) evaluaron en estado de plántula, 180 poblaciones de maíz (Zea mayz L.) de la raza Ratón provenientes de tres estados de la República Mexicana, con cloruro de sodio (NaCl) a conductividad eléctrica de 1.85 dS m-1; los resultados mostraron variación genética en las poblaciones. Por otra parte, López-Aguilar et al. (2012) probaron 50, 100, 200, y 300 mM NaCl reportando que C. annuum var. glabriuculum fue más tolerante que C. annuum var. annuum de acuerdo a biomasa de raíz, tallo y hojas. Mientras que, Bojórquez-Quintal et al. (2016) utilizaron sólo 150 mM NaCl, y reportan al chile habanero (Capsicum chinense Jacq.) más tolerante que C. annuum var. annuum.
En la mayoría de los suelos salinos, el NaCl aporta entre 50 y 80% de las sales solubles totales y en cantidades excesivas (sales solubles de Na > 15% junto con una conductividad eléctrica > 4.0 dS m-1) afectan el crecimiento y desarrollo de las plantas (Rengasamy 2010). Su acumulación es común en suelos en donde se cultiva en condiciones de fertirriego intensivo y se agrava en regiones como el Noroeste de México, donde el cambio climático altera los patrones de lluvia (Hassani et al. 2021).
La especie silvestre Capsicum annuum L. var. glabriusculum (Dunal) Heiser & Pickersgill, es conocida como chiles chiltepines o piquines (Romero-Higareda et al. 2023). Es un recurso genético estrechamente vinculado con los cultivos modernos de chile serrano, jalapeño, morrón y ancho. Las poblaciones silvestres son consideradas como un recurso genético valioso, que al expandirse geográficamente (Rice y Mack 1991, Hernández-Verdugo et al. 2008) proporcionan reservorios únicos de diversidad genética útiles en el mejoramiento para sus formas cultivadas (Hernández-Verdugo et al. 1998, Retes-Manjarrez et al. 2018, Alcalá-Rico et al. 2023).
Varios investigadores han documentado la variabilidad de esta especie cuando se colecta en campo y de forma silvestre (Hernández-Verdugo et al. 2008). Para investigar la variación cuantitativa entre y dentro de poblaciones de C. annuum L. var. glabriusculum se han combinado varias técnicas: estudios con isoenzimas (Hernández-Verdugo et al. 2001), RAPD (Oyama et al. 2006) y microsatélites (Pacheco-Olvera et al. 2012), con resultados que indican un elevado nivel de variación genética entre y dentro de las poblaciones. Al respecto, López-España et al. (2016) en condiciones de invernadero, señalaron que los rasgos foliares presentan la mayor variación fenotípica, seguidos de los rasgos reproductivos y vegetativos. Mientras que Romero-Higareda et al. (2022) detectaron diferenciación fenotípica como resultado de diferentes regímenes de selección natural en cada población, considerando los factores de agua y luz.
Diversos estudios han cuantificado el nivel de variación dentro de poblaciones de Capsicum, seleccionando un número menor de poblaciones y aumentando el número de individuos por población (Hernández-Verdugo et al. (2008) en un estudio con poblaciones del Noroeste de México, documentaron que la mayor proporción de variación fenotípica de C. annuum var. glabriusculum se distribuyó dentro de familias, seguida entre familias y entre poblaciones y agregan que de la variación genética total (38.2%), la mayor proporción se detectó dentro de las poblaciones (69.9%) seguida entre poblaciones (31.9%). Mientras que Romero-Higareda et al. (2023) con poblaciones de varias regiones de México reportó valores de variación fenotípica dentro de familia de 49.8% y de esta 50.1% se debe a una base genética. Por lo anterior, el objetivo fue determinar la distribución de la variación fenotípica entre poblaciones, entre y dentro de familias, y estimar la proporción de la variación fenotípica que tiene una base genética en diferentes rasgos en respuesta a tres niveles de NaCl en condiciones de invernadero.
Materiales y métodos
Sitios de colecta
Se recolectaron muestras de frutos fisiológicamente maduros de seis poblaciones de Capsicum annuum L. var. glabriusculum (Dunal) Heiser y Pickersgill en los meses de noviembre y diciembre de los años 2014 y 2015. Las plantas se ubicaron en su hábitat silvestre, la vegetación circundante corresponde a matorral espinoso de piedemonte y bosque bajo caducifolio nativo del noroeste de México distribuido en un gradiente latitudinal entre 29° 31’ N y 23° 55’ N (± 1 000 km) (Figura 1).
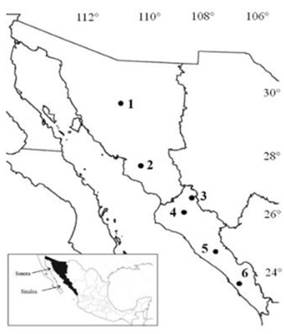
Figura 1 Localización geográfica de 6 poblaciones silvestres de C. annuum L. recolectadas en los estados de Sonora y Sinaloa, México. Mazocahui (1), Presa Oviachic (2), Yecorato (3), Lo de Vega (3), Cosalá (4) y El Roble (5).
En cada población se obtuvo una muestra de suelo compuesta (de 6 a 22 sub muestras individuales) se recolectaron a una profundidad de 30 cm y a una distancia promedio de 40 cm del tallo de las plantas. Previo al análisis del suelo, cada muestra se secó a temperatura ambiente (21 a 32 °C), se trituró y tamizó en malla de 2 mm. La determinación de la conductividad eléctrica, pH, Na+ y Cl- se obtuvo por extracto de saturación con base en la NOM-021-SEMARNAT-2000 (Tabla 1).
Tabla 1 Datos geográficos, climáticos y edáficos de las seis poblaciones silvestres de Capsicum anuumm del Noroeste de México.
| Población | LAT | LON | TMA | PMA | CE | pH | Na+ | Cl- |
|---|---|---|---|---|---|---|---|---|
| 1. Mazocahui | 29°31’ | 110°05’ | 21.3 | 534 | 0.7 | 6.6 | 0.3 | 4.0 |
| 2. Presa Oviachic | 27°46’ | 109°54’ | 24.7 | 410 | 1.0 | 7.8 | 1.2 | 3.5 |
| 3. Yecorato | 26°26’ | 108°12’ | 24.1 | 818 | 1.0 | 6.8 | 1.4 | 3.1 |
| 4. Lo de Vega | 26°08’ | 108°32’ | 23.6 | 628 | 0.8 | 7.6 | 0.7 | 3.2 |
| 5. Cosalá | 24°24’ | 106°36’ | 24.9 | 1098 | 0.8 | 7.5 | 0.4 | 3.4 |
| 6. El Roble | 23°55’ | 106°53’ | 23.5 | 587 | 0.8 | 7.8 | 0.9 | 2.5 |
LAT: Latitud Norte; LON: Longitud Oeste; TMA: temperatura media anual (°C). PMA: precipitación media anual (mm); CE: conductividad eléctrica (dS m-1). pH: potencial hidrógeno. Na+ y Cl- en mM.
Los sitios de muestreo (Figura 1) fueron elegidos para representar una amplia distribución geográfica y diferentes hábitats en los que se encuentran las poblaciones silvestres de esta especie en el Noroeste de México.
Descripción de la planta
El hábito de reproducción de C. annuum var. glabriusculum silvestre es exclusivamente a través de semillas. Las plantas son perenes, erectas o arbustivas de 1 a 4 m de altura. Muestran un hábito de crecimiento arbustivo y un estado reproductivo espontáneo. Sus frutos en etapa madura son picantes, pequeños, rojos, casi redondos y erectos que incentivaban el consumo por aves frugívoras favoreciendo su amplia dispersión (IPGRI, AVRDC y CATIE 1995, Votava et al. 2002, Barboza et al. 2022).
Diseño experimental
En campo, se seleccionaron las plantas que presentaran frutos fisiológicamente maduros o próximos a verse completamente rojos. Así, en Mazocahui fueron 4, Presa Oviachic 11, Yecorato 17, Lo de Vega 7, Cosalá 16 y El Roble 20 plantas. Los frutos se recolectaron e identificaron por planta. Se secaron a la sombra a temperatura ambiente (21 a 32 °C). Para su traslado se guardaron en bolsas de plástico a temperatura de 5 °C y se resguardaron en el Centro de Recursos Genéticos de la Facultad de Agronomía de la Universidad Autónoma de Sinaloa. Las semillas de los frutos se extrajeron a mano y se remojaron en 1 000 mg L-1 de ácido giberélico durante 24 h. Se germinaron en charolas de poliestireno de 60 cavidades (cavidad individual = 230 cm3) rellenas con turba como sustrato, en un invernadero de ventana cenital fija, cubierta plástica con 88% de transmitancia y paredes con malla antiáfidos. Durante el experimento prevaleció una temperatura media de 22.3 °C y humedad relativa de 67%. Después de germinar, las plántulas crecieron en condiciones uniformes de riego y luz y cuando tuvieron de dos a cinco hojas verdaderas se trasplantaron a nuevas charolas de poliestireno de 60 cavidades con turba (1 plántula por cavidad). Cada planta colectada en campo representó una familia. De cada familia se sembraron sus semillas y eligieron tres individuos. Con base al número de plantas colectadas se formaron diferente número familias en cada una de las seis poblaciones: Mazocahui 4, Presa Oviachic 11, Yecorato 17, Lo de Vega 7, Cosalá 16 y El Roble 20 familias. En estas seis poblaciones se analizaron tres tratamientos diseñados a partir de la solución universal de Steiner (Steiner 1984) expresada en mM: 12 NO3 -, 1 H2PO4 -, 3.5 SO4 2-, 7 K+, 4.5 Ca2 +, 2 Mg2+. Se usó agua destilada para su preparación. Esta solución no contiene cloruro de sodio, por lo que se les incorporó, formando los tratamientos: 1) 0 (control), 2) 25 y 3) 50 mM NaCl obteniendo una conductividad eléctrica de 2.0, 4.5 y 7.0 dS m-1 y un pH de 6.78, 6.71 y 6.47, respectivamente. El número de repeticiones en cada tratamiento fue de 225. Dando un total de 675 plantas en el experimento. La unidad experimental consistió en una planta. Los tratamientos se iniciaron a los 30 días después del trasplante y se continuó durante 42 días más. Los tratamientos iniciaron al 25% de las dosis de NaCl durante los primeros 10 días hasta llegar al 100% 15 días después. Los riegos fueron por inmersión hasta el punto de escurrimiento y durante la mañana. Por el tipo de sustrato empleado y contenedor, cada planta tenía disponible 150 mL de agua (Delgado et al. 2016). Las sales fertilizantes utilizadas fueron: cloruro de sodio grado analítico; mientras que, el nitrato de calcio, nitrato de potasio, sulfato de potasio, sulfato de magnesio, fosfato monopotásico y complejo de microelementos fueron grado comercial.
Rasgos evaluados
A los 42 días de aplicados los tratamientos de salinidad, en cada planta se midieron los siguientes caracteres: (1) peso seco de la planta (g) se usó una balanza analítica marca Sartorius® con precisión 0.01 g, el secado se hizo a 60-70 °C durante 72 h en un horno de secado Felisa® FE-292; este rasgo se dividió en (2) peso seco de raíz, (3) de tallo y (4) de hojas (g); (5) área foliar (cm2), se obtuvo con el medidor de área foliar Li-3100C, LI-COR® Biosciences, Lincoln, Ne, EE. UU.; (6) número de hojas total en cada planta; (7) grosor de hoja (μm), esta medición se hizo en hojas completamente maduras e hidratas usando un micrómetro DRAPER® SM-510 con precisión 0.01-12.5 mm; (8) índice de verdor en lecturas SPAD (Soil Plant Analysis Development 502, Konica Minolta Sensing®, Tokyo, Japan); (9) altura de planta (cm) medida desde la superficie del sustrato hasta el meristemo apical más alto, con un flexometro, y (10) diámetro de tallo (mm), medido a dos centímetros por encima del nivel del suelo obtenido con vernier digital Truper® CALDI-6MP.
Análisis estadístico
Se utilizó un análisis de varianza anidado para evaluar la distribución de las cantidades relativas de variación fenotípica en cada tratamiento en donde se determinó la variación entre poblaciones, entre familias dentro de poblaciones y la variación dentro de familias para cada característica fenotípica medida. Tanto las poblaciones como las familias dentro de las poblaciones fueron considerados factores aleatorios. Para estimar las contribuciones genéticas en relación al ambiente en la variación de las características, se usó la varianza ambiental o componente de plasticidad, y la suma de la variación entre población y entre familia como un estimador del componente genético (Venable y Búrquez 1989, Hernández-Verdugo et al. 2008). Los efectos de los tratamientos de la concentración de sal en los rasgos evaluados y las diferencias entre poblaciones se analizaron con un ANOVA de una vía, cuando las diferencias fueron significativas (P ≤ 0.05) se realizó la comparación múltiple de medias Tukey (α = 0.05). Para evaluar el nivel de variación de la diferenciación fenotípica entre rasgos se utilizó el coeficiente de variación (CV) de los rasgos medidos.
Resultados
Efecto de la salinidad
En todas las características morfológicas de plantas de C. annuum se observaron diferencias significativas por efecto de la salinidad (Figura 2). La mayoría de los rasgos evaluados tendieron a disminuir con niveles de 25 y 50 mM de NaCl (Figura 2A, 2B, 2C, 2D, 2E, 2F, 2H, 2I y 2J), excepto el grosor de hoja, que aumentó de forma significativa con algún nivel de salinidad (25 y 50 mM). Cabe mencionar que, ambos niveles de NaCl fueron estadísticamente diferentes en los caracteres de peso seco total, raíz y hojas; así como, área foliar, número de hojas, lectura SPAD y diámetro de tallo (Figura 2A, 2B, 2D, 2E, 2F, 2H, 2I y 2J, respectivamente). Mientras que, el peso seco de tallo, grosor de hoja y altura de planta se comportaron estadísticamente igual (Figura 2B, 2G y 2I). Por otro lado, las plantas crecidas sin condiciones de salinidad (0 mM) presentaron mayor biomasa de raíz, tallo y hojas, así como, mayor área foliar, número de hojas, lecturas SPAD, altura y diámetro de tallo (Figura 2G).
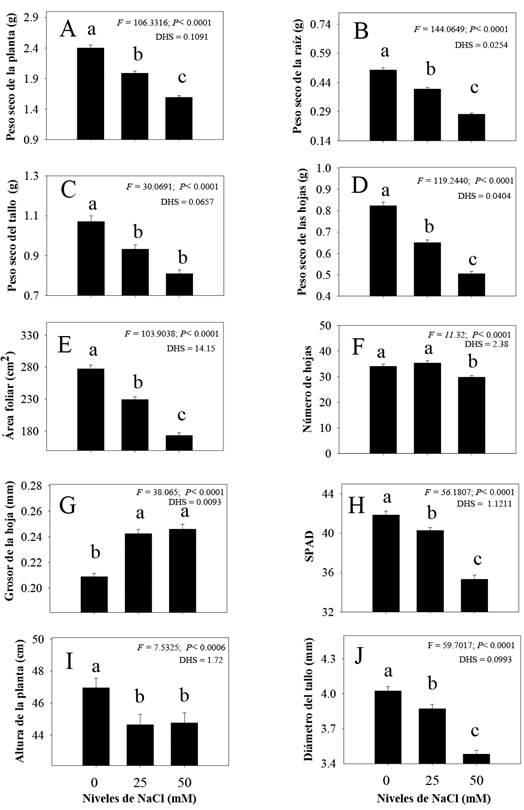
Figura 2 Promedios de los rasgos (± E. E.) de C. annuum silvestre con diferentes niveles de NaCl: 0 mM, 25 mM, y 50 mM. Barras con misma literal dentro de cada parámetro (rasgo) no son estadísticamente diferentes, (Tukey, α = 0.05).
Es importante señalar que la reducción de los rasgos analizados fue mayor con el nivel más alto (50 mM) de salinidad. En este sentido, los rasgos más sensibles en este nivel de salinidad fueron la materia seca de raíz (45.2%), materia seca de hojas (38.7%), área foliar (37.6%), biomasa total (33.7%) y materia seca de tallos (24.4%).
Variación dentro de familias
En los tres niveles de NaCl, la mayor cantidad relativa de variación total se distribuyó dentro de familias (VFDF) (Tabla 2). En el nivel de 0 mM, el valor promedio total fue de 54.6%; mientras que, en 25 mM se redujo a 52.8%, en 50 mM fue de 50.8%. Todas las características evaluadas presentaron mayor variación dentro de familia a excepción de altura de planta, que se registró entre familias (VFEF) en los tres niveles, y el peso seco de hoja que fue en VFEP con 25 mM. Los valores de variación dentro de familias oscilaron desde el 41.5% en peso seco total hasta 83.5% en grosor foliar en 0 mM. Mientras que, en 25 mM, fueron entre 34.2% en altura de planta a 71% en lecturas SPAD. Finalmente, en las condiciones de 50 mM de NaCl, el valor más bajo fue en la altura de planta con 22.4% y el más elevado fue de 67.3% en lecturas SPAD.
Tabla 2 Porcentaje de variación fenotípica entre poblaciones (VFEP), entre familias (VFEF) y dentro de familias (VFDF). Variación genética total (VGT = VFEP + VFEF)/VFEP + VFEF + VFDF), variación genética entre poblaciones (VGP = VFEP / VFEP + VFEF) y variación genética entre familias (VGF = VFEF / VFEP + VEF), para diez caracteres medidos en poblaciones de C. annuum silvestre del Noroeste de México bajo tres niveles de NaCl.
| 0 mM NaCl | 25 mM NaCl | 50 mM NaCl | |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Rasgo | VFEP | VFEF | VFDF | VGT | VGP | VGF | VFEP | VFEF | VFDF | VGT | VGP | VGF | VFEP | VFEF | VFDF | VGT | VGP | VGF | |||
| Peso seco total | 29.2 | 29.3 | 41.5 | 58.5 | 50.0 | 50.0 | 24.7 | 29.5 | 45.8 | 54.2 | 45.6 | 54.4 | 35.6 | 25.9 | 38.5 | 61.5 | 57.9 | 42.1 | |||
| Raíz | 20.6 | 22.6 | 56.8 | 43.2 | 47.7 | 52.3 | 18.4 | 37.5 | 44.1 | 55.9 | 32.9 | 67.1 | 29.9 | 22.1 | 48.0 | 52.0 | 57.6 | 42.4 | |||
| Tallo | 30.2 | 27.3 | 42.5 | 57.5 | 52.6 | 47.4 | 4.2 | 35.1 | 60.7 | 39.3 | 10.6 | 89.4 | 27.1 | 33.8 | 39.1 | 60.9 | 44.6 | 55.4 | |||
| Hoja | 21.6 | 32.3 | 46.1 | 53.9 | 40.1 | 59.9 | 43.8 | 15.2 | 41.0 | 59.0 | 74.2 | 25.8 | 20.4 | 21.7 | 57.9 | 42.1 | 48.5 | 51.5 | |||
| Área foliar | 23.6 | 30.2 | 46.2 | 53.8 | 43.9 | 56.1 | 22.6 | 33.4 | 44.0 | 56.0 | 40.3 | 59.7 | 22.8 | 35.4 | 41.8 | 58.2 | 39.1 | 60.9 | |||
| Número de hojas | 16.7 | 21.6 | 61.7 | 38.3 | 43.5 | 56.5 | 7.3 | 35.6 | 57.1 | 42.9 | 17.1 | 82.9 | 3.3 | 30.4 | 66.3 | 33.7 | 9.7 | 90.3 | |||
| Grosor de hoja | 2.3 | 14.2 | 83.5 | 16.5 | 13.8 | 86.2 | 11.5 | 28.7 | 59.8 | 40.2 | 28.7 | 71.3 | 2.9 | 30.8 | 66.4 | 33.6 | 8.5 | 91.5 | |||
| SPAD | 11.2 | 26.4 | 62.4 | 37.6 | 29.7 | 70.3 | 13.0 | 16.1 | 71.0 | 29.0 | 44.7 | 55.3 | 19.9 | 12.8 | 67.3 | 32.7 | 60.7 | 39.3 | |||
| Altura de planta | 8.7 | 47.2 | 44.1 | 55.9 | 15.6 | 84.4 | 2.5 | 63.3 | 34.2 | 65.8 | 3.8 | 96.2 | 13.2 | 64.4 | 22.4 | 77.6 | 17.0 | 83.0 | |||
| Diámetro de tallo | 12.9 | 26.1 | 61.0 | 39.0 | 33.1 | 66.9 | 13.4 | 16.7 | 69.9 | 30.1 | 44.5 | 55.5 | 25.7 | 13.8 | 60.4 | 39.6 | 65.0 | 35.0 | |||
| Media | 17.7 | 27.7 | 54.6 | 45.4 | 37.0 | 63.0 | 16.1 | 31.1 | 52.8 | 47.2 | 34.2 | 65.8 | 20.1 | 29.1 | 50.8 | 49.2 | 40.9 | 59.1 | |||
Variación entre familias
La variación fenotípica dentro de cada población, en cada tratamiento, presentó rasgos que aumentaron con el incremento del nivel de NaCl como el área foliar, grosor de hoja y la altura de planta (Tabla 2). De ellos, el grosor de hoja fue el rasgo que más aumentó, ya que pasó de 14.2 a 28.7% en el nivel de 0 mM; mientras que, en las dos condiciones de salinidad (25 y 50 mM) se obtuvo el 30%. En cuanto a la altura de planta se registraron valores altos en los tres niveles de salinidad; 47% en 0 mM, 63% en 25 mM y 64.4% en 50 mM. Por otra parte, la lectura SPAD y diámetro de tallo fueron rasgos que redujeron su variación fenotípica en ambos niveles de NaCl. En este sentido, las lecturas SPAD en el nivel 0 mM tuvo 26.4%, 16.1% en 25 mM y 12.8% en 50 mM. El diámetro de tallo en 0 mM fue de 26.1%, 16.7% en 25 mM y 13.8% en 50 mM.
Es importante señalar que, en los tres niveles de salinidad la menor variación fenotípica total promedio se presentó entre poblaciones (VFEP), ya que en 0 mM se obtuvo el 17.7%, en 25 mM el 16.1% y en 50 mM el 20.1%. Los extremos de variación por nivel de NaCl fueron de 2.3% en grosor de hoja a 30.2% en peso seco de tallo en 0 mM. En el nivel intermedio de salinidad (25 mM), la altura de planta presentó 2.5 a 43.8% en peso seco de hojas. Finalmente, en el nivel más alto (50 mM) se detectó 2.9% en grosor de hoja a 35.6% en peso seco total.
Variación Genética
De la variación fenotípica total observada, el 45.4% en 0 mM, 47.2% en 25 mM y 49.2% en 50 mM tiene una base genética (VGT). Para los tres niveles de salinidad (0, 25 y 50 mM) la mayor variación se distribuyó dentro de poblaciones (63.0, 65.8 y 59.1%, respectivamente) y el resto (37.0, 34.2 y 40.9%, respectivamente) entre poblaciones. En 0 mM, el peso seco total, peso de tallo, altura de planta, peso de hoja y área foliar presentaron valores superiores al 50%; mientras que, el grosor de hoja tuvo el valor más bajo (16.5%). En 25 mM, la altura de planta, peso seco de hojas, área foliar, peso seco de raíz y peso seco total presentaron variación genética superiores al 50%; en cambio, las lecturas SPAD registró el valor más bajo (29.0%). En 50 mM, la altura de planta, peso seco total, peso seco de tallo, área foliar y peso seco de raíz presentaron valores mayores al 50%; en contraste, el grosor de hoja y lecturas SPAD presentaron valores promedios por debajo de 35%.
Variación entre poblaciones
Las comparaciones de medias muestran que las poblaciones difieren en todas las características con excepción de altura de planta (Figura 3). Mientras que la población Mazocahui presentó las hojas más gruesas y menor área foliar (Figura 3G y 3E). En tanto que Presa Oviachic se caracterizó por tener la mayor producción de biomasa total, raíz, tallo y hoja (Figura 3A, 3B, 3C y 3D); así como, los valores más altos en área foliar, número de hojas, diámetro de tallo y el menor grosor de hojas (Figura 3E, 3F, 3J y 3G). La población Yecorato destaco por presentar hojas con altas lecturas SPAD; pero, bajos contenidos de biomasa en raíz (Figura 3H y 3B). En lo referente a la población Lo de Vega tuvo el mayor contenido de clorofila (Figura 3H) y valores intermedios en los demás rasgos. Los individuos de la población Cosalá mostraron los valores más bajos de peso seco de hoja, contenido de clorofila y diámetro de tallo (Figura 3D, 3H y 3J). Por último, El Roble exhibió los menores promedios en peso seco total, de raíz, peso seco de tallo y número de hojas (Figura 3A, 3B, 3C y 3D).
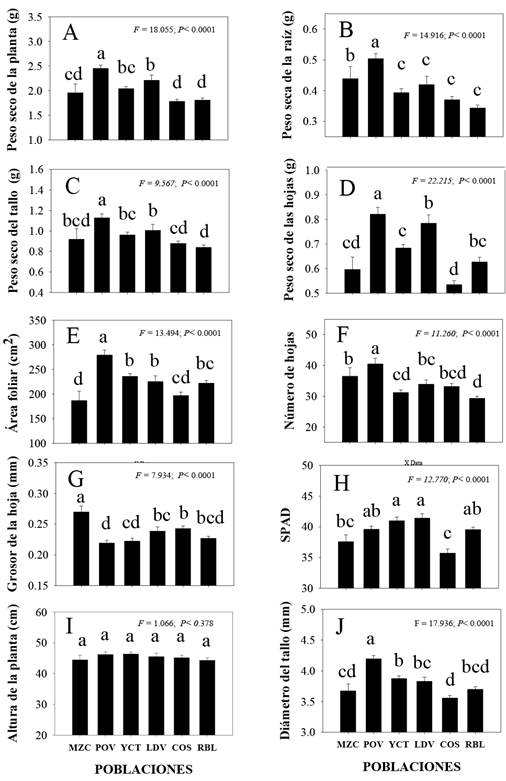
Figura 3 Promedios de los rasgos (± E. E.) en plantas de seis poblaciones de C. annuum silvestre del Noroeste de México. MZC: Mazocahui, POV: Presa Oviachic, YCT: Yecorato, LDV: Lo de Vega, COS: Cosalá y RBL: El roble. Datos agrupados de tres niveles de NaCl. Letras diferentes en minúsculas indican diferencias de medias entre poblaciones. (Tukey, α = 0.05).
Variación fenotípica
Los resultados obtenidos indican que las poblaciones silvestres de C. annuum estudiadas con los tres niveles de salinidad, expresaron altos niveles de variación fenotípica (Tabla 3). De diez rasgos morfológicos, ocho mantuvieron coeficientes de variación por arriba de 20%. Los caracteres más variables fueron materia seca de raíz (41.8%), número de hojas (39.8%), peso seco de tallo (39.6%), área foliar (38.7%), peso seco de hojas (38.5%), peso seco total (33.9%), grosor de hoja (22.8%), altura de planta (20.8%). El promedio general de variación fue de 30.9% para los rasgos fenotípicos. Entre las poblaciones, la que presentó la mayor variación fue Mazocahui (41.3%), seguida de Lo de Vega (31.8%), Cosalá (29.4%), El Roble (27.9%), Presa Oviachic (27.7%) y Yecorato (26.9%).
Tabla 3 Coeficientes de variación (%) de rasgos morfológicos de poblaciones silvestres de C. annuum del Noroeste de México. Datos agrupados de tres niveles de NaCl.
| Rasgo | Mazocahui | Presa Oviachic | Yecorato | Lo de Vega | Cosalá | El Roble | Promedio |
|---|---|---|---|---|---|---|---|
| Peso seco total | 56.0 | 28.0 | 27.6 | 38.6 | 28.7 | 30.0 | 33.9 |
| Raíz | 53.5 | 31.5 | 40.9 | 52.2 | 36.6 | 35.9 | 41.8 |
| Tallo | 67.4 | 35.6 | 34.7 | 45.9 | 32.6 | 35.2 | 39.6 |
| Hojas | 50.3 | 34.0 | 26.1 | 34.2 | 37.5 | 40.8 | 38.5 |
| Área foliar | 61.4 | 36.5 | 29.7 | 42.1 | 42.3 | 32.7 | 38.7 |
| Número de hojas | 46.0 | 46.6 | 34.7 | 33.8 | 36.1 | 32.4 | 39.8 |
| Grosor de hoja | 21.4 | 20.3 | 25.7 | 23.4 | 22.0 | 19.9 | 22.8 |
| SPAD | 17.5 | 12.8 | 17.4 | 14.3 | 22.2 | 13.1 | 17.2 |
| Altura de planta | 20.4 | 19.1 | 18.5 | 18.9 | 21.7 | 23.5 | 20.8 |
| Diámetro de tallo | 18.5 | 12.9 | 13.9 | 14.6 | 14.5 | 15.3 | 15.4 |
| Promedio | 41.3 | 27.7 | 26.9 | 31.8 | 29.4 | 27.9 | 30.9 |
Discusión
Efecto de la salinidad
Bajo estrés salino, las plantas reducen su crecimiento por diferentes alteraciones bioquímicas y fisiológicas. En las primeras encontramos el metabolismo enfocado a acumulación de osmolitos de bajo peso molecular como prolina, mientras que en las segundas está el cierre de estomas que reducen la asimilación de CO2. Así también, el cierre de estomas es ocasionado por moléculas como el ácido abscísico, sintetizado en hojas y raíces (Munns et al. 2010, Zhao et al. 2020, Javed et al. 2022). En este contexto, las raíces permiten a las plantas obtener agua y nutrientes; sin embrago, son las primeras en exponerse al exceso de sales, y en altas concentraciones detienen la división celular y el crecimiento (Acosta-Motos et al. 2017, Van-Zelm et al. 2020); efecto similar ocurre en la parte aérea de la planta reduciendo el área foliar (Fang et al. 2021). Lo descrito anteriormente, se observó en las plantas de C. annuum expuestas a NaCl que presentaron disminución de la materia seca de raíz, hojas, y área foliar; no obstante, el grosor de hoja fue favorecido significativamente con la salinidad, este incremento también se ha reportado en otras plantas como Imperata cylindrica (Hameed et al. 2009) cuando fueron colectadas en sitios donde el suelo presentó conductividad eléctrica de 15.42 dS m-1 y en Parthenium argentatum A. Gray cuando fue sometida a niveles crecientes de NaCl (43 a 684 mM) en un sistema hidropónico con raíces flotantes (Di-Baccio et al. 2024).
Una adaptación relacionada con el estrés salino en periodos prolongados es el aumento del grosor de la hoja (Hameed et al. 2009). En nuestro estudio las plántulas expuestas a los tratamientos 25 y 50 mM NaCl incrementaron este valor en 16.1 y 17.8%, respectivamente. Tal comportamiento se puede relacionar con lo reportado por Fernández-García et al. (2014) donde estudiaron plantas de Lawsonia inermis L. regadas con altas concentraciones de sal y mencionan que el nivel de 75 mM NaCl las hojas aumentaron su grosor como estrategia para maximizar el potencial de la fotosíntesis pero ello implicó una mayor inversión en tejido asimilatorio.
Distribución de la variación fenotípica y genética
Variación fenotípica
La mayor variación fenotípica ocurrió dentro de familias, en los tres niveles de NaCl, seguida de dentro de poblaciones (entre familias) y entre poblaciones. Estos resultados coinciden con Hernandez-Verdugo et al. (2008) al estudiar la variación en la germinación en chile silvestre, reportan el mayor porcentaje de variación fenotípica dentro de familias (61.8%), seguida de entre familias (24.7%) y entre poblaciones (13.5%). La variación dentro de familias fue afectada por el nivel de estrés, se redujó en 3.3% con 25 mM y 7.0% con 50 mM, con respecto a 0 mM, esta reducción en la variabilidad fenotípica al aumentar el estrés, coincide con lo reportado por Kano-Nakata et al. (2019) quienes señalan que la variabilidad fenotípica del sistema radical de genotipos de arroz (Oryza sativa L.) se vio afectada por las intensidades del estrés por sequía; los límites en la variabilidad fenotípica antes señalados, también son señalados por Baeza et al. (2013) en plantas de Typha domingensis y Schoenoplectus americanus usando 6 niveles de salinidad (0 - 12 g L-1 de sólidos disueltos totales) al medir biomasa y altura de planta.
Entre familias, los caracteres grosor de hojas y número de hojas mostraron aumentos en sus niveles de variación; en el nivel de 25 mM se obtuvo 102.1 y 64.8%, respectivamente, con respecto a 0 mM; mientras que, en 50 mM fue de 116.9 y 40.7%, respectivamente. Bajo condiciones de estrés, la variación en la morfología de la hoja juega un papel muy importante en la adaptabilidad de la planta (Verhoeven y van Gurp 2012, Stotz et al. 2021, Romero-Higareda et al. 2022). Bajo pequeñas escalas espaciales (población), se han reportado importantes fuentes de heterogeneidad en las plantas silvestres de C. annuum (Hernández-Verdugo et al. 2008). El exceso de sales en los suelos es un factor que reduce la absorción de agua de las plantas, por lo que adaptarse a esta limitante favorece al reducir el riesgo de morir, estas adaptaciones incluyen el aumento del grosor de la hoja y reducción del área foliar (Acosta-Motos et al. 2017).
Variación genética total (VGT)
De la variación fenotípica total observada el 45.4% en 0 mM, 47.2% en 25 mM y 49.2% en 50 mM, tiene una base genética. Conforme aumentó el nivel de NaCl, la proporción de VGT se incrementó, evidenciando la importancia del componente genético en la diferenciación de las poblaciones estudiadas (Figura 3). El incremento de variación genética en los caracteres de grosor de hoja y peso seco de la raíz fue de 143.6 y 29.4% en 25 mM y de 103.6 y 20.4% en 50 mM, respectivamente. Este componente genético ha sido importante para la adaptación de las plantas de chile silvestre en ambientes heterogéneos, ya sean abióticos como luz (Hernández-Verdugo et al. 2015) y bióticos como virus (Retes-Manjarrez et al. 2018). La detección de VGT en colectas de Maíz ha permitido la selección de genotipos tolerantes con base en el peso seco de la raíz cuando se ha usado una conductividad eléctrica de 18.5 dS m-1 de NaCl en estado de plántula (Félix-Lizárraga et al. 2023).
Variación entre poblaciones
La población Presa Oviachic fue significativamente superior al resto de las poblaciones en la unidad de medida de siete rasgos (peso seco de planta, peso seco de raíz, peso seco de tallo, peso seco de hojas, área foliar, número de hojas y diámetro de tallo); mientras que, Mazocahui, Cosalá y El Roble fueron más afectadas al presentar menor peso seco de la planta, peo seco de la raíz, peso seco del tallo, peso seco de las hojas, área foliar, número de hojas, lecturas SPAD y diámetro de tallo. La supresión del crecimiento de las plantas bajo estrés salino puede deberse a la disminución de la división y elongación celular reduciendo la actividad del meristemo apical aéreo y radical (Efisue e Igoma 2019, Henderson et al. 2020). La reducción de los rasgos morfológicos es algo reportado en plantas de Capsicum annuum, Zea maíz y Parthenium argentatum A. Gray ya que genera un estrés osmótico (disminución del potencial hídrico externo) que compromete la capacidad de la planta para absorber agua que a nivel macroscópico reduce la expansión de las células de la raíz y los brotes, también se compromete su capacidad fotosintética al ser insuficiente para generar nuevos tejidos (Aktas et al. 2006, Félix-Lizarraga et al. 2023, Di-Baccio et al. 2024). Al respecto, Ghonaim et al. (2021) reportaron que la longitud de brotes y raíces fue diferente en seis genotipos de trigo (Triticum aestivum L.) con 200 mM de NaCl, en la misma investigación señalan que algunos genotipos fueron más sensibles que otros coincidiendo con lo encontrado en este trabajo (Figura 3). Por otra parte, un mayor follaje es determinante para un mejor rendimiento en condiciones de NaCl, al respecto Efisue y Dike (2020) indicaron que las variedades de arroz que mejor rendimiento de grano presentaron en cuatro condiciones de NaCl (0, 2, 3 y 6 dS m-1) fueron las que desarrollaron mayor área foliar.
La población Mazocahui generó hojas más gruesas y puede explicarse por la necesidad de mantener una mejor eficiencia, favorecida por un mayor contenido del agua foliar, y un parénquima más esponjoso, lo que podría mejorar la conductividad hídrica y la difusión de CO2 de estas plantas (Velikova 2020). Esta adaptación es reportada en plantas de Atriplex patula (tolerante al exceso de sales) (Glenn et al. 2012) y Lawsonia inermis L. (Fernández-García 2014). De acuerdo con Acosta-Motos et al. (2017) esta adaptación puede implicar una mayor inversión en tejido asimilatorio como estrategia para maximizar el potencial fotosintético; es decir, un costo para una adaptación, que afecta el crecimiento de otras partes de la planta, fenómeno visto en la población Mazocahui.
La variabilidad de las plantas a factores abióticos cambiantes, tiende a aumentar la aptitud para crecer y desarrollarse en diversos ambientes. La baja o nula variabilidad incluso puede ser adaptativa cuando el cambio ambiental no es predecible o cuando ninguna respuesta fenotípica puede superar el desafío ambiental (Valladares et al. 2007). En la presente investigación hubo rasgos, a nivel poblaciones, que no mostraron aumentos en la variabilidad como ocurrió en la altura de planta. Sin embargo, si se diferenciaron poblaciones que se adaptaron mejor a los dos niveles de NaCl. En la Figura 3 Presa Oviachic destacó en rasgos importantes como la acumulación de biomasa total y de raíz, tallo y hojas. Probablemente el entorno en el que ha estado creciendo y reproduciendose le presentó ventajas bajo estrés por NaCl. Otros factores de estrés como la falta de agua o luz ha beneficiado a otras poblaciones como lo reporta Romero-Higareda et al. (2022), donde las poblaciones Lo de Vega y Yecorato fueron las de mayor acumulación de biomasa.
Variación fenotípica (CV)
El carácter adimensional del CV permite una fácil comparación de la magnitud de la variación fenotípica entre rasgos y poblaciones. Los resultados mostraron que las poblaciones de C. annuum silvestre expresan altos niveles de variación fenotípica. Entre poblaciones, Mazocahui presentó el valor más alto. Tal comportamiento, se puede relacionar con lo reportado por Romero-Higareda et al. (2022) quienes encontraron una variación de 23.6% en esta población, al medir 9 caracteres morfológicos en seis poblaciones de C. annuum silvestre sometidas a cuatro tratamientos de agua y luz. Estos autores también registraron un CV similar en los rasgos de altura de planta (19.3%), diámetro de tallo (13.2%) y área foliar (35.4%).
El peso seco de la raíz (41.8%) fue la variable que presentó la mayor variación promedio. Varios estudios han documentado que la variabilidad de los rasgos de las raíces es una ventaja para la adaptación efectiva al estrés por sequía y salinidad (Sandhu et al. 2016, Schneider et al. 2020, Shelden y Munns 2023). En condiciones naturales, las plantas generan adaptaciones del sistema radical a condiciones irregulares de lluvia excesiva o la escasa humedad favorecen condiciones contrastantes que impulsan la evolución de los rasgos funcionales, con resultado en diferenciación genética entre las poblaciones (Rewald et al. 2013). Las técnicas de fenotipado de alta resolución permiten ahora visualizar y medir los rasgos de las raíces en los sistemas edáficos para mejorar la captura de agua, nitrógeno y restringir la absorción de Na+ (Shelden y Munns 2023). En este sentido, identificar materiales silvestres con alta variación su sistema radical, contribuye al mejoramiento genético de los cultivos, ya que se tiene la oportunidad de seleccionar o generar un ideotipo radical, profundo y económico en términos de energía para la planta.
El carácter peso seco de raíz destacó por tener la mayor variación (41.8%) (Tabla 3). Otros caracteres que estuvieron por encima de 30% fueron el número de hojas (39.8%), peso seco de tallo (39.6%), área foliar (38.7%), peso seco de hojas (38.5%) y peso seco total (33.9%). De acuerdo con Hernández-Verdugo et al. (2012) en plantas de C. annuum con valores mayores de 30% coeficiente de variación presentan amplia variación; otros investigadores consideran que un CV superiores a 20% indica la presencia de alta variación (Romero-Higareda et al. 2023). El valor de variación en el peso seco de la raíz es importante ya que se tienen limitaciones en la base genética en chiles modernos cultivados, por lo que ha orillado a los fitomejoradores a buscar en sus parientes silvestres, variación genética natural con el fin de seleccionar plantas tolerantes a NaCl que puedan usarse como porta injertos (Penella et al. 2016, Osuna-Rodríguez et al. 2023).
Conclusiones
Los niveles de NaCl influyeron en la expresión fenotípica de los rasgos estudiados de Capsicumm annuum silvestre. La mayor cantidad de ésta se encontró dentro de familias y tiene su precedente en la variación genética. El aumento de NaCl contribuyó a incrementar la variación fenotípica entre poblaciones. La variación fenotípica y genética varió considerablemente entre rasgos morfológicos. El coeficiente de variación más alto fue para peso seco de raíz, rasgo que superó el 40%; mientras que, el resto de los rasgos superó el 20% con excepción de diámetro de tallo y lecturas SPAD que tuvieron valores inferiores. La salinidad redujo todos los rasgos con excepción de grosor de hoja. La población Mazocahui destacó por presentar hojas gruesas pero menor área foliar y lecturas SPAD. Por otro otra parte, la población Presa Oviachic desarrolló hojas menos gruesas y presentó los valores más altos de biomasa en raíz, tallo y hoja.
















