Introducción
La macrófita Eichhornia crassipes se considera una especie invasiva debido a su adaptabilidad a un amplio tipo de ecosistemas, que afecta de forma considerable el equilibrio natural de lagunas, lagos, etcétera (Vankar & Bajpai, 2008; Vásquez 2012). Una sola planta de E. crassipes que alcance un humedal contaminado por aguas residuales domésticas con exceso de nutrientes está eutrificada, por lo tanto la planta tiene las mejores condiciones nutricionales para crecer y multiplicarse; en promedio, cada tres días se reproduce por estolones, llegando a que esa sola planta posea en seis meses un total de más de 100 000 ejemplares en el mismo humedal. La mejor manera de controlar el crecimiento de la planta E. crassipes es no contaminar los humedales (Carreño-Sayago & Rodríguez-Parra, 2019; Sayago, Castro, Rivera, & Mariaca, 2020). Es una planta que ha sido fuente de muchas investigaciones en el mundo, como en fitorremediación de aguas contaminadas y la producción de bioenergía. En los últimos años se ha demostrado que esta especie se puede maniobrar de manera sustentable y diseñar soluciones sencillas, pero interesantes, en diferentes industrias que contaminan el agua con metales pesados y además como un aporte a la problemática energética que enfrenta el mundo (Zimmels, Kirzhner, & Malkovskaja, 2006); Atehortua & Gartner, 2003); Carreño-Sayago, 2020).
La descontaminación de aguas provenientes de industrias que vierten metales pesados y contaminan el recurso hídrico es una opción eficiente y económica con el aprovechamiento de la biomasa de E. crassipes (Eid et al., 2019; Victor, Ladji, Adjiri, Cyrille, & Sanogo, 2016). La presencia en la celulosa de E. crassipes de grupos hidroxilo (OH), amino (NH2) y carboxilos (C=O) facilita la adsorción de diferentes metales pesados a través de intercambio catiónico (Lin, Yang, Na, & Lin, 2018; Eyley & Thielemans, 2014; Han, Zhou, French, Han, & Wu, 2013; Man et al., 2011; Sayago et al., 2020; Carreño-Sayago, 2021).
El diseño y desarrollo de sistemas de tratamiento con la biomasa de E. crassipes ha tenido resultados significativos en la adsorción de zinc (Atehortua & Gartner, 2003); cobre (Ibrahim, Ammar, Soylak, & Ibrahi, 2012); cromo (Atehortua & Gartner, 2003); arsénico (Sarkar, Rahman, & Bhoumik, 2017; Lin et al., 2018); y plomo (Borker, Mane, Saratale, & Pathade, 2013; Zhou et al., 2011; Ammar, Elhaes, Ibrahim, & Ibrahim, 2014; Deng et al., 2012; (Sayago, 2021).
La biomasa generada en estos tratamientos conlleva una serie de disposiciones finales costosas debido al tipo de residuo; una alternativa es continuar el proceso sostenible, ya que esta biomasa contiene aun los polisacáridos principales para la producción de bioetanol.
E. crassipes contiene grandes contenidos de celulosa y hemicelulosa, lo que la hacen una planta significativa como biomasa para la producción a gran escala de etanol e hidrógeno (Cuervo, Folch, & Quiroz, 2009; Porous, Siregar, & Salem, 2012; Pizarro et al., 2016; Lee, Park, Cho, & Kim, 2018; Zabed, Sahu, Boyce, & Faruq, 2016; Kouwanou et al., 2018).
En la presente investigación se desarrolló un sistema sostenible con la biomasa de E. crassipes, donde se construyó un sistema de fitorremediación para la descontaminación de plomo (II) en un agua sintética; la biomasa producto de este proceso se llevó a un proceso de producción de bioetanol, con el fin de evaluar la capacidad de producción de bioetanol de esta biomasa con plomo adherido utilizada en dicho proceso.
Materiales y métodos
E. crassipes fue tomada en el municipio de Mosquera, cerca de la ciudad de Bogotá; después se lavó con agua para eliminar las trazas de barro, pues en ese humedal hay un alto grado de contaminación. Dos procesos importantes se llevaron a cabo en esta investigación: un proceso de fitorremediación donde se utilizaron E. crassipes para tratar el agua contaminada con plomo (II), y después de esta experimentación, el empleo de la biomasa que se usa para tratar el agua para crear un sistema compuesto por dos biorreactores para la producción de bioetanol.
Desarrollo de la experimental de la fitorremediación
Las dimensiones del modelo experimental de la fitorremediación son de 45 cm de largo, 10 cm de alto y 12 cm de ancho, en donde cada uno tenía 10 l de agua. Este diseño es a escala piloto y tenía 200 gramos de E. crassipes (aproximadamente dos plantas). Se realizaron experimentos por duplicado. En la Figura 1 se pueden apreciar los experimentos.
Donde se obtuvieron la media, las desviaciones estándar y los coeficientes de correlación.
Estas soluciones de plomo están estandarizadas para las pruebas y se asemejan a efluentes industriales, donde se prepararon soluciones de plomo (II) disolviendo sal anhidra de nitrato de plomo en agua desionizada. La evaluación propuesta de tal sistema de tratamiento duró aproximadamente 15 días. Para las evaluaciones de este sistema de tratamiento, las concentraciones en el agua de plomo en (mg/l) se midieron al principio y después cada dos días.
Desarrollo del modelo experimental de producción de bioetanol
La biomasa utilizada en el proceso de fitorremediación anterior se usó en este proceso de la producción de biocombustibles. En la Figura 2 se muestra plomo (II) adherido a la estructura de la planta.
Tres experimentos se llevaron a cabo con tres diferentes tipos de biomasa:
x1 es la biomasa del tratamiento de 500 (mg/l).
x2 es la biomasa de 750 (mg/l).
x0 es la biomasa sin el proceso de la fitorremediación.
Evaluando plomo (II), afecta la producción de bioetanol a partir de este tipo de biomasa. Se representa en la Tabla 1.
Tabla 1 Diferentes tipos de biomasa.
| Experimentar | Representación |
|---|---|
| 1. Biomasa de tratamiento de 500 (mg/l) de plomo (II) | E1 |
| 2. Biomasa de 700 (mg/l) de plomo (II) | E2 |
| 3. Biomasa sin el proceso de fitorremediación | E0 |
El diseño del proceso de generación de bioetanol consiste, para cada experimento, de la construcción de dos biorreactores: un biorreactor para hacer el hidrolizado y un biorreactor para la fermentación. Para todos los experimentos, se contó con 50 gramos de biomasa seca utilizada en el proceso fitorremediación.
Biorreactor hidrólisis. Es de un litro en vidrio, tiene una tapa para la evaporación gases y para algunas muestras de pH y temperatura, también posee un calentador de agitación magnética a 120 rpm a una temperatura de 60 ºC; esta operación se lleva a cabo de manera continua.
Se llevaron 100 g de E. crassipes seco a dicho reactor, donde se mezcló con agua destilada. Se hicieron reaccionar las muestras en 1 % (peso/volumen) de sosa cáustica (NaOH) a una temperatura de 60 °C, durante 12 h; las muestras se lavaron con agua del grifo hasta alcanzar el valor de pH del agua.
Posteriormente, se añadió ácido sulfúrico (H2SO4) 3% (volumen/volumen) a una temperatura de 60 ºC durante 12 h; las muestras se lavaron con agua del grifo hasta que alcanzaron el valor de pH del agua. El contenido de azúcares reductores se determinó mediante el método dinitro ácido salicílico (DNS) (Cuervo et al., 2009), que cuantifica indirectamente el consumo de sustrato. Se obtuvieron dos litros de solución de hidrolizado de E. crassipes para la continuación de la producción de bioetanol.
Biorreactor de la fermentación. Se tuvieron 2.5 litros en vidrio, con las mismas características del biorreactor para el hidrolizado. Se utilizó Sacharomices sereciciae como inóculo del fermentador del hidrolizado de E. crassipes. De acuerdo con los estudios de Cuervo et al. (2009), y Ganguly, Chatterjee y Dey (2012), se determinó que Sacharomyces cerevisiae es adecuada para la producción de etanol con biomasa vegetal.
Se llevaron 40 g del hidrolizado al biorreactor de la fermentación, donde se mezcló con agua destilada y se añadieron 50 gramos del inóculo; el pH inicial se ajustó a 5.5. Los biorreactores se sellaron herméticamente con septos de goma y tapones de aluminio. Durante la fermentación de la hidrólisis de la biomasa de cada tipo de biomasa, las pruebas de los porcentajes de etanol se hicieron por cromatografía de gases a diferentes intervalos de tiempo.
Resultados de la fitorremediación
Las pruebas se llevaron a cabo durante 15 días. En la Tabla 2 y Tabla 3 se muestran los resultados de las dos pruebas de cada experimento, los promedios y desviación estándar de cada experimento.
Tabla 2 Los resultados de experimento con 500 (mg/l) de plomo (II).
| Experimento 1 (mg/l) | Experimento 2 (mg/l) | Media (mg/l) | desviación estándar (mg/l) | Porcentaje (%) de remoción de plomo (II) | |
|---|---|---|---|---|---|
| Día (0) | 500 | 500 | 500 | - | 0 |
| Día (1) | 405 | 433 | 419 | 14 | 16 |
| Día (3) | 305 | 298 | 302 | 3,5 | 40 |
| Día (5) | 182 | 179 | 181 | 1,5 | 64 |
| Día (7) | 151 | 121 | 136 | 15 | 73 |
| Día (11) | 121 | 111 | 116 | 5 | 77 |
| Día (13) | 120 | 105 | 113 | 7,5 | 77 |
| Día (15) | 93 | 95 | 94 | 1,5 | 81 |
Tabla 3 Los resultados de experimento con 750 (mg/l) de plomo (II).
| Experimento 1 (mg/l) | Experimento 2 (mg/l) | Media (mg/l) | Desviación estándar (mg/l) | Porcentaje (%) de remoción de plomo (II) | |
|---|---|---|---|---|---|
| Día (0) | 750 | 750 | - | - | 0 |
| Día 1) | 599 | 622 | 611 | 12 | 19 |
| Día 3) | 480 | 514 | 497 | 17 | 34 |
| Día 5) | 388 | 366 | 377 | 11 | 50 |
| Día (7) | 288 | 255 | 272 | 16 | 64 |
| Día (11) | 179 | 155 | 167 | 12 | 78 |
| Día (13) | 155 | 145 | 150 | 5 | 80 |
| Día (15) | 145 | 159 | 152 | 7 | 80 |
Los resultados de la Tabla 2 y Tabla 3 indican una homogeneidad de los datos; los tres experimentos muestran un promedio significativo debido a la baja desviación estándar, los promedios suficientemente representados en los experimentos, porque a mayor coeficiente de variación mayor es la heterogeneidad de los valores. Desde el coeficiente medio e inferior de variación, mayor homogeneidad en los valores medios (Lin et al., 2018).
Las eliminaciones del proceso de la fitorremediación, con 500 (mg/l) de plomo (II) iniciales, muestran una disminución continua en este metal; se puede observar la estabilización después de 15 días de tratamiento. Las dos pruebas mostraron un comportamiento similar durante todo el proceso y las remociones estuvieron por encima del 80 %; estos resultados podrían ser comparados con Borker et al. (2013), donde obtuvieron remociones de Pb (II) en un 72 %. En la Tabla 3 se presenta un resumen de los datos del experimento con concentraciones iniciales de plomo de 750 (mg/l).
Al igual que el experimento inicial de 500 (mg/l), donde la planta fue capaz de adsorber 100 (mg/l) de plomo (II), en este experimento también se alcanzaron resultados representativos al primer día de tratamiento y en general en todo el proceso de tratamiento en remociones de plomo (II) por parte de E. crassipes, donde alcanzaron concentraciones finales de 152 (mg/l) de este metal pesado, alcanzando una remoción del 80 %.
La celulosa de las raíces atrae el plomo presente en el agua, es el mecanismo por el cual E. crassipes es capaz de retener de forma amplia metales pesados, especialmente plomo (II) (Pizarro et al., 2016; Ibrahim et al., 2012).
Resultados de la producción de bioetanol
La producción de azúcar a través de la hidrólisis de los tres experimentos fue significativa. En la Tabla 4 se muestran los resultados de la producción de cada tipo de biomasa.
Tabla 4 La productividad de azúcares reductores con tres tipos de biomasa.
| (g/l) de azúcares primarios | Rendimiento después de 25 horas | |
|---|---|---|
| Biomasa 500 (mg/l) (E1) | 8 | 110 |
| Biomasa 750 (mg/l) (E2) | 6 | 75 |
| Biomasa de E. crassipes (E0) | 14 | 150 |
Hubo una producción constante en el proceso de hidrólisis. Se puede observar que las concentraciones de plomo (II) adheridas a la estructura de la planta sí afecta a la producción de azúcares reductores en este proceso. Este hidrolizado se pasa al siguiente biorreactor de producción de etanol.
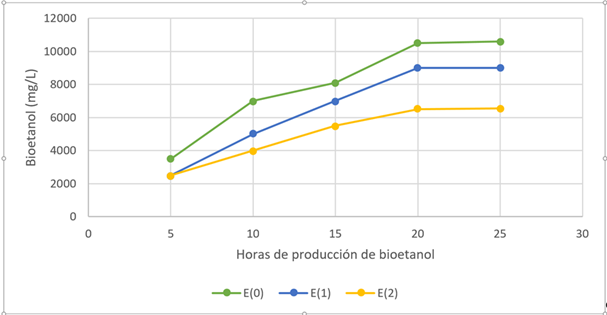
La Figura 3 muestra una producción de etanol más alta para la muestra de E. crassipes sin fitorremediación (E0), en comparación con muestras de biomasa de 500 (E1) y 750 (E2), en un tiempo de 24 horas.
Los tratamientos con la biomasa de E. crassipes con plomo (II) adherido comenzaron en las primeras cinco horas para producir etanol en cantidad menor que la biomasa sin plomo (II). En la Figura 3 se observan las curvas de crecimiento y la estabilización de cada cantidad de biomasa.
Al llevar a cabo el balance de masas se estableció que la producción de etanol a partir de biomasa hidrolizada de E. crassipes (E0) es rentable sin plomo adherido, con una cantidad de 10 000 (mg/l) en 25 horas. Estos diferentes resultados son similares a los estudios hechos por Lee et al. (2018), Zabed et al. (2016) y Kouwanou et al. (2018), donde la producción de bioetanol a partir de la biomasa de E. crassipes se produce con diferentes tipos de hidrólisis y con un agente de fermentación diferente. Estas investigaciones reportaron resultados eficaces, pero ninguno con biomasa cargados de metales pesados.
La biomasa del experimento de 750 (mg/l) (E2) de plomo (II) produjo una cantidad de 4 000 (mg/l) en 10 horas, menos que las otras dos muestras; posteriormente, en la hora 15, se estabilizó al llegar a 6 000 (mg/l) de bioetanol. Mientras que la biomasa del experimento de 500 (mg/l) (E1) alcanza los valores más altos al producir 7 000 (mg/) de bioetanol a la hora 15. Esta biomasa fue menos afectada que (E2); ambos experimentos demostraron algún grado de afectación, pero produjeron bioetanol a pesar de tener grandes cantidades de plomo (II) adherido.
Discusión
En diferentes investigaciones, las capacidades de E. crassipes para bioadsorber metales pesados han sido comprobadas, pero no se discute cuál es la disposición final de esta biomasa con material contaminante adherido a ella. También diferentes investigaciones han concluido que con la biomasa de esta planta se puede extraer biocombustibles debido a su gran cantidad de celulosa y hemicelulosa.
Se desarrolló un proceso sustentable debido al mal uso que se le da a la planta E. crassipes que abunda en las zonas húmedas de diferentes ciudades de Latinoamérica. El proyecto demostró que la fitorremediación con dicha planta es eficiente y también la biomasa utilizada en este tratamiento podría ser utilizado en procesos de hidrólisis y la posterior producción de biocombustibles.
La experimentación con dos tipos de biomasa E. crassipes cargado con diferentes concentraciones de plomo (II) mostró que podían usarse para producir bioetanol u otros biocombustibles, pues su afectación no es significativa. Toda la biomasa de E. crassipes puede emplearse para la fitorremediación, y más tarde para la producción de bioetanol u otros biocombustibles como el biohidrógeno.
Debe promoverse el uso de la planta E. crassipes para los procesos de fitorremediación y el posterior uso de esta biomasa para la producción de biocombustibles en gran escala; es necesario determinar los costos de este macroproyecto y el mercado de su uso en la fitorremediación y bioetanol.
Conclusiones
La biomasa sin carga de plomo (II) obtuvo resultados interesantes en la producción de bioetanol, con una cantidad de 10 000 (mg/l) en 25 horas. Para las muestras con 500 (mg/L) plomo (II) adherido (E1), se produjo un 10 % menos de etanol, siendo aproximadamente 9 000 (mg/l) en las mismas 25 horas. Mientras que el experimento de biomasa de E. crassipes utilizada en las remociones iniciales de plomo (II) de 750 (mg/l) alcanzó un rendimiento de 40 % menos de producción de bioetanol; esta biomasa se vio afectada por la cantidad de plomo (II) adherida. Toda la biomasa de E. crassipes se puede usar tanto para la fitorremediación como para la producción de bioetanol.
La gran presencia de esta planta en los humedales se debe utilizar para proyectos grandes de fitorremediación y producción de biocombustibles. Se recomienda formular un macroproyecto sostenible de fitorremediación y bioenergía utilizando el potencial de la planta de E. crassipes.