Introducción
En las últimas décadas, en México se ha incrementado la producción de planta forestal en viveros, con el objetivo de realizar reforestaciones y acciones de recuperación de zonas degradadas (Comisión Nacional Forestal [Conafor], 2010) y la tendencia sigue en ascenso. Uno de los materiales indispensables para la producción de la planta en vivero es el sustrato, especialmente si se utilizan contendores rígidos (tubetes). La turba de musgo Sphagnum L., conocido como “peat moss”, ha sido uno de los materiales más utilizados como sustrato en los viveros debido a la adaptabilidad que le confieren sus características físicas y químicas (Pane et al., 2011). Sin embargo, su uso ha ocasionado daños ambientales en las turberas debido a los volúmenes de extracción, además de que la demanda de sustratos ha incrementado el costo; No obstante, Caron y Rochefort (2013) indican que la utilización de turba, por ejemplo, no es un problema cuando se emplea en el manejo de humedales (Vandiver et al., 2015).
El uso eficiente de recursos involucrados en la producción de especies forestales en vivero, como los fertilizantes, ha motivado la búsqueda de sustratos alternativos, como son las enmiendas orgánicas a partir de mezclas de biosólidos y compostas. Los biosólidos son subproductos generados por plantas de tratamiento de aguas residuales. En la actualidad, estos residuos se siguen acumulando debido a que no tienen definido un aprovechamiento posterior, lo que hace necesaria una alternativa de reutilización, pues la mayor parte se deposita a cielo abierto con un impacto ambiental negativo.
Como opción, se ha propuesto utilizar este material como sustrato (mezclado con suelo u otras enmiendas), ya que presenta características físicas y químicas adecuadas para el crecimiento de las plantas en vivero; sin embargo, Wang et al. (2021) identificaron que los nutrientes y cationes aportados por los biosólidos pueden acidificar el suelo y modificar el grado de protección mineral de la materia orgánica, lo cual no siempre es conveniente para el desarrollo de especies forestales.
Existen antecedentes del uso de biosólidos como sustrato en la producción de Ceiba speciosa (A. St.-Hil., A. Juss. & Cambess.) Ravenna, cuya aplicación en altas proporciones generó individuos con altura, diámetro y biomasa superiores en comparación con la mezcla de fibra de coco (Alonso et al., 2018). Un resultado similar se registró con plantas de Pinus sylvestris L. producidas con mezclas de biosólidos con diatomita en proporción 75:25 y 50:50 (v/v), las cuales resultaron favorables solo para el diámetro; mientras que en sustrato a base de biosólidos al 100 % presentaron mayor altura, diámetro, biomasa aérea y radicular (Kose et al., 2020). Mañas et al. (2010) refirieron que los lodos activados mostraron mejores respuestas en el crecimiento de plántulas de Pinus halepensis Mill., así como en el contenido de nutrimentos foliares y en la tasa de germinación.
Sin embargo, es conveniente continuar analizando su factibilidad de uso, a pesar de que se ha discutido que la incorporación de biosólidos, especialmente al suelo forestal, y elevadas cantidades de metales pesados pueden ser tóxicos para los microorganismos, y reducir la absorción de nutrimentos esenciales en las plantas, pero en el suelo se incrementa, aunque de forma marginal, la concentración de elementos potencialmente tóxicos para las plantas (Bramryd, 2002, 2013).
En cuanto al uso de compostas, en el ámbito forestal también se han registrado efectos positivos, como lo describen Romero-Arenas et al. (2019) al usar composta a base de residuos de la producción del hongo Lentinula edodes (Berk.) Pegler, en la producción de planta de calidad de Pinus pseudostrobus Lindl. Además de ser una fuente de nutrición, se han observado resultados favorables del uso de té de composta, en forma de biofertilizante, contra agentes patológicos del género Fusarium Link (Otero et al., 2020). No obstante, la calidad de las compostas depende en gran medida de los materiales utilizados para su elaboración; por ello, surge la necesidad de investigar diferentes tipos de compostas y su efecto al mezclarlas con otros sustratos orgánicos, debido a que su combinación con biocarbón supera en 4 % el diámetro, en comparación con el uso de solo composta en plantas de Pinus banksiana Lamb. (Slesak et al., 2022).
Por otro lado, Simiele et al. (2022) describieron una respuesta contraria, debido a que el uso combinado de biocarbón y composta no mostró ningún efecto positivo sinérgico o acumulativo y provocó una reducción en el crecimiento y desarrollo de plantas de Popolus×euramericana Guinier en macetas.
Pinus leiophylla Schiede ex Schltdl. & Cham., originario de América del Norte y distribuido naturalmente en México, a lo largo de la Sierra Madre Oriental, Sierra Madre Occidental y Eje Neovolcánico, se le considera una de las coníferas con mayor abundancia en los bosques templados del país (Flores et al., 2023; Ramírez-Orozco et al., 2022). Tiene importancia ecológica significativa, especialmente, en áreas de transición y en zonas de frontera agrícola, donde puede crecer con restricciones de humedad y salinidad en el suelo, además de resistir siniestros, por su elevada capacidad de rebrote posincendio (Barton et al., 2023; Jimenez-Casas & Zwiazek, 2014).
En dicho contexto, el objetivo de este trabajo fue determinar el efecto de los biosólidos y compostas, como complementos del sustrato, en las características morfológicas y estado nutrimental de Pinus leiophylla producido en vivero. La hipótesis que se planteó fue ¿el uso de biosólidos y composta mezclados con suelo agrícola, mejora la morfología y estado nutrimental foliar de las plantas de P. leiophylla en vivero?
Materiales y Métodos
Ubicación del experimento
El experimento se llevó a cabo de octubre de 2022 a septiembre de 2023 en el Vivero Forestal Experimental de la División de Ciencias Forestales de la Universidad Autónoma Chapingo (UACh), con coordenadas geográficas 19°29′24” N y 98°52′15” O; ubicado a 2 283 msnm. Las semillas de Pinus leiophylla utilizadas procedían de un rodal natural localizado en San Felipe, Tlaxcala, México (19°29′05” N y 98°35′40” O; altitud de 2 500 msnm). Se sembraron el 25 de octubre; como almácigos, se trabajó con charolas de germinación con perlita como sustrato. El trasplante se realizó el 9 de noviembre a tubetes de polipropileno INNOVAPLAST ® con una capacidad de 305 cm3. El sitio experimental estaba cubierto por malla sombra de 70 % de transmisividad lumínica. El clima de la región es templado con temperatura media de 16.4 °C y precipitación media anual de 616.6 mm (Instituto Mexicano de Tecnología del Agua [IMTA], 2013).
Diseño experimental y de tratamientos
Se estableció un diseño experimental completamente al azar con los siguientes tratamientos:
Tratamiento 1. Testigo (T): 100 % suelo agrícola.
Tratamiento 2. M1: 70 % suelo agrícola+30 % biosólidos.
Tratamiento 3. M2: 70 % suelo agrícola+30 % composta orgánica.
Tratamiento 4. M3: 50 % suelo agrícola+30 % biosólidos+20 % composta.
Tratamiento 5. M4: 50 % suelo agrícola+20 % biosólidos+30 % composta.
Se definieron cinco repeticiones por tratamiento y la unidad experimental consistió en charolas forestales de polipropileno de 25 cavidades, cada una con una capacidad de 305 cm3 por cavidad o tubete.
Descripción de los sustratos
El suelo agrícola fue el sustrato base, debido a que es el principal insumo utilizado dentro del propio vivero forestal. Se cribó con una malla de metal de 6×6 mm de apertura y se aplicó Vapam (AMVAC ® Chemical Corporation, USA) en una dosis de 0.5 L en 20 L de agua. Presentó una textura franca, pH de 7.64, conductividad eléctrica de 0.6 dS m-1 y 1.03 % de materia orgánica; concentración de 0.2 % de N, 4.2 mg kg-1 de P y 4.02 cmol kg-1. Los biosólidos se obtuvieron de la Planta de Tratamiento de Aguas Residuales Atotonilco (PTARA) en Atotonilco de Tula, en el estado de Hidalgo. Cumplen con los parámetros y límites máximos permisibles que establece la Norma Oficial Mexicana NOM-004-SEMARNAT-2002 (NOM-004-SEMARNAT-2002, 2002), que permite su aprovechamiento para uso forestal y mejoramiento de suelo. Registraron un pH de 8.65, conductividad eléctrica de 2.3 dS m-1, materia orgánica 46.3 %, humedad del 68.7 % y una concentración de 4.12 % de N, 2.06 % de P y 0.26 % de K.
La composta se obtuvo a partir de abono de ganado ovino y bovino y de desechos domésticos. Presentó un pH de 9.1, conductividad eléctrica de 6.8 dS m-1, 33.3 % de materia orgánica y humedad de 36.2 %. La aportación nutritiva fue de 1.38 %, 0.74 % y 2.37 % de N, P y K respectivamente.
Variables por evaluar
A los 10 meses de edad de las plantas, se determinó el diámetro al cuello de la raíz (D, mm) con un calibrador vernier digital Steren ® Her-411; la altura total (H, cm) con un flexómetro Cadena ® MGA 5020, graduado en cm y mm. Las plantas se separaron en raíz, tallo y follaje y se metieron en una estufa eléctrica Shel Lab ® 1600 Hafo-Series, a 70 °C por 48 horas para determinar los pesos secos (g) con una báscula digital Sartorius ® PRO32F con un centigramo de precisión; se obtuvo el peso seco de la raíz (PSR, g), el peso seco aéreo (PSA, g) y el peso seco total (PST, g). Con estas variables se determinó la Tasa de Crecimiento Relativo en Diámetro (CRD, mm mes-1) y en Altura (CRH, cm mes-1) con la Ecuación 1 (Pallardy, 2008):
Donde:
CR = Crecimiento relativo
ln = Logaritmo natural
X 1 = Variable medida en la primera fecha
X 2 = Variable medida en la última fecha
Δt = Tiempo entre ambas mediciones
La primera fecha de medición fue en enero de 2023 y la última en septiembre de 2023. También, se determinaron los indicadores de calidad de planta, como la relación parte aérea-raíz (PAR), dividiendo el PSA y el PSR; índices como el Índice de Esbeltez (IE) al dividir la H entre el D (Johnson & Cline, 1991) y el Índice de Calidad de Dickson (ICD), Ecuación 2 (Dickson, 1960):
Donde:
PST = Peso seco total
PSA = Peso seco aéreo
PSR = Peso seco de la raíz
Análisis nutrimental
Se determinaron las concentraciones foliares de N, P, K, Ca, Mg, Mn, B, Cu, Fe y Zn; a partir de muestras compuestas de follaje de cinco plantas con cuatro repeticiones por tratamiento. El N se determinó mediante el método Semimicro-Kjeldahl (Bremner, 1965); el resto de los elementos se analizaron en el extracto resultante de la digestión HNO3:HCl4 (2:1, v:v) de tejido vegetal seco y molido, con un espectrofotómetro de emisión atómica (Agilent ® Series ICP-OES 725).
Análisis de datos
El efecto de tratamientos sobre las variables morfológicas, de calidad y nutrimentales se obtuvieron mediante un Análisis de Varianza (ANOVA) en el software R versión 4.3.1 (R Core Team, 2022), con una confiabilidad de 95 % (p<0.05). Para identificar diferencias entre las mezclas, se hizo una comparación de medias con la prueba de Tukey (α=0.05). El diagnóstico del estado nutrimental se realizó mediante el método gráfico de vectores (Timmer & Stone, 1978) y con la interpretación de los nomogramas (López-López & Alvarado-López, 2010); se consideró como punto de referencia el estado nutrimental del tratamiento Testigo. El modelo estadístico empleado fue el siguiente (Ecuación 3):
Donde:
Resultados y Discusión
Variables morfológicas e índices de calidad
El ANOVA indicó diferencias altamente significativas en todas las variables de estudio (p=0.0001); en particular, la mezcla M1 (70 % suelo agrícola+30 % biosólidos), registró los valores más altos de todas las variables morfológicas e índices de calidad, excepto en el peso seco de la raíz y el Índice de Esbeltez (Cuadro 1).
Cuadro 1 Promedio y desviación estándar de las variables morfológicas e índices de calidad de plantas de Pinus leiophylla Schiede ex Schltdl. & Cham. en etapa de vivero producidas en diferentes mezclas de sustratos.
| Variable | Tratamiento | ||||
|---|---|---|---|---|---|
| Testigo | M1 | M2 | M3 | M4 | |
| D (mm) | 3.81±1.00d | 7.50±2.90a | 2.51±0.60e | 6.29±2.50b | 5.03±2.00c |
| H (cm) | 9.23±3.00c | 18.83±90a | 7.45±4.30d | 18.53±12.80a | 14.51±5.90b |
| PSR (g) | 0.75±0.10d | 1.32±0.20b | 0.38±0.10e | 1.54±0.30a | 0.99±0.10c |
| PSA (g) | 0.72±0.10c | 3.45±1.00a | 0.51±0.10c | 3.2±1.10a | 1.95±0.40b |
| PST (g) | 1.47±0.30c | 4.77±1.80a | 0.89±0.20d | 4.75±2.20a | 2.94±1.00b |
| CRD (mm mes-1) | 0.20±0.01d | 0.28±0.02a | 0.16±0.02e | 0.25±0.01b | 0.23±0.02c |
| CRH (cm mes-1) | 0.13±0.01c | 0.23±0.01a | 0.12±0.01c | 0.21±0.01a | 0.19±0.01b |
| PAR | 0.98±0.04d | 2.47±0.6a | 1.45±0.30c | 2.19±0.30b | 2.04±0.10b |
| IE | 2.54±0.40b | 2.68±0.90ab | 3.1±0.60a | 3.08±0.60a | 3.06±0.70a |
| ICD | 0.44±0.05c | 0.94±0.10a | 0.21±0.02d | 0.96±0.20a | 0.62±0.1b |
Testigo = 100 % suelo agrícola; M1 = 70 % suelo agrícola+30 % biosólidos; M2 = 70 % suelo agrícola+30 % composta orgánica; M3 = 50 % suelo agrícola+30 % biosólidos+20 % composta; M4 = 50 % suelo agrícola+20 % biosólidos+30 % composta. D = Diámetro (mm); H = Altura (cm); PSR = Peso seco de la raíz; PSA = Peso seco aéreo; PST = Peso seco total; CRD = Crecimiento relativo en diámetro; CRH = Crecimiento relativo en altura; PAR = Relación parte área-raíz; IE = Índice de Esbeltez; ICD = Índice de Calidad de Dickson. Letras diferentes dentro de una columna indica diferencias (p<0.05) con Tukey.
La M1 superó al tratamiento Testigo por 3.69 mm, 9.6 cm y 3.3 g en diámetro, altura y peso seco total, respectivamente. Además, registró mayores valores de crecimiento relativo en diámetro (0.08 mm mes-1) y altura (0.1 cm mes-1). Los resultados anteriores respecto a los de peso seco aéreo indican una mejor condición de salud de las plantas, ya que presentan mayor follaje, lo que se asocia con los procesos fisiológicos y las raíces de las plantas (Moreno et al., 2021).
Respecto al sustrato M2 (70 % suelo agrícola+30 % composta orgánica) se obtuvieron valores bajos en todas las variables, excepto para el Índice de Esbeltez, cuyos registros fueron inferiores a los del Testigo (1.3 mm en diámetro y 1.78 cm en altura). El valor de PST fue de 0.89 g (0.58 g menos que el Testigo) y 3.88 g menos que la mezcla M1.
Los resultados morfológicos sugieren que la incorporación de biosólidos (30 %) como parte del sustrato es favorable para la producción de planta de Pinus leiophylla. Las mezclas M1 y M3 que incluyeron la porción de 30 % de biosólidos, superaron los 4 mm en diámetro y 15.25 cm en altura y, de acuerdo con los parámetros de calidad recomendados por la Comisión Nacional Forestal, garantizan una mayor supervivencia de la planta en campo (Conafor, 2010). Por otro lado, de acuerdo con la Norma Mexicana NMX-AA-170-SCFI-2016, un diámetro ≥4 mm es aceptable como indicador de calidad de planta en vivero para Pinus leiophylla (NMX-AA-170-SCFI-2016, 2016). Estos datos comparados con el Testigo reflejan que el uso de fuentes de nutrición en vivero favorece de manera directa la morfología de la planta (Grossnickle & MacDonald, 2018; Heras-Marcial et al., 2023). También concuerdan con lo observado por Melo et al. (2019), quienes refieren que los biosólidos combinados con sustratos como la corteza de Bactris gasipaes Kunth (1:2, 1:3 v:v) propician mayores valores en altura, diámetro y materia seca en plantas de Schinus terebinthifolius Raddi de 120 días de edad.
El diámetro promedio de todos los tratamientos fue de 5.03 mm, cifra más alta en comparación con otros individuos de Pinus leiophylla de un año de edad (3.5 mm) producidos bajo un sistema tecnificado con fertilizantes de liberación controlada (Palacios et al., 2015). El promedio de altura fue de 13.7 cm y el Índice de Calidad de Dickson de 0.634, los cuales superan a lo descrito por Buendia et al. (2020) al aplicar fertilización exponencial a ejemplares de Pinus leiophylla de seis meses en vivero. De igual manera, en otro experimento con árboles de la misma especie de cuatro meses de edad y tratamientos de fertilización constante y exponencial, los valores de diámetro, altura, ICD y peso seco total fueron inferiores (Buendia et al., 2016) con una altura promedio menor (13.71 cm), en comparación con individuos de siete meses producidos en sistema de bolsas de polietileno (28.4 cm) (Pineda et al., 2020).
En cuanto al ICD, las mezclas M1, M3 y M4 mostraron valores superiores a 0.5, que indican alta calidad de planta producida de acuerdo a la clasificación de Rueda-Sánchez et al. (2014) y Sáenz et al. (2018). El Índice de Esbeltez (IE) es un indicador de la resistencia de la planta a la desecación por el viento, de la supervivencia y del crecimiento potencial en sitios secos, y su valor debe ser menor a 6; en este caso, todos los tratamientos fueron inferiores a 6 (Rueda-Sánchez et al., 2014). Respecto a la relación parte aérea-raíz (PAR), de acuerdo con Rueda-Sánchez et al. (2014), la planta producida en las mezclas M1, M3 y M4 son clasificadas como planta de media calidad. El indicador relaciona la parte aérea-parte raíz, de acuerdo con los autores, si la biomasa aérea es mayor a la de raíz, esto se asocia con una escasa precipitación y un desarrollo radicular que no es suficiente para proveer a la parte aérea de la planta (Thompson, 1985).
Concentración nutrimental foliar
El tratamiento M1 registró las mayores concentraciones foliares en Mn y B. El Tratamiento M3 (50 % suelo agrícola+30 % biosólidos+20 % composta) supera por 0.35 % de N al Testigo que fue el que presentó menor valor. Al Tratamiento M2 (70 % suelo agrícola+30 % composta orgánica) correspondieron los números más altos de P y K, por encima del Testigo por 96.9 mg kg-1 y 2 638.8 mg kg-1, respectivamente. El Testigo exhibió las mayores concentraciones foliares de Ca, Mg, Cu y Zn, mientras que para el Fe no se obtuvieron diferencias significativas (Cuadro 2).
Cuadro 2 Promedios y desviación estándar de las concentraciones nutrimentales foliares de plantas de Pinus leiophylla Schiede ex Schltdl. & Cham. producidas en vivero en diferentes mezclas de sustratos.
| Variable | Tratamiento | ||||
|---|---|---|---|---|---|
| Testigo | M1 | M2 | M3 | M4 | |
| N (%) | 0.63 ±0.10b | 0.93 ±0.20ab | 0.91 ±0.10ab | 0.98 ±0.10a | 0.89 ±0.20ab |
| P (mg kg-1) | 1 318.50 ±127.40ab | 1 210.10 ±134.60ab | 1 415.40 ±65.10a | 1 175.10 ±82.60b | 1 271.50 ±59.70ab |
| K (mg kg-1) | 2 258.60 ±157.00b | 2 583.10 ±185.00cd | 4 897.40 ±144.00a | 3 159.50 ±216.00bc | 3 692.20 ±412.00b |
| Ca (mg kg-1) | 5 619.40 ±547.70a | 4 432.10 ±218.30b | 3 561.80 ±293.80c | 3 721.20 ±347.1bc | 3 184.20 ±246.00c |
| Mg (mg kg-1) | 2 092.10 ±26.90a | 1 463.40 ±114.70b | 1 667.60 ±166.60b | 1 445.90 ±77.50b | 1 450.90 ±83.50b |
| Mn (mg kg-1) | 34.60 ±3.20b | 122.40 ±29.00a | 19.30 ±0.80b | 52.80 ±13.00b | 23.07 ±2.00b |
| B (mg kg-1) | 28.71 ±1.90b | 37.10 ±4.90a | 35.90 ±2.10ab | 34.21 ±3.00ab | 32.64 ±2.60ab |
| Cu (mg kg-1) | 880.00 ±585.00a | 32.48 ±26.40b | 38.09 ±32.50b | 9.79 ±2.50b | 7.02 ±0.50b |
| Fe (mg kg-1) | 201.50 ±62.00a | 157.37 ±18.60a | 145.80 ±23.90a | 142.70 ±26.20a | 161.60 ±22.30a |
| Zn (mg kg-1) | 72.20a | 41.01ab | 15.00b | 31.59b | 22.69b |
Testigo= 100 % suelo agrícola; M1 = 70 % suelo agrícola+30 % biosólidos; M2 = 70 % suelo agrícola+30 % composta orgánica; M3 = 50 % suelo agrícola+30 % biosólidos+20 % composta; M4 = 50 % suelo agrícola+20 % biosólidos+30 % composta. Letras diferentes dentro de una columna indica diferencias (p<0.05) con Tukey.
Las tendencias se comportan de forma similar en las concentraciones de N (Figura 1A), K (Figura 1C) y B (Figura 1G). Por otro lado, las gráficas de Ca (Figura 1D), Mg (Figura 1E), Cu (Figura 1H), Fe (Figura 1I) y Zn (Figura 1J) reflejan otro grupo de tendencia, lo que fue común en todas las mezclas, pues reflejaron un incremento del peso seco de las acículas. El P (Figura 1B) a excepción de M2, muestra la misma tendencia que el segundo grupo. Esto también se observa para el Mn (Figura 1F ),a excepción de la M2, cuya tendencia coincide con la del primer grupo.
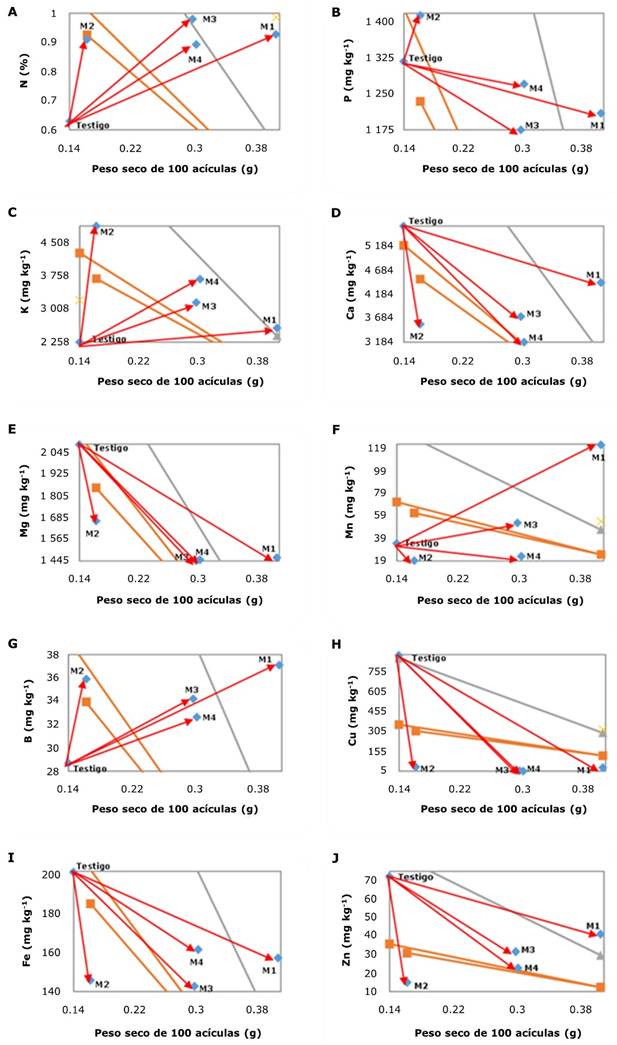
Testigo = 100 % suelo agrícola; M1 = 70 % suelo agrícola+30 % biosólidos; M2 = 70 % suelo agrícola+30 % composta orgánica; M3 = 50 % suelo agrícola+30 % biosólidos+20 % composta; M4 = 50 % suelo agrícola+20 % biosólidos+30 % composta.
Figura 1 Nomogramas de Timmer de las concentraciones nutrimentales foliares de Pinus leiophylla Schiede ex Schltdl. & Cham. producido en vivero en diferentes mezclas de sustratos.
El tratamiento Testigo resultó deficiente en N, K y B, lo cual se subsanó con los tratamientos con biosólidos (M1), composta (M2) y sus combinaciones (M3 y M4), y explica las respuestas positivas en el peso seco de acículas (Figura 1). La promoción del crecimiento por parte de los biosólidos y las compostas, solo aplicados al suelo o combinados con composta, generó la dilución de P, Ca, Mg, Cu, Fe y Zn en el follaje de las plantas, ello indica que ni los biosólidos, ni la composta fueron suficientes para cubrir los requerimientos de las plantas por estos nutrimentos (López-López & Alvarado-López, 2010). Los resultados son equiparables a los obtenidos por Buendía et al. (2016), quienes señalan el promedio de N (0.87 %), P (1 278 mg kg-1) y K (3 318 mg kg-1) de todos los tratamientos estuvo por debajo del promedio de N (2.65 %), P (2 303 mg kg-1) y K (4 235 mg kg-1) con fertilización química, manteniendo la relación nutrimental de los elementos, y el N es menor en 1.6 %, 879 mg kg-1 en P y en 773.34 mg kg-1 de K.
En comparación con otras especies forestales, las concentraciones foliares de P y K son menores de lo que se consigna para plántulas de 10 meses de Pinus greggii Engelm. ex Parl. en vivero, pero no las de N (Vicente-Arbona et al., 2019). Martínez-Nevárez et al. (2023) obtuvieron en un ensayo de fertilización controlada en Pinus cooperi C. E. Blanco de un año de edad, mayores valores en N por 0.4 %, en comparación con el tratamiento Testigo y por 0.4 % en la mezcla M3, pero menor valor promedio en P (787 mg kg-1). Aguilera-Rodríguez et al. (2021) en un ensayo con Pinus patula Schltdl. & Cham. de siete meses de edad y diferentes tipos de aserrín y fertilizantes químicos, citan mayores valores en N (1.39 %), P (2 055 mg kg-1), K (48 855 mg kg-1) y Mn (287 mg kg-1); mientras que Ca (2 264 mg kg-1), Mg (791 mg kg-1), B (19 mg kg-1), Cu (11 mg kg-1), Fe (68 mg kg-1) y Zn (27 mg kg-1) fueron mayores en este estudio. Lo anterior puede ser un reflejo del propio sustrato y fuente de nutrición, en este caso los biosólidos, además de la diferencia entre especies. Lo anterior es un indicativo de la importancia de conocer la proporción adecuada de biosólidos para no aumentar la concentración de nutrimentos como el Cu y Zn en las plantas. Sin embargo, de manera general, la adición de biosólidos en solitario con el suelo y mezclada con composta reflejó un aumento en las características morfológicas de las plántulas, que coincide con lo observado en otras especies como Pinus cembroides Zucc. (Madrid-Aispuro et al., 2020) después de 14 meses en vivero. Se ha mostrado viabilidad en el uso de composta en vivero como una alternativa de sustrato en especies como Juniperus polycarpos K. Koch (Negi et al., 2022) y Castanea sativa Mill. (Fuertes-Mendizábal et al., 2021), con proporciones más bajas a las aplicadas en este estudio.
Conclusiones
Las características morfológicas de las plantas de Pinus leiophylla producidas en sustratos a base de biosólidos y compostas desarrollan mejor diámetro, altura y biomasa, en comparación con las producidas en suelo agrícola (Testigo). Los índices de calidad de planta y las concentraciones nutrimentales en follaje muestran que el uso de biosólidos para la producción de planta forestal son una buena alternativa, con impactos benéficos en el ahorro de fertilizantes químicos. Los tratamientos ensayados fueron aplicados aun cuando los biosólidos presentaron intervalos de pH por arriba de la recomendación; sin embargo, proporciones equilibradas con suelo y composta son agronómicamente viables para la producción del género Pinus. En perspectiva, se reconoce la aplicación de biosólidos en especies no comestibles, como algodón, flor de corte y otras especies forestales, por lo que se sugiere continuar con el análisis sobre la viabilidad del uso de biosólidos como complemento al suelo.
















