Introducción
Desde la década de los 80´s, las biotecnologías reproductivas en bovinos han evolucionado eficientemente, mediante el desarrollo de diversas técnicas, lo que ha ayudado a aumentar rápidamente la capacidad reproductiva y aumentar el costo económico de cada ternero nacido1. Las técnicas que mayor aplicación han tenido son la transferencia de embriones (TE), la criopreservación de embriones así como la manipulación de embriones (bipartición), con el fin de obtener más animales con mayor potencial de productividad2).
La bipartición de embriones bovinos es una técnica muy útil para generar gemelos homocigotos y una ventaja importante es la de obtener un mayor aprovechamiento de embriones de alto valor genético2,3; otra ventaja de esta técnica es la de aumentar el número de oportunidades que tiene un embrión para implantarse y así tener un mejor aprovechamiento del material genético y de las hembras receptoras4. Las tasas de preñez de embriones bovinos frescos bipartidos y transferidos frescos van del 55 al 61%, y son similares a la tasa de preñez de embriones transferidos completos, que es del 50 al 60 %5.
La transferencia de embriones es una técnica que se implementa en programas de progreso genético, que buscan obtener un mayor número de crías de hembras donantes con un alto potencial productivo6; además, estos programas se complementan con la criopreservación de embriones que no son transferidos en fresco o de embriones que se destinan para su comercialización y almacenamiento para su posterior transferencia7.
Uno de los métodos de criopreservación de embriones es la técnica de vitrificación, que permite el paso del estado líquido al sólido sin formación de cristales de hielo intracelulares8. La vitrificación es una técnica opcional de conservación de embriones con porcentajes de viabilidad óptimos, siendo además una técnica sencilla, fácil de ejecutar y rentable9. Los porcentajes de gestación después de la transferencia de embriones bovinos calentados (desvitrificados) van del 45 al 65 %10,11,12.
En el trópico mexicano, el sistema de producción bovino predominante es el llamado de doble propósito, donde comúnmente existen vacas donantes de embriones de alto valor. Con base en lo anterior y ante la escasa información reciente acerca de este tema, el objetivo de este estudio fue evaluar el efecto de la bipartición de embriones bovinos vitrificados y calentados, sobre el desarrollo in vivo e in vitro; de no haber un efecto negativo, esto permitiría aumentar el número de crías obtenidas por embrión y un óptimo aprovechamiento de ellos.
Material y métodos
Producción de embriones y tratamientos
Se contó con un banco de 90 blastocistos calidad 1 (de acuerdo a la clasificación de le IETS) Bos taurus x Bos indicus, producidos in vivo criopreservados por vitrificación en Cryotop® (Kitazato Supply, Fujinomiya, Japón)13.
El desarrollo in vitro fue evaluado mediante cultivo embrionario (CE) por 72 h post calentamiento. La evaluación del desarrollo in vivo se realizó determinando la tasa de gestación después de la transferencia de embriones (TG). Cada experimento se dividió en dos grupos: CE1= cultivo de 11 embriones bipartidos (22 hemiembriones) y CE2= cultivo de 10 embriones completos; TG1= tasa de gestación de receptoras transferidas con hemiembriones (n= 62) y TG2= tasa de gestación de receptoras transferidas con embriones completos (n= 38).
Vitrificación de embriones
Los embriones fueron vitrificados de acuerdo a lo descrito previamente14. Los embriones y hemiembriones se colocaron en una gota de 25 ul de solución de equilibrio (SE; PBS con 7.5 % v/v de etilen glicol y 7.5 % v/v de dimetilsulfóxido), durante 10 min. Después de esto, los embriones y hemiembriones se pasaron por 4 gotas de 25 ul en solución de vitrificación (SV; PBS con 15 % v/v de etilen glicol y 15 % v/v de dimetilsulfóxido) durante un min en total, es decir, desde que se colocaron en la primera gota hasta la cuarta gota. Inmediatamente despúes los embriones y hemiembriones se colocaron en el dispositivo cryotop en el mínimo volumen posible (aproximadamente de 1 a 2 ul) y se sumergieron en nitrógeno líquido.
Calentamiento de embriones
Para esto se utilizó solución de calentamiento (SC), (solución buffer fosfato (PBS) con 20 % de sustituto de suero sintético (SSS) y 1 M sacarosa), solución de dilución (SD), (PBS con SSS a 20 % y sacarosa 0.5 M), y solución de lavado (SL), (PBS con 20 % SSS). El Cryotop® se sacó del nitrógeno líquido, se destapó y se sumergió en SC durante 1 min, en SD durante 2 min en cada gota de 25 ul y en SL durante 3 min en cada gota de 25 ul14. Después, los embriones se colocaron en medio de cultivo y los embriones a transferir en PBS y se colocaron en pajillas de 0.25 ml para su transferencia a las receptoras.
Bipartición de embriones
Después del calentamiento y antes de ser introducidos para cultivo embrionario o para ser transferidos, se bipartieron 53 embriones, mediante la modificación de la técnica descrita por Lopes et al5, que consiste en colocar el embrión en una placa de Petri desechable (100 x 15 mm; Corning(, New York, USA) con medio de micro manipulación (DPBS, Dulbecco's Phosphate-Buffered Saline). La división se realizó con un micromanipulador (MWS-1A, Narishige, Tokio, Japón) colocado en un microscopio invertido (CK2, Olympus(, Tokio, Japón), al que se le adaptó una microcuchilla, haciendo el corte de tal manera de dividir en partes iguales la masa celular interna. Después de la bipartición, los hemiembriones se colocaron en medio de cultivo o cargados en pajillas de 0.25 ml para ser transferidos a las receptoras.
Evaluación del desarrollo embrionario in vitro
Cultivo de embriones
Se utilizaron 21 embriones calentados, de los cuales 11 fueron bipartitos, resultando 22 hemiembriones (CE1) y los 10 restantes se cultivaron enteros (CE2). Todos los hemiembriones y embriones se cultivaron en medio IVC3 (In Vitro Care, Maryland, EE. UU.) en una incubadora a 38.5 ºC, 5 % de CO2 en aire y humedad del 95 %. Estos fueron revisados cada 24 h durante 72 h, para evaluar el desarrollo de la multiplicación de los blastómeros (reexpansión) y de los embriones completos hasta la eclosión15.
Evaluación del desarrollo embrionario in vivo
Transferencia de embriones
La Comisión de Bioética y Bienestar Animal de la FMVZ-UV aprobó el uso de animales y los procedimientos incluidos en el estudio. Para la transferencia de embriones (n= 69), se seleccionaron 100 hembras receptoras Bos Taurus x Bos Indicus, con una edad promedio de 60 ± 2.71 meses, 2.26 ± 1.04 partos, 454 ± 6.09 kg de peso, condición corporal entre 2.5 y 3.0 (escala de 5 puntos: 1= demacrado y 5= obeso)16 y clínicamente sanas. Las receptoras se evaluaron mediante palpación transrectal para corroborar su estado cíclico. Se utilizaron receptoras que estuvieran ciclando, es decir, que contaran con un cuerpo lúteo en alguno de los dos ovarios y que no se detectaran patologías en el tracto reproductivo. Las receptoras estuvieron en pastoreo rotacional de pasto Pangola (Digitaria eriantha) y pasto insurgente (Brachiaria brizantha), recibieron sales minerales, agua ad libitum y cada una recibió 4 kg de alimento concentrado por día (el alimento contenía 20 % de proteína cruda y se administró 30 días antes y 30 días después de la TE). El día -60 (día 30= inicio del tratamiento TE), las receptoras recibieron vía intramusculares vitaminas A, D y E 1(1,250 000, 35 0000 y 350 UI respectivamente; Synt-ADE®, Zoetis, México), selenio más vitamina E (40 y 400 mg, respectivamente; Selenie®, Virbac, México) y fósforo (2 g; Phospho 20®, Virbac, México).
Sincronización de la ovulación de las receptoras
Para la transferencia de embriones las receptoras se dividieron en dos tratamientos, TG1: 62 (hemiembriones) y TG2: 38 (embriones completos). El día 0, las receptoras recibieron un dispositivo intravaginal con 1,9 g de progesterona (CIDR®, Zoetis, México), y 2,5 mg de benzoato de estradiol i.m. (Benzoato de Estradiol®, Zoetis, México). El día 5 se aplicó 400 UI de gonadotropina coriónica equina eCG i.m. (Novormon®, Zoetis, México) y 25 mg de dinoprost trometamina i.m. (Lutalyse®, Zoetis, México). El día 8, se retiró CIDR-B® y se aplicó 1 mg de cipionato de estradiol i.m. (E.C.P.®, Zoetis, México)17.
Transferencia no quirúrgica de embriones
La transferencia embrionaria sólo se realizó en aquellas hembras que presentaban un cuerpo lúteo de calidad 1 (20 mm de diámetro) detectado por ecografía. La transferencia embrionaria se realizó 9 días después de retirado el CIDR-B®; se administró anestesia epidural 5 min antes de la transferencia (100 mg, Lidocaine®, Lab MSD). Los embriones completos o hemiembriones se colocaron en el cuerno uterino ipsilateral del cuerpo lúteo18. Cada una de las receptoras recibió un hemiembrión (n= 62) o un embrión completo (n= 38).
Diagnóstico de gestación
El día 60 post-transferencia, se realizó el diagnóstico de gestación mediante ecografía. Este tiempo de espera es necesario, ya que existe información de que, si se realiza antes de los 60 días de gestación, principal período de organogénesis, constituye una causa iatrogénica importante de daño irreversible o pérdida fetal19.
Análisis estadístico
Para el análisis de la tasa de gestación se utilizó un modelo de umbral mixto20,21,22 con PROC GLIMMIX (SAS, 2014). Condicionada a efectos fijos y aleatorios, se supuso que la tasa de gestación seguía una distribución de Bernoulli. Para analizar la tasa de gestación y la viabilidad de los hemiembriones frente a la de embriones completos a las 24, 48 y 72 h, el modelo incluyó solo el efecto del tratamiento. La función de enlace utilizada fue la función probit. Las soluciones para efectos fijos aleatorios se basaron en técnicas de máxima verosimilitud utilizando el algoritmo de matriz de información promedio para estimar los componentes de la varianza. Para el cálculo de los grados de libertad se utilizó el enfoque de Satterthwaite. Las comparaciones entre los efectos de las medias considerados en el modelo se realizaron con base en la diferencia mínima significativa de Fisher.
Resultados
Viabilidad in vitro de hemiembriones y embriones completos
Para el tratamiento CE1 se encontró una viabilidad de 86.3 % (19/22) a las 24 h, disminuyendo a 81.8 % (18/22) a las 48 h y finalmente al 77.3 % (17/22) a las 72 h de la multiplicación de blastómeros (reexpansión; Figura 1).
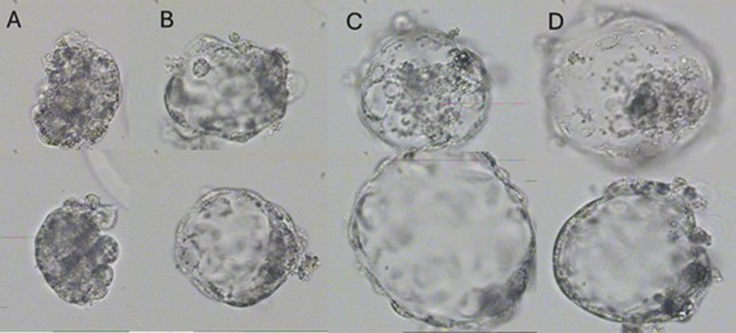
Figura 1 Cultivo de hemiembriones por 72 h A) Hemiembriones a 0 h de cultivo, B) Reexpansión de hemiembriones a las 24 h, C) Reexpansión de hemiembriones a las 48 h, D) Reexpansión de hemiembriones a las 72 h
Para el tratamiento CE2, los embriones enteros cultivados tuvieron una viabilidad en la primera revisión 24 h del 90 % (9/10), para las 48 h se mantuvo la misma tasa de expansión (90 % (9/10), pero a las 72 h el porcentaje de eclosión alcanzó el 80 % (8/10; Figura 2).
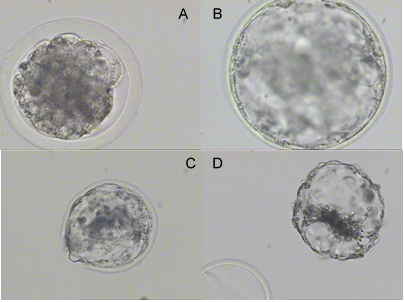
Figura 2 Cultivo de embriones completos: A) Embrión recién calentado (0 h), B) Embrión cultivado a las 24 h, C) Embrión cultivado a las 48 h, D) Embrión cultivado a las 72 h
Al momento de analizar la viabilidad embrionaria de ambos grupos, no se encontró diferencia estadística (P>0.05) en los diferentes tiempos de evaluación (Cuadro 1).
Viabilidad in vivo de hemiembriones y embriones completos
Tasa de gestación con embriones producidos in vivo, vitrificados, bipartitos y completos
Para el tratamiento TG1 (n= 62 hemiembriones), se obtuvo una tasa de gestación del 19.35 % (12/62). Las transferencias restantes pertenecieron al tratamiento TG2 (n= 38) con embriones completos, se encontró un 31.6 % (12/38) en tasa de gestación (Cuadro 2).
Cuadro 2 Tasa de gestación de hemiembriones y embriones enteros
| Embriones (n) |
Transferencias (n) |
Gestantes (n) |
Tasa de gestación por transferencia (%) |
|---|---|---|---|
| TG1: Bipartido (31) | 62 | 12 | 19.3 |
| TG2: Completo (38 | 38 | 12 | 31.6 |
(P>0.05).
Por lo tanto, para ambos grupos no se encontraron diferencias estadísticas (P>0.05). Tanto el grupo de hemiembriones como el de embriones completo obtuvieron un total de 12 gestaciones, pero con la diferencia que en el grupo de hemiembriones se utilizó una menor cantidad de embriones.
Discusión
En el presente estudio la tasa de viabilidad promedio de hemiembriones y embriones completos fue del 78.65 % utilizando el medio IVC3. Existe escasa información acerca de en el desarrollo de embriones bovinos que fueron producidos in vitro, bipartidos, vitrificados y desvitrificados, por lo tanto, el presente trabajo contribuye al conocimiento sobre la viabilidad de hemiembriones y embriones bovinos completos producidos in vivo.
Con base en los resultados del presente estudio en cultivo embrionario se encontró 86.3 % y 90 % de viabilidad para hemiembriones y embriones completos 24 h post calentamiento. Este porcentaje es mayor que lo reportado previamente en conejos23; en ese estudio utilizaron 125 embriones de conejo producidos in vivo, un grupo fue de embriones fueron vitrificados y bipartidos (como en el presente trabajo) y otro de bipartidos y luego vitrificados; la tasa de desarrollo in vitro fue del 36 % en los vitrificados/bipartidos y del 10 % para los bipartidos/vitrificados. Estos investigadores mencionan que esto pudo deberse a que los hemiembriones pierden cohesion y reducción del número de células, y que la bipartición deja que las céulas queden expuestas a los criopretectores utilizados en la vitrificación, los cuales pueden ser tóxicos y afectar el desarrollo embrionario; por tanto, concluyeron que la calidad del embrión es el principal factor del éxito de estos procedimientos. Otros investigadores mencionan que se ha comprobado que las células de la masa interna (alrededor del 10 %) se dañan debido al procedimiento de división24 y que una proporción adicional de células morirá durante la congelación y descongelación. Al respecto, cabe mencionar que, si bien en el presente estudio no se realizó tinción para determinar la viabilidad, el hecho de obtener una tasa de 77.3 y 80 % de viabilidad in vitro 72 h post calentamiento, para hemiembriones y embriones enteros, demuestra que al menos bajo las condiciones del presente trabajo, la bipartición de embriones vitrificados/calentados no afectó el desarrollo in vitro de hemiembriones y embriones enteros (P>0.05). Es importante mencionar que en el presente estudio se utilizaron solamente embriones grado 1, mientras que en el estudio antes mencionado se utilizaron embriones calidad 1 y 2.
La criopreservación reduce la división embrionaria. Algunos estudios han reportado tasas de desarrollo del 52 % para embriones biopsiados congelados-descongelados en comparación con el 60 % para embriones frescos. Por otra parte, se han publicado tasas de supervivencia del 86 % para embriones vitrificados y calentados a los cuales se les había realizado la eclosión asistida25.
La tasa de gestación general (TG= 25.5 %) obtenida en el presente estudio con hemiembriones y embriones completos en receptoras de doble propósito fue inferior a la reportada por otros autores26,27,28, sin embargo, estas variaciones que se obtienen en los TG dependen de varios factores relacionados, por un lado, con la receptora y por otro con el embrión que se transfiere29,30,31. Los principales factores que se han correlacionado con el éxito de la gestación son: calidad del embrión, método de criopreservación, protocolo de sincronización, además del técnico que lo transfiere12; sin embargo, en el presente estudio solo se utilizaron blastocitos calidad 1, se evaluó su viabilidad después de la descongelación y el técnico que realizó las transferencias fue el mismo, por lo que estos factores probablemente no afectaron los resultados de la gestación.
Respecto al protocolo de sincronización de receptores basado en CIDR-B, se ha reportado que estos influyen en los TG a partir de la calidad del cuerpo lúteo formado y el ambiente que se propicia en el útero luego de la sincronización31. En esta investigación no se encontró diferencia en el tamaño del cuerpo lúteo (≥20 mm) al momento de la transferencia en TG; lamentablemente no fue posible medir P4 en suero sanguíneo para reafirmarlo, sin embargo resultados similares fueron reportados32, no encontrándose relación entre el diámetro del cuerpo lúteo (>1.6 cm) y su función (P4 en plasma >1 ng/ml) el día 6 de ovulación en novillas tratadas con CIDR-Bs y BE como base del protocolo. En contraste17, otros investigadores reportaron un aumento de los TG en novillas receptoras (cruces Bos indicus) al presentar mayor diámetro del cuerpo lúteo al momento de la transferencia embrionaria, las receptoras fueron clasificadas según el área del cuerpo lúteo como CL1 (> 2.0 cm2), CL2 (1.5-2.0 cm2) y CL3 (<1.5 cm2), y los TG obtenidos fueron 58.4, 41.5 y 31.8 %, respectivamente. Estas diferencias sugieren que durante la fase intermedia entre la fase de crecimiento (hasta el día 7) y la fase estática del cuerpo lúteo (día 8 al 16), el flujo sanguíneo lúteo puede ser más indicativo de la función del cuerpo lúteo que su tamaño máximo alcanzado en TG33. Esta posibilidad sugiere que la fase lútea inducida en las receptoras del presente estudio fue la adecuada en duración, y lo que seguramente estuvo comprometido fue el desarrollo temprano de los embriones, al grado que no fueron capaces de generar la señal adecuada de reconocimiento temprano del embarazo (interferon-()34,35,36. En este sentido, en el caso de hemiembriones, se debe tener en cuenta que un factor que puede afectar la implantación de los embriones es un fallo durante la señal que envía el embrión en el reconocimiento materno mediante la producción de interferón- (37,38, los hemiembriones pueden tener una menor producción de interferón porque tienen menos células del trofoectodermo38,39. Por eso es importante mencionar que para realizar el reconocimiento embrionario materno, es que el embrión debe encontrar un ambiente uterino apropiado, influenciado por la progesterona producida por un cuerpo lúteo de buena calidad, ya que estimula la producción de una variedad de secreciones endometriales, como MUC-1 (mucina glicoproteína-1), lactógeno placentario y osteopontina, necesarios para el correcto desarrollo de los embriones37. En otra investigación acerca de la bipartición de embriones38, compararon la tasa de gestación de receptoras transferidas con embriones frescos producidos in vivo completos y hemiembriones, obteniendo mayor tasa de gestación con embriones completos (67 %) que con hemiembriones (35 %) (P<0.05). Estos resultados son mayores a los del presente estudio donde no se encontró diferencia estadística entre embriones completos y hemiembriones (31.6 vs 19.3 % repectivamente). Una de las posibles causas del mayor porcentaje es que utilizaron novillas de raza Holstein, las cuales resultan ser una raza de origen Bos taurus y que presentan mayor fertilidad en comparación con las receptoras que fueron utilizadas en el sistema de producción doble propósito cruzas Bos taurus vs Bos indicus. Además, otra causa es que los embriones fueron transferidos frescos producidos in vivo en comparación con este trabajo, donde los porcentajes fueron menores tomando en cuenta que los embriones pasaron por un tratamiento de vitrificación y calentamiento, y por tanto durante el descenso de temperatura se pueden inducir daños al embrión.
Recientemente39 se evaluó el efecto de la bipartición durante la transferencia de los embriones; se utilizaron embriones en estadio de blastocisto, los cuales fueron bipartidos y transferidos a las receptoras. Catorce días después de la transferencia, se procedió a la recolección embrionaria vía no quirúrgica y se obtuvieron 37.5 % de hemiembriones alargados vs 52.9 % de embriones completos alargados; estos resultados son mayores a los obtenidos en el presente trabajo que fue 19.35 vs 31.6 % para hemiembriones y embriones completos. Sin embargo, los resultados podrían considerarse favorables teniendo en cuenta que pasaron por un proceso de criopreservación, y esto podría tener un efecto negativo para lograr una adecuada implantación en la receptora. Aunque en el presente estudio no se analizó el alargamiento de los embriones transferidos, se podría suponer que, al estar alargados los embriones, es muy probable que hubieran implantado y producido gestaciones. Por eso se comparó con la tasa de gestación obtenida en el presente estudio. En este sentido, investigaciones acerca de la criopreservación de embriones40, han mencionado que ésta no es un proceso libre de problemas, ya que induce variaciones extremas en las propiedades físicas y químicas de la membrana celular, los orgánulos y la delicada interacción célula-célula inherente a los embriones a criopreservar. Asimismo, los períodos críticos para la supervivencia embrionaria durante la criopreservación son la fase inicial de congelación y el período de retorno a las condiciones fisiológicas. Las lesiones embrionarias crioinducidas se explican por la formación de cristales de hielo intracelulares y el estrés osmótico al que se ve sometida la membrana plasmática durante la congelación41.
Durante mucho tiempo ha existido la preocupación de saber si los becerros nacidos de hemiembriones se comportan de igual manera que aquellos producidos por embriones enteros. Una publicación reciente arrojó información valiosa acerca de esto42; al comparar el desarrollo de embriones y hemiembriones desde los 60 días de gestación hasta los 550 días de edad, no se detectaron diferencias en el diámetro biparietal, abdominal, cordón umbilical, orbital y aórtico. Tampoco hubo diferencias en el peso al nacer, al destete, y cada 30 días hasta los 550 días. Por lo tanto, concluyeron que no hay diferencias discernibles físicamente entre crías de embriones y de hemiembriones, lo cual es importante para poder utilizar la técnica de bipartición de manera segura. Esto cobra importancia, sobre todo porque la vitrificación y la bipartición son técnicas de reproducción asistida que tienen el potencial de ser utilizadas, no solo en especies de interés zootécnico, sino también en especies en peligro de extinción43.
Conclusiones e implicaciones
Bajo las condiciones del presente trabajo, la bipartición de embriones bovinos producidos in vivo, no afecta el desarrollo in vitro ni la tasa de gestación. Con la bipartición embrionaria se obtuvo el mismo número de gestaciones con menos embriones, aportando información reciente sobre estas biotecnologías.
















