Introducción
El sistema de conductos radiculares es de gran complejidad en cada diente, donde se incluyen irregularidades anatómicas; como los conductos accesorios, laterales, istmos y deltas apicales, que junto con los microorganismos son vectores para generar una patología pulpar. Durante la instrumentación se busca desorganizar el biofilm, eliminar los restos de tejido orgánico dentro de los conductos, y desalojarlos mediante la irrigación. No obstante, la acumulación de desechos y la formación de la capa de lodillo dentinario, también contribuye a la retención de tejido y bacterias, que en conjunto con las áreas no instrumentadas representan focos potenciales de reinfección, que ponen en riesgo el éxito del tratamiento1.
La irrigación con un agente antimicrobiano efectivo produce el arrastre físico de las bacterias y los escombros producto de la preparación. Adicionalmente, desde el punto de vista químico, los irrigantes maximizan la desinfección del conducto radicular, y facilitan la dilución de tejidos orgánicos. La sustancia irrigante más destacada es el hipoclorito de sodio, excelente antibacteriano, capaz de disolver tejido pulpar vital, necrótico, además de componentes orgánicos de la dentina y biopelículas2. Su velocidad y profundidad de acción dependen de la concentración y la temperatura. Sin embargo, su acción no afecta la materia inorgánica, creando un bajo impacto en el lodillo dentinario lo que hace necesaria su asociación con agentes quelantes, como el ácido etilendiaminotetracético (EDTA), que elimina los residuos finales y aumenta la permeabilidad de la dentina, mejorando el sellado de los conductos accesorios y los túbulos dentinarios durante la obturación3.
Los sistemas de activación para eliminar el detritus han dado mejores resultados en el tercio apical de los conductos radiculares, en comparación con la irrigación convencional de jeringa y aguja4, debido a que este último distribuye la solución no más allá de 0-1.1 mm, dando como resultado una limpieza inadecuada e incompleta para la compleja anatomía del sistema de conductos radiculares5. Uno de los principales sistemas de activación es la irrigación ultrasónica pasiva, descrita por Weller et al.6, consistente en la transmisión de energía acústica de una lima oscilante, o un alambre liso, a un irrigante en el conducto radicular. La cavitación puede perturbar y disgregar la biopelícula endodóntica, disminuyendo las bacterias planctónicas, debido a la formación de burbujas microscópicas en el irrigante, que luego colapsan y explotan7.
El sistema XP-Endo® Finisher de la marca FKG Swiss endo, a base de níquel titanio con una aleación patentada MaxWire (Martensita, Austentita, Electopulido FleX), reacciona a diferentes niveles de temperatura8. Cuando se enfría, se encuentra en la fase martensita presentando una forma recta; al calentarse con la temperatura corporal cambia a una fase austenita, presentando una forma de C en el último tercio, esta propiedad facilita la limpieza final en los tratamientos de conductos radiculares9.
La lima tiene un núcleo pequeño con un ISO de 25 de diámetro y conicidad cero5, por lo que fue diseñada para ser utilizada en conductos instrumentados al menos con el mismo calibre10. Se adapta a lo largo de toda la pared del conducto, sin debilitar la estructura del diente, ya que no corta dentina11, permitiendo un mejor manejo en morfologías complejas10, particularmente en conductos curvos y estrechos. Durante la activación, la solución irrigante se agita mediante un movimiento corono apical dentro del conducto. El instrumento puede expandirse hasta 6 mm de diámetro, asegurando el flujo del irrigante en toda la pared del conducto.
Material y métodos
Se realizó un estudio in vitro utilizando 32 raíces mesiales de molares inferiores extraídos, los cuales debían contar con raíces divergentes. Al inicio los dientes fueron fotografiados; posteriormente se tomó radiografía inicial para observar la anatomía y permeabilidad de los conductos. Previo a la eliminación de la corona clínica, se realizaron los accesos con una fresa FG-6 SSW®, y se rectificaron con Endo Z de la marca Dentsply®. Al finalizar, la porción radicular se dividió con un disco de carburo de baja velocidad, conservando sólo la raíz mesial, cuya longitud estándar apico-coronal fue de 15 mm, corroborada con un radiovisiógrafo Planmeca ProSensor® HD, y una lima ISO 15 tipo K Flexofile Dentsply® Sirona a través de imágenes vestíbulo-lingual y mesio-distal. El ápice fue sellado con barniz de uñas para evitar la salida de detritus o irrigante a través de éste. Las raíces fueron montadas en una base de silicón pesado para facilitar su manipulación. La preparación del conducto se inició con una lima ISO 15 tipo K Flexofile Dentsply® Sirona, y se utilizó para asegurar la permeabilidad del conducto después de la lima rotatoria. La preparación biomecánica se realizó con un motor X-Smart® Plus, y el sistema WaveOne® Gold (Primary 25/.07), ambos de Dentsply® Sirona. Durante la instrumentación se mantuvo una irrigación constante, utilizando 5 mL de hipoclorito de sodio al 5.25% con jeringa hipodérmica, y aguja 27Ga Endo-Eze™ de Ultradent® Products, Inc. Finalmente se irrigó con 5 mL de solución fisiológica. Posteriormente las raíces se dividieron aleatoriamente para recibir los distintos protocolos de irrigación.
Control positivo: Se seleccionaron 2 raíces a las que no se les aplicó protocolo de irrigación final, para observar la acumulación de lodillo dentinario en las paredes del conducto.
I. Control negativo: Constituido por 10 raíces, las cuales fueron irrigadas con 5 mL de MD-Cleanser (EDTA Solution MetaBiomed®) al 17% durante 60 segundos, colocando la aguja 1 mm por arriba de la longitud de trabajo, sin realizar activación adicional del irrigante. Posteriormente se realizó un lavado con 3 mL de solución salina para prevenir los efectos del EDTA, seguida de una descarga de 1 mL de hipoclorito de sodio al 5.25%, y un último lavado con 3 mL de solución salina. Finalmente se secaron los conductos con puntas de papel estéril.
II. Grupo experimental 1: Se incluyeron 10 raíces para ser irrigadas con 5 mL de MD-Cleanser (EDTA Solution MetaBiomed®), al 17% activado con el sistema XP-Endo® Finisher durante 60 segundos, a una velocidad de 800 rpm y un torque de 1 Ncm. De acuerdo con las indicaciones del fabricante, se colocó la lima XP-Endo® Finisher en contra-ángulo, se fijó la longitud de trabajo, mediante el tubo de plástico milimetrado incluido en el blister, y posteriormente se enfrió mediante spray Endo ICE (Hygienic®, Coltene), con la intención de mantener la lima recta (fase austenítica), debido a que la punta presenta una forma en C (fase martensítica). Una vez que la lima se encuentra recta se retira del tubo para introducirla en el conducto. Se colocó 0.5 mL de irrigante dentro del conducto, se insertó la lima dentro del mismo, se inició la rotación realizando movimientos longitudinales con una amplitud de 7-8 mm de manera suave, recargándose sobre las paredes. Se mantuvo la irrigación constante durante 60 segundos con 3.5 ml de EDTA al 17%. Al finalizar, se retiró la lima XP-Endo® Finisher del conducto mientras continuaba en rotación (Figura 1).

Figura 1 Preparación de la lima. A. Enfriamiento de la lima con Spray Endo ICE (Hygienic). B. Lima en fase austenítica. C. Lima en fase martensítica. D. Uso de la lima.
III. Grupo experimental 2: Se seleccionaron 10 raíces para ser irrigadas con 5 mL de MD-Cleanser (EDTA Solution MetaBiomed®), al 17% activado con ultrasonido DTE-D5®, punta E14, utilizando la función Endo nivel de velocidad 3 durante 60 segundos, siguiendo la secuencia propuesta por De-Deus et al.11: Se colocaron 0.5 mL de irrigante dentro del conducto; se posicionó la punta de ultrasonido 2 mm por arriba de la longitud de trabajo, y se realizaron tres ciclos de activación de 20 segundos cada uno. Entre cada intervalo se hizo un recambio con 1.5 mL de EDTA al 17%, completando 5 mL. Finalmente se realizó un lavado con 3 mL de solución salina, seguida de una descarga de 1 mL de hipoclorito de sodio al 5.25% y un último lavado con 3 mL de solución salina, secando los conductos con puntas de papel estéril.
Al finalizar el protocolo de irrigación, y con la intención de observar y cuantificar los túbulos dentinarios mediante el microscopio de barrido, las muestras fueron divididas longitudinalmente con disco de diamante de baja velocidad. El corte se realizó en las caras vestibular y lingual de cada raíz antes de alcanzar el conducto radicular. Posteriormente los segmentos fueron separados con ayuda de un cincel, conservando la porción radicular con mayor estructura. A esta última se le realizaron dos marcas cada 5 mm, a lo largo del conducto instrumentado, delimitando el tercio cervical, medio y apical.
Las muestras sin protocolo de irrigación final Control positivo (C+) mostraron una capa densa de lodillo dentinario sobre la pared del conducto en los tres tercios (Figura 2. A, E, I.). En el tercio cervical, los tres grupos; irrigación convencional (C-), activación con XP- Endo® Finisher (E1), y ultrasonido (E2), mostraron diferencias significativas con respecto al grupo control positivo (C+). De igual manera se observa mayor remoción del lodillo dentinario en este tercio, comparadas con el tercio medio y apical. (Figura 2). Sobre el tercio medio se observa una mayor apertura de los túbulos dentinarios con el sistema XP-Endo® Finisher (Figura 2. G), en algunas muestras que recibieron la activación de EDTA con ultrasonido se visualiza la pared del conducto modificada. (Figura 2. H). Finalmente, en el tercio apical las diferencias se vuelven más significativas; las muestras que fueron activadas con sistema XP-Endo® Finisher presentan túbulos más abiertos (Figura 2. K), mientras que en los grupos de irrigación convencional y activación con ultrasonido se observa una mayor cantidad de lodillo dentinario y túbulos obliterados (Figura 2. J-L).
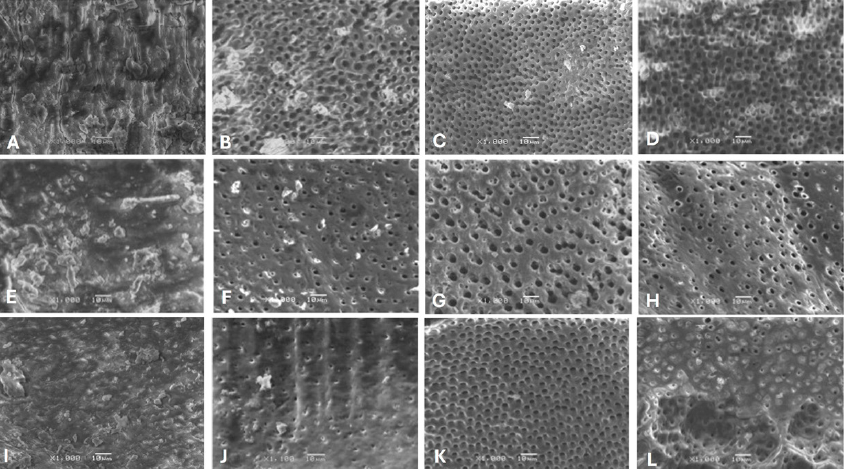
Figura 2 Fotomicrografías. Tercio cervical: A. Sin protocolo de irrigación final. B. Irrigación de EDTA 60s sin activación. C. Irrigación de EDTA 60s activación XP-Endo® Finisher. D. Irrigación de EDTA 60s con activación de ultrasonido. Tercio medio: E. Sin protocolo de irrigación final. F. Irrigación de EDTA 60s sin activación. G. Irrigación de EDTA 60s activación XP-Endo® Finisher. H. Irrigación de EDTA 60s activación ultrasonido. Tercio apical: I. Sin protocolo de irrigación final. J. Irrigación de EDTA 60s sin activación. K. Irrigación de EDTA 60s activación XP-Endo® Finisher. L. Irrigación de EDTA 60s con activación de ultrasonido.
Para contabilizar la presencia o ausencia de lodillo dentinario a lo largo de la superficie del conducto radicular, se utilizaron dos procedimientos que permiten evaluar mediante fotomicrografías los túbulos dentinarios; el primero propuesto por Torabinejad et al.12 con los siguientes parámetros:
Puntaje 1 (sin lodillo dentinario). No hay presencia de lodillo dentinario en la superficie de los conductos radiculares, los túbulos están limpios y abiertos.
Puntaje 2 (lodillo dentinario moderado). Sin lodillo dentinario en la superficie del conducto, los túbulos dentinarios presentan partículas remanentes (debris).
Puntaje 3 (con lodillo dentinario). El lodillo dentinario cubre totalmente los túbulos dentinarios
La segunda observación es una propuesta derivada de esta investigación en busca de un método más objetivo para evaluar la presencia de lodillo dentinario. Para ello se analizaron las fotomicrografías con el programa de procesamiento de imagen digital de dominio público ImageJ (National Institutes of Health, NIH), que permitió realizar el conteo de los túbulos dentinarios abiertos. Las imágenes se calibraron dentro del programa, tomando como referencia la escala de 10 µm. De las 96 capturas se seleccionó una imagen representativa de cada tercio, y se realizó un acercamiento para determinar el área del túbulo dentinario: La media obtenida en el acercamiento de los túbulos fue de 2.5 µm para cada tercio. Este parámetro sirvió como referencia para que el programa contabilizara únicamente los túbulos que tienen un área igual o mayor, descartando aquellos de menor tamaño suponiendo que contienen lodillo dentinario. El conteo de partículas se realizó mediante el despliegue de una imagen contrastada en rojo que muestra los túbulos que entraron dentro del parámetro establecido. Este proceso se realizó en cada una de las fotomicrografías (Figura 3).
Resultados
Las cifras obtenidas en ambos sistemas fueron tabuladas en hojas de Microsoft Excel, y se aplicó la prueba estadística de Chi-cuadrado (X2) para su evaluación. Los resultados muestran diferencias significativas entre el grupo control y los tres métodos evaluados, se observaron túbulos dentinarios abiertos (P<0.05), sin embargo, ninguno de los métodos eliminó completamente la capa de lodillo remanente (Tablas 1 y 2). El análisis estadístico aplicado; muestra en la escala de Torabinejad una discrepancia en el tercio medio con respecto al programa de ImageJ (Tablas 1 y 2). La misma aplicación mostró diferencias significativas para XP-Endo® Finisher en los tres tercios.
Tabla 1 Escala Torabinejad
| Tercio Cervical | ||||||
|---|---|---|---|---|---|---|
| Código | Grupos | Total | Análisis | |||
| EDTA | XP-Endo® Finisher |
Ultra Sonido | (X2) Tabla | (X2) Calculado |
||
| 1 | 3 | 9 | 3 | 15 | 9.487 | 13.800 |
| 2 | 3 | 1 | 6 | 10 | ||
| 3 | 4 | 0 | 1 | 5 | ||
| Total | 10 | 10 | 10 | 30 | ||
| Tercio Medio | ||||||
| 1 | 1 | 5 | 1 | 7 | 9.487 | 6.771 |
| 2 | 3 | 3 | 4 | 10 | ||
| 3 | 6 | 2 | 5 | 13 | ||
| Total | 10 | 10 | 10 | 30 | ||
| Tercio Apical | ||||||
| 1 | 0 | 4 | 0 | 4 | 9.487 | 10.583 |
| 2 | 2 | 3 | 3 | 8 | ||
| 3 | 8 | 3 | 7 | 18 | ||
| Total | 10 | 10 | 10 | 30 | ||
Tabla 2 Escala ImageJ
| Tercio Cervical | ||||||
|---|---|---|---|---|---|---|
| Muestra | Grupos | Total | Análisis | |||
| EDTA | XP-Endo® Finisher |
Ultra Sonido | (X2) Tabla | (X2) Calculado |
||
| A | 133 | 120 | 236 | 489 | 28.869 | 813.648 |
| B | 273 | 150 | 131 | 554 | ||
| C | 279 | 391 | 181 | 851 | ||
| D | 248 | 248 | 178 | 674 | ||
| E | 100 | 253 | 124 | 477 | ||
| F | 76 | 238 | 178 | 492 | ||
| G | 66 | 236 | 36 | 338 | ||
| H | 256 | 119 | 44 | 419 | ||
| I | 185 | 288 | 192 | 665 | ||
| J | 49 | 406 | 236 | 691 | ||
| Total | 1665 | 2449 | 1536 | 5650 | ||
| Tercio Medio | ||||||
| A | 23 | 128 | 60 | 211 | 28.869 | 908.619 |
| B | 90 | 206 | 105 | 401 | ||
| C | 104 | 319 | 82 | 505 | ||
| D | 17 | 358 | 2 | 377 | ||
| E | 139 | 226 | 129 | 494 | ||
| F | 39 | 24 | 196 | 259 | ||
| G | 7 | 139 | 92 | 238 | ||
| H | 25 | 132 | 213 | 370 | ||
| I | 16 | 302 | 217 | 535 | ||
| J | 10 | 59 | 81 | 150 | ||
| Total | 470 | 1893 | 1177 | 3540 | ||
| Tercio Apical | ||||||
| A | 1 | 89 | 3 | 93 | 28.869 | 737.117 |
| B | 108 | 167 | 39 | 314 | ||
| C | 87 | 311 | 18 | 416 | ||
| D | 20 | 324 | 86 | 430 | ||
| E | 13 | 24 | 1 | 38 | ||
| F | 9 | 45 | 55 | 109 | ||
| G | 1 | 57 | 1 | 59 | ||
| H | 1 | 73 | 65 | 139 | ||
| I | 1 | 124 | 48 | 173 | ||
| J | 146 | 53 | 40 | 239 | ||
| Total | 387 | 1267 | 356 | 2010 | ||
Discusión
Se ha demostrado en diversas investigaciones que, sin importar el sistema de instrumentación utilizado durante la conformación de los conductos1, siempre se genera una capa de lodillo dentinario que se adhiere a las paredes y oblitera los túbulos dentinarios11, como lo observado en las muestras del grupo control (C-). Esta investigación revisó la activación de EDTA con ultrasonido y XP-Endo® Finisher para eliminar la capa de lodillo dentinario. Ambos sistemas favorecieron la limpieza de las paredes del conducto, obteniendo resultados similares a los de Leoni et al.13 donde la disminución del lodillo dentinario se logró sin importar el método de activación del EDTA.
El sistema XP-Endo® Finisher fue el único que tuvo acción significativa sobre la capa de lodillo dentinario, debido a que se observó mayor cantidad de túbulos dentinarios abiertos, particularmente en el tercio apical. Estos hallazgos contrastan con diversas investigaciones sobre la instrumentación en dicho segmento, y señalan que, a pesar de ello, se pueden alojar bacterias en los túbulos dentinarios, o en el mismo lodillo con alto potencial patógeno, favoreciendo una irritación persistente del tejido periradicular, retardando la cicatrización14, por lo que cualquier método que mejore las condiciones de esta zona favorece ampliamente el pronóstico del tratamiento. Los resultados se analizaron con los dos métodos de puntuación referidos en esta investigación, tanto la escala de Torabinejad, como la propuesta de ImageJ, ambos permitieron contrastar los diferentes protocolos de activación del EDTA y determinar la eficacia de cada uno en la eliminación de la capa de lodillo dentinario. Aunque de manera general los resultados fueron similares para ambos sistemas, la escala de Torabinejad mostró discrepancia en el tercio medio, lo cual podría ser causado por la apreciación subjetiva del operador al observar las fotomicrografías. Por ello, se propone el uso de ImageJ (National Institutes of Health NIH), un programa de procesamiento de imagen digital de dominio público, con el fin de establecer un método más objetivo y accesible para cualquier investigador, basado en un análisis cuantitativo.
Conclusión
Dentro de las limitaciones del presente estudio, se puede concluir que la activación de EDTA con la lima XP-Endo® Finisher mostró ser más efectiva en la eliminación de la capa de lodillo dentinario, en comparación con el uso de ultrasonido, particularmente en el tercio apical, donde mostró ser el único sistema capaz de tener incidencia significativa, a pesar de la poca instrumentación y las irregularidades de esta área. Estos resultados se podrían extrapolar a la práctica clínica, considerando las ventajas y desventajas que ofrece el sistema. Sin embargo, es pertinente cuestionar la necesidad de emplearlo de manera generalizada, o utilizarse de manera selectiva solamente en pacientes que presenten periodontitis apical, o retratamientos con lesiones persistentes que requieren mayor atención del tercio apical. Debido a que ninguno de los métodos evaluados eliminó por completo la capa de lodillo dentinario, las investigaciones en esta área deben continuar en busca de un protocolo de irrigación final que garantice por completo la desinfección del sistema de conductos.
















