Introducción
El oscurecimiento del grano de frijol es una característica indeseable, debido a que el consumidor rechaza su adquisición. El comercializador resulta afectado por la corta vida útil de los tipos y variedades de frijol que se oscurecen rápidamente, ya que cuentan con un tiempo menor para colocarlo en el mercado. La vida de anaquel del frijol con esta característica es de aproximadamente dos meses, en cambio los frijoles de oscurecimiento lento pueden tener vida de anaquel de varios años. Esta es una característica tan importante para el consumidor que la variedad Pinto Saltillo, de oscurecimiento lento, sacó del mercado a la variedad Pinto Villa, de oscurecimiento rápido, a pesar de que ambas son tolerantes a sequía. El oscurecimiento de la testa de la semilla es una característica común de la mayoría de los tipos de frijol que se consumen en México, exceptuando los frijoles de tipo negro, los azufrados y algunos pintos. Este fenómeno es particularmente evidente en los tipos pinto, flor de mayo y flor de junio.
El Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP) desarrolló la variedad de frijol ‘Pinto Saltillo’, de la raza Durango, que tiene como características sobresalientes la tolerancia a sequía y el oscurecimiento lento de su semilla, que la han convertido en la variedad de cultivo preferente en zonas amplias del territorio nacional, particularmente en el Centro y Norte-Centro del país. El acervo genético a partir del cual se generó Pinto Saltillo se ha venido usando como fuente para el desarrollo de nuevas variedades de frijol pinto de oscurecimiento lento: Pinto Coloso (Rosales-Serna et al., 2010), Pinto Bravo (Rosales-Serna et al., 2011), Pinto Centauro (Rosales-Serna et al., 2012a), Pinto Centenario (Rosales-Serna et al., 2012b) y Pinto Libertad (Rosales-Serna et al., 2012c), todas ellas adaptadas al Altiplano Semiárido, especialmente en el estado de Durango. Por su parte, Acosta-Gallegos et al. (2016) liberaron la variedad de frijol pinto San Rafael, que tiene como características principales reacción neutral al fotoperiodo (puede sembrarse en cualquier época del año y latitud sin que se modifique su ciclo), resistencia a tizón de halo, antracnosis y roya y tolerancia al oscurecimiento, lo que le confiere una mayor vida de anaquel.
En la literatura científica se han descrito procedimientos para llevar a cabo la selección de individuos de oscurecimiento lento a través de la aplicación de luz ultravioleta para imitar el envejecimiento de la semilla (Salvador et al., 2022); los individuos seleccionados tienen el potencial para usarse como progenitores en los programas de mejoramiento. El oscurecimiento de la testa se acentúa por condiciones desfavorables, como alta humedad y temperatura, causando pérdidas económicas debido a la declinación de la calidad visual del grano, que los consumidores relacionan con frijol ‘viejo’ que tiene mal sabor y que requiere mayor tiempo de cocción (Wiesinger et al., 2021).
Las causas precisas del oscurecimiento se desconocen, pero incluyen una combinación de efecto ambiental, genético y cambios bioquímicos en la cubierta de la semilla (Islam et al., 2020). Los flavonoides protegen a las plantas contra diversos tipos de estrés biótico y abiótico (Pourcel et al., 2007) y su presencia en la dieta humana contribuye a la prevención de enfermedades degenerativas. Muchos de los roles biológicos de los flavonoides se atribuyen a su potencial citotoxicidad y capacidad antioxidante. La oxidación de flavonoides contribuye a estas propiedades químicas y biológicas y puede conducir a la formación de pigmentos marrones en los tejidos de las plantas, así como en los alimentos y bebidas derivados de ellas. La oxidación de flavonoides in planta está principalmente catalizada por enzimas polifenol oxidasas (PPO) (catecol oxidasas y lacasas) y peroxidasas. Estas actividades se inducen durante el desarrollo de semillas y plantas y por tensiones ambientales, como ataques de patógenos (Wiesinger et al., 2021).
En este sentido, Marles et al. (2008) propusieron por primera vez que las características de oscurecimiento de la testa del frijol se relacionaban directamente con la actividad de la enzima polifenol oxidasa y con la acumulación diferencial de polifenoles, particularmente de los flavonoides. Esto fue confirmado por Chen et al. (2015) al estudiar los compuestos fenólicos libres y conjugados en la testa de las semillas de frijol tipo cranberry (rojo), ya que reportaron que los fenotipos de oscurecimiento regular contenían flavonoides de manera exclusiva en extractos fenólicos libres, a diferencia de los fenotipos de oscurecimiento lento, los cuales carecían de estos compuestos; además, el contenido total de compuestos fenólicos fue mayor en los fenotipos de oscurecimiento regular.
Aparte de la polifenol oxidasa, existen otras enzimas capaces de catalizar la oxidación de fenoles y aminas en una forma no específica; al respecto, Turlapati et al. (2011) describieron la multifamilia de las lacasas en Arabidopsis thaliana, en un esfuerzo para precisar las funciones de los genes relacionados, aunque las funciones fisiológicas y bioquímicas precisas en plantas superiores aún son desconocidas entre los 17 genes que codifican para este tipo de proteínas. Ellos determinaron que la LAC15 se encuentra en la pared celular de la testa de la semilla y probablemente está involucrada en su oscurecimiento por oxidación. Cabe resaltar que, en un trabajo previo, Cai et al. (2006) desarrollaron mutantes de lacasas en Arabidopsis y encontraron que lac15 producía plantas con el color de la semilla alterado, presentando un color amarillo pálido.
De acuerdo con Basset (2007) el oscurecimiento de la cubierta de la semilla está controlado por un solo gen, el J, y la expresión del alelo recesivo j es responsable de genotipos menos susceptibles al oscurecimiento de la testa en comparación con genotipos con el alelo dominante. da Silva et al. (2008) estudiaron el control genético del oscurecimiento de la testa en frijol de tipo carioca y propusieron que había un solo gen involucrado en este fenómeno y que el alelo dominante era el de oscurecimiento temprano (regular). Sin embargo, Elsadr et al. (2011) describieron un modelo con dos genes, J y Sd, interactuando en epistasis, lo que produce tres fenotipos: no oscurecimiento, oscurecimiento lento y oscurecimiento regular. Recientemente, Islam et al. (2020) propusieron que el gen P sd , un alelo del factor de transcripción del tipo hélice-asa-hélice, regula el oscurecimiento postcosecha del frijol pinto. La utilidad de estos modelos frecuentemente depende del origen del germoplasma. Por ello es necesario realizar investigación con variedades de frijol desarrolladas en México.
El objetivo fue identificar genes de fenol oxidasas asociados al oscurecimiento de la testa del grano de distintos tipos de frijol, cuyos niveles de expresión sean útiles como marcadores para identificar genotipos de oscurecimiento lento.
Materiales y métodos
Material genético
Se utilizaron las variedades de tipo pinto: Salinas, Rarámuri, Pinto Saltillo y Pinto Villa, de tipo flor de junio: ‘Dalia’ y ‘León’ y de tipo flor de mayo: Eugenia y Dolores. Pinto Saltillo y Pinto Villa se emplearon como controles, ya que son de oscurecimiento lento y regular (se oscurece rápidamente), respectivamente. Todos los materiales fueron proporcionados por el Programa de Mejoramiento de Frijol del INIFAP, provenientes de los ciclos de riego y temporal, cuyas siembras se realizaron en febrero y julio de 2017, respectivamente, en Celaya, Guanajuato. Para determinar la acumulación de transcritos en órganos vegetativos y reproductivos, las semillas se germinaron en condiciones asépticas, para lo que se usó una solución de hipoclorito de sodio al 1 % en la que se sumergieron las semillas por 3 min, transcurrido ese tiempo se lavaron con agua destilada estéril y se colocaron en una cámara húmeda formada por una charola de plástico y papel absorbente humedecido con agua estéril. Después se trasplantaron a invernadero 10 semillas de cada variedad en macetas de 2 kg que contenían sustrato tipo turba (Sunshine Mix 3®). El riego se aplicó tres veces a la semana y se siguió el crecimiento y desarrollo de las plantas.
Inducción de oscurecimiento con luz UV
Con el objetivo de conocer el fenotipo de oscurecimiento de los materiales se realizó una cinética consistente en la aplicación de luz UV durante 144 horas a 15 semillas de cada variedad, siguiendo la técnica descrita por Junk-Knievel et al. (2008). Las semillas se colocaron a 11 cm de una lámpara de luz UV de 30 W con una longitud de onda de 254 nm (Tecnolite G30T8). Se midió el parámetro de luminosidad L* cada 24 h con un colorímetro Konica Minolta CR-400. La medición se realizó por triplicado y entre cada una de ellas se tomaron al azar cinco semillas para realizar la lectura. La interpretación de los datos se basó en el sistema de medición de color, espacio CIELAB. El oscurecimiento producido se estimó mediante la retención de luminosidad de cada variedad, considerando su valor en el tiempo cero como el 100 %. El oscurecimiento de las semillas se documentó cada 24 h con una cámara Sony α35.
Análisis de expresión
Se estudió la expresión de tres genes difenol oxidasa lacasa, dos difenol oxidasa y tres polifenol oxidasa(Cuadro 1). Estos genes se identificaron en el genoma del frijol de acervo mesoamericano BAT 93 alojado en NCBI ID BioProject PRJNA221782 (Vlasova et al., 2016). Los iniciadores específicos (Cuadro 1) se diseñaron con la aplicación Primer3Plus (https://www.bioinformatics.nl/cgi-bin/primer3plus/primer3plus.cgi).
Cuadro 1 Información de los iniciadores y genes de las fenol oxidasas de frijol seleccionadas para estudios de expresión.
| Gen | Secuencia£ | Inicio | Fin | Tamaño | Iniciadores (5’- 3’) | Amplicón |
| DOL1 | Scaffold00014 | 1184559 | 1185290 | 731 | F TAGTAAAAAGGGGGCAAAGTAAGC R GGAACCCGAACTGTGGAAGGA | 175 |
| DOL2 | Scaffold00022 | 769101 | 769392 | 201 | F AAGAGCAGAATGTGCCGGTT R TGGATCCAGGGCAGAACTTG | 174 |
| DOL3 | Scaffold00476 | 126290 | 126746 | 456 | F AGTGCAAGGAGTGTTCACCA R GAATCGGGTGGTTCTCAGGG | 188 |
| DO1 | Scaffold00549 | 95491 | 95801 | 310 | F CGTGGACATCCAGCCATAGG R GGGTGCGTGTCTTGTCATCA | 170 |
| DO2 | Scaffold00023 | 53293 | 53560 | 267 | F AACGCACCGTTTCACCCT R ATTTGGGTTCGAACGCTTACA | 168 |
| PPO1 | Scaffold00076 | 797616 | 797994 | 378 | F ACAAGTCCACAACTCCTGGC R GAACCAGCACGATAAGGGCT | 378 |
| PPO2 | Scaffold00125 | 311280 | 311700 | 420 | F GCTTACCGTGCTGGAGATGA R CTACCTTCCGAGCCCTTGAC | 400 |
| PPO3 | Scaffold00396 | 348095 | 348341 | 246 | F CTCCGACACCAGAAACACCT R GGCTCCAC CAACCCATGTAT | 246 |
£ Ensamble del genoma donde se encuentra la secuencia del gen. DOL1: difenol oxidasa lacasa 1, DOL2: difenol oxidasa lacasa 2, DOL3: difenol oxidasa lacasa 3, DO1: difenol oxidasa 1, DO2: difenol oxidasa 2, PPO1: polifenol oxidasa 1, PPO2: polifenol oxidasa 2, PPO3: polifenol oxidasa 3.
La acumulación de transcritos se estudió en semillas completas y en sus fracciones disectadas de testa, endospermo y embrión (Figura 1B), así como en otros órganos vegetativos y reproductivos (hojas, botones florales en estado globoso, flores abiertas, vainas jóvenes de 1 a 2 centímetros de longitud y vainas inmaduras de al menos 3 cm de longitud).
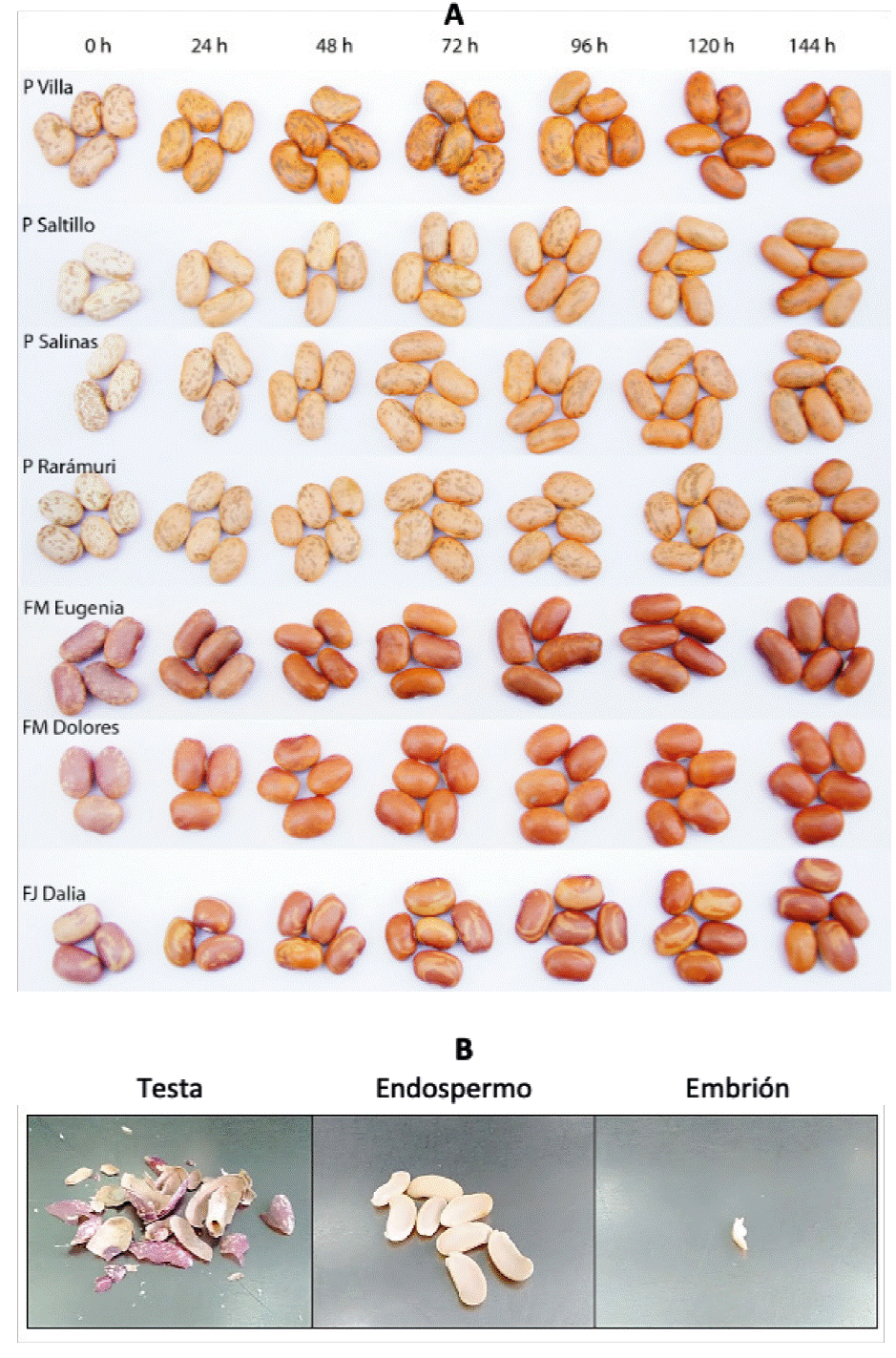
Figura 1 A) Cinética del oscurecimiento de la testa del grano de variedades de frijol de los tipos pinto, flor de mayo y flor de junio. El tiempo cero muestra el color del grano de una cosecha reciente. B) Aspecto de las fracciones de semilla disectadas para determinar los niveles de expresión de genes que codifican para enzimas fenol oxidasas.
El ARN total de cada variedad se extrajo a partir de 20 semillas completas y 20 semillas disectadas en sus fracciones de testa, embrión y endospermo siguiendo el método descrito por Logemann et al. (1987). Los órganos vegetativos y reproductivos se disectaron de 5 plantas: un foliolo de la parte media de cada planta, todos los botones florales, tres vainas jóvenes (no mayores a 3 cm de longitud) y una vaina madura (en llenado de grano) por cada planta. La concentración de los RNAs se igualó visualmente por medio de geles de agarosa desnaturalizante al 1.5 % con 12.3 M de formaldehido y 10 X MOPS, los cuales se visualizaron con bromuro de etidio (0.5 mg mL-1 EtBr) y luz UV en un fotodocumentador Gel Logic 112 de Kodak Science y el software Molecular Imaging v5 (Carestream, WoodBridge, CT, USA). Posteriormente, la concentración real y la pureza del ARN total se determinaron midiendo la absorción de luz UV usando un espectrofotómetro Nanodrop 800™ (Thermo Fisher Scientific). Con los ARNs así tratados se formó una solución equimolar de cada origen mezclando 2 µL de cada muestra en el mismo tubo.
A partir del RNA total se sintetizó ADN complementario de cadena sencilla (cDNA) por transcripción reversa con la enzima SuperScript™ II (Invitrogen). Como testigo para estandarizar los niveles de expresión basales se usó el gen constitutivo 26S, como se describe en Montero-Tavera et al. (2017). La Reacción en Cadena de la Polimerasa a partir de la Transcripción Reversa (RT-PCR) se llevó a cabo usando 1 μL de la reacción de cDNA, 0.8 mM dNTPs, 1X regulador de PCR, 2 mM MgCl2, 0.4 mM de cada iniciador y 1 U de Taq Polimerasa en un volumen de reacción de 25 μL. Las condiciones de amplificación para todos los iniciadores fueron las mismas que para la estandarización, con la excepción de que se usaron 15 ciclos de amplificación adicionales. Los productos de PCR se visualizaron en geles de agarosa al 1.5 %. El análisis densitométrico se realizó con el software TotalLab Quant TL120 1D v2009 y la cuantificación de la expresión diferencial con el programa ImageJ.
Resultados y discusión
Inducción de oscurecimiento con luz UV
Los resultados de la cinética de oscurecimiento inducido por luz UV se muestran en la Figura 1A. Aunque Junk-Knievel et al. (2008) indican que el tratamiento por 72 horas es equivalente al oscurecimiento natural durante un año, en esta investigación el tratamiento se llevó a condiciones extremas de 144 horas, con el fin de encontrar una relación más clara entre el oscurecimiento y la acumulación de transcritos de fenol oxidasas. Se observa que desde las 24 horas Pinto Villa exhibe un oscurecimiento acelerado comparado con las otras variedades de frijol pinto, las que muestran un oscurecimiento lento. Entre las variedades de color rosa claro las diferencias no son tan evidentes, puesto que la luminosidad al tiempo cero es variable entre ellas. Sin embargo, tanto a las 48 como a las 144 horas, Flor de Mayo Dolores es la variedad que más se oscurece con respecto a las cero horas. Estos resultados se muestran con mayor claridad en las gráficas de la Figura 2. En los paneles A y B se observa la luminosidad retenida a través del tiempo para frijoles pintos y rosa claro; entre los pintos, Salinas es la variedad con mayor retención de luminosidad a las 72 horas de tratamiento, mientras que Pinto Villa se oscurece aceleradamente. A las 48 horas, Pinto Saltillo tiene una retención de luminosidad similar a Pinto Villa; sin embargo, a las 72 horas Pinto Saltillo ya presenta mayores valores de luminosidad retenida. Por otro lado, aunque a las 72 horas Salinas y Rarámuri tienen valores diferentes, a las 144 horas son similares. Entre las variedades de color rosa claro, Flor de Junio Dalia y Flor de Mayo Eugenia presentan los valores mayores a través de toda la cinética, mientras que Dolores presenta los menores valores de retención de luminosidad. En los paneles C y D de la Figura 2 se observan los resultados a las 72 y 144 horas. Se sigue la misma tendencia en ambos tratamientos, aunque con valores menores de luminosidad retenida en el tiempo final.
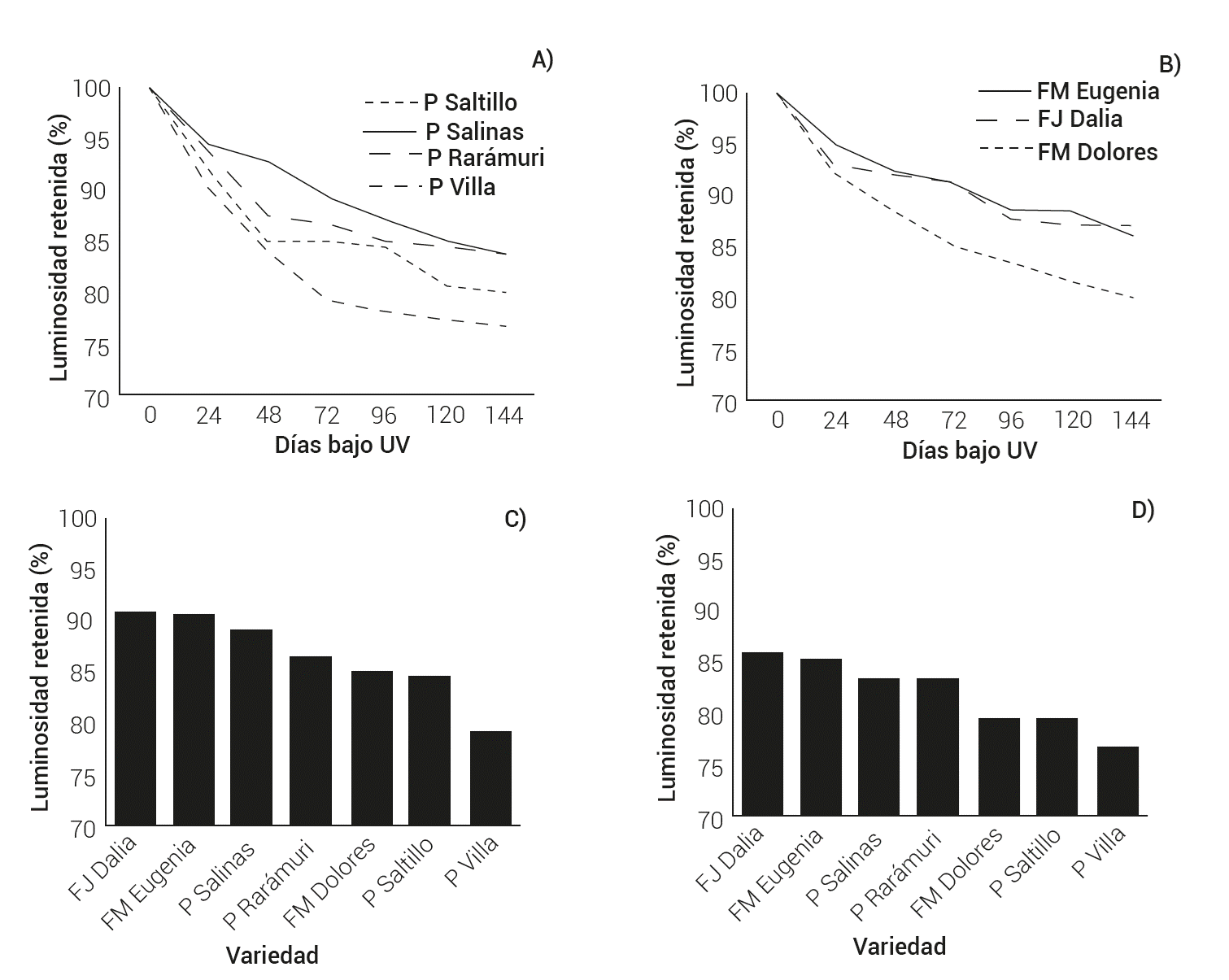
Figura 2 Retención de luminosidad en testa de semillas de variedades de frijol de color pinto y rosa claro. A) Variedades de tipo pinto. B) Variedades de tipo rosa claro. C) Luminosidad retenida a 72 horas bajo luz UV. D) Luminosidad retenida a 144 horas bajo luz UV.
Se ha desarrollado un amplio número de investigaciones que demuestran que el color de las semillas es en gran medida producido por la acumulación de proantocianidinas y se propone que su oxidación es la causa del oscurecimiento de la testa (Islam y Dhaubhadel, 2023). Sin embargo, los mecanismos genéticos y metabólicos que regulan este fenómeno aún son desconocidos. Se debe considerar que el color de las semillas de frijoles pintos es muy similar cuando son de cosecha reciente; es decir, que la distribución de las proantocianidinas es similar, independientemente si se trata de genotipos de oscurecimiento regular, oscurecimiento lento o no oscurecimiento. Esto indica que debe haber funciones de enzimas reguladas diferencialmente entre los tres fenotipos.
Expresión de fenol oxidasas
Los genes difenol oxidasas lacasas 1, 2 y 3 (DOL1, DOL2, DOL3) y difenol oxidasa 1 (DO1) presentan una clara acumulación de transcritos en las semillas de Pinto Saltillo comparadas con la expresión en otros órganos. En semillas de Pinto Villa solo se expresa considerablemente la DOL1; además, resalta que este gen acumula mayor cantidad de transcritos conforme el desarrollo de la semilla avanza desde botones florales jóvenes hasta semillas maduras (Figura 3A). Las polifenol oxidasas no se expresaron apreciablemente en este experimento.
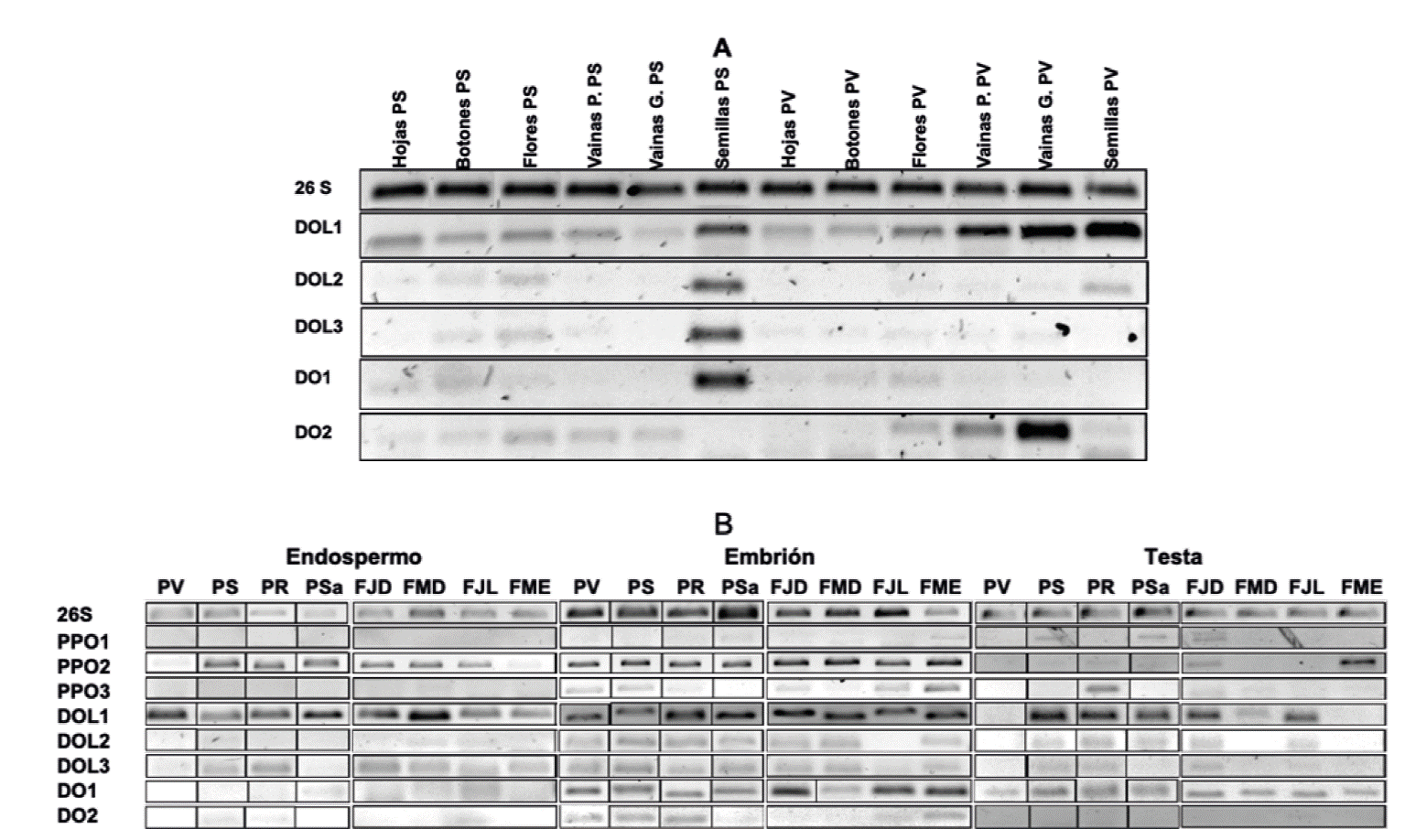
Figura 3 RT-PCR de fenol oxidasas en las fracciones de endospermo embrión y testa de variedades de frijol de tipos pinto y rosa claro. PV: Pinto Villa, PS: Pinto Saltillo, PR: Pinto Rarámuri, PSa: Pinto Salinas, FJD: Flor de Junio Dalia, FMD: Flor de Mayo Dolores, FJL: Flor de Junio León, FME: Flor de Mayo Eugenia.
Dado que la semilla es una estructura compleja, se estudió la acumulación de transcritos en sus principales componentes; es decir, tanto en la testa y el endospermo como en el embrión. Los resultados se observan en la Figura 3B. En el endospermo solo PPO2 y DOL1 se expresan de manera clara en todas las variedades, aunque la primera no se expresa en Pinto Villa, lo que podría sugerir que se asocia al oscurecimiento lento; sin embargo, no se expresa en testa, lo que anula esa posibilidad; DOL1 se expresa incluso en Pinto Villa, lo que sugiere que no se asocia con el oscurecimiento lento, ya que esta variedad es de oscurecimiento regular. En el embrión de todas las variedades se expresan los genes de todas las fenol oxidasas, excepto PPO1, por lo que no hay un patrón de asociación con el oscurecimiento.
En testa DOL1, DOL2 y DOL3 se expresan en las variedades de tipo pinto (Saltillo, Rarámuri y Salinas), pero no en Pinto Villa, lo que sugiere que su actividad se asocia con el oscurecimiento lento. La posible asociación de DO1 con el oscurecimiento lento no es tan clara ya que, aunque presenta mayor acumulación de transcritos en las variedades de frijol pinto de oscurecimiento lento, también se observa una expresión basal en Pinto Villa. La expresión de los tres genes difenol oxidasas lacasas sugiere que Flor de Junio Dalia y Flor de Junio León se pueden clasificar como de oscurecimiento lento, lo que en el caso de Dalia se corrobora por ser una de las variedades con mayor retención de luminosidad; además, esta variedad expresa todas las fenol oxidasas, excepto DO2. Flor de Mayo Eugenia es un caso interesante, ya que, aunque no presenta el perfil de expresión de las variedades de frijol pinto y de los del tipo flor de junio (no presenta expresión de DOL2), es una de las variedades con mayor luminosidad retenida; por el contrario, Flor de Mayo Dolores, cuyo perfil de expresión difiere solo en la DOL2 con respecto a los pintos y flores de junio, es una de las variedades con menor valor de luminosidad retenida, solo superada por Pinto Villa. Aparentemente, las variedades de tipo flor de mayo poseen mecanismos diferentes a los pintos y flores de junio, aunque se requieren mayores estudios para confirmarlo.
Los resultados anteriores se comprobaron mediante un estudio volumétrico, donde se calculó la suma de niveles de gris de todos los pixeles que forman una banda expresada en un gel (Cuadro 2). Adicionalmente, se observó que, aunque la acumulación de transcritos es baja, PPO1 presenta un perfil similar a DOL1, DOL2 y DOL3; es decir, ausente en Pinto Villa y presente en los pintos de oscurecimiento lento, por lo que este gen también podría tener un papel en el oscurecimiento lento del frijol.
Cuadro 2 Análisis volumétrico de niveles de expresión de fenol oxidasas en testa de semillas de variedades de frijol de color pinto y rosa claro.
| Transcrito | Villa | Saltillo | Rarámuri | Salinas | Dalia | Dolores | León | Eugenia |
| 26S | 13473 | 15061 | 18662 | 21929 | 16533 | 15130 | 14801 | 16052 |
| PPO1 | NE | 4834 | NE | 4806 | 13122 | NE | NE | NE |
| PPO2 | NE | 5643 | 7733 | 8358 | 8522 | NE | NE | 16939 |
| PPO3 | NE | NE | 10095 | NE | 7521 | 6297 | NE | 6312 |
| DOL1 | NE | 25607 | 23523 | 20095 | 21757 | 12165 | 19842 | NE |
| DOL2 | NE | 6160 | 9210 | 9130 | 9122 | NE | 7696 | NE |
| DOL3 | NE | 13046 | 12516 | 6500 | 10821 | NE | 10638 | NE |
| DO1 | 9012 | 16690 | 17280 | 15067 | 11197 | 9443 | 11091 | 6575 |
| DO2 | NE | NE | NE | NE | NE | NE | 7745 | NE |
NE: no expresado. Las negritas señalan los valores volumétricos de acumulación de transcritos potencialmente asociados con el oscurecimiento lento.
En la literatura científica no se han reportado resultados que relacionen la acumulación de transcritos con la actividad de polifenol oxidasas y lacasas y su capacidad para inducir el oscurecimiento de la testa. Sin embargo, Blaschek y Pesquet (2021) mencionan que las PPO pueden catalizar dos reacciones distintas, una de ellas es la oxidación de orto-difenoles o catecoles para producir orto-quinonas, las cuales poseen el color café típico del oscurecimiento de la testa, en cambio las DOL, además de oxidar orto y para difenoles, para producir neolignanos, presentan funciones más amplias, ya que promueven la oxidación anabólica o catabólica de los flavonoides, actuando como polimerizador o despolimerizador de las antocianidinas; es decir, que podrían modificar la actividad oxidativa de las PPO. Además, los mismos autores señalan que la localización de las PPO es en el lumen de plástidos, principalmente vacuolas, mientras que las DOL se localizan en el apoplasto celular. Esto las podría convertir en la primera línea de expresión como respuesta al estrés, como el ocasionado por la luz UV. Dado que en esta investigación las DOL se presentaron en las variedades de frijol pinto de oscurecimiento lento y las variedades flor de junio, se sugiere que podrían presentar un mecanismo similar; sin embargo, los mecanismos de acción, localización celular y especificidad de los sustratos de las PPO y DOL aún deben ser dilucidados mediante nuevos experimentos.
Conclusiones
Se identificaron cuatro genes relacionados con el oscurecimiento de la testa, tres difenol oxidas lacasas y la polifenol oxidasa 2. La inducción de su transcripción se asocia con el oscurecimiento lento y su ausencia con el regular en los frijoles de tipo pinto. En el caso de las variedades de color rosa claro es necesario identificar genotipos de oscurecimiento diferencial, para confirmar si la expresión de los mismos genes está relacionada con este fenómeno.















