Introducción
El maíz morado (Zea mays L.) es una variedad nativa de América que se caracteriza por su intenso color púrpura, el cual proviene de su alto contenido en antocianinas y compuestos fenólicos con actividad antioxidante (Guillén-Sánchez et al., 2014). En México y en diversos países de Latinoamérica, este grano es ampliamente empleado en la elaboración de alimentos tradicionales como el atole agrio tradicional del municipio de Ixtenco, Tlaxcala, México (Fig. 1), o la chicha morada del Perú (Leiva González et al., 2016). Estos alimentos, además de tener un valor simbólico en diversas ceremonias y celebraciones indígenas, reflejan la profunda conexión entre el maíz y la identidad cultural de los pueblos originarios (Vargas-Yana et al., 2020).

Figura 1: El maíz morado (Zea mays L.) del municipio Ixtenco, Tlaxcala, México, es el ingrediente principal para la elaboración del atole agrio, alimento tradicional de esta localidad.
El maíz morado ha despertado un interés creciente en la industria alimentaria, no solo por sus propiedades antioxidantes, sino también por sus efectos beneficiosos en la salud, que incluyen propiedades antiinflamatorias, antimutagénicas y anticancerígenas (Lao et al., 2017). Además, el maíz morado es una fuente rica en compuestos fenólicos, lo que contribuye a su potencial para combatir enfermedades crónicas como la obesidad, la diabetes y enfermedades cardiovasculares (Tsuda et al., 2003). Investigaciones sobre el control de la diabetes tipo 2 han revelado que las antocianinas presentes en el maíz morado pueden mejorar la secreción de insulina y la captación de glucosa en células pancreáticas y hepáticas, lo que sugiere un potencial terapéutico en la regulación de la glucosa y la mitigación de las complicaciones asociadas con esta enfermedad (Luna-Vital y Gonzalez de Mejia, 2018).
Estos beneficios para la salud están directamente relacionados con su capacidad para neutralizar los radicales libres y reducir los procesos oxidativos en el cuerpo humano, lo que lo convierte en un alimento funcional altamente valorado (Mrad et al., 2014). Adicionalmente, estudios recientes han demostrado que el maíz morado puede desempeñar un papel importante en la prevención y tratamiento de ciertos tipos de cáncer, gracias a sus efectos antiproliferativos y proapoptóticos sobre células cancerígenas (Mazewski et al., 2017).
Este trabajo de revisión tuvo como principal objetivo recopilar información sobre los estudios realizados en el maíz morado, enfocándose en sus propiedades fisicoquímicas, como el contenido de antocianinas, antioxidantes, así como también en sus propiedades funcionales, con el fin de reconocer los múltiples beneficios nutricionales y a la salud aportados por este alimento. Contar con esta evidencia documental podría conducir a la valorización y al reconocimiento del maíz morado como un recurso natural de alto impacto socioeconómico y científico.
Materiales y Métodos
Búsqueda y recopilación de datos
Para delinear los ejes temáticos del presente artículo de revisión, se llevó a cabo un análisis bibliométrico utilizando la base de datos Scopus (Scopus, 2024). Esta base de datos fue seleccionada debido a su cobertura selectiva de publicaciones científicas fiables, multidisciplinarias y de fuentes independientes. La búsqueda en la base de datos Scopus (Scopus, 2024), se realizó el 17 de julio de 2024, utilizando la siguiente operación lógica: TITLE-ABS-KEY (purple AND corn) AND TITLE-ABS-KEY (anthocyanins). La herramienta VOSviewer© v. 1.6.12 (VOSviewer, 2025) fue elegida por su capacidad para construir y visualizar redes bibliométricas, así como crear mapas que muestren las relaciones entre revistas, autores o publicaciones, basándose en citas, coautoría, co-ocurrencia y otros indicadores bibliométricos. Además de permitir el análisis de grandes cantidades de información bibliográfica de manera eficiente.
Gestión y análisis de metadatos
Los metadatos correspondientes a los documentos identificados fueron exportados de Scopus (Scopus, 2024) en formato CSV para su posterior procesamiento en el software VOSviewer© v. 1.6.12 (VOSviewer, 2025). Se llevó a cabo un proceso de limpieza y normalización que incluyó la eliminación de palabras clave duplicadas y la depuración de registros incompletos con el objetivo de evitar inconsistencias durante el análisis.
El análisis en VOSviewer© v. 1.6.12 (VOSviewer, 2025) incluyó la construcción de redes bibliométricas basadas en la co-ocurrencia de palabras clave relevantes. Este análisis permitió identificar patrones y densidades relacionadas con los términos de estudio.
Elección de ejes temáticos
A partir de los resultados obtenidos del análisis bibliométrico, se realizó una revisión detallada de la literatura para abordar las propiedades funcionales del maíz morado. Los ejes temáticos que estructuran esta revisión son los siguientes: 1) Antocianinas: características químicas y funcionales; 2) Compuestos antioxidantes: potencial bioactivo; 3) Características nutricionales: valor nutritivo del maíz morado y 4) Efectos benéficos en la salud humana: impacto en la prevención y tratamiento de enfermedades.
Resultados y Discusión
Análisis bibliométrico sobre maíz morado
Mediante el análisis bibliométrico, se identificaron 308 documentos, publicados entre 1979 y 2024, relacionados con los términos maíz morado y antocianinas. Además, el análisis resaltó las principales áreas temáticas y las conexiones entre términos clave, así como las tendencias emergentes en el campo de estudio comprendidas en el periodo de tiempo antes mencionado, como puede observarse en la figura 2. Es importante mencionar que la primera publicación que agrupó los dos términos mencionados arriba apareció en 1979. Sin embargo, fue a partir del año 2005 cuando se incrementó sustancialmente el número de publicaciones con estas temáticas.
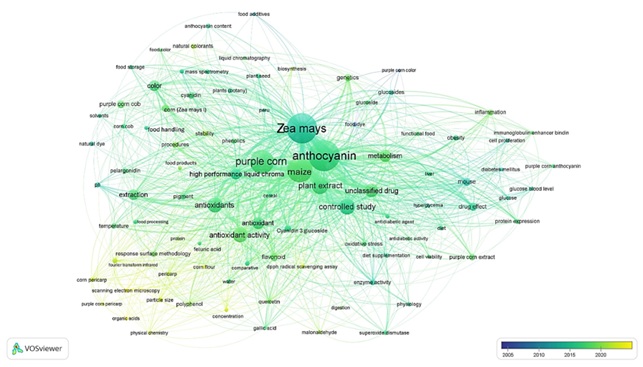
Figura 2: Mapa de términos relacionados con el maíz morado (Zea mays L.) y tendencias recientes de estudio durante el periodo 1979-2024, elaborado con VOSviewer (VOSviewer, 2025). El tamaño de los nodos está relacionado con la frecuencia de repetición de los términos palabras clave (“keywords”). Las líneas que interconectan los nodos representan los términos que aparecen juntos en los mismos artículos. El color de los nodos y las líneas están relacionados con el año de publicación de los artículos que incluyen estos términos. La escala cronológica aparece en la esquina inferior derecha.
La figura 2 también muestra el mapa de términos relacionados derivado del análisis bibliométrico, en el que las palabras "antioxidant activity" (actividad antioxidante) y "functional food" (alimentos funcionales) están fuertemente interconectadas, sugiriendo que una gran parte de la investigación se centra en los beneficios para la salud del maíz morado.
Es importante resaltar que los términos mostrados en esta figura están correlacionados con las palabras clave (“keywords”) de los 308 artículos identificados, por lo que indican los términos más relevantes. Adicionalmente, el análisis cronológico sugiere un interés creciente en la aplicación del maíz morado en la prevención y tratamiento de enfermedades crónicas, como se evidencia por la aparición de términos como "drug effect” (efecto de fármacos), "inflammation" (inflamación) y "obesity" (obesidad).
Cabe destacar que las publicaciones más recientes están relacionadas con el estudio del “corn pericarp” (pericarpio) y la aplicación de técnicas como "chromatography high pressure" (cromatografía de alta presión), utilizadas en el aislamiento y la identificación de compuestos bioactivos, como las antocianinas. La presencia de términos relacionados con técnicas de laboratorio, como "fourier transform infrared" (Espectroscopía infrarroja por transformada de Fourier) y "scanning electron microscopy" (Microscopía electrónica de barrido), señala el uso creciente de estas herramientas en análisis de los compuestos y la microestructura del maíz morado, ya que permiten caracterizar de manera detallada este alimento.
Adicionalmente, el nodo más intenso en la figura 2 corresponde al término “anthocyanin”, por lo que enfatiza la correlación con el maíz púrpura. Otros nodos de intensidad relevante se corresponden con los términos “antioxidant activity” (actividad antioxidante), “antioxidant” (antioxidante) y “antioxidants” (antioxidantes), por lo que resaltan esta característica química de los compuestos presentes en el maíz morado. En contraste, el término de “functional food” (alimento funcional) aparece con un nodo de baja intensidad, pero su presencia indica la relevancia del maíz morado como un alimento nutritivo que aporta moléculas bioactivas benignas.
De manera similar, los términos como “metabolism” (metabolismo), “inflammation” (inflamación), “obesity” (obesidad), “diabetes mellitus”, “glucose” (glucosa), “immunoglobulin enhancer binding” (potenciador de la unión a immnunoglobulina) y “purple corn extract” (extracto de maíz morado) son de baja intensidad. Sin embargo, en conjunto enfatizan el potencial nutracéutico que posee esta raza de maíz.
Como se mencionó previamente, el maíz morado ha sido objeto de creciente interés científico en la última década, debido a sus diferentes propiedades bioactivas, las cuales han mostrado potencial en diversas aplicaciones industriales y de salud. Los estudios sobre el maíz morado han puesto un fuerte énfasis en la identificación y cuantificación de sus compuestos bioactivos, principalmente las antocianinas y otros compuestos fenólicos (Cai et al., 2023). Para ello, se han empleado técnicas como la cromatografía líquida de alto rendimiento (HPLC), con el fin de identificar y cuantificar estos compuestos químicos presentes en diferentes tejidos del maíz morado (Li et al., 2017; Guillén Sánchez et al., 2023).
En estudios recientes se ha demostrado que el contenido de antocianinas en el maíz morado es significativamente superior al de otras variedades, lo que lo posiciona como una fuente destacada de antioxidantes (Paucar-Menacho et al., 2017; Ranilla et al., 2021). En cuanto a las metodologías de extracción de estos compuestos, los esfuerzos se han enfocado en la extracción asistida por ultrasonido y la extracción por presión dinámica, ya que han mostrado ser significativamente más eficientes que los métodos tradicionales, logrando una recuperación superior de antocianinas sin comprometer su integridad bioquímica (Jing et al., 2007; Cristianini y Guillén Sánchez, 2020). También se ha explorado el uso de la extracción por fluidos supercríticos como una técnica innovadora y amigable con el medio ambiente para obtener extractos con alto contenido de compuestos bioactivos (Monroy et al., 2016; Barba et al., 2022).
Debe de destacarse que para el maíz morado se han encontrado nuevas aplicaciones en varios procesos industriales. Por ejemplo, en la industria alimentaria, las antocianinas extraídas del maíz morado se utilizan como colorantes naturales en alimentos y bebidas (Lao et al., 2017; Barba et al., 2022; Kim et al., 2023). En la industria farmacéutica existe un creciente interés en la extracción de compuestos bioactivos como las antocianinas y los flavonoides, debido a sus propiedades antioxidantes, antiinflamatorias, neuroprotectoras, anticancerígenas y cardioprotectoras, que les confieren un alto potencial terapéutico (Guillén-Sánchez et al., 2014; Cristianini y Guillén Sánchez, 2020). De igual forma, en la industria cosmética este grano posee gran interés por sus propiedades antioxidantes, componente importante para el cuidado de la piel (Kurambhatti et al., 2020).
Finalmente, tomando como directriz los hallazgos del análisis bibliométrico anteriormente mencionado, a continuación, se presentan los resultados de la revisión bibliográfica de las principales contribuciones relacionadas con la investigación de las propiedades funcionales del maíz morado dirigidas al estudio de las antocianinas, los compuestos antioxidantes, las características nutricionales y los efectos benéficos para la salud humana.
Las antocianinas en el maíz morado
Las antocianinas son pigmentos naturales, solubles en agua, derivados de los flavonoides, que se distribuyen comúnmente en los órganos y tejidos vegetales, responsables de dar color en tonalidades que cubren la gama de los azules, morados y rojos (Yoshida, 2024). Se ha reportado que estos compuestos pueden mejorar la eficiencia fotosintética, proteger a las plantas de los daños causados por la luz ultravioleta y mejorar la resistencia al estrés oxidativo (Venkatesh et al., 2023). Por ello, diversos grupos de investigación han realizado estudios extensos sobre las rutas de biosíntesis de estos metabolitos secundarios en las plantas (que pueden ser consideradas subramas de la biosíntesis de flavonoides), lo que ha conducido a la identificación de la mayoría de las enzimas biosintéticas y sus correspondientes genes (Strygina et al., 2019).
Las antocianinas presentes en el maíz morado son los pigmentos responsables del color característico de esta variedad de maíz (Medina-Hoyos et al., 2020). Las propiedades saludables aportadas por estas moléculas están asociadas con sus características y estructura química, ya que son muy susceptibles frente a especies reactivas de oxígeno debido a su deficiencia electrónica (Sadowska-Bartosz y Bartosz, 2024). La presencia del ión flavilio les confiere una carga positiva sobre el átomo de oxígeno y es muy frecuente observar en su estructura la adición de unidades de glicosilación, que puede ocurrir en los diferentes grupos hidroxilo de la molécula (Bueno et al., 2012). Sin embargo, la posición 3-OH es el sitio de glicosilación más abundante en la naturaleza, lo que da lugar a 3-O-β-glucósidos (Mattioli et al., 2020).
Las principales antocianinas que se han identificado en este grano son compuestos glucosidados que se pueden clasificar en cuatro grupos principales: cianidinas, pelargonidinas, peonidinas y malvidinas (ver estructuras en la figura 3) (Salinas Moreno et al., 2013). El contenido de antocianinas totales en los granos de maíz puede variar en función del color del grano, ya que el contenido es mayor en maíces con tonalidades azul, morado, púrpura o magenta que en los granos de color rojo (Lopez-Martinez et al., 2009). En la siguiente sección, se describen las características particulares de cada uno de los grupos de antocianinas antes mencionados.
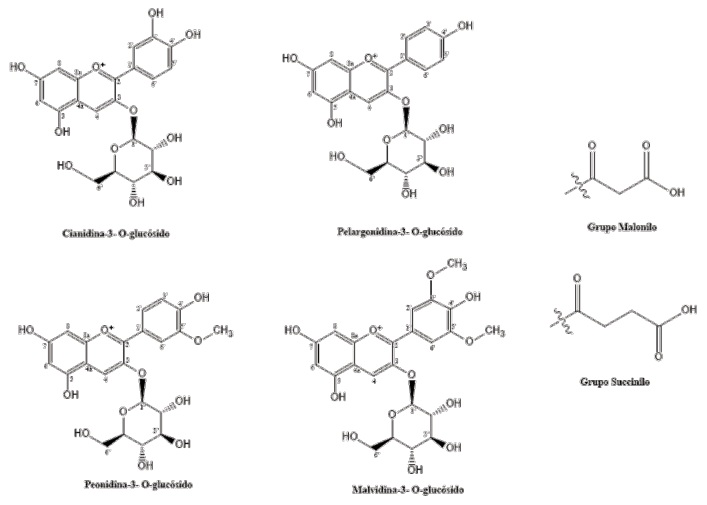
Figura 3: Estructura química de las antocianinas reportadas en maíz morado (Zea mays L.). Se muestran cuatro diferentes antocianinas: cianidinas, pelargonidinas, peonidinas y malvidinas. También se incluyen los grupos malonilo y succinilo que frecuentemente se unen a la glucosa en la posición 6’’-O (Magaña Cerino et al., 2020; Peniche-Pavía y Tiessen, 2020; Hao et al., 2023).
Cianidinas
Las cianidinas y sus glicósidos constituyen uno de los principales grupos de antocianinas de origen natural. De hecho, son las antocianinas más distribuidas en el reino vegetal (Yang et al., 2019), por lo que sus propiedades antioxidantes y biológicas han sido ampliamente investigadas. Están presentes en la dieta humana a través del consumo de legumbres, frutas, verduras, maíz (variedades roja, azul y morada, principalmente), lo que sugiere que se ingieren cantidades significativas de estos compuestos a diario (Galvano et al., 2004). A continuación, se proporciona información relevante asociada con algunos compuestos que integran este grupo.
La cianidina-3-O-glucósido es una antocianina que brinda coloraciones rojas a azules en varias frutas y verduras (zarzamora, granada), legumbres (frijol negro), granos (maíz azul y morado), tubérculos y bebidas (vino tinto, jerez) (Galvano et al., 2007). Su estructura se caracteriza por tener una glucosa unida a la cianidina en la posición 3 (Olivas-Aguirre et al., 2016; Zhang et al., 2021; ver Fig. 3). Es susceptible a la degradación por factores fisicoquímicos, tales como el pH, la luz, el oxígeno, los disolventes, la temperatura y ciertos iones metálicos (Liang et al., 2018).
Además, después de su ingesta la cianidina-3-O-glucósido está expuesta a diversos factores a lo largo del tracto gastrointestinal (pH, fuerza iónica, entre otros), los cuales afectan su biodisponibilidad y posterior bioactividad (Olivas-Aguirre et al., 2016). A pesar de ello, posee múltiples beneficios para la salud, como potente antioxidante y antiinflamatorio neutralizando los radicales libres y reduciendo la inflamación celular (Tan et al., 2019). La cianidina-3-O-glucósido se encuentra predominantemente en los granos de maíz morado, particularmente en el endospermo, la aleurona y el pericarpio (Peniche-Pavía y Tiessen, 2020).
La cianidina-3-O-(6’’-malonil-glucósido) pertenece a la categoría de antocianidina-3-O-glucósidos (Aoki et al., 2002). En esta molécula, además del enlace O-glucosídico, hay un enlace a un grupo malonilo en la posición 6’’ de la glucosa (Apéndice). Esta antociana se ha encontrado en alta concentración en frutos rojos como las moras, los arándanos y las frambuesas, y en una concentración más baja en naranjas dulces y lechugas (Yamaguchi et al., 1996), por lo que se ha propuesto como un biomarcador del consumo de estos alimentos. La cianidina-3-O-(6’’-malonilglucósido) también se ha detectado en maíz morado (Peniche-Pavía y Tiessen, 2020). En el apéndice se reportan las distintas cianidinas glucosiladas que se han identificado en el maíz morado.
Pelargonidinas
Esta familia de antocianinas se caracteriza por la presencia de grupos hidroxi en las posiciones 3, 5, 7 y 4’ del ion flavilio (Estévez y Mosquera, 2007). Las pelargonidinas son las principales responsables de la coloración naranja del salmón y los tonos rosados y rojizos de las uvas (Asokapandian et al., 2018). Adicionalmente, como otras antocianinas, tiene múltiples beneficios a la salud. Por ejemplo, en un estudio preclínico basado en un modelo in vivo en ratas, la pelargonidina mejoró la recuperación funcional y atenuó el dolor neuropático producido por daño en la médula espinal (Kooshki et al., 2025). Este efecto resalta su relevancia neuroprotectora y antiinflamatoria (Rashed et al., 2022).
Por otra parte, en múltiples organismos vegetales, la pelargonidina está unida a una molécula de glucosa para formar a la pelargonidina 3-O-glucosido, por acción de la antocianina 3-O-glucosiltransferasa (Wang et al., 2023). Su estructura se caracteriza por un grupo hidroxilo en la posición 3' y una glucosa unida a la posición 3 del anillo C (Fig. 3). Esta glucosilación reduce su actividad antioxidante y cambia su longitud de onda de máxima absorción de 520 a 516 nm (Li et al., 2021).
Además de sus propiedades antioxidantes, estudios recientes han mostrado que esta antocianina tiene un potente efecto antiinflamatorio, particularmente en el tratamiento de enfermedades intestinales inflamatorias como la colitis, disminuyendo la inflamación intestinal y promoviendo la regeneración celular (Ghattamaneni et al., 2020). La pelargonidina 3-O-glucósido se encuentra en frutas como las fresas y los rábanos (Xu et al., 2018). En un estudio del maíz morado andino del Perú, se demostró la presencia de esta antocianina en los extractos hidroalcohólicos de olote (Pedreschi y Cisneros-Zevallos, 2007). En el caso del grano de maíz morado de México, se reportó que la pelargonidina 3-O-glucósido se ubica principalmente en el pericarpio (Peniche-Pavía y Tiessen, 2020).
Por otra parte, la pelargonidina-3-O-(6’’-succinil-glucósido) es un derivado de la pelargonidina 3-O-glucósido, en la que se encuentra enlazado un grupo succinilo en la posición 6’’ de la glucosa. A diferencia de otras antocianinas, esta molécula es poco soluble en agua, es débilmente ácida y se ha detectado naturalmente distribuida en frutos rojos como las moras, fresas y frambuesas. También ha sido reportada su presencia en el grano de maíz morado (Peniche-Pavía y Tiessen, 2020). Las pelargonidinas glucosiladas que han sido identificadas en el maíz morado se enlistan en el apéndice.
Peonidinas
Las peonidinas son otro grupo antocianinas derivado de la cianidina (Martens et al., 2014). Estos compuestos aportan una coloración púrpura a rojiza en flores y frutas (Bureau et al., 2009). Como otras antocianinas, su coloración es sensible a los cambios ácido-base: a pH 2.0, la peonidina es de color rojo cereza, a pH 5.0 es de color rojo-púrpura y a pH 8.0 se torna azul intenso (Zaffino et al., 2015). Sin embargo, a diferencia de otras antocianinas es estable a pH alto (Khoo et al., 2017).
Entre las peonidinas, la más abundante en flores y frutos es la peonidina 3-glucósido. Esta antocianina es responsable del color rojo de diversas flores y algunos frutos como las uvas rojas y las moras (Kurt-Celebi et al., 2020). En su estructura posee un grupo metoxi en la posición 3' y una glucosa en la posición 3 del anillo C (Fig. 3).
Esta molécula ha mostrado actividad antioxidante, antiinflamatoria y cardioprotectora (Chen et al., 2005). La peonidina 3-glucósido demostró ser eficaz en la protección contra el daño oxidativo inducido por el estrés en el corazón y otros tejidos sensibles a la oxidación (Paun et al., 2022). Además, en combinación con otros compuestos presentes en las plantas, puede contribuir a la mejora del perfil lipídico y la reducción del riesgo de enfermedades cardiovasculares (Petroni et al., 2017). La peonidina 3-glucósido también se puede encontrar tanto en semilla como olote del maíz morado (Yang y Zhai, 2010).
Un estudio reciente en células in vitro demostró que la peonidina-3-O-glucósido aislada del olote de maíz morado podría contribuir a disminuir la enfermedad del hígado graso no alcohólico, al regular las funciones mitocondriales y lisosómicas para reducir el estrés oxidativo y la inflamación (Hao et al., 2023). La peonidina 3-O-(6’’-malonil-glucósido) es un derivado de la peonidina 3-O-glucósido, en la que al carbono 6’’ de la glucosa se encuentra enlazado un grupo malonilo (Apéndice). Este compuesto ha sido identificado en el olote y las hojas de maíz morado proveniente de Colombia (Carrera et al., 2023). Estas y otras peonidinas glucosiladas encontradas en maíz morado se listan en el apéndice.
Malvidinas
La malvidina es una antocianina dimetoxilada en las posiciones 3’ y 5’. Este compuesto es el principal responsable del color rojo del vino (Zhao et al., 2010). También ha sido considerado como un biomarcador de la ingesta de arándanos azules. La solubilidad de la malvidina en agua es mayor que en metanol o etanol (Wu et al., 2017). Sin embargo, la solubilidad disminuye conforme aumenta el grado de glucosilación y acilación. La malvidina está constituida por una unidad de ácido siríngico y una unidad de ácido 4-hidroxibenzoico (Devi et al., 2020). Cuando la malvidina es sometida a condiciones de pH alto, como pH>7, la molécula se rompe liberando ácido siríngico (Srinivas et al., 2011). La malvidina se caracteriza por tener cuatro donadores de puentes de hidrógeno, lo que la hace un potencial atenuador de especies reactivas de oxígeno (Chamizo-González et al., 2023). Por ello, la malvidina y sus glicósidos juegan un papel central como agentes antioxidantes y antiinflamatorios (Merecz-Sadowska et al., 2023).
Entre ellos, destaca la malvidina-3-O-glucósido que es el principal pigmento presente en las uvas rojas (Kallithraka et al., 2009). Al ser un derivado de la malvidina, su estructura se compone de una glucosa unida en el átomo de oxígeno de la posición 3. A esta molécula se le atribuyen potentes propiedades antioxidantes y antiinflamatorias, lo que la convierte en un compuesto de interés en la protección contra enfermedades cardiovasculares y cáncer, por lo que su consumo se ha asociado con una mejora en la función cognitiva y la protección de las neuronas contra el daño oxidativo (Ortega y Guerra, 2006). La malvidina-3-O-glucósido está presente tanto en el grano como en el olote del maíz morado (Yang y Zhai, 2010). La estructura de este compuesto puede verse en la figura 3.
Por otra parte, el grupo de investigación de Cevallos-Casals y Cisneros-Zevallos (2003) publicó que los granos y el olote de maíz morado nativo de los Andes son ricos en contenido de antocianinas, lo que concuerda con los hallazgos sobre este grano informado por otros científicos (Cai et al., 2023; Mendoza-Mendoza et al., 2023). Sin embargo, algunos estudios mencionan que existe variabilidad del contenido de antocianinas debido a influencias genéticas y ambientales como tipo de suelo, altitud y exposición a la luz solar (Del Pozo-Insfran et al., 2006). En el cuadro 1 se muestra una recopilación sobre el contenido de antocianinas obtenido del grano, olote y pericarpio del maíz morado, así como del método experimental que dio lugar a la obtención de estos valores.
Cuadro 1: Contenido de antocianinas en distintas accesiones de maíz morado (Zea mays L.). HPLC=Cromatografía líquida de alta resolución, HCI=Ácido clorhídrico.
| Parte de la planta | Contenido de antocianinas por cada 100 g | Metodología | Referencias |
| Mazorca | 1370 a 1430 mg | Extracción con 40%, 50% y 70% EtOH acidificado y análisis | Lao y Giusti, 2018 |
| mediante cromatografía líquida (HPLC) | |||
| Grano y pericarpio | Grano: 0.085 g | Extracción asistida por ultrasonido utilizando etanol y | Mendoza-Mendoza et al., 2023 |
| Pericarpio: 0.959 g | ácido clorhídrico, seguida de espectrofotometría | ||
| Grano y olote | Grano: 496.3 mg | Extracción con metanol acidificado con ácido clorhídrico | Aguilar-Hernández et al., 2019 |
| Olote: 967.9 mg | al 1%. Cuantificación por espectrofotometría; análisis de | ||
| espectros por cromatografía líquida de alta resolución | |||
| (HPLC) | |||
| Grano y olote | Grano: 55.8 mg | Extracción con etanol-agua, cuantificación por | Yang y Zhai, 2010 |
| Olote: 92.3 mg | espectrofotometría | ||
| Grano | 496.3 mg | Extracción con metanol, purificación en columna C18, | Lee y Choung, 2011 |
| análisis mediante espectrometría UV-Vis y HPLC | |||
| Olote | 290 a 1333 mg | Extracción con acetona acuosa al 70% acidificada con HCl. | Jing et al., 2007 |
| Cuantificación con espectrofotometría y HPLC |
Biosíntesis y expresión de genes de las antocianinas en el maíz morado
La biosíntesis de antocianinas en el maíz morado es un proceso metabólico complejo, iniciado con la transformación de la fenilalanina en ácido cinámico por la acción de la enzima fenilalanina amonio-liasa (PAL), y continúa con la conversión de este compuesto en el precursor clave 4-coumaroil-CoA (Guo et al., 2024). Este precursor es condensado con malonil-CoA por la chalcona sintasa (CHS) para formar naringenina chalcona, marcando un paso limitante en la vía de los flavonoides (Dixon et al., 2002). Posteriormente, la chalcona isomerasa (CHI) transforma la naringenina chalcona en naringenina, que es hidroxilada por la flavanona 3-hidroxilasa (F3H) para formar dihidrokaempferol (Park et al., 2011).
Este compuesto es sometido a modificaciones adicionales por enzimas como el flavonoide 3'-hidroxilasa (F3’H), produciendo intermediarios clave como la dihidroquercetina, que son reducidos a leucoantocianidinas por la dihidroflavonol-4-reductasa (DFR) (Sharma et al., 2011). Estas leucoantocianidinas son convertidas en antocianidinas por la antocianidina sintasa (ANS) y estabilizadas mediante glucosilación por la flavonoide-3-O-glucosiltransferasa (UFGT), lo que da lugar a antocianinas solubles y estables (Holton y Cornish, 1995; He et al., 2010).
Los genes asociados a las antocianinas en el maíz morado
La biosíntesis de antocianinas en el maíz morado es un proceso que está controlado por genes estructurales que codifican a las enzimas implicadas y, también, por genes reguladores que determinan la expresión específica en distintos tejidos (Li et al., 2022). El complejo MYB-bHLH-WDR (myeloblastosis-basic Helix-Loop-Helix-WD40) regula la transcripción de genes como CHS, CHI, F3H y DFR, permitiendo un control preciso en la acumulación espacial y temporal de antocianinas (Zhang et al., 2020). También se ha demostrado que factores genéticos específicos, como Booster1 (B1) y Plant color1 (Pl1), desempeñan un papel clave en la regulación de la síntesis en tejidos específicos del maíz (Styles y Coe, 1986). Por otra parte, las antocianinas sintetizadas son transportadas y almacenadas en las vacuolas celulares, donde se agrupan en inclusiones vacuolares que protegen a estas moléculas de la degradación y aseguran su funcionalidad (Goodman et al., 2004).
Factores ambientales y externos
Además de las variables genéticas y biosintéticas, los factores ambientales externos influyen significativamente en la síntesis y acumulación de antocianinas (Shi et al., 2023). La luz es un factor esencial que regula esta biosíntesis a través de fotoreceptores como fitocromos y receptores de luz azul, promoviendo la acumulación de precursores clave como la PAL y la CHS (Fan et al., 2016). Las bajas temperaturas también inducen la expresión de genes estructurales y reguladores, aumentando la síntesis de antocianinas, mientras que temperaturas elevadas pueden degradar estas moléculas debido al incremento de especies reactivas de oxígeno (Christie et al., 1994). El pH del entorno también desempeña un papel crítico: las antocianinas son más estables en condiciones ácidas, donde adoptan formas catiónicas altamente solubles y coloridas (Vankar y Srivastava, 2010). En conjunto, la interacción entre la regulación genética y los factores ambientales permite una producción eficiente y controlada de antocianinas, optimizando su acumulación en el maíz morado.
Compuestos antioxidantes en maíz morado
Como se ha mencionado anteriormente, el maíz morado destaca por su abundancia de antocianinas, un tipo de flavonoides que otorgan su característico color morado vibrante. En varios estudios, las antocianinas del maíz morado han mostrado una potente actividad antioxidante in vitro e in vivo, protegiendo las células de la peroxidación lipídica y el daño oxidativo al ADN (Pedreschi y Cisneros-Zevallos, 2006; Cuevas Montilla et al., 2011). Entre las antocianinas, la cianidina-3-O-glucósido es la más destacada. Estas moléculas tienen la capacidad de neutralizar radicales libres, que son especies reactivas de oxígeno responsables de causar daño celular y contribuir al envejecimiento y enfermedades crónicas como el cáncer y enfermedades cardiovasculares (Meng et al., 2017).
Además de las antocianinas, el maíz morado también contiene otros compuestos fenólicos, como los ácidos protocatecuico y ferúlico, así como derivados de la quercetina que complementan el efecto antioxidante al proteger contra el daño oxidativo en diferentes sistemas celulares (Cuevas Montilla et al., 2011; Suriano et al., 2021). En el cuadro 2 se muestra una recopilación sobre el contenido de antioxidantes obtenido de diferentes partes del maíz morado, así como del método de obtención de estos valores.
Cuadro 2: Contenido de antioxidantes en distintas partes de la planta del maíz morado (Zea mays L.). TE=equivalentes de Trolox, DPPH=2,2-Diphenyl-1-picrylhydrazyl, TEAC=Capacidad Antioxidante Equivalente a Trolox, FRAP=Poder Antioxidante Reductor Férrico, ABTS=2,2’-azino-bis-3-etilbenzotiazolina-6-ácido sulfónico, RP-HPLC-UV=Cromatografía Líquida de Alta Resolución en Fase Reversa con detector ultravioleta, HPLC=Cromatografía líquida de alta resolución, HPLC-FD=Cromatografía Líquida de Alta Resolución con detección de fluorescencia, HPLC-UV=Cromatografía Líquida de Alta Resolución con detector ultravioleta, FA=Ácido ferúlico, GAE=Equivalentes de ácido gálico, CGE=Equivalentes de catequina galato.
| Parte de la planta | Contenido total de antioxidante | Tipo de antioxidantes | Método de evaluación | Referencia |
| Pericarpio | 9.51 μmol TE/ml | Compuestos fenólicos | DPPH y TEAC | Díaz-García et al., 2021 |
| Grano de maíz | 154±1.9 mg FA/100 g | Ácido ferúlico | RP-HPLC-UV | Lopez-Martinez et al., 2009 |
| Grano de maíz | 1.019±0.05 y 0.838±0.11 µg | Antocianinas, derivados de | Ensayo de DPPH y | Pedreschi y Cisneros-Zevallos, 2006 |
| Trolox/µg de fenoles | quercetina | fraccionamiento por | ||
| HPLC | ||||
| Grano de maíz | ABTS: 4.25±0.08 μg/ml; | Melatonina, serotonina, | HPLC-FD, HPLC-UV, | Ratha et al., 2023 |
| DPPH: 7.32±0.26 μg/ml; | ácido protocatecuico | Método de DPPH, FRAP, | ||
| FRAP: 44.41±0.11mmole/g | DPPH | |||
| Grano de maíz | TEAC: 43.1±0.5 μg/ml; | Antioxidantes | Método de DPPH, FRAP, | Yang y Zhai, 2010 |
| DPPH: 48.5±0.5 μg/ml; | TEAC | |||
| FRAP: 16.2±0.5 mmol FeSO4/g | ||||
| Olote | 23.426 a 76.962 mg GAE/g de | Fenoles totales | Método de extracción | Gorriti Gutierrez et al., 2009 |
| fenoles totales | etanólica, determinación | |||
| por DPPH | ||||
| Grano, olote y hoja | Grano: 29.93-69.17 mg GAE/g; | Antocianinas, fenoles | Ensayo de DPPH y TEAC | Simla et al., 2016 |
| Olote: 48.95-271.33mg | totales | |||
| GAE/g; Hoja: 23.48-210.25 mg | ||||
| CGE/100g |
Características nutricionales del maíz morado
El maíz morado es un alimento con una rica composición nutricional, tiene un contenido significativo de fibra, lo que contribuye a la salud digestiva y al control de peso (Subrin et al., 2022). En estudios comparativos se ha demostrado que el maíz morado contiene mayor fibra cruda en comparación con el maíz amarillo (Bayomy, 2017). El contenido proteico del maíz morado es variable, pero se ha encontrado que puede ser superior a otras variedades de maíz, alcanzando valores hasta de 12% (Guillén-Sánchez et al., 2014).
Al igual que otros tipos de maíz, el maíz morado es una fuente rica de carbohidratos, que proporciona energía esencial (Guillén-Sánchez et al., 2014). Un estudio realizado con una variedad subnigroviolácea del Perú encontró que los almidones representan aproximadamente 80% del contenido del maíz morado (Guillén-Sánchez et al., 2014). En el cuadro 3 se muestra un análisis comparativo de la composición nutricional del maíz morado proveniente de diferentes regiones de México, así como de otros países.
Cuadro 3: Datos de la composición proximal de maíz morado (Zea mays L.) de varias regiones del mundo.
| Variables | |||||||
| Lugar | Humedad (%) | Cenizas (%) | Grasas (%) | Proteínas (%) | Carbohidratos (%) | Fibra (%) | Referencia |
| Campeche, México | 10.43±1.03 | 1.42±0.11 | 4.07±0.59 | 6.76±0.27 | 74.30±0.81 | 3.32±0.13 | Mex-Álvarez et al., 2016 |
| Sonora, México | 12.37±0.45 | 1.40±0.13 | 2.07±0.05 | 8.01±0.33 | 59.45±0.90 | 2.07±0.10 | Rodríguez Pérez et al., 2023 |
| Sierra Gorda, Querétaro | 12.12±0.00 | 2.00±0.24 | 1.95±0.11 | 10.74±0.38 | 70.29±0.15 | 2.90±0.06 | Feregrino-Pérez et al., 2024 |
| Ica, Perú | 9.30±0.23 | 3.37±0.09 | 0.04±0.01 | 6.02±0.18 | 81.27±0.80 | --- | Valle Campos et al., 2019 |
| Perú | 11.49±0.17 | 1.03±0.42 | 4.51±0.22 | 10.84±0.55 | 68.86±0.79 | 2.27±0.07 | Guillén-Sánchez et al., 2014 |
| Argentina | --- | 1.85 | 6.1 | 10.2 | --- | --- | Rodríguez et al., 2024 |
| Egipto | 10.73±0.31 | 1.89±0.61 | 3.95±0.20 | 12.56±0.24 | 67.29±0.83 | 3.58±0.21 | Bayomy, 2017 |
Efectos benéficos del maíz morado en la salud humana
Por otra parte, el maíz morado ha sido ampliamente estudiado por sus beneficios para la salud humana debido a su alto contenido de compuestos fenólicos, principalmente antocianinas, que le otorgan una amplia gama de propiedades bioactivas. A continuación, se detallan los efectos benéficos del maíz morado sobre la salud humana.
Prevención de la obesidad
Uno de los hallazgos más significativos de los estudios es el potencial del maíz morado para prevenir la obesidad y regular el metabolismo de las grasas (Luna-Vital et al., 2020). Las antocianinas presentes en este tipo de maíz han demostrado ser eficaces en la reducción del aumento de peso en animales alimentados con dietas altas en grasas (Lefevre et al., 2011). En estos estudios, la administración de antocianinas redujo el aumento de peso corporal, disminuyó la acumulación de grasa epididimal y reguló los niveles de triglicéridos y colesterol en el suero (Tsuda et al., 2003; Xu et al., 2021).
Los efectos mencionados están mediados por la activación de la AMPK (proteína quinasa activada por monofosfato de adenosina) en el hígado, que es un regulador clave del metabolismo energético (Luna-Vital et al., 2020). La activación de esta vía promueve la oxidación de ácidos grasos y reduce la síntesis de lípidos, lo que sugiere que las antocianinas del maíz morado podrían ser útiles en la prevención de la obesidad y el tratamiento de desórdenes metabólicos como el síndrome metabólico y la resistencia a la insulina (Xu et al., 2021). Investigaciones previas indican que el consumo de maíz pigmentado (azul, morado, magenta) está asociado a un índice glucémico más bajo que el maíz blanco (Agama-Acevedo et al., 2011), lo que lo hace un alimento benéfico para la salud.
Reducción de la resistencia a la insulina
La ingesta de maíz morado en la dieta también ha mostrado efectos beneficiosos sobre la regulación de los niveles de glucosa en sangre y la disminución de la resistencia a la insulina (Huang et al., 2015), lo que lo convierte en un potencial agente terapéutico en el tratamiento de la diabetes tipo 2 y en su prevención. En estudios con ratones alimentados con dietas ricas en grasas, la suplementación con extractos de maíz morado redujo la hiperglucemia e hiperinsulinemia, normalizando los niveles de insulina y glucosa en sangre (Chayati et al., 2019). Estos resultados sugieren que el consumo de maíz morado puede ayudar a mejorar la sensibilidad a la insulina y prevenir el desarrollo de diabetes inducida por la obesidad (Tsuda et al., 2003). Las antocianinas del maíz morado activan el receptor de ácidos grasos libres 1 (FFAR1) y la glucocinasa, lo que mejora la secreción de insulina y la captación de glucosa en el hígado (Luna-Vital y Gonzalez de Mejia, 2018).
Efecto benigno en la función hepática
El maíz morado, rico en antocianinas como la cianidina-3-O-glucósido, mejora significativamente la función hepática a través de múltiples mecanismos (Cui et al., 2021). Estas antocianinas activan la vía AMPK en el hígado, regulando el metabolismo lipídico al inhibir la síntesis de ácidos grasos y promover su oxidación, lo que previene la acumulación de lípidos y la aparición de hígado graso no alcohólico (Xu et al., 2021). Además, reduce los niveles de estrés oxidativo y marcadores inflamatorios, favoreciendo la regeneración celular hepática y protegiendo contra daños inducidos por dietas altas en grasas (Tsuda et al., 2003). También mejora la captación de glucosa en las células hepáticas y regula la gluconeogénesis, contribuyendo al control de los niveles de glucosa en sangre, un beneficio especialmente relevante en condiciones como la resistencia a la insulina (Pedreschi y Cisneros-Zevallos, 2007). Estos efectos combinados destacan al maíz morado como un alimento funcional con gran potencial para prevenir y tratar trastornos (Rolandelli et al., 2023).
Prevención de la hipertensión
La prevención de la hipertensión ha sido vinculada con el consumo de maíz morado, ya que este contiene antocianinas y otros compuestos que presentan efectos vasoprotectores (Finkel et al., 2013). En estudios preclínicos, se ha observado que estos compuestos mejoran la función endotelial y reducen la presión arterial en modelos animales con hipertensión inducida, lo cual es prometedor para el tratamiento de la hipertensión en humanos, una de las principales causas de enfermedades cardiovasculares (Cuevas Montilla et al., 2011). Además, los compuestos fenólicos del maíz morado contribuyen a la mejora de la elasticidad de los vasos sanguíneos y a la reducción de la inflamación vascular, lo que también se ha asociado con un menor riesgo de enfermedades cardiovasculares (Lao et al., 2017).
Efectos antiinflamatorios
Las antocianinas presentes en este alimento, en particular la cianidina-3-O-glucósido, han demostrado tener la capacidad de reducir los niveles de citocinas inflamatorias como el factor de necrosis tumoral (TNF-α) (Sun y Li, 2018). El TNF-α juega un papel importante en los procesos de la inflamación crónica relacionada con enfermedades como la artritis, las enfermedades cardiovasculares (Pedreschi y Cisneros-Zevallos, 2007) y la enfermedad renal crónica (Saucedo et al., 2018), entre otras. Este efecto antiinflamatorio se atribuye en gran medida a la capacidad de las antocianinas para modular el estrés oxidativo, actuando como agentes neutralizantes de especies reactivas de oxígeno (ROS).
El estrés oxidativo es un proceso clave en la patogénesis de diversas enfermedades crónicas, incluyendo el cáncer y los trastornos cardiovasculares (Lao et al., 2017; Mazewski et al., 2017). De hecho, la acción de las antocianinas para disminuir la inflamación inducida por el TNF-α ha sido asociada a los mecanismos de diferenciación de adipocitos y la reducción de la acumulación lipídica en tejidos in vitro (Luna-Vital et al., 2017). Estos hallazgos enfatizan el carácter antiinflamatorio de estos compuestos.
Beneficios cardiovasculares
Los polifenoles presentes en el maíz morado, como la quercetina y otros flavonoides, también han mostrado efectos positivos en la salud cardiovascular (Ramos-Escudero et al., 2012). Estos compuestos mejoran la elasticidad de los vasos sanguíneos al promover la producción de óxido nítrico, un vasodilatador natural, lo que favorece la relajación vascular y previene la rigidez arterial (Tian et al., 2018).
Los extractos de maíz morado reducen la presión arterial al regular la vasodilatación y disminuir la inflamación en los tejidos vasculares (Saikaew et al., 2018). También ayudan a reducir los niveles de colesterol LDL, inhibiendo su oxidación y previniendo la formación de placas ateroscleróticas, fundamentales en la prevención de la aterosclerosis (Trehan et al., 2018).
Los beneficios observados se sustentan en estudios in vitro, donde las antocianinas demostraron eliminar radicales libres (Harakotr et al., 2014), y en estudios in vivo, donde modelos animales mostraron mejoras en presión arterial, perfiles lipídicos e inflamación sistémica tras el consumo de extractos de maíz morado (Tian et al., 2021). En humanos, el consumo de estos extractos también ha mostrado mejoras en pacientes con hipertensión leve a moderada (Finkel et al., 2013). Este conjunto de evidencias posiciona al maíz morado como un recurso natural prometedor para la prevención y tratamiento de enfermedades cardiovasculares (Kim et al., 2023).
Propiedades anticancerígenas
Las antocianinas del maíz morado también han sido capaces de inhibir el crecimiento de células cancerosas en estudios in vitro y han mostrado efectos antimutagénicos en diferentes modelos (Guillen-Sánchez et al., 2014). Se ha demostrado que el consumo de maíz morado puede prevenir la carcinogénesis colorrectal inducida químicamente en ratas, lo que sugiere su posible aplicación en la prevención del cáncer en humanos (Pedreschi y Cisneros-Zevallos, 2007; Cuevas Montilla et al., 2011). Complementariamente, los extractos ricos en antocianinas han evidenciado un efecto antiproliferativo sobre las células de cáncer colorrectal, promoviendo la apoptosis (muerte celular programada) y suprimiendo la angiogénesis (formación de nuevos vasos sanguíneos) en los tumores (Mazewski et al., 2017).
Conclusiones
El maíz morado (Zea mays) es un producto agrícola de gran relevancia científica y cultural, gracias a su composición rica en compuestos bioactivos como las antocianinas y antioxidantes, que contribuyen a múltiples beneficios para la salud humana. Este grano no solo representa un símbolo gastronómico y cultural de varias regiones de México y Latinoamérica, sino también destaca por su potencial terapéutico, demostrado por sus propiedades antiinflamatorias, anticancerígenas, y por la prevención de enfermedades metabólicas como la obesidad, diabetes tipo 2 y trastornos cardiovasculares. Además, las investigaciones recientes han impulsado el desarrollo de técnicas avanzadas para la extracción y caracterización de sus compuestos bioactivos, maximizando su aplicación en las industrias alimentaria, farmacéutica y cosmética.
Cabe destacar que este trabajo no solo compila y analiza los avances en el conocimiento sobre las propiedades funcionales y aplicaciones del maíz morado, sino que también proporciona evidencia del potencial de este recurso natural en la salud humana y en su aprovechamiento como alimento funcional. Estos hallazgos resaltan la necesidad de continuar explorando la composición química que da al maíz morado sus propiedades únicas, su impacto en la salud y de desarrollar innovaciones que faciliten su integración en dietas globales y productos terapéuticos.
















