Introducción
La familia Apocynaceae tiene distribución cosmopolita e incluye más de 4300 especies de herbáceas perennes, arbustos, lianas y suculentas agrupadas en cinco subfamilias y alrededor de 322 géneros (Christenhusz et al., 2017). En México, esta familia ocupa el lugar número 12 en diversidad con más de 418 especies, 52 géneros y tres subfamilias: Rauvolfioideae, Apocynoideae y Asclepiadoideae, siendo esta última la más diversa con aproximadamente 75% de las especies del país (Alvarado-Cárdenas et al., 2020).
Dentro de Apocynaceae se encuentran especies de interés farmacéutico (medicamentos y compuestos tóxicos), industrial (p.ej., caucho y pigmentos) y alimenticio. Por ejemplo, del tallo y hojas de Catharanthus roseus (L.) G. Don (Rauvolfioideae) se obtienen alcaloides (vinblastina y vincristina) empleados como antineoplásicos (Bhadane et al., 2018). De especies de los géneros Asclepias L., Nerium L., Cerbera L., Thevetia L., Strophanthus DC. y Apocynum L. se han aislado cardenólidos empleados contra la insuficiencia cardiaca y compuestos tóxicos (Al-Snafi, 2015; Bhadane et al., 2018). En el género Asclepias se han reportado especies con alcaloides potencialmente mortales, mientras que otras son empleadas en medicina tradicional por sus propiedades analgésicas y para tratar problemas dermatológicos y respiratorios (p.ej., A. albicans S. Watson, A. glaucescens Kunth y A. quinquedentata A. Gray; Al-Snafi, 2015; Fernández-Brewer et al., 2008).
Por otro lado, a pesar de la gran cantidad de géneros y especies con demostrada toxicidad, quizás el uso más frecuente de especies de Apocynaceae es como alimento. Por ejemplo, la ciruela de Natal (Carissa macrocarpa (Eckl.) A. DC.) y otras especies africanas de Carissa L. producen frutos comestibles, al igual que varias especies de los géneros Araujia Brot. y Gonolobus Michx. en Sudamérica (Bayón y Arambarri, 1999; Stevens 2005; Christenhusz et al., 2017). Las raíces o bulbos de diferentes especies de Ceropegia L. y Marsdenia R. Br. también se consumen, así como las hojas de Dregea E. Mey. (Christenhusz et al., 2017) y de varias Asclepias mexicanas (Fernández-Brewer et al., 2008; González-Elizondo et al., 2024).
En México, los frutos comestibles de diferentes especies de la subfamilia Asclepiadoideae reciben comúnmente el nombre de talayotes, e incluye especies de diferentes géneros como Cynanchum L., Gonolobus, Polystemma Decne. (citados como Matelea Aubl.), Ruehssia H. Karst. (citados como Marsdenia) y Talayotea L.O. Alvarado (Ávila-Uribe et al., 1994; Yetman y Van Devender, 2002; Pío-León et al., 2017; Alvarado-Cárdenas, 2021; Sandoval-Ortega et al., 2023). Estos frutos se consumen crudos directamente de la planta cuando son tiernos o asados, o hervidos en agua con sal en etapas de maduración intermedia. De manera similar, de las inflorescencias y los frutos tiernos de especies de Funastrum E. Fourn. se ha reportado su consumo como quelites en el noroeste de México, principalmente entre las comunidades nativas de Sonora (Hodgson, 2001). Sin embargo, a pesar de la amplia tradición en el consumo de talayotes en México y de los potenciales efectos tóxicos que existen en la familia Apocynaceae, no existen estudios sobre la composición nutricional, fitoquímica o posible toxicidad de estas especies para recomendar o advertir sobre su consumo.
En el presente trabajo se analiza la composición nutricional, fitoquímica, antioxidante y toxicidad de cinco especies de la subfamilia Asclepiadoideae (Apocynaceae) del noroeste de México, con el propósito de contribuir al conocimiento sobre los aportes a la nutrición o posibles efectos perjudiciales de su consumo.
Materiales y Métodos
Material vegetal
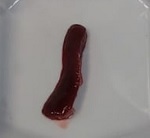
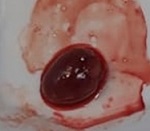
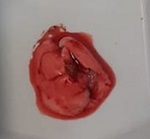
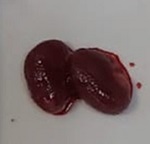
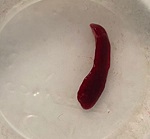
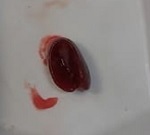
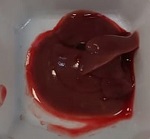
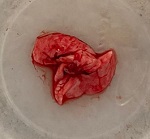
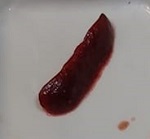
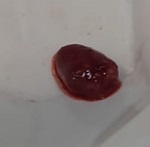
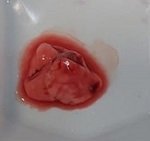
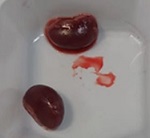
Se estudiaron los frutos de Funastrum clausum (Jacq.) Schltr., Funastrum heterophyllum (Engelm. ex Torr.) Standl., Gonolobus naturalistae M.G. Chávez, Pío-León & L.O. Alvarado y Ruehssia tholiformis (Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado, así como inflorescencias de Funastrum clausum, F. heterophyllum y F. pannosum (Decne.) Schltr. (Fig. 1). Los materiales se recolectaron del medio silvestre en diferentes municipios de Sinaloa, México (Cuadro 1). Los frutos se cosecharon en madurez comercial, de acuerdo con sus recomendaciones de consumo que, para estas especies, es previo a la madurez fisiológica. Para las inflorescencias se seleccionaron tanto botones como flores en antesis. De los frutos se recolectaron aproximadamente 2 kg y de las inflorescencias 1 kg. En cada caso, los materiales recolectados se trasladaron inmediatamente al laboratorio de la Facultad de Ciencias Químico-Biológica de la Universidad Autónoma de Sinaloa, donde se lavaron en agua corriente, se cortaron en rodajas de 1 cm de ancho (frutos) y se congelaron a -70 °C (ThermoScientific TS series, Thermo Fisher Scientific Inc., Massachusetts, EUA) para liofilización y posteriormente a -20 °C (CH-25, Torrey, Nuevo León, México) hasta su posterior uso. El material para el análisis proximal se procesó mediante las metodologías señaladas para cada componente, mientras que para el resto de análisis se emplearon extractos metanólicos.

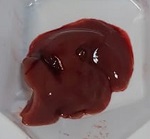
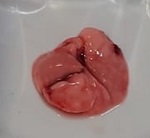
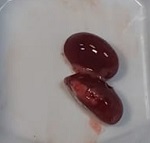
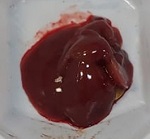
Figura 1: Especies de Asclepiadoideae evaluadas en el presente estudio. A, E. Funastrum heterophyllum (Engelm. ex Torr.) Standl.; B, D. Funastrum clausum (Jacq.) Schltr.; C. Funastrum pannosum (Decne.) Schltr.; F. Gonolobus naturalistae M.G. Chávez, Pío-León & L.O. Alvarado; G. Ruehssia tholiformis (Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado; H, I. Diferentes formas de preparación para consumo de los frutos de Ruehssia tholiformis y otras especies de Ruehssia en Sinaloa, México. Fotos de Juan Fernando Pío León (A-F, G, I) y Gabriela López Angulo (H).
Cuadro 1: Localidades y fecha de colecta de las especies comestibles de Asclepiadoideae empleadas en este estudio
| Especies | Municipios de colecta | Coordenadas | Fecha de colecta | No. de colecta/obs. en iNaturalistMX | |
| Frutos | Ruehssia tholiformis (Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado | San Ignacio | 24.0867,-106.6439 | 21.IX.2021 | Pio-León 356 CIIDIR115820617 |
| Elota | 23.4078,-106.5219 | 25.VI.2021 | |||
| Gonolobus naturalistae M.G. Chávez, Pio-León & L.O. Alvarado | Mazatlán | 23.5256,-106.2712 | 3.X.2021 | Pio-León 246, CIIDIR | |
| Funastrum heterophyllum (Engelm. ex Torr.) Standl. | Elota | 23.8517,-106.8517 | 21.VI.2021 | 115820609 | |
| Funastrum clausum (Jacq.) Schltr. | Elota | 23.8978,-106.9174 | 19.VII.2021 | Pio-León 378 CIIDIR115820620 | |
| Inflorescencias | Funastrum heterophyllum (Engelm. ex Torr.) Standl. | Elota | 23.8517,-106.8517 | 21.VI.2021 | 115820609 |
| Funastrum clausum (Jacq.) Schltr. | Elota | 23.8978,-106.9174 | 19.VII.2021 | Pio-León 378 CIIDIR115820620 | |
| Funastrum pannosum (Decne.) Schltr. | Elota | 23.3080,-106.4857 | 20.VII.2021 | Pio-León 229 CIIDIR57867302 | |
| Parte aérea | Asclepias curassavica L. | Culiacán | 24.8137,-106.3905 | 14.VIII.2021 | 294398591 |
| Asclepias curassavica L. | Elota | 24.0959,-106.6768 | 14.VIII.2021 | 291292300 |
Para cada especie se prepararon especímenes que se depositaron en los herbarios CIIDIR y MEXU, así como registros fotográficos en la plataforma iNaturalistMX: Funastrum heterophyllum (iNaturalistMX, 2024a), Funastrum clausum (Pío-León 378, CIIDIR!, iNaturalistMX, 2024b), Funastrum pannosum (Pío-León 229, CIIDIR!; iNaturalistMX, 2024c), Gonolobus naturalistae (Pío-León 246, CIIDIR!) y Ruehssia tholiformis (Pío-León 356, CIIDIR!, iNaturalistMX, 2024d). Adicionalmente, para el tamizaje fitoquímico y pruebas de toxicidad se emplearon las partes aéreas de Asclepias curassavica L. (iNaturalistMX, 2020e, f) como control positivo.
Preparación de extractos metanólicos (EM)
El material vegetal fue liofilizado, molido y tamizado por una malla número 40 para obtener la harina correspondiente. Posteriormente, la harina y el metanol se mezclaron en proporción 1:20 p/v, cambiando el disolvente cada 24 horas. Al final todas las fases de metanol fueron mezcladas y concentradas por evaporación del solvente en un rotavapor (Buchi Labortechnik AG, Flawil, Suiza). Los EM se almacenaron a -20 °C en condiciones de oscuridad hasta su uso.
Análisis fitoquímico cualitativo
La presencia o ausencia de las principales familias de fitoquímicos se determinó por ensayos colorimétricos y de precipitación, así como por cromatografía en capa fina (Harbone, 1984): hidrólisis ácida y revelación en capa fina con vainillina y UV a 253 para fenólicos; reacción de Salkowski para terpenos y esteroles; prueba de Shinoda para flavonoides; reacción con solución de gelatina al 1% y solución de sulfato de quinina con FeCl3 para taninos; formación de espuma para saponinas; fluorescencia amarilla por reacción de NaOH para cumarinas; reacción de Bornträger por antracénicos para la detección de quinonas; reactivos de Dragendorff, Mayer y Wagner para la identificación de alcaloides; y reactivos de Baljet, Raymond-Marthoud, Keller-Killiani, Lieberman-Burchard y Salkowski para cardiotónicos. Los resultados de cada reacción se expresaron en términos cualitativos de acuerdo con la intensidad de la reacción observada: - = ausente, + = presente, ++ = abundante, +++ = muy abundante.
Toxicidad en Artemia salina
Se utilizó la metodología descrita por Meyer et al. (1982) con algunas modificaciones. Los EM se disolvieron en DMSO al 10% en solución salina para obtener una solución concentrada de 2000 µg/ml. La evaluación se realizó por triplicado en tubos de ensayo y se empleó DMSO al 10% v/v como control negativo. De resultar tóxicos, cada EM se evaluó a concentraciones en el rango de 10 a 1500 µg/ml. El nivel de toxicidad se estableció con la escala de CYTED (Meyer et al., 1982; Navarro et al., 2010): extremadamente tóxico (1-10 µg/ml), altamente tóxico (10-100 µg/ml), moderadamente tóxico (100-500 µg/ml), ligeramente tóxico (500-1000 µg/ml), prácticamente no tóxico (1000-1500 µg/ml) y relativamente inocuo (>1500 µg/ml).
Toxicidad aguda en modelo de ratón
Este ensayo se realizó siguiendo el método establecido por la OECD (2002), aprobado por el comité de ética de la Facultad de Medicina Veterinaria y Zootecnia de la Universidad Autónoma de Sinaloa (protocolo 33/0521). Se emplearon ratones balb/c hembras de entre 8 y 12 semanas de edad y con un peso promedio de 24 a 28 g. Los animales se mantuvieron en el bioterio de la Facultad de Ciencias Químico -Biológicas de la Universidad Autónoma de Sinaloa, a 25 °C, ciclos de luz/oscuridad de 12 h y agua y dieta ad libitum. Los ratones fueron distribuidos de manera aleatoria en 8 grupos (n = 3) y un grupo para el control negativo. Los extractos homogenizados en Tween 80 al 10% en agua destilada fueron administrados por vía intragástrica en dosis única (2000 mg/kg p.c.). Al grupo control negativo se le administró solo el Tween 80. Los animales fueron tratados bajo los lineamientos de la Norma Oficial Mexicana para el Uso y Bienestar de los Animales de Laboratorio (DOF, 2021).
Después de administrar la dosis, cada ratón fue monitoreado de manera individual y continua durante los primeros 30 min, posteriormente cada 30 min hasta las 4 h y enseguida cada 24 h durante 15 días. El peso de los animales se registró antes de administrarles las dosis y en el día 30 antes del sacrificio. Los animales fueron sedados y sacrificados por dislocación cervical, posteriormente a sus órganos se les hizo un análisis macroscópico.
Fenólicos totales
Los fenólicos totales se determinaron mediante el método de Folin-Ciocalteu (Singleton y Rosi, 1965). Se prepararon soluciones de 5 y 10 mg/ml de los extractos metanólicos en metanol. Las muestras se colocaron en una microplaca de 96 pocillos para medir la absorbancia a 765 nm en un lector Synergy HTX (Agilent, Santa Clara, California, EUA). Para el blanco se utilizó metanol puro. Para la cuantificación se elaboró una curva de calibración con ácido gálico (0-500 µg/ml) y los resultados se expresaron como microgramos Equivalentes de Ácido Gálico por gramo de muestra seca (mg EAG/g b.s.).
Flavonoides totales
Los flavonoides totales se analizaron en microplaca siguiendo la metodología de Quettier-Deleu et al. (2000). Los extractos metanólicos se evaluaron a 5 y 20 mg/ml. En la cuantificación se empleó una curva de calibración con quercetina (0-500 mg/ml), midiendo la absorbancia a 405 nm en el lector de microplacas Synergy HTX y registrando los resultados como Equivalentes de Quercetina (mg EQ/g b.s.).
Taninos condensados
Para la cuantificación de taninos totales se prepararon soluciones de vainillina al 0.5% y de HCl al 4% como lo describe la metodología de Price et al. (1978). El extracto metanólico (10 mg) se disolvió en 1 ml de metanol y se homogenizó en vórtex; para el blanco se empleó metanol. El ensayo se realizó en microplaca de 96 pocillos y se leyó a una absorbancia de 500 nm en el lector Synergy HTX. El contenido de taninos totales se determinó empleando una curva de calibración de catequina (0-200 µg/ml en metanol) y se expresó como µg Equivalentes de Catequina por mg de harina en peso seco (mg EC/g b.s.).
Actividad antioxidante in vitro
Método DPPH
El método mide la capacidad de las sustancias para donar electrones al radical 1,1-difenil-picrilhidrazilo (DPPH) (Brand-Williams et al., 1995). Las muestras se disolvieron en DMSO (20 mg/ml) y 50 µl se mezclaron con 150 µl de metanol para obtener una concentración de 5 mg/ml. Como blanco y para la corrección de color se utilizó metanol. En la cuantificación se utilizó una curva de calibración con soluciones de Trolox (0-200 µg/ml), procesándose de la misma manera que las muestras. El ensayo se realizó en microplaca y se registró la absorbancia a 515 nm obtenida en lector Synergy HTX. La actividad antioxidante fue expresada en micromoles Equivalentes de Trolox (µmol ET/g de EM).
Método ABTS
Este método colorimétrico se basa en la oxidación del reactivo ABTS (ácido 2,2´-azinobis-3-etilbenzotiazolina-6-sulfónico); el radical formado es inactivado por antioxidantes mediante la transferencia de electrones o átomos de hidrógeno (Re et al., 1999). El ABTS•+ se preparó mezclando 5 ml de reactivo ABTS 7 mM y 88 µl de persulfato de potasio 140 mM y la mezcla se dejó reposar en la oscuridad durante 12-16 h a 25 °C. El radical ABTS•+ fue diluido en una solución tampón de fosfato (PBS) (7 mM, pH 7.4) para obtener una absorbancia de 0.700 ± 0.020 a 734 nm. Las muestras fueron preparadas de la misma manera que en el ensayo por DPPH. Para el llenado de la placa, a cada pozo se añadieron 25 µl de la muestra y 175 µl de la solución de ABTS•+; como blanco se utilizó ABTS•+. La placa fue incubada en oscuridad a 37 °C durante 10 min y se registró la absorbancia a 734 nm en el lector Synergy HTX. Para la cuantificación se preparó una curva de calibración de Trolox (0-200 µg/ml) y la actividad antioxidante fue expresada en micromoles Equivalentes de Trolox (µmol ET/g g.s.).
Método ORAC
Este método mide la inactivación de radicales peroxilo a través de una disminución de fluorescencia (Huang et al., 2022; Prior et al., 2005). Las muestras se prepararon a una concentración 1:20 v/v en PBS (75 mM, pH 7.4). Posteriormente, en una microplaca negra de 96 pocillos se añadieron 25 µl de muestra, 25 µl de PBS como blanco o 25 µl de Trolox (25-125 µM). La microplaca se colocó en el lector Synergy HTX que automáticamente añadió 200 µl de fluoresceína (0.96 µM) y 75 µl de APPH (95.8 mM). Las longitudes de onda empleadas en la medición de la fluorescencia fueron 485 nm (ex) y 525 nm (em); las lecturas se tomaron cada minuto hasta los 75 min. La actividad antioxidante fue determinada contrastando el área bajo la curva obtenida con Trolox y la obtenida con la muestra. Los resultados son expresados como micromoles Equivalentes de Trolox (µmol TE/g b.s.).
Composición proximal
El análisis proximal se basó en las metodologías de la AOAC (1999): Kjeldahl (960.52) para proteínas, Soxhlet (945.16) para lípidos, cenizas por calcinación (940.26), humedad (925.09) y fibra cruda (985.29). La fibra dietaria se determinó empleando el paquete comercial Total Dietary Fiber Assay Kit y siguiendo las especificaciones de Sigma-Aldrich Co. (St. Louis, MO, USA). Los carbohidratos totales se calcularon por diferencia de peso y el contenido calórico se calculó considerando 9 kcal/g de lípido y 4 kcal/g de proteína o carbohidrato.
Análisis estadístico
Los datos de análisis proximal, cuantificación fitoquímica y capacidad antioxidante se evaluaron mediante ANDEVA de una sola vía y las medias se compararon por la prueba de Fisher (α = 0.05). En el estudio in vivo se realizó la prueba de normalidad Kolmogorov-Smirnov. Los datos no normales fueron contrastados mediante la prueba no paramétrica de Kruskal-Wallis y los datos normales fueron analizados por ANDEVA de una sola vía; las medias se compararon por la prueba de Dunnet (α = 0.05). Las muestras se analizaron en al menos dos experimentos independientes por triplicado. Para determinar las pruebas fueron empleados los softwares Microsoft Excel v. 2019 (Microsoft Corporation, 2019), Minitab v. 2019, Statgraphics Centurion v. 16.1 (Statgraphics, 2019) e IBM SPSS Statistics v. 28.0.1.0. (IBM, 2021). La matriz de correlación se construyó mediante el software Microsoft Excel empleando la función coeficiente de correlación del menú análisis de datos.
Resultados
Caracterización fitoquímica
Todas las inflorescencias y frutos evaluados fueron positivos para fenólicos, flavonoides y triterpenos, pero negativas para alcaloides y saponinas, a excepción de Asclepias curassavica (Cuadro 2). La mayoría de los materiales contienen cardiotónicos, excepto las inflorescencias de Funastrum pannosum y los frutos de Gonolobus naturalistae. Los flavonoides mostraron reacciones más intensas que los compuestos fenólicos en cinco de las ocho muestras evaluadas.
Toxicidad en Artemia salina
Las inflorescencias y frutos de las especies comestibles de talayotes fueron inocuas contra Artemia salina (L., 1758), 1758 (CL50 > 2000 ppm). En contraste, el extracto de Asclepias curassavica indujo parálisis a 2000 ppm, que se considera un signo de toxicidad positiva de acuerdo con el criterio de Schmidt (1985).
Cuadro 2: Caracterización fitoquímica de los extractos metanólicos de inflorescencias y frutos de especies comestibles de Asclepiadoideae. Abundancia relativa: += presente; ++= abundante; +++= muy abundante; -= no detectado.
| Metabolitos secundarios | Especies | ||||||||
| Inflorescencias | Frutos | Parte aérea | |||||||
| Funastrum heterophyllum(Engelm. ex Torr.) Standl. | Funastrum clausum(Jacq.) Schltr. | Funastrum pannosum(Decne.) Schltr. | Funastrum heterophyllum(Engelm. ex Torr.) Standl. | Funastrum clausum(Jacq.) Schltr. | Ruehssia tholiformis(Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado | Gonolobus naturalistaeM.G. Chávez, Pio-León & L.O. Alvarado | Asclepias curassavica L. | ||
| Fenólicos | ++ | ++ | ++ | + | + | + | + | + | + |
| Saponinas | - | - | - | - | - | - | - | - | - |
| Flavonoides | +++ | ++ | +++ | ++ | ++ | + | + | + | + |
| Alcaloides | - | - | - | - | - | - | - | - | - |
| Triterpenos | + | + | + | + | + | + | + | + | + |
| Cumarinas | ++ | - | +++ | - | - | - | - | - | - |
| Antracénicos | + | + | + | + | + | + | + | + | + |
| Cardiotónicos | - | - | - | - | - | - | - | - | - |
| Azúcares reductores | + | + | + | + | + | + | + | ++ | + |
Toxicidad en modelo de ratón
En concordancia con los resultados del ensayo en Artemia, las especies comestibles también fueron inocuas en el estudio in vivo de toxicidad aguda (DL50 > 2000 mg/kg p.c.) (OECD, 2002). Los ratones tratados mostraron comportamiento y características normales hasta el día 30 de observación, similar al exhibido por los animales del grupo control (Tween 80 al 10%). La ganancia de peso de los ratones y el peso de sus órganos no presentó diferencias significativas comparadas entre los grupos evaluados con el grupo control (Cuadro 3). La observación macroscópica de los órganos también mostró características normales (Apéndice). La toxicidad in vivo en ratones del extracto de Asclepias curassavica no se evaluó debido a los resultados del análisis fitoquímico (presencia de alcaloides), toxicidad en Artemia salina y los reportes publicados de toxicidad (Rodrigues-Maciel et al., 2019; Alonso-Castro et al., 2021).
Cuadro 3: Evaluación de toxicidad in vivo de los extractos metanólicos de especies comestibles de Asclepiadoideae en ratones Balb/c. Los resultados están expresados como media ± DE del peso relativo de órganos (n = 3). En datos con distribución normal (pulmón, LSD = 0.06) se empleó ANDEVA de una vía, seguido de comparación múltiples de medias (Fischer, P<0.05). En datos no paramétricos (ganancia de peso, hígado, riñón, bazo y corazón) se empleó Kruskal-Wallis (P<0.05). Letras superíndice diferentes en una misma columna indican que son significativamente diferentes (P<0.05).
| Tejido | Especies | Ganancia de peso (g) | Peso relativo de órganos (g/100 g de peso corporal) | ||||
| Hígado | Riñón | Bazo | Corazón | Pulmón | |||
| Control | 4.97±1.16a | 5.66±0.89a | 1.29±0.07a | 0.43±0.09a | 0.51±0.02a | 0.72±0.09a | |
| Frutos | Funastrum heterophyllum(Engelm. ex Torr.) Standl. | 4.77±0.61a | 5.14±0.34a | 1.28±0.08a | 0.40±0.09a | 0.60±0.15a | 0.61±0.07a |
| Funastrum clausum (Jacq.) Schltr. | 6.00±4.27a | 4.57±1.08a | 1.26±0.10a | 0.32±0.03a | 0.54±0.07a | 0.75±0.12a | |
| Ruehssia tholiformis(Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado | 5.57±3.33a | 4.72±0.21a | 1.39±0.03a | 0.34±0.04a | 0.49±0.04a | 0.64±0.16a | |
| Gonolobus naturalistaeM.G. Chávez, Pio-León & L.O. Alvarado | 7.80±4.37a | 5.18±0.38a | 1.26±0.05a | 0.42±0.12a | 0.56±0.06a | 0.63±0.08a | |
| Inflorescencias | Funastrum heterophyllum(Engelm. ex Torr.) Standl. | 5.93±2.44a | 5.26±0.22a | 1.25±0.12a | 0.42±0.08a | 0.49±0.06a | 0.72±0.10a |
| Funastrum clausum (Jacq.) Schltr. | 7.93±1.25a | 5.68±0.70a | 1.38±0.08a | 0.37±0.09a | 0.56±0.10a | 0.76±0.18a | |
| Funastrum pannosum (Decne.) Schltr. | 4.77±1.37a | 4.61±0.23a | 1.29±0.06a | 0.39±0.09a | 0.50±0.07a | 0.70±0.08a | |
Contenido de fenólicos y flavonoides totales
El contenido de fenólicos totales varió desde nulo o escaso para Ruehssia tholiformis hasta 19.45 mg EAG/100 g para los frutos de Funastrum clausum (Cuadro 4). La concentración de flavonoides fue considerablemente mayor en las inflorescencias (14.82-17.49 mg EQ/100 g) que en los frutos (1.42-2.72 mg EQ/100 g). Ninguno de los materiales presentó taninos cuantificables por el método empleado.
Cuadro 4: Contenido en fenólicos totales, flavonoides totales y actividad antioxidante por tres métodos (DPPH, ABTS y ORAC) en inflorescencias y frutos de especies comestibles de Asclepiadoideae. Los resultados son expresados como media ± DE del porcentaje en base seca (n = 3). Para el análisis de los datos se empleó ANDEVA de una vía, seguido de comparación múltiple de medias (Fischer, P<0.05). Letras superíndice diferentes en una misma columna indican diferencias significativas. Donde: EM = extracto metanólico; EAG = equivalentes de ácido gálico; EQ = equivalentes de quercetina; ET = equivalentes de Trolox; LSD = LSD de Fisher o diferencia mínima significativa, por sus siglas en inglés.
| Especies | Fenólicos totales(µg EAG/g b.s.) | Flavonoides totales(µg EQ/g b.s.) | Actividad antioxidante (µmol ET/g b.s.) | |||
| DPPH | ABTS | ORAC | ||||
| Frutos | Ruehssia tholiformis (Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado | - | 2.72±0.29d | 30.90±2.49c | 98.66±9.32e | 50.73±4.21d |
| Gonolobus naturalistae M.G. Chávez, Pio-León & L.O. Alvarado | 8.52±1.09d,e | 2.48±0.54d | 26.29±1.01d | 94.92±6.32e | 32.01±2.07e | |
| Funastrum heterophyllum (Engelm. ex Torr.) Standl. | 7.05±0.51e | 1.33±0.32d | 31.05±1.18c | 94.54±1.71e | 48.17±4.02d | |
| Funastrum clausum (Jacq.) Schltr. | 19.45±2.15a | 1.42±0.41d | 51.86±1.94b | 284.18±5.95a | 270.76±76.54a | |
| Inflorescencias | Funastrum heterophyllum (Engelm. ex Torr.) Standl. | 9.82±0.2d | 14.82±1.78b | 29.53±1.45c | 206.38±36.84b | 126.02±8.80c |
| Funastrum clausum (Jacq.) Schltr. | 12.37±0.40c | 11.45±0.90c | 36.99±1.86b | 220.77±16.08c | 183.86±0.01b | |
| Funastrum pannosum (Decne.) Schltr. | 15.48±1.46b | 17.89±1.60a | 51.03±0.54a | 262.39±35.27b | 193.52±6.27a | |
| LSD | 1.91 | 1.79 | 2.38 | 11.12 | 9.30 | |
Actividad antioxidante
La mayor actividad antioxidante por los tres métodos se encontró en las inflorescencias de Funastrum pannosum y los frutos de Funastrum clausum, mientras que las menores fueron registradas para los frutos de Gobolobus naturalistae, Funastrum heterophyllum y Ruehssia tholiformis (Cuadro 4). El contenido de fenólicos totales mostró correlación alta con los tres métodos antioxidantes (0.835-0.896), mientras que para el contenido de flavonoides fue moderada (0.500-0.707) (Cuadro 5).
Cuadro 5: Análisis de correlación entre el contenido de fenólicos y flavonoides totales con la actividad antioxidante evaluada por tres métodos en especies comestibles de Asclepiadoideae. Donde: DPPH = 2,2-difenil-1-picrilhidrazil; ABTS = ácido 2,2'-azino-bis(3-etilbenzotiazolina-6-sulfónico); ORAC = capacidad de absorción de radicales de oxígeno, por sus siglas en inglés.
| Fenólicos totales | Flavonoides totales | DPPH | ABTS | ORAC | |
| Fenólicos totales | 1 | ||||
| Flavonoides totales | 0.475 | 1 | |||
| DPPH | 0.835 | 0.500 | 1 | ||
| ABTS | 0.896 | 0.707 | 0.860 | 1 | |
| ORAC | 0.881 | 0.677 | 0.870 | 0.983 | 1 |
Análisis proximal
Los principales componentes en las inflorescencias y frutos de todas las especies evaluadas fueron los carbohidratos (40.41-58.10%), seguido de fibra dietaria (24.15-41.04%) y proteínas (10.74-13.45%) (Cuadro 6). El mayor contenido de proteínas se encontró para las inflorescencias de Funastrum pannosum y el de fibra dietaria para los frutos de Funastrum heterophyllum. Los lípidos fueron los macronutrientes de menor concentración, con valores desde 3.97% (inflorescencias de Funastrum heterophyllum) a 7.19% (frutos de Funastrum heterophyllum).
Cuadro 6: Composición proximal (% base seca) y contenido calórico en especies comestibles de especies de Asclepiadoideae. Los resultados son expresados como media ± DE del porcentaje en base seca (n = 3). Para el análisis de los datos se empleó ANDEVA de una vía, seguido de comparación múltiple de medias (Fischer, P<0.05). Letras superíndices diferentes en una misma columna indican diferencias significativas. Donde: LSD = LSD de Fisher o diferencia mínima significativa, por sus siglas en inglés.
| Especies | Lípidos | Proteínas | Cenizas | Fibra dietaria total | Carbohidratos | Kcal/100 g | |
| Frutos | Ruehssia tholiformis (Juárez-Jaimes & L.O. Alvarado) L.O. Alvarado | 4.71±1.22e | 10.85±0.24a | 7.65±0.37c | 35.66±0.23b | 45.81±0.77b | 269.0 |
| Gonolobus naturalistae M.G. Chávez, Pio-León & L.O. Alvarado | 4.81±0.3f | 11.12±0.23a | 6.81±0.74d | 29.77±0.16c | 52.22±0.66a | 276.7 | |
| Funastrum heterophyllum (Engelm. ex Torr.) Standl. | 7.19±0.18d | 12.11±2.70a,b | 6.85±0.17d | 41.04±0.92a | 40.41±2.66c | 274.8 | |
| Funastrum clausum (Jacq.) Schltr. | 8.30±0.21b | 11.76±0.63a,b | 5.20±0.12e | 24.15±1.84d | 58.10±1.33a | 354.1 | |
| Inflorescencias | Funastrum heterophyllum (Engelm. ex Torr.) Standl. | 3.97±0.01c | 14.31±0.21c | 11.15±0.23a | 32.62±0.91c | 42.40±0.59b | 264.2 |
| Funastrum clausum (Jacq.) Schltr. | 5.43±0.07b | 10.74±1.20a | 9.37±0.13b | 36.78±0.83c | 47.37±3.20b | 281.3 | |
| Funastrum pannosum (Decne.) Schltr. | 4.98±0.04a | 13.45±0.07b,c | 9.82±0.67b | 29.20±5.48c | 45.94±4.66b | 282.4 | |
| >LSD | 0.35 | 2.01 | 0.74 | 3.49 | 4.33 | – |
Discusión
A diferencia de Asclepias curassavica, ninguna de las inflorescencias o frutos de las especies evaluadas mostraron presencia de compuestos potencialmente tóxicos como alcaloides, saponinas o antracénicos (Cuadro 2). Estos resultados concuerdan con los obtenidos en ambos estudios de toxicidad y avalan a estas especies como potencialmente inocuas y aptas para el consumo, mientras que ya existen reportes de la toxicidad de Asclepias curassavica (Rodríguez-Maciel et al., 2019; Alonso-Castro et al., 2021). Este trabajo demostró la presencia de más de un tipo de fitoquímico potencialmente tóxico en el extracto de Asclepias curassavica y la inducción de parálisis en el ensayo de Artemia salina. Las familias de fitoquímicos detectadas en las especies de Funastrum coinciden con la reportadas por Beltrán-Villanueva et al. (2013), quienes tampoco encontraron alcaloides, cumarinas o saponinas, pero sí antracénicos en hojas de Funastrum clausum (reportado como Sarcostemma clausum (Jacq.) Schult.).
Con excepción de los frutos de Funastrum clausum, la concentración de fenólicos totales, flavonoides totales y actividad antioxidante fue mayor en las inflorescencias que en los frutos de las especies evaluadas (Cuadro 4). El contenido de fenólicos totales en las inflorescencias (9.82-15.48 mg EAG/g) estuvo dentro del rango reportado para otras flores o inflorescencias ampliamente consumidas en México, como las de Yucca filifera Chabaud (10-14 mg EAG/g) o Agave salmiana Otto ex Salm-Dyck (12-16 mg EAG/g), pero inferior a las de Diphysa americana (Mill.) M. Sousa (39-59 mg EAG/g) (Marcos-Gómez et al., 2024). La concentración de flavonoides fue considerablemente superior a la de Yucca filifera o Agave salmiana (1.3-4.3 mg EQ/g) y similar al de Diphysa americana (11-24 mg EQ/g). En cuanto a los frutos, excepto el de Ruehssia tholiformis, el contenido de compuestos fenólicos (7.05-19.45 mg EAG/g) fue similar o ligeramente superior al de verduras ampliamente consumidas y con usos culinarios similares como brócoli, zanahoria, chayote, pepino o nopales, cuyos valores oscilan aproximadamente entre 4 y 9 mg/g en base seca (b.s.) (Kaur y Kapor, 2002; Astello-García et al., 2015; Peña-Galván et al., 2017; Díaz-de-Cerio et al., 2019). Por el contrario, el contenido de flavonoides en chayote (~38 mg EQ/g b.s.) fue considerablemente superior al de todos los materiales evaluados en el presente trabajo (Peña-Galván et al., 2017), donde también coincidió que éstos fueran superiores a los fenólicos. Todas estas verduras, incluidas los talayotes, poseen sabores suaves y son poco o nada astringentes o ácidos. Estas son características opuestas a las registradas para frutos con alto contenido en compuestos fenólicos como los de los géneros Rubus L., Vitis L., Vaccinium L. o Fragaria L., cuyos valores en base fresca superan los 100 mg/g (Paredes-López et al., 2010).
Dos de las muestras evaluadas (frutos de Ruehssia tholiformis e inflorescencias de Funastrum heterophyllum) presentaron valores de flavonoides ligeramente superior al de fenólicos totales. Si bien los flavonoides son un tipo de compuesto fenólico y se esperaría que los primeros siempre sean inferiores a los segundos, esto no siempre se cumple debido a la no especificidad de los métodos (Pinedo-Espinosa et al., 2020). El método de Folin-Coicalteu puede ser poco o nada sensible a la presencia de flavonas que carecen de grupos hidroxilo libres, mientras que la reacción con AlCl3 para flavonoides es especialmente sensible a flavonoides de tipo flavonas (Pękal y Pyrzynska, 2014; Pérez et al., 2023). Por lo tanto, una posible explicación es que los compuestos fenólicos mayoritarios en los frutos de Ruehssia tholiformis e inflorescencias de Funastrum heterophyllum sean flavonoides de tipo flavonas con grupos hidroxilos sustituidos o ausentes. Lo anterior también se justifica en parte por los resultados del análisis fitoquímico cualitativo, donde la reacción para flavonoides fue de mayor intensidad relativa que la de fenólicos.
Los tres métodos antioxidantes evaluados mostraron alta correlación entre sí (0.86-0.98) (Cuadro 5), lo que sugiere que los compuestos antioxidantes de los materiales evaluados están actuando principalmente a través de la transferencia de átomos de hidrógeno (Prior et al., 2005). Considerando el método DPPH (Cuadro 4), los valores mostrados por los frutos e inflorescencias de las especies evaluadas (26.29-51.03 µmol ET/g) estuvieron dentro del rango obtenido para flores e inflorescencias comúnmente consumidas en Oaxaca, como Yucca filifera, Agave salmiana, Diphysa americana y Chamaedorea tepejilote Liebm. (14-185 µmol ET/g b.s.) (Marcos-Gómez et al., 2024). Sin embargo, estuvieron muy por debajo si se compara con frutos del género Rubus, cuyos valores superan los 25 µmol ET/g b.f., equivalente a aproximadamente 250 µmol ET/g b.s., considerando un aproximado de 90% de humedad (Paredes-López et al., 2010). No obstante, los valores obtenidos para ORAC (32.01-202.77 µmol ET/g b.s.) y ABTS (94.54-284.18 µmol ET/g b.s.) sí llegaron a ser similares a los reportados para frutos de los géneros Rubus, Vaccinium o Fragaria (ORAC = ~310-440 µmol ET/g b.s.; ABTS = ~120-140 µmol ET/g b.s.) (Paredes-López et al., 2010), principalmente los de las inflorescencias de Funastrum pannosum y frutos de Funastrum clausum.
El contenido de fibra dietaria en los frutos de los talayotes (24 - 41% b.s.) (Cuadro 6) fue superior al de algunas de las verduras mayormente consumidas en México, como brócoli (12.5% b.s.), chayote (16.7% b.s.), calabacita criolla (17.8% b.s.) o pepino (18.75% b.s.), resultando comparable al de los nopales (35% b.s.) (Ledesma-Solano et al., 2010). Por su parte, las inflorescencias mostraron contenidos de fibra superior al de las flores de calabazas (9.8% b.s.) y similares al de las espinacas (33% b.s.). En cuanto a proteínas, los valores encontrados para todas las muestras (10-12% b.s.) fueron inferiores a los del brócoli, calabacita y chayote (23-32% b.s.), similar al del pepino (12.3% b.s.) y superior a los del chayote (8.7% b.s.) (Ledesma-Solano et al., 2010). El porcentaje de lípidos y carbohidratos fue similar al de estos mismos productos, excepto en el caso del contenido de lípidos en los frutos de Funastrum heterophyllum y Funastrum clausum que fue aproximadamente el doble (Ledesma-Solano et al., 2010).
Los principales macronutrientes que aportan las especies evaluadas fueron carbohidratos (40.41-58.10% b.s.) y fibra dietaria (24.15-41.04% b.s.) (Cuadro 6). El consumo de 100 g de producto seco cubriría prácticamente el 100% de la ingesta diaria recomendada de fibra dietaria para hombres (38 g/d) y mujeres (25 g/d) adultos, mientras que si se considera un estimado de 90% de humedad, el aporte por 100 g de producto fresco contribuiría con aproximadamente el 10 y el 15% de los requerimientos de hombres y mujeres, respectivamente (USDA, 2020), por lo que aún se considerarían una buena fuente. Por su parte, el contenido de lípidos y proteínas de estas especies sería insuficiente para cubrir los requerimientos dietarios. Sin embargo, la inclusión de estas especies en la dieta puede aportar cantidades significativas de fibra dietaria y ser bajas en calorías, lo que sería adecuado para tratamientos de reducción de peso y grasa corporal, así como para mejorar el tránsito gastrointestinal. El aporte calórico de las especies evaluadas (~26-33 kcal/100 g de producto fresco) es similar al de verduras ampliamente consumidas en México como brócoli, calabacitas, chayote, pepinos o nopales, cuyos valores oscilan entre 26 y 34 kcal/100 g de producto fresco (Ledesma-Solano et al., 2010).
Conclusiones
Las especies comestibles de la subfamilia Asclepiadoideae evaluadas carecen de fitoquímicos potencialmente tóxicos y fueron inocuas, lo que justifica su consumo por habitantes de las comunidades locales. Comparado con la composición de la mayoría de verduras que comúnmente se consumen en México, el contenido de fibra dietaria de las especies analizadas es superior, pero similar al de los nopales; mientras que el contenido de compuestos fenólicos, actividad antioxidante y macronutrientes resultó similar. La inclusión de estas especies a la dieta local puede aportar beneficios a la salud, principalmente por su alto aporte en fibra dietaria y bajo contenido calórico.