Introducción
En los manglares del pacífico colombiano, la flora de algas asociadas a las raíces de los mangles se conoce comúnmente como el complejo Bostrychietum, que es una agrupación de algas compuestas principalmente por los géneros Bostrychia Montagne (Rhodomelaceae, Ceramiales), Caloglossa (Harvey) G. Martens (Delesseriaceae, Ceramiales), Catenella Greville (Caulacanthaceae, Gigartinales) y la especie Rhizoclonium riparium (Roth) Harvey (Cladophoraceae, Cladophorales) (Gyi y Htun, 2013; Murillo-Muñoz y Peña-Salamanca, 2014; Salgado y Peña-Salamanca, 2016; Peña-Salamanca, 2017). Estas algas no solo contribuyen significativamente a la producción de carbono orgánico y de nitrógeno (Ortega et al., 2020; Regina Hershey et al., 2021; Erlania et al., 2023), sino que también actúan como bioindicadores de contaminación (Rios-Marin et al., 2021). Las raíces del manglar les proporcionan una superficie amplia y húmeda disponible para su colonización por estas algas (Peña-Salamanca, 2017). Sin embargo, el manglar impone retos ambientales importantes a estos organismos debido a las fluctuaciones de humedad, salinidad, luz, temperatura, nutrientes, desecación durante las mareas bajas y acción de las olas (Banerjee et al., 2009; Peña-Salamanca, 2017; Borburema et al., 2020). Además, presentan presiones biológicas como depredación, competencia, parasitismo y alelopatía (Park et al., 2023).
Como respuesta adaptativa a estas condiciones estresantes, las macroalgas de los manglares sintetizan una variedad de compuestos bioactivos que les permiten sobrevivir. Por ejemplo, se ha documentado que las especies del género Bostrychia presentan estrategias fisiológicas para tolerar el cambio climático, como el aumento en la síntesis y acumulación de osmolitos, tales como el dulcitol y sorbitol, en respuesta al incremento de temperatura y estrés salino (Borburema et al., 2022, 2024). Además, estas especies producen carotenoides, clorofilas y aminoácidos similares a micosporinas para resistir el estrés lumínico (Orfanoudaki et al., 2023; Urrea-Victoria et al., 2023). Por otro lado, en Catenella repens (Lightfoot) Batters se han observado variaciones en la concentración de proteínas, lípidos, carbohidratos y astaxantina como adaptación a la variación de las condiciones climáticas en el manglar del delta del Ganges, India (Banerjee et al., 2009).
Además de estas adaptaciones, varios estudios han identificado compuestos bioactivos en macroalgas de manglares con importantes propiedades biológicas. En particular, los extractos de Bostrychia tenella (J.V.Lamouroux) J.Agardh han demostrado propiedades antioxidantes (Martins et al., 2013), antiparasíticas y antifúngicas (de Felício et al., 2010). Mientras que en Bostrychia montagnei Harvey se han extraído galactanos sulfatados con actividad antiviral (Duarte et al., 2001). Por otro lado, los extractos de Caloglossa ogasawaraensis Okamura y Caloglossa beccarii (Zanardini) De Toni han mostrado actividad antioxidante (Chankaew et al., 2016, 2021). Asimismo, en Rhizoclonium riparium se identificaron polisacáridos solubles que presentan propiedades inmunológicas (Hsu et al., 2006). A pesar de estos hallazgos, el potencial biotecnológico de las macroalgas de manglares es poco explorado, lo cual revela una brecha significativa en el conocimiento científico sobre estas especies.
Por otro lado, las algas marinas en general se caracterizan por su alta concentración de minerales esenciales (Lorenzo et al., 2017; Neto et al., 2018; Campos et al., 2022; Čmiková et al., 2022). Llegan a tener aplicaciones tanto en la formulación de suplementos dietéticos para humanos y animales (Wan et al., 2019; Morais et al., 2020; Peñalver et al., 2020; Narvaez-Izquierdo et al., 2024), como en la producción de fertilizantes (Aron Santhosh Kumar et al., 2024). Por ejemplo, la aplicación de Sargassum sp. y Ascophyllum nodosum (L.) Le Jolis mejora la composición mineral del suelo, estimula la germinación, el crecimiento, floración y fructificación de las plantas, además de promover su resistencia a las enfermedades y la tolerancia a la sequía (Shukla et al., 2019; Thompson et al., 2020; Aron Santhosh Kumar et al., 2024).
En el caso de las macroalgas asociadas a los manglares, los estudios sobre su contenido mineral son limitados. No obstante, en especies como Rhizoclonium riparium se ha documentado una notable concentración de minerales, especialmente yodo (Afonso et al., 2018). Se estima que el consumo de 2 g de esta alga seca podría ser suficiente para cubrir las ingestas diarias recomendadas de yodo (Afonso et al., 2018), lo que la convierte en una candidata potencial para el desarrollo de suplementos alimenticios, especialmente en regiones donde la deficiencia de yodo representa un problema de salud pública (FAO, 2018).
A pesar de la importancia de las algas asociadas a los manglares, las investigaciones dedicadas a la exploración de su composición nutricional y química son limitadas, especialmente en especies del pacífico colombiano (por ejemplo, Lenis et al., 2007; Urrea-Victoria et al., 2023). Debido a lo anterior, el objetivo de este estudio fue determinar la composición nutricional y fitoquímica de tres especies silvestres asociadas a las raíces de Rhizophora mangle L. en la Bahía de Buenaventura: Bostrychia calliptera (Montagne) Montagne, Catenella impudica (Montagne) J. Agardh y Rhizoclonium riparium.
Muestreo
Se recolectaron talos de Bostrychia calliptera (Fig. 1A), Rhizoclonium riparium (Fig. 1B) y Catenella impudica (Fig. 1C) en el manglar ubicado en la desembocadura del río Dagua (3°51'41.1''N, 77°03'59.5''W), frente a la Bahía de Buenaventura, departamento del Valle del Cauca, Colombia, en junio 2023. Las algas se recolectaron de las raíces de Rhizophora mangle (Fig. 1 D). Para la especie Bostrychia calliptera, se tomaron muestras según su distribución de crecimiento vertical a lo largo de la raíz del manglar, clasificándolas en zona media y zona alta, siendo esta última el nivel correspondiente a la máxima inundación mareal (Peña-Salamanca, 2017).
Posteriormente las muestras fueron almacenadas en bolsas de cierre herméticas marca Ziploc®, refrigeradas a 4 °C y transportadas al Laboratorio de Fisiología Vegetal del Departamento de Biología de la Universidad del Valle (Colombia) para su procesamiento. La identificación de las especies se basó en las descripciones taxonómicas de Salgado y Peña-Salamanca (2016). Los especímenes se depositaron en el herbario CUVC de la Universidad del Valle, con los siguientes números de registro: Bostrychia calliptera (85538 y 85539), Catenella impudica (85540) y Rhizoclonium riparium (85541).

Figura 1: Fotografías del ecosistema de manglar de Buenaventura, Colombia. A. Bostrychia calliptera (Montagne) Montagne; B. Rhizoclonium riparium (Roth) Harvey; C. Catenella impudica (Montagne) J. Agardh; D. Rhizophora mangle L. Fotografías: Angie Cristina Zuñiga Lara.
Análisis nutricional
Se realizó un análisis de composición nutricional de las algas colectadas, que incluyó la determinación del porcentaje de cenizas, fibra cruda, proteína cruda y minerales (fósforo, potasio, calcio, magnesio, azufre, boro, cobre, hierro, manganeso, zinc y sodio), utilizando los métodos de la Asociación de Colaboración Analítica Oficial (AOAC, 2006). El contenido de nitrógeno orgánico se calculó con el método de Kjendahl, donde el porcentaje de proteína fue divido por 6.25 (Nova et al., 2023).
Extracción
Las algas se secaron en horno (Heraeus modelo SUT6060, Hanau, Alemania) a 60 °C durante 48 horas, luego se maceraron con mortero y se sometieron a extracción con acetona (99.5%). Se añadieron 10 ml de acetona por cada 2 g de muestra y se dejaron en reposo durante 24 horas. Posteriormente, se trató la muestra en un ultra sonicador (Branson Ultrasonics modelo 5510R-MT, Brookfield, EUA) durante 20 minutos y se filtró para recoger el solvente con los extractos. El solvente fue evaporado utilizando un evaporador rotativo (IKA modelo RV 10 digital, Staufen, Alemania), ajustado a 60 °C, 80 RPM y una presión de 556 mbar.
Tamizaje fitoquímico
Los extractos obtenidos fueron evaluados para determinar la presencia de metabolitos secundarios, mediante las siguientes técnicas: la prueba de Dragendorff para la detección de alcaloides (Mubashrah et al., 2020), la prueba de cloruro férrico para la detección de taninos (Mubashrah et al., 2020), la prueba de Liebermann-Burchard para la identificación de esteroles y terpenos (Silva et al., 2020), la prueba de Kedde para la determinación de glucósidos cardiotónicos (García-Granados et al., 2019), la prueba de Shinoda para la detección de flavonoides (Abdu et al., 2019), y la prueba de Salkowski para la identificación de saponinas (Mubashrah et al., 2020).
Análisis GC-MS
Los análisis de cromatografía de gases acoplado a espectroscopia de masas (GC-MS) se llevaron a cabo en el laboratorio del Grupo de Investigación en Productos Naturales y Alimentos (GIPNA) de la Universidad del Valle, Colombia. Se utilizaron 2 mg de cada extracto, a los cuales se les agregó 1 ml de metanol (99.9% grado HPCL) y se sometieron a sonicación (Branson Ultrasonics modelo 5510R-MT, Brookfield, EUA) durante 10 minutos. De la solución resultante de extracto con metanol, se tomaron 2 μl para los análisis. Se utilizó un cromatógrafo de gases acoplado a un espectrómetro de masas (Shimadzu Scientific Instruments, modelo QP2010 Ultra, Kioto, Japón), equipado con una columna capilar Rxi-1HT GC (30 m × 0.32 mm, 0.10 μm) (Restek Corporation, Bellefont, EUA). El programa de temperatura del horno de columna (Shimadzu Scientific Instruments, modelo QP2010 Ultra, Kioto, Japón) comenzó con 40 °C durante 2 minutos, con un aumento de 10 °C/min hasta alcanzar 360 °C manteniendo esta temperatura durante 10 minutos. Las temperaturas del IonSource y de la Interfaz fueron de 240 y 200 °C, respectivamente. La temperatura del módulo de entrada de las muestras se incrementó a una tasa de 10 °C min-1 hasta 350 °C y se mantuvo durante 20 minutos. El rango de masas analizado fue de 35 a 600 m/z, con una velocidad de escaneo de 1250 unidades por segundo. Los datos se adquirieron desde los 5 hasta los 44 minutos. Los compuestos orgánicos volátiles presentes en las muestras fueron anotados mediante la comparación de los espectros de masas con la biblioteca espectral NIST WEBBOOK (Linstrom y Mallard, 2001).
Resultados
Análisis nutricional
La composición proximal de las especies Bostrychia calliptera, Catenella impudica y Rhizoclonium riparium se presenta en la figura 2. El porcentaje de cenizas varió entre 16.9 y 24.9%. La fibra cruda mostró variabilidad, con valores entre 2.52 y 10.6% para las dos algas rojas, mientras que Rhizoclonium riparium presentó una mayor cantidad de fibra cruda (30.2%). El contenido de proteínas fue similar, oscilando entre 14.6 y 25%. Por su parte, el contenido de nitrógeno fue mayor en Bostrychia calliptera (4.01%), seguido de Rhizoclonium riparium (3.15%) y Catenella impudica (2.38%).
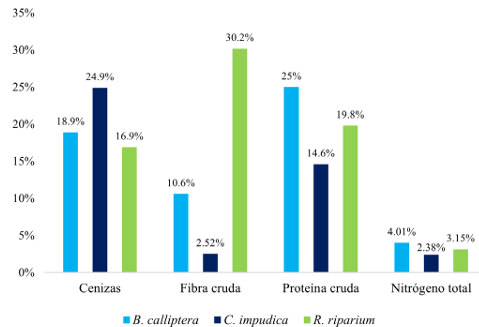
Figura 2: Porcentaje de cenizas, fibra cruda, proteína cruda y nitrógeno total en Bostrychia calliptera (Montagne) Montagne (azul claro), Catenella impudica (Montagne) J. Agardh (azul oscuro) y Rhizoclonium riparium (Roth) Harvey (verde).
En relación con la composición mineral de las algas, los macrominerales como el fósforo (800-1270 mg kg-1), potasio (30,100-35,000 mg kg-1) y calcio (50,106,860 mg kg-1) presentaron una menor variabilidad en sus rangos en comparación con el magnesio (7960-16,600 mg kg-1), azufre (29,400-70,600 mg kg-1) y sodio (7330-46,700 mg kg-1). Por otro lado, los micronutrientes mostraron una mayor variabilidad en sus concentraciones, incluyendo al hierro (1880-9180 mg kg-1), manganeso (204-4730 mg kg-1), cobre (20.7-73.1 mg kg-1), zinc (26.4-50.2 mg kg-1) y boro (51.2-143 mg kg-1) (Cuadro 1).
Cuadro 1: Concentración de minerales (mg kg-1) en tres especies de macroalgas asociadas a manglares: Bostrychia calliptera (Montagne) Montagne, Catenella impudica (Montagne) J. Agardh y Rhizoclonium riparium (Roth) Harvey. Los minerales evaluados incluyen potasio (K), azufre (S), hierro (Fe), sodio (Na), magnesio (Mg), calcio (Ca), manganeso (Mn), fósforo (P), cobre (Cu), boro (B) y zinc (Zn).
| Minerales | B. calliptera (Montagne) Montagne(mg kg-1) | C. impudica (Montagne) J. Agardh(mg kg-1) | R. riparium (Roth) Harvey(mg kg-1) |
| Potasio (K) | 30,100 | 31,200 | 35,000 |
| Azufre (S) | 29,400 | 70,600 | 30,000 |
| Hierro (Fe) | 9180 | 1880 | 6320 |
| Sodio (Na) | 7450 | 46,700 | 7330 |
| Magnesio (Mg) | 7960 | 16,600 | 9600 |
| Calcio (Ca) | 5510 | 6860 | 5010 |
| Manganeso (Mn) | 4730 | 204 | 755 |
| Fósforo (P) | 1210 | 800 | 1270 |
| Cobre (Cu) | 73.1 | 20.7 | 22.8 |
| Boro (B) | 77.7 | 51.2 | 143 |
| Zinc (Zn) | 50.2 | 26.4 | 28 |
Tamizaje fitoquímico y análisis GC-MS
De acuerdo con el tamizaje fitoquímico, en los extractos algales de todas las especies se detectó la presencia de alcaloides, esteroles, terpenos, glicósidos cardiotónicos y saponinas. Por otro lado, mediante los análisis de cromatografía de gases acoplado a espectroscopia de masas (GC-MS), se identificaron 14 compuestos volátiles en los extractos de Bostrychia calliptera de zona media (ocho compuestos) y zona alta (8), Catenella impudica (2) y Rhizoclonium riparium (7) (Cuadro 2).
Cuadro 2: Compuestos identificados en Bostrychia calliptera (Montagne) Montagne (zona media (M) y alta (A)), Catenella impudica (Montagne) J. Agardh y Rhizoclonium riparium (Roth) Harvey mediante cromatografía de gases acoplada a espectrometría de masas (GC-MS). Se incluye la clase de compuesto, masa molecular (g mol-1), tiempo de retención y el porcentaje de área relativo para cada especie (% área).
| % Área | ||||||||
| Clase | Compuesto | Masa molecular (g mol-1) | Tiempo de retención (min) | B. calliptera (Montagne) Montagne (M) | B. calliptera (Montagne) Montagne(A) | C. impudica (Montagne) J. Agardh | R. riparium (Roth) Harvey | |
| Eicosano | 282.5 | 19.5 | 13.1 | 6.6 | 64.1 | 45.2 | ||
| 2-metiloctacosano | 408.8 | 21.3 | 4.8 | 35.2 | 35.9 | 26.6 | ||
| Octadecano | 254.5 | 17.6 | 8.1 | 5.4 | ||||
| Alcano | 9-metilnonadecano | 282.5 | 19 | 1.4 | ||||
| 2-Metileicosano | 296.6 | 19.3 | 2.8 | 3.6 | ||||
| 3-Metileicosano | 310.6 | 21.1 | 4.3 | 3.4 | ||||
| 2-4-dimetileicosano | 310.6 | 20.9 | 5.5 | |||||
| Tetracosano | 338.7 | 23 | 10.2 | |||||
| Éster bis(2-etilhexílico) del ácido 1,3-bencenodicarboxílico | 390.6 | 25.4 | 13.4 | 41.5 | ||||
| Éster | Ácido octadecanoico, éster etílico | 312.5 | 21.2 | 3.3 | ||||
| Ácido hexadecanoico, éster etílico | 284.5 | 19.3 | 36.2 | 6 | ||||
| Ácido hexadecanoico, éster metílico | 270.5 | 18.7 | 2.2 | |||||
| Octocrileno | 361.5 | 24.7 | 10.5 | |||||
| Esteroide | Colesterol | 386.7 | 27.9 | 10.6 | ||||
Se encontró que en Bostrychia calliptera de la zona media, el compuesto más relativamente abundante fue el ácido hexadecanoico, éster etílico (36.2%), seguido del éster bis (2-etilhexílico) del ácido 1,3-bencenodicarboxílico (13.4%), eicosano (13.1%), colesterol (10.6%), octocrileno (10.5%) y el octadecano (8.1%). Por otro lado, en la muestra de zona alta, el éster bis (2-etilhexílico) del ácido 1,3-bencenodicarboxílico (41.5%) fue el más representativo, seguido del 2-metiloctacosano (35.2%), eicosano (6.6%), y el ácido hexadecanoico, éster etílico (6%).
Por su parte, en Catenella impudica se identificaron dos compuestos, el eicosano (64.1%) y el 2-metiloctacosano (35.9%). Finalmente, en Rhizoclonium riparium el eicosano (45.2%), 2-metiloctacosano (26.6%), tetracosano (10.2%), 2,4-dimetileicosano (5.5%) y el octadecano (5.4%) fueron los compuestos principales. En el cuadro 2 se detallan las composiciones químicas de las especies estudiadas, incluyendo la clase de compuesto, masa molecular (g mol-1), tiempo de retención y su área (%). Los cromatogramas se muestran en la figura 3.
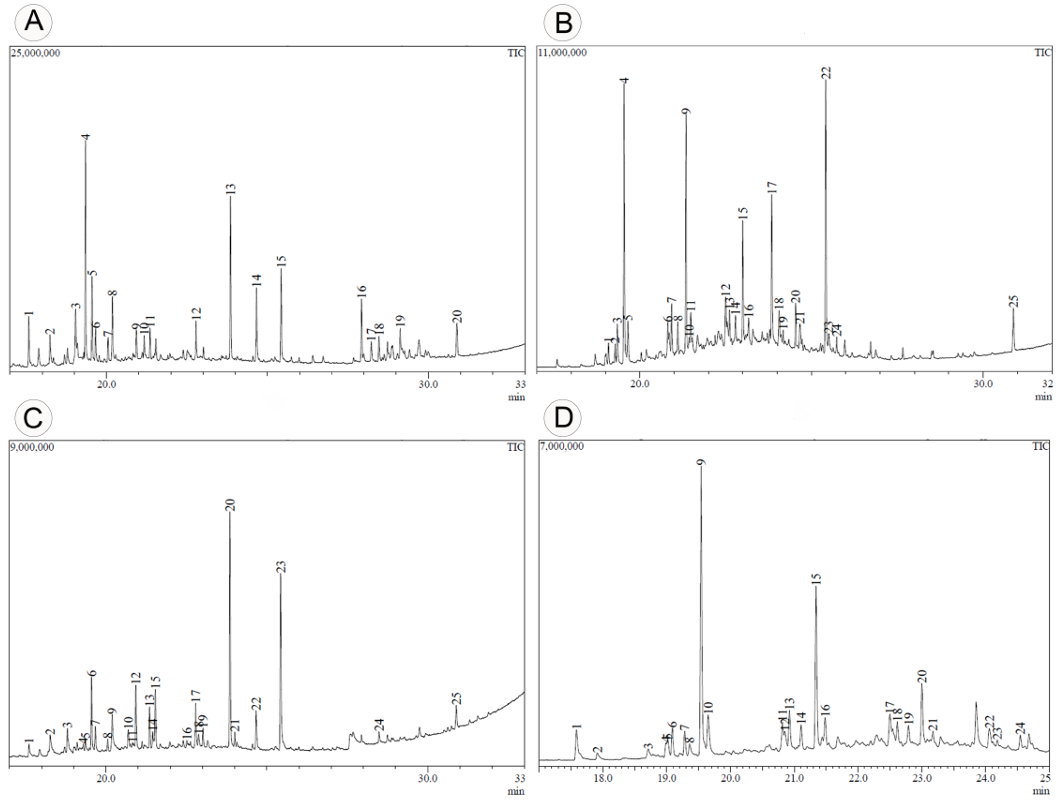
Figura 3: Cromatogramas de los compuestos orgánicos obtenidos por GC-MS. A. Bostrychia calliptera (Montagne) Montagne zona media; B. Bostrychia calliptera zona alta (Montagne) Montagne; C. Catenella impudica (Montagne) J. Agardh; D. Rhizoclonium riparium (Roth) Harvey. Cada gráfico presenta picos en diferentes tiempos de retención (eje x), representando diferentes compuestos presentes en una muestra.
En cuanto a la clase de compuestos identificados, se encontró que, en Bostrychia calliptera de la zona media, los ésteres representaron el porcentaje más alto (63.4%), seguido de los alcanos (26%) y esteroides (10.6%) (Fig. 4). En comparación, en la muestra de la zona alta, los ésteres (50.3%) y alcanos (49.7%) estuvieron en cantidades similares. Por su parte, en Catenella impudica y Rhizoclonium riparium solo se identificaron alcanos (Fig. 4).
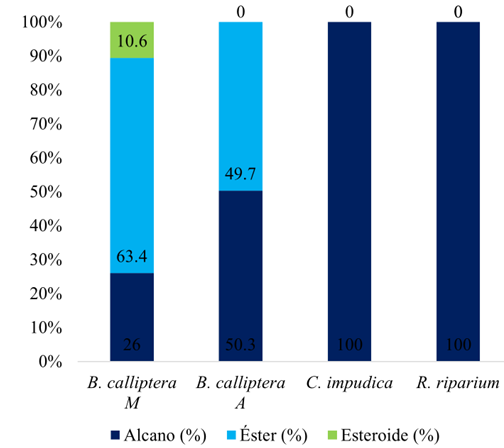
Figura 4: Composición porcentual de compuestos químicos identificados en Bostrychia calliptera (Montagne) Montagne de zona media (M) y alta (A); Catenella impudica (Montagne) J. Agardh y Rhizoclonium riparium (Roth) Harvey. Los compuestos se clasifican en alcanos (azul oscuro), ésteres (azul claro) y esteroides (verde).
Discusión
Análisis nutricional
Los bosques de manglar son uno de los ecosistemas más relevantes en Colombia, debido a los múltiples servicios ecosistémicos que proporcionan (Palacios y Cantera, 2017; Rojas et al., 2019). Sin embargo, la información sobre los organismos asociados a estos ecosistemas sigue siendo limitada. Un reciente estudio sobre metabolitos secundarios de hongos endofíticos del manglar de Buenaventura en el pacífico colombiano destacó el interés por explorar la biota de estos entornos (Vallejo et al., 2024). No obstante, aún son escasas las investigaciones dedicadas a la composición química de las algas marinas de estos ecosistemas (Lenis et al., 2007).
En ese contexto, los resultados de este estudio no solo confirman la importancia de las algas marinas como fuente de compuestos bioactivos, sino que también aportan nueva información sobre su composición química, especialmente en las especies Bostrychia calliptera, Catenella impudica y Rhizoclonium riparium. La variabilidad observada en su composición proximal es consistente con lo reportado en la literatura, la cual indica que el contenido de proteínas, carbohidratos, fibra, lípidos y minerales puede diferir ampliamente entre las especies de algas marinas (Peñalver et al., 2020; Campos et al., 2022; Narvaez-Izquierdo et al., 2024). Estas diferencias en la composición se atribuyen a factores ambientales o genéticos que influyen en la química de las especies (Peñalver et al., 2020; Ilyas et al., 2023).
En particular, la especie Rhizoclonium riparium destacó por su elevado contenido de fibra, alcanzando 30.2% de su peso seco, superando tanto a las demás especies analizadas (Fig. 2), como al promedio estimado para las algas verdes en general (6.58%) (Narvaez-Izquierdo et al., 2024). Además, su porcentaje de cenizas fue de 16.9%, un valor consistente con reportes previos de 15.9% (Chao et al., 1999). En cuanto al contenido de proteínas (19.8%), fue mayor al promedio estimado para las algas verdes en general (15.54%) (Narvaez-Izquierdo et al., 2024). Investigaciones anteriores sugieren que, debido a su morfología fibrilar y su elevado contenido de celulosa, Rhizoclonium riparium tiene un potencial uso como sustituto parcial de la fibra de madera utilizada en la producción de papel (Chao et al., 1999; 2000).
Por su parte, Bostrychia calliptera presentó los valores más altos de proteínas (25%) y nitrógeno orgánico (4.01%) (Fig. 2). Los porcentajes de proteína son comparables con los estimados para Gracilaria gracilis (Stackhouse) Steentoft, L.M.Irvine y Farnham y Porphyra sp., dos algas de relevancia en la industria alimentaria, en las que se han registrado contenidos proteicos de hasta 28.8 y 35%, respectivamente (Campos et al., 2022; Nova et al., 2023). En cuanto al nitrógeno orgánico, en algas rojas se estima un valor promedio de 4.09% (Narvaez-Izquierdo et al., 2024).
Adicionalmente, Catenella impudica presentó un contenido proteico de 14.6%, el cual es congruente con lo reportado por Banerjee et al. (2009). Estos autores encontraron que en Catenella repens el contenido de proteínas varía entre 2.78 y 16.03%, dependiendo de las fluctuaciones estacionales en los bosques de manglar de la India. En dicho estudio, se observó una correlación positiva entre el contenido de proteínas y la concentración de nitrato disuelto, mientras que factores como la temperatura del agua y la salinidad mostraron una correlación negativa. Por otro lado, en Catenella impudica se observó el mayor contenido de cenizas (24.9%), seguido por Bostrychia calliptera (18.9%) (Fig. 2), similar a lo reportado para algas rojas (Peñalver et al., 2020).
En general, se observaron concentraciones altas y variables de diferentes minerales en las tres especies analizadas. Los elementos más representativos por su concentración fueron el potasio, azufre, hierro, sodio, magnesio, calcio, fósforo y manganeso. El cobre, boro y zinc también estuvieron presentes en todas las especies, pero en cantidades menores (Cuadro 1). Estos minerales son esenciales para el funcionamiento de los procesos metabólicos y se presentan en bajas concentraciones (Wan et al., 2019).
Se incluye el cuadro 3 con el fin de comparar la composición elemental de Bostrychia calliptera, Catenella impudica y Rhizoclonium riparium con los valores reportados en otras especies de importancia económica. Este cuadro incluye la composición elemental reportada para Gracilaria spp. (Wen et al., 2006; Neto et al., 2018; Torres et al., 2019; Nova et al., 2023), Sargassum naozhouense C.K.Tseng y Lu Baoren (Peng et al., 2013) y Ascophyllum spp. (MacArtain et al., 2007; Lorenzo et al., 2017). Sargassum spp. y Ascophyllum spp. se utilizan principalmente como biofertilizantes y se ha encontrado que su aplicación en el suelo mejora la composición orgánica y estimula el crecimiento de las plantas (Shukla et al., 2019; Thompson et al., 2020).
Cuadro 3: Concentración de minerales (mg kg-1) de tres macroalgas asociadas a manglares (Bostrychia calliptera (Montagne) Montagne, Catenella impudica (Montagne) J. Agardh y Rhizoclonium riparium (Roth) Harvey) en comparación con especies de algas marinas de importancia comercial (Gracilaria spp., Sargassum naozhouense C.K.Tseng & Lu Baoren y Ascophyllum spp.). Los minerales evaluados incluyen potasio (K), azufre (S), hierro (Fe), sodio (Na), magnesio (Mg), calcio (Ca), manganeso (Mn), fósforo (P), cobre (Cu), boro (B) y zinc (Zn). Información tomada de Wen et al., 2006; MacArtain et al., 2007; Peng et al., 2013; Lorenzo et al., 2017; Neto et al., 2018; Torres et al., 2019; Thompson et al., 2020; Nova et al., 2023.
| Minerales | B. calliptera (Montagne) Montagne (mg kg-1) | C. impudica (Montagne) J. Agardh (mg kg-1) | R. riparium (Roth) Harvey (mg kg-1) | Gracilaria spp. (mg kg-1) | S. naozhouense C.K.Tseng & Lu Baoren (mg kg-1) | Ascophyllum spp. (mg kg-1) |
| Potasio (K) | 30,100 | 31,200 | 35,000 | 89,200-92,431 | 41,700 | 7650-37,813.5 |
| Azufre (S) | 29,400 | 70,600 | 30,000 | 260.9-1650 | 1470 | 133.4-149 |
| Hierro (Fe) | 9180 | 1880 | 6320 | 26,130-159,470 | 32,500 | 11,738-45,757.1 |
| Sodio (Na) | 7450 | 46,700 | 7330 | 4020 | - | 2250-8678.2 |
| Magnesio (Mg) | 7960 | 16,600 | 9600 | 1391.3-6240 | 669.8 | 5750-9847.3 |
| Calcio (Ca) | 5510 | 6860 | 5010 | 67-240 | 58.4 | 19.6 |
| Manganeso (Mn) | 4730 | 204 | 755 | 1899.7-4150 | 1200 | - |
| Fósforo (P) | 1210 | 800 | 1270 | 26-32.7 | 3.6 | 80 |
| Cobre (Cu) | 73.1 | 20.7 | 22.8 | 32.7-64.2 | 90.8 | - |
| Boro (B) | 77.7 | 51.2 | 143 | - | - | - |
| Zinc (Zn) | 50.2 | 26.4 | 28 | - | - | - |
Se ha encontrado que las macroalgas tienen una notable capacidad para acumular concentraciones elevadas de macroelementos directamente de su entorno, como el sodio, magnesio, fósforo, calcio y potasio, así como oligoelementos, incluyendo el manganeso, hierro, cobalto, níquel, zinc y selenio (Wan et al., 2019). La tasa de acumulación de estos minerales puede variar dependiendo de la tasa de crecimiento, la edad del alga y factores abióticos como la temperatura, la disponibilidad de nutrientes, la intensidad de la luz y la salinidad (Banerjee et al., 2009; Wan et al., 2019).
En cuanto a la composición elemental de las especies analizadas, no se han publicado estudios previos que detallen los perfiles de Bostrychia calliptera y Catenella impudica. No obstante, para Rhizoclonium riparium, Afonso et al. (2018) encontraron niveles de yodo (281.5 mg kg-1), estroncio (141.4 mg kg-1), manganeso (135.1 mg kg-1), cobre (68.9 mg kg-1) y zinc (59.3 mg kg-1). En contraste, nuestras mediciones revelaron una mayor concentración de manganeso (755 mg kg-1), mientras que las concentraciones de cobre (22.8 mg kg-1) y zinc (28 mg kg-1) fueron similares a las reportadas en dicho estudio (Cuadro 1). Además, las concentraciones de estos elementos en Rhizoclonium riparium fueron superiores a las registradas en Gracilaria spp., Sargassum naozhouense y Ascophyllum spp., excepto en el caso del zinc, cuya concentración en estas especies comerciales no ha sido reportada, al igual que la del boro (Cuadro 3).
En el caso de Catenella impudica, se detectaron los valores más altos de azufre (70,600 mg kg-1), sodio (46,700 mg kg-1) y magnesio (16,600 mg kg-1) (Cuadro 1). Los ecosistemas marinos, como los manglares, suelen ser reservorios de azufre (Sherman et al., 1998). Este elemento se encuentra presente en las algas en forma de compuestos como proteínas, péptidos, aminoácidos, polisacáridos, etc. (Giordano et al., 2008). El contenido de azufre en Catenella impudica es notablemente superior al registrado en Sargassum naozhouense (1470 mg kg-1) y Gracilaria spp. (260.9-1650 mg kg-1). Asimismo, el contenido de sodio en Catenella impudica fue mayor al de Ascophyllum spp. (2250-8678.2 mg kg-1) y al de Gracilaria spp. (4020 mg kg-1).
Finalmente, los niveles de potasio (30,100-35,000 mg kg-1), en particular, fueron comparables a los reportadas en Sargassum naozhouense (41,700 mg kg-1) y Ascophyllum spp. (37,813.5 mg kg-1) (Cuadro 3). Este elemento, junto con el nitrógeno y fósforo son fundamentales para el crecimiento de las plantas (Shukla et al., 2019). La presencia de potasio en niveles relativamente altos, junto con las concentraciones de calcio (5010-6860 mg kg-1), fósforo (800-1270 mg kg-1) y nitrógeno (2.38-4.01%), sugiere un potencial uso de Bostrychia calliptera, Catenella impudica y Rhizoclonium riparium como biofertilizantes. No obstante, dado que la biomasa de las poblaciones naturales de estas especies en las áreas de estudio es relativamente baja y se encuentran asociadas específicamente a las raíces del mangle (Peña-Salamanca, 2008), su aprovechamiento sostenible requerirá el desarrollo de sistemas de cultivo que incrementen su biomasa a nivel comercial.
Compuestos identificados por GC-MS
El método de cromatografía de gases acoplado a espectroscopia de masas (GC-MS) ha sido ampliamente utilizado para el análisis de metabolitos volátiles de algas marinas (Park et al., 2023). Por ejemplo, de Felício et al. (2010) aplicaron esta técnica en el análisis de Bostrychia tenella, identificando alcanos, ésteres y derivados del colesterol, lo cual es coherente con el tipo de compuestos encontrados en Bostrychia calliptera en el presente estudio (Fig. 4). En esta especie, se identificaron compuestos específicos de la zona media y alta del manglar, aunque con variaciones en sus concentraciones. Entre ellos, se encontraron ésteres lipídicos como el éster bis(2-etilhexílico) del ácido 1,3-bencenodicarboxílico (13.4 y 41.5% en la zona media y alta, respectivamente) y el ácido hexadecanoico, éster etílico (36.2 y 6% en la zona media y alta, respectivamente) (Cuadro 2). Este tipo de lípidos se forman por esterificación de ácidos grasos con alcoholes (Guschina y Harwood, 2009). Además, se detectaron compuestos exclusivos de cada zona. En la zona media, se encontraron el octocrileno (10.5%), el ácido octadecanoico, éster etílico (3.3%) y el colesterol (10.6%). El colesterol es el principal esterol en algas rojas, aunque su concentración varía entre las distintas familias (Kumari et al.,2013; Hannan et al., 2020). Por su parte, en la zona alta, se identificaron el ácido hexadecanoico, éster metílico (2.2%) y el 9-metilnonadecano (1.4%).
Una posible explicación para las diferencias en las concentraciones de los ésteres lipídicos observadas en Bostrychia calliptera entre la zona media y alta, es que, en organismos fotosintéticos, la composición de lípidos puede verse afectada por factores ambientales como la intensidad de luz, temperatura, pH, salinidad y disponibilidad de nutrientes (Guschina y Harwood, 2009). Por ejemplo, De Jong et al. (2021) examinaron el impacto combinado de la intensidad lumínica y la disponibilidad de nutrientes en el contenido de esteroles de Saccharina latissima (L.) C.E.Lane, C.Mayes, Druehl y G.W. Saunders, observando un aumento en las concentraciones con el incremento de irradiancia bajo condiciones de baja disponibilidad de nutrientes. Por su parte, Toth et al. (2020) analizaron la composición de ácidos grasos en Ulva fenestrata Postels y Ruprecht bajo diferentes niveles de irradiancia, temperatura, nutrientes y pCO₂, encontrando una mayor concentración de estos compuestos bajo condiciones de baja irradiancia y alta concentración de nutrientes, especialmente de nitrato.
La información reportada sobre los cambios en las concentraciones de metabolitos en macroalgas asociadas a manglares es escasa y se ha enfocado en la respuesta adaptativa de estas al estrés salinidad, temperatura, luz y pH (Borburema et al., 2022, 2024; Orfanoudaki et al., 2020; Urrea-Victoria et al., 2023). El estudio de Peña-Salamanca (2017) reportó variaciones en las tasas fotosintéticas y metabólicas de las especies del complejo Bostrychetium según su distribución vertical en los manglares. De igual forma, Banerjee et al. (2009) encontraron que la concentración de astaxantina en Catenella repens está influenciada por las condiciones del manglar donde habita.
Por otro lado, cabe mencionar que el ácido hexadecanoico, éster metílico (2.2%) y el 9-metilnonadecano (1.4%), identificados en Bostrychia calliptera son conocidos por sus actividades biológicas. El ácido hexadecanoico, éster metílico ha demostrado propiedades antiinflamatorias, antiartríticas y anticancerígenas (Abdel-Jaleel et al., 2021; Breeta et al., 2021; Olowofolahan et al., 2021), mientras que el 9-metil nonadecano ha mostrado actividad antibacteriana (Mehboudi et al., 2023). Diferentes actividades biológicas han sido estudiadas previamente en especies de Bostrychia, entre ellas la actividad antioxidante, antiparasítica, antifúngica y antiviral (Duarte et al., 2001; de Felício et al., 2010; Martins et al., 2013). En Rhizoclonium riparium, se detectaron dos compuestos únicos de sus extractos, el 2,4-dimetileicosano (5.5%) y el tetracosano (10.2%). Este último ha sido evaluado previamente por su actividad citotóxica significativa contra células de cáncer de colon (Uddin et al., 2012). Los polisacáridos solubles extraídos de Rhizoclonium riparium también han demostrado propiedades inmunológicas, como la estimulación de la expresión del gen IL-1 en macrófagos murinos (Hsu et al., 2006).
Los compuestos que estuvieron presentes en todas las especies fueron el eicosano, 2-metiloctacosano, 2-metileicosano y el 3-metileicosano. De estos, el eicosano fue el más abundante en Catenella impudica y Rhizoclonium riparium. Este compuesto ha sido evaluado previamente por su actividad antioxidante (Beema Shafreen et al., 2022; Balachandran et al., 2023; Bhat et al., 2024). Finalmente, todos los extractos algales contenían alcaloides, esteroles, terpenos, glicósidos cardiotónicos y saponinas. Estos compuestos son conocidos por su propiedades y beneficios para la salud humana y sus aplicaciones industriales en los sectores farmacéutico, alimentario, cosmético y agrícola (Park et al., 2023).
El presente estudio constituye un avance significativo en la caracterización fitoquímica de las algas marinas asociadas a los manglares, pero presenta algunas limitaciones. Una de ellas es que la técnica de GC-MS, aunque adecuada para la identificación de compuestos volátiles y térmicamente estables, no permite la detección completa de todos los metabolitos presentes en estas especies (Park et al., 2023). En este sentido, futuras investigaciones podrían enfocarse en la aplicación de técnicas como la cromatografía líquida acoplada a espectrometría de masas (LC-MS), que ofrece un espectro más amplio para la identificación de compuestos bioactivos (Park et al., 2023).
Conclusiones
Este estudio amplía el conocimiento sobre la composición nutricional y fitoquímica de las algas asociadas a los ecosistemas de manglar, destacando el valor de especies como Bostrychia calliptera, Catenella impudica y Rhizoclonium riparium como fuentes potenciales de compuestos bioactivos. Los resultados confirman que estas especies presentan una composición nutricional variada, con diferencias en proteínas, fibras, minerales y metabolitos secundarios. En particular, Rhizoclonium riparium destacó por su alto contenido de fibra y minerales esenciales, mientras que Bostrychia calliptera presentó una elevada concentración de proteínas y compuestos bioactivos de interés farmacéutico y nutricional. Además, el contenido mineral de estas algas, especialmente de potasio, azufre, fosforo y nitrógeno, sugiere su posible utilización como biofertilizantes. Los análisis mediante GC-MS revelaron la presencia de diversos compuestos bioactivos en todas las especies, incluyendo ácidos grasos, esteroles y alcanos, con potenciales aplicaciones en las industrias farmacéutica y cosmética. Sin embargo, se reconocen las limitaciones de este estudio, ya que la técnica de GC-MS no permite una identificación exhaustiva de todos los metabolitos presentes. Por ello, se recomienda incorporar técnicas más avanzadas en investigaciones futuras, para lograr un análisis más detallado de los compuestos bioactivos.
Financiamiento
Este estudio fue financiado por el proyecto “Investigación para el aprovechamiento sostenible de la biodiversidad de los microorganismos asociados al ecosistema de manglar y la exploración de su potencial biotecnológico en la costa pacífica del Valle del Cauca” con el código BPIN 2021000100488, de la convocatoria del Ministerio de Ciencias, Tecnologías e Innovación de Colombia 18-1-PLAN BIENAL SGR 2021-2022.
















