Introducción
Phytophthora capsici es el agente causal de la marchitez del chile, considerada una de las enfermedades más destructivas del género Capsicum (Majid et al., 2017). El oomiceto puede afectar al cultivo en cualquier etapa de desarrollo, causando pérdida de turgencia en la planta, clorosis, pudrición radical, caída de hojas y muerte, es decir, con nivel de afectación entre el 10 y 100 % (Jiménez-Camargo et al., 2018).
Entre los métodos alternativos para controlar la marchitez del chile se encuentra el uso de portainjertos resistentes (Zhao et al., 2011). El Serrano Criollo de Morelos 334 (CM- 334) destaca por su alta resistencia a P. capsici (Castro-Rocha et al, 2016; Naegele y Hausbeck, 2020); no obstante, el uso de portainjertos podría afectar positiva o negativamente la producción y calidad del fruto (Greathouse et al., 2021), lo que podría derivarse de la alteración en la arquitectura radical lo que reduce el transporte de agua y nutrientes (Ropokis et al., 2019). No obstante, la aplicación exógena de auxinas y T. harzianum puede promover y acelerar la formación de raíces adventicias en plantas injertadas (Saini y Deepanshu, 2023; Larios et al., 2019).
En chile manzano Pérez-Grajales et al. (2021) comprobaron la compatibilidad entre híbridos de este tipo de chile y el portainjerto CM-334, en condiciones de hidroponía. Sin embargo, es necesario comprobar el comportamiento de plantas injertadas en presencia de P. capsici. Por lo tanto, en el presente estudio se evaluó el comportamiento de la biomasa radical del CM-334 como portainjerto de híbridos comerciales de chile manzano ‘Maruca’, ‘Jhos’ y ‘Dali’ en condiciones de hidroponia; y también la resistencia a P. capsici de plantas injertadas del híbrido ‘Dali’ sobre el CM-334 vs las no injertadas en condiciones de suelo infestado con el oomiceto. Además, se evaluó el efecto en rendimiento de fruto del híbrido ‘Dali’ y biomasa radical del CM-334 en respuesta a las aplicaciones de auxinas y T. harzianum.
Materiales y Métodos
Sitio experimental. La investigación se desarrolló condiciones de invernadero de la Universidad Autónoma Chapingo, Estado de México (19° 29’ 22.2” LN y 98° 52’ 24.7” LO, a una altitud de 2250 m). Los niveles promedio de temperatura, humedad relativa, radiación fotosintéticamente activa y CO2 fueron 18.7 °C, 68.9 %, 525 µmoles de fotones m2 s-1 y 450 ppm.
Biomasa radical de híbridos injertados y no injertados cultivados en hidroponía. En marzo de 2017 se establecieron en macetas e hidroponía en invernadero, plantas de chile manzano de los híbridos ‘Maruca’, ‘Jhos’ y ‘Dali’ (con registros SNICS 1351, 1298 y 1299), injertadas en el CM-334 y plantas no injertadas. El experimento se estableció en un diseño completamente al azar con seis tratamientos (tres híbridos injertados y tres sin injertar) y siete repeticiones cada uno, la unidad experimental y de muestreo fue una planta. Las plantas fueron cultivadas durante dos años, en condiciones de invernadero e hidroponía con un sistema de conducción de plantas a dos tallos en ‘V’ de acuerdo a la propuesta de Pérez y Castro (2008). En mayo de 2019 se realizó la determinación de la biomasa radical de los seis tratamientos, para ello, se extrajeron las raíces de las macetas y se lavaron con abundante agua, después se pesaron en una balanza granataria con sensibilidad de 0.1 g (Ohaus®, México) y se midió el volumen de raíz por desplazamiento de agua en un recipiente de 10 L graduado en mL. También se obtuvo el peso seco (g) por medio de una estufa de secado (Teknolab®, México) a 70 °C durante 72 horas.
A los datos de peso fresco, volumen y peso seco de raíz de los tratamientos se les aplicó análisis de varianza (ANOVA) y prueba de comparación múltiple de medias de Tukey (P≤0.05), y “t” de Student (P≤0.05) para dos poblaciones (plantas injertadas y no injertadas). En todos los procedimientos se empleó el programa de análisis estadístico SAS 9.1.3.
Resistencia a P. capsici, rendimiento de fruto y biomasa radical de plantas injertadas y no injertadas cultivadas en suelo
Caracterización morfológica de P. capsici aislado de suelo. Para determinar la presencia de P. capsici a utilizar en el experimento, se desarrolló una técnica de recuperación de esporangios de P. capsici a partir de una muestra compuesta de suelo tipo limoso (1 kg), que fue obtenida a 30 cm de profundidad, en cinco diferentes puntos de una hectárea de superficie de terreno del lote X4 del campo experimental de Fitotecnia de la UACh, donde se tiene antecedentes de la presencia del oomiceto, por la sintomatología presentada en cultivos anteriores.
Para el aislamiento de P. capsici a partir de suelo, se empleó la metodología propuesta por Aristizábal y Torres (2015) con algunas modificaciones. Para ello, se pesaron 10 g de suelo con siete repeticiones y se mezclaron con 90 mL de agua destilada estéril, de esta solución se tomó una alícuota de 1 mL y se aforó con agua destilada estéril a 10 mL, esto se repitió dos veces. Después se colocó una gota de la última dilución en una caja Petri estéril y se llenó con medio PDA líquido a temperatura ambiente, se dejó reposar durante siete días para el crecimiento del micelio. Para purificar el hongo se realizó punta de hifa, y para la formación de esporangios fue transferido a cajas Petri que contenía jugo V8- agar como medio de cultivo, en donde permaneció seis días a 26 °C y en completa oscuridad. Para la liberación de oosporas, el oomiceto fue sometido a estrés térmico, es decir, dos horas a 5 °C y una hora a 26 °C (Ortíz y Camargo, 2005). Posteriormente, se realizaron preparaciones en porta y cubreobjetos y con la ayuda del programa Motic Plus
3.0 se medió largo y ancho de papilas de 50 esporangios del oomiceto. La identificación morfológica se realizó con el apoyo de claves tabulares propuestas por Martin et al. (2012).
Material vegetal. El material vegetal empleado como injerto fue el híbrido ‘Dali’, seleccionado por su alto rendimiento y calidad de fruto, con registro SNICS 1299. El portainjerto fue el cultivar de chile Serrano Criollo de Morelos 334 (CM-334), resistente universal a P. capsici. La técnica de injerto se hizo de acuerdo con lo descrito por Pérez- Grajales et al. (2021).
Manejo de plantas injertadas y no injertadas. Setenta días después de realizar el injerto, las plantas del híbrido ‘Dali’ injertadas, así como las no injertadas fueron trasplantadas en bolsas de plástico de 50 x 50 cm (calibre 600) rellenas de suelo previamente analizado. Las plantas se cultivaron y manejaron en invernadero, como propone Pérez y Castro (2008). Tres meses después del trasplante se inició con aplicaciones de Ácido 4-indol-3 butírico (AIB) y T. harzianum (Th) dirigidas a la raíz de plantas injertadas y no injertadas (durante cuatro meses), de acuerdo a los tratamientos siguientes: 1) 0.18 g de Th por planta cada 20 días; 2) 0.18 g de Th combinado con 1200 ppm de AIB cada 20 días; 3) AIB a 1600 ppm cada15 días; 4) AIB a 1600 ppm cada 30 días; 5) AIB a 1600 ppm cada 45 días; 6) AIB a 1200 ppm cada15 días; 7) AIB a 1200
ppm cada 30 días; 8) AIB a 1200 ppm cada 45 días; 9) AIB 800 ppm a los 15 días; 10)
AIB 800 ppm cada 30 días; 11) AIB 800 ppm cada 45 días; y 12) el testigo sin aplicación de auxinas y T. harzianum. El diseño experimental fue completamente al azar con cuatro repeticiones, la unidad experimental y de muestreo fue una planta.
Evaluación de incidencia y ABCPE. La evaluación de incidencia se realizó mediante la identificación de plantas con síntomas típicos del oomiceto respecto al número total de plantas del experimento, mientras que para el nivel de daño se propuso una escala arbitraria de acuerdo al porcentaje de marchitamiento del follaje (Figura 1). Con los datos obtenidos del nivel de daño, se calculó el porcentaje de severidad del ataque de P. capsici y se calculó el área bajo la curva del progreso de la enfermedad (ABCPE). Para ello se empleó el método de integración trapezoidal propuesto por Shaner y Finney (1977). Los datos fueron sometidos a un análisis de varianza (ANOVA) y una prueba de comparación múltiple de medias LSD de Fisher (P≤0.05), y se utilizó el paquete estadístico SAS 9.1.3.

Figura 1 Escala arbitraria para evaluación de incidencia y severidad causada por P. capsici en plantas del híbrido ‘Dali’ de Chile manzano (Capsicum pubescens) cultivado en macetas con suelo infestado de P. capsici. Chapingo, México de 2020 a 2021.
Caracterización morfológica de P. capsici aislado de tejido vegetal. Una vez observada la sintomatología de marchitez en plantas no injertadas del híbrido ‘Dali’, se realizaron tres muestreos al azar (en diferentes tiempos) de cinco plantas enfermas para aislar el agente causal. Para ello se tomaron cinco porciones de 1 cm de tallo y raíz y fueron desinfectadas con hipoclorito de sodio al 3 % y sembradas en medio PDA (Soto- Plancarte et al., 2017); a los siete días se inició el proceso de purificación mediante punta de hifa. Una vez purificado, se realizaron preparaciones que fueron observadas en microscopio compuesto y con la ayuda del programa Motic Plus 3.0 se midió el largo y ancho de papilas de 50 esporangios. La identificación morfológica se realizó con el apoyo de claves tabulares de Martin et al. (2012).
Rendimiento. Se realizaron siete cosechas de fruto (una cada 15 días) y se contabilizó el número y peso de los frutos totales por planta; y el rendimiento por hectárea se calculó al considerar una densidad de 0.694 plantas/m2 por el peso de fruto por planta.
Biomasa radical. La determinación de biomasa de raíces se llevó a cabo a los 14 meses después del trasplante, una vez concluida la evaluación de rendimiento de fruto. Las raíces fueron lavadas con abundante agua hasta eliminar la mayor cantidad de suelo. Posteriormente, a cada una de tres plantas, se les midió la longitud de raíz con una cinta métrica graduada en mm y se pesó en una balanza granataria con sensibilidad de 0.1 g (Ohaus®, México). El volumen de raíz se calculó por desplazamiento de agua en un recipiente de 10 L graduado en mL (Gamboa-Angulo et al., 2020); y el peso seco (g) por medio de una estufa de secado (Teknolab®, USA) a 70 °C durante 72 horas.
Análisis estadístico. Se realizó análisis de varianza (ANOVA) y comparación múltiple de medias con la prueba de Tukey (P≤0.05), y “t” de Student (P≤0.05) para dos poblaciones (plantas injertadas y no injertadas). En todos los procedimientos se utilizó el programa de análisis estadístico SAS 9.1.3.
Resultados y Discusión
Biomasa radical de híbridos injertados y no injertados cultivados en hidroponía. La biomasa radical de los híbridos sin injertar en promedio fue de 52, 70 y 50 % superiores en volumen, peso fresco y seco de raíz respecto a los híbridos injertados en CM-334 (Cuadro 1 y Figura 2). El comportamiento de menor biomasa radical de las plantas injertadas se explica porque el portainjerto CM-334 es una planta de porte pequeño, de ciclo anual y pertenece a C. annuum; en contraste, el injerto (híbridos de chile manzano) es de porte alto, de ciclo perenne y es C. pubescens. Para favorecer la formación de raíces en el portainjerto CM-334 que favorezcan la absorción de nutrimentos se sugiere la aplicación exógena de auxinas y Trichoderma spp. Al respecto, López-Elías et al. (2005) mencionan incrementos de hasta 42 % en volumen de raíz, 35 % de peso fresco y 4 % en peso seco con aplicaciones de ácido indolbutírico (AIB) en pimiento y para chile habanero. Así mismo, Larios et al. (2019), indican incrementos de 41.57 y 55 % de longitud y volumen de raíz, respectivamente, con el uso de Trichoderma spp.
Cuadro 1 Volumen, peso fresco y peso seco de raíces de plantas de chile manzano de los híbridos ‘Maruca’, ‘Jhos’ y ‘Dali’ injertadas en CM-334 vs plantas no injertadas cultivadas en Chapingo, México. Ciclo 2017-2019.
| Tratamiento | Volumen (mL) | Peso fresco (g) | Peso seco (g) |
|---|---|---|---|
| ‘Maruca’ | 512.86 a* | 506.50 a* | 133.714 a* |
| ‘Maruca’ injertado | 267.14 b | 145.37 b | 67.586 b |
| ‘Jhos’ | 468.57 a* | 513.57 a* | 140.214 a* |
| ‘Jhos’ injertado | 197.14 b | 164.81 b | 70.186 b |
| ‘Dali’ | 515.71 a* | 511.69 a* | 134.243 a* |
| ‘Dali’ injertado | 204.29 b | 148.70 b | 67.429 b |
| Coeficiente de variación | 13.91 | 12.82 | 13.11 |
Medias con letras iguales no son estadísticamente diferencias (Tukey, 0.05). *Significativo de acuerdo con la prueba de “t” de Student (P≤0.05).
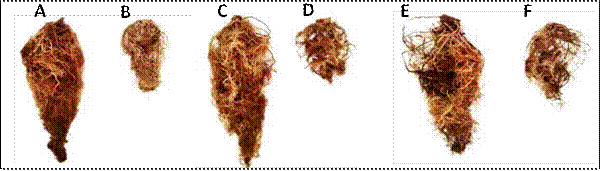
Figura 2 Raíz del híbrido de chile manzano sin injertar vs injertado en CM-334 cultivados en hidroponía e invernadero en Chapingo, México de 2017 a 2019. A) Maruca, B) Maruca injertado, C) Jhos, D) Jhos injertado, E) ‘Dali’, F) ‘Dali’ injertado.
Resistencia a P. capsici, rendimiento de fruto y biomasa radical de plantas injertadas y no injertadas
Caracterización morfológica de P. capsici aislado de suelo. El aislado obtenido del suelo infestado mostró crecimiento micelial cenocítico blanco algodonoso con 15 esporangios por mL (alícuota). Los esporangios presentaron 28.24 a 49.61 µm de largo,
27.29 a 37.41 µm de ancho, y de 4.8 a 6.5 µm ancho de papila (Figura 3). Las características morfológicas observadas del oomiceto concuerdan con las descritas por Díaz-Nájera et al. (2015) para P. capsici en cucurbitáceas y Silva-Rojas et al. (2009) para
C. annuum. Por lo que se confirma que el suelo utilizado en el experimento estaba infestado de manera natural con P. capsici.

Figura 3 Esporangio bipapilado y micelio liso; B) Esporangio unipapilado con zoosporas de P. capsici obtenido de suelo infestado en Chapingo, México.
Incidencia y ABCPE. En las plantas no injertadas, la incidencia de P. capsici fue del 70
% e inició a los 100 días después del trasplante (ddt). Mientras que en plantas injertadas no se observó incidencia de la enfermedad. Lo que confirma el alto nivel de resistencia del portainjerto Serrano Criollo de Morelos 334 (CM-334) a P. capsici (Lamour et al., 2012). De tal manera que el uso de plantas injertadas de chile manzano sobre el CM-334 es una alternativa viable de producción en suelos infestados con este patógeno.
La sintomatología de las plantas infestadas inició con pérdida de turgencia del área foliar, seguido por lesiones color marrón en tejidos de hojas (Figura 1), cuello del tallo y oscurecimiento del sistema radical. Estos síntomas son típicos de la marchitez del chile ocasionada por P. capsici, y concuerdan con los reportados por Callaghan et al. (2016) y Moreira-Morrillo et al. (2022) para el género Capsicum. La severidad de los síntomas en las plantas afectadas se fue incrementando hasta alcanzar la marchitez total de la parte aérea y necrosis del sistema radical, a esto se consideró como 100 % de daño. La muerte de las plantas se presentó en promedio a los 14 días después de iniciados los síntomas de marchitez y concuerdan con los resultados mencionados por Barchenger et al. (2018) para plantas adultas de Capsicum.
Con el área bajo la curva del progreso de la enfermedad (ABCPE) se corroboró que todos los tratamientos con plantas injertadas no presentaron la enfermedad en ninguna etapa fenológica de estudio. De la comparación múltiple de medias LSD de Fisher, se encontraron diferencias significativas entre tratamientos con aplicaciones de auxinas y T. harzianum (Figura 4). Las plantas del híbrido ‘Dali’ con 1200 ppm de AIB cada 15 días presentaron la mayor severidad de la enfermedad; en contraste, las aplicaciones que incluyeron T. harzianum no mostraron diferencias significativas en el ABCPE respecto a los tratamientos con plantas injertadas, a pesar de que la incidencia de la enfermedad fue del 50 %. Al respecto, Gallegos-Morales et al. (2022) mencionaron que con el uso de T. harzianum se incrementó en 30 % el rendimiento de chile serrano variedad Tampiqueño, y la incidencia por P. capsici disminuyó 71 %. Romero-Arenas et al. (2017) indican una incidencia de la enfermedad del 60 al 70 % al inocular P. capsici en plantas de jitomate previamente tratadas con T. harzianum, esto se atribuyó a la relación antagónica entre los microorganismos involucrados. Ita et al. (2021) señalan que T. harzianum tiene mayor velocidad de crecimiento que P. capsici, por lo que inhibe su desarrollo, considerándose como agente de biocontrol (Mousumi et al. 2018). También, La Spada et al. (2020) afirman que Trichoderma puede inducir respuestas de defensa en raíces cuando los fitopatógenos penetran su región rizodérmica, aumentando la actividad de las enzimas peroxidasa y quitinasa así como la deposición de calosa en sus paredes celulares.
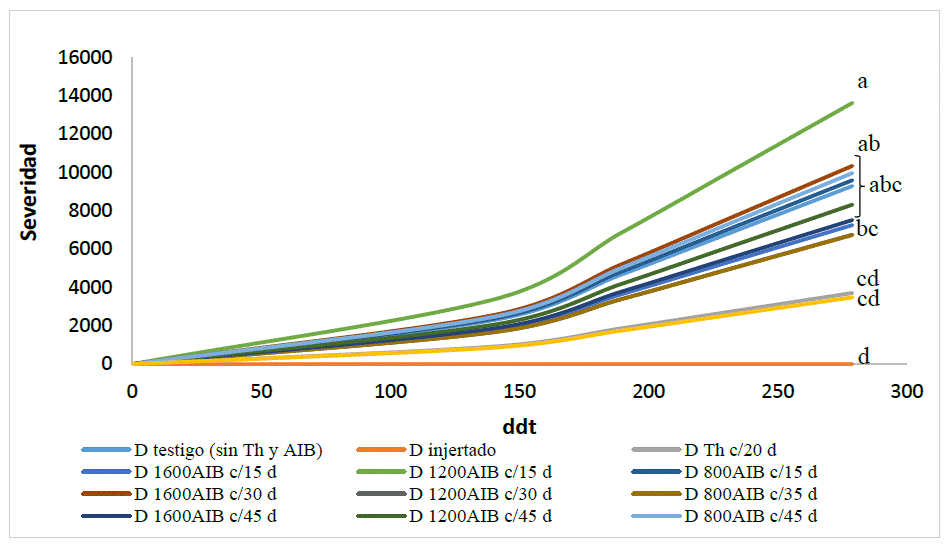
Figura 4 Área bajo la curva del progreso de P. capsici en chile manzano en plantas cultivadas en Chapingo, México, de 2020 a 2021. ddt: días después del trasplante. D: Híbrido ‘Dali’ sin injertar, d: días (frecuencia de aplicación). zLetras iguales indican que no existe diferencias estadísticamente significativas (LSD de Fisher P≤0.05).
Caracterización morfológica de P. capsici aislado de tejido vegetal. El aislado de plantas con síntomas de marchitez presentó crecimiento micelial cenocítico blanco algodonoso con esporangios de 24.01 a 44.45 µm de largo y 17.4 a 35.17 µm de ancho, y bipapilas de 3.3 a 6.8 µm de ancho (Figura 5). Las características morfológicas observadas son típicas de P. capsici y concuerdan con las descritas por Callaghan et al. (2016) y Moreira-Morillo et al. (2022) para C. annuum, por lo que se confirmó la presencia de este oomiceto en las plantas de ‘Dali’ (C. pubescens) cultivadas en suelo infestado de manera natural con P. capsici.

Figura 5 Caracterización morfológica de P. capsici en plantas enfermas. A) crecimiento algodonoso, B y C) esporangios bipapilados de P. capsici en chile manzano en Chapingo, México.
Rendimiento. Los tratamientos con mayor número de frutos fueron ‘Dali’ sin injertar con aplicaciones de 800 ppm de AIB cada 15 días y ‘Dali’ injertado con aplicaciones de auxinas combinado con T. harzianum con un promedio de 86 y 88 frutos por planta (Cuadro 2). En contraste, el tratamiento testigo (híbrido ‘Dali’ sin injertar), sin aplicaciones de auxinas y sin Trichoderma, tuvo el menor número de frutos con 70. No obstante, los tratamientos con aplicaciones de auxinas que tuvieron los menores valores y fueron ‘Dali’ a 1200 ppm y ‘Dali’ sin injertar a 800 ppm cada 45 días, ambas con 66 frutos (Cuadro 2). Por lo tanto, no se observó una tendencia clara en el comportamiento del número de frutos por las aplicaciones de auxinas y T. harzianum, es decir, mayor número de frutos por efecto de estos tratamientos.
Cuadro 2 Medias de número y peso de frutos por planta y rendimiento por hectárea de chile manzano de plantas injertadas sobre CM-334 vs no injertadas, con y sin aplicación de AIB y T. harzianum cultivadas en Chapingo, México. Ciclo 2020 y 2021.
| Tratamientos | Frutos totales por planta | Peso total de frutos por planta (kg) | Rendimiento (t ha-1) |
|---|---|---|---|
| D testigo sin Th y AIB | 69.66 hz * | 6.00 jkns | 41.64 jkns |
| Di testigo sin Th y AIB | 74.66 g | 5.99 jk | 41.55 jk |
| D Th+AIB 1200 ppm cada 20 días | 66.66 ij* | 6.32 efg* | 43.88 efg* |
| Di Th+AIB 1200 ppm cada 20 días | 87.66 a | 6.85 abc | 46.91 abc |
| D Th 1200 ppm cada 20 días | 69.66 h* | 6.19 ef* | 42.98 g* |
| Di Th 1200 ppm cada 20 días | 77.66 e | 6.85 a | 47.54 a |
| D AIB 1600 ppm cada 15 días | 83.33 bc* | 6.82 ab* | 47.35 ab* |
| Di AIB 1600 ppm cada 15 días | 70.33 h | 6.66 c | 46.20 c |
| D AIB 1200 ppm cada 15 días | 76.66 ef * | 6.69 bcns | 46.43 bc* |
| Di AIB 1200 ppm cada 15 días | 74.66 g | 6.46 de | 44.81 de |
| D AIB 800 ppm cada 15 días | 86.00 a* | 6.49 d* | 45.02 d* |
| Di AIB 800 ppm cada 15 días | 81.66 cd | 6.40 def | 44.39 def |
| D AIB 1600 ppm cada 30 días | 80.33 d* | 6.29 fgh* | 43.68 fgh* |
| Di AIB 1600 ppm cada 30 días | 74.33 g | 6.17 hi | 42.82 hi |
| D AIB 1200 ppm cada 30 días | 67.66 i* | 6.49 d* | 45.02 d* |
| Di AIB 1200 ppm cada 30 días | 74.66 g | 6.32 efg | 43.86 efg |
| D AIB 800 ppm cada 30 días | 67.66 i* | 6.85 a* | 47.54 a* |
| Di AIB 800 ppm cada 30 días | 83.66 b | 6.67 c | 46.29 c |
| D AIB 1600 ppm cada 45 días | 74.66 g NS | 6.09 ij* | 42.26 ij* |
| Di AIB 1600 ppm cada 45 días | 73.66 g | 5.91 kl | 41.04 kl |
| D AIB 1200 ppm cada 45 días | 75.33 fg* | 5.97 jkl* | 41.43 jkl* |
| Di AIB 1200 ppm cada 45 días | 65.66j | 5.82 l | 40.41 l |
| D AIB 800 ppm cada 45 días | 65.66 j * | 6.19 ghi* | 41.70 jk* |
| Di AIB 800 ppm cada 45 días | 67.66 i | 5.8 kl | 40.81 kl |
| Coeficiente de variación | 2.80 | 3.74 | 3.74 |
D: híbrido ‘Dali’ sin injertar, Di: híbrido ‘Dali’ injertado sobre el portainjerto CM-334, Th: T. harzianum, AIB: Ácido 4-indol- 3 butírico, zLetras iguales indican que no existe diferencias estadísticamente significativas (Tukey, 0.05), *Significativo y ns: No significativo de acuerdo con la prueba de “t” de Student (P≤0.05).
En contraste, en peso de fruto por planta, al extrapolarse como rendimiento por hectárea, se encontraron dos tratamientos, con mayor rendimiento de fruto: ‘Dali’ injertado con aplicaciones de T. harzianum cada 20 días y ‘Dali’ sin injertar a 800 ppm de AIB cada 30 días ambos con 47.54 t ha-1; seguido de ‘Dali’ sin injertar con aplicaciones de auxinas a 1600 ppm cada 15 días y ‘Dali’ injertado sobre CM-334 con aplicaciones de
T. harzianum y auxinas a 1200 ppm cada 20 días con 47.3 y 46.9 t ha-1, respectivamente (Cuadro 2). En tanto, que los testigos sin aplicación de auxinas y T. harzianum (‘Dali’ no injertado e injertado) presentaron rendimientos más bajos con 41.6 y 41. 5 t ha-1, respectivamente. Estos resultados son similares a los tratamientos con aplicaciones de auxinas cada 45 días, lo que indica que las aplicaciones exógenas de auxinas dirigida a raíz cada 45 días no tiene efectos sobre el peso de fruto, pero sí con aplicaciones más frecuentes, es decir, cada 15 y 30 días (Cuadro 2). El incremento del rendimiento de fruto con el uso de auxinas puede atribuirse a que son hormonas vegetales encargadas de regular varios aspectos del crecimiento, desarrollo de las plantas, tejidos y órganos, al inducir la división, crecimiento y diferenciación celular (Jordán y Casaretto, 2006). Al respecto, Salas et al. (2009) señalan incrementos en el rendimiento de fruto en pimiento con el uso de auxinas en el sistema de riego. No obstante, también para pimiento, Pérez- Jiménez et al. (2015) no encontraron diferencias significativas entre plantas con aplicaciones de ácido indol-3-acético (AIA) y el testigo sin aplicación. Por otra parte, en relación al uso de T. harzianum, Kumari et al. (2019) mencionan mayor número de frutos por planta en pimiento morrón e incluso Khan et al. (2017) indican un incremento de hasta 300 %. Estos resultados positivos al usar Trichoderma se relacionan con la producción de fitohormonas de este ascoomiceto que disminuyen el pH del suelo y promueven la disponibilidad de fosfatos y otros minerales necesarios para el metabolismo de las plantas (Sharma y Gothalwal, 2017).
Al comparar el efecto del portainjerto CM-334 en plantas de chile manzano, el 75 % de las 12 comparaciones “t” de Student (Cuadro 2) se encontró una disminución del rendimiento de tan solo 2 % y en ningún caso se presentó incidencia de P. capsici. En tanto que, en plantas no injertadas, el 73 % de ellas, murieron entre los 100 a 290 días después del trasplante. Esto indica que el injerto CM-334 es una alternativa de viable y sustentable disminuir la incidencia de P. capsici en chile manzano. Ninguna de las plantas injertadas mostró síntomas de marchitez y el rendimiento es similar en plantas no injertadas en el primer ciclo de producción, con la ventaja de que las plantas injertadas continuaron produciendo durante más ciclos (al menos 4 años), dado que es de comportamiento perenne (Pérez y Castro, 2008). De forma parcial, los encontraron García-Rodríguez et al. (2010) al mencionar que, en chile ancho rebelde, las plantas injertadas sobre el CM-334 no presentaron síntomas relacionado con P. capsici; no obstante, el vigor de las plantas y rendimiento fue significativamente menor. Leal- Fernández et al. (2013) mencionan que el portainjerto CM-334 disminuyó significativamente el rendimiento en el cultivar de pimiento dulce Triple Star, lo cual puede estar influenciado por factores como la absorción de nutrientes, sistema radical, o una mayor producción de hormonas endógenas. La disminución de rendimiento en plantas injertadas, Zhao et al. (2011) lo atribuyen al riego, fertilización, el tipo de combinaciones de portainjerto y el tiempo de cosecha. En el presente estudio, las plantas injertadas, iniciaron la producción de frutos comerciales tres semanas después de los híbridos sin injertar.
También Pintado-López et al. (2017) mencionan que el cultivar Camino Real de Harris Moran es altamente susceptible a P. capsici pero al injertarse en CM-334, la planta es capaz de producir frutos sin afectar su rendimiento. Pérez Grajales et al. (2021) concluyen que no tuvieron diferencias significativas en rendimiento de fruto entre híbridos de chile manzano (Maruca, Jhos y ‘Dali’) sin injertar e injertados en el portainjerto CM-334 y cultivados en condiciones de invernadero-hidroponia.
Por otra parte, se encontró que con la aplicación T. harzianum cada 20 días, combinado con auxinas a 1200 ppm incrementa el rendimiento en 8 % en plantas injertadas en relación a las no injertadas (Cuadro 2). Por lo tanto, estos resultados sugieren que el uso de plantas injertadas de chile manzano en CM-334 es una alternativa viable en el manejo comercial del cultivo ya que se puede producir sin daño por P. capsici y a la vez obtener un buen rendimiento de fruto ayudado con aplicaciones de T. harzianum combinado con vs y auxinas.
Biomasa radical de plantas injertadas y no injertadas con aplicaciones de auxinas y
T. harzianum. Debido a la incidencia y severidad de P. capsici en follaje y raíces, no se evaluaron todos los tratamientos de plantas de ‘Dali’ sin injertar, se evaluaron 6 de 24 tratamientos debido a síntomas de pudrición del tallo, el cuello, la raíz y el tizón de la corona, hoja y fruta causado por P. capsici que puede generar pérdidas de hasta el 100 % (Jiménez-Camargo et al., 2018. Las aplicaciones de auxinas y T. harzianum en plantas del híbrido ‘Dali’ de chile manzano injertadas y no injertadas, incrementaron la longitud, volumen, peso fresco y seco de la raíz (Cuadro 3). La mayor biomasa radical se presentó en raíces de plantas no injertadas con aplicaciones de T. harzianum solo o combinado con
Cuadro 3 Biomasa de raíces de plantas de chile manzano no injertadas e injertadas sobre el CM-334, con y sin aplicación de AIB y
| Tratamientos | Longitud(cm) | Volumen(mL) | Peso fresco(g) | Peso seco(g) |
|---|---|---|---|---|
| D testigo sin Th y AIB | 53.00 ab* | 933.33 bc* | 1104.0 bcdef* | 550.00 ab* |
| Di testigo sin Th y AIB | 37.33 abc | 283.33 i | 363.0 j | 112.00 d |
| D Th+AIB 1200 ppm cada 20 días | 47.33 abcns | 1366.67 a* | 1604.0 a* | 593.00 a* |
| Di Th+AIB 1200 ppm cada 20 días | 36.00 abc | 708.33 cdef | 812.0 defgh | 154.67 cd |
| D Th 1200 ppm cada 20 días | 54.67 a* | 1266.67 a* | 1420.3 ab* | 587.33 a* |
| Di Th 1200 ppm cada 20 días | 37.00 abc | 666.67 ef | 773.3 efghi | 94.67 d |
| Di AIB 1600 ppm cada 15 días | 34.00 bc | 283.33 i | 349.3 i | 116.67 d |
| Di AIB 1200 ppm cada 15 días | 37.00 abc | 683.33 def | 869.7 cdefg | 180.33 cd |
| Di AIB 800 ppm cada 15 días | 46.33 abc | 625.00 fg | 734.3 fghij | 118.00 d |
| Di AIB 1600 ppm cada 30 días | 31.667 c | 383.33ghi | 448.3 hij | 105.33 d |
| Di AIB 1200 ppm cada 30 días | 36.00 abc | 750.00 bcdef | 867.7 cdefg | 164.33 cd |
| D AIB 800 ppm cada 30 días | 48.00 abc* | 966.67 b* | 1239.0 abc* | 401.67 ab* |
| Di AIB 800 ppm cada 30 días | 32.667 c | 333.33 hi | 411.0 ij | 97.67 d |
| D AIB 1600 ppm cada 45 días | 36.33 abcns | 875.00 bcde* | 1174.7 bcd* | 443.33 ab* |
| Di AIB 1600 ppm cada 45 días | 36.67 abc | 550.00 fgh | 662.0 ghij | 112.33 d |
| D AIB 1200 ppm cada 45 días | 44.00 abcns | 925.00 bcd* | 1130.0 bcde* | 346.67 bc* |
| Di AIB 1200 ppm cada 45 días | 39.00 abc | 616.67 fg | 587.0 ghij | 103.00 d |
| Di AIB 800 ppm cada 45 días | 35.00 bc | 400.00 ghi | 510.7 ghij | 128.00 d |
| Coeficiente de variación | 15.52 | 11.42 | 15.33 | 28.35 |
D: híbrido ‘Dali’ sin injertar, Di: híbrido ‘Dali’ injertado sobre el portainjerto CM-334, Th: T. harzianum, AIB: Ácido 4-indol- 3 butírico, zLetras iguales indican que no existe diferencias estadísticamente significativas (Tukey, 0.05), *Significativo y ns: No significativo de acuerdo con la prueba de “t” de Student (P≤0.05).
AIB a 1200 ppm cada 20 días, con longitud de 47.4 cm, volumen de 1,367 mL, peso fresco de 1,604 g y seco de 593.3 g (Cuadro 3). Este tratamiento también alcanzó los más altos rendimientos de fruto con 47.5 t ha-1 (Cuadro 1). En contraste, la menor biomasa radical correspondió a plantas injertadas sin aplicaciones de auxinas y T. harzianum con valores de 37 cm, 283 mL, 363 g y 112 g, respectivamente, con rendimiento de fruto de
41.5 t ha-1. Lo que demuestra la efectividad de las aplicaciones de auxinas y T. harzianum en plantas injertadas de chile manzano al incrementar la biomasa radical del portainjerto CM-334 que a su vez se reflejó en mayor rendimiento de fruto. El tratamiento ‘Dali’ injertado con aplicaciones de AIB a 1200 ppm combinado con aplicaciones de T. harzianum cada 20 días tuvo 46.91 t ha-1, que representa un incremento del 11 % en relación a las plantas ‘Dali’ injertadas sin aplicaciones con 41.55 t ha-1. Gamboa-Angulo et al. (2020) indican incrementos de volumen de raíz en plantas de chile xcat´ik (C. annuum) tratadas con T. harzianum, aunque no encontraron diferencias significativas entre número de frutos y rendimiento. Larios et al. (2019) publican un incremento de
41.57 y 55 % en longitud y volumen de raíz, respectivamente, en chile habanero al aplicar Trichoderma spp. Estos incrementos se adjudican a que Trichoderma spp. produce auxinas que son capaces de estimular el crecimiento de la planta, en particular en el crecimiento del sistema radical (Contreras-Cornejo et al., 2009). Según Tucci et al. (2011)Trichoderma spp. tiene la capacidad de solubilizar fosfatos, micronutrientes y cationes minerales útiles para el metabolismo de las plantas.
En la comparación entre plantas injertadas y no injertadas (Cuadro 3), se encontró que el 50 % de las seis comparaciones (tratamientos), las plantas no injertadas tuvieron 32 % de mayor longitud de raíz respecto a las injertadas en el portainjerto CM-334. Pero el 100
% de las comparaciones, las raíces de las plantas no injertadas presentaron 50 % de mayor volumen y peso fresco y 76 % más de peso seco. Y coincide con los resultados obtenidos en el primer experimento de este estudio para los tres híbridos injertados (‘Maruca’, ‘Jhos’ y ‘Dali’) en el CM-334 presentados en el Cuadro 1. Esto es, que existe la necesidad de hacer aplicaciones de auxinas y T. harzianum cuando se lleva a cabo el injerto de chile manzano en el portainjerto CM-334, ya que por una parte se alcanza mayor biomasa radical, y esto está relacionado con mayor abasto de agua y nutrimentos, que a su vez se refleja en mayor rendimiento de fruto (Cuadro 1) y por otra, el uso del portainjerto garantiza la resistencia a P. capsici (Figura 4). De tal manera que emplear híbridos (injerto) de chile manzano que se caracterizan por su alto rendimiento y calidad de fruto (Pérez y Castro, 2008) en la producción comercial, es una alternativa viable y sustentable cuando se injertan en el CM-334 (portainjerto) dado que garantiza su resistencia a P. capsici y una mayor biomasa radical con aplicaciones de auxinas y T. harzianum (Cuadro 3).
Conclusiones
La biomasa radical de los híbridos ‘Maruca’, ‘Jhos’ y ‘Dali’ de chile manzano injertados sobre el portainjerto CM-334 presentaron 50, 53 y 75 % menos volumen radical, peso fresco y seco, respectivamente, en relación con los híbridos no injertados.
Las plantas no injertadas presentaron 70 % de incidencia de P. capsici cuando se cultivaron en condiciones de suelo infestado, en contraste, con el uso del portainjerto CM- 334 no se presentó incidencia del ooomiceto. De tal manera que el injerto de híbridos de chile manzano (Capsicum pubescens) en CM-334 (Capsicum annuum), es una alternativa viable y sustentable para los productores de este tipo de chile, ya que la mayoría de ellos cultivan en suelos infestados de manera natural por P. capsici.
El rendimiento de fruto del híbrido ‘Dali’ de chile manzano disminuyó en promedio 2
% cuando se injertaron en el CM-334 e incluso tuvieron 8 % de mayor rendimiento cuando se aplicó T. harzianum solo o combinado con auxinas a 1200 ppm cada 20 días.
Las plantas injertadas del híbrido ‘Dali’ en el CM-334 presentaron 32 % de menor longitud de raíz, 50 % de menor volumen y peso fresco y 76 % de menor peso seco, respecto a las plantas no injertadas. Por lo que se sugiere aplicaciones dirigidas a la raíz de T. harzianum (1.25 kg ha-1) más AIB (1200 ppm) cada 20 días para incrementar biomasa de raíces del portainjerto.















