Introducción
Michoacán aporta 94.6% de la producción nacional de aguacate (P. americana). En los últimos 10 años, se ha registrado un incremento de 70712 ha de superficie sembrada de un total de 183385 (SIAP, 2022), de las cuales 142481 (78 %) están certificadas para exportación. Esta superficie se distribuye aproximadamente en 44 mil huertos y 43 municipios (CESAVEMICH, 2022). De estos, Tancítaro posee la mayor superficie sembrada, seguido de Uruapan, Tacámbaro, Salvador Escalante, Ario de Rosales y Peribán (SIAP, 2022). En 2022, Jalisco inició su programa de exportación y certificación de huertos de aguacate para EUA con 12000 ha (SADER, 2022). Esta expansión productiva genera riesgos por movilización de plantas de vivero con nula o limitada certificación fitosanitaria. Entre los potenciales problemas por movilización se incluyen organismos parasíticos asociados a raíz. A nivel comercial se tiene registro de Phytophthora cinnamomi, Rosellinia necatrix, Verticillium albo- atrum y Armillaria sp. asociados a enfermedades de raíz (Téliz y Mora, 2007). Recientemente, miembros de la familia Nectriaceae (Ascomycota, Hypocreales) también se han reportado asociados a diversos cultivos agrícolas y forestales en países con clima tropical o subtropical (Mora et al., 2018, Parkinson et al., 2016). En Michoacán, prospecciones recientes han evidenciado la implicación de nectriales con síntomas de marchitez, amarillamiento, defoliación apical y muerte de plántulas en vivero y plantas en huertos recién establecidos (Michua C. J. 2022. No publicado). Estos organismos se han reportado en Sudáfrica, Israel, España, Chile, Italia, Australia y Sudamérica en Vitis vinifera, Rubus glaucus, Panax ginseng, Prunus dulcis, P. avium, P. persica, Actinidia deliciosa, Pistaciavera, Olea europaea y Juglans regia (Lawrence et al., 2019; dos Santos et al., 2015; Cedeño et al., 2004).
La caracterización biológica y molecular con fines taxonómicos de estos hongos es compleja por la variabilidad fenotípica y ausencia de genes constitutivos con viabilidad amplia para discriminar a nivel intra- e inter-género (Androsiuk et al., 2022). Por esta razón, algunos autores utilizan análisis filogenético-concatenados con genes/regiones como TEF 1-α, HIS, tubulina e ITS, o se emplea el genoma mitocondrial en adición a la caracterización morfológica y estudios de compatibilidad sexual (Androsiuk et al., 2022; Lawrence et al., 2019; Crous et al., 2004). Esta complejidad se denota, por ejemplo,
con Dactylonectria, en que a nivel cultural se pueden observar diferencias contrastantes entre aislados, ser sexualmente compatibles y ubicarse en clados filogenéticos distintos (Crous et al., 2004). En otros casos los estudios son escasos e inconclusos como en Mariannaea (Lawrence et al., 2019). Un reciente trabajo filogenético con base en 15 genes clasificó a 45 especies Hypocreales en seis clados principales correspondientes a igual número de familias, entre ellas a Nectriaceae. Interesantemente, Ilyonectria destructor, perteneciente a esta familia, se encontró fuertemente emparentado con 10 especies de Fusarium (Androsiuk et al., 2022).
En Australia se han aislado especies de Calonectria, Gliocladiopsis sp. y Neonectria de raíces sintomáticas de árboles jóvenes de P. americana con detrimento productivo o muerte posterior al trasplante. En contraste, en árboles adultos se ha identificado un complejo de especies de Cylindrocarpon, Cylindrocladium e Ilyonectria a partir de raíces secundarias (Dann et al., 2011). En general, la prevalencia de nectriales se ha vinculado con características fisicoquímicas del suelo, principalmente pH, MO, Ca y Fe (Parkinson et al., 2017). Por lo anterior, se planteó la hipótesis de la existencia, independiente o combinado con otros hongos de raíz del aguacate, de un complejo de nectriales con distribución endémica y baja prevalencia en Michoacán promovida por el gradual deterioro de salud del suelo; cambio abrupto de áreas forestales a cultivación de aguacate; y alteración del régimen hídrico. Consecuentemente, el objetivo de este trabajo fue caracterizar biológica y/o molecularmente especies de nectriales y otros hongos asociados a pudrición de raí z de P. americana en huertos comerciales provenientes de condiciones geográficas contrastantes de la franja aguacatera de Michoacán.
Materiales y Métodos
Muestreo de árboles y aislamiento. En 2019 y 2022, 39 huertos de 13 municipios de la franja aguacatera árboles fueron muestreados para diagnóstico etiológico. Se seleccionaron árboles con síntomas de marchitez, amarillamiento, defoliación, y reducción de crecimiento de fruto. La muestra consistió en trozos de raíces secundarias las cuales exhibieron coloraciones rojizas en tejido central pero no en epidermis y necrosis medular con diferente intensidad. Por huerto se tomaron de 2 - 6 muestras compuestas. Adicionalmente, por árbol muestreado se evaluó el daño en dosel con una escala de 5 clases donde 0 = aparentemente sano, 1 = 25 % de dosel sintomático, 2 = 50 %, 3 = 75 % y 4 = árbol muerto. Adicionalmente, se registró fotográficamente cada árbol y raíces muestreadas para generar una escala nominal de severidad específica a nectriales una vez identificados los hongos presentes. Por huerto, se calculó el promedio de daño en dosel para su integración a un análisis geoestadístico regional. Los aislados fungosos se obtuvieron de 10 segmentos (0.5 - 1 cm) de raíz de 1 - 2 cm de diámetro. La desinfestación consistió en inmersión en hipoclorito de sodio al 2 % durante 2 min; enjuague en agua destilada estéril seguida de sumersión en solución de etanol al 70 % durante 1 min y lavado final con agua destilada estéril. Las raíces desinfestadas se sembraron en placas Petri (9 mm) con Extracto de Malta Agar (EMA) (2 %) con adición de estreptomicina (0.250 g L-1). Las placas se incubaron a temperatura ambiente durante siete días con exposiciones a luz ultravioleta a intervalos de 30 min. Todos los aislados fueron purificados mediante cultivos monospóricos en tres medios de cultivo EMA, Papa
Dextrosa Agar (PDA) y Avena Agar (AA). En total, se seleccionaron 30 aislados nectriales mediante criterios culturales, representatividad regional, y tipología agronómica de huertos para caracterización genómica (Cuadro 1). Adicionalmente, aislados de Fusarium, Armillaria y Phytophthora cinnamomi fueron purificados y caracterizados a nivel de género o especie para estudios de potencial asociatividad patogénica (Michua-Cedillo et al., 2024; López-Bautista et al. 2020;). Todo el acervo biológico se mantiene en conservación in vitro en condiciones de laboratorio.
Cuadro 1 Origen de aislados de nectriales asociados a árboles de aguacate seleccionados para extracción de ADN y PCR- amplificación con TEF 1-α y RPB2.
| ID | Huerto | Municipio | Latitud | Longitud | Altitud (msnm) | VariedadX | Severidady | Aisla do | Injerto |
|---|---|---|---|---|---|---|---|---|---|
| Mich 03 | PA | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 09 | SM | Pátzcuaro | 19.27300 | -101.42420 | 2288 | Hass | 2 | Raíz | Criollo |
| Mich 11 | SM | Pátzcuaro. | 19.27302 | -101.42422 | 2288 | Hass | 2 | Raíz | Criollo |
| Mich 12 | SM | Pátzcuaro | 19.27303 | -101.42423 | 2288 | Hass | 3 | Raíz | Criollo |
| Mich 14 | PA | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 15 | SM | Pátzcuaro | 19.27300 | -101.42420 | 2288 | Hass | 3 | Raíz | Criollo |
| Mich 16 | SM | Pátzcuaro | 19.27300 | -101.42420 | 2288 | Hass | 3 | Raíz | Criollo |
| Mich 24 | G | Uruapan | 19.30260 | -102.02530 | 2111 | Hass | 2 | Raíz | Criollo |
| Mich 25 | G | Uruapan | 19.30260 | -102.02530 | 2111 | Hass | 2 | Raíz | Criollo |
| Mich 26 | Q | Tingüindin | 19.68777 | -102.44619 | 1747 | H, M,FM | 2 | Raíz | Criollo |
| Mich 34 | PA 1 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 35 | PA 2 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 36 | PA 3 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 37 | PA 4 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 39 | PA 6 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 40 | PA 7 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 41 | PA 8 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 44 | PA 5 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 45 | G1 | Uruapan | 19.39360 | -102.20520 | 2050 | Hass | 2 | Raíz | Criollo |
| Mich 46 | H18 | Uruapan | 19.27010 | -102.0040 | 1781 | Hass | 2 | Raíz | Criollo |
| Mich 51 | PA 9 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 52 | PA 10 | Ario de R. | 19.16470 | -101.42140 | 1483 | Hass | 2 | Raíz | Criollo |
| Mich 53 | ElC 32 | Salvador E. | 19.19450 | -101.41260 | 2157 | Hass | 2 | Raíz | Criollo |
| Mich 54 | LaC | Uruapan | 19.56342 | -102.34829 | 2045 | Hass | 2 | Raíz | Criollo |
| Mich 55 | LaR | Salvador E. | 19.20210 | -101.41490 | 1379 | Hass | 2 | Raíz | Criollo |
| Mich 57 Mich 59 | LaC LaPP | Uruapan Tancítaro | 19.56344 19.42310 | -102.34829 -102.46702 | 2045 2148 | Hass Hass | 2 2 | Raíz Raíz | Criollo Criollo |
| Mich 64 | Y | Tancítaro | 19.35525 | -102.36393 | 2148 | Hass | 1 | Raíz | Criollo |
| Mich 66 | ElT12 | Tancítaro | 19.42399 | -102.40619 | 2145 | Hass | 2 | Raíz | Criollo |
| Mich 67 | ElZ | Charapan | 19.64823 | -102.25045 | 2829 | Hass | 2 | Raíz | Criollo |
| Mich 68 | ElB | Tancítaro | 19.42309 | -102.46702 | 1711 | Hass | 2 | Raíz | Criollo |
| Mich 69 | AF | Peribán | 19.32260 | -102.24040 | 1487 | H, M | 2 | Raíz | Criollo |
| Mich 70 | Z | Uruapan | 19.54065 | -102.34328 | 1944 | Hass | 2 | Raíz | Criollo |
XVariedad: H=Hass; M= Méndez; FM= Flor de María; ySeveridad en escala nominal de 0 = aparentemente sano a 4 = muerto.
Extracción de ADN, amplificación y secuenciación. El micelio se obtuvo a partir de aislados monospóricos sembrados en EMA durante 10 días y transferidos a medio líquido PD para la extracción con micelio deshidratado. La extracción de ADN se realizó con el protocolo de AP (SDS 1 %) (Sambrook y Russell, 2001). Para amplificación por PCR, la concentración se ajustó a 40 ng μL-1. El protocolo de PCR para TEF 1-α y RPB2 fue el adaptado por CP-LANREF (López-Bautista et al. 2020). Los iniciadores fueron EF1 (5’- ATG GGT AAG GAR GAV AAG AC) y EF2 (5’-GGA DGT ACC AGT RAT CAT G) para TEF 1-α; y 5F2 (5’ - CTG GGG HGA YCA RAA RAA RGC) y 7cR (5’ - CCA
TRG CYT GYT TRC CCA TRG C) para RPB2 (Lombard et al., 2015). Las amplificaciones se realizaron en termociclador T-100 de BioRad. El programa PCR para TEF 1-α consistió en: desnaturalización inicial a 94 °C por 5 min y 30 ciclos con desnaturalización a 94 °C por 30 s, alineamiento a 58 °C por 40 s, extensión a 72 °C por 55 s y una extensión final de 72 °C por 7 min (Mendoza et al. 2021). Para RPB2 las condiciones de PCR fueron 94 °C por 90 s, seguido por 40 ciclos a 94 °C por 30 s, a 61
°C por 90 s y a 68 °C por 2 min y una extensión final a 68 °C por 5 min (López-Bautista et al., 2020). Los fragmentos amplificados se sometieron a electroforesis en gel de agarosa al 1.5 % a 90 volts por 90 min. Los productos de PCR se enviaron a Macrogen Inc., South Korea para su secuenciación.
Análisis filogenético. Las secuencias obtenidas se editaron con el software SeqAssem (v07/2008) eliminando ambigüedades en los extremos. Se analizaron con la función BLASTn en NCBI para identificación de especies tomando como base el porcentaje de identidad. Inicialmente se incluyeron secuencias con porcentaje de identidad mayor a 98
% respecto a los aislamientos tipo y a secuencias de especies asociadas a nectriales publicadas por Lombard et al. (2015) y Lawrence et al. (2019) (n = 66 para RPB2; n = 65 para TEF 1-α) y disponibles en NCBI. Posteriormente se incluyeron otras con homologías > 94 % que conformaron clados con especies ya reportadas. Esto debido a la variabilidad de nectriales (Androsiuk et al., 2022). Se realizó el alineamiento de secuencias empleando el servidor MAFFT ver 4.0 configurado con los parámetros predefinidos (Katoh et al., 2017). El archivo en formato FASTA obtenido del alineamiento se convirtió a extensión NEXUS con el software Mesquite v. 3.10 (Parkinson et al. 2017). Para cada gen / región se realizó el análisis filogenético utilizando el criterio máxima parsimonia con el software PAUP ver 4.0. Se utilizaron Stachybotrys chartarum, Fusarium solani, F. oxysporum, F. circinatum, Nectria cinnabarina, N. rubicola, y N. balansae como especies externas, las cuales fueron seleccionadas por su asociación con árboles de aguacate, especies forestales o uso en estudios filogenéticos previos (Lombard et al., 2015). El análisis de inferencia Bayesiana se generó en MrBayes
v. 3.2.5 con Markov Chain Monte Carlo (MCMC) (Huelsenbeck y Ronquist, 2001). Los
árboles filogenéticos se visualizaron y editaron empleando los softwares FigTree v1.4.2 e iTOL: Interactive Tree Of Life.
Análisis de distribución geográfica. En ArcMap® v10.3, una matriz de frecuencias, agrupada por sitio de muestreo, a nivel de género y especies de nectriales, y de otros hongos y pseudohongos aislados de raíz, se importó y visualizó mediante Pie chart para determinar la ocurrencia y co-ocurrencia regional. Adicionalmente, un mapa interpolado mediante IDW2 con la severidad promedio en dosel de árbol por sitio se usó como referencia para determinar la asociatividad de nectriales, y otros hongos y pseudohongos con potencial inductividad epidémica.
Asociatividad de especies de nectriales con otros hongos y pseudohongos. En RStudio® 2023.06.2, la matriz de frecuencias a nivel de género y especies de nectriales, y otros hongos y pseudohongos, se ajustó a un análisis de correlación de Pearson (r) mediante la función cor (librería Base). La visualización de la correlación se realizó mediante la función corrplot (librería Corrplot). Adicionalmente, las 25 correlaciones de mayor asociatividad y significancia (p-value < 0.05) se visualizaron mediante la función cross-correlation (librería lares). Este análisis tuvo como propósito demostrar la asociatividad potencialmente patogénica entre especies de hongos y pseudohongos con los síntomas previamente descritos.
Resultados y Discusión
Sintomatología. Los síntomas identificados en campo asociados a nectriales consistieron en una marchitez generalizada de intensidad variable; defoliación descendente progresiva a partir de ramas apicales superiores; y reducción del crecimiento de fruto. En raíces secundarias, inicialmente se forman lesiones rojizas subcorticales, seguido de lesiones necróticas invasivas en médula y eventualmente subcorticales con formación de pequeñas protuberancias en árboles con severidad 75 - 100 % (Figuras 1 y 2). Se generó una escala nominal de severidad de seis clases específica para nectriales, i.e. a partir de aquellos árboles sin detección de otros organismos con efectos sintomatológicos análogos. Las clases propuestas incluyeron daño en dosel y raíz pudiéndose encontrar árboles severamente defoliados y necrosis invasiva cortical - medular con deformación en raíz secundaria, pero no muerte de árbol. Aunque se observó alta variabilidad en intensidad de lesión en raíz, necrosis en xilema y floema primario y secundario, fue la condición predominante (clase 4) (Figura 2). Sin embargo, debido a la presencia en Michoacán (Michua-Cedillo et al., 2024; Olalde-Lira et al., 2020; Rivas-Valencia et al., 2017), también confirmados en este trabajo, de Armillaria, Phytophthora cinnamomi, Fusarium y Verticillium, los cuales pueden causar síntomas similares, para una correcta identificación de síntomas de nectriales es fundamental complementar con diagnósticos de laboratorio (Figura 1). Adicionalmente, prospecciones de campo con base en síntomas pueden ser complejas e imprecisas debido a síntomas inconsistentes entre especies nectriales y la frecuente asociación entre estos, y los otros organismos reportados en este trabajo (Figura 2). Aunque restrictivo para proyectar el efecto patogénico en árboles adultos (> 10 años) (Olalde-Lira et al., 2020; Parkinson et al., 2017; Dann et al., 2011), condición en la que predominantemente se han detectado síntomas de nectriales, trabajos de patogenicidad adicionales son necesarios para comprender efectos individuales y combinados de estos organismos en sintomatología y fisiología de planta.
Cuadro 2 Características fisicoquímicas de algunos huertos de aguacate muestreados y especies de nectriales identificados.
| Municipio / Huerto | pH | MO | Ca | Fe | CE | Especies Nectriales / ID |
|---|---|---|---|---|---|---|
| I. liriodendri (Mich03, Mich35, Mich36, Mich40, Mich44, Mich52) | ||||||
| D. macrodidyma (Mich41) | ||||||
| Ario de Rosales / PA | 5.8 | 7.6 | 725 | 11.3 | 0.6 | D. novozelandica (Mich34, Mich37, Mich39, Mich51) |
| M. samuelsii (Mich14) | ||||||
| Pátzcuaro / SM | 6.0 | 7.7 | 1139.6 | 21.9 | 0.6 | I. liriodendri (Mich09, Mich10, Mich11, Mich12, Mich13, Mich15, Mich16) |
| Uruapan / G1 | 6.2 | 5.0 | 1285.2 | 67.8 | 0.3 | I. liriodendri (Mich45) |
| Salvador E. / ElC32 | 6.4 | 6.4 | 1275.1 | 22.9 | 0.4 | D. novozelandica (Mich53) |
| I. liriodendri (Mich54) | ||||||
| Uruapan / LaC | 6.3 | 3.6 | 2104.8 | 25.5 | 1.3 | T. lucida (Mich57) |
| D. macrodidyma (Mich58) | ||||||
| Tancítaro / ElT12 | 6.1 | 4.1 | 988.5 | 14.9 | 0.09 | I. liriodendri (Mich66) |
| Charapan / ElZ | 5.9 | 5.3 | 576.7 | 22 | 0.1 | I. liriodendri (Mich67) |
| Tancítaro / ElB | 5.7 | 2.6 | 1433 | 16 | 0.5 | I. liriodendri (Mich68) |
| Uruapan / Z | 6.4 | 1.5 | 1382.2 | 20.8 | 0.2 | D. macrodidyma (Mich70) |
La presencia de nectriales aparentemente se asoció con huertos con pH 5.8 - 6.4. independientemente del nivel de MO, Ca, Fe y CE. Previos reportes han relacionado mayor necrosis en raíces secundarias en suelos con pH > 5, en comparación con pH ≥ 7.0 (Rahman y Punja, 2005). Esta tendencia también se ha observado en otros hipocreales, como Fusarium spp., los cuales pueden exhibir mayor severidad de síntomas de marchitez (Lopez-Bautista et al., 2020). Adicionalmente, en aguacate se ha demostrado que el contenido de humedad es un factor determinante en la presencia o ausencia de estos organismos. En condiciones de estrés hídrico la frecuencia de nectriales es mayor comparado con humedad > 40 %, debido a disminución en carga de inóculo (Agustí y Armengol, 2013). Posiblemente, la prevalencia e incidencia de nectriales, considerados en general de baja agresividad (Lombar) y otros organismos asociados puede explicarse por la expansión del cultivo de aguacate en Michoacán hacia zonas de transición climática de templado a cálido (p.e. Ario de Rosales: (A)C(w2) (w)a(e), sensu Enriqueta García), y la creciente conversión de áreas forestales con implicación en cambio de régimen hídrico detrimental.
Morfotipos culturales. Se observaron cinco morfotipos en EMA, PDA y AA, diferenciados por color de micelio, crecimiento y pigmentación. Los aislados presentaron crecimiento lento (10-15 días) con crecimiento radial uniforme o irregular fimbrado; micelio algodonoso - aéreo o deprimido; pigmentación combinada en amarillo, blanco cremoso o marrón; y presencia de macroconidios hialinos, o ligeramente pigmentados, 0-
4 septos, cilíndricos rectos con extremos redondeados o ligeramente en punta, y microconidios unicelulares (Figura 3). Estas características en general coinciden con descripciones de la familia Nectricacea (Lombard et al., 2015). El medio de cultivo EMA, seguido de AA permitió la mejor caracterización. Estos morfotipos correspondieron a las especies Dactylonectria macrodidyma, D. novozelandica, Ilyonectria liriodendri, Mariannaea samuelsii y Thelonectria lucida (ver sección Análisis Filogenético).

Figure 1 A. Árbol aparentemente sano y corte longitudinal y transversal de raíz de 1.5 cm de diámetro y asociación de Ilyonectria liriodendri; B. Defoliación apical, corte logitudinal y transversal de raíz con necrosis restringida asociados a I. liriodendri; C. Reducción del tamaño de frutos, corte longitudinal y transversal de raíz con necrosis invasiva asociada a I. liriodendri; D. Defoliación y hoja pequeña asociada a Armillaria + I. liriodendri y raíz con necrosis medular; E. marchitez moderada asociada a Phytophthora cinnamomi + I. liriodendri y corte longitudinal de raíz con necrosis restringida; F. Follaje amarillo, hoja pequeña y reducción de copa asociado a Fusarium spp + Dactylonectria macrodidyma y raíz con necrosis medular invasiva. G. Marchitez progresiva y raíz con necrosis y micelio invasivo en raíz de raíz asociado a Armillaria sp.; H. Marchitez, amarillamiento de follaje y raíz con necrosis subcortical asociada a Phytophthora cinnamomi; I. Marchitez general, follaje necrótico adherido a ramas, raíz con líneas de necrosis en raíz vascular asociado a Verticillium sp.

Figura 2 Escala nominal de seis clases de vigor y daño raíces secundarias de aguacate asociados a cuatro géneros y cinco especies de nectriales: 0. Árbol sano con 100% de vigor y raíz sin lesiones; 1. Defoliación apical en ramas superiores, raíz con lesiones rojizas <1 cm en raíz central (80% vigor en copa); 2. Defoliación apical progresiva en ramas superiores, amarillamiento en estrato foliar inferior, raíz con líneas rojizas en parénquima medular (75% vigor); 3. Defoliación, marchitez y raíz con necrosis invasiva en raíz subcortical y medular (50% vigor); 4. Defoliación parcial, hojas pequeñas y raíz con necrosis en xilema y floema primario y secundario raíz (35% vigor); y 5. Árbol defoliado y raíz con necrosis invasiva (15% vigor).
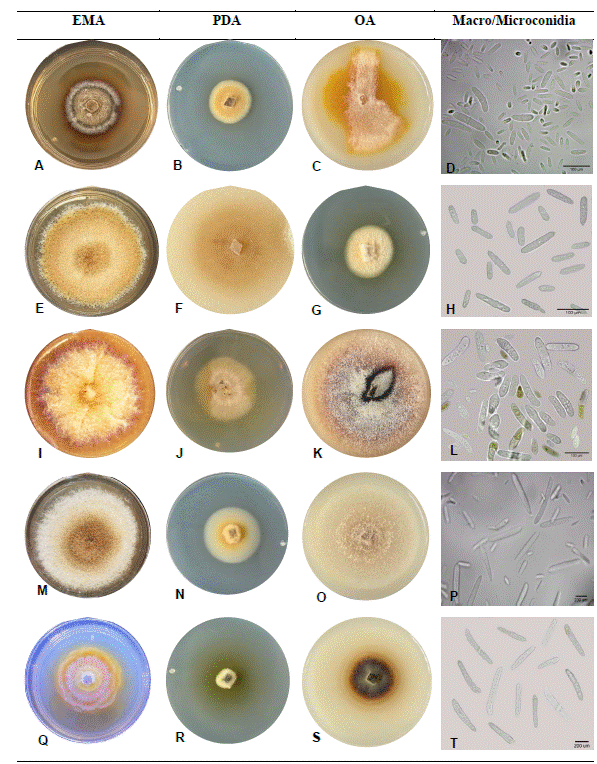
Figura 3 Morfotipos culturales de nectriales aislados de raíces de aguacate con síntomas en dosel y raíces según descripción en Figura 2 e identificados molecularmente con homologías > 97% para la region/gen RPB2 y TEF 1-α. A-D. Dactylonectria macrodidyma; E-H. Dactylonectria novozelandica; I-L. Ilyonectria liriodendri; M-P. Mariannaea samuelsii; y Q-T. Thelonectria lucida.
Se observaron algunas similitudes entre macroconidios deIlyonectriay
Dactylonectria, no obstante, no es una variable robusta para discriminar entre estos
géneros. Mariannaea presentó macroconidios con 1-2 septos, pared celular gruesa y extremos con terminación ligeramente en punta. Thelonectria fue el único género que presentó crecimiento miceliar anillado cremoso amarillo en EMA o coloración marrón en AA después de 15 días de crecimiento. Petit y Gubler (2005) indicaron que, aunque los conidios de D. macrodidyma son más grandes que los de I. destructans, no son significativamente diferentes, por lo que determinaron que el análisis molecular es necesario para obtener un diagnóstico confirmatorio a nivel especie comparando Dactylonectria e Ilyonectria. La morfología de colonia y atributos de conidios se han utilizado ampliamente para delimitar especies miembros de Nectriaceae (Schroers et al. 2008). Sin embargo, este enfoque requiere alta especialización y experiencia taxonómica. En vid, se han observado diferencias culturales y conidiales entre una colección de aislados de Neonectria liriodendri obtenidos de plantas asintomáticas y sintomáticas (Halleen et al. 2004). Aunque en este estudio los morfotipos fueron aislados de árboles predominantemente sintomáticos, se sugiere procesar raíces de árboles asintomáticos para discriminar diferencias morfológicas. En general, en los cuatro géneros se observó presencia de macro y microconidios, presencia de vesículas y clamidosporas en cadena o solitarias. Particularmente, Ilyonectria presentó macroconidios cilíndricos con 1-4 septos, microconidios aseptados, elípticos y clamidosporas globosas a subglobosas con micelio hialino, similares a estudios análogos en California (Lawrence et al., 2019). Estas características fueron observadas en 17 cepas aisladas de raíz de aguacate. Los macroconidios de Dactylonectria fueron cilíndricos, hialinos, rectos a ligeramente curvados, 1-4 septos, microconidios elipsoides a ovoides, hialinos, 0 - 1 septo, con hilio diminuto. Las clamidosporas globosas a subglobosas formadas en cadenas. En Thelonectria se observaron macroconidios septados, curvos, a menudo más anchos en el tercio superior, con células apicales redondeadas y células basales aplanadas o redondeadas con hilio discreto y clamidosporas solitarias. Mariannaea posee macronidios con 1-2 septos, hialinos, clamidosporas de globosas a elipsoidales, hialinas, formadas en cadenas intercalares. Las características de estos géneros en general concuerdan con reportes previos (Lombard et al. 2015). Adicionalmente, se aislaron dos especies de Armillaria, tres de Fusarium (F. oxysporum, F. solani y Fusarium sp.) y de Phytophthora cinnamomi (Figura 4). También se detectó en menor frecuencia a Mortierella sp., Paecilomyces sp., Acremonium sp. y Acrostalagmus sp., los cuales mostraron asociatividad con algunos síntomas descritos, combinados o no, con las especies nectriales identificadas.

Figura 4 Morfotipos culturales en EMA al 2% (A, B) y PDA (C, D) aislados de raíces de aguacate con síntomas putativos a nectriales. A. Armillaria sp; B. Armillaria gallica; C. Phytophthora cinnamomi; y D. Fusarium sp.
Identificación y análisis filogenético. Se obtuvieron amplicones de aproximadamente 900 y 600 pb, asociados a RPB2 y TEF 1-α, respectivamente, para todos los aislados (Cuadro 1). El análisis de máximo parsimonia e inferencia Bayesiana coincidieron en la conformación de clados para los 30 aislados. Con RPB2 se identificaron cuatro géneros y cinco especies con homología ?γτ; 97 %: Dactylonectria macrodidyma, D. novo- zelandica, Ilyonectria liriodendri, Mariannaea samuelsii y Thelonectria lucida. TEF 1-α permitió identificar a D. macrodidyma y I. liriodendri con homología ?γτ; 97 %. Mientras que M. catenulata tuvo una homología de 64 % considerado muy bajo para una identificación taxonómica. Las secuencias de nucleótidos se registraron en el GenBank de NCBI con los siguientes números de accesión: I. liriodendri (Mich 3, OR593990; Mich 9, OR593991; Mich 11, OR593992; Mich15, OR593993; Mich 26, OR593994; T. lucida (Mich 57, OR607642); y M. samuelsii (Mich 14, OR593995; Mich 24, OR593996).
La estructura filogenética conformó cuatro clados principales con RPB2 de los cuales el específico al género Ilyonectria fue el de mayor prevalencia seguido del Dactylonectria, Mariannaea, Thelonectria y un aislado que no conformó clado con una especie(s) nectrial (MICH59) (Figura 5). Con TEF 1-α se conformaron tres clados (Figura 6). Las filogenias individuales por gen / región con el algoritmo de inferencia Bayesiana mostraron resolución baja a moderada con definición de clados interespecíficos. Con RPB2 esto fue evidente para Dactylonectria, Mariannaea y Thelonectria (Figura 5). Para el género Ilyonectria, TEF 1-α y RPB2, conformaron clados principales definidos con I. liriodendri, mientras que I. robusta e I. destructans conformaron subclados. Los porcentajes de similitud y cobertura con secuencias del BLAST fueron entre 97 y 100% respectivamente. Con TEF 1-α, las cepas MICH3, MICH9, MICH11 y MICH12 se agruparon con I. liriodendri, mientras que con RPB2 se integraron 14 aislados dentro del clado pero con distancias entre 0.022 y 0.043, lo que sugieren la presencia de haplotipos o alta variabilidad intraespecífica.
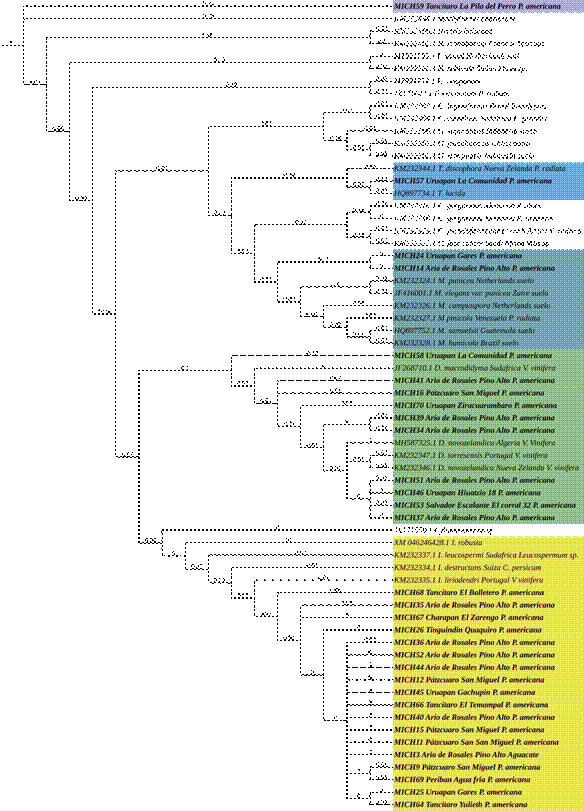
Figura 5 Árbol filogenético generado por análisis de Inferencia bayesiana de secuencias de la región RPB2 generados a partir de aislados de nectriales de árboles de aguacate comercial. Los aislados provenientes de este trabajo están indicadas con el prefijo MICH. El análisis incluyó ocho especies de referencia externa (ramas superiores y Cylindrocarpon). La barra de escala representa el número esperado de cambios de nucleótidos por sitio.
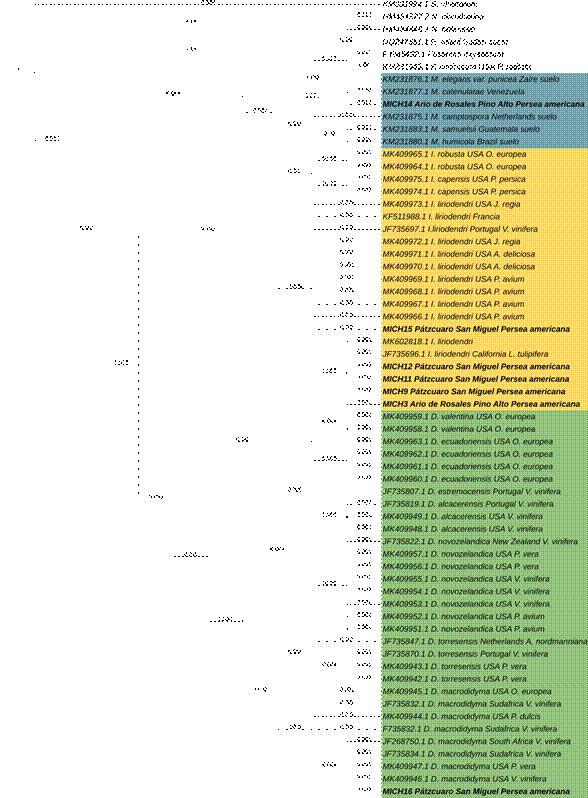
Figura 6 Árbol filogenético generado por análisis de inferencia bayesiana de secuencias del gen TEF 1-α generados a partir de aislados de nectriales de árboles de aguacate comercial. Los aislados provenientes de este trabajo están indicadas con el prefijo MICH. El análisis incluyó seis especies de referencia externa. La barra de escala representa el número esperado de cambios de nucleótidos por sitio.
La estructura filogenética con máxima parsimonia y RPB2 mostró que el aislado MICH16 se integró con D. novo-zelandica mientras que inferencia Bayesiana se agrupó con D. macrodidyma (Figura 6). Los dos algoritmos empleados colocaron en similar clado a MICH14 con varias especies de Mariannaea. La cepa MICH57 estuvo emparentada con Thelonectria lucida, siendo la única que representó a este clado. En contraste, el aislado MICH59 no estuvo agrupado en ningún clado, incluso quedó fuera de las especies referencia, las cuales claramente quedaron fuera de la estructura filogenética que conformaron la mayoría de los aislados de aguacate.
Regiones parciales o completas de los genes ITS, TEF 1-α, TUB e HIS, se han utilizado ampliamente en análisis filogenéticos moleculares de ascomicetos. Sin embargo, en la familia Nectriaceae se han observado discrepancias analíticas filogenéticas al emplear secuencias integradas por algunos genes, en particular la identificación precisa de Dactylonectria spp. (Lawrence et al. 2019). Se ha demostrado que el locus HIS es un marcador idóneo para la delimitar especies con alta proximidad a Cylindrocarpon (Cabral et al., 2012a). Este gen taxonómicamente ha resuelto a D. macrodidyma (Gordillo et al., 2017). Sin embargo, la selección de regiones genómicas debe estar basada en el número de sitios informativos y conservados para obtener un porcentaje útil de la secuencia. Los genes TEF 1-α y RPB2 poseen un porcentaje informativo de 81 % y 64 %, y número de sitios invariables de 94 % y 48 %, respectivamente (Lombard et al. 2015). Sin embargo, en esta investigación RPB2 resultó más efectivo para la identificación taxonómica y generó una estructura filogenética más consistente para discriminar los aislados entre géneros nectriales. Adicionalmente, la inferencia Bayesiana mostró mayor consistencia filogenética. Los géneros Cylindrocladiella, Cylindrocladium, Dactylonectria, Gliocladiopsis, Ilyonectria y Mariannaea se han reportado en P. americana usando ITS, HIS y TUB con análisis concatenado de secuencias; además, los genes hibridizados han sido eficientes para identificar Ilyonectria y Dactylonectria (Parkinson et al., 2017). Contrariamente, Thelonectria y Mariannaea han sido poco estudiados, y en particular Mariannaea no es un patógeno frecuente en cultivos de importancia económica (Hu et al. 2016). Considerando que las secuencias de las especies de Mariannaea utilizadas en este análisis filogenético provienen de rizosfera y de raíz con síntomas de necrosis, sugiere que los aislados identificados dentro de este género podrían ser parásitos facultativos o saprófitos. Este género se ha encontrado en una amplia gama de hospedantes perennes en California (Rosman et al. 2016). Asimismo, se ha documentado que el uso acotado a dos genes no tiene precisión para algunas especies como T. aurea, sin embargo, la concatenación o análisis multilocus permite separar discriminar linajes de nectriales en general (Lawrence et al., 2019; Lombard et al., 2015). En este trabajo se optó por realizar en una primera etapa estudios filogenéticos independientes con el fin de priorizar la capacidad informativa de cada gen / región. Estudios futuros deben integrar otros genes con el fin de encontrar los análisis multilocus más pertinentes (Lombard et al., 2015).
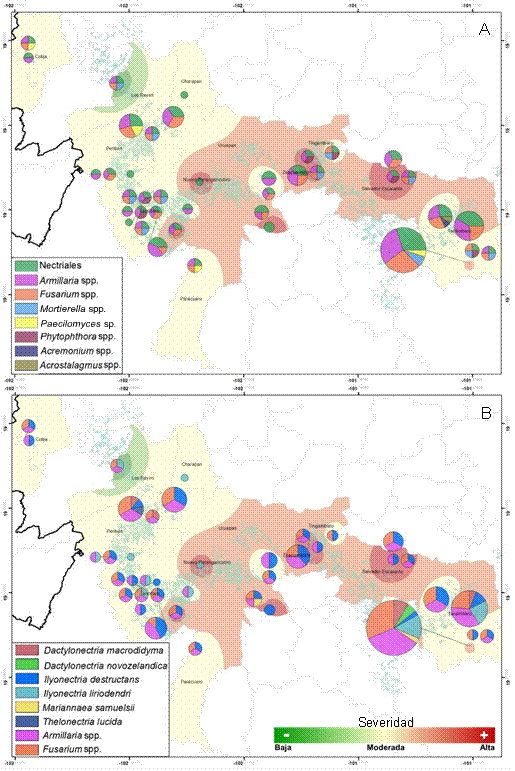
Figura 7 Distribución y prevalencia regional de comunidades en raíz de organismos putativamente asociados con el decaimiento y síndrome de marchitez del aguacate en 13 municipios de Michoacán. A. Distribución filogeográfica de cuatro géneros nectriales. B. Distribución filogeográfica de seis especies nectriales. Se incluyen Armillaria spp. y Fusarium spp. como especies de alta prevalencia regional (fines comparativos). Las zonas verde-amarillo-marrón en ambos mapas muestra la proyección geoestadística de intensidad epidémica (escala de color: baja, moderada y alta) evaluada mediante escala de severidad de daño en dosel de árbol. El punteado color azul verdoso representa polígonos del inventario de huertas de aguacate.
Análisis geográfico y asociatividad entre organismos. A nivel regional, al menos una especie nectrial se encontró en 100 % de sitios y municipios muestreados y en co- ocurrencia alta con Armillaria spp (97.1 %), Fusarium spp. (92.9 %) (r = 0.60 - 0.88, p
≤ 0.05) (Figura1D y 1F), y moderada con Mortierella spp. (47.3 %) y Paecilomyces spp. (56.4 %) (r = 0.41 - 0.63, p ≤ 0.05), con el resto de los géneros no se encontró co- ocurrencia significativa, incluido Phytophthora cinnamomi a pesar de antecedentes regionales causando marchitez en árboles de aguacate (r = - 0.19 - 0.0) (Figura 1H; Figura 7A, Figura 8A) (Teliz y Mora, 2007). En general, Armillaria spp. y Fusarium spp. fueron las especies más ampliamente distribuidas y con mayor co-ocurrencia y asociatividad (r
= 0.94, Figura 7A y Figura 8A y 8B). La asociatividad infecciosa de Armillaria spp. con Fusarium oxysporum, se ha reportado en Michoacán causando muerte descendente de Prunus sp. (Rivas-Valencia et al., 2017). La especie A. gallica está consignada en aguacate (Michua-Cedillo et al., 2024). Esta especie, y otra por determinar, se confirmaron en este trabajo. Fusarium oxysporum y F. solani, encontradas en esta investigación, han sido previamente reportadas en este cultivo y región (Olalde-Lira et al., 2020). Interesantemente, en sitios donde no se encontraron especies nectriales, p.e., Charapan, Tancítaro y Nuevo Parangaricutiro, Armillaria spp fue el hongo predominante relacionado con áreas regionales con inductividad potencialmente epidémica moderada - alta (Figura 1G; Figura 7A). En general, la asociación de Armillaria spp., Fusarium spp. y nectriales implicó regiones con inductividad de daño regional alta (severidad en planta
> 50 %). Interesantemente, en áreas de inductividad epidémica baja - moderada, estos géneros tuvieron co-ocurrencia moderada (r = 0.49 - 0.65) con Mortierella spp. (Figura 7A, Figura 8A). Las proyecciones espaciales se generaron con escalas de daño en copa y pueden ser un indicativo de endemicidad y de riesgo epidémico que representa el complejo de organismos asociados con síntomas de raíz y copa descritos (Figura 1 y 2). Los datos de este estudio sugieren que el riego actual es moderado y requieren intervención regional preventiva.
De 30 aislados procesados para caracterización morfológica y molecular, el 56 % fueron identificados como I. liriodendri en Ario de Rosales, Charapan, Peribán, Tancítaro, Tingüindín y Uruapan en huertos de 10 - 40 años, suelo con textura franco- arenosa e interesantemente, una región con nivel de inductividad potencialmente epidémica baja - moderada (Figura 7B). Estas características sugieren que este género podría ser el ancestro de las especies encontradas a nivel regional, y que los aislados dentro del clado pueden ser haplotipos que ha experimentado evolución histórica, lo cual explica su mayor prevalencia regional (adaptabilidad) y nivel de inductividad baja - moderada. Adicionalmente, esta especie se asoció significativamente con Armillaria spp. (r = 0.76, Figura 8A - 8B). Sin embargo, otro subclado de aislados de I. liridendri estuvo vinculado regionalmente con niveles de inductividad alta en asociación moderada con Fusarium spp. y Armillaria spp. (r = 0.28 y 0.34, respectivamente), sugiriendo un potencial efecto sinergético vinculado con daños más severos en dosel - raíz (Figura 7B, Figura 8A - 8B). Dactylonectria macrodidyma y Dactylonectria novozelandica representaron el 33 % de especies principalmente en Tacambaro y Peribán, asociadas con Fusarium spp. y Armillaria spp. (r = 0.83 - 0.88, Figura 8A - 8B). Mariannaea samuelsii (6 %) y Thelonectria lucida (3 %) se identificaron de forma local en Nuevo Parangaricutiro, Tacámbaro y Peribán (Figura 7 - 8). En particular, Mariannaea samuelsii tuvo una co-ocurrencia regional moderada con Armillaria spp., Fusarium spp., Mortierella spp., y Paecilomyces spp. (Figura 7A y 8A-8B). Los resultados sugieren que la prevalencia, distribución y diversidad de especies está relacionada con variables fisicoquímicas de suelo, zonas productivas de transición aguacatera, y estrés abiótico, las cuales alguna potencialmente pueden condicionar el potencial virulento de organismos como Mariannea spp. que se reporta ampliamente como saprófito (Hu et al. 2016).
En general, la mayor diversidad de especies se observó en Uruapan y Tacámbaro (Figura 7 y 8), considerados como pioneros en la producción de aguacate en la región, por lo cual se esperaría encontrar menor diversidad de especies como consecuencia del manejo intensivo del cultivo, en comparación con huertos de Charapan que están establecidos en zonas forestales y son huertos relativamente jóvenes (menores de 15 años). En este municipio, la incidencia de Armillaria spp. fue mayor al 90 %, vinculado con conversión de zonas forestales a aguacateras con alta capacidad patogénica y saprófita de este basidiomyceto. La asociatividad de organismos puede generar una expresión de síntomas diversos en dosel y raíz en función del efecto parasitismo de cada especie implicada (López-Bautista et al. 2019). En campo, para la asociación Armillaria
- Ilyonectria los síntomas se observaron en árboles longevos con declinamiento lento comparado con árboles de menores a 15 años, donde los síntomas fueron atenuados particularmente en temporada de lluvias. Sin embargo, se sugiere muestreos regionales complementarios para evaluar la correlación de variables de incidencia, severidad, prevalencia, densidad de inóculo de especies identificadas en este estudio y otras con potencial patogénico. Debido a la endemicidad y asociatividad diferenciada de especies de nectriales con otros hongos, de los cuales ya se ha demostrado su patogenicidad (Olalde-Lira et al., 2020; Parkinson et al., 2017; Dann et al., 2011), en este trabajo se postula el término ‘síndrome de declinamiento del aguacate’ para referirse a un complejo de síntomas en dosel y raíz (Figura 1 y 2), cuya severidad puede depender de las especies de hongos implicados, manejo y edad de huerto, y características físico-químicas del suelo. Debido a la baja frecuencia de P. cinnamomi en este estudio, y al cambio detrimental de régimen hídrico, posiblemente este organismo está siendo desplazado por otros hongos con mayor capacidad parasítica.
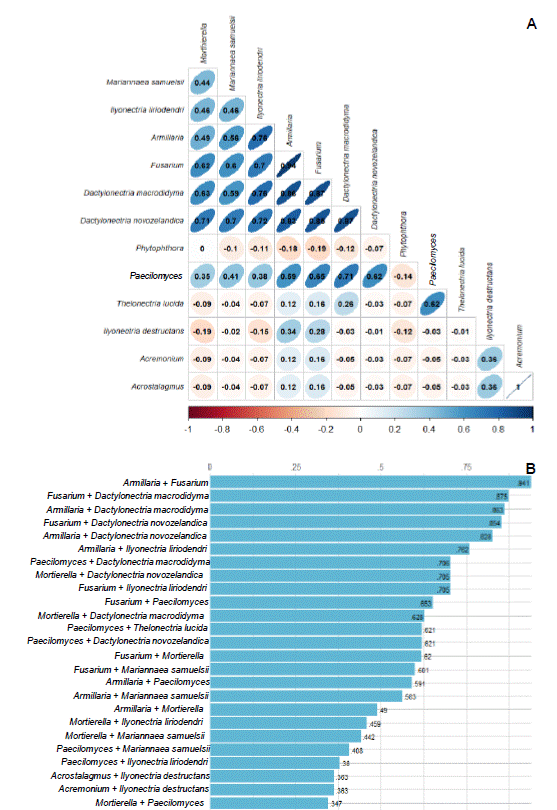
Figura 8 Gráficas de asociatividad de organismos aislados de raíces de aguacate con síntomas de síndrome de declinamiento. A. Correlación de Pearson (r) que muestra asociación entre nectriales y otros organismos de raíz; y B. Cross- correlación en pares y ordenada por nivel de asociatividad para las 25 principales correlaciones significativas.
Conclusiones
Este es el primer reporte que proporciona evidencias de la implicación regional de un complejo hongos, con potencial asociación de especies nectriales, en un proceso infeccioso que resulta en síntomas de marchitez generalizada de intensidad variable; defoliación descendente progresiva; reducción del crecimiento de hojas y frutos; raíces secundarias con lesiones rojizas subcorticales, seguido de lesiones necróticas invasivas en médula y subcorticales. Se propone el ´síndrome de declinamiento del aguacate´ para denotar a este enfermedad. A nivel mundial se reporta por segunda ocasión a Mariannaea samuelsii asociado a aguacate, y Thelonectria lucida por primera vez. Otros nectriales con menor frecuencia regional fueron Dactylonectria macrodidyma, y D. novo-zelandica. Sin embargo, I. liriodendri fue el más prevalente y recurrentemente asociado con Armillaria spp. y Fusarium spp., en regiones con mayor inductividad epidémica potencial. Este escenario parasítico complejo representa un riesgo emergente para la producción de aguacate en Michoacán y otras regiones. Esta investigación se debe complementar con pruebas de patogenicidad y estudios de prevalencia-diversidad de especies, haplotipos y niveles de agresividad con el fin de coadyuvar a un manejo sustentable del cultivo.















