Introducción
El género Phaseolus (Fabaceae: Papilionoideae), con Mesoamérica y Sudamérica como centros de origen, está ampliamente distribuido en el mundo (Graham y Ranalli, 1997). Este género contiene 56 especies nativas de Mesoamérica (MoraAguilera et al., 2023), de las cuales el frijol Ayocote (Phaseolus coccineus) ostenta el tercer lugar en importancia económica después del frijol ancho (P. lunatus) y frijol común (P. vulgaris) (De Ron y Santalla, 2013; Santalla et al., 2004). Además de México, materiales criollos o variedades de P. coccineus se cultivan en América Central, Sudamérica, África, Asia y Europa (Giurca, 2009; Watanabe y Tojo, 2006). El Ayocote es una planta semiperenne vigorosa, aporta 18.4 % de proteína, cantidad menor al promedio del frijol común (Pérez et al., 2002), posee tolerancia al frío y a fitopatógenos como Colletotrichum sp., Uromyces sp., Sclerotinia sclerotiorum y Xanthomonas campestris (Vargas et al., 2014; Giurca, 2009; Schwartz et al., 2006). Es notorio que, a partir de genotipos introducidos de Japón, este frijol ha mostrado susceptibilidad a Pythium myriotylum con necrosis en tallo y raíz en plantaciones comerciales, y hasta 93-100 % de incidencia en inoculaciones controladas (Watanabe y Tojo, 2006). Este hongo, no se ha reportado en este cultivo en México. Respecto a enfermedades virales, se ha consignado al Cowpea mild mottle virus (Betaflexiviridae: Carlavirus) en condición sintomática (lesiones cloróticas, moteado moderado y severo, mosaico moderado y deformación foliar) y asintomática en colectas de Jalisco y Nayarit (Chiquito-Almanza et al., 2018); sin embargo, la prevalencia de agentes virales en frijol Ayocote es menor al 20 %, mientras que en frijol común supera el 97 % en el occidente de México (Chiquito-Almanza et al., 2021).
Estos trabajos permiten sustentar que P. coccineus exhibe mayor tolerancia a patógenos que P. vulgaris. Esta condición se puede deber a una limitada manipulación genética de la especie lo que ha permitido mantener su natural adaptación a factores de estrés parasítico. Por otra parte, P. coccineus exhibe mayor alogamia respecto al frijol común, lo que resulta en mayor diversidad genética expresada en su plasticidad fenotípica, duración de ciclos productivos, color y peso de grano (Vargas et al., 2014). La tolerancia parasítica del frijol Ayocote ha justificado su incorporación a programas de fitomejoramiento en México, aunque con mayor énfasis a mejorar atributos productivos. Blanco Tlaxcala fue la primera variedad generada por Instituto Nacional de Investigaciones Forestales, Agrícolas y Pecuarias (INIFAP) con este enfoque manteniendo su tolerancia natural a roya y antracnosis (Vargas et al., 2014; Pérez et al., 2002). No obstante, P. coccineus ha sido de interés como fuente de resistencia para el manejo de Sclerotinia sclerotiorum y Bean golden yellow mosaic virus (Osorno et al., 2007; Schwartz et al., 2006).
En el campo experimental de Colegio de Postgraduados, Campus Montecillo, Estado de México, en un lote de P. coccineus de 3100 m2 establecido para producción de semilla con fines de mejoramiento genético, se detectó alta incidencia de un síntoma presuntivo a cenicilla, en adición a la presencia de distorsión y amarillamiento foliar putativos a infección viral y/o fitoplásmico. Debido a la reconocida tolerancia del Ayocote a fitopatógenos, y con el propósito de caracterizar el comportamiento parasítico para su consideración en futuros estudios de mejoramiento, este trabajo tuvo como propósito determinar la etiología de los síntomas descritos; y establecer el comportamiento espacial de contagio de la putativa cenicilla, el problema más prevalente, para determinar su aptitud epidemiológica considerando que la región de estudio está incluida en el centro de origen y diversificación de P. coccineus.
Materiales y Métodos
Unidad experimental. En julio 2022, ciclo verano-otoño, se seleccionó una parcela experimental (50 x 62 m) de frijol Ayocote en etapa de floración ubicada en el Colegio de Postgraduados, Campus Montecillo Texcoco, Estado de México (19°46´80´´N, 98°89´76´´O). Las plantas, rebrotes de segundo año, exhibían síntomas severos de una presuntiva cenicilla polvosa y de tipo viral/fitoplásmico (Figura 1). La parcela tuvo una densidad irregular, heterogeneidad en cobertura, manejo agronómico moderado, control químico de malezas y riego por inundación. Se tomó una imagen de 13mpx mediante un vuelo vertical de 50 m con drone Phantom 3 DJI® para diseñar el muestreo espacial. La parcela se dividió en 80 cuadrantes de 6x6 m y 720 subcuadrantes de 2x2 m para evaluar la severidad del síntoma tipo cenicilla y otros daños predominantes (Figura 1A). La delimitación de cuadrantes en campo se realizó con estacas de madera periferales y una red de listón de rafia (Figura 1B). En el centroide de parcela se colocó un sensor climático HOBO u23 Pro v2 para medir humedad relativa (HR) y temperatura (°C) a intervalos de 30 min entre 16-julio y 11-agosto de 2022.
Identificación etiológica y genómica del hongo
Identificación morfológica del hongo. Se realizó un muestreo dirigido en 25 plantas con diferente grado de severidad del síntoma tipo cenicilla, único síntoma fungoso detectado. A partir de hojas sintomáticas, con la técnica de cinta adhesivasolución acuosa, se prepararon portaobjetos directamente en campo y laboratorio para revisión de estructuras en microscopio compuesto (40x) e identificación del hongo a nivel género con claves taxonómicas (Barnet y Hunter, 1998). Se realizaron mediciones de 60 conidios con el software ImageJ® y se calculó la media ± desviación estándar de largo y ancho de conidios mediante una muestra estimada con el programa Muestra-N Cuanti v.1 (CP-LANREF, 2020. No publicado). Las observaciones microscópicas se compararon con descripciones taxonómicas especializadas (Takamatsu, 2014; Cook y Braun, 2009; Glawe, 2008).
Extracción de ADN e identificación genómica del hongo. Mediante muestreo dirigido se seleccionaron 10 plantas distribuidas espacialmente en la parcela. Por planta, se colectaron 3-5 hojas con signos del hongo y se colocaron independientemente en bolsas polipapel para traslado a laboratorio donde de inmediato se fotografiaron y seleccionó un foliolo por cantidad y calidad de síntoma-signo. Para evitar contaminantes fungosos, de un foliolo por planta se raspó micelio superficial de infecciones jóvenes con signos activos y crecimiento vigoroso y se colocó en

Figura 1 Muestreo para identificar y evaluar intensidad de síntomas fungosos, putativos virales/fitoplásmicos, y entomológicos en Phaseolus coccineus. A. Imagen de 13mpx 50m con drone Phantom 3 DJI®, muestra la cuadrantización de la parcela experimental. En líneas amarillas cuadrantes de 6x6 m, y en blanco subcuadrantes de 2x2 m. Asteriscos indican subcuadrantes/cuadrante seleccionados aleatoriamente; B. Instalación grid para delimitación de cuadrantes en campo; C. Selección de subcuadrante colocando marco de madera 1x1 m para referencia de evaluación; D. Síntomas de mosaico punteado (izquierda) y aclaramiento de nervaduras (derecha), putativos a virosis. Plantas marcadas con estacas para trazabilidad; E. Amarillamiento generalizado con reducción de crecimiento (izquierda), mosaico con deformación foliar (derecha) presuntivamente viral; F. Síntoma foliar con signo micelial fungoso blanquecino putativo a cenicilla; G. Haz de foliolo con signo micelial blanquecino. H. Macrodactylus sp. adultos, y color-morfología floral de P. coccineus. Notar en algunos pétalos manchas pequeñas blanquecinas (ver flechas).
tubo Eppendorf con 600 µL de buffer AP y dos balines 1/8. Cada tubo constituyó una muestra/planta. El micelio del tubo se maceró en un disruptor a 30 frecuencias por 15 min. Se retiraron los balines y se agregó 1 µL de β-mercaptoetanol y se pasó por vórtex por 10 s. Se incubó a 56 °C por 45 min. Después se agregó 400 µL de fenol:cloroformo:alcohol isoamílico (25:24:1) y se homogenizó por vórtex. Se centrifugó a 13,500 rpm por 10 min a temperatura ambiente. Se recuperó 500 µL de la fase acuosa y se agregó 500 µL de isopropanol y 50 µL de acetato de amonio, se mezcló por inmersión y se incubó a -20 °C por una noche. Posteriormente, se centrifugó a 13,500 rpm por 10 min. Se desechó el sobrenadante y se lavó con 500 µL de etanol al 80 %. Se centrifugó a 13,500 rpm por 3 min. Se desechó el sobrenadante y se secó la pastilla por 1 h y finalmente se resuspendió en 50 µL de agua libre de nucleasas y se conservó a -20 °C. Por muestra se cuantificó la concentración y pureza de ácidos nucleicos totales con NanoDrop 2000 (Thermo Fisher Scientific 2000, EUA).
Para PCR, se utilizaron iniciadores ITS1 e ITS4 que amplifican la región ITS del ADN (Cuadro 1). La mezcla de reacción consistió en 10 µL de cada iniciador, 0.2 µL de Taq DNA Polimerasa (Invitrogen), 2 µL de ADN (40 ng µL-1) y 16.5 µL agua libre de nucleasas. Las condiciones de PCR incluyeron desnaturalización inicial a 95 °C por 5 min y 31 ciclos con desnaturalización a 94 °C por 1 min, alineamiento a 55 °C por 1 min, extensión a 72 °C por 90 s y una extensión final de 72 °C por 5 min. Los productos PCR se analizaron por electroforesis en gel de agarosa 1.5 % teñido con bromuro de etidio y se visualizaron en un
Cuadro 1 Iniciadores, secuencias y tamaño de amplicon para la identificación genómica de Potyvirus, Begomovirus, Fitoplasmas y microorganismos eucariontes en plantas de P. coccineus con signos de hongo tipo cenicilla, y síntomas putativos a virus y fitoplasma.
| Organismo | Iniciador | Secuencia | Tamaño (pb) | Referencia |
|---|---|---|---|---|
| Hongo | ITS1 ITS4 | TCCGTAGGTGAACCTGCGG TCCTCCGCTTATTGATATGC | ~500 | White et al., 1990 |
| Potyvirus | NIb2F NIb3R | GTITGYGTIGAYGAYTTYAAYAA TCIACIACIGTIGAIGGYTGNCC | 350 | Zheng et al., 2008 |
| Begomovirus | PBL1v2040 PCR1c | CARTGRTCKATCTTCATACA CATATTTACRARWATGCCA | 500~650 | Rojas et al., 1993 |
| AV494 AC1048 | GCCYATRTAYAGRAAGCCMAG GGRTTDGARGCATGHGTACATG | ⁓550 | Wyatt y Brown, 1996 | |
| Phytoplasmas | P1 P7 | AAGAGTTTGATCCTGCAGGAT CGTCCTTCATCGGCTCTT | 1,800 | Deng y Hiruki, 1991; Samart et al., 1996 |
| FU5 RU3N | CGGCAATGGAGGAAACT TTCAGCTACTCTTTGTAACA | 890 | Lorenz et al., 1995 |
x Se emplearon iniciadores universales.
fotodocumentador (UVP, Biolmaging Systems, Epi Chemi II Darkroom). Cinco de 10 muestras amplificaron y se enviaron a secuenciar a Macrogen®, Corea del Sur. Cuatro secuencias de cinco amplicones tuvieron calidad para estudios de identificación (FAC6, FAC7, FAC8 y FAC9). Estas se editaron con el programa SeqAssem (https://acortar.link/r0FdRx) y se compararon en BLASTn (https://blast.ncbi.nlm. nih.gov/Blast.cgi) con secuencias del banco de genes (GenBank) para determinar identidad con base a similitud comparativa expresado en porcentaje de identidad y e-value.
Análisis filogenético. Una vez identificado a Erysiphe sp., para determinar la relación filogenética con otras especies de este género y confirmar la identificación, las secuencias obtenidas fueron alineadas con secuencias descargadas del GenBank usando el algoritmo MUSCLE en Mega 11 (Cuadro 2). El análisis filogenético se realizó con mismo programa, el método estadístico Máxima verosimilitud (ML), y el modelo de sustitución Hasegawa-Kishino-Yano con 1000 replicaciones Bootstrap. Se incluyó a Oidium sp. (número de accesión: EU377475) como grupo externo. El análisis involucró 12 secuencias de aproximadamente 561 pb.
Cuadro 2 Secuencias obtenidas del banco de genes NCBI utilizadas para generar la estructura filogenética y comparar con secuencias de amplicones obtenidos de cuatro muestras del hongo tipo cenicilla presente en plantas de P. coccineus.
| Especie causante de cenicilla | Número Genbank | Planta Hospedante | Lugar y Fecha de reporte |
|---|---|---|---|
| Erysiphe diffusa | FJ378880 | Glycine max | Australia, 2006 |
| E. fallax | LC228618 | Carica papaya | USA, 2017 |
| E. manihoticola | MT106660 | Manihot esculenta | Argentina |
| E. pisi | KR912079 | Pisum sativum | China, 2016 |
| E. vignae | MW293895 | Vigna radiata | Australia, 2019 |
| E. vignae | MT628286 | V. radiata | Australia, 2019 |
| Erysiphe sp. | JQ730709 | Senna septemtrionalis | México, 2012 |
| Oidium sp. | EU377475 | Knautia arvensi | USA, 2009 |
Identificación genómica de virus y fitoplasma
Colecta de material vegetal. En campo se seleccionaron plantas con síntomas presuntivos a Potyvirus, Begomovirus y Fitoplasma. Los síntomas consistieron en mosaicos tenues, deformación foliar moderada, amarillamiento generalizado, clorosis foliar, aclaramiento de nervaduras, reducción foliar, y coloración violácea en hojas, pedúnculos y tallos. Las plantas seleccionadas fueron marcadas con estacas y etiquetadas para su posterior muestreo. Se realizaron dos muestreos en diferentes tiempos; en el primer muestreo, se colectaron dos hojas trifoliadas de 32 plantas, cada hoja como repetición (64 muestras) y en el segundo muestreo se colectaron 31 plantas.
Extracción de ácidos nucleicos (ARN y ADN). Tejido foliar de las 64 muestras del primer muestreo se maceró con nitrógeno líquido. Se pesó 0.1 g de 32 muestras seleccionadas por sintomatología y se realizó extracción de ARN total con el método modificado de Green y Sambrook (2012). Para el segundo muestreo, se realizó la extracción del ARN y ADN total por el método de CTAB 2 % (Yu, 2012; modificado por CP-LANREF, 2021). Por muestra, la concentración y pureza de los ácidos nucleicos fueron cuantificados con el NanoDrop 2000 (Thermo Fisher Scientific 2000, EUA).
Identificación genómica de Potyvirus . Se consideró ácido nucleico de 28 y 18 muestras del primer y segundo muestreo respectivamente. Se emplearon los iniciadores universales NIb2F y NIb3R (Cuadro 1) que amplifican parcialmente la región codificadora del genoma del género Potyvirus (350 pb) para la proteína B de inclusión nuclear (NIb) (Zheng et al., 2008). Primeramente, se realizó la síntesis de ADNc a partir de ARN total y posteriormente la RT-PCR de acuerdo con el protocolo de Gonzalez-Cruces et al. (2022). Se realizó una mezcla de reacción de pre RT-PCR con 9.75 µL de H2O libre de nucleasas, 500 nM por iniciador y 2.5 µL de ARN total, incubado a 85 °C durante 3 min. Para RT-PCR, se añadió a la reacción en pre RT-PCR una mezcla con: 2 mM de mix dNTP´s, 1X buffer-RT y 100 U de la enzima transcriptasa inversa (M-MLV-RT), todos de Promega Corp. EUA para obtener un volumen total de reacción de 25 µL. Las condiciones de RT-PCR fueron a 44 °C durante 60 min para incubación, seguido de 92 °C durante 10 min. El volumen final de reacción fue 25 µL constituido por: 12.5 µL de mix Gotaq® G2 Hot star, 500 nM de cada iniciador y 2.5 µL de ADNc. Se ejecutó un programa con desnaturalización inicial a 95 °C por 2 min y 35 ciclos con desnaturalización a 95 °C por 45 s, alineamiento a 45 °C por 45 s, extensión a 72 °C por 45 s y una extensión final a 72 °C por 5 min.
Identificación genómica de Begomovirus . Se analizó material vegetal de 17 muestras (segundo muestreo). Se utilizaron dos pares de iniciadores universales para el género Begomovirus: PBL1v2040 / PCR1c (Rojas et al., 1993) y Av494 / Ac1048 (Cuadro 1) (Wyatt y Brown, 1996). La mezcla de PCR con los iniciadores PBL1v2040 / PCR1c se realizaron con un volumen final de 25 µL: 1X de buffer GoTaq®, 0.2 mM de mix dNTP´s, 300 nM de los iniciadores PBL1v2040 PCR1c,
0.5 U de GoTaq® G2 y 2 µL de ADN. El volumen final se aforó con agua libre de nucleasas hasta obtener 25 µL. El programa incluyó desnaturalización inicial a 95 °C por 3 min y 30 ciclos con desnaturalización a 94 °C por 30 s, alineamien to a 50 °C por 30 s, extensión a 72 °C por 45 s, y una extensión final de 72 °C por 5 min. El PCR se realizó en el termociclador Arktik Thermal Cycler (Thermo Fisher Scientific). Para el caso de iniciadores AV494 / AC1048, la mezcla de PCR consistió en un volumen final de 25 µL: 15 μL de H2O, 5 μL de Buffer Green 5X, 2 μL de MgCl2 (7.5 mM), 0.5 μL de dNTPs (10 mM), 0.5 μL de cada iniciador (10 mM), 0.25 μL de GoTaq® DNA Polimerasa (U μL-1) (Promega) y 2 μL de ADN. Las condiciones de PCR incluyeron desnaturalización inicial a 95 °C por 4 min y 30 ciclos con desnaturalización a 95 °C por 1 min, alineamiento a 55 °C por 2 min, extensión a 72 °C por 60 s, y una extensión final de 72 °C por 10 min.
Identificación genómica de fitoplasmas. Se analizó material vegetal de 42 muestras (segundo muestreo). Para la primera etapa de PCR anidado se utilizaron los iniciadores P1 / P7 (Samart et al., 1996; Deng y Hiruki, 1991). La mezcla de PCR se preparó para un volumen final de 25 µL integrada por: 12 μL de H2O libre de nucleasas, 2.5 μL de Buffer 1X, 0.6 μL de MgCl2 (50 mM), 0.5 μL de dNTPs (10 mM), 2 μL de cada iniciador (10 mM), 0.4 μL de Taq DNA Polimerasa (U μL-1) (Invitrogen) y 5 μL de ADN. Se ejecutó un programa consistente en desnaturalización inicial a 95 ºC por 5 min, seguido de 35 ciclos a 95 ºC por 30 s, alineamiento a 52 ºC por 75 s, extensión a 72 ºC por 90 s y extensión final a 72 ºC por 10 min. El PCR se realizó en el termociclador T-100 (BioRad).
En la segunda etapa de PCR anidado se utilizaron los iniciadores FU5 y RU3N dirigidos a la región amplificada 16S (Lorenz et al., 1995). Los productos obtenidos en la PCR-directa se diluyeron (1:30) con agua destilada estéril y se utilizó como ADN molde con las mismas concentraciones anteriormente descritas. Se ejecutó un programa consistente en desnaturalización inicial a 94 ºC por 2 min, seguido de 40 ciclos a 94 ºC por 30 s, alineamiento a 56 ºC por 40 s, extensión a 72 ºC por 90 s y extensión final a 72 ºC por 5 min. El PCR se realizó en el termociclador T-100 (BioRad). El producto de PCR se analizó por electroforesis en gel de agarosa
1.5 % teñido con bromuro de etidio y se visualizó con luz UV en fotodocumentador (UVP, Biolmaging Systems, Epi Chemi II Darkroom).
Análisis epidemiológico
Muestreo y evaluación. Por cuadrante, se seleccionaron 3/9 subcuadrantes como unidades de muestreo para evaluar variables de intensidad de daño y ocurrencia de adultos de Macrodactylus sp. (Coleoptera: Scarabaeidae) como posible agente dispersor de presuntiva cenicilla en estructuras florales. La selección de subcuadrantes se hizo mediante un método aleatorio con MS Excel Aleatoriza v1.0 (CP-LANREF, 2022. No publicado) (Figura 1A). Cada unidad de muestreo se delimitó con un marco de madera portátil de 1x1 m ubicado en el centroide del subcuadrante para acotar el área de evaluación de variables (Figura 1C-D). En unidades de muestreo con menos del 25 % de cobertura foliar, el muestreo se direccionó a otra sección del subcuadrante correspondiente.
Variables evaluadas. Se utilizó App-Monitor® v1.1 Android®, disponible en PlayStore® (CP-LANREF, 2022) para caracterizar la parcela experimental y medición de variables. Se registró coordenada geográfica, entidad federativa, municipio, localidad, nombre del cultivo, superficie, fenología, nivel de tecnificación, riego y densidad de plantación. Se configuró un muestreo de severidad de cenicilla, daño de flor y vigor de planta mediante una escala aritmética de 5-clases: 1=0 %, 2=0.0125 %, 3=25.01-50 %, 4=50.01-75 % y 5=75.01-100 % (Figura 1F-G). Adicional-mente, se contabilizó el número de adultos de Macrodactylus sp. (Figura 1H). Las evaluaciones se realizaron integrando la cobertura total de tejido vegetal visible acotado al marco de muestreo, independiente del número de plantas.
Análisis geoespacial. Los registros en App-Monitor®v1.1, se exportaron en MS Excel®. La matriz de datos se estructuró en formato espacial de tipo: X = filas (cuadrante-i), Y = columnas (subcuadrante-j) y Z = variables-k para análisis espacial geoestadístico en Golden Surfer® v10. Para generar un valor por cuadrante, a partir de los tres subcuadrantes evaluados, se seleccionó el máximo obtenido con la escala aritmética de 5-clases para severidad de cenicilla, daño de flor y vigor de planta. Para Macrodactylus sp., se obtuvo el acumulado de insectos por cuadrante. El análisis geoestadístico por variable se realizó con el método Kriging representado en mapas de contornos. La dependencia y autocorrelación espacial se calculó mediante variogramas omnidireccionales (360°) ajustados a un modelo esférico. Se obtuvieron los indicadores variográficos lag-distance y sill o meseta (σ2-s) para determinar la dependencia espacial a nivel parcela (Gonzalez-Cruces et al., 2021).
Resultados y Discusión
Identificación morfológica y génica del hongo. Los síntomas observados en campo consistieron en manchas irregulares de aspecto blanco polvoso sobre el haz foliar, principalmente en hojas del estrato medio y bajo de la planta. En síntomas avanzados se identificaron manchas de color amarillento. En hojas jóvenes, se observó una ligera distorsión y reducción de área foliar debido a mayor abundancia del hongo. En flores se presentó ligera distorsión foliar y manchas blanquecinas en ausencia del aspecto polvoso. También se observó presencia abundante de Macrodactylus sp., principalmente en la flor. Esta es una plaga de algunos cultivos como el maíz y frijol (Aragón et al., 2021), por lo que potencialmente podría ser un dispersor fungoso debido a sus hábitos alimenticios y movilidad.
En microscopio compuesto se confirmó que el aspecto polvoso correspondió a signos del hongo representado por conidios, conidióforos e hifas (Figura 2A-C). En flor no se logró obtener estructuras fungosas. Los conidióforos fueron cilíndricos y erectos, con célula basal recta o ligeramente curva seguidas por dos células apicales más cortas. Exhibieron conidiogénesis tipo Pseudoidium (maduración de conidios asincrónica, uno a la vez) (Figura 2B-C). Conidios hialinos, ovoides a elipsoides de 31.74 ± 0.3419 µm x 15.11 ± 0.1579 µm sin presencia de cuerpos de fibrosina (Figura 2A-E). Tubos germinativos con longitud de 1-2 veces el largo de los conidios, con desarrollo terminal o subterminal y ápices lobulados (Figura 2D-E). De acuerdo a las características morfológicas se determinó que el hongo pertenece al género Erysiphe (Bradshaw et al., 2020; Tovar-Pedraza et al., 2018; Takamatsu, 2014; Cook y Braun, 2009; Glawe, 2008). No se observaron estructuras sexuales. Electroforesis en gel de agarosa confirmó la amplificación de la región espaciadora interna transcrita (ITS) del ADN ribosómico nuclear (~500 pb) de cinco muestras de ADN del hongo, así como ADN de controles positivos de PCR pertenecientes a los géneros Alternaria y Fusarium (Figura 2G). Cuatro secuencias tuvieron la calidad para análisis comparativo con acervos del GenBank mediante BLASTn. Este análisis permitió confirmar al género y determinar que el agente causal de cenilla en frijol Ayocote fue Erysiphe vignae con porcentaje de homología del 100 % (evalue = 0). Las secuencias fueron registradas en GenBank con números de accesión OQ448664 (FAC6), OQ448665 (FAC7), Q448666 (FAC8), y OQ448667 (FAC9).
Asimismo, con una confiabilidad del 94 %, las cuatro secuencias se agruparon con dos secuencias pertenecientes a Erysiphe vignae (MW293895, MT628286) asociadas a Vigna radiata (Fabaceae) de Australia (Figura 2H). Los resultados morfológicos y genómicos de este estudio fueron consistentes con las características reportadas para esta especie por Kelly et al. (2021) y Deng et al. (2022).
Además de reportes de E. vignae infectando Vigna radiata (Kelly et al., 2021), se ha consignado en otras fabáceas como en frijol negro (V. mungo) en Austra lia, espelón (V. unguiculata) en Brasil, y en frijol común (Phaseolus vulgaris) en Sudamérica y China (Deng et al., 2022; Kelly et al., 2021). En Sinaloa, México, se ha reportado a E. diffusa como agente causal de la cenicilla en frijol común con incidencias de hasta el 10 % del área sembrada (Félix-Gastélum et al., 2017; FélixGastélum et al., 2011). Sin embargo, no existen reportes de E. vignae afectando a fabáceas en México (Schoch et al., 2020). Por lo anterior, este trabajo representa el primer reporte de E. vignae asociado al frijol Ayocote (Phaseolus coccineus) en condiciones del Altiplano central mexicano. Este género, y en general los Erysiphales, son parásitos obligados con relativa especificidad de hospedero (Deng et al., 2022; Félix-Gastélum et al., 2017), por lo que puede ser asumido que la asociación hongo-planta es indicativo de causalidad. No obstante, estudios etiológicos formales deben ser conducidos en el futuro para determinar la patogénesis y para evaluar
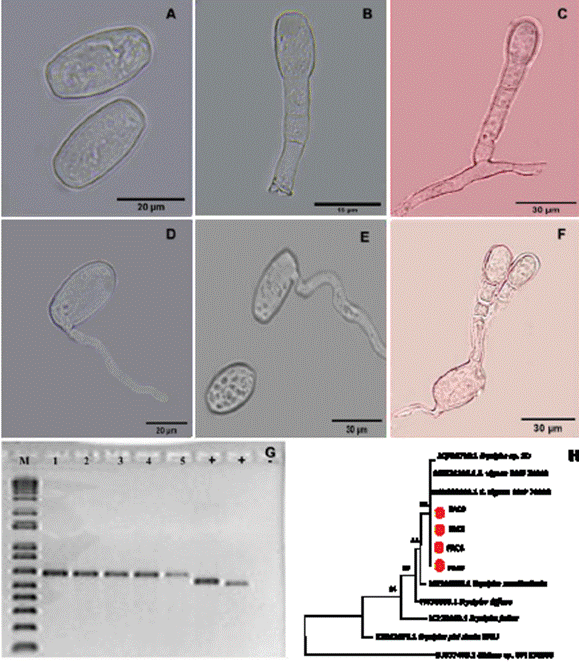
Figura 2 Identificación morfológica y genómica de la cenicilla en frijol Ayocote (Phaseolus coccineus). A. conidios hialinos, ovoides a elipsoides; B-C. conidióforos cilíndricos y erectos; D-F. conidios en germinación; G. Amplificación de la región espaciadora interna transcrita (ITS) del ADN ribosómico nuclear (~500 pb) de cinco muestras de ADN de cenicilla (1-5), dos controles positivos de PCR (+) pertenecientes a la región ITS del género Alternaria y Fusarium, marcador de peso molecular (M) de 1 kb plus Invitrogen y control negativo de PCR (-); H. árbol filogenético realizado por Máxima verosimilitud (ML) y el modelo de sustitución Hasegawa-Kishino-Yano con 1000 replicaciones Bootstrap, basado en la región ITS de secuencias de hongos pertenecientes al género Erysiphe (Cuadro 2). Las secuencias de estudio son: FAC6, FAC7, FAC8 y FAC9 (punto rojo). Se incluyó a Oidium sp. (número de accesión: EU377475) como grupo externo.
el comportamiento de acervos de P. coccineus a la infección del hongo, análogo a trabajos con frijol común (Deng et al., 2022).
El frijol Ayocote ha sido reconocido en general por su resistencia y tolerancia a plagas, enfermedades y al frio (Chiquito-Almanza et al., 2021; 2018; Schwember et al., 2017; Vargas et al., 2014; Giurca, 2009; Osorno et al., 2007; Schwartz et al., 2006). Por ejemplo, Ruíz-Salazar y colaboradores (2019) resaltan que el frijol Ayocote presenta resistencia al tizón común (Xanthomonas axonopodis pv. phaseoli) y antracnosis (Colletotrichum lindemutianum). Sin embargo, en ningún trabajo se reporta E. vignae. La cenicilla, causada por otras especies de Erysiphe, es un factor limitante del rendimiento en algunas regiones productoras de frijol común a nivel mundial y puede causar hasta 69 % de pérdidas (Deng et al., 2022; Félix-Gastélum et al., 2017).
Identificación genómica de virus y fitoplasmas. Con los iniciadores universales empleados (Zheng et al., 2008), no se detectó la presencia de Potyvirus en un total de 46 foliolos con síntomas de mosaico, amarillamiento, deformación foliar y aclaramiento de nervaduras (Figura 1D, F). Similarmente, con dos pares de iniciadores universales (Wyatt y Brown, 1996; Rojas et al., 1993), no se detectó al género Begomovirus en 17 muestras con síntomas de amarillamiento generalizado y ligera deformación (Figura 1E). En frijol común, ambos géneros se han reportado en México por lo que fueron enfatizados en este estudio y por coincidencia de algunos centros de origen y cultivación entre éste y el Ayocote (Mora-Aguilera et al., 2023). En particular, el muestreo se incrementó para Potyvirus por la mayor prevalencia del Bean common mosaic virus, posiblemente por su aptitud de transmisión por semilla y por varias especies de áfidos (Hemitera: Aphididade) (Gonzalez-Cruces et al., 2022; Chiquito-Almanza et al., 2021). La ocurrencia de Begomovirus, i.e. Bean golden yellow mosaic virus, ha declinado a partir de los 90’s cuando tuvo impacto epidémico en frijol (Chiquito-Almanza et al., 2021; Rojas et al., 1993). En frijol común se ha reportado a nivel mundial 23 especies virales pertenecientes a nueve géneros (Potyvirus, Comovirus Nepovirus, Sobemovirus, Alfamovirus, Cucumovirus, Tobamovirus, Begomovirus y Curtovirus), predominando 11 especies del género Potyvirus como principales enfermedades virales en frijol (Meziadi et al., 2017). En frijol Ayocote existen escasos estudios etiológicos virales en México (Chiquito-Almanza et al., 2021; 2018). Osorno y colaboradores (2007) sugieren que P. coccineus exhibe resistencia al Bean golden yellow mosaic virus, debido a dos genes. Un gen recesivo, que confiere resistencia a clorosis foliar y un gen dominante que evita la deformación de vainas infectadas con el virus. Sin embargo, el Cowpea mild mottle virus (Betaflexiviridae: Carlavirus), con Bemisia tabaci (Hemitera: Aleyrodidae) como vector, se ha reportado en Jalisco y Nayarit en condición sintomática (lesiones cloróticas, moteado severo y moderado, moderado mosaico y deformación foliar) y asintomática (Chiquito-Almanza et al., 2018). Ese virus no fue analizado en este estudio por lo que se debe considerar en el futuro. No obstante, los resultados de este trabajo y otros sugieren la tolerancia y/o resistencia de P. coccineus a patógenos virales. Por ejemplo, en un estudio regional al occidente de México se determinó que la incidencia de plantas con síntomas virales en esta especie fue menor al 20 %, consignándose únicamente al Cowpea mild mottle virus, mientras que en frijol común superó el 97 % asociado al menos a 1/9 especies de un total de cinco géneros de virus identificados (Chiquito-Almanza et al., 2021).
El diagnóstico para fitoplasma también resultó negativo en 42 muestras analizadas con iniciadores universales y PCR anidado (Samart et al., 1996; Lorenz et al., 1995; Deng y Hiruki, 1991). Este análisis se repitió varias veces, con ajuste del protocolo PCR y remuestreo en campo, debido a los síntomas observados, en general asociados con estos organismos. Estos incluyeron deformación foliar, coloración café o violeta, con evidente coloración violácea en nervaduras del envés de hojas más jóvenes, achaparramiento y acortamiento de entrenudos, ligero amarillamiento en hojas del estrato medio, y aborto y/o retraso de emisión floral (Figura 3A-B). Sin embargo, la electroforesis en gel de agarosa para los productos PCR obtenidos sólo mostró bandas del testigo positivo (Figura 3C). Actualmente, solo se ha reportado a ‘Candidatus Phytoplasma asteris’ en las fabáceas Macroptilium lathyroides (Alves et al., 2018) y Crotalaria juncea (Bianco et al., 2014), con síntomas de reducción foliar, amarillamiento y atrofia. Así mismo, se ha reportado a las chicharritas Empoasca kraemeri, E. fabae y E. papayae (Hemiptera: Cicadellidae) asociados a un complejo de síntomas de tipo viral y fitoplásmico en frijol común (LozanoGutiérrez et al., 2017; Sánchez-Castro et al., 2016).
En este trabajo se detectó presencia de adultos de chicharritas, pero no se procedió a su identificación. Esto sugiere la necesidad de investigaciones futuras para descartar la presencia de fitoplasma(s) en frijol Ayocote con empleo de mayor número de unidades productivas y muestras vegetales, y establecer la asociación de estos mollicutes en potenciales insectos vectores. La relevancia principal, más que productiva, podría ser en el empleo de P. coccineus como eventual fuente de resistencia en estudios de mejoramiento con frijol común, lo cual requiere una completa caracterización fitosanitaria en esta especie.
Análisis geoespacial. El análisis geoestadístico por el método Kriging y variogramas omnidireccionales de inductividad epidémica de la cenicilla, daño en flor, densidad de frailecillo y vigor de planta evidenciaron claramente la alta capacidad infectiva de la cenicilla (E. vignae), en frijol Ayocote considerando que los presuntivos síntomas virales y fitoplásmicos no fueron etiológicamente confirmados (Figura 4A-C). La incidencia de cenicilla fue 65.3 % (unidad subcuadrante) con severidad promedio de 22.7 % (±16.9, rango: 0 - 66.5 %). Estos niveles de daño son moderados a altos por lo que E. vignae debe considerarse un patógeno de alto riesgo para P. coccineus.

Figura 3 Síntomas en campo presuntivos a infección por fitoplasma en frijol Ayocote (Phaseolus coccineus). A. Síntomas putativos a fitoplasmas. Incluye deformación foliar, coloración café o violeta, con evidente coloración violáceas en nervaduras del envés de hojas jóvenes, achaparramiento, ligero amarillamiento foliar B. Ejemplo de seis hojas trifoliadas con síntomas presuntivos a fitoplasmas incluidas en diagnóstico PCR; C. Electroforesis en gel de agarosa de 24 muestras procesadas por PCR anidado. Únicamente los testigos positivos amplificaron por PCR.
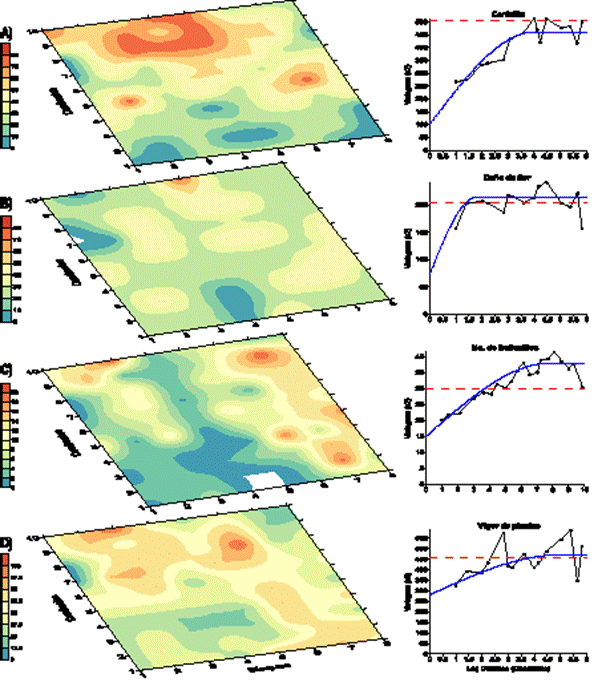
Figura 4 Mapas de contorno geoestadístico Kriging y variogramas gráficos de variables fitosanitarias y vigor en frijol Ayocote. A. Severidad de cenicilla, B. Daño en flor, C. Densidad de frailecillo (Macrodactylus sp.) y, D. Vigor de planta. Para el análisis de frailecillos se obtuvo la suma de tres subcuadrantes analizados por cuadrante. Para el análisis de severidad de cenicilla, daño de flor, y vigor de planta se consideró el daño máximo obtenido por cuadrante. Variogramas omnidireccionales se obtuvieron por el método esférico. Eje X = lag de distancia en cuadrantes y Y = la varianza (σ2).
El contagio de la cenicilla exhibió un patrón de agregados con dependencia espacial máxima de cuatro cuadrantes en el foco principal (96 m2, lag = 4 y σ2-s =450) y de 1-2 cuadrantes en los focos secundarios (48 m2, lag = 2 y σ2-s= 350, Figura 4A). El foco principal, exhibido por la continuidad del color rojo de la escala de daño, tuvo un rango de severidad 60 - 80 % y un marcado efecto de orilla asociado al mayor porcentaje de vigor de planta (entre 50-75 %) (Figura 4D). Esta aseveración se evidencia con la coincidencia en general de los contornos colorimétricos de mayor valor en la escala entre los cuadrantes (c) 6-10 y bloques (b) 2-6 (Figura 4A y 4D). Esto concuerda con la naturaleza foliar infecciosa de estos hongos, los cuales garantizan la reinfección a mayor biomasa ya que esta favorece condiciones microclimáticas aptas para el patógeno como la posibilidad de reducir la exposición directa a luz solar la cual inhibe la germinación de esporas (Craig y Weyne, 2012; Hückelhoven y Panstruga, 2011). En este trabajo, la cenicilla en campo se presentó con una temperatura y humedad relativa promedio (julio-agosto) de 16.3°C (±5.8) y 92.8 % (±10.7), respectivamente. La dependencia espacial direccional, y la forma de los agregados; sin embargo, también validó el efecto de vientos dominantes Norte-Sur para la conformación de gradientes. Es también conocida la alta aptitud epidemiológica de los Erysiphales debido a la abundante producción intermitente de conidios con fácil liberación y dispersión aérea (Deng et al., 2022; Glawe, 2008). La heterogeneidad del vigor en planta, quizás debido al segundo año de cultivación o la plasticidad fenotípica (Vargas et al., 2014), explicó la conformación de agregados diferenciados de vigor y la identificación de dependencia espacial (lag = 4 y σ2-s = 470) (Figura 4D). Epidemiológicamente, el daño de flor no fue conclusivo en su asociación con la incidencia de cenicilla. Esto concordó con la ausencia de signos a nivel microscópico. Espacialmente, este daño tuvo una distribución aleatoria de focos moderados con dependencia de 1-2 cuadrantes y 30- 40 % severidad (lag = 1.5 y σ2-s = 250) (Figura 4B). La ausencia de correspondencia colorimétrica de este mapa de contorno con el de cenicilla foliar (Figura 4A) sugiere que estos eventos no están infecciosamente correlacionados.
Análogamente, la densidad espacial de adultos de Macrodactylus sp., aunque fue heterogénea y se observaron dos grandes agregados principales, entre 1-10 c y 6-8 b, y entre 5-10 c y 1-3 b, con uno y cuatro focos (> 18 insectos/centroide), respectivamente (Figura 4C), tampoco se asoció con el mapa de contorno de dispersión de daño en flor, o de cenicilla en hoja, como se hipotetizó originalmente. No se detectó daño por alimentación del insecto en flores, órgano donde se le detectó con mayor prevalencia (Figura 1H). Su rol como posible polinizador, importante en P. coccineus, no fue evaluado. Se ha reportado que Macrodactylus sp. en etapas adultas pueden alimentarse de flores, frutos, granos de polen y secreciones de savia dulce de diversos cultivos como maíz y frijol común (Aragón et al., 2021). La implicación del frailecillo en la dispersión de E. vignae no puede considerarse concluyente. Para ese fin, es necesario conducir estudios espacio-temporales extensivos.
Conclusiones
El patógeno asociado a cenicilla en Phaseolus coccineus fue Erysiphe vignae (Erysiphales: Erysiphacea). Este representa el primer reporte en frijol Ayocote en México. La cenicilla exhibió incidencia del 65.3 % y severidad promedio de 22.7 % (±16.9, rango: 0 - 66.5 %). Estos niveles de daño son moderados a altos por lo que E. vignae debe considerarse un patógeno de riesgo para P. coccineus. El patrón agregado de contagio de E. vignae estuvo asociado con vigor de planta y direccionalidad de vientos dominantes. Este patrón no se relacionó con otros daños como manchas blanquecinas en flores y ocurrencia de Macrodactylus (Coleoptera: Scarabaeidae). E. vignae podría también ser de riesgo para frijol común (P. vulgaris) en México ya que no se ha reportado. No se detectaron especies del género Potyvirus y Begomovirus, ni mollicutes de tipo fitoplasma asociados a síntomas de amarillamiento, distorsión foliar, mosaico moderado, acortamiento de entrenudos y coloración morada foliar y de tallo lo que valida la tolerancia/resistencia reportada en general para P. coccineus. La importancia potencial alimenticia del frijol Ayocote, y su aplicabilidad en programas de resistencia, obliga a incentivar investigaciones etiológico-epidemiológicas en P. coccineus.















