Introducción
El borrego cimarrón (Ovis canadensis Shaw) es un herbívoro rumiante de la familia Bovidae que participa en la dinámica de la vegetación y el ciclo de nutrientes en los matorrales desérticos del norte de México (Tarango et al., 2002; Gastelum-Mendoza et al., 2021). Es la especie cinegética de mayor valor económico en México, lo que impulsa el desarrollo de la economía rural y la conservación de su hábitat (Lee, 2011; Lee et al., 2012). Existen tres subespecies en México: O. c. cremnobates y O. c. weemsi en la península de Baja California, y O. c. mexicana en Sonora (Sandoval et al., 2019). Sin embargo, la caza no regulada, la fragmentación del hábitat y la transmisión de enfermedades por el ganado doméstico, provocaron la desaparición de sus poblaciones en los estados mexicanos de Chihuahua, Coahuila, Nuevo León y Tamaulipas a finales del siglo XIX (Lee & Mellink, 1996; Krausman, 2000). Para la década de 1970, el borrego cimarrón había sido extirpado de Coahuila (Sánchez, 2005) y Chihuahua (Heffelfinger & Márquez-Muñoz, 2005).
En respuesta, autoridades y propietarios de predios han implementado proyectos de reintroducción del borrego cimarrón en Norteamérica (Taylor et al., 2017). La primera translocación de borregos ocurrió en 1954 en Texas, Estados Unidos de América, mediante la colaboración entre agencias estadounidenses y mexicanas (Whiting et al., 2023). Desde 1998, más de 200 borregos han sido translocados desde la Isla Tiburón, Sonora, hacia los matorrales desérticos de Coahuila y Chihuahua, principalmente (Uranga-Thomas, 2001; Gobierno del Estado de Chihuahua, 2007; Gobierno del Estado de Coahuila de Zaragoza, 2008). El incremento de las poblaciones del borrego berberisco (Ammotragus lervia Pallas), una especie exótica invasora originaria del norte de África, representa un desafío para la reintroducción del borrego cimarrón, debido a su potencial competencia directa por espacio y recursos alimenticios (Sánchez, 2005; Gastelum-Mendoza et al., 2023). La Unidad de Manejo para la Conservación de la Vida Silvestre (UMA) Rancho San Juan (clave de registro SEMARNAT DGVS-CR-EX-3133-COA) ha realizado esfuerzos para reintroducir al borrego cimarrón en su hábitat natural dentro del matorral desértico rosetófilo en la región este de Coahuila. Los proyectos de reintroducción del borrego cimarrón deben incorporar, dentro de sus fases de planificación y monitoreo poblacional, la evaluación de los cambios en la estructura y composición del matorral desértico rosetófilo antes y después de la liberación de los individuos (Whiting et al., 2023). Estos factores son fundamentales para el establecimiento y la dinámica de las poblaciones de borrego cimarrón, ya que inciden directamente en la capacidad de carga, entendida como el número máximo de individuos que el hábitat puede sostener sin afectar su equilibrio y funcionalidad a mediano plazo (Holechek et al., 2001). Aunque los matorrales xerófilos constituyen el tipo de vegetación mejor representado en el norte de México (Rzedowski, 1978), el matorral desértico rosetófilo es el subtipo menos estudiado, en comparación con otros tipos de matorrales desérticos (Jiménez-Pérez et al., 2013). En México, no existen estudios que evalúen la capacidad de carga del matorral desértico rosetófilo en las zonas donde se manejan y reintroducen poblaciones silvestres de borrego cimarrón, como un aspecto importante en el diseño e implementación de estrategias de conservación eficientes del hábitat. Por lo anterior, el objetivo del presente estudio fue estimar la composición y diversidad del matorral desértico rosetófilo, así como la producción estacional de forraje disponible para el borrego cimarrón, con el fin de evaluar la capacidad de carga del hábitat. Estos resultados proporcionan una base científica para formular recomendaciones de manejo adecuadas para el restablecimiento de las poblaciones de borrego cimarrón y la conservación de su hábitat en el estado de Coahuila.
Materiales y métodos
Área de estudio. El estudio se realizó en la UMA Rancho San Juan, ubicada a 40 km al este del municipio de Monclova, Coahuila, México (Fig. 1). Dentro de la UMA, se delimitaron dos áreas de estudio: 1) una reserva destinada al manejo del borrego cimarrón, con una superficie aproximada de 450 ha (en adelante, “la reserva”); y 2) Sierra Las Hormigas, un área cercada de aproximadamente 650 ha, destinada a confinar una población de borrego berberisco (Fig. 2). El tipo de vegetación predominante es el matorral desértico rosetófilo, y en menor proporción, el matorral desértico micrófilo (Fig. 1). Las especies vegetales más representativas incluyen lechuguilla (Agave lechuguilla Torr.), guapilla (Hechtia glomerata Zucc.), candelilla (Euphorbia antisyphilitica Zucc.) y huizache (Vachellia farnesiana L.). El clima de la región es semiárido (BS), con una temperatura media anual de 21 °C, alcanzando más de 40 °C en verano y descendiendo por debajo de 0 °C en invierno (García, 1988). La precipitación anual varía entre 200 y 900 mm.
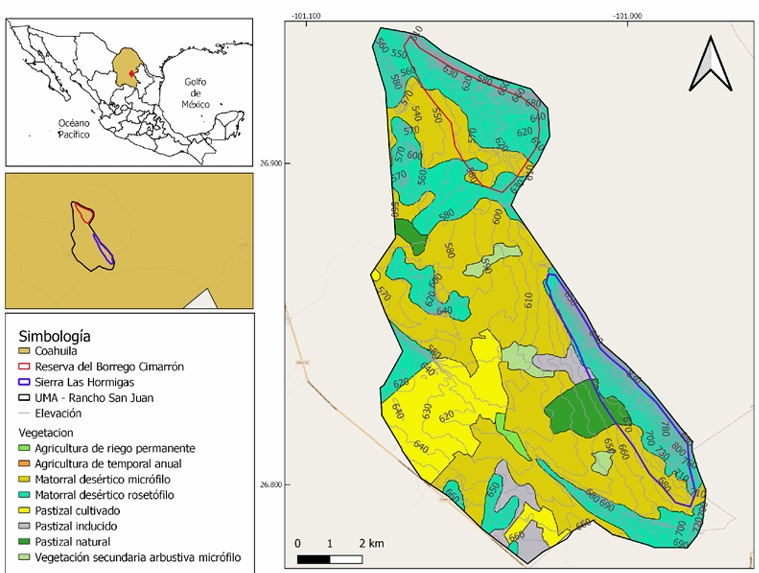
Figura 1 Ubicación, tipo de vegetación y rango de elevación de los sitios de estudio en la UMA Rancho San Juan.
Composición y diversidad vegetal. Se estimó la composición y diversidad del matorral desértico rosetófilo en las dos áreas de estudio utilizando el método de intersección de línea, según la técnica de Canfield (1941), durante las cuatro estaciones del año: otoño (octubre de 2018), invierno (febrero de 2019), primavera (mayo de 2019) y verano (agosto de 2019). Este método consiste en registrar la altura y la cobertura de cada especie vegetal que intercepte las líneas de muestreo. Se establecieron de forma aleatoria 18 líneas permanentes de 25 m de longitud, mientras que, en Sierra Las Hormigas se instalaron 23 líneas de la misma longitud. El número de líneas se determinó con base en un pre-muestreo realizado en agosto de 2018, que consistió en ocho líneas de 25 m de longitud por sitio de estudio. A partir de este muestreo, se estimó el número potencial de especies por sitio utilizando los estimadores no paramétricos Jackknife (Efron, 1992) y Chao 1 (Chao & Lee, 1992). Los resultados de este análisis se utilizaron para calcular el tamaño de muestra (número de líneas de 25 m de longitud) para una población finita (N). Las especies registradas en cada línea se clasificaron según su altura y forma biológica en cuatro grupos: arbóreas y arbustivas, herbáceas, pastos y suculentas. El método de intersección de línea de Canfield se utilizó para estimar el Índice de Valor de Importancia (IVI) de cada especie. Este índice se obtiene sumando los valores relativos de abundancia (Ar), frecuencia (Fr) y dominancia (Dr), lo que permite integrar tanto la diversidad como la composición de la vegetación en un valor porcentual (Curtis & McIntosh, 1951). La diversidad vegetal estacional en la Reserva y en Sierra Las Hormigas se estimó utilizando varios índices.
La riqueza potencial de especies se estimó mediante el índice de Margalef (1958), con la siguiente ecuación:
Donde: S es el número total de especies presentes, y N , es el número total de individuos.
La dominancia de especies se calculó utilizando el índice de Simpson (1949), de acuerdo con la siguiente ecuación:
Donde: ni , es el número de individuos de cada especie; y N , es el número total de individuos en la muestra. Cuanto mayor sea el valor de D , menor será la diversidad, y se expresa como la probabilidad de que dos individuos seleccionados al azar pertenezcan a la misma especie. Este índice varía entre 0 y 1, siendo inversamente proporcional a la diversidad: valores cercanos a 1 indican una mayor dominancia de ciertas especies y, por lo tanto, menor diversidad.
La diversidad alfa (α) se estimó por sitio y estación del año utilizando el índice de Shannon (1948), considerando la siguiente formula:
Donde: S , es el número de especies (riqueza de especies); pi , proporción de individuos de la especie i respecto al total de individuos; ni , es el número de individuos de la especie i ; y N , es el número de todos los individuos de todas las especies.
Por último, se aplicó la prueba no paramétrica de Kruskal-Wallis (α ≤ 0.05) para evaluar las diferencias en la diversidad, dominancia y riqueza de especies entre los sitios y estaciones del año.
Producción de biomasa y capacidad de carga. La producción estacional de biomasa se expresó en kg ha-1 de materia seca, clasificada por estrato vegetal: alto (especies con altura mayor a 1.5 m), medio (especies con altura menor a 1.5 m) y bajo (pastos y herbáceas) (Fulbright & Ortega, 2006). Para ello, se empleó el método de Adelaide (Foroughbakhch et al., 2005). La evaluación de la producción de biomasa en el estrato alto y medio se realizó colocando 18 parcelas de 50 m² y 25 m², respectivamente, a lo largo de las líneas de Canfield. En cada parcela se tomó una unidad de referencia, consistente en una muestra vegetal representativa (en forma y densidad foliar) de cada especie presente en las parcelas. Con esta unidad de referencia se estimó el número de unidades por individuo y por especie muestreada. Para el estrato bajo, se efectuó la corta total en 18 parcelas de 1 m² (Chávez, 2000). Las muestras de biomasa de pastos, herbáceas y las unidades de referencia fueron colocadas en bolsas de papel, etiquetadas y secadas en horno INOX (120VAC, 60HZ) a 75°C hasta alcanzar un peso constante. Posteriormente, las muestras se pesaron en una balanza ENTRIS 8201-1S para obtener el peso seco. Una vez obtenido el peso seco, se multiplicó por cada una de las repeticiones presentes en cada planta para obtener un valor de producción en kg ha-1. Las diferencias en la producción de biomasa por sitio y estación se calcularon mediante la prueba no paramétrica de Kruskal-Wallis (α ≤ 0.05), utilizando la plataforma R Studio (RStudio Team, 2016). La capacidad de carga (K) se expresó en número de hectáreas por borrego cimarrón y se estimó para cada estación del año de acuerdo con el modelo descrito por Holechek et al. (2001):
Donde: Pv, el peso vivo del animal; Cdms, es el consumo diario de materia seca (3 % de Pv); Cp , el ciclo de pastoreo (365 días); 0.25, es el porcentaje de uso permitido del forraje; y Pms , es la producción de materia seca (kg ha-1).
Resultados
En la reserva, se identificaron 42 especies vegetales en las cuatro estaciones del año, representadas por 17 familias taxonómicas. Las más importantes fueron Asteraceae (7 spp.), Fabaceae (5 spp.) y Poaceae (5 spp.); 26 de las 42 especies fueron árboles y arbustos, y solo tres fueron herbáceas. De acuerdo con el IVI promedio anual, las especies más importantes fueron: A. lechuguilla (12.35 ± 3.8 %), E. antisyphilitica (11.44 ± 5.84 %), Lippia graveolens (Kunth; 9.67 ± 19.37 %), Jatropha dioica (Sessé; 6.55 ± 6.15 %) y Opuntia microdasys ((Lehm.) Pfeiff.; 6.28 ± 3.68 %; Cuadro 1). Además, se consideraron 18 especies dominantes, ya que estuvieron disponibles durante todo el año (Fig. 3). En Sierra Las Hormigas, la cobertura vegetal se constituyó por 50 especies de plantas, de las cuales 31 fueron árboles y arbustos, nueve suculentas, cinco hierbas y cinco pastos. De las 22 familias taxonómicas, las más comunes fueron Fabaceae (9 spp.), Asteraceae (5 spp.), Poaceae (5 spp.) y Asparagaceae (4 spp.). En relación con el IVI, tres especies fueron las más importantes: H. glomerata (49.7 ± 4.92 %), A. lechuguilla (48.74 ± 9.23 %) y E. antisyphilitica (45.81 ± 7.86 %). Al igual que en la reserva, se identificaron 18 especies dominantes (Fig. 3). La diversidad vegetal fue diferente en función del sitio y la estación del año (p ≤ 0.05). En particular, los índices de riqueza y diversidad de especies en la Reserva fueron mayores en otoño (p ≤ 0.05), mientras que la dominancia se mantuvo constante durante todo el año. En el caso de Sierra Las Hormigas, la riqueza de especies fue mayor en invierno (p ≤ 0.05), la dominancia se mantuvo constante y la diversidad aumentó en invierno (p ≤ 0.05; Cuadro 2).
Cuadro 1 Variaciones estacionales del Índice de Valor de Importancia (IVI) del matorral desértico rosetófilo de acuerdo con el sitio de estudio y la estación del año en la UMA Rancho San Juan, municipio de Monclova, Coahuila, México.
| Especie | Primavera (%) | Verano (%) | Otoño (%) | Invierno (%) |
| Reserva | ||||
| Agave lechuguilla | 12.79 | 11.25 | 13.93 | 11.41 |
| Cenchrus ciliaris | 3.50 | 4.77 | 1.47 | 4.41 |
| Euphorbia antisyphilitica | 12.08 | 9.05 | 10.96 | 13.68 |
| Eysenhardtia texana | 3.10 | 3.32 | 2.97 | 1.53 |
| Forestiera angustifolia | 2.75 | 1.61 | 0.28 | 0.56 |
| Gochnatia hypoleuca | 4.04 | 1.73 | 1.25 | 1.47 |
| Guaiacum angustifolium | 1.02 | 0.59 | 1.44 | 1.18 |
| Hechtia glomerata | 4.56 | 4.30 | 4.49 | 4.12 |
| Jatropha dioica | 9.02 | 7.23 | 4.24 | 5.71 |
| Karwinskia humboldtiana | 0.98 | 1.28 | 1.07 | 2.97 |
| Larrea tridentata | 0.93 | 0.29 | 0.49 | 0.30 |
| Opuntia engelmannii | 3.53 | 5.90 | 2.13 | 3.29 |
| Opuntia leptocaulis | 1.58 | 1.12 | 1.37 | 0.24 |
| Opuntia microdasys | 7.98 | 5.06 | 5.94 | 6.14 |
| Salvia coccinea | 3.99 | 5.79 | 2.17 | 3.79 |
| Senegalia berlandieri | 5.00 | 2.46 | 2.20 | 3.76 |
| Vachellia rigidula | 6.02 | 3.38 | 3.60 | 4.58 |
| Viguiera stenoloba | 8.53 | 3.43 | 1.79 | 4.02 |
| Sierra Las Hormigas | ||||
| Agave lechuguilla | 16.45 | 12.11 | 10.92 | 9.25 |
| Cenchrus ciliaris | 0.63 | 3.89 | 0.14 | 12.86 |
| Dasylirion berlandieri | 7.59 | 2.17 | 4.40 | 1.86 |
| Euphorbia antisyphilitica | 8.01 | 14.28 | 11.22 | 12.30 |
| Eysenhardtia texana | 0.57 | 1.48 | 1.36 | 0.59 |
| Forestiera angustifolia | 0.62 | 0.22 | 0.56 | 0.53 |
| Gochnatia hypoleuca | 2.39 | 0.23 | 1.10 | 1.03 |
| Guaiacum angustifolium | 2.85 | 1.76 | 2.43 | 1.70 |
| Hechtia glomerata | 14.13 | 13.42 | 10.56 | 11.59 |
| Jatropha dioica | 3.18 | 2.69 | 0.44 | 1.26 |
| Karwinskia humboldtiana | 4.85 | 4.26 | 3.42 | 3.80 |
| Leucophyllum frutescens | 1.48 | 1.37 | 0.59 | 0.75 |
| Opuntia engelmannii | 5.07 | 4.15 | 1.19 | 3.91 |
| Salvia coccinea | 2.47 | 2.05 | 1.03 | 1.24 |
| Senegalia berlandieri | 2.26 | 3.47 | 2.70 | 1.96 |
| Vachellia rigidula | 9.58 | 5.31 | 4.44 | 5.85 |
| Viguiera stenoloba | 1.02 | 2.32 | 4.71 | 1.97 |
| Ziziphus obtusifolia | 2.17 | 2.69 | 2.38 | 0.53 |
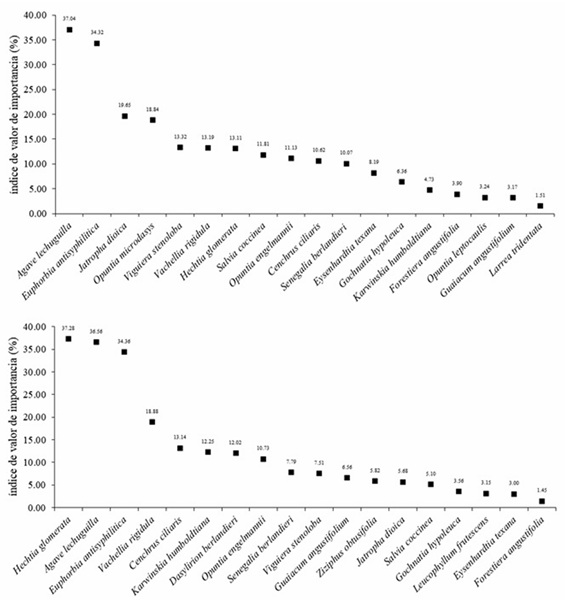
Figura 3 Especies vegetales dominantes en el matorral desértico rosetófilo, en relación con el Índice de Valor de Importancia (IVI) y el sitio de estudio en la UMA Rancho San Juan, municipio de Monclova, Coahuila, México (las líneas verticales sobre las barras indican el error estándar).
Cuadro 2 Variaciones estacionales en los índices de diversidad vegetal del matorral desértico rosetófilo de acuerdo con el sitio de estudio en la UMA Rancho San Juan, municipio de Monclova, Coahuila, México.
| Sitio | Estación 2018 - 2019 | Índice de riqueza de Margalef | Índice de dominancia de Simpson | Índice de diversidad de Shannon |
| Reserva | Primavera | 3.77 | 0.9 | 2.59 |
| Verano | 3.78 | 0.92 | 2.74 | |
| Otoño | 5.24 (p ≤ 0.05) | 0.9 | 2.76 | |
| Invierno | 4.22 | 0.9 | 2.69 | |
| Sierra Las Hormigas | Primavera | 4.01 | 0.86 | 2.42 |
| Verano | 4.18 | 0.88 | 2.55 | |
| Otoño | 4.85 | 0.89 | 2.62 | |
| Invierno | 5.08 (p ≤ 0.05) | 0.89 | 2.65 |
En cuanto a la producción de biomasa, se estimó que en la Reserva se generaron anualmente en promedio 703.89 ± 298 kg ha-1, mientras que, en Sierra Las Hormigas se registró una producción de 1,066.05 ± 337 kg ha-1. En ambos sitios de estudio, y durante las cuatro estaciones del año, el estrato medio fue el que aportó la mayor cantidad de biomasa en relación con el estrato alto y bajo (p ≤ 0.05). En la reserva, el estrato medio produjo un promedio de 545 ± 353 kg ha-1, lo que representó el 77.4 % de la producción total durante el período de estudio. En Sierra Las Hormigas, el estrato medio aportó un promedio estacional de 677 ± 406 kg ha-1, equivalente al 63.54 % de la productividad anual (Fig. 4). Sin embargo, no se encontraron diferencias en la producción anual del estrato alto entre los dos sitios. En cuanto a la productividad estacional de biomasa, se observó que durante el verano se produjeron 1,150.67 kg ha-1, lo que representó el 40.87 % de la producción anual de la reserva. Asimismo, en Sierra Las Hormigas, durante primavera y verano, la producción alcanzó los 2,704.8 kg ha-1, equivalente al 63.48 % del total anual de producción de biomasa (Fig. 4).
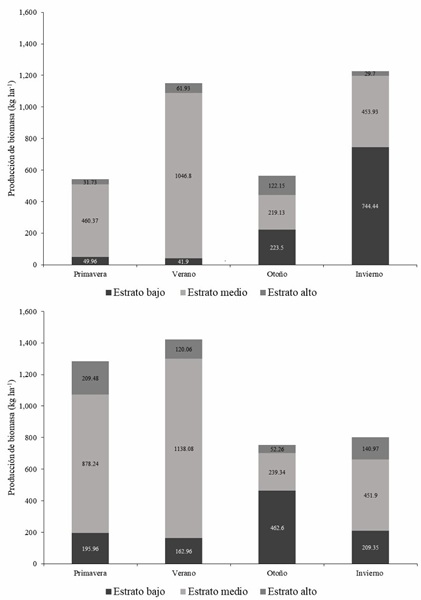
Figura 4 Variaciones en la producción de biomasa estacional en relación con el estrato vegetal y el sitio de estudio (arriba, Reserva; abajo, Sierra Las Hormigas) en la UMA Rancho San Juan, municipio de Monclova, Coahuila, México.
La producción de biomasa presentó variaciones en relación con las especies vegetales, el estrato vegetal y el sitio (Fig. 5; p ≤ 0.05). Por ejemplo, en la reserva, L. graveolens, Dasylirion berlandieri (S.Watson) y Senegalia berlandieri ((Benth.) Britton & Rose) aportaron un promedio de 139.86 kg ha-1 de biomasa en el estrato alto, representando el 57 % de la productividad total de este estrato. En el estrato medio, A. lechuguilla, E. antisyphilitica y O. microdasys produjeron un promedio anual de 1,510.76 kg ha-1, lo que representa el 69.3 % de la productividad total del estrato medio. De manera similar, en Sierra Las Hormigas, S. berlandieri y D. berlandieri generaron 259.18 kg ha-1, lo que corresponde al 50 % de la producción anual de biomasa del estrato alto. Asimismo, A. lechuguilla y E. antisyphilitica contribuyeron con 1,347.45 kg ha-1, representando la mitad de la productividad de biomasa del estrato medio. La estimación de la producción de biomasa del matorral desértico rosetófilo con base en el modelo de Holechek, se utilizó como base para calcular la capacidad de carga de la reserva, que fue de 4.67 ha por borrego, equivalente a 86 borregos en una superficie de 400 ha. En cambio, en Sierra Las Hormigas, se determinó la capacidad de carga (K) en 3.08 ha por borrego, es decir, 357 borregos en 1,100 ha. Estos datos revelan una diferencia en los valores de K, en función de la estación del año y el sitio (Cuadro 3).
Cuadro 3 Variaciones estacionales en la capacidad de carga del matorral desértico rosetófilo en relación con el sitio y la producción de biomasa en la UMA Rancho San Juan, municipio de Monclova, Coahuila, México.
| Estación 2018 - 2019 | Reserva para manejo de borrego cimarrón | Sierra Las Hormigas | ||||
| Kg ha-1 | K | Total en 400 ha | Kg ha-1 | K | Total en 1,100 ha | |
| Primavera | 542.06 | 6.06 | 66 | 1,286.68 | 2.55 | 431 |
| Verano | 1,150.61 | 2.85 | 140 | 1,421.09 | 2.3 | 476 |
| (p ≤ 0.05) | (p ≤ 0.05) | (p ≤ 0.05) | 1 | |||
| Otoño | 564.77 | 5.82 | 69 | 754.2 | 4.3 | 252 |
| 6 | ||||||
| Invierno | 558.06 | 5.89 | 68 | 802.22 | 4.0 | 269 |
| 9 | ||||||
| X̄ | 703.89 (± 298) | 467 | 86 | 1,066.05 | 3.0 | 357 |
| (± 337) | 8 | |||||
Discusión
La riqueza de especies de los dos sitios de estudio fue menor en comparación con lo reportado por Alanís-Rodríguez et al. (2015), quienes registraron en una mayor superficie de muestreo en el estado de Nuevo León, solo 35 especies, una riqueza inferior a la del presente trabajo (42 y 50 spp., respectivamente) Sin embargo, la riqueza fue similar a lo que documentaron Molina-Guerra et al. (2017) en el municipio de Arteaga, Coahuila. Para el borrego cimarrón, la cobertura vegetal de arbustos perennes es una de las variables principales que determinan la estructura de su hábitat ideal (Stephens et al., 2009; Fig. 2). Este componente es clave en la evaluación de la calidad del hábitat, ya que está relacionado con el terreno de escape, es decir, áreas en las que los borregos pueden detectar y escapar de sus depredadores (Krausman et al., 1989; Wakeling & Miller, 1989). Por esta razón, el borrego prefiere áreas abiertas con vegetación baja, lo cual le proporciona alta visibilidad y facilita el establecimiento de rutas de escape (Krausman et al., 1989). En este contexto, la composición vegetal del matorral desempeña un papel fundamental al ofrecer cobertura para protección y forraje, además de visibilidad, un aspecto esencial en su estrategia de evasión de depredadores (Krausman & Leopold, 1986). La dominancia y la importancia ecológica de arbustos bajos (menos de 1.5 m de altura), como A. lechuguilla, E. antisyphilitica, L. graveolens y J. dioica, presentes en la Reserva y en la Sierra Las Hormigas (Fig. 3), proveen la estructura del hábitat necesaria para el desarrollo de las poblaciones de borrego cimarrón. Aunque el terreno de escape resulta de la combinación de los atributos de la cobertura vegetal y la topografía, en México, la mayoría de los estudios se han centrado en describir el uso y selección de variables topográficas por el borrego cimarrón (Álvarez-Cárdenas et al., 2009; Ruíz-Mondragón et al., 2018). Sin embargo, aún no se han realizado investigaciones que detallen la composición y estructura de la cobertura vegetal como un componente clave del hábitat, fundamental en su estrategia de supervivencia y en los proyectos de reintroducción de esta especie en el noreste de México. Un análisis preliminar sugiere que la Sierra Las Hormigas presenta los elementos estructurales esenciales, como pendientes y características orográficas, así como una cobertura vegetal favorable para el sostenimiento de una población viable de borrego cimarrón (Fig. 2). Sin embargo, en esta sierra existe una población estimada de 420 borrego berberisco, confinada mediante una malla perimetral de 2.4 m de altura, lo que puede tener un efecto negativo sobre la capacidad de carga del hábitat para el borrego cimarrón. Aunque actualmente gran parte de la Sierra Las Hormigas está delimitada con malla alta para evitar la dispersión del borrego berberisco hacia el medio natural, esta zona presenta un alto potencial para el manejo del borrego cimarrón en vida libre en el estado de Coahuila. Esta sierra forma parte de un complejo de serranías interconectadas, con un bajo grado de fragmentación antropogénica, especialmente en la zona no interrumpida por la carretera que conecta los municipios de Monclova y Candela. La Sierra Las Hormigas se localiza a 10 km al noreste de la Sierra Pájaros Azules, que abarca aproximadamente 35,600 ha; a 15 km al norte de la Sierra La Rata, con una superficie de 8,600 ha; y a 25 km al noreste de la Mesa de Cartujanos, que comprende 18,000 ha. Estos sistemas montañosos están conectados por lomeríos de menor altitud que actúan como parches de hábitat, facilitando la conectividad ecológica entre sierras mediante eventos ocasionales de migración local.
Por lo tanto, resulta indispensable realizar una evaluación de los componentes del hábitat potencial para el borrego cimarrón en estas áreas, así como llevar a cabo un censo poblacional del borrego berberisco, con el fin de desarrollar una estrategia estatal de control de esta especie exótica invasora. Aunque diversos estudios indican que el borrego cimarrón es un herbívoro oportunista, adaptado al consumo de una amplia variedad de especies, en el norte de México su dieta se basa principalmente en especies arbustivas (Tarango et al., 2002; Guerrero-Cárdenas et al., 2016, 2018; Gastelum-Mendoza et al., 2021; 2024). A pesar de que estas especies predominan en su hábitat, Gastelum-Mendoza et al. (2024), a través de análisis microhistológico de excretas, determinaron que su dieta incluye principalmente Tiquilia canescens ((DC) A.T. Richardson), Gymnosperma glutinosum ((Spreng.) Less.), O. microdasys, Medicago sativa (L.) y Erioneuron pulchellum (Kunth). No obstante, en los muestreos de campo solo se registró O. microdasys, con una importancia ecológica del 6.28 % según el IVI. Esto sugiere que las especies forrajeras preferidas para el borrego cimarrón presentan una baja disponibilidad y que evita consumir aquellas que predominan en el matorral desértico rosetófilo, como A. lechuguilla y E. antisyphilitica. En la Sierra Las Hormigas, Gastelum-Mendoza et al. (2023) también reportan que el borrego berberisco evitó consumir las especies vegetales dominantes, prefiriendo aquellas menos abundantes. Según estos autores, Vachellia rigidula ((Benth.) Seigler & Ebinger), T. canescens, M. sativa y O. engelmannii constituyeron el 46.49 % de la dieta de esta especie. Sin embargo, solo V. rigidula y O. engelmannii alcanzaron un IVI promedio anual del 9.87 %, lo que no representó un valor significativo en comparación con las especies vegetales dominantes.
La presencia de pastos en el hábitat del borrego cimarrón constituye un componente esencial de su dieta, debido a adaptaciones fisiológicas que optimizan su capacidad para procesar estos recursos, como molares elongados y una capacidad ruminal eficiente (Guerrero-Cárdenas et al., 2018). Diversos estudios han documentado la importancia de los pastos en la dieta del borrego cimarrón. Guerrero-Cárdenas et al. (2016), reportaron un consumo estacional superior al 10 % en la Sierra El Mechudo, Baja California Sur. De manera similar, Gastelum-Mendoza et al. (2021) observaron en el Desierto Sonorense consumos superiores al 20 % durante la época de segregación sexual, mientras que Gastelum-Mendoza et al. (2024) registraron un consumo anual del 17 % en Coahuila. El IVI de los pastos fue mayor en la Reserva durante el verano y otoño, mientras que en la Sierra Las Hormigas alcanzó su máximo en otoño e invierno, coincidiendo con la temporada húmeda y el rebrote de los pastos en el noreste de México (Ramírez et al., 2000).
Entre los pastos clave para la alimentación del borrego cimarrón en el norte de México se destacan el zacate tres barbas (Aristida adscensionis L.), el zacate buffel (Cenchrus ciliaris L. y especies del género Bouteloua (Tarango et al., 2002; Guerrero-Cárdenas et al., 2016; Gastelum-Mendoza et al., 2021; 2024). No obstante, estas especies no son características del matorral desértico rosetófilo en el noreste de México (Alanís-Rodríguez et al., 2015). En el área de estudio, estas gramíneas presentaron un IVI de 6.2 %, mientras que, en la Sierra Las Hormigas este valor aumentó a 10.93 %. Estos valores no son relativamente altos, en comparación con las especies dominantes del matorral desértico rosetófilo.
Una gramínea con potencial forrajero relevante para el restablecimiento de las poblaciones de borrego cimarrón en Coahuila es el zacate buffel (Cruz et al., 2015). Esta especie, introducida en los agostaderos mexicanos en la década de 1950, es originaria de África y no es característica del matorral desértico rosetófilo (Alanís-Rodríguez et al., 2015); sin embargo, representa una fuente importante de alimento perenne para el borrego y otros herbívoros silvestres, especialmente después de la temporada de lluvias, cuando sus rebrotes mejoran la digestibilidad del forraje (Ibarra et al., 2005). Además, posee raíces profundas que le confieren alta resistencia a la sequía, el pastoreo intensivo y las quemas. El zacate buffel destaca por su alto rendimiento forrajero (Gómez et al., 2007), produciendo entre dos y diez veces más biomasa que los pastos nativos (Cruz et al., 2015). Sin embargo, la evidencia científica indica que es una especie forrajera creciente (aumenta su disponibilidad como consecuencia de su bajo consumo), ya que no se ha documentado un alto consumo de este zacate por las poblaciones de borregos en el norte de México (Tarango et al., 2002; Guerrero-Cárdenas et al., 2016; 2018; Gastelum-Mendoza et al., 2024). No obstante, puede representar una alternativa forrajera para el borrego durante periodos de baja disponibilidad de especies forrajeras importantes.
En las regiones áridas del norte de Coahuila, se ha registrado un notable historial de uso ganadero, lo que ha resultado en una degradación significativa de la estructura y composición de los matorrales desérticos (Ochoa-Espinoza et al., 2017). Un indicador de esta situación es la invasión de especies como el mezquite (Prosopis spp.), la gobernadora (Larrea tridentata (Sessé & Moc. ex DC.) Coville) y los nopales (Opuntia spp.) en los matorrales desérticos rosetófilos (Molina-Guerra et al., 2017). En particular, en la reserva, las especies leñosas presentaron un IVI del 11.67 %; mientras que, en la Sierra Las Hormigas se estimó un IVI del 5.67 %. A pesar de que estas especies leñosas brindan alimento, refugio y áreas de descanso para el borrego, su presencia también puede repercutir negativamente en la accesibilidad, visibilidad y producción de forraje (Álvarez-Cárdenas et al., 2009). Esto afecta la calidad del hábitat y puede impactar el desarrollo de las poblaciones (Whiting et al., 2023). Aunque las especies leñosas no fueron dominantes en el matorral desértico rosetófilo durante este estudio, se identificaron varios arbustos leñosos, incluyendo V. rigidula, S. berlandieri, Prosopis glandulosa ((Torr.) Britton & Rose), Karwinskia humboldtiana ((Schult.) Zucc.), Gochnatia hypoleuca ((DC.) A.Gray), Diospyros texana (Scheele), Guaiacum angustifolium (Engelm.) y Forestiera angustifolia (Torr.). Estos arbustos tienen el potencial de proporcionar cobertura térmica al borrego cimarrón, particularmente durante el periodo cálido que abarca de mayo a septiembre (Krausman et al., 1989). Este análisis resalta la necesidad de implementar estrategias de manejo sostenible en las zonas áridas del norte de Coahuila, con el fin de mitigar la degradación ambiental y aumentar la diversidad de las especies características del matorral desértico rosetófilo, como hábitat potencial del borrego cimarrón en Coahuila.
La producción de biomasa de las especies leñosas en la Reserva alcanzó un promedio anual de 52.47 ±14 kg ha-1, lo que representa el 7.5 % de la producción total. En contraste, en la Sierra Las Hormigas, este grupo de plantas mostró una producción mayor, con un promedio de 410.15 ± 23 kg ha-1, equivalente al 39 % de la producción total. Dentro de la reserva, las especies más destacadas en términos de producción de biomasa fueron S. berlandieri y V. rigidula, que contribuyeron con 70.67 kg ha-1 y 66.67 kg ha-1, respectivamente. Por otro lado, en la Sierra Las Hormigas, el aporte de biomasa de las especies leñosas se representó por V. rigidula y K. humboldtiana, que presentaron producciones de 90.63 y 152 kg ha-1, respectivamente. Estos resultados indican la variabilidad en la producción de biomasa entre sitios (p ≤ 0.05) y subrayan la importancia de las especies leñosas en la estructura y funcionamiento del matorral desértico rosetófilo.
En el noreste de México, los arbustos del género Vachellia son importantes como alimento para la fauna silvestre (Ramírez et al., 2000; Gastelum-Mendoza et al., 2020) y son componentes importantes del matorral desértico rosetófilo (Alanís-Rodríguez et al., 2015). Al respecto, V. rigidula se destaca por su alto valor nutricional y forrajero para los herbívoros silvestres (Ramírez et al., 2000). Su condición perenne le permite permanecer verde durante los inviernos húmedos y mantener un valor nutricional constante a lo largo del año, a diferencia de los pastos y hierbas, que tienden a disminuir su calidad nutricional y disponibilidad durante la época seca (Guerrero-Cárdenas et al., 2018). Lo anterior, resalta la necesidad de una gestión adecuada de las especies del género Vachellia dentro de los proyectos de reintroducción del borrego cimarrón en el estado de Coahuila, reconociendo sus beneficios como sus riesgos, con el fin de garantizar la salud y sostenibilidad de las poblaciones de borrego. Otros arbustos, como el guajillo (S. berlandieri) también se considera una fuente suplementaria de nitrógeno no proteico para los herbívoros manejados extensivamente. Sin embargo, su consumo prolongado puede provocar enfermedades, por las altas concentraciones de sustancias químicas que contiene, incluidos alcaloides, taninos y feniletilaminas (Ramírez et al., 2000).
Las especies suculentas, especialmente los nopales del género Opuntia, son importantes en la dieta del borrego cimarrón, debido a su alto contenido hídrico y digestibilidad (Tarango et al., 2002; Guerrero-Cárdenas et al., 2018; Gastelum-Mendoza et al., 2021; 2024). Estas plantas transforman el agua y el CO₂ en energía digestible de manera más eficiente que los pastos y las leguminosas, lo que las convierte en un recurso valioso en ecosistemas áridos. En la reserva, la producción promedio de nopales se estimó en 97.57 ± 59 kg ha-1, lo que representa el 13.87 % de la producción anual total. En comparación, en la Sierra Las Hormigas, los nopales aportaron 90.10 ± 80 kg ha-1, equivalente al 8.46 % de la producción anual total. Aunque los nopales son consumidos por el borrego cimarrón (Tarango et al., 2002; Guerrero-Cárdenas et al., 2016; Gastelum-Mendoza et al., 2024) es fundamental destacar que su ingesta por sí sola no proporciona una nutrición completa (Ramírez et al., 2000). Por lo tanto, es importante mantener una alta diversidad de especies en el matorral desértico rosetófilo para asegurar una dieta de alta calidad nutricional para las poblaciones de borrego e incrementar la capacidad de carga del hábitat. Al respecto, Fulbright y Ortega (2006), mencionan que la capacidad de carga, considerando la producción anual de biomasa es una aproximación teórica y debe considerarse únicamente como un parámetro que indica los cambios en las condiciones del hábitat. Los valores estimados de K, variaron en función del sitio y la estación del año (Cuadro 3), ya que este modelo se fundamenta en la producción de biomasa, la cual, en los matorrales desérticos del norte de México, está influenciada directamente por los eventos de precipitación (Molina-Guerra et al., 2017). Asimismo, las poblaciones de borrego berberisco pueden influir negativamente en la capacidad de carga del hábitat para el borrego cimarrón. Esto es relevante si el borrego berberisco consume una proporción significativa del forraje disponible, ya que ello reduce proporcionalmente la capacidad del ecosistema para sostener poblaciones viables de borrego cimarrón (Gastelum-Mendoza et al., 2023). Esta competencia por los recursos puede generar desplazamientos, aumentar el estrés fisiológico e incluso disminuir el reclutamiento (nacimientos exitosos) en las poblaciones de borrego cimarrón. Además, si ambas especies utilizan los mismos parches de vegetación, refugios o fuentes de agua, puede presentarse una superposición espacial que derive en exclusión competitiva (Krausman, 2000). En ciertas condiciones, el borrego berberisco puede mostrar comportamientos más agresivos o dominantes, desplazando al borrego cimarrón de hábitats óptimos (Krausman et al., 1989). Los resultados de este estudio son útiles para diseñar una estrategia de repoblación del borrego cimarrón en la Sierra Las Hormigas, la cual debe contemplar el control de las poblaciones de borrego berberisco. Finalmente, los hallazgos presentados destacan la importancia del matorral desértico rosetófilo para la conservación del borrego cimarrón en el norte de México.
Conclusiones
Aunque las especies dominantes del matorral desértico rosetófilo no se consideran forrajeras importantes para el borrego cimarrón, desempeñan un papel crucial en el establecimiento de la cobertura de escape y en las estrategias de evasión de depredadores. Se identificó la presencia de especies que reflejan una degradación en la composición vegetal. La Sierra Las Hormigas ofrece forraje y cobertura adecuados para el diseño e implementación de un proyecto de reintroducción del borrego cimarrón. Se recomienda evaluar la topografía de la Sierra Las Hormigas mediante sistemas de información geográfica (SIG) y establecer un programa de control para la población de borrego berberisco.

















