Introducción
La conducta aloparental es el cuidado proporcionado a un infante por miembros de la misma especie, sin ser los padres biológicos (Riedman, 1982). La conducta aloparental incluye la conducta alomaterna y alopaterna, la diferencia entre éstas es el sexo del individuo que proporciona cuidados a las crías, debido a que ambos sexos de una especie aloparental proporcionan los mismos cuidados a las crías. La conducta aloparental está presente en varias especies de mamíferos, por ejemplo, la especie humana (Bogin et al., 2014), así como en algunas especies de roedores biparentales, como el topillo mandarin, Microtus mandarinus (Song et al., 2010; Wu et al., 2013), el topillo de la pradera, Microtus ochrogaster (Olazábal & Young, 2005) y el jerbo Mongolia, Meriones unguiculatus (Elwood, 1975; Ostermeyer & Elwood, 1989). Este roedor es una especie monógama, en la cual el macho participa activamente en el cuidado de las crías. Hembras vírgenes adultas del jerbo de Mongolia pueden exhibir conductas de cuidado relacionadas con la alomaternidad o conductas agresivas hacia las crías de su especie (Elwood, 1983).
A pesar de la importancia de la conducta aloparental en la estructura social de las especies que exhiben esta conducta (Numan, 2020), pocos estudios se han realizado sobre la regulación neural de conducta aloparental (Pedersen et al., 1994; Pedersen et al., 2006; Kenkel et al., 2017; Romero-Morales, et al., 2018). Hay evidencias que indican que el circuito neural que regula la conducta aloparental es homólogo al de la conducta materna (Numan, 2020). Este circuito está integrado por el área preóptica media (mPOA), el lecho del núcleo de la estría terminalis (BNST), el núcleo hipotalámico anterior, el núcleo hipotalámico ventromedial y la sustancia gris periacueductal (Numan, 2006; Bosch y Neumann, 2012; Lonstein et al., 2015, Horrell et al., 2018). El mPOA y BNST forman la parte positiva del circuito porque facilitan la exhibición de la conducta materna, mientras que los otros núcleos están implicados en regular la aversión hacia las crías, integrando la parte negativa de este circuito. Tanto la parte positiva, como la negativa de este circuito tienen múltiples conexiones con la amígdala media, que a su vez recibe proyecciones del bulbo olfatorio (OB) (Numan & Insel, 2003; Numan, 2014; Bales & Saltzman, 2016; Horrell et al., 2018; Taylor y Grieb, 2022).
La oxitocina (OT) y su receptor (OTR) participan en la regulación de las conductas maternas y alomaternas (Lonstein et al., 2015; Yoshihara et al., 2017; Horrell et al., 2018). La OT es un neuropéptido sintetizado en el núcleo paraventricular y el núcleo supraóptico del hipotálamo. Axones de las células neurosecretoras de estos núcleos hipotalámicos liberan OT en el lóbulo posterior de la glándula pituitaria, desde donde esta neurohormona es liberada a la circulación sanguínea a través del plexo capilar (Gimpl y Fahrenholz, 2001). La OT también es liberada centralmente, fibras OT y OTR están presentes en varias regiones del cerebro, como el núcleo accumbens (NAcc), BNST, mPOA, hipotálamo anterior, amígdala, área tegmental ventral, OB y la sustancia gris periacueductal, entre otros (Freund-Mercier, et al., 1994; Numan, 2020). Hembras prepúberes y adultas del topillo de la pradera (Microtus ochrogaster) que despliegan conducta alomaterna tienen una cantidad mayor de células OTR inmunorreactivas (ir) en el NAcc y la región lateral del área tegmental que hembras alomaternas de la rata laboratorio, el ratón laboratorio y el topillo de la pradera oriental (Microtus pennsylvanicus), roedores en los cuales los cuidados alomaternos no son naturales (Olazábal & Young, 2006 a). Las hembras adultas del topillo de la pradera que abrigaron, acicalaron y olfatearon a crías ajenas de la especie tuvieron una mayor densidad de OTR en NAcc en comparación con las hembras agresivas con las crías. Sin embargo, en mPOA y septo lateral no se encontraron diferencias en la densidad de OTR entre hembras alomaternas y agresivas con las crías (Olazábal & Young, 2006 b). Aunque en el topillo de la pradera se ha analizado la presencia de OTR en mPOA, NAcc y septo lateral, a la fecha no se han realizado estudios que asocien la conducta alomaterna con la presencia de OT y OTR en los núcleos neurales que integran el circuito neural positivo de la conducta materna, tales como mPOA, BNST, MeA y BO (Lonstein et al., 2015; Numan, 2020). Bajo esta perspectiva el objetivo de este estudio fue determinar si la conducta alomaterna en hembras adultas del jerbo de Mongolia está asociada con altas concentraciones de OT en plasma y la presencia de OTR en mPOA, BNST, MeA y OB. Aunque la conducta de alomaternidad es independiente de los cambios fisiológicos asociados a la preñez y el parto, se propone la hipótesis de que en el jerbo de Mongolia la conducta alomaterna es facilitada por un sistema oxitocinérgico más activo, caracterizado por concentraciones basales altas de OT y una mayor presencia de OTR en los núcleos cerebrales que integran el circuito positivo de la conducta materna.
Materiales y métodos
Animales. En este estudio se utilizaron hembras vírgenes, adultas del jerbo de Mongolia de entre 180 y 210 días de edad. Los animales fueron obtenidos de una colonia establecida en la Facultad de Estudios Superiores Iztacala, de la Universidad Nacional Autónoma de México. Los animales de la colonia y los jerbos utilizados en este estudio se mantuvieron bajo un fotoperiodo invertido de 12 h: 12 h (ciclo de luz-oscuridad, inicio de luz a las 18:00 h) a una temperatura de laboratorio entre 17 y 21°C. Los animales fueron alimentados con nutricubos (Lab Chow 5001, Nutrimentos Purina, México) y agua potable ad libitum. También se les proporcionó zanahoria en rodajas pequeñas una vez por semana. Los jerbos fueron destetados entre los 25 y 28 días de edad (Elwood, 1975). Se alojaron dos o tres hembras en una jaula de policarbonato (37 × 27 × 15 cm) con cama de aserrín. Se las mantuvo en esta condición desde el destete hasta que fueron expuestas a crías de la misma especie.
Todos los experimentos se realizaron de acuerdo con los lineamientos éticos de la Guía para el Cuidado y Uso de Animales de Laboratorio de los Institutos Nacionales de Salud (Publicación NIH No. 8023) y los lineamientos éticos y especificaciones técnicas de la Norma Oficial Mexicana para la Producción, Cuidado y Uso de animales de laboratorio (Sikes y el Comité de Uso y Cuidado de Animales de la Sociedad Estadounidense de Mammalogists, 2011).
Selección y pruebas de conducta alomaterna. De un total de 30 hembras vírgenes fueron seleccionadas 10 hembras alomaternas y 10 agresivas con las crías a través de breves exposiciones a las crías de la especie. Para seleccionar a los animales de estudio, cada hembra fue colocada en una jaula con las mismas características que la jaula de alojamiento y cama de aserrín limpio. Después de 10 minutos de habituación, fueron introducidas a la jaula dos crías de 1 a 3 días de edad, colocándolas en el lado opuesto al que se encontraba la hembra. Las hembras fueron consideradas alomaternas cuando exhibieron abrigo, acicalamiento y olfateo de las crías, la exposición a las crías duró cinco minutos, pero si las atacaba (primera mordida), la exposición fue terminada inmediatamente. Entre 15 y 20 días siguientes a la exposición de las crías, tanto las hembras alomaternas, como las agresivas con las crías fueron sometidas nuevamente a pruebas de conducta alomaterna, siguiendo el mismo procedimiento descrito anteriormente. Las hembras alomaternas y agresivas mostraron el mismo patrón conductual en la primera y segunda exposición a las crías. En las interacciones alomaternas, el periodo de observación fue de 15 minutos. Se registró la latencia de aproximación (el tiempo que transcurrió desde que las crías fueron introducidas a la jaula hasta que la hembra hizo contacto con una de ellas. También se registró el tiempo dedicado al abrigo, acicalamiento y olfateo de las crías. Cuando las hembras fueron agresivas con las crías, sólo se registró la latencia de ataque (tiempo que transcurre desde que las crías son introducidas a la jaula hasta que la hembra ataca a una de ellas). Tanto durante las exposiciones breves, como durante las pruebas de conducta alomaterna las crías sólo fueron utilizadas una vez. Cuatro crías fueron mordidas levemente, sus heridas fueron tratadas con violeta de genciana (1%) y enseguida fueron devueltas a sus padres. Todas las pruebas de conducta alomaterna se llevaron a cabo entre las 10:00 y las 13:00 h, durante el período de oscuridad, bajo iluminación de luz roja. Las sesiones fueron grabadas con una cámara infrarroja de alta definición (cámara IR Bullet, 2,1 megapíxeles). Una sólo persona analizó los videos.
Análisis hormonal. Inmediatamente después de completar las pruebas de conducta alomaterna se colectaron muestras de sangre (250 μL) del seno retro-orbital de las hembras alomaterna y agresivas con las crías, con tubos capilares heparinizados. Este procedimiento se realizó en hembras previamente anestesiadas con xilacina (5 mg/kg) y ketamina (60 mg/kg im). Enseguida, a cinco hembras elegidas al azar se les administró una segunda dosis de anestesia para dormirlas profundamente (xilacina 5 mg/kg, ketamina 30 mg/kg por vía im) y fueron perfundidas, como se describe en la siguiente sección. Las muestras sanguíneas fueron colectadas con tubos capilares heparinizados entre las 11:00 y las 14:00 h. El plasma se separó por centrifugación y se almacenó a -60°C. Las concentraciones de OT se cuantificaron mediante ELISA con un kit comercial (Abcam, Reino Unido, ab133050), con una sensibilidad de 15 pg/ml. Este kit ha sido utilizado para la cuantificación de OT en el ratón de laboratorio, encontrándose diferencias significativas en la concentración de esta neurohormona en plasma entre ratones expuestos a temperaturas frías y los controles mantenidos en condiciones estándar (Yuan et al., 2020). Los coeficientes de variación intraensayo e interensayo fueron del 10% y el 11%, respectivamente. Los resultados mostraron una correlación entre las diluciones de suero y la curva estándar. La tasa de recuperación de OT fue del 100% (r = 1,0). La placa se leyó en un lector de placas (modelo Multiskan Ascent V1.25 con un filtro de longitud de onda de 450 nm; Thermo Electron Corporation).
Análisis inmunohistoquímico OTR. Las hembras fueron perfundidas a través del corazón, pasando a la circulación solución salina fisiológica, seguida de paraformaldehído al 4% en tampón fosfato de sodio (0,1 M, pH 7.6). Al terminar la perfusión, el cerebro fue extraído y se mantuvo durante 16 h en la misma solución fijadora. El tejido cerebral se procesó histológicamente, y se cortó en secciones coronales de 7 μm de espesor con un micrótomo (Leica 820). Las áreas neurales se localizaron utilizando el Atlas estereotáxico del jerbo Mongolia (Loskota et al., 1974). La ubicación de mPOA y BNST fue de −0,1 mm en la imagen 520, mientras que MeA estaba en −0,888 mm en la imagen 590 y el OB estaba en +1,7 mm en la imagen 300. Después de obtener secciones de las diferentes áreas neurales, las muestras fueron colocadas en portaobjetos gelatinizados (Nutrient Gelatin, 70151-500G-F; Sigma-Aldrich, CA, EE. UU.). Cada uno de los siguientes pasos fue seguido por un enjuague en solución salina tamponada (PBS) durante 5 min: (1) 10 min de incubación en 3% H2O2 en PBS, (2) 20 min de incubación en 5% de suero normal de cabra (Vectastain Kit ABC, PK-4000; Vector Laboratories) en PBS, y (3) 16 h de incubación a 25 °C con una dilución 1:500 de anticuerpo OTR (anticuerpos Bioss, bs-1314R) en PBS. Después de dos enjuagues de 5 minutos en PBS, las secciones se incubaron con anticuerpo anticonejo de cabra biotinilado en PBS durante 90 minutos y se enjuagaron dos veces en PBS (kit Vectastain ABC, PK-6102; Vector Laboratories). Luego, las secciones se incubaron durante 30 minutos con un complejo de avidina-biotina (kit Vectastain ABC, PK-6100; Vector Laboratories), seguido de dos enjuagues adicionales con PBS. Finalmente, la unión se visualizó utilizando 3,3′‑diaminobencidina como cromógeno (sustrato de peroxidasa DAB, SK-4100; Vector Laboratories). Las secciones de tejido cerebral se deshidrataron y montaron en porta objetos. Para las secciones de control negativo, se omitió la incubación con el primer anticuerpo. El anticuerpo OTR (anticuerpos Bioss, bs-1314R) ya fue validado en otro estudio de esta especie mediante Western blot (Romero-Morales et al., 2024).
Análisis de imágenes. El número de células OTR-ir en mPOA, BNST, MeA y OB se cuantificó en los cerebros de cinco hembras alomaternas y cinco agresivas con las crías. La cuantificación se realizó bilateralmente, en cuatro laminillas por hembra. El recuento de células OTR-ir se realizó en microfotografías en áreas de 180 μm2, que es la dimensión del área de muestreo de cada núcleo analizado. Las microfotografías se tomaron con una cámara Motic (10 megapíxeles) adaptada a un microscopio Leica.
Análisis estadístico. Las concentraciones de OT en plasma en hembras alomaternas y agresivas con las crías se contrastaron mediante la prueba no paramétrica de U de Mann-Whitney, debido a que los residuales no se distribuyeron normalmente (Prueba de Anderson-Darling, P > 0,05). Asimismo, se comparó el número de células OTR-ir en mPOA, BNST, MeA y OB entre hembras alomaternas y agresivas con las crías, aplicando también la prueba U de Mann-Whitney. Se utilizó la d de Cohen para calcular el tamaño del efecto. Se realizaron correlaciones de Pearson para determinar potenciales correlaciones entre las concentraciones de OT en plasma y el número de células OTR-ir en mPOA, BNST, MeA y BO.
El análisis estadístico se realizó utilizando SPSS versión 21.0 (IBM SPSS, Armonk, NY).
Resultados
Las hembras alomaternas se aproximaron a las crías con una latencia, cuya mediana fue de 13 s (rango de 8-13 s) (Fig. 1). Las conductas registradas durante las pruebas de conducta alomaterna fueron el abrigo, acicalamiento y olfateo/contacto (Fig. 1). Las concentraciones de OT en plasma fueron significativamente más altas en las hembras alomaternas que en las agresivas (U = 126.0, P < 0.05, d = 1.86, Fig. 2). Asimismo, en las hembras alomaternas, el número de células OTR-ir en mPOA (U = 40.0, P < 0.05, d = 1.87, Figs. 3 y 4) y BNST (U = 40.0, P < 0.05, d = 1.87, Figs. 3 y 4) fue significativamente más alto que en las hembras agresivas con las crías. Mientras que el número de células OTR-ir en MeA (U = 29.5, P > 0.05, d = 0.38, Figs. 3 y 4) y OB (U = 28.5, P > 0.05, d = 0.12, Figs. 3 y 4) no difirió significativamente entre las hembras alomaternas y agresivas con las crías.
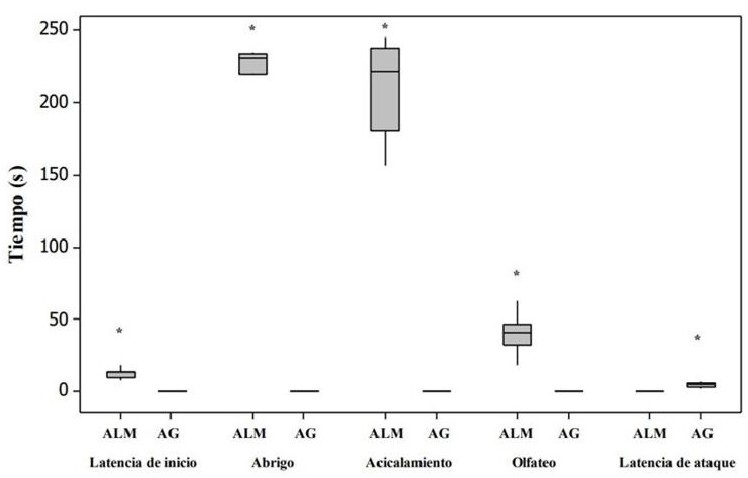
Figura 1 Actividades exhibidas por las hembras alomaternas el gerbo de Mongolia. Los datos están representados en medianas y cuartiles. El * indica diferencias significativas en el tiempo invertido en las actividades alomaternas.
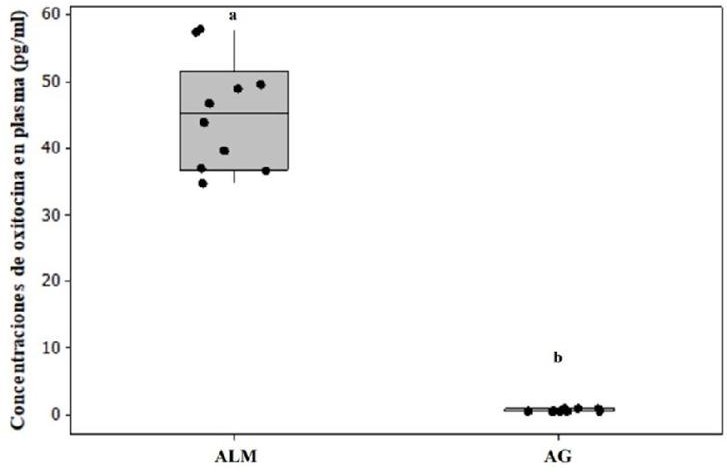
Figura 2 Las hembras alomaternas (ALM) del jerbo de Mongolia tuvieron concentraciones de OT en plasma significativamente más altas que las hembras agresivas (AG) con las crías (n = 10, P < 0.05). Los datos están representados en medianas. Las letras indican diferencias significativas entre los grupos.
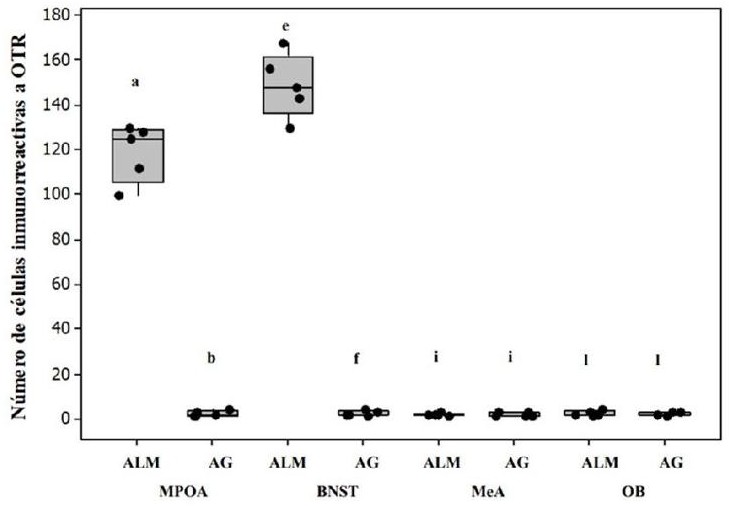
Figura 3 El número de células OTR-ir en mPOA y BNST en hembras alomaternas (ALM) del jerbo de Mongolia fue significativamente más alto que en hembras agresivas con las crías (AG) (n = 5, P < 0.05). Los datos están representados en medianas. Las letras indican diferencias significativas entre los grupos.
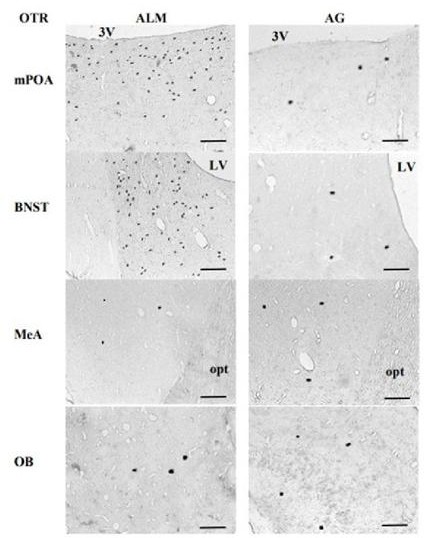
Figura 4 Fotomicrofotografías que muestran células OTR-ir en el mPOA, BNST, MeA y OB en hembras alomaternas, y agresivas con las crías del jerbo de Mongolia. 3V = tercer ventrículo, LV = ventrículo lateral, opt = tracto óptico. Secciones coronales. Escala de la barra = 100 µm.
No se observaron correlaciones entre las concentraciones de OT en plasma y el número de células OTR-ir en mPOA (r = 0.72, P = 0.15), BNST (r = 0.42, P = 0.26), MeA (r = 0.37, P = 0.31) y OB (r = 0.25, P = 0.68).
Discusión
Las hembras alomaternas del gerbo de Mongolia exhibieron actividades como el abrigo, acicalamiento y olfateo de las crías. Estas actividades han sido registradas en machos y hembras juveniles de este roedor, como parte de la conducta aloparental (Ostermeyer y Elwood, 1989), y también como actividades de la conducta materna (Elwood, 1975). Las concentraciones OT en plasma en las hembras que desplegaron conducta alomaterna fueron significativamente más altas que en las hembras agresivas con las crías. Este resultado sugiere que una alta concentración de OT en plasma es requerida para que actividades alomaternas, tales como el abrigo, el acicalamiento y el olfateo sean exhibidas espontáneamente ante la presencia de las crías. En la rata de laboratorio y la oveja, se ha mostrado que la OT periférica no estimula actividades maternas, como el acarreo, acicalamiento, abrigo y la construcción del nido, sino la liberada centralmente; esta OT es la que coordina los cambios conductuales que conllevan al despliegue de la conducta materna, y otras conductas sociales (Kendrick et al., 1987; Pedersen y Prange, 1982). Sin embargo, la concentración de OT en plasma puede ser un biomarcador de la actividad del sistema central de la OT (Neumann y Landgraf, 2012); en el ratón de laboratorio, en el área anteroventral del núcleo periventricular del hipotálamo hay un grupo de neuronas que participan en la regulación de la conducta materna a través de la OT. Cuando este grupo de neuronas es activado optogenéticamente las neuronas del núcleo paraventricular, productoras de OT se activan, resultando en un aumento de OT en plasma, así como una alta respuesta materna, que incluye la exhibición de actividades, tales como el acicalamiento, el abrigo, el acarreo y la construcción del nido (Scott et al., 2015).
Las hembras alomaternas del jerbo de Mongolia que desplegaron acicalamiento, abrigo y olfateo de las crías, tuvieron un número significativamente más alto de células OTR-ir en el mPOA y BNST que las hembras que fueron agresivas con las crías. El mPOA y el BNST, como ya se mencionó, facilitan el despliegue de la conducta materna, por lo cual la presencia significativa de OTR-ir en estas áreas cerebrales puede ser crítica para la exhibición de la conducta alomaterna de este roedor. Aunque no hay estudios sobre la presencia de OTR en mPOA y BNST, en otros núcleos cerebrales como NAcc que es excitado por el mPOA para activar el circuito de recompensa de la conducta materna (Numan, 2007; Numan y Stolzenberg, 2008), se ha encontrado que en el topillo de la pradera hay una notoria variación en la conducta alopaterna, la cual está positivamente correlacionada con la densidad de OTR en el NAcc (Olazábal y Young, 2006 a). Olazábal (2014) menciona que en especies biparentales que forman familias o grupos sociales, los miembros no reproductivos que proporcionan cuidados a los infantes tienen altas densidades de OTR en el NAcc, lo cual puede ser una adaptación en el despliegue de la conducta aloparental.
En ratas parturientas el inicio de la conducta materna está asociada con un aumento significativo en la liberación central OT y la expresión de OTR en áreas neurales que regulan la conducta materna, lo cual no ocurre en la conducta alomaterna (Lonstein et al., 2015; Horrell, et al., 2018). Esto ha llevado plantear que es altamente probable que la OT y OTR no participan en la regulación de esta conducta (Numan, 2020). Sin embargo, en este estudio se encontró que la exhibición de la conducta alomaterna en el jerbo de Mongolia estuvo asociada con altas concentraciones de OT en plasma, y la presencia significativa de OTR en núcleos cerebrales críticos en la regulación de la conducta parental en comparación con los gerbos agresivos con las crías, lo cual sugiere que OT y su receptor participan en la regulación de las actividades alomaternas de este roedor.
En este estudio se encontró que el número de OTR-ir en la MeA y el OB no difirió significativamente entre hembras alomaternas y agresivas con las crías, probablemente porque estas regiones neurales tienen como función llevar los estímulos de las crías tanto a los núcleos que regulan positivamente la conducta materna, como aquellos que participan en la aversión hacia éstas. Utilizando la proteína c-Fos como marcador de actividad neural se encontró que estos núcleos neurales se activan de manera similar en machos alopaternos y agresivos con las crías de la especie (Romero-Morales et al., 2018). Sugiriendo que ambos núcleos desempeñan la misma función el contexto aloparental y el de agresión hacia las crías. Cabe mencionar, que en los machos alopaternos de este roedor tampoco hubo diferencias en el número de células OTR-ir en MeA y OB en comparación con los machos agresivos con las crías (Romero-Morales et al., 2024).
Numan (2020), señala que un aumento de los cuidados maternos es la causa de incrementos de OT en plasma, antes de que incrementos de OT sean la causa de altos cuidados maternos. Nosotros creemos que las hembras alomaternas del jerbo de Mongolia tienen per se altas concentraciones de OT en plasma y un alto número de OTR en los núcleos neurales que regulan la conducta materna, lo cual marca la diferencia conductual entre hembras alomaternas y agresivas con las crías. Sin embargo, esto no implica que la interacción con las crías de su especie también ocasione un aumento en la concentración de OT y el número de OTR.
Los resultados de este estudio sugieren que la conducta alomaterna utiliza los mismos mecanismos neuroendocrinos que regulan la conducta materna, y en general la parental, lo cual apoya la hipótesis de que desde el punto de vista evolutivo es más fácil utilizar las vías neuroendocrinas ya existentes que crear otras (Numan, 2020).
En el jerbo de Mongolia la exhibición de la conducta alomaterna estuvo asociada con altas concentraciones de OT en plasma, así como la presencia significativa de OTR en mPOA y BNST, lo cual sugiere que OT y su receptor participan en la regulación de la conducta alomaterna de este roedor. Aunque sólo estudios manipulativos podrán demostrar el papel de la OT y OTR en la regulación de esta conducta. Futuros estudios podrían analizar el efecto en la conducta alomaterna de la administración de OT o antagonistas de OTR en mPOA y BNST.
















