Introducción
Los líquenes conforman una asociación simbiótica, mutualista, estable y ecológicamente obligada entre hongos y un conjunto de organismos fotosintéticos que pueden ser algas y/o cianobacterias (Kosanić y Ranković 2019). El resultado de esta asociación es diferente a la apariencia independiente de estos organismos, ya que su compleja asociación tiene un alto grado de organización y caracteres morfofisiológicos peculiares (ANPA 2001), que permite habiten aproximadamente el 8 % de los ecosistemas terrestres: desérticos, tropicales y fríos (Kirk et al. 2008, Hawksworth y Lücking 2017). Se caracterizan por su capacidad de colonizar la roca desnuda y formar suelo junto con otros organismos, constituyendo lo que se conoce como costras biológicas (Castillo-Monroy y Maestre 2011, Castillo-Monroy y Benítez 2015). Favorecen la prevención de la desertificación y restauración del suelo erosionado e influyen en la distribución y abundancia de plantas, animales y microorganismos del suelo (Shepherd et al. 2002, Castillo-Monroy y Maestre 2011). Son productores primarios que conforman parte de la dieta de algunos animales (Barreno-Rodríguez y Pérez-Ortega 2003, Seaward 2008). Constituyen el hábitat y refugio para invertebrados, utilizados por aves para anidación y camuflaje (Brodo et al. 2001, Nash III 2008). Tienen capacidad de bioacumulación de elementos como nitrógeno, fósforo y azufre e incluso contaminantes orgánicos y metálicos (Boonpeng et al. 2017). Además del papel importante en el ecosistema, son sensores naturales ante cambios estructurales del bosque, por lo que se implementan como indicadores complementarios de perturbación del bosque y como una medida para su gestión y manejo (McCune 2000).
En México se han estimado alrededor de 2,833 taxones de líquenes (2,722 especies y 111 infraespecíficas) (Herrera-Campos et al. 2014), cuyos estudios se han concentrado más en bosques templados de coníferas y encinos de las regiones del centro y sur de México, principalmente en los estados de Hidalgo, Jalisco, Michoacán, Puebla, Tlaxcala y Veracruz, con mayor frecuencia en líquenes de tipo cortícolas (Gómez-Peralta y Gómez-Reyes 2005, Sánchez-Jácome y Guzmán-Dávalos 2011, Gregorio-Cipriano et al. 2016); sin embargo, los estudios de estos organismos en Chihuahua son escasos donde se estiman cerca de 500 especies (Herrera-Campos et al. 2014).
Chihuahua cuenta con la mayor superficie forestal en México, con cinco millones de hectáreas de bosque (CONABIO 2013), en la parte sureste se localiza la Sierra Tarahumara, la cual se caracteriza por su gran variedad de hábitats y la mayor diversidad de asociaciones de pinos, encinos y madroños a nivel mundial (González-Elizondo et al. 2012). Los diferentes tipos de bosques templados que caracterizan esta zona (bosque de pino, pino-encino, encino-pino, bosque bajo de tipo chaparral) están determinados principalmente por el gradiente altitudinal, la influencia del clima (temperatura y precipitación) y las condiciones del suelo (Lebgue-Keleng et al. 2014). Por lo que se considera que estas características influyen en la riqueza, formas de crecimiento y tipo de sustrato de los líquenes. El objetivo de este trabajo es generar un inventario taxonómico de líquenes, donde se indique la forma de crecimiento y el tipo de sustrato en el que se desarrollan, en algunos bosques de pino y bosques mixtos de la Sierra Tarahumara de Chihuahua.
Materiales y métodos
Descripción del área de estudio
Se ubica en la Sierra Tarahumara, caracterizada por ser una cadena montañosa que forma parte de la Sierra Madre Occidental de Chihuahua, en el norte de México. Se encuentra a una altitud de 1,600-2,400 m s.n.m. El clima se clasifica en semihúmedo y frío, con una temperatura máxima de 31.1 ºC y una mínima de -17.8 ºC (INAFED y SEGOB 2010). El muestreo fue no probabilístico de tipo dirigido en los municipios de Bocoyna, Guachochi, Madera, Temósachic, Ocampo y Urique, que corresponden a ecosistemas de bosque bajo y bosque templado de pino y pino-encino, principalmente.
Recolecta de líquenes
El periodo de recolecta se realizó durante los meses de junio-agosto del 2009-2020 en 12 localidades de seis municipios de la Sierra Tarahumara, Chihuahua, en total fueron 17 zonas de muestreo (Tabla 1). Para cada una se delimitaron cuatro parcelas de 25 × 50 m (1,250 m2), con una superficie de 5,000 m2, al final se juntaron todos los resultados obtenidos de las parcelas para presentarse a nivel de localidad. Posteriormente se registraron las diferentes especies de líquenes según el tipo sustrato: suelo, roca, corteza o musgo. Los especímenes se guardaron en una bolsa de papel para el adecuado traslado al Laboratorio de Biodiversidad de la Universidad Autónoma de Ciudad Juárez (UACJ).
Tabla 1 Zonas de muestreo de líquenes por localidad en la Sierra Tarahumara, Chihuahua
| Número | Localidad y Municipio | Vegetación | Altitud (m s.n.m.) | Latitud (N) | Longitud (O) |
| 1 | Arareco, Bocoyna | BP | 2597 | 28° 11’ 09.4” | 108° 00’ 15.7” |
| BPE | 2307 | 27° 42’ 21.3” | 107° 35’ 72.4” | ||
| 2 | Creel, Bocoyna | BPE | 2350 | 27° 45’ 17.2” | 107° 35’ 50.3” |
| BPE | 2419 | 27° 45’ 16.2” | 107° 37’ 39.7” | ||
| BPE | 2419 | 27° 45’ 15.2” | 107° 37’ 38.4” | ||
| 3 | Huetosacachi, Bocoyna | BPE | 2242 | 27° 47’ 24” | 107° 38’ 32” |
| 4 | Situriachic, Bocoyna | BPE | 2398 | 27° 56’ 43.6” | 107° 38’ 33.5” |
| 5 | San Juanito, Bocoyna | BPE | 2501 | 27° 58’ 17.2” | 107° 36’ 00.2” |
| BPE | 2391 | 28° 00’ 40.9” | 107° 35’ 39.0” | ||
| 6 | Cusarare, Guachochi | BPE | 2205 | 27° 37’ 56.7” | 107° 33’ 34.4” |
| 7 | Peñitas, Madera | CH | 2153 | 29° 16’ 39.6” | 108° 07’ 12” |
| CH | 2118 | 29° 11’ 58.2” | 108° 09’ 31.2” | ||
| 8 | Basaseachi, Ocampo | BPE | 2365 | 28°15’32.53” | 107° 46′ 49.41” |
| 9 | Yepachi, Temósachi | BEP | 1818 | 28° 25’ 50.1” | 108° 23’ 57” |
| 10 | Cuiteco, Urique | BEP | 1970 | 27° 25’ 10.0” | 107° 59’ 28.2” |
| 11 | El Divisadero, Urique | BEP | 2327 | 27 11’ 03.07” | 108°09’ 19.31” |
| 12 | San Rafael, Urique | BPE | 2097 | 27° 30’ 06.6” | 107° 52’ 27.9” |
BEP: Bosque de Encino-Pino; BP: Bosque de Pino; BPE: Bosque de Pino-Encino; CH: Chaparral.
Identificación y descripción de los líquenes
Para la determinación de los géneros y especies de líquenes se realizaron estudios macro y micromorfológicos de estructuras externas e internas. Para la caracterización macroscópica se observó el tipo de talo, tamaño de lóbulos, coloración, diámetro y tipo de los apotecios, presencia o ausencia de rizinas, cilios, tomento, cifelas, picnidios, isidios, soredios, etc., bajo un microscopio estereoscópico. Posterior, se sometieron a pruebas químicas con hipoclorito de sodio (NaClO), hidróxido de potasio (KOH) al 10 % y en combinación de ambos reactivos, observando las reacciones del ejemplar bajo lupa. Para la caracterización microscópica se hicieron preparaciones temporales de cortes del talo, apotecios y peritecios para examinar las ascas y esporas con KOH al 10 % (Nash III 2008, Nash III et al. 2002) para disolver sustancias cristalinas y clarificar secciones oscuras; luego se observó el tipo de conformación de células del talo; tamaño, forma, ornamentación, coloración y número de septos de las esporas.
Las características registradas se contrastaron con diferentes claves taxonómicas de líquenes (Sierk 1964, Hale 1975, 1976, 1980, 1984, Meyer 1985, Scheidegger 1993, Herrera-Campos et al. 1998, Brodo et al. 2001, 2019, Nash III et al. 2002, 2007, Søhrabi y Jamshidikia 2007, Søchting et al. 2008, Randlane et al. 2009, Junji-Kitaura 2012, Jayalal et al. 2013, 2014, Park et al. 2019). Una vez determinada la especie o género se revisó su descripción. La nomenclatura se corroboró en la base de datos de Index Fungorum (http://www.indexfungorum.org/). Finalmente, se obtuvo la frecuencia relativa (%) de las especies con base en su tipo de talo, sustrato y localidad.
Resultados
Diversidad de líquenes
La diversidad total de líquenes fue de 67 especies, ubicadas taxonómicamente en el reino Fungi, phylum Ascomycota, subphylum Pezizomycotina, en tres clases, nueve órdenes, 16 familias y 33 géneros (Tabla 2). La familia Parmeliaceae fue la más frecuente en la Sierra Tarahumara, destacando las especies de Flavopunctelia, Hypotrachyna, Parmotrema, Pseudevernia, Punctelia y Usnea, presentes en ocho de las 12 localidades estudiadas. En la Figura 1 se muestran algunas de las especies determinadas.
Tabla 2 Especies de líquenes de las 12 localidades de la Sierra Tarahumara. Se indica el número de registro con el que se encuentra deposi tado en el Laboratorio de Biodiversidad de la UACJ
| Especie | Forma de crecimiento | Sustrato | Localidad | Registro |
| Clase CANDELARIOMYCETES | ||||
| CANDELARIALES | ||||
| Familia Candelariaceae | ||||
| Candelina submexicana (B. de Lesd.) Poelt (1974). | CR | SX | 6, 7, 8 | UACJ 006, UACJ 014, UACJ 091 |
| Clase EUROTIOMYCETES | ||||
| VERRUCARIALES | ||||
| Familia Verrucariaceae | ||||
| Dermatocarpon sp. Eschw. (1824) | FL | SX | 1,8 | UACJ 002, UACJ 016 |
| ACAROSPORALES | ||||
| Familia Acarosporaceae | ||||
| *Acarospora contigua H. Magn. (1929) | CR | SX | 7 | UACJ 117 |
| Familia Caliciaceae | ||||
| Amandinea punctata (Hoffm.) Coppins y Scheid. (1993) | CR | CT | 1,2 | LBL 011, LBL 094 |
| Clase LECANOROMYCETES | ||||
| CALICIALES | ||||
| Familia Physciaceae | ||||
| Heterodermia diademata (Taylor) D.D. Awasthi (1973) | FL | CT | 7 | UACJ 053 |
| Heterodermia tropica (Kurok.) Sipman (1996) | FL | TR | 8 | UACJ 051, UACJ 055 |
| Heterodermia sp. Trevis (1868) | FL | CT | 1,2 | LBL 124 |
| Leucodermia appalachensis (Kurok.) Kalb (2015) | FL | CT-MS | 6,8 | UACJ 049, UACJ 052 |
| Leucodermia boryi (Fée) Kalb (2015) | FL | CT | 9 | UACJ 050 |
| Leucodermia leucomelos (L.) Kalb (2015) | FL | MS-SX | 8 | UACJ 093 |
| Physcia halei J.W. Thomson (1963) | FL | CT | 6 | UACJ 103 |
| Polyblastidium hypoleucum (Ach.) Kalb (2015) | FL | TR | 8 | UACJ 054 |
| Familia Cladoniaceae | ||||
| Cladonia sp. P. Browne (1756) | CO | TR | 1,2 | LBL 096 |
| Cladonia jaliscana Ahti y Guzm.-Dáv (1998) | CO | TR-HM | 1,2,3,8 | UACJ 033, UACJ 036, UACJ 037, UACJ 039, LBL 006 |
| Familia Haematommataceae | ||||
| Haematomma fenzlianum A. Massal (1961) | CR | SX-CT | 6 | UACJ 102 |
| LECANORALES | ||||
| Familia Lecanoraceae | ||||
| Lecanora albella (Pers.) Ach. (1810) | CR | CT | 6,8 | UACJ 098, UACJ, 100 |
| Lecanora caesiorubella Ach. (1810) | CR | CT | 1,2 | LBL 071, LBL 120 |
| Lecanora sp. Brodo y Vitik (1984) | CR | CT | 1,2 | LBL 55, LBL 116 |
| Ochrolechia sp. A. Massal (1852) | CR | CT | 1,2 | LBL 111 |
| Familia Parmeliaceae | ||||
| Alectoria sp. Link (1833) | FR | CT | 6,9 | UACJ 106, UACJ 127 |
| Bulbothrix sp. Hale (1974) | FL | CT | 7 | UACJ 047 |
| Flavoparmelia caperata (L.) Hale (1986) | FL | CT-SX | 1, 5, 6 | UACJ 058, UACJ 059, UACJ 060, UACJ 061, UAC 063 |
| Flavoparmelia rutidota (Hook. f. & Taylor) Hale (1986) | FL | CT-SX | 1, 6 | UACJ 057, UACJ 062 |
| Flavopunctelia darrowii (J.W. Thomson) Hale (1984) | FL | CT | 1, 2, 5 | LBL 103, UACJ 065, UACJ 066 |
| Flavopunctelia flaventior (Stirt.) Hale (1984) | FL | CT | 2 | LBL 050 |
| Flavopunctelia praesignis (Nyl.) Hale (1984) | FL | CT | 1,2 | LBL 075, LBL 118 |
| Flavopunctelia soredica (Nyl.) Hale (1984) | FL | CT | 2 | LBL 011 |
| *Hypotrachyna boquetensis (Hale) Hale (1975) | FL | CT | 2 | LBL 054B |
| Hypotrachyna brevirhiza (Kurok.) Hale (1975) | FL | CT | 1 | LBL 054A |
| *Hypotrachyna livida (Taylor) Hale (1975) | FL | CT | 2 | LBL 011B |
| Hypotrachyna pulvinata (Fée) Hale (1975). BP | FL | CT | 1, 2 | LBL 094 |
| Imshaugia placorodia (Ach.) S.L.F. Mey. (1985) | FL | CT | 2 | LBL 102 |
| *Parmelina tiliacea (Hoffm.) Hale (1974) | FL | CT | 2 | LBL 25, LBL 101 |
| *Parmotrema cristiferum (Taylor) Hale (1974) | FL | SX-MS | 6 | UACJ 122 |
| Parmotrema cetratum (Ach.) Hale (1974) | FL | CT | 2 | LBL 054C |
| Parmotrema sp. A. Massal (1860) | FL | SX-HM-MS | 6 | UACJ 125 |
| Parmotrema stuppeum (Taylor) Hale (1974) | FL | CT | 5 | UACJ 068 |
| Parmotrema subtinctorium (Zahlbr.) Hale (1974) | FL | CT | 2 | LBL 135 |
| *Pseudevernia cladonia (Tuck.) Hale & W.L. Culb. (1966) | FR | CT | 5, 6 | UACJ 021, UACJ 022, UACJ 023, UACJ 031 |
| Pseudevernia consocians (Vain.) Hale WL Culb. (1966) | FL-FR | CT | 2, 4, 5, 6 | LBL 71, LBL 120, UACJ 028, UACJ 029, UACJ 030 |
| Pseudevernia intensa (Nyl.) Hale & W.L. Culb. (1966) | FL-FR | CT | 2, 4, 5, 7, 8 | LBL 002, UACJ 003, UACJ 012, UACJ 024, UACJ 025, UACJ 026, UACJ 027, UACJ 032 |
| *Punctelia borreri (Turner) Krog (1982) | FL | CT-SX | 6 | UACJ 070, UACJ 072 |
| Punctelia rudecta (Ach.) Krog (1982) | FL | SX | 8 | UACJ 071 |
| *Punctelia stictica (Delise ex Duby) Krog (1982) | FL | SX | 12 | UACJ 069, UACJ 073 |
| Punctelia subrudecta (Nyl.) Krog (1982) | FL | MS-SX | 8 | UACJ 074 |
| Usnea intermedia (A. Massal.) Jata (1909) | FR | CT | 1,2 | LBL 001, LBL 130 |
| Usnea sp. Dill. Ex Adans (1763) | FR | CT | 6 | UACJ 108 |
| Xanthoparmelia sp. (Vain.) Hale (1974) | FL | SX | 8 | UACJ 111 |
| Familia Coccocarpiaceae Coccocarpia sp. Pers. In Gaud. (1827) | FL | MS-TR | 8 | UACJ 093 |
| PELTIGERALES Familia Collemataceae Leptogium arsenei Sierk (1964) | FL | CT | 2 | LBL 078 |
| Leptogium burnetiae C.W. Dodge (1964) | FL | CT | 7 | UACJ 077 |
| Leptogium chloromelum (Ach.) Nyl. (1857) | FL | CT | 2 | LBL 072 |
| Leptogium rugosum Sierk (1964) | FL | CT | 2, 7 | LBL 132, UACJ 080 |
| Familia Lobariaceae Sticta beauvoisii Delise (1822) | FL | MS-HM | 1, 6 | UACJ 005, UACJ 015 |
| Familia Peltigeraceae *Peltigera polydactylon (Neck.) Hoffm. (1789) | FL | HM-MS-TR | 10, 11 | UACJ 010 |
| PERTUSARIALES Familia Megasporaceae *Circinaria contorta (Hoffm.) A. Nordin, Savić & Tibell (2010) | CR | SX | 8 | UACJ 123 |
| TELOSCHISTALES Familia Teloschistaceae Blastenia crenularia (With.) Arup, Søchting & Frödén (2013) | CR | CT | 2 | LBL 121, LBL, 134 |
| Caloplaca sp. Th. P. (1860) | CR | SX-MS | 5, 6, 8 | UACJ 086, UACJ 087, UACJ 088, UACJ 089, UACJ 090 |
| *Gyalolechia flavorubescens (Huds.) Søchting, Frödén & Arup (2013) | CR | CT | 5, 6 | UACJ 082, UACJ 084 |
| Gyalolechia flavovirescens (Wulfen) Søchting, Frödén & Arup (2013) | CR | SX | 12 | UACJ 083 |
| UMBILICARIALES Familia Umbilicariaceae Lasallia papulosa (Ach.) Llano (1950) | FL | SX | 5, 6 | UACJ 017, UACJ 018 |
Forma de crecimiento= CR: Crustoso. FL: Folioso. FR: Fruticoso. CO: Compuesto. Sustrato= SX: Saxícola. CT: Cortícola. MS: Muscícola. HM: Humícola. TR: Terrícola.
*Nuevo registro para Chihuahua.
LBL= Laboratorio de Biodiversidad Líquenes.

Figura 1 Ejemplares de líquenes presentes en las zonas de estudio. A: apotecios de Heterodermia tropica (UACJ 055). B: Lasallia papulosa (UACJ 018). C: Leptogium rugosum (UACJ 080). D: ascas de H. tropica. E: espora de L. papulosa. F: espora de L. rugosum. G: Candelina submexicana (UACJ 091). H: Acarospora contigua (UACJ 117). I: Gyalolechia flavorubescens (UACJ 082). J: Cladonia jaliscana (UACJ 033). K: Haematomma fenzlianum (UACJ 102). L: Pseudevernia cladonia (UACJ 021). M: Punctelia subrudecta (UACJ 074). N: Usnea sp. (UACJ 108). O: Xanthoparmelia sp. (UACJ 111). P: Punctelia rudecta (UACJ 071). Q: Bulbotrix sp. (UACJ 047). Barra de escala: A-C, G-Q= 1 cm; D-F= 10 µm.
De los 363 géneros reportados por Herrera-Campos et al. (2014) en México, se encontraron 33, lo que representa un 9 % de la riqueza nacional. Los géneros que tuvieron el mayor número de especies son: Leptogium (4), Heterodermia (3), Leucodermia (3), Flavoparmelia (3), Pseudovernia (3), Flavopunctelia (4), Hypotrachyna (4), Parmotrema (4) y Punctelia (4), los últimos siete dentro de la familia Parmeliaceae. Se registran por primera vez para Chihuahua 11 especies de líquenes (16.4 %) pertenecientes a Acarospora, Circinaria, Gyalolechia, Hypotrachyna, Parmelina, Parmotrema, Pseudevrnia, Punctelia y Peltigera.
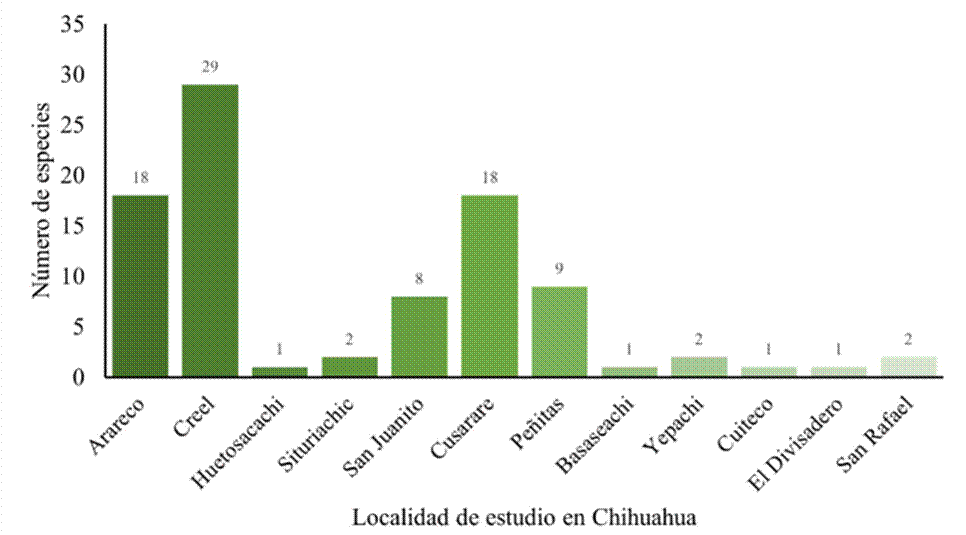
La familia Parmeliaceae presentó el mayor número de registros (34), seguido de Physciaceae (8), Lecanoraceae y Colemataceae (6, en ambas) (Figura 2). De las 12 localidades estudiadas, en Creel se encontró más diversidad de taxones (29), seguida de Arareco (18) y Cusárare (18); en las localidades restantes varió de nueve a una especie (Figura 3). De acuerdo con el tipo de vegetación se encontró una alta riqueza de líquenes en BPE (53), seguido de BP (17), CH (6) y BEP (3).
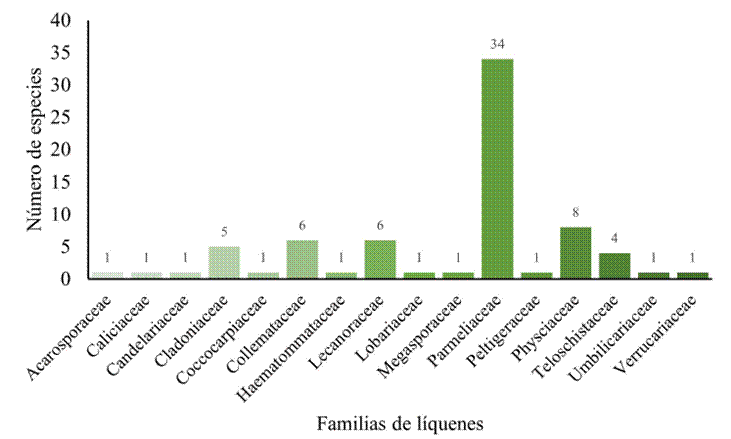
Figura 2 Número de especies por familias de líquenes registradas en las 12 localidades de la Sierra Tarahumara.
Forma de crecimiento
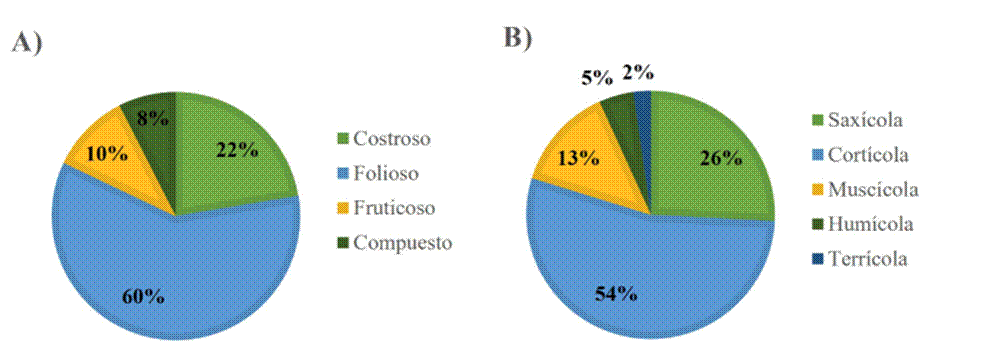
La forma de crecimiento más frecuente fue la de tipo folioso con 35 especies, ocupando el 60 % del total, seguida por el talo costroso (22 %), fruticoso (10 %) y compuesto (8 %) (Figura 4A). La frecuencia de líquenes en cuanto a preferencia de sustrato fue mayor en tipo cortícola, también llamados líquenes epífitos, se registraron 48 especies que corresponden al 54 % del total, seguida de saxícolas (23 spp.), muscícolas (12 spp.), humícolas (4 spp.) y terrícolas (2 spp.) (Figura 4B).
Discusión
Las 67 especies determinadas representan un aproximado del 13 % de la riqueza estimada a nivel estatal de 500 especies por Herrera-Campos et al. (2014). Parmeliaceae fue la familia mejor representada (29 spp.), lo cual concuerda con lo reportado por León-González y Pérez-Pérez (2020) quienes también determinaron a esta familia como la más abundante (45 spp.) en bosques templados de Oaxaca. Gollaway (2008) menciona que esto es debido a su carácter cosmopolita; asimismo, Herrera-Campos et al. (2014), estimaron que existen alrededor de 48 géneros y 519 especies con 17 endémicas pertenecientes a esta familia, siendo también la más numerosa en el país y las más frecuentes en bosques templados. Otros géneros reportados anteriormente como abundantes y concuerdan con los encontrados en la Sierra Tarahumara son: Acarospora, Caloplaca, Cladonia, Hypotrachyna, Lecanora, Parmotrema, Physcia, Usnea y Xanthoparmelia.
De los 21 órdenes registrados para México (Herrera-Campos et al. 2014), en el presente estudio se citan nueve, siendo el orden Lecanorales el de mayor proporción de especies (50.7 %). A nivel de familia se encontraron 16 de las 84 reportadas en el país. Parmeliaceae presentó el mayor número de especies con 29 (43 %), seguido de Physciaceae (8 spp.), esto es similar a estudios sobre líquenes en comunidades vegetales conformadas por bosques de coníferas y bosques mixtos realizados en México en los estados de Oaxaca (León-González y Pérez-Pérez 2020) y Michoacán (Gregorio-Cipriano et al. 2016), y en los Estados Unidos de América en Colorado (Leavitt et al. 2016) y Carolina del Norte (Perlmutter 2006). En todos estos casos se encontró una mayor representación de Parmeliaceae y Physciaceae, debido a la preferencia de climas templados y chaparrales. Otras familias conocidas en el país por su alto número de especies (Herrera-Campos et al. 2014), encontradas con pocos representantes en el estudio fueron Teloschitaceae, Lecanoraceae y Verrucariaceae, un aspecto importante es que se caracterizan por presentar un talo pequeño y costroso, y se encuentran comúnmente en las rocas y suelo en la mayoría de ecosistemas montañosos y matorrales xerofitos; sin embargo, son obviados en los muestreos donde la vegetación es prominente (Leavitt et al. 2021). Es importante destacar la presencia de familias reportadas con poca representación en México como Megasporaceae, Peltigeraceae, Umbilicariaceae y Acarosporaceae (Herrera-Campos et al. 2014), ya que se registraron al menos con una especie.
Los nuevos registros en Chihuahua corresponden a Acarospora contigua (Acarosporaceae), previamente citada en Sonora, Baja California Sur y Nuevo León (Herrera-Campos et al. 2020); Hypotrachyna boquetensis (Parmeliaceae) reportada en Durango (Nash III et al. 2016); H. livida en Nuevo León, Michoacán (Nash III et al. 2016) y Jalisco (Herrera-Campos et al. 2020); Parmelina tiliacea en San Luis Potosí (Herrera-Campos et al. 2020); Parmotrema cristiferum en Baja California Sur, Sonora, Guanajuato, Durango, Coahuila, Nuevo León, Tamaulipas, Guerrero, Morelos, Chiapas (Herrera-Campos et al. 2020), Veracruz (Pérez-Pérez et al. 2015) y Oaxaca (León-González y Pérez-Pérez, 2020); Pseudevernia cladonia en Oaxaca (Herrera-Campos et al. 2020); Punctelia borreri en Sonora, Nuevo León, Jalisco, Michoacán, Morelos y Veracruz (Herrera-Campos et al. 2020); P. stictica para la Ciudad de México, Hidalgo y Tlaxcala (Herrera-Campos et al. 2020); Peltigera polydactylon en Sinaloa, Nuevo León, Estado de México, Veracruz y Chiapas (Herrera-Campos et al. 2020). Con respecto a la familia Megasporaceae: Circinaria contorta se ha reportado en Baja California Sur (Herrera-Campos et al. 2020) y Aguascalientes (Miguel-Vázquez et al. 2021). Finalmente, para la familia Teloschistaceae: Gyalolechia flavourubescens se ha registrado en Baja California, Baja California Sur y Jalisco (Herrera-Campos et al. 2020). Estos nuevos registros destacan la importancia de los estudios taxonómicos para documentar la flora liquénica de México como lo mencionan Cortés-Hernández et al. (2012) con 15 nuevos registros para Hidalgo, Gregorio-Cipriano et al. (2016) con 39 para Michoacán y León-González y Pérez-Pérez (2020) con 59 para Oaxaca. Estos resultados representan una contribución importante a la diversidad de hongos liquenizados del Noroeste de México.
El tipo de talo se relaciona con los requerimientos ecológicos y fisiológicos de estos organismos (Marini et al. 2011, Benítez et al. 2012). Las especies fruticosas como Usnea intermedia (Brodo et al. 2001, Nash III et al. 2007) y foliosas con lóbulos estrechos como especies de los géneros Flavopunctelia, Hypotrachyna y Pseudevernia son más abundantes en bosques abiertos o perturbados (Giordani et al. 2012, Koch et al. 2013, Li et al. 2013), las cuales se observaron principalmente en los bosques del municipio de Bocoyna, el cual se caracteriza por comunidades de Pinus arizonica con sustitución de matorrales formados generalmente por Quercus depressipes y Arctostaphylos pungens, que además de tener impacto en la disminución de la cobertura y biomasa, está fuertemente impactado por actividades agroforestales (Quiñonez-Martínez et al. 2008). Por otra parte, Leptogium arsenei, L. chloromelum y L. rugosum que poseen cianobacterias son más abundantes en bosques primarios o no perturbados (Rosabal et al. 2010, Benítez et al. 2012, Aragón et al. 2013, Li et al. 2013), entre los cuales destacan algunos bosques de pino y pino-encino en Bocoyna, Ocampo y Urique, así como los chaparrales en Madera.
La importancia de ubicar zonas con riqueza de líquenes reside en la relación entre las condiciones ecológicas específicas de la zona y los cambios estructurales del bosque producidos por la perturbación natural y humana (Benítez et al. 2018). Los líquenes saxícolas como las especies de Punctelia y Caloplaca pueden mostrar una relación con los ácidos del suelo, rocas e incluso parámetros climáticos, sugiriendo pueden estar involucrados en funciones como la acumulación de metales y la tolerancia al estrés (Paukov et al. 2019). Otras especies como Flavopunctelia praesignis e Hypotrachyna brevirhiza se han empleado como indicadores para monitorear la emisión de elementos volátiles y calidad del aire (Calvelo et al. 2009, Bubach et al. 2012). Las especies de Cladonia están bien adaptadas a altos grados de contaminación, jugando un papel fundamental en la restauración natural de hábitats fuertemente afectados (Osyczka y Rola 2013, Osyczka et al. 2016). Lo anterior promovería el uso de especies de líquenes como bioindicadores complementarios en muchos de los ecosistemas de la Sierra Tarahumara en Chihuahua, principalmente en municipios con explotación maderera como Bocoyna, influencia turística (Arareco, Creel, Guachochi, Urique), así como en monitoreo y manejo de áreas naturales protegidas (Arareco, Basaseachi, Cusarare y El Divisadero).
Conclusiones
Las localidades muestreadas de la Sierra Tarahumara poseen las condiciones favorables para el desarrollo de los líquenes. Desde 2009 hasta 2020 se registraron 67 especies de líquenes con 11 nuevos reportes para Chihuahua. La familia Parmeliaceae presentó la mayor diversidad de especies. Se determinó en mayor proporción taxones con talo folioso. La importancia de los inventarios taxonómicos de estas especies destaca en su aplicación ecológica, debido a que pueden utilizarse como indicadores de contaminación del aire y suelo, calidad y disturbio de hábitats y en la evaluación y monitoreo de los cambios estructurales del bosque.